서 언
재료 및 방법
시험 재료
수확직후 대추 품질 특성 분석
구성 성분 및 대사체 구성 성분 분석
유리 아미노산 분석
총 페놀성 화합물, 총 플라보노이드, 총 안토시아닌 함량 분석
항산화활성 분석
지방산 분석
페놀성 화합물 분석
통계분석
표적 대사체학 분석
결과 및 고찰
수확직후 대추 과일의 품질 특성
건왕대추에 함유된 성분
서 언
대추나무(Ziziphus jujuba Mill.)는 갈매나무과(Rhamnaceae) 대추나무속에 속하는 교목성 과수로 열대, 아열대 및 온대 지역에 약 40종이 분포하고 있다. 우리나라에서는 경산, 밀양, 보은 등이 주산지이며, 재래종으로 복조, 보은, 산조대추 등이 분포하고 있다(Park et al. 2008).
대추의 국내 생산량은 2018년 70,734톤에서 2019년 9,436톤, 2022년에 8,088톤으로 감소하였다. 현재 재배되고 있는 대추 품종은 크게 일반대추와 왕대추로 구분할 수 있다. 일반 대추 품종으로는 ‘복조’ 등 재래종 및 개발 품종들이 있고, 왕대추 품종으로는 ‘황실’, ‘대능’ 등이 있다. 왕대추는 기존의 대추나무를 개량하여 열매가 굵고 다수확할 수 있도록 육종한 것으로 대왕대추, 계란대추, 사과대추, 대설대추 등 다양한 이름으로 불리우고 있다. 왕대추는 재래종에 비해 2–3배정도 크기가 크고, 당도는 미숙과가 20°Bx, 80% 이상 착색시 30°Bx 정도이며, 시중에서 쉽게 접할 수 있는 기호성 있는 신선 과일로 2010년대 이래 공급이 확산되고 있다.
대추에는 트리테르페노이드 배당체, 싸이클로펩타이드 알칼로이드, 플라보노이드 및 네오리그난 등 다양한 생리활성 대사산물들이 함유되어 있으며, 이 성분들의 항산화, 항염증, 항균, 위장 보호, 심혈관 보호, 신경 보호, 항암, 항 HIV, 진정 및 항불안 작용 등이 보고되었다(Mahajan and Chopda 2009; Liu et al. 2020). 대추 품종별 함유 성분 및 활성에 대해 국내산 약대추와 복조 열매의 신선 그리고 건조품에 대한 이화학적 특성으로 당도, 조단백질, 조지방, 조회분, 식이섬유, Ca, P, Fe 성분 비교(Choi et al. 2016), 37품종의 중국 대추에 대해 총 페놀성 화합물, 총 플라보노이드, 트리테르페노이드, 다당류, 비타민 C, 개별 페놀성 화합물 및 항산화활성(Zhang et al. 2021), 당(Zhang et al. 2018), 아미노산(Song et al. 2019; Wang et al. 2020), 지방산(Kohei et al. 1991), 101가지의 플라보노이드 대사산물(Qiu et al. 2023), 환원당, 유기산 및 미네랄(Wang et al. 2018), 그리고 대추 야생종과 재배 품종 간 아스코르빈산 함량의 차이와 그 대사적 메커니즘(Wang et al. 2022) 이 보고되었다. Liu et al.(2023)은 야생 대추와 재배 최근 비표적 대사산물 프로파일링을 통하여 중국의 중요한 세 품종의 대추에서 1,059개의 대사 산물을 찾아 이들의 구조적 특징을 기준으로 11가지 계열로 분류하였고 품종간 대사 산물의 차이에 관하여 보고하였다(Liu et al. 2023). 그러나 한국에서 재배되는 대추 품종별 대사체 비교에 대한 연구는 많지 않다.
대추는 전통적으로 열매를 수확 후 건조시켜 식재료 및 완화제, 이뇨제, 강장제, 거담제, 기관지염, 결핵 등에 약재로 폭넓게 이용되었다(Kwon et al. 1997).
본 실험에서는 주로 신선 과일로 섭취되고 있는 왕대추가 기존에 한약재로 사용되어 온 ‘복조’와 비교하여 약용 및 식재료로 이용 가능성이 있는 지를 평가하고자 하였다. 이를 위해 재래종인 ‘복조’와 왕대추 신품종인 ‘황실’, ‘대능’, ‘천황’의 건조 과일을 대상으로 대사산물 분석을 수행하였으며, 성분 간 연관성과 품종 특성을 파악하였다. 이 연구 결과는 건조 왕대추의 기능성 식품 및 약용 소재로의 활용 가능성을 제시하는 기초자료로 활용될 수 있을 것이다.
재료 및 방법
시험 재료
대추 시료는 왕대추 ‘황실’, ‘대능’, 및 ‘천황’을, 대조구로는 재래종 ‘복조’를 사용하였다. ‘복조’는 한국에서 가장 일반적으로 재배되며 약재 및 식재료로 이용되고 있다. 실험에 이용한 네 품종 모두 2019년 하우스 재배된 4–5년생 대추나무의 열매를 30% 착색기에 수확한 직후(Fig. 1) 기계건조한 후 음건을 거쳐 0–5°C에 약 6개월간 저장된 것을 동결 마쇄하여 ‒58°C에 보관하면서 분석 시료로 사용하였다.
수확직후 대추 품질 특성 분석
수확 직후 대추 열매의 품질은 무게(g), 구형지수, 색(Hunter Lab), 경도(N), SSC(%), TA(%) 등으로 평가하였다. 무게는 수확당시 신선 대추 열매의 중량을 측정하여 평균값으로 계산하였다. 구형지수는 대추 열매의 가로와 세로길이의 비율로 구형지수가 1에 근접할수록 원형에 가까운 형태임을 의미한다. 과피색은 과일 한 개당 적도 부분의 반대편 2곳을 색차계(Minolta CR-300, Minolta co., Osaka, JP)로 측정하여 명도(L*), 녹색–적색(a*), 청색–황색(b*)으로 표시하였다. 경도는 경도계(TAHDi/500, TAHD, London, UK)에 5mm 탐침을 이용하여 2mm/s의 속력으로 과피로부터 내부로 5mm를 뚫고 들어가는 동안의 최대 압력을 뉴턴(N)으로 표시하였다. 대추씨를 제거한 과일 전체를 착즙하여 가용성고형물 함량은 디지털 굴절계(PR-101, Atago Co., Ltd., Tokyo, Japan)를 사용하여 측정한 후 %로, 유기산 함량은 적정기(Titrette® bottle-top burette, BrandTech® Scientific, Inc., Wertheim, Germany)를 이용하여 과즙 5mL를 pH 8.2의 종말점까지 0.1N NaOH를 이용하여 적정한 후 %로 환산하였다. 모든 실험장소의 온도는 20–25°C로 유지하였다.
구성 성분 및 대사체 구성 성분 분석
무기물 분석
건대추에 함유된 무기물 함량은 ICP assay 방법(Hong et al. 2016)을 수정하여 분석하였다. 동결건조된 시료 0.1g을 digestion tube에 넣고 60% HNO3 4mL(Daejung chemical co., Korea)를 혼합하여 실온에서 24 시간 동안 유지시켰다. 이 튜브를 200°C의 digestion oven에 옮긴 후 용액이 투명해질 때까지 3mL H2O2를 첨가하였다. 그 후 1,000ppm의 La+를 포함하는 1N HCl을 첨가하여 최종 부피를 100mL로 만들었다. 무기물 함량은 ICP-OES(Optima 5300 DV, PerkinElmer Inc., 91Wellesley, MA, USA)로 분석하였고 이 때 기기의 operation power는 1300W, 샘플 유속은 15.0L·min-1, auxiliary flow rate는 0.2L·min-1, nebulizer flow rate는 0.8L·min-1이었다. ICP에 대한 모든 표준 물질은 Sigma-Aldrich Co.(St. Louis, MO, USA)에서 구입하였다.
가용성 탄수화물 및 유기산 분석
가용성 탄수화물은 시료 10µL를 300 × 6.5mm sugar-pak(Waters Co., Milford, MA, USA)과 Shodex RI-101 검출기(Shodex, Tokyo, Japan)가 장착된 Dionex Ultimate 3000(Thermo Dionex Co., Sunnyvale, CA, USA)에 주입하여 정량하였다. 데이터 처리에는 Chromeleon Ver. Six software를 사용하였다. 이동상으로는 증류수를 flow rate 0.5mL·min-1, 온도 70°C로 사용하였다. 결과는 건조 중량 기준으로 g·kg-1로 표시하였다. 유기산 함량은 Aminex 87H 컬럼(300 × 10 mm, Bio-Rad Co., Hercules, CA, USA)과 210nm의 RI 검출기(ERC, RefractoMAX520, DataApex, Prague, Czech Republic)를 갖춘 Ultimate 3000(Thermo Dionex Co., Sunnyvale, CA, USA)을 사용하여 측정하였다. 40°C 온도에서 유속 0.5mL·min-1로 0.01N H2SO4를 첨가하여 이동상의 용매 조성을 바꾸면서 분석물을 용출시켰다. 시료 주입량은 10µL, 결과는 건조중량 기준으로 g·kg-1로 표시하였다.
유리 아미노산 분석
유리 아미노산 분석은 기존에 보고된 방법(Byeon and Lee 2020)을 수정하여 이용하였다. 상등액 1µL을 5µL의 borate buffer, 1µL의 o-phthalaldehyde 및 1µL의 fluorenylmethyloxycarbonyl chloride과 혼합한 후, 32µL의 증류수를 추가하였다. 그 중 0.5µL를 Dionex Ultimate 3000 HPLC 시스템(Thermo Dionex Co., Sunnyvale, CA, USA)에 주입하였다. 이 시스템은 자외선 검출기(Ultimate 300, Thermo Dionex Co., Sunnyvale, CA, USA), 형광 검출기(Agilent 1260 Infinity, Santa Clara, CA, USA; 450 × 340 nm, OPA; 93305 × 266 nm, FMOC), 및 Inno C18 컬럼(4.6mm × 150 mm, 5µm, Youngjin Biochrom, Seoul, Korea)을 장착하였다. 컬럼 온도는 40°C로 유지되었으며, 자외선 검출기의 파장은 338nm를 이용하였다. 이동상의 유속은 0.5mL·min-1로 일정하게 유지하였다. 이동상은 용매 A와 용매 B 두 가지를 이용하였는데, 용매 A는 40mM sodium phosphate(pH 7), 용매 B는 water/Acetonitrile/Methanol(10:45:45, v/v %)였다. 단계적 기울기 조건은 시간에 따라 0–3분은 95% (A)와 5% (B), 3–24분은 45% (A)와 55% (B), 24–31분은 10% (A)와 90% (B), 31–35분은 95% (A)와 5% (B)로 조성하였다. 아미노산의 동정 및 정량은 표준물질의 유지시간을 기준으로 하였다. 모든 농도는 건조 중량 기준으로 mg·kg-1로 표시하였다.
총 페놀성 화합물, 총 플라보노이드, 총 안토시아닌 함량 분석
총 페놀성 화합물 함량은 Folin-Ciocalteu’s 방법(Singleton et al. 1999)에 따라 시료 0.1mL, 증류수 8.4mL, 2N Folin-Ciocalteu reagent(Sigma-Aldrich Co., St. Louis, Mo, USA) 0.5mL, 20% Na2CO3 1mL를 혼합하여 1시간 반응시킨 후 725nm에서 분광광도계를 통해 흡광도 값을 측정하였다. 페놀화합물 함량은 표준물질인 gallic acid(Sigma-Aldrich Co.)를 사용하여 작성한 표준곡선으로 양을 환산하였고, 추출물 중의 mg gallic acid equivalent(GAE, dry basis)로 나타내었다.
총 플라보노이드 함량은 (+)-catechin을 표준품으로 사용하여 aluminium trichloride 방법으로 측정하였다(Zhishen et al. 1999). 125µL의 추출물을 5% NaNO2 75µL의 용액에 첨가한 후, 혼합물을 6분 동안 방치한 후, 10% aluminium trichloride 150µL를 첨가하고 5분 동안 인큐베이션 한 후, 1M NaOH 750µL를 첨가하였다. 증류수를 사용하여 용액의 최종 부피를 2,500µL로 조정하였다. 15분간 인큐베이션 후, 혼합물의 흡광도를 510nm에서 측정하였다. 총 플라보노이드 함량은 g catechin 100g-1 DW로 계산하였다.
총 안토시아닌 함량(TAC)은 pH-differential 방법에 의해 분석하였다(Giusti and Wrolstad 2001). 1mL 추출 용액을 10mL 플라스크로 옮기고, 한 플라스크는 potassium chloride buffer(pH 1.0)로 조절하고 다른 하나는 sodium acetate buffer(pH 4.5)로 각각 희석하였다. 이 희석액을 15분 동안 평형 상태로 두었고 blank로 증류수를 셀에 채워 510 및 700nm에서 흡광도를 측정하였다. 관찰 시간이 증가하면 값이 증가하는 경향이 있으므로 모든 측정은 샘플 준비 후 15분에서 1시간 사이에 수행하였다. 다음의 계산식으로 총 안토시아닌 함량을 계산하였다.
Total anthocyanin (mg·L-1) = (A × MW × DF × 1000) / (ε × 1)
A = (Abs520 – Abs700) pH 1.0 – (Abs520 – Abs700) pH 4.5; MW = 449.2(cyanidin-3-glucoside 분자량); DF = 4(희석배수); 1000 = g을 mg으로 변환하는 상수; ε = 26,900(molar absorptivity); l = pathlength in cm
Total anthocyanin (mg C3GE·kg-1) = [(pH 1.0 Abs520 – pH 1.0 Abs700) – (pH 4.5 Abs520 – pH 4.5 Abs700)] × coefficient (66.7955).
항산화활성 분석
항산화활성은 DPPH radical scavenging activity(Ku et al. 2010)와 ABTS radical scavenging activity(Re et al. 1999) 두가지 방법으로 분석하였다. DPPH 라디칼 소거 활성은 에탄올에 용해된 시료 0.5mL를 100µM의 DPPH용액 3mL에 첨가하여 반응액을 완전히 섞은 후에 실온에서 10분간 반응시킨 후, 남아있는 DPPH의 양을 측정하기 위해서 spectrophotometer(Multiskan go, Thermo Scientific, Waltham, MA, USA)를 이용하여 517nm에서 흡광도를 측정하였다. DPPH 라디칼 소거능은 다음의 식으로 구하였다.
DPPH radical scavenging activity (%) = [(Abs control – Abs sample) / Abs control] × 100
ABTS(2,2-azino-3-ethylbenzothiazoline-6-sulfonic acid, Sigma-Aldrich Co.) 라디칼 소거활성은 7.4mM ABTS와 2.6mM potassium persulfate를 하룻동안 암소에 방치하여 ABTS 양이온을 형성시킨 후 이 용액을 735nm에서 흡광도 값이 1.4–1.5가 되도록 몰 흡광계수(ε= 3.6 × 104 M-1cm-1)를 이용하여 증류수로 희석하였다. 희석된 ABTS 용액 1mL에 추출액 50µL를 가하여 흡광도의 변화를 30분 후에 측정하였다. ABTS 라디칼 소거능은 다음의 식에 의해서 구하였다.
ABTS radical scavenging activity (%) = [(Abs control – Abs sample) / Abs control] × 100
지방산 분석
지방산은 GC 분석법(Garcés and Mancha 1993)을 수정하여 분석하였다. 동결 건조된 분말 시료 100mg과 20µL의 내부표준물질(pentadecanoic acid, 5.0mg·mL-1, ≥ 99%, Sigma-Aldrich Co, St. Louis, MO, USA)을 Teflon cap이 있는 유리 시험관에 넣었다. 이후 methanol:benzene:2,2-DMP:H2SO4 (39:20:5:2, v/v %) 2mL와 heptan 1mL를 첨가하였다. 시험관을 흔들어준 후 80°C에서 2시간 동안 추출하였다. 추출 후 시료를 냉각시킨 후, 상등액을 분석용 시료 바이알로 옮겼다. 시료는 GC(Agilent 7890A, Agilent Technologies, Inc., Santa Clara, CA, USA)를 사용하여 분석하였다. GC에는 DB-23 컬럼(60m × 0.25mm, 0.25µm, Agilent Technologies, Inc., Santa Clara, CA, USA) 및 화염 이온화 검출기(FID)를 장착하였다. 컬럼 오븐 온도는 처음 50°C에서 1분간 유지한 후 25°C·min-1의 속도로 130°C까지 4.2분 동안 상승시켰으며, 이후 8°C·min-1로 170°C까지 9.2분 동안 상승시켰다. 이후 온도를 2°C·min-1로 210°C까지 상승시킨 후 10분 동안 유지하였고, 추가로 9.2분 동안 유지하였다. 마지막으로 250°C까지 10°C·min-1의 속도로 상승시킨 후 45.2분 동안 유지하였다. 주입구 온도는 250°C, 캐리어 가스(He)의 유속은 4mL·min-1로 설정하였다. 검출기 온도는 280°C, H2의 유속은 35mL·min-1, air는 350mL·min-1, He은 35mL·min-1로 설정하였다. Fatty acid methyl ester 표준물질(Supelco 37 Component FAME Mix, Merck KGaA, Darmstadt, Germany)은 Supelco Inc. (Bellefonte, PA, USA)에서 구입하였다.
페놀성 화합물 분석
동결 건조 및 분쇄된 시료 0.5g을 2% formic acid가 포함된 70% methanol 5.0mL에 첨가하고, 20초 동안 균질화하였다. 이 균질액을 페놀성 화합물의 분해를 방지하기 위해 얼음 수조에서 20분간 초음파 처리한 후, 4°C에서 10,000 × g로 10분간 원심분리하였다. 상등액을 0.45µm PVDF 필터(BioFACT Co., Ltd., Daejeon, Korea)로 여과하여 분석시료로 이용하였다. 개별 페놀성 화합물은 pump(Waters 1525 binary HPLC pump, Waters Co., Milford, MA, USA), UV-Vis 검출기(Waters 2489 UV/Visible detector, Waters Co., Milford, MA, USA), 및 ZORBAX Eclipse XDB-C18 컬럼(4.6 × 250 mm, 5µm; Agilent Technologies, Inc., Santa Clara, CA, USA)이 장착된 HPLC UltiMate®3000(Dionex, Sunnyvale, CA, USA)을 이용하여 분석하였다(Lwin and Lee 2020). 용매 A는 HPLC급 물에 0.5% formic acid 함유, 용매 B는 acetonitrile에 0.5% formic acid 함유되도록 조제하였고, 단계적 기울기는 95% A + 5% B (0분), 90% A + 10% B (25분), 78% A + 22% B (42분), 60% A + 40% B (60분), 5% A + 95% B (80분)로 조절하였다. 컬럼 온도는 30°C로 유지하였으며, 검출기 파장은 catechin, phloridzin, gallic acid는 280nm, chlorogenic acid와 caffeic acid는 320nm에서 측정하도록 설정하였다. 주입량은 10µL, 유속은 1.0mL·min-1로 설정하였다. 개별 페놀성 화합물의 표준물질은 모두 Sigma-Aldrich(St. Louis, MO, USA)에서 구입하였다. 결과는 건조 중량 기준 mg·kg-1로 나타내었다(Zhang et al. 2010).
통계분석
대추 열매의 품질 인자는 완전 임의 배치를 적용하여 평가하였다. 탄수화물, 유기산, 무기성분, 유리 아미노산 및 개별 페놀성 화합물은 5개 과일을 한 반복으로 하여 3반복으로 분석하였다. 총 페놀성 화합물, 총 플라보노이드, 총 안토시아닌 및 항산화활성은 각각 5개의 과일을 한반복으로 하여 6반복으로 분석하였다. 데이터는 평균 ± 표준오차로 표시하였다. SPSS v.27.0(SPSS Inc., Chicago, IL, USA) 프로그램으로 Duncan의 multiple range test(p < 0.05)와 ANOVA test를 수행하여 유의차를 검정하였다.
표적 대사체학 분석
샘플간 차이를 시각적으로 평가하고 주요 변수의 기여도를 분석하기 위하여 웹 기반 플랫폼인 MetaboAnalyst 5.0(https://www.metaboanalyst.ca/)를 이용한 방법(Pang et al. 2021)으로 다변량 통계분석을 수행하였다. 네 품종의 대추에 함유된 성분들에 대한 유의차는 Fisher의 LSD 검정(p < 0.05)을 사용하여 평가하였다. 얻은 모든 데이터를 중앙값 scaling을 통해 정규화하였다. PLS-DA 분석은 변수 간 다중공선성이 높은 경우에도 그룹 간 차이를 효과적으로 구분할 수 있도록 차원을 축소하여 변별력을 극대화하는 분석 기법이다. 본 연구에서는 품종을 응답변수로 사용하여 품종별 구성성분의 분포 및 차이를 시각적으로 확인하는데 이용하였다. VIP score plot은 PLS-DA 모델에서 각 변수가 그룹 구분에 미치는 기여도를 정량적으로 평가하는 지표이다. 일반적으로 VIP score가 1.0 이상인 변수는 모델의 예측 및 분류에 중요한 역할을 한다. 본 연구에서는 주요 차별화 대사물질 성분을 선별하기 위해 사용하였다. 품종 간 유사성을 기반으로 계층적으로 군집을 형성하여 그룹 간 관계를 시각적으로 표현하는 계층적 군집 분석(hierarchical cluster analysis, HCA)을 실시하였다. 그리고 히트맵 분석을 통하여 각 대사산물들 간의 연관성을 분석하였다.
결과 및 고찰
수확직후 대추 과일의 품질 특성
30% 착색기에 수확한 신선 대추 과일의 한 알 크기는 ‘천황’이 21.4g으로 가장 컸고, 재래종인 ‘복조’가 15.7g으로 가장 작았다. 과일의 모양은 ‘황실’이 구형지수 1.0으로 완전한 원형이었고 ‘대능’, ‘천황’, ‘복조’ 순으로 구형지수가 낮아져 타원형을 보였다. 과일의 표피 색도는 ‘복조’의 a*값이 가장 높고 b*값은 가장 낮으며 명도도 가장 낮아 네 품종 중 가장 어두운 갈색을 보였다. 경도는 ‘황실’, ‘천황’, ‘복조’, ‘대능’ 순으로 높았고, 가용성 고형물 함량은 ‘복조’가 약 30%로 가장 높았으며, 총 유기산 함량은 ‘복조’, ‘황실’, ‘천황’, ‘대능’ 순으로 높았다(Table 1).
Table 1.
Quality characteristics of fresh jujube fruits at harvesting time according to the cultivar
| Variety |
Weight (g) |
Head shape index | Color (Hunter) |
Firmness (N) |
TSS (°Bx) |
TA (%) | ||
| L* | a* | b* | ||||||
| Bokjo | 15.67 ± 1.73z | 0.83 | 38.47 ± 2.95 | 18.73 ± 1.49 | 25.81 ± 4.07 | 26.69 ± 4.40 | 30.38 ± 2.57 | 0.82 ± 0.12 |
| Cheonhwang | 21.44 ± 2.34 | 0.90 | 57.06 ± 12.34 | 4.22 ± 10.54 | 37.53 ± 6.41 | 28.99 ± 5.67 | 23.39 ± 2.47 | 0.63 ± 0.10 |
| Daeneung | 17.62 ± 1.62 | 0.95 | 51.55 ± 12.66 | 9.83 ± 12.99 | 34.07 ± 5.69 | 20.65 ± 3.77 | 22.62 ± 2.18 | 0.50 ± 0.09 |
| Hwangsil | 17.82 ± 1.77 | 1.00 | 48.79 ± 8.18 | 13.81 ± 6.00 | 35.73 ± 6.00 | 34.49 ± 7.31 | 23.69 ± 2.52 | 0.65 ± 0.12 |
건왕대추에 함유된 성분
유리당, 유기산 함량
수확 후 건조한 네 품종의 대추 열매에서 sucrose, glucose, fructose가 검출되었다. 총 유리당 함량은 ‘천황’ 149.43g·kg-1, ‘대능’ 146.75g·kg-1, ‘황실’ 144.94g·kg-1, 그리고 ‘복조’ 130.52g·kg-1 순으로 높았다. ‘복조’, ‘대능’, ‘천황’은 glucose, fructose, sucrose 순, 그리고 ‘황실’은 sucrose, glucose, fructose 순으로 함량이 높았다(Table 2).
Table 2.
Soluble carbohydrates and organic acids contents in dried fruits of ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars
| Component | Unit | Cultivar | |||
| Bokjo | Cheonhwang | Daeneung | Hwangsil | ||
| Sucrose | g/kg | 28.41 ± 0.24z by | 12.53 ± 0.06 d | 14.43 ± 0.47 c | 58.59 ± 0.93 a |
| Glucose | g/kg | 51.28 ± 0.38 c | 70.74 ± 1.04 a | 67.15 ± 0.50 b | 45.11 ± 0.70 d |
| Fructose | g/kg | 50.83 ± 0.20 b | 66.16 ± 0.86 a | 65.17 ± 0.71 a | 41.24 ± 0.56 c |
| Mannitol | g/kg | n.a | n.a | n.a | n.a |
| Sorbitol | g/kg | n.a | n.a | n.a | n.a |
| Total | g/kg | 130.52 | 149.43 | 146.75 | 144.94 |
| Malic acid | g/kg | 15.32 ± 0.29 c | 17.44 ± 0.15 b | 22.37 ± 0.29 a | 14.11 ± 0.30 d |
| Acetic acid | g/kg | 2.82 ± 0.03 a | 1.41 ± 0.00 b | 0.91 ± 0.02 c | 2.88 ± 0.01 a |
| Fumaric acid | g/kg | 0.26 ± 0.00 b | 0.23 ± 0.00 c | 0.44 ± 0.01 a | 0.23 ± 0.00 c |
| Citric acid | g/kg | n.a | n.a | n.a | n.a |
| Shikimic acid | g/kg | n.a | n.a | n.a | n.a |
| Total | g/kg | 18.40 | 19.08 | 23.72 | 17.22 |
유기산 함량은 ‘대능’ 23.72g·kg-1, ‘천황’ 19.08g·kg-1, ‘복조’ 18.40g·kg-1, 그리고 ‘황실’ 17.22g·kg-1 순으로 함유되어 있었다. 건대추의 유기산은 대부분 malic acid였고, 이어 acetic acid, fumaric acid 순으로 함량이 높았다.
총 무기성분 함량은 ‘복조’ 15.77g·kg-1, ‘황실’11.91g·kg-1, ‘대능’ 9.82g·kg-1, 그리고 ‘천황’ 8.72g·kg-1 순으로 함유되어 있었다(Table 2). 미네랄 성분 중 대량 요소로는 P, K, Ca, Mg, Na이 g·kg-1 단위로, 미량 요소로 Fe, Zn, Cu, Mn, B는 mg·kg-1 단위로 함유되어 있었다. ‘복조’와 ‘황실’은 K, Al, P, Ca, Mg 순, ‘대능’은 K, P, Al, Ca, Mg 순, 그리고 ‘천황’은 K, P, Mg, Ca, Al 순으로 높게 함유되어 있었다(Table 3).
Table 3.
Mineral contents in dried fruits of ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars
| Component | Unit | Cultivar | |||
| Bokjo | Cheonhwang | Daeneung | Hwangsil | ||
| P | g/kg | 0.96 ± 0.01z cy | 1.11 ± 0.03 b | 1.58 ± 0.03 a | 1.09 ± 0.02 b |
| K | g/kg | 8.39 ± 0.31 a | 6.30 ± 0.02 c | 6.49 ± 0.08 c | 7.48 ± 0.32 b |
| Ca | g/kg | 0.43 ± 0.01 b | 0.26 ± 0.00 d | 0.36 ± 0.02 c | 0.53 ± 0.02 a |
| Mg | g/kg | 0.41 ± 0.02 a | 0.30 ± 0.01 b | 0.31 ± 0.01 b | 0.35 ± 0.03 ab |
| Na | g/kg | 0.29 ± 0.01 a | 0.21 ± 0.01 b | 0.21 ± 0.02 b | 0.20 ± 0.01 b |
| Al | g/kg | 4.73 ± 0.76 a | 0.21 ± 0.07 b | 0.57 ± 0.14 b | 1.62 ± 0.34 b |
| Fe | mg/kg | 89.81 ± 12.57 a | 36.58 ± 1.00 b | 39.47 ± 6.34 b | 60.16 ± 5.33 b |
| Zn | mg/kg | 10.07 ± 0.72 a | 7.11 ± 0.52 bc | 4.96 ± 0.33 c | 5.61 ± 0.32 b |
| Cu | mg/kg | 5.66 ± 0.25 a | 4.87 ± 0.07 a | 4.73 ± 0.07 b | 5.78 ± 0.11 b |
| Mn | mg/kg | 5.14 ± 0.37 a | 5.85 ± 0.18 a | 5.94 ± 0.23 a | 6.00 ± 0.19 a |
| B | mg/kg | 12.45 ± 2.31 c | 20.88 ± 0.56 a | 16.08 ± 0.62 c | 26.19 ± 1.15 b |
| Ca | g/kg | 0.43 ± 0.01 b | 0.26 ± 0.00 d | 0.36 ± 0.02 c | 0.53 ± 0.02 a |
| Total | 15.77 | 8.72 | 9.82 | 11.91 | |
건대추 네 품종의 과일에 함유된 아미노산 분석 결과 분석한 22 성분 중 18성분이 검출되었고, methionine, cystine, tryptophan, taurine은 검출되지 않았다. 품종별 총 아미노산 함량은 ‘복조’ 568.4mg·L-1, 황실 553.6mg·L-1, ‘천황’ 524.1mg·L-1, 그리고 ‘대능’ 471.8mg·L-1 순으로 함유되어 있었다. 건대추 네 품종에 다량 함유된 아미노산은 asparagine, proline, GABA, arginine, aspartic acid, alanine으로 총 아미노산 함량 중 91–96%를 점유하였다(Table 4).
Table 4.
Amino acid contents in dried fruits of ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars
| Component | Unit | Cultivar | |||
| Bokjo | Cheonhwang | Daeneung | Hwangsil | ||
| Alanine | mg/kg | 12.85 ± 0.16z by | 15.66 ± 0.22 a | 6.75 ± 0.14 d | 8.14 ± 0.18 c |
| Arginine | mg/kg | 11.15 ± 0.08 c | 20.03 ± 0.44 b | 33.88 ± 0.59 a | 19.89 ± 0.50 b |
| Asparagine | mg/kg | 280.71 ± 4.04 a | 177.70 ± 1.53 d | 193.07 ± 3.92 c | 227.47 ± 5.42 b |
| Aspartic acid | mg/kg | 12.39 ± 0.30 b | 9.03 ± 0.11 c | 9.76 ± 0.17 c | 13.85 ± 0.44 a |
| GABA | mg/kg | 30.77 ± 0.26 b | 39.30 ± 0.51 a | 22.80 ± 0.56 c | 30.44 ± 0.72 b |
| Glutamic acid | mg/kg | 3.21 ± 0.17 a | 2.60 ± 0.09 b | 1.61 ± 0.05 c | 2.33 ± 0.09 b |
| Glutamine | mg/kg | 2.14 ± 0.06 c | 7.41 ± 0.09 a | 1.50 ± 0.03 d | 3.77 ± 0.16 b |
| Glycine | mg/kg | 1.87 ± 0.01 b | 2.87 ± 0.04 a | 1.83 ± 0.07 b | 1.81 ± 0.06 b |
| Histidine | mg/kg | 1.13 ± 0.04 b | 1.54 ± 0.17 a | 1.44 ± 0.07 a | 1.71 ± 0.06 a |
| Leucine | mg/kg | 2.78 ± 0.02 b | 3.12 ± 0.05 a | 2.60 ± 0.05 b | 1.67 ± 0.10 c |
| Isoleucine | mg/kg | 1.45 ± 0.03 b | 2.06 ± 0.02 a | 1.24 ± 0.04 c | 1.09 ± 0.03 d |
| Lysine | mg/kg | 1.76 ± 0.21 b | 2.93 ± 0.23 a | 1.98 ± 0.17 b | 1.53 ± 0.14 b |
| Phenylalanine | mg/kg | 1.22 ± 0.07 c | 2.03 ± 0.12 a | 1.42 ± 0.06 b | 0.98 ± 0.02 c |
| Proline | mg/kg | 193.30 ± 1.05 b | 170.59 ± 1.07 c | 234.68 ± 4.84 a | 227.89 ± 5.77 a |
| Serine | mg/kg | 5.14 ± 0.08 b | 6.09 ± 0.07 a | 4.03 ± 0.12 d | 4.54 ± 0.06 c |
| Threonine | mg/kg | 2.57 ± 0.04 c | 3.74 ± 0.06 a | 2.44 ± 0.04 c | 3.31 ± 0.08 b |
| Tyrosine | mg/kg | 1.29 ± 0.01 b | 1.68 ± 0.12 a | 1.12 ± 0.02 bc | 1.00 ± 0.05 c |
| Valine | mg/kg | 2.74 ± 0.05 b | 3.41 ± 0.04 a | 1.90 ± 0.07 d | 2.14 ± 0.06 c |
| Total | mg/kg | 568.47 | 471.79 | 524.05 | 553.56 |
네 품종의 건대추에 함유된 지방산은 탄소길이 14개에서 24개까지 범위에서 9가지 지방산이 검출되었다. 그 중 불포화지방산이 5개 성분(palmitoleic acid, myristoleic acid, linoleic acid, oleic acid, α-linolenic acid), 포화지방산이4개 성분(stearic acid, palmitic acid, myristic acid, behenic acid)이 함유되어 있었다. 지방산 함유량은 ‘복조’ 5,033.95mg·kg-1, ‘황실’ 5,025.82mg·kg-1, ‘대능’ 4,621.15mg·kg-1, 그리고 ‘천황’ 4,082.40mg·kg-1 순으로 높았다. 건대추에는 지방산 성분 중 stearic acid 함량이 가장 높았고, 이어 palmitoleic acid, palmitic acid, myristoleic acid, 그리고 linoleic acid 순으로 높은 함량을 보였다(Table 5).
Table 5.
Fatty acid contents in dried fruits ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars
| Component | Unit | Cultivar | |||
| Bokjo | Cheonhwang | Daeneung | Hwangsil | ||
| Myristic acid | mg/kg | 111.65 ± 0.76 z by | 92.26 ± 13.33 c | 139.66 ± 2.19 a | 142.64 ± 1.06 a |
| Myristoleic acid | mg/kg | 520.66 ± 8.02 a | 323.96 ± 37.68 b | 534.82 ± 10.57 a | 513.38 ± 2.59 a |
| Palmitic acid | mg/kg | 606.00 ± 9.19 b | 374.61 ± 51.14 d | 413.38 ± 1.97 c | 714.91 ± 5.06 a |
| Palmitoleic acid | mg/kg | 854.69 ± 10.33 bc | 792.87 ± 113.61 c | 892.06 ± 33.07 ab | 945.18 ± 13.34 a |
| Stearic acid | mg/kg | 1885.68 ± 44.68 b | 1916.44 ± 88.36 b | 1922.15 ± 57.33 b | 2081.31 ± 51.16 a |
| Oleic acid | mg/kg | 237.94 ± 5.11 a | 244.90 ± 34.59 a | 192.38 ± 5.74 b | 237.02 ± 5.00 a |
| Linoleic acid | mg/kg | 482.85 ± 11.79 a | 210.98 ± 28.42 d | 320.39 ± 11.55 b | 241.31 ± 2.23 c |
| a-linolenic acid | mg/kg | 264.62 ± 15.16 a | 75.36 ± 9.23 c | 135.25 ± 8.17 b | 87.48 ± 0.68 c |
| Behenic acid | mg/kg | 69.86 ± 4.16 a | 51.02 ± 5.00 b | 71.06 ± 1.83 a | 62.59 ± 2.22 a |
| Total | mg/kg | 5,033.95 | 4,082.40 | 4,621.15 | 5,025.82 |
건대추 열매에 함유된 주요 페놀성 화합물은 rutin, quercetin, gallic acid였다. ‘복조’, ‘황실’, ‘천황’에는 rutin과 quercetin이, ‘대능’에는 rutin과 gallic acid가 주로 함유되어 있었다(Table 6).
Table 6.
Individual phenolic compound contents in dried fruits of ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars
| Component | Unit | Cultivar | |||
| Bokjo | Cheonhwang | Daeneung | Hwangsil | ||
| Gallic acid | mg/kg | 11.22 ± 0.08z cy | 10.97 ± 0.04d | 30.70 ± 0.36 a | 15.70 ± 0.09 b |
| (+)-catechin | mg/kg | 9.04 ± 1.07 c | 14.30 ± 0.01 b | 19.05 ± 0.38 a | 1.70 ± 0.02 d |
| Chlorogenic acid | mg/kg | 2.52 ± 0.07 b | 3.29 ± 0.06 a | 3.47 ± 0.11 a | 2.25 ± 0.03 c |
| Caffeic acid | mg/kg | 1.85 ± 0.85 a | 0.10 ± 0.00 b | 0.85 ± 0.09 ab | 1.47 ± 0.14 ab |
| Syringic acid | mg/kg | 1.87 ± 0.41 a | 1.46 ± 0.13 a | 1.40 ± 0.02 a | 1.11 ± 0.10 a |
| (‒)-epicatechin | mg/kg | 0.84 ± 0.05 a | 0.78 ± 0.47 a | 1.26 ± 0.38 a | 2.31 ± 0.73 a |
| p-coumaric acid | mg/kg | 3.76 ± 0.15 a | 3.86 ± 0.06 a | 1.99 ± 0.03 c | 3.07 ± 0.08 b |
| Ferulic acid | mg/kg | 9.85 ± 0.64 a | 0.36 ± 0.03 c | 0.23 ± 0.02 c | 4.42 ± 1.72 b |
| Rutin | mg/kg | 55.08 ± 3.24 a | 38.19 ± 0.76 b | 54.34 ± 4.36 a | 61.73 ± 2.29 a |
| Hyperin | mg/kg | 11.52 ± 0.01 d | 12.63 ± 0.02 a | 11.93 ± 0.06 c | 12.16 ± 0.01 b |
| Isoquercitrin | mg/kg | 8.32 ± 0.29 a | 8.15 ± 0.10 a | 9.46 ± 0.84 a | 9.55 ± 0.03 a |
| Quercitrin | mg/kg | 9.52 ± 0.06 b | 11.17 ± 0.25 a | 8.81 ± 0.05 c | 11.30 ± 0.28 a |
| Phloridzin | mg/kg | 9.80 ± 0.06 a | 9.58 ± 0.00 b | 9.60 ± 0.01 b | 9.58 ± 0.00 b |
| Quercetin | mg/kg | 53.28 ± 1.69 a | 32.47 ± 0.22 b | 21.71 ± 0.22 d | 25.99 ± 0.09 c |
| Total | mg/kg | 188.47 | 147.31 | 174.8 | 162.34 |
건대추 열매에 함유된 총 페놀성 화합물 함량은 ‘대능’이 9.584g GAE·kg-1로 가장 높았으며, 이어 ‘복조’, ‘황실’, ‘천황’ 순으로 높았다. 총 플라보노이드 함량은 ‘황실’이 1.3702g CE·kg-1로 가장 높았고, 총 안토시아닌 함량은 ‘복조’가 57.4505mg C3GE·kg-1로 다른 품종에 비해 유의적으로 높았다(Fig. 2). 항산화 활성 평가 결과, DPPH 라디칼 소거능은 ‘황실’과 ‘대능’이 70.2–70.7%로 가장 높았고, ‘복조’는 69.2%, ‘천황’은 66.5%로 가장 낮게 나타났다. 반면, ABTS 라디칼 소거능은 네 품종 모두 68.3–69.2% 범위로 품종 간 유의차는 없었다(Fig. 2). 품종 간 차이를 보인 DPPH 항산화 활성은 66.5–70.7%의 범위로, 최대값과 최소값의 차이는 4.2%, 변동률은 5.9%였다. 일반적으로 항산화 활성 실험에서 5–10% 이상의 차이가 날 때 품종간 차이가 뚜렷하다고 간주된다. 따라서 본 실험의 차이는 통계적으로 유의미한 차이가 있었으나, 극적으로 다른 수준은 아니며, 품종 간 변동이 어느 정도 존재하는 정도로 해석할 수 있다. DPPH와 ABTS 항산화 활성의 품종별 차이는 항산화 성분의 친유성 및 친수성 특성이 다를 수 있음을 의미한다. DPPH 항산화 활성은 주로 지용성 항산화 성분에 반응하는 반면, ABTS 라디칼 소거법은 친수성 및 친유성 항산화 성분을 모두 측정할 수 있다. 따라서 DPPH 분석에서 나타난 품종 간 항산화 활성 차이는 각 품종이 함유한 지용성 항산화 성분, 예로 지용성 지방산, quercetin 등의 함량 차이에 기인할 수 있다. 반면, ABTS 분석에서 품종 간 차이가 유의하지 않았던 것은 네 품종의 대추가 친수성 항산화 성분, 예로 유기산, 페놀산, rutin이나 hyperin 등 플라보노이드 배당체 등이 유사한 성분 함량을 가질 가능성을 나타낸다.
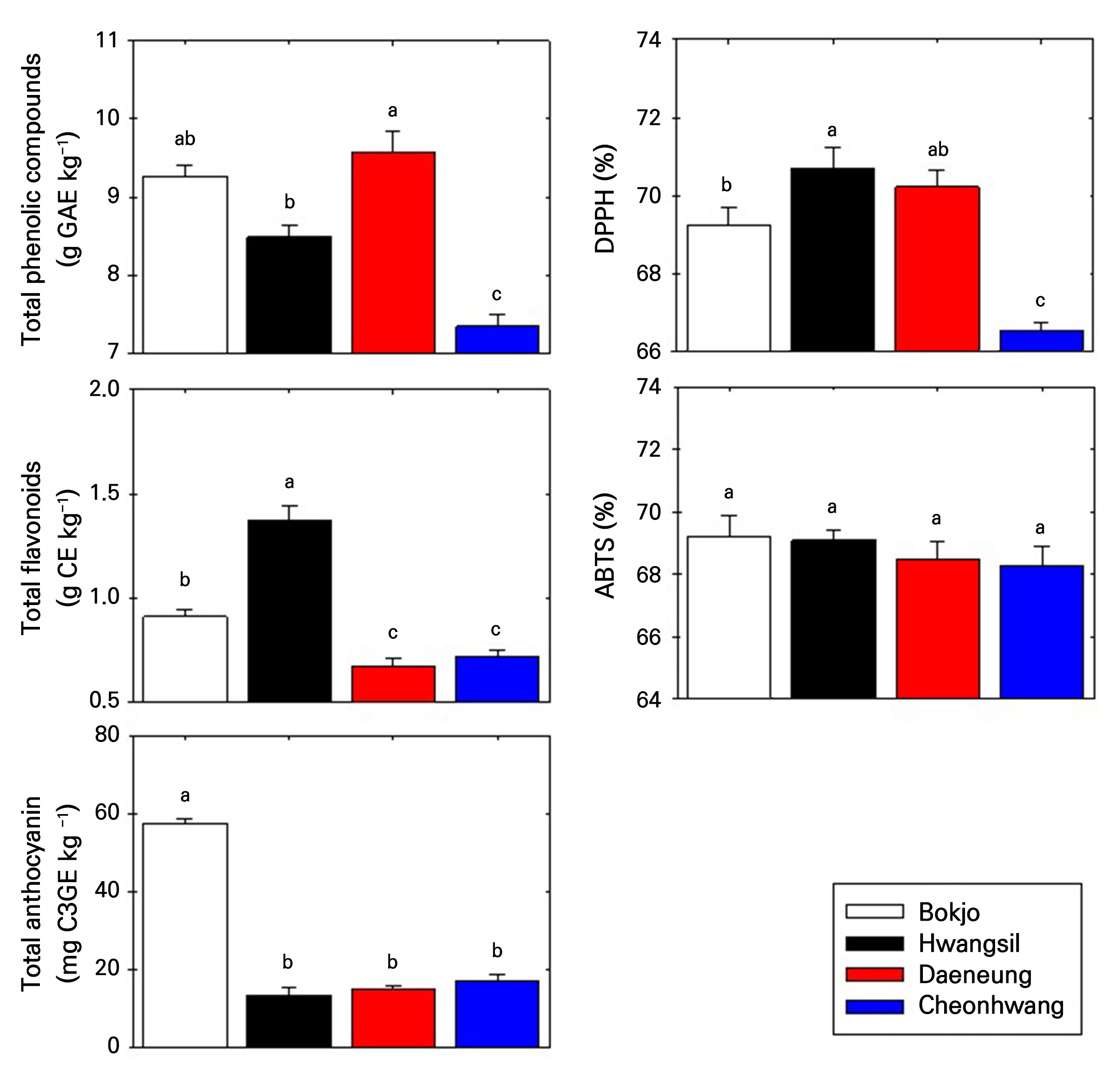
Fig. 2.
Responses of total phenolic compounds, total flavonoids, total anthocyanin, and total antioxidant activity (DPPH and ABTS) in dried fruits of ‘Bokjo’, ‘Cheonhwang’, ‘Daeneung’, and ‘Hwangsil’ jujube cultivars. Data are expressed as the mean ± SE (n=6). Means with the same letters are not significantly different from each other (p < 0.05) according to Duncan’s multiple range test.
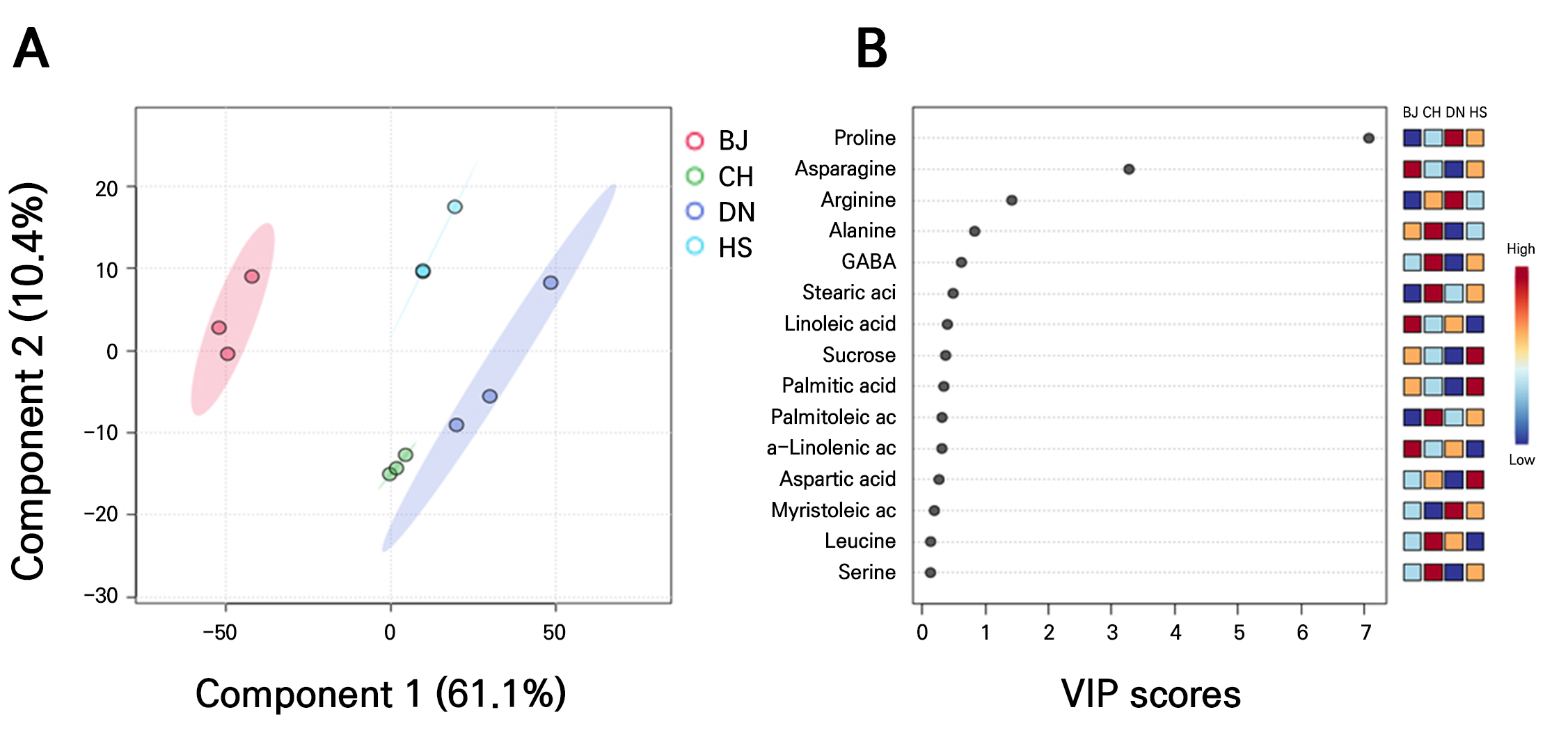
PLS-DA score plot 분석 결과(Fig. 3), 건대추 네 품종은 주성분 1(61.1%)과 주성분 2(10.4%)에 의해 명확히 구별되었으며, 이 두 성분은 전체 변이의 71.5%를 설명하였다. ‘복조’는 다른 품종과 뚜렷이 구별되는 단일 클러스터를 형성하였고, ‘황실’과 ‘대능’은 일부 성분 차이에 따라 독립된 클러스터를 구성하였으나 유사한 성분 구성을 가질 가능성을 보였다. ‘천황’과 ‘대능’은 서로 가까운 위치에 분포하며, 대사체 조성이 유사할 가능성을 보였다. 이러한 결과는 계층적 클러스터 분석 결과(Fig. 4)와도 일치하였다. VIP score는 PLS-DA 모델에서 품종을 구분하는데 중요한 역할을 하는 성분을 나타낸다(Fig. 3B). Proline, asparagine, arginine, alanine, GABA 등 아미노산 계열 성분이 가장 높은 VIP 값을 가지며, 품종 간 차이를 설명하는 주요 요인임을 보여주었다. Stearic acid, linoleic acid, palmitic acid, palmitoleic acid 등 지방산도 품종 차이에 기여하는 주요 성분이었으며, sucrose 역시 VIP 스코어가 높은 성분 중 하나로, 당 함량 차이가 품종 간 대사적 차이에 영향을 미칠 가능성이 있음을 보여주었다. VIP score 그래프의 우측에 색상 블록은 각 성분의 품종별 상대적 함량을 나타낸다. Proline, asparagine, arginine과 같은 아미노산은 ‘복조’에서 높게 나타나며, 이는 ‘복조’ 품종이 다른 품종과 뚜렷하게 구별되는 이유일 수 있다. 지방산 조성은 ‘대능’과 ‘황실’에서 높은 경향을 보였다.
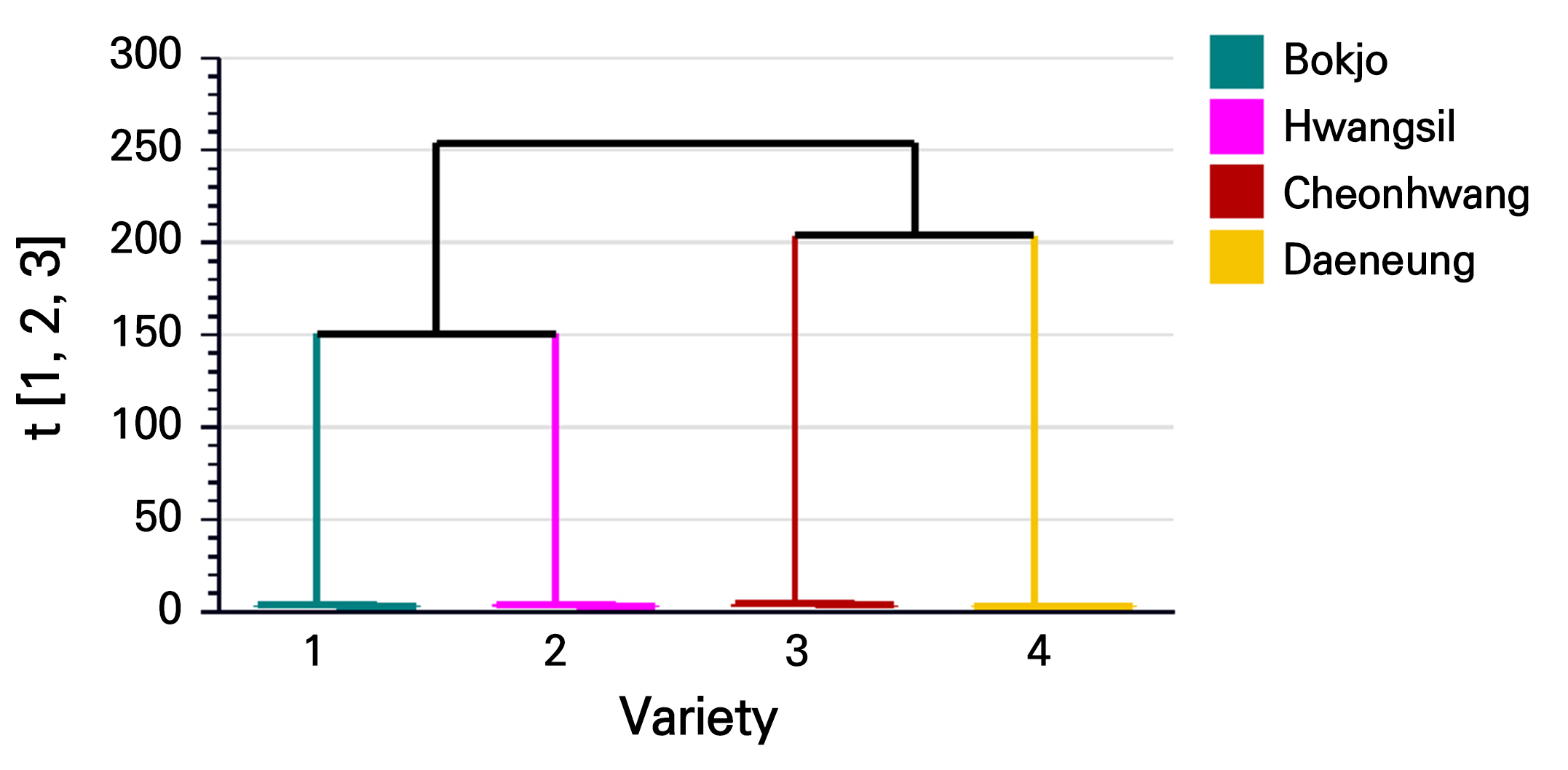
건대추 네 품종에 대해 계층적 클러스터 분석을 통하여 품종간 차이를 나타내었다(Fig. 4). 먼저, ‘복조’와 ‘황실’ 품종이 먼저 하나의 그룹으로 묶였고, 이는 이 두 품종이 다른 품종보다 유사한 구성 성분을 가지고 있음을 의미한다. ‘천황’과 ‘황실’도 별도의 그룹으로 묶였으며, 이는 이 두 품종이 ‘복조’–‘황실’ 그룹과 구별되는 특징을 공유함을 의미한다. 마지막으로, ‘복조’–‘황실’ 그룹과 ‘천황’–‘대능’ 그룹이 하나의 상위 군집으로 통합되며, 이는 네 품종이 전체적으로 유사한 경향을 보이지만, 두 개의 주요 그룹으로 나뉠 수 있음을 보여준다. 이는 ‘복조’와 ‘황실’이 ‘천황’ 및 ‘대능’과는 다른 화학적 특성을 가질 가능성이 있으며, 이는 대추 품종 간 생리활성 물질의 차이 또는 대사 경로의 차이로 인해 나타날 수 있다.
Fig. 5의 Pearson 상관관계 히트맵 분석 결과를 통해 네 품종의 건대추에 함유된 다양한 대사체, 영양성분 및 항산화 활성(DPPH, ABTS) 간의 상관관계를 확인하였다. 색상 구배는 상관계수(r)의 크기와 방향을 반영하는데, 적색 계열은 양의 상관관계, 청색 계열은 음의 상관관계를 나타낸다.
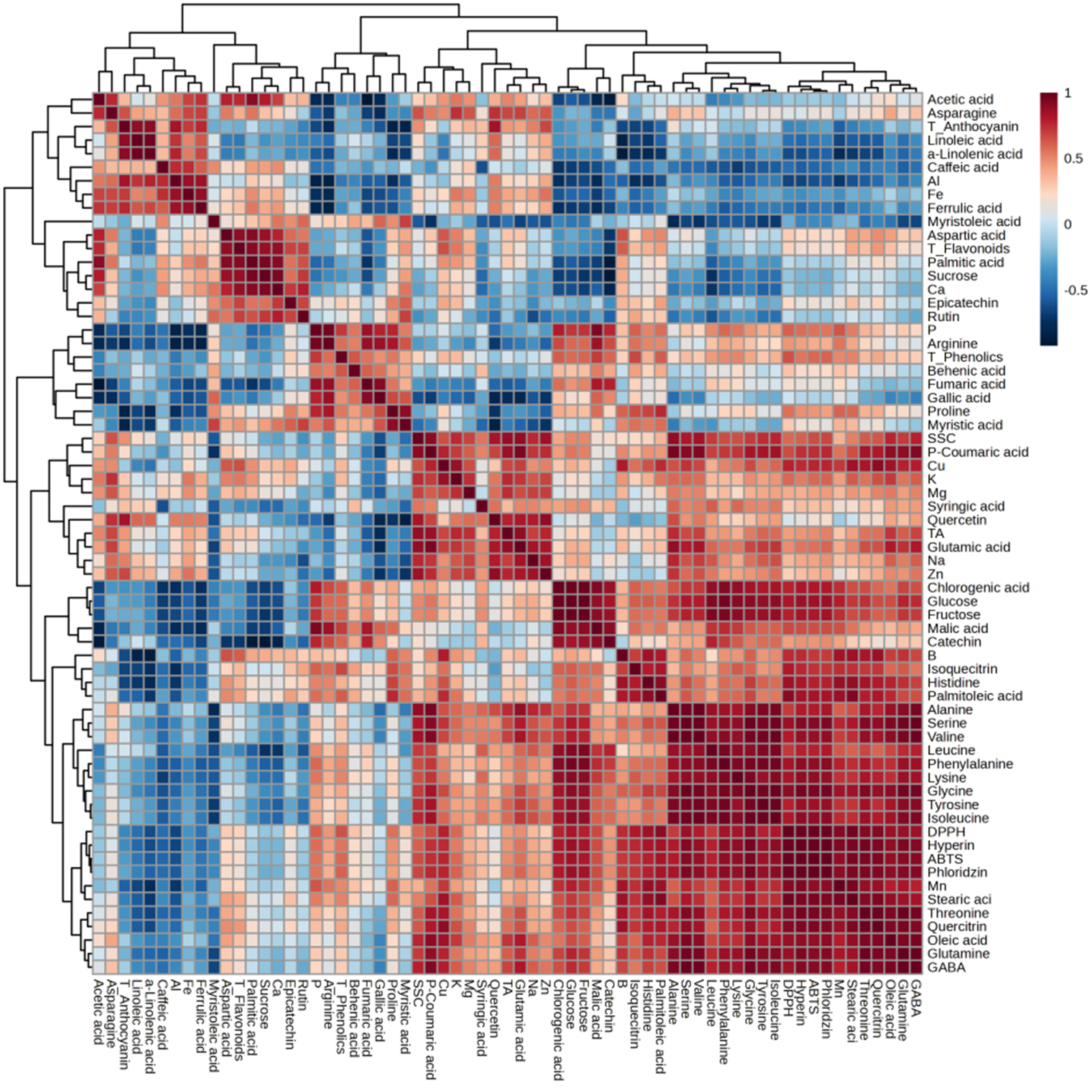
Fig. 5.
Pearson’s correlation coefficient heatmap matrix among the response variables of the fruit components of dried jujube fruits according to the cultivar. The figure legend indicates the correlation coefficient (r) results. Red and blue denote positive and negative correlation coefficients between the variables, respectively.
DPPH 항산화 활성은 quercetin, isoquercitrin, catechin 등의 플라보노이드와 chlorogenic acid, syringic acid 등 다양한 폴리페놀 화합물과 강한 양의 상관관계를 보였다. 이는 플라보노이드 및 페놀성 화합물이 DPPH 라디칼 소거능 증가에 기여함을 의미하며, 특히 quercetin 및 그 유도체가 주요한 역할을 하는 것으로 판단된다. 또한, stearic acid 및 oleic acid와 같은 일부 지방산 성분도 DPPH 활성과 양의 상관성을 나타내었는데, 이는 지용성 항산화 성분이 항산화 활성에 기여할 가능성을 보여준다. 반면, ABTS 항산화 활성의 경우 DPPH 활성과 유사한 경향성을 보이면서도, 특정 아미노산(glutamine, glutamic acid) 및 미네랄(Mn, Zn)과의 상관성이 비교적 높게 나타났다. 이는 미네랄이 항산화 시스템 내에서 보조적인 항산화 기작에 관여할 가능성을 의미하며, 아미노산 대사체 또한 항산화 활성을 조절하는 중요한 요인으로 작용할 수 있음을 시사한다. 일부 유기산(malic acid, fumaric acid) 및 당류(glucose, fructose)는 DPPH 및 ABTS 활성과 음의 상관관계를 나타내었다. 이는 해당 대사체들이 항산화 활성에 직접적인 기여를 하지 않거나, 대추의 숙성과정에서 당 축적이 페놀성 화합물의 합성과 반비례하는 경향을 보일 수 있음을 의미한다.
히트맵의 계층적 군집화 결과, 유사한 대사 경로 또는 기능적 역할을 수행하는 성분들이 그룹을 형성하는 경향이 확인되었다. 첫째, 페놀성 화합물 및 플라보노이드 클러스터로 quercetin, isoquercitrin, catechin, chlorogenic acid, syringic acid 등이 강한 양의 상관관계를 보였으며, 이는 대추의 항산화 기능과 밀접한 연관성을 시사한다. 둘째, 아미노산 클러스터로 phenylalanine, tyrosine, glutamine, arginine 등 특정 아미노산들이 유사한 패턴을 보이며 그룹을 형성하였다. 이는 단백질 대사뿐 아니라, phenylpropanoid 경로를 통한 폴리페놀 및 플라보노이드 생합성과 연계될 가능성이 있음을 시사한다. 셋째, 유기산 및 당류 클러스터로 malic acid, fumaric acid, glucose, fructose 등의 성분이 함께 그룹을 이루었으며, 이는 탄수화물 대사 및 에너지 생성과 관련된 유기산 회로(TCA cycle)와 연관될 가능성이 크다. 이 결과는 페놀성 화합물 및 플라보노이드의 생합성이 항산화 활성과 강한 연관성을 보이며, 탄수화물 대사 및 숙성 과정이 이러한 기능성 성분의 함량 변화에 영향을 줄 수 있음을 의미한다.
건대추 열매에 함유된 대사체들의 함량을 대사경로에 따라 Fig. 6에 표시하였다. shikimic acid경로를 통해 합성된 방향족 아미노산(tyrosine, phenylalanine, tryptophan) 및 그 유도체(chlorogenic acid, caffeic acid, ferulic acid)는 품종간 함량 차이가 두드러졌다. 플라보노이드 생합성 경로에서는 rutin, quercetin, catechin, epicatechin 등은 품종에 따라 서로 다른 축적 패턴을 보였다. ‘천황’은 glucose와 fructose 함량이 높았고, pyruvate 계열과 serine 계열의 아미노산인 valine, leucine, alanine, serine, glycine 함량이 높았다. ‘황실’은 sucrose 함량이 높았고, rutin, phloridzin, isoquercitrin, quercitrin, hyperin 등 플라보노이드의 함량이 다른 품종에 비해 유의하게 높았다. ‘대능’은 TCA cycle 경로 중 malic acid와 fumaric acid의 함량이 높았고, 페놀성 화합물인 gallic acid와 플라보노이드 중 (+)-catechin의 함량이 높았으나 그 외 다른 1차와 2차 대사체 성분 함량은 다른 품종에 비해 대부분 낮았다. 대조구인 재래종 ‘복조’는 pyruvate 계열의 아미노산인 valine, leucine, alanine 함량이 높았고, 페놀성 화합물로는 p-coumaric acid, caffeic acid, ferulic acid가 높았으며, 플라보노이드 중에서는 quercetin의 함량이 높았다.
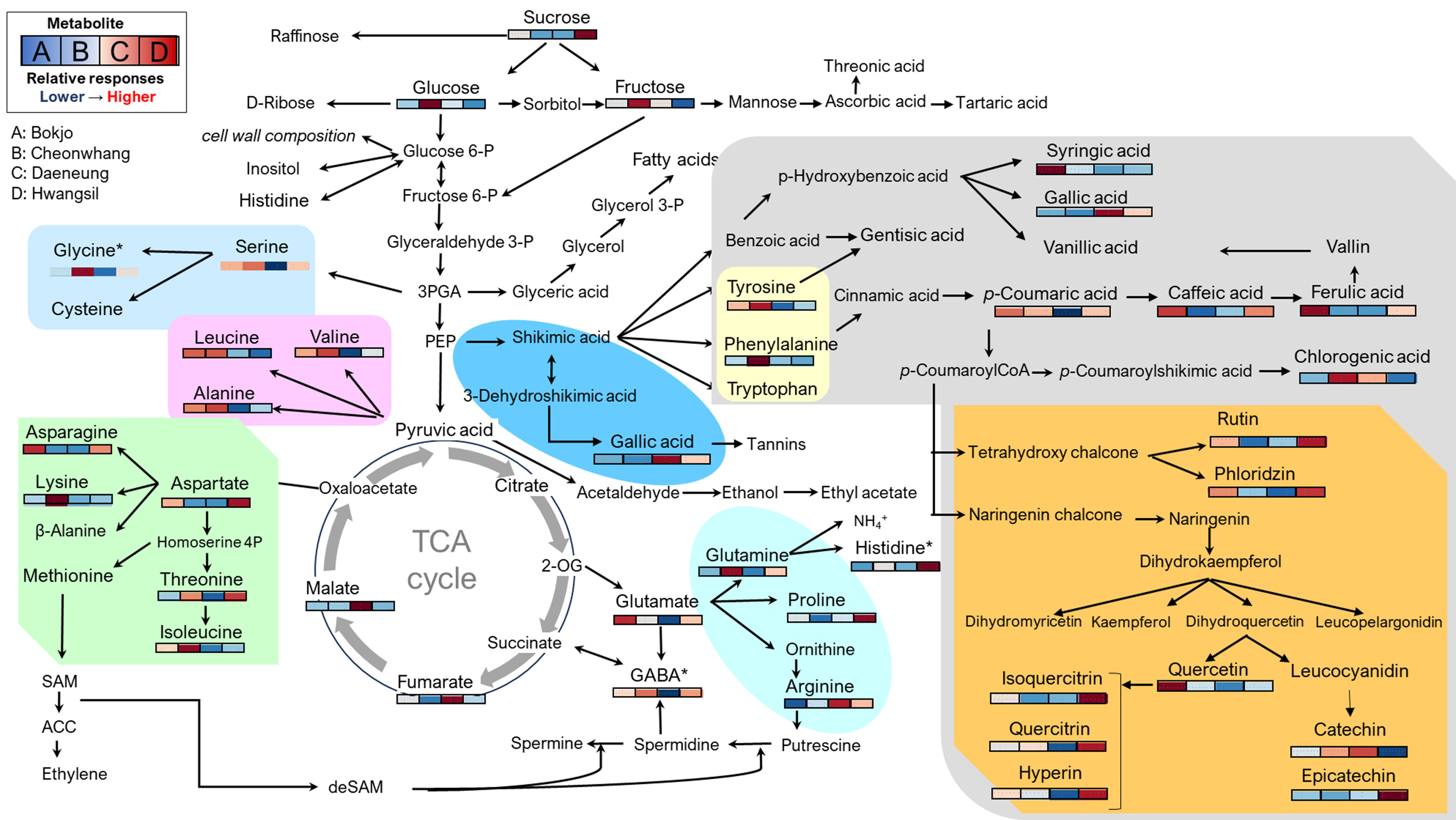
Fig. 6.
Schematic diagram of the metabolomic pathway and relative abundance of dried jujube fruits of Bokjo, Cheonhwang, Daeneung and Hwangsil.  ; Amino acids of the serine family,
; Amino acids of the serine family,  ; Amino acids of the pyruvate family,
; Amino acids of the pyruvate family,  ; Amino acids of the aspartate family,
; Amino acids of the aspartate family,  ; Aromatic amino acids,
; Aromatic amino acids,  ; Amino acids of the glutamate family,
; Amino acids of the glutamate family,  ; Shikimic acid pathway,
; Shikimic acid pathway,  ; Flavonoid biosynthesis,
; Flavonoid biosynthesis,  ; Polyphenol biosynthesis.
; Polyphenol biosynthesis.
한국에서 재래종 대추는 주로 건조하여 약용 및 식재료로 이용해 왔다. 현재 대한민국약전(KP)에는 생약으로서의 대추에 대해 대추나무 Zizyphus jujuba Miller var. inermis Rehder 또는 보은대추나무 Zizyphus jujuba Miller var. hoonensis T. B. Lee (갈매나무과 Rhamnaceae)의 잘 익은 열매로 규정하고 있다. 이 중 Zizyphus jujuba Mill. var. inermis (Bunge) Rehder는 2013년 국가표준식물목록에서 Ziziphus jujuba Mill.이라는 정명으로 변경되었고, Zizyphus jujuba Miller var. hoonensis T. B. Lee는 ‘훈’이라는 지명을 따서 명명된 것으로 보이나 국제식물명명규약(ICBN)에 따른 공식적인 학명으로 인정되지 않아 비합법명으로 분류되어 있다(Doh and Lee 2013). 왕대추나무는 기존의 대추나무를 개량한 품종들로 Ziziphus jujuba Mill. 에 속한다. 본 연구는 왕대추를 건조시켰을 때 함유 성분 및 기능 성분을 대표적인 재래종 대추인 ‘복조’와 비교하여, 왕건대추를 약용 및 기능식품으로 사용할 수 있는지 밝히고자 1차 대사산물로 당류, 유기산, 아미노산, 미네랄, 지방산을, 2차 대사산물로 페놀성 화합물, 특히 플라보노이드 성분에 초점을 맞추어 네 품종 간의 차이를 구명하였다. 본 연구와 비교할 수 있는 대추 품종별 열매의 대사산물의 차이에 대한 기존의 보고는 많지 않다. 몇몇 보고된 결과들을 비교 시에는 같은 품종이라도 연구자에 따라 대사산물의 구성 및 함량에 차이가 많았다.
‘복조’의 신선 및 건조 열매에 대한 품질특성 및 미네랄 함량을 조사한 결과(Choi et al. 2016)를 본 실험 결과와 비교 시 열매의 무게, 색도 등 외관 특성 뿐 아니라 미네랄 성분 중 Ca, P, Fe 의 함량 또한 본 실험 결과와 일치하지 않았다. Choi et al.(2016)은 건조한 ‘복조’ 열매에 Ca가 0.306g/kg, P는 0.887g/kg 그리고 Fe는 14mg/kg이 함유되어 있었다고 보고하였는데, 본 실험에서는 Ca와 P 함량은 각각 0.43g/kg, P는 0.96g/kg으로 최 등의 결과와 어느 정도 유사하나 Fe는 89.8mg/kg으로 차이가 컸다. 이러한 차이는 수확시기, 재배한 해의 기후, 재배방법, 채취 높이, 대추나무의 방향 등 다양한 요인이 영향을 미칠 수 있기 때문이다(Zhang et al. 2021; Liu et al. 2023). Zhang et al.(2021)은 37 품종의 대추에 대해 총 페놀성 화합물, 총 플라보노이드, 비타민 C, 다당류, 트리테르펜산 및 항산화 활성 등을 분석한 결과 품종별로 활성 성분과 항산화능에 차이가 있어 생산 및 기능식품 개발 시 품종 선택이 필요하다고 하였고, 항산화 활성과 높은 양의 상관관계를 가지고 있는 성분은 (+)-catechin, caffeic acid 그리고 rutin이라고 밝혔다. 본 실험에서는 이 성분들 중 (+)-catechin이 항산화 활성과 높은 양의 상관관계를 보였으나 caffeic acid와 rutin은 부의 상관관계를 보였다.
Qiu et al.(2023)은 중국계 대추의 부위별 플라보노이드의 구성성분 및 정량분석을 수행한 결과 총 101 성분의 플라보노이드 대사체를 검출하였으며, 이 중 열매의 주요 플라보노이드는 (‒)-epicatechin, (‒)-catechin, 그리고 rutin으로 각각 56.33%, 27.31%, 그리고 14.37%를 함유한다고 밝혔다. Xue et al.(2021)은 중국계 대추 20품종의 과일의 숙기별 및 부위별 대사체를 분석한 결과 미숙과에는 (+)-catechin이 47.78%, epicatechin이 24.23%, gallic acid가 12.97% 그리고 rutin이 9.93% 순으로 함유되었다가, 30% 착색기에는 epicatechin 함량이 (+)-catechin 함량보다 높아져 42.74–57.76%를 함유하며, 이어 (+)-catechin이 20.89–33.29%, gallic acid가 12.55–15.70%, rutin이 3.34–5.49% 함유되어 있다고 밝혔다. 본 연구에서 분석한 네 품종에서는 rutin(31.1%)과 quercetin(19.83%)이 다른 플라보노이드에 비해 가장 많이 함유되어 있었고, 이어 gallic acid(10.2%), hyperin(7.2%), (+)-catechin(6.6%), quercitrin(6.1%), phloridzin(5.7%) 순으로 나타났다. 반면, (‒)-epicatechin은 상대적으로 소량 함유되어 기존의 보고와는 다른 양상을 보였다. 이러한 차이는 대추의 품종, 수확시기, 재배 환경 등 다양한 요인에 기인하는 것으로 판단된다. Wang et al.(2022) 또한 야생종과 재배종 대추를 대상으로 열매의 발달 단계별 유기산 및 아스코르브산 함량을 비교한 결과, 산함량은 확대기(개화 후 30일)에 급격히 감소한 뒤 점차 증가하고, 아스코르빈산은 백숙기(개화 후 50일)에 최대치에 도달하였으며, 전 발달 단계에서 야생종이 재배종 보다 높은 함량을 유지한다고 보고하였다. 이러한 결과는 성분 함량이 품종 뿐만 아니라 열매의 생리적 성숙 단계에 따라서도 달라질 수 있음을 보여준다. 이와 유사하게 Kim et al.(2014)은 토마토 식물의 2차 대사산물 축적이 조직의 발달 단계와 생리적 기능에 따라 유기적으로 조절되며, 어린 잎, 어린 줄기 또는 미성숙 과실에는 항균 및 살충 기능의 대사산물이, 성숙 과일에는 색소 및 향미 성분이 주로 축적된다고 하였다. 이는 식물이 환경 적응 및 생존 전략의 일환으로 조직별, 시기별 특이적인 2차 대사산물 분포를 조절함을 의미한다.
건대추 네 품종이 구성 성분에 대한 차이를 PLS-DA분석과 계층적 클러스터 분석을 통해 파악한결과, 네 품종이 전체적으로 유사한 경향을 보이지만, 재래종인 ‘복조’는 왕건대추 세 품종과 거리가 있는 구성 성분을 함유하는 것으로 나타났고, ‘복조’–‘황실’ 그룹과 ‘천황’–‘대능’ 그룹으로 나뉠 수 있음을 보여주었다. 품종간 구성 성분과 이용성의 차이를 표현하는 가장 총괄적인 요인을 총 페놀성 화합물, 총 플라보노이드, 총 안토시아닌 및 항산화 활성으로 볼 수 있다. Rahman et al.(2018)은 대추 4품종을 분석한 결과, 특정 품종에서 총 페놀성 화합물과 총 플라보노이드 함량이 더 높은 유의차를 보였고 이로 인해 항산화 활성도 높았다고 보고하였다. 그리고 항산화 활성이 높을수록 전통 한의학에서 약용 가치를 더 높게 평가할 가능성이 있음을 언급하였다(Rahman et al. 2018). 본 실험 결과, 총 페놀성 화합물, 총 플라보노이드, 총 안토시아닌 함량에서는 유의한 품종 간 차이가 보였으나, 항산화 활성, 특히 ABTS 활성에서는 유의한 차이가 없었으며, DPPH 활성의 변동률 또한 5.9%로 크지 않은 차이를 보였다. 이는 항산화 활성은 성분들의 단순한 합산이 아닌 전체적인 항산화 네트워크의 작용, 개별 항산화제의 활성, 구조적 차이, 그리고 상호작용의 복합적 요인에 의해 결정되며, 특정 성분이 높다 하더라도 다른 보조적인 항산화 물질이 부족하거나 분자 간 상호작용에 의해 총 항산화 활성의 차이가 상쇄될 가능성이 있기 때문이다.
현재까지 대추 품종별로 한약재로의 이용성 차이에 대해 직접적으로 언급한 논문은 거의 없다. 본 실험 결과는 신선 과일로 섭취되고 있는 왕대추를 건조 시 재래종인 복조 품종과는 다른 활성 성분을 가지나 항산화활성은 유사하여 약용 및 기능성 식품 소재로 활용 가능성을 시사한다. 다만, 각 품종별로 함유한 활성 성분에는 차이가 있었으며, 향후 품종별 주요 활성 성분 비교, 각 품종의 약리학적 효과의 차이, 그리고 한의학적 처방에서 특정 품종의 선호 여부에 대한 연구가 필요할 것으로 사료된다.