서 언
재료 및 방법
시 약
실험재료
시료 추출물의 제조
생육 및 과실 품질 측정
총 phenol성 화합물 함량 측정
총 flavonoid 함량 측정
총 anthocyanin 함량 측정
Phenolic acid와 flavonoid 조성 및 함량 측정
항산화 활성 측정
통계분석
결과 및 고찰
과실 품질 특성
총 phenol성 화합물 함량
총 flavonoid 함량
총 anthocyanin 함량
Phenolic acid와 flavonoid 조성과 함량
항산화 활성
서 언
나무딸기(Rubus idaeus L.) 는 장미과에 속하는 관목의 열매로 유럽, 아시아, 북아메리카 등지에 널리 분포되어 있다. 나무딸기는 경남 김해 등지에서 수십 년 전부터 재배되어 왔으나 잘 알려지지 않다가 최근 생산량 및 재배면적이 매년 증가하고 있는추세이다. 나무딸기의 품질은 다양한 색상, 맛과 향기, 생리활성 성분의 함량에 좌우되며(Mikulic-Petkovsek et al., 2012) 적색을 띄는 것이 일반적이다. 그러나 안토시아닌함유량에 따라자색이나 흑색을 띄는 것도 있고, 적색 나무딸기의 돌연변이로 만들어진황색 나무딸기도 있다(Dossett et al., 2011). 복분자(Rubus coreanus Miq.) 는 장미과에 속하는 과실로 국내에서는 가장인기 있는 베리류 과실이다. 복분자는 오래 전부터민간에서 약용으로 사용되어왔으며 다양한 약리작용이 대두되면서 생과나술과 주스 등의 가공식품으로 이용도가 증가함에따라(Jeong et al., 2010; Lee et al., 2014) 2015 년 국내 총 생산량은 9,630 톤으로 산딸기 생산량1,579 톤의6배 이상 높았다(KFS, 2016). 블랙베리(Rubus fruticosus L.) 역시 장미과에 속하는관목의 열매로북아메리카와 유럽에서 가장 많이 생산되었으나 점차 세계적으로 재배지역이 증가하고 있으며(Ramos-Solano et al., 2014), 국내에서는 전북 고창, 정읍에서 주로 재배되고 있다(Cho et al., 2014). 블랙베리는 복분자와 색상과 형태는유사하지만, 복분자보다 크기가 크고 가시가 없는 품종이 개발되어 수확하기 용이한 특징이 있다(Shin et al., 2005).
나무딸기, 딸기, 복분자, 블랙베리와 같은 베리류 과실이 비만, 당뇨, 동맥경화 등 만성질환 예방에 효과적이라고 알려지면서소비자의 관심을 증가시키고 있다(Cheplick et al., 2007; Dossett et al., 2011; Ramos-Solano et al., 2014; Chung et al., 2016). 만성질환의 원인은 인체내 대사과정에서 생성되는 활성산소(Sarkar et al., 2016) 이며, 과도한 활성산소의 생성으로 산화적 스트레스가 발생되면 세포기능을 상실하게 되므로 세포를 보호하고 만성질환의 예방을 위해 항산화 성분이 풍부한 과실, 채소와같은 식물성 식품 섭취가 권장된다(Sarkar et al., 2016). 베리류 과실의 이러한 효능은 활성산소 생성을 억제하거나 소거하는anthocyanin, ellagic acid, flavonoid, phenolic acid 와 같은 phenol 성 화합물과 ascorbic acid 등에기인하는 것이 다수의 연구에서 밝혀졌다(Benvenuti et al., 2004; Bobinaitė et al., 2012; Dragišić Maksimović et al., 2013; Kim et al., 2015). Anttonen and Karjalainen(2005) 은 베리류 과실의phenol 성 화합물 함량에 영향을 미치는 요인이 많이 있지만, 품종의 유전특성(genotype) 이 가장 중요하다고 하였다.
소비자의 요구를 충족시킬 항산화 성분이 풍부한 과실을 재배하기 위해서 과실의 품종에 따른 기능성 성분의 종류 및 함량에관한 정보는 필수적인 것으로 사료된다. 최근 건강기능성 식품으로 소비자의 수요가 급증하고 있는 국내 재배종 나무딸기(Lee et al., 2014; Lee et al., 2015) 와 블랙베리(Oh et al., 2008; Jung et al., 2012; Cho et al., 2014) 는 품종에 따른 유효성분과 기능성에 관한 연구는거의이루어져 있지 않고 있다. 이에 본 연구에서는 황색 나무딸기‘Golden Harvest’, 재배종 적색 나무딸기, 야생종복분자 및 블랙베리 ‘Abundant Fruit’ 의 현재까지 보고되지 않은genotype 과 함께적색 나무딸기 ‘Canby’, 재배종 복분자, 블랙베리 ‘Thornfree’ 를 사용하여 과실의 품질특성, phenol 성 화합물의 조성과 함량(총 phenol 성 화합물, 총 flavonoid, 총 anthocyanin) 및 항산화 활성을 측정하였다. 적색 나무딸기 ‘Canby’ 는 냉동식품용 품종으로 미국에서 육종되었으나(Waldo, 1953) 이의 유효성분 함량에 관한 연구는 거의 행해지고 있지 않고(Wang and Lin, 2000), 블랙베리 ‘Thornfree’ 와 함께 국내에서 재배하여 행해진 보고는 처음이며, 재배종 복분자는 비교적 많은 보고가 있으나 야생종 복분자와 품질을 비교해 보기 위해측정하였다.
재료및방법
시 약
Folin-Ciocalteu reagent, DPPH, ABTS, potassium persulfate, trichloroacetic acid(TCA), 그리고 potassium ferricyanide 는 Sigma-Aldrich(St. Louis, MO, USA) 에서 구입하였다. Phenolic acid 표준물질로caffeic acid, p-coumaric acid, 3,4-dihy-droxybenzoic acid, 4-hydroxybenzoic acid, ferulic acid, sinapic acid, 그리고syringic acid 및 flavonoid 표준물질로epi-catechin, catechin 및 rutin 을 Sigma-Aldrich(St. Louis, MO, USA) 에서 구입하였다. Phenolic acid 와 flavonoid 분석에는HPLC 급 water 와 acetonitrile 을 Duksan(Ansan, Korea) 에서 구입하여 사용하였다.
실험재료
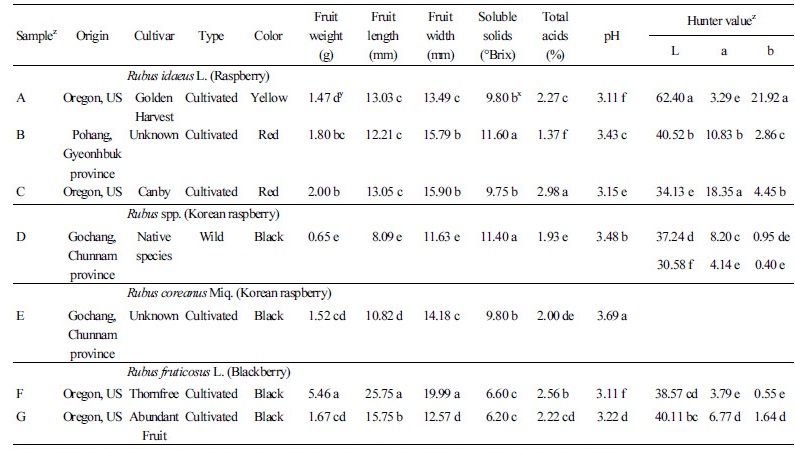
실험에는색상과 품종이 다른 나무딸기 3품종, 복분자 2품종 및 블랙베리 2품종의 과실을 사용하였다(Table 1). 나무딸기 시료는 ‘Golden Harvest’( 황색), ‘Canby’( 적색) 및 품종이 명확하지 않은 재배종(적색)을 사용하였고, 복분자 시료는 야생종과 고창농협에서 구입한2012년도 생산된 과실을 사용하였으며, 블랙베리 시료는 ‘Thornfree’ 와 ‘Abundant Fruit’ 을 사용하였다.
‘Golden Harvest’, ‘Canby’, ‘Thornfree’ 와 ‘Abundant Fruit’ 은 미국 Oregon 주에서 채집하여 냉동상태로 가져왔으며, 구입한 2012년산복분자 이외의 과실은모두 복분자시험장(전북 고창)에서 재배하였다. 시료 과실은 2012년도 6월 13-14 일에 걸쳐수확하였고, 수확 직후-20°C 에서 냉동하여 실험에 사용하였다.
시료 추출물의 제조
과실추출물은 생과 8g에 60% ethanol 32mL 를 가해 실온에서 100rpm 에서 혼합기(SLRM-3, Seoulin Bioscience, Korea) 로 3회 반복 추출하여 제조하였다. 이어서 추출물은 감압, 농축하여 ethanol 을 제거한 후 동결건조(FD8512, IlshinBioBase, Korea) 하고 냉동보관하면서 실험에 사용하였다.
생육 및 과실품질 측정
종경, 횡경 및 과중은 과실 한 개씩 총20회를 측정하였다. 당도는 과실을 분쇄기(HM-3310, Shinil, Korea) 로 분쇄한 후 얻어진 과즙을 굴절당도계(N-1E, Atago, Japan) 를 사용하여 측정하였다. 적정산도는 과즙10mL 를 0.1N NaOH 로 pH 8.3 까지 적정한 후 citric acid% 로 계산하였고, pH 는 pH meter(LE438, Mettler-Toledo, Switzerland) 를 사용하여 측정한 과즙의 pH로 나타내었다. 색도는 색도계(CR-200, Minolta Co., Japan) 를 사용하여 과피의 L, a, b 값을 측정하였다.
총 phenol성 화합물함량측정
총 phenol 성 화합물은 Arnous et al.(2001) 의 방법에 의해 측정하였다. 동결건조한 과실추출물에 증류수를 가해 용해한 것을시료액으로 하여 Folin-Ciocalteu 용액(Sigma-Aldrich, USA) 을 첨가한 후750nm 에서흡광도를 측정하였다. 다음gallic acid (Sigma-Aldrich, USA) 를 표준물질로 하여 표준곡선을 작성하고 이로부터 총 phenol 성 화합물 함량을 구하였다. 결과는mg/100g FW(fresh weight) 로 나타내었다.
총 flavonoid 함량측정
총 flavonoid 함량은 Shen et al.(2009) 의 방법에 의해 동결건조한 과실추출물에 증류수를 가해 용해한 것을 시료액으로하여415nm 에서흡광도를 측정하였다. Quercetin(Sigma-Aldrich, USA) 을 표준물질로 하여 작성한 검량선을 사용하여총flavonoid 함량을 구하고, 결과는 mg/100g FW(fresh weight) 로 나타내었다.
총 anthocyanin 함량 측정
총 anthocyanin 함량은 Pantelidis et al.(2007) 의 방법에 의해 측정하였다. 시료액은 동결건조한 과실추출물에증류수를 가해 용해한 것을 사용하였고, 다음의 식으로 계산하였다.
Contents of total anthocyanin(mg·g-1) = [(A × MW × 103 × dilution factor)] /ε.
A = (A520-A700)pH1.0-(A520-A700)pH4.5.
ε = molar extinction coefficient for cyaniding-3-glucoside(26,900).
MW = molecular weight of cyanidin-3-glucoside(449.2g·mol-1).
Phenolic acid 와 flavonoid 조성및함량 측정
Phenolic acid 와 flavonoid 는 Vasco et al.(2009) 의 방법을 참고로 하여Shimadzu Prominence HPLC(Japan) 를 사용하여 측정하였다. Syncronis C18(250mm × 4.6 mm id, particle size 5µm, Thermo, USA) column 을 사용하여 30°C 에서 과실 추출물을 분리하였고, diode array detector(DAD) 를 이용해250nm, 280nm, 및 320nm 의 파장에서검출하였다. 유속은0.5mL·min-1 으로 하여40분간 분석하였고, injection volume 은 20µL 로 하였다. 이동상으로A용액은 1% formic acid, B 용액은 acetonitrile 을 사용하였다. 0분에 A용액을 95%(B 용액5%) 로 하여20분에는 A용액70%(B 용액30%) 로 B용액의 비율을 높였고, 30 분에A용액70%(B 용액30%) 를 유지하다가, 31 분에A용액95%(B 용액5%) 로 처음과 같은 조건으로 돌아간 후, 40 분까지 A용액95%(B 용액5%) 로 column 을 세척하였다. 시료액은 동결건조한 시료를 60% ethanol 로 30mg·mL-1의 농도가 되도록 용해하였고, 모든 표준물질은 1mg·mL-1의 농도로 methanol 에 용해한후 희석하여 사용하였다.
항산화활성측정
Ferric reducing antioxidant power(FRAP) 법에 의한 항산화력은 Benzie and Strain(1996) 의 방법에 따라 혼합물을 상온의암실에서 30분간 반응시킨 후 흡광도의 변화를 593nm 에서 측정하고 trolox(Sigma-Aldrich, USA) 를 표준물질로 사용하여 µM trolox equivalent(TE)/g FW 로 표시하였다. 2,2-diphenyl-1-picrylhydrazyl(DPPH) radical 소거능은 Brand-Willians et al. (1995) 의 방법에 따라methanol 에 용해한 DPPH 용액에 시료액을 첨가한 후 515nm 에서 흡광도의 변화를 측정하고 trolox equivalent(TE)/gFW 로 표시하였다. 2,2-azinobis-(3-ethylbenzo-thiazoline-6-sulphonic acid(ABTS) radical 소거능은 Re et al.(1999) 의 방법에 따라 측정하였다. 2.45mM potassium persulfate 와 7mM ABTS 용액을 1:1(v:v) 의 비율로 혼합한 후 12-16 시간암소에 방치한 후, ABTS 용액을 methanol 로 734nm 에서흡광도치가 0.70 가 되도록희석하였다. 0.3mL 의 추출물에 3mL 의 ABTS 용액을 가하고 6분간암소에 방치한 후734nm 에서 흡광도의 변화를 측정하였다. 결과는 trolox equivalent(TE)/g FW로 표시하였다.
통계분석
실험결과의 유의성은 SPSS 12.0 version 으로 분산분석(ANOVA) 을 실시하였으며, p < 0.05 수준에서Duncan’s multiple range test 로 검정하였다.
결과및고찰
과실 품질 특성
Rubus 속 시료 과실의과중, 종경, 횡경은Table 1 과 같이 genotype 에 따라 큰 차이가있었다. 3종 나무딸기의 중량은 1.47-2.00g, 길이는12.21-13.05mm, 폭은 13.49-15.79mm 의 범위로 나무딸기 중 적색‘Canby’(C) 의 크기가 가장컸다. 나무딸기와 동일하게(Lee et al., 2014) 야생 복분자(D) 는 재배종 복분자(E) 보다 크기와 중량이 작았다. 블랙베리‘Thornfree’(F) 는 시료 과실 중 가장 컸고, 야생 복분자(D) 가 가장 작았다.
Rubus속 시료 과실의 당도, 산도, pH는 genotype에 따라 큰 차이가 있었다. 시료 과실의 당도의 경우(Table 1), 당도가 가장 높 은 genotype은 재배종 나무딸기(B)와 야생 복분자(D)가 11.40°Brix 이상으로 가장 높았고, 블랙베리 2품종이 가장 낮았다(p < 0.05). 산도는 적색 나무딸기 ‘Canby’(C)가 2.98%로 가장 높았고, 이어서 블랙베리 ‘Thornfree’(F), 황색 나무딸기 ‘Golden Harvest’(A), ‘Abundant Fruit’(G)의 순으로 높았다. 재배종 나무 딸기(B)와 야생 복분자(D)는 1.37%와 1.93%로 시료 중 가장 낮았다. 이들 결과로부터 재배종 나무딸기(B)와 야생 복분자(D)는 단맛은 강하고 신맛이 적어 맛에 대한 소비자의 기호도가 높 을 것으로 예상되었으나, 크기가 매우 작은 야생 복분자(D)는 과일로 이용하기에 적당하지 않은 것으로 사료되었다. 또한 황색 나무딸기 ‘Golden Harvest’(A)와 나무딸기 ‘Canby’(C)는 단맛은 강하지 않은데 신맛이 강하고, 블랙베리 2품종은 단맛은 없 고 신맛이 강한 특성을 가진 것으로 조사되었다. 미국에서 재배한 ‘Caroline’ 적색 나무딸기의 산도 및 당도는 1.4%, 11°Brix로 국내 재배종 나무딸기(B)와 유사하였다(Wang et al., 2009). 재배종 복분자(E)의 당도는 전보(Youn et al., 2009; Choi and Kwak, 2014)의 결과와 유사하였으나 산도는 2배 높아 차이가 있었는데, 동일한 품종이라도 재배지와 재배년도가 다르기 때문인 것으로 생각되었다. 한편 블랙베리 ‘Thornfree’(F)와 ‘Abundant Fruit’(G)의 6.2-6.6% 당도는 ‘Choctaw’, ‘Thornless Evergreen’, ‘Chester Thornless’ 및 ‘Hull Thornless’의 9.8-11.5%보다 낮은(Pantelidis et al., 2007) 것으로 조사되었다. 이 같은 결과는 genotype이 다르기 때문일 수도 있고, 착색은 충분히 되었으나 F와 G 과실의 수확이 다소 빨라 산도가 높게 측정될 수 있는 것 으로 생각되었다. 당도와 산도는 과실의 맛과 향에 기여하는 성분으로, 나무딸기는 성숙함에 따라 당도는 증가하고 산도는 감 소하는 부의 상관관계가 있다(Wang et al., 2009)고 알려져 있다.
색도도 genotype 에 따라 큰 차이가 있었다(Table 1). 황색 나무딸기 ‘Golden Harvest’(A) 의 명도와 황색도는 시료 과실 중 가장 높았고, 적색도는 가장 낮았다. 재배종 나무딸기(B) 의 명도는34.13 으로‘Canby’(C) 보다 높았으나, 적색도는 ‘Canby’(C) 보다낮아 ‘Canby’(C) 가 국내산 나무딸기보다 더욱붉게 보이는 것으로 생각되었다. 복분자(D, E) 와 블랙베리(F, G) 는 나무딸기(B, C) 보다 적색도, 황색도값이 모두 낮았고, 특히 재배종 복분자(E) 는 명도, 적색도, 황색도가 시료 과실 중 가장낮은 genotype 으로 나타났다. 이상의 결과로부터 재배종 적색 나무딸기(B) 와 재배종 복분자(E) 는 다른 과실보다단맛과신맛이 적절하여 생과로서의 품질은 가장 우수한 것으로 생각되었다.
총 phenol성 화합물함량
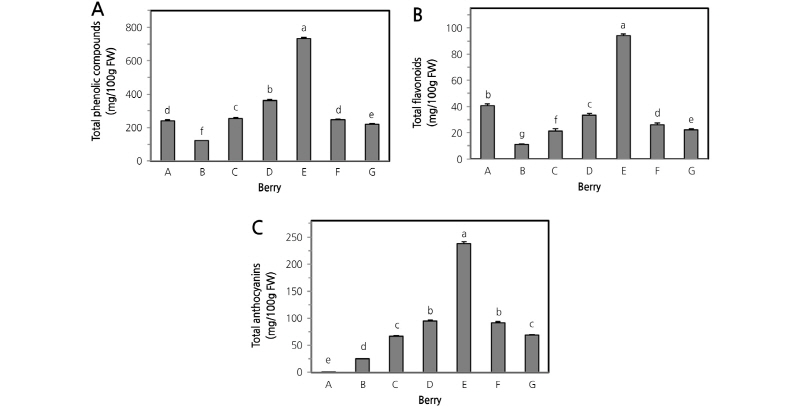
Rubus 속 시료 과실의 총 phenol 성 화합물 함량은genotype 에 따라 큰 차이가 있었다(Fig. 1A). Phenol 성 화합물은 식물계에널리 분포되어 있는 2차 대사산물로phenylpropanoid 생합성경로를 통해 생성된benzoic acid, hydroxycinnamic acid 와 같은phenolic acid, lignin 및 flavonoid 생합성경로에서 생성된 flavonoid 를 포함한다(André et al., 2009). 흑색 나무딸기의 일종인복분자(E) 가 731.08mg/100g FW 으로 가장 많았고, 다음 야생 복분자(D) 362.41mg/100g FW, 적색 나무딸기 ‘Canby’(C) 253.33mg/100g FW 의 순으로 많았다. 이어서 황색 나무딸기 ‘Golden Harvest’(A) 와 블랙베리‘Thornfree’(F) 간에는 차이가없었고, 재배종 나무딸기(B) 의 함량이 가장 적었다.
재배종 복분자(E) 의 총 phenol 성 화합물 함량은2011 년산584.81mg/100g FW(Choi and Kwak, 2014), 2008 년산560mg/ 100g FW(Jeong et al., 2010) 보다 높은 것으로 나타나 재배년도에 따라 차이가 있었다. 나무딸기 ‘Canby’(C) 의 총 phenol 성 화합물 함량은 재배종 산딸기(B) 120.94mg/100g FW 및 다른 국내 나무딸기 품종(115.70-182.97mg/100g FW) 보다 높았다(Lee et al., 2014). 미국에서 재배한 나무딸기 ‘Autumn Bliss’ 와 ‘Polka’ 의 총phenol 성 화합물함량은372 와 314mg/100g FW (Dragišić Maksimović et al., 2013) 였고, ‘Caloline’ 은 350mg/100g FW 이상(Wang et al., 2009) 이었고, 리투아니아에서 재배한 17품종 나무딸기는278.6-503.9mg/100g FW(Bobinaité et al., 2012) 의 범위로genotype 에 따라 차이가 매우컸다. 한편 황색 나무딸기 ‘Golden Harvest’(A) 는 239.03mg/100g FW 를 함유하였는데, 다른 황색 나무딸기 ‘Beglianka’ 는 391.1mg/100g FW(Bobinaité et al., 2012) 으로 이의 60% 정도로 적어genotype 에 의한 차이를 보였다. Anttonen and Karjalaine(2005), Lee et al.(2014) 의 결과에서도 나무딸기의genotype 에 따라 총 phenol 성 화합물 함량은큰 차이가있었다.
블랙베리‘Thornfree’(F) 와 ‘Abundant Fruit’(G) 의 총phenol 성 화합물 함량은 미국에서 재배한 블랙베리‘A2215’ 와 ‘Natchez’ 의 225, 210mg/100g FW(Sarkar et al., 2016), ‘Hull Thornless’ 의 236.7mg/100g FW(Benvenuti et al., 2004) 와 유사하였다. 그러나 ‘Chester’ 와 ‘Thornless Boy Sembes’ 의 함량은 351.7 와 329.1mg/100g FW(Benvenuti et al., 2004) 으로‘Thornfree’(F) 와 ‘Abundant Fruit’(G) 보다 많았다. 본 결과는 과실의총phenol 성 화합물함량이 흑색나무딸기378-714 mg/100g FW, 적색 나무딸기115-500mg/100g FW, 황색 나무딸기 240-400mg/100g FW, 블랙베리 125-351mg/100g FW 의 순으로 감소하는 전보의 결과와 유사하였다(Benvenuti et al., 2004; Anttonen and Karjalaine, 2005; Pantelidis et al., 2007; Johnson et al., 2011; Bobinaitė et al., 2012; Lee et al., 2014; Sarkar et al., 2016). 이상의 결과로부터 육종이나 건강기능성 식품제조를 위한 genotype 은 phenol 성 화합물함량이 많은 황색나무딸기(A), 야생종 복분자(D) 및 재배종복분자(E) 인 것으로생각되었다.
총 flavonoid 함량
Rubus 속 시료 과실의 총 flavonoid 함량은 genotype 에 따라큰 차이가있었다(Fig. 1B). Flavonoid 는 저분자phenol 성 화합물로phenylpropanoid 생합성경로에서 생성된p-coumaroyl CoA 와 3분자의 malonyl CoA 분자의 축합으로부터몇단계의 효소반응에 의해flavonoid 생합성경로에서 catechin, epicatechin, quercetin, anthocyanin 과 같은 다양한 종류의 flavonoid 화합물이 생성된다(Wang et al., 2012).
재배종 복분자(E) 가 94.10mg/100g FW 으로 시료 중 가장 높았고, 다음은 황색 나무딸기 ‘Golden Harvest’(A), 야생 복분자(D), 블랙베리‘Thornfree’(F), ‘Abundant fruit’(G) 의 순서로 높았다. 재배종 복분자(E) 의 총 flavonoid 함량은 2011 년 재배한복분자 함량97.51mg/100g FW(Choi and Kwak, 2014) 과 재배년도는달라도 차이는 크게 없었다. Anttonen and Karjalaine (2005) 도 산딸기의quercetin 함량이 2001 년도와 2002 년도로 재배년도가 다를 때genotype 에 따라차이가 있는경우도 있고, 없는 경우도 있다고 보고하였다. 일반적으로 베리류 과실의 phenol 성 화합물 함량은 유전적 및 환경적 영향을 받는 것으로 알려져 있다. 낮과 밤의 기온이 높을수록(Wang and Zheng, 2001), 이산화탄소 농도(Wang et al., 2003) 가 높을때 딸기의 phenol 성 화합물 함량과 항산화능은 증가하였다. 일광조사 역시 중요한 영향인자로, 광합성으로부터 합성된 탄소의 20% 가 생장호르몬, phenol 성 화합물과 같은2차 대사산물 합성에 이용된다(Bentley, 1990).
Lee et al.(2014) 의 결과에서도적색 나무딸기의 genotype 에 따라총flavonoid 함량은 큰 차이가 있었다. Flavonoid 는 식물체내에서 색소, 신호전달물질 및 다양한 생물학적 기능을가지며 UV조사, 온도변화, 해충, 영양물질이나 수분결핍 및 산화와같은 스트레스로부터 식물을 보호한다(Liu et al., 2013). 쌀(Lenka et al., 2011) 과 감자(André et al., 2009) 를 수분이 결핍된 상태로 재배했을 때flavonoid 생합성경로와 관련한 유전자발현의 증가로 flavonoid 함량이 증가하여 flavonoid 는 스트레스에 반응하는 물질임이 확인되었다. Flavonoid 와 hydroxycinnamic acid 와 같은 phenolic acid 화합물은 UV-B 가 조사되는 부위에 농도가 신속하게 증가하여 빛을 차단하는 것으로 알려져있다(Burchard et al., 2000). UV-B 는 290-320nm 파장의 자외선의 일종으로 DNA이나단백질 등을 손상시키므로피부에 조사되면 노화, 화상, 각종 피부질환의 원인으로 작용한다. 이와 같은 사실로부터 재배종 복분자(E), 황색 나무딸기 ‘Golden Harvest’(A) 및 야생 복분자(D) 와 같이flavonoid 함량이 높은 과실은 미백효능이 있는 기능성 화장품 원료로서의 유용성도 높은 것으로 사료되었다.
총 anthocyanin 함량
Rubus 속 시료 과실의 총 anthocyanin 함량은genotype 에 따라큰 차이가 있었다(Fig. 1C). Anthocyanin 은 베리류 과실에서높은 항산화능을 가진 주요 phenol 성 화합물이다(Kula et al., 2016). 재배종 복분자(E) 는 237.81mg/100g FW 으로 총 antho-cyanin 함량이 가장 많은genotype 인 것으로나타났고, 다음은 야생 복분자(D) 와 블랙베리 ‘Thornfree’(F) 가 94.99, 91.96mg/ 100g FW 으로 차이없이 많았다. 이어서 적색나무딸기‘Canby’(C) 는 블랙베리 ‘Abundant fruit’(G) 와 유사하였고(p < 0.05), 재배종 산딸기(B) 는 anthocyanin 을 함유한 시료 과실 중 함량이 가장 적었다. 색도 측정의 결과(Table 1) 에서 적색 재배종 나무딸기(B) 는 ‘Canby’(C) 에비해 높은 명도와 낮은 적색도를보였는데 이는anthocyanin 함량이 C에 비해적었기 때문인것으로 나타났다. Anttonen and Karjalaine(2005), Lee et al.(2014), Kula et al.(2016) 의 결과에서도나무딸기의 genotype 에 따라총 anthocyanin 함량은큰 차이가 있었다. 딸기(Kim et al., 2015), 오디(Choi et al., 2012) 및 블루베리(Cardeñosa et al., 2016) 의 anthocyanin 함량도 genotype 간 차이가컸다.
흑색 나무딸기의 일종인 복분자(E) 의 총 anthocyanin 함량은 적색나무딸기 C와 B보다 각각3.6 배, 9.6 배 높았는데, Kula et al.(2016) 의 결과에서도 흑색 나무딸기의 총 anthocyanin 함량은 적색 나무딸기 품종보다 4.6-11.4 배 높았다. 적색과 흑색 나무딸기는 cyanidin-3-rutinoside, cyanidin-3-glucoside 등 동일한 anthocyanin 화합물을 함유하기도 하지만, 흑색 나무딸기에만다량존재하는 cyanidin-3-xylosylrutinoside 와 같은anthocyanin 화합물도 보고되었다(Kula et al., 2016).
이탈리아 남부지역에서 재배한 7종의 블랙베리 중 ‘Smooth Stem’, ‘Darrow’, ‘Chester’, ‘Hull Thornless’ 및 ‘Black Satin’ 품종에는 67.4-88.7mg/100g FW 범위의anthocyanin 이 함유되어 있어(Benvenuti et al., 2004) ‘Thornfree’(F) 와 ‘Abundant Fruit’ (G) 와차이가 크지 않았다. 그러나 ‘Black Diamond’, ‘Thornless Boy Sembes’ 의 블랙베리 과 실내anthocyanin 함량은각각119.3, 126.9mg/100g FW(Benvenuti et al., 2004) 으로 총 phenol 성 화합물과 총 anthocyanin 함량이 높은 품종으로 보고되었다. 그리스에서 재배한 ‘Choctaw’, ‘Thornless Evergreen’, ‘Chester Thornless’ 및 ‘Hull Thornless’ 에는125.6-152.2mg/ 100g FW의 총 anthocyanin 이 함유되어 있어(Pantelidis et al., 2007) ‘Thornfree’(F), ‘Abundant Fruit’(G) 보다1.3-2 배정도 높았다.
적색 나무딸기 ‘Canby’(C) 의 총 anthocyanin 함량은 66.59mg/100g FW 로 재배종 산딸기(B) 및 국내 나무딸기의 함량 12.63-30.48mg/100g FW(Lee et al., 2014) 보다 2-5 배나 높았다. 또한 ‘Canby’(C) 는 이탈리아 남부 지방에서 재배한 ‘September’, ‘Summer’ 의 함량29.2, 41.2mg/100g FW(Benvenuti et al., 2004), 미국에서 재배한 ‘Caroline’ 45mg/100g FW(Wang et al., 2009), Norway 에서 가공용으로 가장 중요한적색나무딸기 품종인 ‘Veten’ 56.6mg/100gFW 및 생과로 이용되기 적당한 품종으로 알려진 ‘Malling Admiral’, ‘Malling Orion’, ‘Glen Lyon’ 및 ‘Glen Ample’ 의 함량33.0-40.7mg/100g FW(Haffner et al., 2002) 보다 높은 것으로 나타났다. 본결과는 흑색 나무딸기가 최대494mg/100g FW 으로anthocyanin 함량이 가장 높고, 다음블랙베리 150mg/100g FW 이하, 적색 나무딸기20-130mg/100g FW, 황색 나무딸기0-3.4mg/100g FW 의 순으로 보고된 전보의 결과와 유사하였다(Anttonen and Karjalaine, 2005; Pantelidis et al., 2007; Bowen-Forbes et al., 2010; Johnson et al., 2011; Bobinaité et al., 2012).
적색과 흑색 나무딸기의 중요한 색소물질인 anthocyanin 은 flavonoid 생합성경로를통해 합성된pelagonidin, cyanin, delp-hinidin 의 3가지anthocyanidin(anthocyanin 의 aglycone) 이 당화되어 만들어진다(Lim et al., 2011; Wang et al., 2012). 자색을띄는꽃과 과실에서 anthocyanin 합성경로에 대해서는 많은 연구가 행해져 왔으나, 이에 비해anthocyanin 색소가 합성되지 않아 황색을 띄는 원인에 대해서는 잘알려져 있지않다. Carvalho et al.(2013) 은 taxifolin 과 같은 생합성경로 저해물질이 다량 축적되면 무색의 leuanthocyanidin 에서 색소인anthocyanidin 으로바뀌는 단계에서 유전자발현이 저해되어 최종적으로 antho-cyanin 을 합성하지 못한다고 추정하였고, Docett et al.(2011) 은 흑색나무딸기에서 돌연변이가 anthocyanin 합성을 저해한다고 하였다. 딸기의 경우도 anthocyanin 생합성경 로중 돌연변이gene 에 의해 황색을 띄는 품종(‘Yellow Wonder’) 이 생긴다(Xu et al., 2014). 이상의 결과로부터 적색 나무딸기‘Canby’(C) 는 산도가 높아(Table 1) 생과로 먹기는 적당하지 않으나총phenol 화합물과 총anthocyanin 함량이 많으므로 신맛을 보완하여 주스나 요구르트 등의 건강기능성 식품 제조에 적당한 품종으로 사료되었다. 한편황색 나무딸기는 적색 나무딸기보다 고혈압 및 당뇨 억제효과(Cheplick et al., 2007) 가 더 높았다는결과로부터 황색 나무딸기 ‘Golden Harvest’(A) 는 의약품 원료로서도 활용가치가 높은 것으로 생각되었다.
Phenolic acid 와 flavonoid 조성과 함량
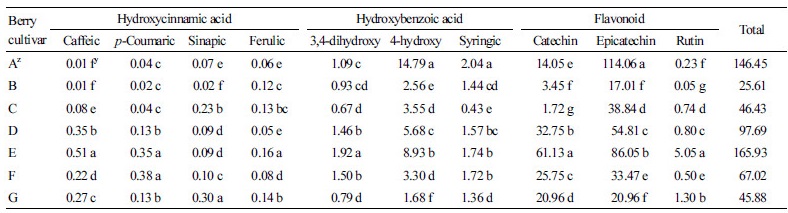
Rubus 속 시료 과실의 phenolic acid 와 flavonoid 화합물의 조성과함량은genotype 에 따라큰 차이가 있었다(Table 2). Hyd-roxylcinnamic acid 계 phenolic acid 로는 caffeic acid, p-coumaric acid, sinapic acid 및 ferulic acid 가, hydroxybenzoic acid 계 phenolic acid 로는3,4-dihtdroxybenzoic acid, 4-hydroxybenzoic acid 및 syringic acid 가 검출되었다. 검출된phenolic acid 와 flavonoid 화합물 총량은 재배종 복분자(E) 가 시료 중 가장 높았으며, 다음은 황색 나무딸기 ‘Golden Harvest’(A), 야생 복분자
(D), 블랙베리 ‘Thornfree’(F) 의 순으로 높았다. 4-hydroxybenzoic acid 가 검출된 phenolic acid 중 함량이 가장 많았고, 다음은syringic acid 가 많았다. Obón et al.(2011) 의 보고에서는 적색 나무딸기에서 caffeic acid, 3,4-dihydroxybenzoic acid, 4-hyd-roxybenzoic acid 및 syringic acid 가 검출되었으나, ferulic acid 는 검출되지 않았다. Zhang et al.(2010) 은 적색과 황색 나무딸기 7품종에서 caffeic acid, chlorogenic acid, p-coumaric acid, ferulic acid, gallic acid, gentisic acid 및 4-hydroxybenzoic acid 가 검출되었고, 이중 ferulic acid 와 gentisic acid 의 함량이 가장 높았다고보고하였다. Carvalho et al.(2013) 은 적색과 황색나무딸기에서caffeic, p-coumaric 및 ferulic acid 가 주요phenolic acid 라고 하였고, Cheplick et al.(2007) 은 다양한 색상의 나무딸기의 주요phenolic acid 는 procatechuic acid 와 coumaric acid 라고 보고하였다. 이와 같이 연구 결과에 따라 나무딸기 중의phenolic acid 조성과 함량이 다른 것은 분석조건에 따라검출되는 phenolic acid 의 종류와 검출량이 달라질 수 있기 때문인 것으로 사료되었다. 한편‘Anne’ 황색 나무딸기에서 4-hydroxybenzoic acid 함량이 적색 산딸기보다 3-10 배 정도 많았다고 하였는데, 본 연구에서도 황색산딸기 ‘Golden Harvest’(A) 의 4-hydroxy benzoic acid 함량이가장 많은 것으로 나타나 일치하였다(Zhang et al., 2010).
Flavonoid 측정결과, 모든 시료 과실에서 epicatechin, catechin 및 rutin 이 검출되었는데epicatechin 함량이 phenol 성 화합물중 가장 높았고, 다음은 catechin 이 높았으며, rutin 은 미량 함유되어 있었다. 황색산딸기 ‘Golden Harvest’(A) 는 epicatechin 을 114.06mg/100g FW 함유하고 있어 가장 함량이 많은 genotype 이었고, 다음은 재배종 복분자(E) 86.05mg/100g FW, 야생복분자(D) 의 순서로 높았다. Carvalho et al.(2013) 의 보고에서도 epicatechin 은 4품종의 나무딸기에서 30-40mg/100g FW, 5 품종의 황색 나무딸기에서25-30mg/100g FW 범위로 검출되어 phenol 성 화합물 중 함량이 가장 높았다. 황색 나무딸기(A) 의 epicatechin 함량은 Carvalho et al.(2013) 의황색나무딸기 결과와 차이가 있었으나, 재배종 나무딸기(B) 와 ‘Canby’(C) 의 함량은 각각17.01, 38.84mg/100g FW 으로‘Tulamen’, ‘Sugana’, ‘Autumn Bliss’ 및 ‘Heritage’ 품종의 적색나무딸기와 유사하였다(Carvalho et al., 2013).
또한 rutin 의 경우 황색 나무딸기 ‘Fall Gold’ 가 2.2mg/100g FW 으로 시료 중 가장 많았고, 이를 제외한나무딸기 품종은0.2-1.0mg/100g FW(Carvalho et al., 2013) 의 범위로 함유되어 있어 재배종 복분자(E) 이외의 과실의 함량과 유사하였다.
Dragišić Maksimović et al.(2013) 도 ‘Autumn Bliss’ 와 ‘Polka’ 나무딸기에서epicatechin > catechin > rutin 의 순서로검출되었다고 하였으나, epicatechin 함량은 4.28, 3.55mg/100g FW 으로 Carvalho et al.(2013) 의 보고와 본 연구에서조사된 함량보다 매우 적은 경향을 보였다. 이상의 결과로부터 황색 나무딸기(A) 와 재배종복분자(E) 는 다른genotype 보다 epicatechin 과 catechin 을 다량 함유하고 있어 육종 및 건강기능성 식품제조에 가장 적당한 것으로 생각되었다.
항산화활성
Rubus 속 시료 과실의 항산화 활성은 genotype 에 따라 큰 차이가 있었다. FRAP 법에 의한 항산화 활성은 재배종 복분자(E) 가 363.51uM TE/g FW 로 시료 중 가장 높은 genotype 였고, 다음은 야생 복분자(D), 블랙베리 ‘Thornfree’(F), 적색 나무딸기‘Canby’(C) 의 순서로 높았다(Fig. 2A). 황색 나무딸기‘Golden Harvest’(A) 는 61.71µM TE/g FW 로 가장낮았다. FRAP 법에의한 항산화 활성측정 결과는 총 anthocyanin 결과(Fig. 1C) 와 유사한 경향을 보였다. Lee et al.(2014) 도 FRAP 법에 의한 항산화활성은 총phenol 성 화합물과 anthocyanin 함량이 관련이 있다고 하였다.
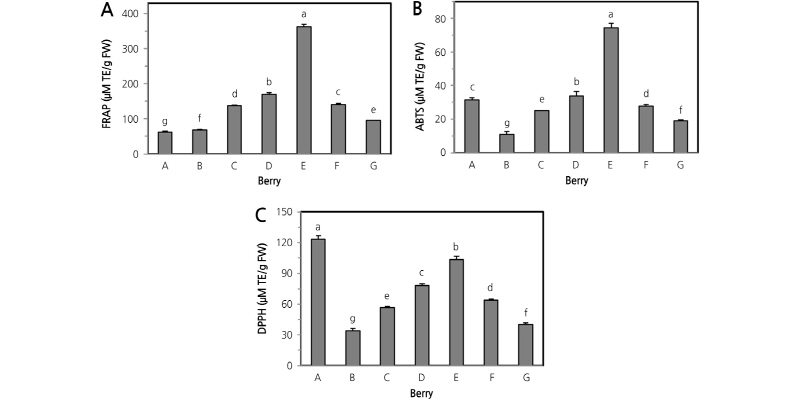
Fig. 2.
Antioxidant activities in berry fruits. Bars with different letters are significantly different at the p < 0.05 byDuncan’s multiplerangetest(n =3).TE:Troloxequivalent.FW:freshweight.A,FRAP(ferricreducingantioxidantpower);B,ABTS [2,2-azinobis-(3-ethylbenzo-thiazoline-6-sulphonic acid)] free radical scavenging activity; C, DPPH (2,2-diphenyl-1-picrylhydrazyl) free radical scavenging activity. Refer to berry cultivars of Table 1.
ABTS radical 소거능은 재배종복분자(E) 가 가장높았고, 이어서 야생 복분자(D), ‘Golden Harvest’(A), ‘Thornfree’(F), ‘Canby’(C) 의 순서로 높았다(Fig. 2B). ABTS radical 소거능의 결과는 총 phenol 성 화합물과 총 flavonoid 결과(Fig. 1A and 1B) 와 유사한 경향을 보여 황색산딸기 ‘Golden Harvest’(A) 가 가장 낮았던FRAP 법에 의한 결과와 차이가 있었다. 이는 FRAP 법과 ABTS 법의 반응구조가 다르기 때문인 것으로 사료되었다. FRAP 법은 항산화물질과 반응시 Fe3+가 Fe2+로 환원되어2,4,6-tris(2-pyridyl)-s-triazine 과 결합해 청색으로 나타나는 환원력을 측정(Benzie and Strain, 1996) 하며, ABTS 법(Re et al., 1999)과 DPPH 법(Brand-Williams et al., 1995) 은 free radical 소거능을 평가하는 방법이다.
DPPH radical 소거능은 황색 나무딸기‘Golden Harvest’(A) 가 가장 높아FRAP 법에 의한항산화 활성 결과와반대로 나타났으나ABTS radical 소거능 결과와는 유사하였다(Fig. 2C). 이어서 재배종복분자(E), 야생 복분자(D), 블랙베리(F), 나무딸기(C) 의 순으로 높았다. 황색 나무딸기(A) 에는epicatechin 과 4-hydroxybenzoic acid 함량이 시료 중 가장높았던 결과(Table 2)로부터 flavonoid 나 phenolic acid 와 같은phenol 성 화합물이 anthocyanin 보다free radical 소거에더 효과적이며, 특히DPPH radical 소거와 관련이 높은 것으로 추측되었다. Bowen-Forbes et al.(2010) 은 anthocyanin 을 함유하지 않은 ‘Golden’ 황색 나무딸기의 지질과산화 활성은anthocyanin 을 다량 함유한 자메이카산 흑색 나무딸기보다 2배 이상 높았다고 하여 본DPPH radical 소거능 결과와유사하였다. Plumb et al.(1998) 은 catechin 화합물의 free radical 소거능 및 다양한 산화 억제 효과에 대해 보고하였다. Zhang et al.(2010) 의 보고에서도 황색 나무딸기 ‘Anne’ 과 ‘Fall Cold’ 의 총 phenol 성화합물은 적색 나무딸기보다 크게낮았으나 DPPH radical 소거능은 적색 나무딸기와 차이가 없었다고 보고하였다.
나무딸기(Zhang et al., 2010) 와 블랙베리(Sarkar et al., 2016) 의 결과에서도 genotype 에 따라 항산화 활성은 큰 차이가있었다. Anttonen and Karjalainen(2005) 는 나무딸기의 항산화능은 총 phenol 성 화합물 함량과 직접적으로 관련이 높은 것으로 보고되어 왔으므로, 나무딸기의 항산화능을높이기 위한genotype 을 선정할때 총 phenol 성 화합물의 함량은 신뢰할 수 있는 특성이라고 하였다. 본 연구결과에서도 적색과 흑색 나무딸기, 복분자, 블랙베리 과실의 항산화능은 총 phenol 성 화합물의 함량과 일치하였다. 그러나 황색 나무딸기와 같이anthocyanin 을 함유하지 않고flavonoid 함량이 높은 과실의항산화능은 총flavonoid 화합물 함량이 총 phenol 성 화합물보다 더욱 관련이 있는 것으로생각되었다.
Rubus 속 과실에는 phenol 성 화합물이 다량 함유되어있어 건강기능성식품으로 소비자의 관심이 높은 과실이다. 이에 과실생산자는 소비자의 건강증진효과에 대한기대를 충족시킬 수 있도록 유효성분 함량이많은 품종의선택에 관심을 가질 필요가있을 것으로 생각된다. 특히 황색 나무딸기와 야생복분자는 재배종 복분자에비해유효성분 함량은 적지만 다른 Rubus속 과실보다 높으므로 육종자원으로서 가치가 높은 것으로 사료된다. 본 과실별 품종에 따른 유효성분 함량 및 항산화 활성 차이에 대한 결과는 과실의품종선택, 육종, 건강기능식품, 의약품 및 화장품 원료 등 다양한 분야에서 사용될 수 있을것으로 사료된다.