서 언
재료 및 방법
덩굴쪼김병균의 분리 및 동정
최적배지 선발
접종원 준비
식물 재배
덩굴쪼김병균 접종
발병 및 병조사
결과 및 고찰
균주 동정
GR 균주의 Race 검정
최적배지 선발
시판 멜론 품종의 덩굴쪼김병에 대한 저항성
생육 시기에 따른 멜론 덩굴쪼김병 발생
뿌리 상처에 따른 멜론 덩굴쪼김병 발생
침지시간에 따른 멜론 덩굴쪼김병 발생
접종원 농도에 따른 멜론 덩굴쪼김병 발생
재배 온도에 따른 멜론 덩굴쪼김병 발생
서 언
최근 고품질 소비추세와 웰빙 식품의 선호에 따라 멜론의 대중적인 소비가 증가하고 있다(RDA, 2006). 멜론(Cucumis melo L.)은 박과 작물에 속하는 1년생 식물로 수분을 제외한 대부분의 성분이 탄수화물이며, 이 중 대부분은 가용성 당 성분이고 식이섬유도 소량 함유되어 있다. 수확하여 후숙을 시키면 단맛과 특이한 향기가 나는 것이 멜론의 주요 특징이다. 멜론이 고온, 건조를 요하는 작물이기 때문에 우리나라에서 생산되는 멜론은 대부분 시설 내에서 토경 재배를 하여 연중 출하되고 있다. 일반적으로 멜론은 다른 과실에 비하여 생육기간이 짧아 전업으로 재배할 경우 봄・여름・가을・겨울의 연간 4회 재배가 가능하다(Cha et al., 2013).
Fusarium oxysporum은 형태상으로는 구별이 되지 않지만 적어도 80개 이상의 분화형을 가지며 각각의 기주에 높은 특이성을 나타낸다고 알려져 있다. 하지만 최근 오이나 수박 등 박과 작물 간에 교차 병원성을 나타낸다는 보고도 있다(Cafri et al., 2005; Owen, 1955; Zhou and Everts, 2007). 멜론 덩굴쪼김병은 Fusarium oxysporum f. sp. melonis에 의해 발생하며, 세계적으로 심각한 수량 손실을 일으켜 멜론 재배에서 가장 피해가 큰 병해 중 하나이다. 덩굴쪼김병균은 식물의 뿌리로 침입한 후, 기주의 도관에 정착하여 식물에 시들음 증상을 나타내고 결국 유묘나 성숙한 식물체가 고사하게 된다. 그리고 이 병원균은 토양에 한 번 유입되면 끊임없이 생존하여 연작장애를 일으킨다(Banihashemi et al., 1975). 하지만 멜론의 덩굴쪼김병을 방제할 수 있는 살균제가 거의 없는 실정이므로 저항성 대목 품종을 이용한 접목 재배 방법이 가장 널리 사용되고 있으나 이것은 노동력이 많이 소요되는 단점이 있다. 따라서 환경친화적인 저항성 품종의 재배가 효율적인 방제 방법으로 알려져 있다(Freeman et al., 2002).
멜론에 덩굴쪼김병을 일으키는 F. oxysporum f. sp. melonis에는 4개의 race가 보고되어 있다(Risser et al., 1976). Race 0, 1, 2, 그리고 1, 2인데, 저항성 유전자가 없는 감수성 품종에만 병을 일으키는 race 0, 감수성 품종과 Fom-1 저항성 유전자를 가지는 저항성 품종에 병을 일으키는 race 1, 감수성 품종과 Fom-2 저항성 유전자가 도입된 저항성 품종에 병을 일으키는 race 2, 그리고 Fom-1과 Fom-2 둘 다 가지는 품종에도 병을 일으키는 race 1, 2(race 3)가 보고되어 있다. Race 1, 2는 1976년 Southern California에서 처음 보고되었으며, 병징에 따라 식물이 고사되기 전에 황화증상이 나타나는 race 1, 2y와 식물 고사되기 전에 황화증상 없이 시들음 증상이 나타나는 race 1, 2w로 구분하기도 한다(Bouhot, 1981). Fom-1과 Fom-2 저항성 유전자는 단인자 우성 유전을 한다고 알려져 있으며(Zuniga et al., 1999), 현재 race 0, 1, 그리고 2에 저항성인 멜론 품종이 개발되어 있으나, race 1, 2에 대한 저항성인 멜론 품종은 아직 개발된 적이 없다(Matsumoto et al., 2011). 따라서 멜론 덩굴쪼김병에 대한 새로운 저항성 유전자원 탐색과 저항성 품종 개발을 위해서는 대량의 시료에 대하여 효율적으로 병 저항성을 검정하는 것이 필요하다. 하지만 균주의 병원성 조사를 위한 간편 접종법 개발 그리고 침지 접종법을 보다 용이하게 하기 위하여 고안한 새로운 방법들과 기존 방법의 비교에 관한 논문 등이 보고되어 있으나(Freeman and Rodriguez, 1993; Latin and Snell, 1986), 덩굴쪼김병균에 대한 멜론의 저항성을 검정하기 위한 효율적이고 체계적인 방법의 확립에 관한 논문은 보고된 바 없다.
본 연구는 덩굴쪼김병이 발생한 멜론 식물로부터 분리한 균주를 동정하고, Risser et al.(1976)의 방법에 따라 race를 판별하였다. 그리고 F. oxysporum f. sp. melonis의 접종원 대량 생산을 위한 최적배지를 선발하였다. 그리고 멜론의 저항성 품종을 개발하기 위한 효율적인 덩굴쪼김병 저항성 검정 방법을 확립하고자 시판 중인 22개 멜론 품종과 6개 대목 품종의 덩굴쪼김병 저항성 정도를 실험하고, 이들 중 저항성의 정도가 서로 다른 6개 멜론 품종을 선발하여 멜론의 생육 시기, 뿌리 상처, 접종원 농도, 침지시간, 재배 온도 등 다양한 발병 조건에 따른 멜론 품종들의 덩굴쪼김병 발생 정도를 조사하였다.
재료 및 방법
덩굴쪼김병균의 분리 및 동정
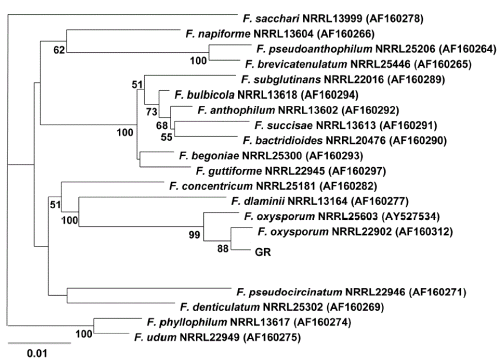
고령 지역의 온실에서 덩굴쪼김병이 발생한 멜론을 채집하고 이로부터 병원균을 단포자 분리하고 GR 균주로 명명하였다. 분리한 덩굴쪼김병균은 광학현미경 하에서 대형분생포자와 소형분생포자의 형태, 후막포자 형성 유무, 균총 색 등의 형태학적인 관찰(Nelson et al., 1983)과 분자생물학적인 방법으로 동정하였다. 분자생물학적 동정을 위해 GR 균주를 potato dextrose agar(PDA; Becton, Dickinson and Co.) 배지에 접종하고 25°C에서 7일 동안 배양한 후에 균사체를 수확하였다. 이것을 InstaGene Matrix #732-6020 solution 20µL에 현탁하여 12,000rpm으로 5분간 원심분리한 후에 상등액 1µL를 PCR에 사용하였다. 염기서열 분석을 위하여 ITS1(5'-TCCGTAGGTGAACCTGCGG-3')와 ITS4(5'-TCCT CCGCTTATTGATATGC-3') 프라이머(White et al., 1990) 그리고 EF-1(5'-ATGGGTAAGGAGGACAAGAC-3') 프라이머와 EF-2(5'-GGAAGTACCAGTGATCATGTT-3') 프라이머(O’Donnell et al., 1998)를 사용하여 PCR을 하였다. 두 프라이머 세트를 이용하여 InstaGene Matrix 산물 1µL, 10mM dNTP 1µL, 10 × PCR buffer 3µL, 10pmol의 프라이머 각각 1µL, 2.5unit/µL의 EF-Taq DNA polymerase(Solgent, Korea) 0.2µL을 넣고 멸균수를 첨가하여 최종 30µL의 반응액을 만들어 PCR 증폭 하였다. PCR은 95°C에서 2분간 initial denaturation을 실시한 후에 denaturation 95°C・30s-1, annealing 54°C・30s-1, extention 72°C・min-1으로 35 cycle을 수행하고 final extention 72°C에서 10분간 실시하였다(Wagacha et al., 2010). 그리고 PCR 산물은 Big Dye® terminator v3.1 cycle sequencing kits(Applied Biosystems, USA)로 반응 후 각각의 프라이머로 DNA Engine Tetrad 2 peltier thermal cycler (Bio-Rad, USA)을 이용하여 PCR 반응을 수행하고 ABI Prism 3730xl Analyzer 96 capillary type(Applied Biosystems, USA)로 염기서열 분석결과를 얻었다. 분석된 염기서열은 BLAST search에 의해 GenBank(www.ncbi.nlm.nih.gov)에 등록된 ITS와 TEF영역의 염기서열과 비교하였다. GR 균주와 GenBank로부터 얻은 염기서열은 CLUSTAL X(Thompson et al., 1994)와 PHYDIT program(Chun, 1995)을 이용하여 분석하였다. Neighbor-joining tree는 PHYLIP 3.57c package(Felsenstein, 1985)의 Kimura’s 2-parameter distance model(Kimura, 1980)을 이용하여 작성하였다.
최적배지 선발
접종원 대량생산을 위한 최적배지를 선발하기 위하여 GR 균주를 PDA 배지에 접종하고 25°C incubator에서 7일 동안 전배양 하였다. Fusarium oxysporum의 포자 생산을 위해 많은 연구자들이 사용하고 있는 6종 배지, malt extract broth (MEB; Becton, Dickinson and Co.), Czapek-dox broth(CDB; Becton, Dickinson and Co.), potato dextrose broth(PDB; Becton, Dickinson and Co.), V8-juice broth[V8 broth; V8 Juice(Campbell Soup Co.) 200mL, CaCO3 3g(Samchun Chem. Co., LTD), distilled water 1L], Clarified V8 broth(C-V8 broth; V8-juice broth를 4,000rpm에서 15분 동안 원심분리하여 침전물을 제거한 배지), glucose-peptone-yeast extract broth[GPYB; Glucose(Junsei Chem. Co., Japan) 20g, peptone (Becton, Dickinson and Co.) 5g, yeast extract(Becton, Dickinson and Co.) 5g, distilled water 1L)를 선발하여 125mL 삼각플라스크당 배지를 50mL씩 넣고 멸균하여 준비하였다. 이들 배지에 전배양한 GR 균주의 균총 말단부위로부터 7mm cork borer를 사용하여 떼어낸 균사 조각을 플라스크당 3개씩 접종하고 이들을 shaking incubator(25°C, 150rpm)에서 배양하였다. 생산된 포자(소형분생포자)의 수를 측정하기 위하여, 접종 2일 후부터 8일 후까지 하루에 한 번 배양액을 1mL씩 수확하여 4겹 거즈로 거르고 hemocytometer를 이용하여 광학현미경 하에서 포자의 수를 측정하였다. 실험은 배지당 3개 플라스크씩 그리고 플라스크당 2회씩 조사하였다.
접종원 준비
PDA 배지 중앙에 GR 균주의 균사 조각을 접종하고 25°C에서 7일 동안 배양한 균총으로부터 균사 조각을 떼어 V8- juice broth 배지에 접종하였다. 그리고 이를 25°C 암 상태에서 7일 동안 150rpm으로 진탕배양 하였다. GR 균주 배양액을 수확하여 4겹의 거즈로 걸러 균사를 제거하고 원심분리하여(4,300g, 10분, 4°C, Beckman Coulter Inc.) 배양여액을 제거하였다. 포자 침전물에 멸균수를 넣고 잘 현탁한 후에 hematocytometer를 이용하여 광학현미경하에서 포자(소형분생포자)의 농도를 측정하였다.
접종원 농도에 따른 멜론 품종들의 덩굴쪼김병 발생 실험을 제외한 모든 실험에서는 포자 농도가 3.3 × 106conidia/mL이 되도록 접종원을 준비하였다. 한편, 접종원 농도에 따른 발병 실험을 위해서는 1.3 × 104, 4.0 × 104, 1.2 × 105, 3.6 × 105, 1.1 × 106conidia/mL로 조정하여 실험에 사용하였다.
식물 재배
분리한 GR 균주의 기주 특이성을 조사하기 위하여 오이(Cucumis sativus), 멜론(C. melo), 참외(Cucumis melo var. makuwa), 수박(Citrullus lanatus) 등의 박과 작물에 대한 GR 균주의 병원성을 조사하였다. 오이는 ‘아시아청장’(아시아종묘)과 ‘백미백다다기’(동부팜한농), 멜론은 ‘베타리치’(동부팜한농)와 ‘아시아황금’(아시아종묘), 참외는 ‘금제’(아시아종묘)와 ‘조은대’(신젠타종묘) 그리고 수박은 ‘서태자’(아시아종묘)와 ‘꼬꼬마수박’(아시아종묘) 품종을 시중에서 구입하여 실험에 사용하였다. 각 박과 작물의 종자를 8 × 16 육묘용 연결 포트(15mL/pot, 범농사)에 원예용상토 5호(부농사)를 넣고 1립씩 파종하여 온실(25 ± 5°C)에서 7일 동안 재배하였다.
F. oxysporum f. sp. melonis GR 균주의 race를 검정하기 위하여 Risser et al.(1976)의 방법에 따라 감수성인 ‘Charentais T’, Fom-1 저항성 유전자를 가지는 ‘Charentais Fom-1’, Fom-2 저항성 유전자가 도입된 ‘Charentais Fom-2’ 그리고 Fom-1과 Fom-2를 지니는 ‘MR-1’ 등 4종의 멜론 품종들을 농업유전자원센터(KACC)로 부터 분양 받아 실험에 사용하였다. Race 판별 품종의 재배는 앞에서와 같은 방법으로 실험하였다.
시판 중인 멜론 품종과 멜론용 대목 품종들의 F. oxysporum f. sp. melonis GR 균주에 대한 저항성을 조사하기 위하여 멜론 22개 품종, ‘아시아황금’(아시아종묘), ‘아세아조춘만추’(아시아종묘), ‘아시아파파야’(아시아종묘), ‘아시아성하’(아시아종묘), ‘베타리치’(동부팜한농), ‘얼스엘리제’(신젠타종묘), ‘얼스골드킹’(코레곤종묘), ‘얼스해피’(코레곤종묘), ‘얼스킹’(코레곤종묘), ‘얼스마운트하계’(아시아종묘), ‘얼스파티’(신젠타종묘), ‘얼스탑원’(아시아종묘), ‘얼스VIP’(농협종묘), ‘얼룩파파야’(아시아종묘), ‘장춘FR파파이야’(장춘종묘), ‘JJ하계’(아시아종묘), ‘JJ원탑’(아시아종묘), ‘레드퀸’(농협종묘), ‘세지오케이’(동부팜한농), ‘썸머쿨’(코레곤종묘), ‘슈퍼세지’(아시아종묘)과 멜론용 대목 6개 품종, ‘강근토좌’(아시아종묘), ‘황제토좌’(코레곤종묘), ‘중토좌’(코레곤종묘), ‘NO.8’(한국다끼이), ‘RS111’(신젠타종묘), ‘신토좌’(아시아종묘)를 시중에서 구입하여 실험에 사용하였다. 멜론 품종 및 대목들의 재배는 앞에서와 동일한 방법으로 하였다.
발병 조건에 따른 멜론 품종들의 덩굴쪼김병 저항성 차이 실험을 위해서는 저항성으로 ‘레드퀸’(농협종묘), ‘썸머쿨’(코레곤종묘), ‘슈퍼세지’(아시아종묘)를, 중도저항성으로 아시아파파야’(아시아종묘)를, 그리고 감수성으로 ‘얼룩파파야’(아시아종묘)와 ‘아시아황금’(아시아종묘) 등 6개 멜론 품종을 실험에 사용하였다. 6개 품종의 종자를 8 × 16 육묘용 연결 포트(포트 당 토양 21mL/pot, 범농사)에 원예용상토 5호(부농사)를 넣고 종자를 1립씩 파종하여 온실(25 ± 5°C)에서 재배하였다.
멜론의 생육 시기에 따른 덩굴쪼김병 발생 실험을 제외한 모든 실험은 종자를 파종하고 7일 동안 재배한 유묘를 실험에 사용하였다. 멜론의 생육 시기에 따른 발병 실험을 위해서 접종하기 7, 10, 13, 16일 전에 각각 파종하고 온실에서 재배하여 실험에 사용하였다.
덩굴쪼김병균 접종
온실에서 재배한 멜론 유묘의 뿌리를 물로 세척하여 흙을 제거한 후에 GR 균주의 포자현탁액에 30분 동안 침지하여 접종하였다. 그리고 5 × 8 연결 포트(포트당 토양 80mL/pot, 범농사)에 원예용상토 5호(부농사)를 넣고 접종한 멜론 유묘를 이식하였다.
그 외 뿌리 상처 유무에 따른 6개 멜론 품종의 덩굴쪼김병 발생 실험에서 상처처리구는 앞에서와 같은 방법으로 준비한 멜론 유묘의 뿌리가 2.0-2.5cm 정도 남도록 가위로 잘라서 상처를 낸 후에 앞에서와 동일한 방법으로 GR 균주의 포자현탁액에 침지하여 접종하였다.
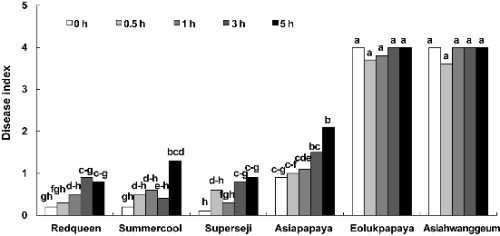
또한 침지시간에 따른 멜론 품종들의 덩굴쪼김병 발생의 경우에는 준비한 GR 균주 포자현탁액에 각각 0, 0.5, 1, 3 및 5시간 동안 침지하여 접종하였다. 0시간 처리를 위해서는 씻어서 준비한 멜론 뿌리를 포자현탁액에 침지한 즉시 꺼내 토양에 이식하였다.
발병 및 병조사
접종 후 재배 온도에 따른 멜론의 덩굴쪼김병 발생 실험을 제외한 모든 실험은 접종한 멜론 유묘를 25°C 습실상에서 1일 동안 배양한 후에 25°C 항온항습실로 옮기고 하루에 12시간씩 광을 조사하면서 6일 동안 재배하였다. 그리고 28°C에서 약 2주 동안 더 재배한 후에 덩굴쪼김병 발생을 조사 하였다.
재배 온도에 따른 발병 실험은 접종한 멜론 유묘를 20, 25 및 30°C 습실상에서 1일 동안 배양한 후에 각각 20, 25 및 30°C 항온항습실로 이동하고 하루에 12시간씩 광을 조사하면서 약 3주 동안 재배한 후에 병 발생을 조사하였다.
병조사는 접종 3주일 후에 각 식물체의 덩굴쪼김병 발생 정도(disease severity)를 조사하였다. 발병 정도는 다음과 같은 발병도(disease index)로 조사하였는데, 0 = 건전, 1 = 도관이 갈변되고 생육이 약간 억제된 것, 2 = 도관이 갈변되고 생육이 억제된 것, 3 = 도관이 갈변되고 생육이 심하게 억제되고 황화된 것, 4 = 고사 등의 5단계로 하였다. 그리고 평균 발병도가 1.0 이하인 경우에는 저항성, 1.1-2.5는 중도저항성, 2.6 이상은 감수성으로 판정하였다.
모든 덩굴쪼김병 발생 실험은 10반복으로 2회 실시하였다. 통계분석은 SAS(SAS Institute, Inc., 1989, Cary, NC) 프로그램을 이용하여 ANOVA 분석을 하였으며, 처리 평균간 비교를 위하여 Duncan’s multiple range test(p = 0.05)를 실시하였다.
결과 및 고찰
균주 동정
덩굴쪼김병이 발생한 멜론 시료로부터 분리한 GR 균주는 PDA 배지에서 균사 생장이 빠르고 균총의 색은 흰색이고 배지에 보라색 색소를 분비하며, 3-5개의 격막을 가지는 Fusarium의 전형적인 낫 모양의 대형분생포자를 형성하고, false head에 kidney-shaped의 소형분생포자와 후막포자를 형성하는 등의 형태적 특징을 바탕으로 F. oxysporum으로 동정되었다(Nelson et al., 1983).
또한 분자생물학적으로도 동정하였는데 GR 균주의 ITS 영역(White et al., 1990)과 translation elongation factor 1-α(TEF) 영역(O'Donnell et al., 1998)의 염기서열을 NCBI에 등록된 Fusarium 종들과 비교한 결과, 두 영역 모두에서 F. oxysporum과 100%의 상동성을 보였다. 그리고 두 영역 각각에 대하여 phylogenic tree를 작성하였을 때 둘 다 F. oxysporum과 동일한 그룹을 형성하였다(Fig. 1). ITS 영역은 일반적으로 곰팡이의 종을 구분하기 위하여 널리 사용되고 있으며, Fusarium 속의 종간 구별을 위해서는 TEF 유전자가 가장 적당하다고 알려져 있다(Geiser et al., 2004). 하지만 본 실험의 GR 균주는 두 유전자 영역 모두에서 F. oxysporum과 일치하였다. 그러므로 이상의 형태적 및 분자생물학적 동정 결과에 따라 GR 균주는 F. oxysporum으로 동정되었다.
GR 균주의 기주 특이성을 조사하기 위하여 오이, 멜론, 수박 그리고 참외의 2개 품종씩에 GR 균주를 접종하고 덩굴쪼김병 발생을 조사한 결과, 멜론(‘베타리치’와 ‘아시아황금’)과 참외(‘금제’와 ‘조은대’)에서는 덩굴쪼김병이 심하게 발생하였다(Table 1). 반면에 오이(‘아시아청장’과 ‘백미백다다기’)와 수박(‘서태자’와 ‘꼬꼬마수박’)에는 덩굴쪼김병이 거의 발생하지 않았다. 따라서 GR 균주는 멜론 또는 참외에만 병을 일으키는 F. oxysporum f. sp. melonis임을 알 수 있었다.
GR 균주의 Race 검정
Risser et al.(1976)의 방법에 따라 F. oxysporum f. sp. melonis GR 균주의 race를 확인하기 위하여 4종 판별품종을 사용하여 실험한 결과, 감수성인 ‘Charentais T’ 그리고 Fom-1 저항성 유전자를 가진 ‘Charentais Fom-1'에서는 발병도 3.9 이상의 높은 덩굴쪼김병 발생이 있었으나, Fom-2 유전자가 도입된 ‘Charentais Fom-2'는 덩굴쪼김병이 발생하지 않았다. 그리고 Fom-1와 Fom-2 모두를 가지는 ‘MR-1’은 GR 균주에 대해 저항성을 나타냈다(Table 2). 이상의 결과로부터 F. oxysporum f. sp. melonis GR 균주는 race 1임을 알 수 있었다(Risser et al., 1976).
F. oxysporum f. sp. melonis은 세계적으로 4개의 race 즉 race 0, 1, 2 및 1,2가 보고되어 있다(Cohen et al., 1989; Gerlach et al., 1988; Leary and Wilbur, 1976; Risser et al., 1976). 미국에서는 race 2가 우점 race이고, 유럽에서는 race 1이 가장 널리 분포되어 있다(Martyn and Gordon, 1996). 일본의 경우에는 race 0과 2가 널리 퍼져 있으며, race 1과 1, 2y가 제한적인 지역에서 보고되고 있다(Namiki et al., 1998, 2000). 하지만 우리나라에서 멜론 덩굴쪼김병균의 race 분포에 대한 보고는 거의 없는 실정이다.
최적배지 선발
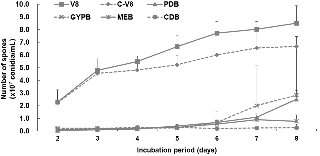
일반적으로 F. oxysporum의 포자 형성을 위해 많이 사용하고 있는 6종 배지(V8-juice broth, Clarified V8 broth, malt extract broth, Czapek-dox broth, potato dextrose broth 및 glucose-peptone-yeast extract broth)에 GR 균주를 접종하고 8일 후까지 포자 형성량을 매일 조사한 결과, GR 균주는 실험한 배지 중 V8-juice broth 배지에서 가장 많은 포자(소형분생포자)를 형성하였다(Fig. 2). 그리고 Clarified V8 broth 배지에서는 V8 배지보다는 포자 형성이 다소 적었지만 나머지 4종 배지보다는 많은 양의 포자를 생산하였다. 따라서 F. oxysporum f. sp. melonis GR 균주의 접종원인 소형분생포자를 대량 생산하기 위해서는 V8-juice broth 배지에서 약 7일 동안 150rpm으로 진탕배양하는 것이 효율적일 것이다.
시판 멜론 품종의 덩굴쪼김병에 대한 저항성
시판 중인 멜론 품종 22종과 멜론 재배용 대목 품종 6종의 F. oxysporum f. sp. melonis GR 균주(race 1)에 대한 저항성 정도를 조사한 결과, 종자회사에서 덩굴쪼김병 저항성으로 판매하고 있는 멜론 재배용 대목 6개 품종(‘강근토좌’, ‘황제토좌’, ‘중토좌’, ‘NO.8’, ‘RS111’, ‘신토좌’)에서는 덩굴쪼김병이 전혀 발생하지 않았다. 따라서 이들 대목 품종들은 GR 균주에 대한 고도의 저항성 품종임을 알 수 있었다.
실험한 22종 멜론 품종 중 종자회사에서 덩굴쪼김병에 대한 저항성 품종으로 판매하고 있는 5개 품종(‘레드퀸’, ‘썸머쿨’, ‘아시아성하’, ‘아세아조춘만추’, ‘장춘FR파파이야’) 중 ‘아세아조춘만추’와 ‘장춘FR파파이야’를 제외한 나머지 3종은 모두 1.0 이하의 낮은 발병도를 보여 이들은 race 1 균주에 대한 높은 저항성 품종임을 알 수 있었다(Table 3). 따라서 이들 품종에는 ‘Fom-2’ 저항성 유전자가 단독으로 혹은 ‘Fom-1’ 유전자와 함께 도입되어 있을 것으로 생각되었다. 한편 덩굴쪼김병 저항성 품종으로 판매되고 있는 ‘장춘FR파파이야’는 race 1인 GR 균주에 대하여 감수성을 보였으므로 이 품종은 ‘Fom-1’ 저항성 유전자를 가지는 품종으로 추정되었다.
그 외 덩굴쪼김병 저항성 품종으로 공시되지 않은 17종 품종 중 2개 ‘아시아황금’과 ‘얼룩파파야’에서는 발병도 4.0을 보여 높은 감수성 품종임을 알 수 있었다. 그리고 나머지 15개 품종 중 ‘JJ원탑’와 ‘세지오케이’는 발병도 2.2와 2.4의 다소 낮은 저항성을 나타냈으며, 그 외 13개 멜론 품종들은 발병도 0.9-2.0의 덩굴쪼김병 발생을 보였다(Table 3). 따라서 판매되고 있는 멜론 품종들 중 종자회사에서 공시하는 저항성 품종은 5개뿐이나 실험한 시판 멜론품종 대부분은 저항성 정도에 차이는 있지만 race 1에 대한 저항성 품종임을 알 수 있었다.
멜론 덩굴쪼김병에 대한 효율적인 저항성 검정 방법을 확립하기 위하여 여러 발병조건에 따른 멜론 품종들의 F. oxysporum f. sp. melonis에 대한 저항성 차이를 조사하기 위하여, 실험한 22종 멜론 품종으로부터 GR 균주에 대한 저항성 정도가 서로 다른 6개 품종, 저항성인 ‘레드퀸’, ‘썸머쿨’ 및 ‘슈퍼세지’, 중도저항성인 ‘아시아파파야’, 그리고 감수성인 ‘얼룩파파야’와 ‘아시아황금’ 품종을 선발하였다.
생육 시기에 따른 멜론 덩굴쪼김병 발생
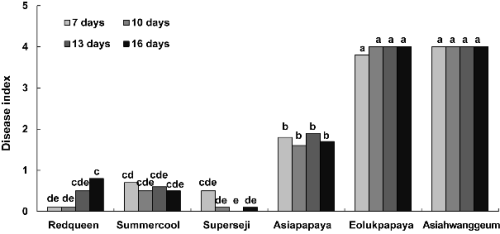
유묘의 생육 시기에 따른 멜론 품종들의 덩굴쪼김병 발생 정도를 실험하기 위하여 선발한 6개 품종을 파종하고 7, 10, 13, 16일 후에 접종하여 병 발생을 조사한 결과, 감수성 품종인 ‘얼룩파파야’와 ‘아시아황금’은 실험한 모든 생육 시기의 식물에서 덩굴쪼김병이 심하게 발생하였다. 그리고 저항성 품종들에서는 멜론의 생육 시기에 관계없이 ‘레드퀸’, ‘썸머쿨’, ‘슈퍼세지’는 저항성을, ‘아시아파파야’는 중도저항성을 보였다(Fig. 3).
Latin and Snell(1986)은 F. oxysporum f. sp. melonis의 접종방법 비교 실험 중 11일 이상 키운 유묘는 6일 동안 키운 유묘에 비해 병 발생이 적다고 보고하였으나, 본 실험에서는 유묘의 생육 시기에 따른 덩굴쪼김병 발생의 차이가 저항성 검정에 영향을 미칠 만큼 크지 않음이 확인되었다. 따라서 실험에 사용하는 멜론 유묘가 어릴수록 이식 후 활착율이 높은 점 등을 고려하여 멜론 덩굴쪼김병의 저항성 검정을 위해서는 멜론을 파종하고 7일 동안 재배한 유묘를 실험에 사용하는 것이 효율적이라 생각되었다.
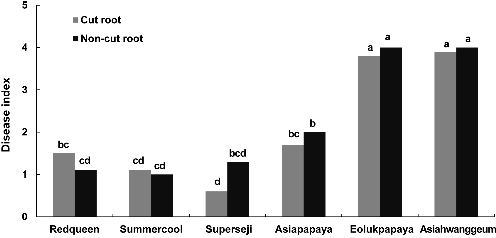
뿌리 상처에 따른 멜론 덩굴쪼김병 발생
파종 후 7일 동안 재배한 유묘를 뽑아 물로 씻어 토양을 제거한 후에 가위로 멜론의 뿌리를 자르고 덩굴쪼김병균(F. oxysporum f. sp. melonis GR)을 접종하거나, 뿌리를 자르지 않고 접종하여 가위 상처 유무에 따른 6개 품종 멜론의 덩굴쪼김병의 저항성 차이를 실험하였다. 가위 상처 유무에 따른 멜론 품종들의 덩굴쪼김병 발생에서 통계적으로 유의성 있는 차이를 보이지 않았지만, 가위로 인한 인위적인 상처 없이 저항성 품종인 ‘레드퀸’과 ‘썸머쿨’, 그리고 감수성 품종인 ‘얼룩파파야’와 ‘아시아황금’이 각각 고도의 저항성과 높은 감수성을 보이며 저항성 특성을 잘 나타내었다(Fig. 4). 인위적인 상처를 내지 않아도 저항성 검정에 충분한 덩굴쪼김병 발생을 보이므로 멜론 덩굴쪼김병에 대한 저항성 검정을 위해서는 멜론 유묘의 뿌리를 뽑아 물로 깨끗하게 씻어 흙을 제거한 후에 가위로 뿌리를 자르지 않고 F. oxysporum f. sp. melonis의 포자현탁액에 침지하여 접종하는 것이 효율적이라 생각되었다.
침지시간에 따른 멜론 덩굴쪼김병 발생
멜론 유묘의 뿌리를 포자현탁액에 0, 0.5, 1, 3, 5시간 동안 침지하여 접종한 6개 품종들의 덩굴쪼김병 발생 차이를 실험한 결과, 감수성 품종들은 실험한 침지시간에 관계없이 모든 처리구에서 높은 감수성을 보였다(Fig. 5). 그러나 저항성 품종들은 침지시간이 증가함에 따라 덩굴쪼김병 발생이 증가하였다. 그리고 포자현탁액에 침지한 즉시 꺼내는 0분 처리구에서 중도저항성 대조 품종인 ‘아시아파파야’도 고도의 저항성을 나타냈다(Fig. 5).
멜론 유묘의 뿌리에 포자 현탁액을 침지하는 방법으로 덩굴쪼김병을 접종하는 경우 많은 실험에서 1분 미만의 매우 짧은 시간 동안의 접종으로 병 발생을 유도하고 있으나(Freeman et al., 2002; Jacobson and Gordon, 1988; Namiki et al., 2000), 멜론 유묘에서 안정적인 F. oxysporum f. sp. melonis의 접종을 위해서는 멜론의 뿌리를 포자현탁액에 30분 정도 침지하여 접종하는 것이 더 바람직하다고 생각되었다.
접종원 농도에 따른 멜론 덩굴쪼김병 발생
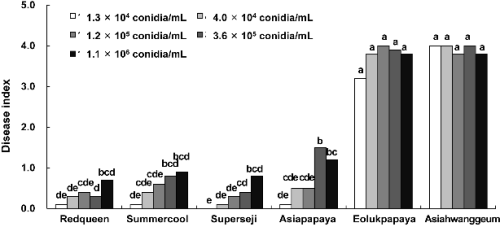
준비한 멜론 유묘를 GR 균주의 다섯 가지 농도(1.3 × 104,4.0 × 104,1.2 × 105,3.6 × 105, 1.1 × 106conidia/mL)의 포자현탁액에 침지하고 이식하여 6개 멜론 품종의 덩굴쪼김병 발생 정도를 실험한 결과, ‘얼룩파파야’와 ‘아시아황금’은 접종원 농도와 관계없이 모든 농도에서 높은 감수성을 나타냈다. 그러나 저항성 품종에서는 대부분의 품종에서 접종원의 포자 농도가 증가함에 따라 덩굴쪼김병의 발병도도 증가하였다(Fig. 6). 1.2 × 105conidia/mL 농도 접종구에서는 저항성 품종들뿐만 아니라 중도저항성인 ‘아시아파파야’도 고도의 저항성을 보였다. 그리고 Kuc(1987, 1994)는 식물체의 병 저항성 검정에서 고농도로 병원균을 접종하면 식물체가 조기 낙엽되어 저항성을 유도할 수 있는 잎이 없어 정확한 저항성 검정이 이루어질 수 없다고 보고한 바 있다.
따라서 예비실험을 통해 선택한 3.3 × 106conidia/mL의 접종원 농도를 사용하여 멜론의 생육 시기, 접종 후 재배온도, 침지 시간 등에 따른 덩굴쪼김병 발생을 실험하였으나, 최종적으로 선정된 멜론의 생육 시기, 접종 후 재배온도, 침지 시간을 이용하여 접종 농도에 따른 덩굴쪼김병 발생을 실험한 결과에서 포자 농도를 1.3 × 104,4.0 × 104,1.2 × 105,3.6 × 105, 1.1 × 106conidia/mL로 더 낮추어 실험한 결과, F. oxysporum f. sp. melonis에 대한 멜론의 저항성 정도는 3 × 105conidia/mL농도의 포자현탁액에 침지하여 접종하는 것이 더 효과적이라 생각되었다.
재배 온도에 따른 멜론 덩굴쪼김병 발생
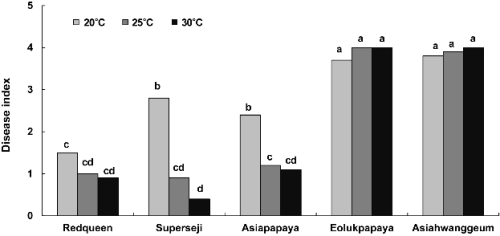
덩굴쪼김병균을 접종한 유묘의 재배 온도(20, 25, 30°C)에 따른 6종 멜론 품종들의 저항성이 차이를 조사한 결과, 감수성 품종들에서는 실험한 재배 온도에 관계없이 덩굴쪼김병이 심하게 발생하였다(Fig. 7). 하지만 저항성 품종들은 25°C와 30°C에서 높은 저항성을 나타냈으나, 20°C에서는 저항성이 무너지면서 높은 덩굴쪼김병 발생을 보였다(Fig. 7).
저항성 품종들의 평균 덩굴쪼김병 발생은 통계적으로 유의성 있는 차이는 없으나 25°C보다 30°C에서 다소 적었다. 하지만 30°C에서는 이식 후에 유묘들의 활착율이 떨어지는 경우가 많다. 따라서 멜론 덩굴쪼김병의 저항성 검정을 위해서는 접종한 후에 멜론 유묘를 25-28°C에서 재배하는 것이 효율적이라 생각되었다.