서 언
재료 및 방법
실험재료
아황산가스(SO2) 처리
순광합성률(Net photosynthetic Rate, PN) 측정
엽록소와 카로티노이드 함량(Chlorophyll and Carotenoid Contents) 측정
가시적인 피해증상 관찰
기공의 형태 관찰 및 크기 측정
시스테인(Cysteine), 감마 글루타밀 시스테인(γ-glutamylcysteine)과 글루타치온(GSH) 함량 측정
통계분석
결과 및 고찰
광합성률
수분이용효율
엽록소와 카로티노이드 분석
가시적 피해증상 관찰
잎의 형태학적 특성
시스테인(cysteine), 감마-글루타밀시스테인(γ-glutamylcysteine)과 글루타치온(glutathione, GSH) 함량
서 언
대기 중에는 다양한 오염물질이 존재하며 대부분이 화석연료 연소과정이나 배기가스를 통해 인위적으로 배출이 되는데 질소산화물(NOx), 이산화황(아황산가스, SO2), 일산화탄소(CO) 등이 있다(Lee et al.,
2017). 또한 이런 물질들은 온실 내에서도 존재할 수 있는데, 특히 겨울철 시설재배 시 가온을 위한 난방기 사용으로 SO2가 발생하기도 한다(Kim, 2006; Lee et al., 2009). 겨울철 온실 내 난방기 가동에 있어서, 온실 내 식물은 난방기의 연료가 연소되는 과정에서 가스가 새어 나와 엽내로 유입될 수 있다. 더군다나, 온실처럼 한정된 공간에 SO2와 같은 유해가스가 유입되면 짧은 시간 내에도 작물의 생장에 영향을 미치고, 장기간 축적되면 농작물의 생산량에도 영향을 미치게 되며, 농작업자에게 피해를 유발할 수 있다(MAFRA, 2015).
일반적으로 SO2는 기공을 통해 식물체 내에 흡수된 후 산화과정을 거쳐 활성산소를 생성하게 된다(Peiser and Yang, 1977). 기공을 통해 유입된 SO2는식물 세포 내에서 superoxide(O2-), hydrogen peroxide(H2O2), hydroxyl radical(OH-)와 같은 활성산소를 생성하여 산화적 손상을 유발하고(Hernández-Pérez et al., 2016), 광합성 색소의 파괴와 세포막 손상을 일으키며, 가시적인 피해도 발생시키지만(Gheorghe and Ion, 2011; Ashraf and Harris, 2013), sulfite reductase에 의하여 SH-로 환원되면서 황대사에 유입되어 대사과정을 거치며 cysteine desulfhydrase에 의해 시스테인으로 합성되고 시스테인에 의해 메티오닌이나 글루타치온으로 합성된다(Gigolashvili and Kopriva, 2014). 식물체 내로 유입된 SO2가 황산염으로 빠르게 전환되어 뿌리에서 직접적으로 이용하거나, 식물체 내에 축적된다. 또한 토양 내 황이 부족한 경우에는 황 대사로 유입될 수도 있지만, 장기간 노출되면 만성피해를 일으킬 수 있다(Malhotra and Hocking, 1976). 반면, 급성피해는 고농도의 SO2를 단기간 흡수했을 때 발생되며, 엽록소의 파괴 및 세포 괴사 등을 발생하여 식물의 정상적인 대사과정을 저해하고 기공폐쇄를 유도하여 광합성능력을 감소시킨다(Singh et al., 2013).
식물은 여러 가지 환경 스트레스를 받으며 생장한다. 하지만 온실과 같은 제한된 공간 내에서 발생한 대기오염이 시설재배 작물에 어떠한 영향을 미치는지에 대한 것은 보고가 부족한 실정이다. 따라서, 이 실험은 겨울철 난방사용으로 인해 온실 내 발생하는 SO2 피해에 따른 시설재배작물의 생리, 형태적인 영향을 알아보고 SO2가 식물의 황대사에 미치는 영향에 대해 알아보고자 하였다
재료 및 방법
실험재료
시험 재료는 시설재배작물로 많이 이용되는 고추(Capsicum annuum L.)와 가지(Solanum melangena L.)를 대상으로 환경조절이 되는 식물환경조절실험장치(phytotron)에서 수행되었다. 식물은 경기도 여주육묘장 인공발아시설에서 2015년 9월 30일에 파종하여 90일 지난 고추(‘녹광’, 흥농, 한국)와 가지(‘축양’, 다키이종묘, 일본) 유묘를 분양받아, 원예용 상토(Green Partner, Nongwoo Bio, Korea)를 채운 직경 12cm 포트에 이식하여 2016년 1월 10일부터 1월 19일까지 10일간 생장시켜 실험에 사용하였다. 모든 실험은 3반복으로 행하였고, 대조구와 처리구에서 각각, 엽색이 비슷하고 균일한 상태의 잎을 실험 재료로 사용하였다.
아황산가스(SO2) 처리
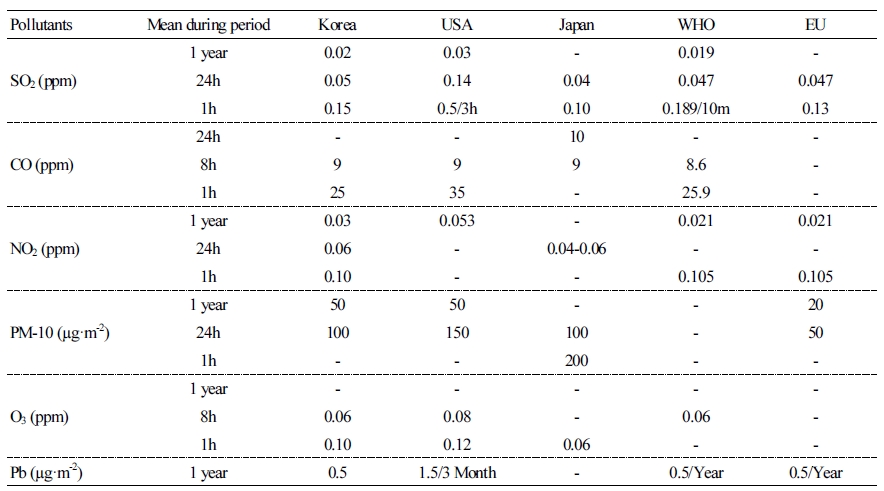
고추와 가지의 유묘를 주야간 온도(25.0±0.5°C), 습도(60.0±5.0%), 아황산가스 농도가 조절되는 식물환경조절장치 phytotron(150×150×200cm; Koito Industries, Japan)으로 옮겨 2016년 1월 20일부터 1월 24일까지 5일간 순화시킨 후 대조구와 SO2 처리구로 나누어 진행하였다. 아황산가스 처리구 챔버에는 SO2 50µg·kg-1 농도로 24시간 동안 2016년 1월 25일부터 2월 15일까지 20일간 처리하였다. 농도 설정은 국가대기오염기준표를 참고하여 설정하였다(Table 1). SO2 농도의 처리는 SO2(98%)+N2(2%) balance를 이용하여 이를 phytotron 내로 유입하였으며, 농도 조절은 자동조절 제어시스템을 이용하여 유지시켰다.
Table 1. Air pollutant standards in select countries
National Institute of Environmental Research (2014)
 |
순광합성률(Net photosynthetic Rate, PN) 측정
두 수종의 순광합성 능력은 Li-6400 휴대용 광합성 측정기(Li-6400XT, Li-Cor Inc., USA)를 사용하여 오전 9시부터 오후 1시까지 측정하였다. 광합성 측정 시 leaf chamber 내부 온도는 26±5°C, 상대습도는 60± 5%로 유지하고, CO2 농도는 400µmol·mol-1로 유지하였다. 순광합성률은 아래 식을 이용하여 구하였다(Von Caemmerer and Farquhar, 1981). 광도별 반응 곡선 측정은 PPFD 0, 10, 20, 30, 50, 100, 200, 400, 600, 800, 1,000, 1,200µmol·m-2·s-1으로 광도 변화를 주어 광합성률 변화를 측정하였다.
PN : net photosynthetic rate (µmol CO2/m2·s-1)
Ue : mole flow rate of air entering the leaf chamber (µmol·s-1)
Ce : mole fraction of CO2 in the leaf chamber (µmol CO2/mol1 air)
Cs : mole fraction of CO2 entering in the leaf chamber (µmol CO2/mol1 air)
s : leaf area (cm2)
E : transpiration rate (mmol H2O/m2·s-1)
수분이용효율(Water Use Efficiency, WUE) 계산
수분이용효율(WUE)은 광합성능력(PN)을 증산량(Tr)으로 나누어 구하였다(Zhang et al., 2004). Li-6400 휴대용 광합성 측정기기(Li-6400, Li-Cor Inc., USA)를 사용하여 얻을 수 있는 PN과 Tr값을 이용하여 WUE값을 얻었다. 수분이용효율은 다음과 같은 식으로 계산하였다.
WUE = PN / Tr
WUE : water use efficiency (µmol CO2 mmol H2O-1)
PN : leaf net CO2 assimilation rate (µmol CO2 m−2 s−1)
Tr : transpiration rate (mmol H2O m-2 s-1)
엽록소와 카로티노이드 함량(Chlorophyll and Carotenoid Contents) 측정
엽록소와 카로티노이드 함량을 분석하기 위해 0.1g을 아세톤(80%) 8mL에 넣고 4°C 냉암소에서 7일간 충분히 침출시킨 후 흡광도를 측정하였다. 흡광도는 microplate reader(Epoch Microplate Spectrophotometer, Synergy-Bio Tek, USA)를 이용하여 663nm, 645nm와 470nm 파장에서 측정하였다. 엽록소 a(Chl a), 엽록소 b(Chl b), 총 엽록소(Chl a + Chl b)와 카로티노이드 함량은 다음 식을 이용해 계산하였다(Arnon, 1949).
Chlorophyll a = 12.7 × A663 – 2.69 × A645
Chlorophyll b = 22.9 × A645 – 4.68 × A663
Total Chlorophyll = 20.2 × A645 + 8.02 × A663
Total Carotenoid = (1000 × A470 – 1.82 × Chl a – 85.02 × Chl b)/198
(A, absorbance; pigment concentration calculated as mg·g-1 FW from µg·ml-1 cuvette of extract)
가시적인 피해증상 관찰
SO2에 의해 나타나는 주요 피해현상은 황색, 백색, 갈색 반점과 황화, 백화현상, 탈색 및 괴사 등이 가시적으로 관찰된다(Nandi et al., 1990; Novak et al., 2003; Kumari and Prakash, 2015). 모든 식물은 SO2 처리 후 실험 마지막 날 기준으로 실험하였다.
기공의 형태 관찰 및 크기 측정
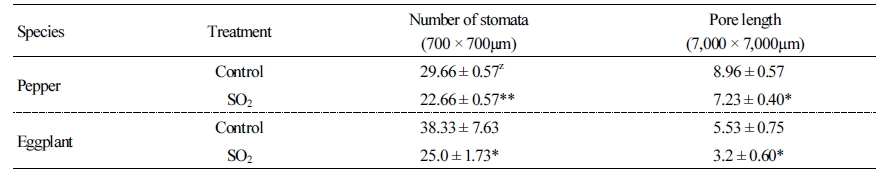
잎의 기공 변화를 관찰하기 위해 실험 종료 후 각 처리구 당 3-5개의 잎을 수확하여 동결건조기(freeze dryer)에서 7일간 건조시켰다. 완전히 건조시킨 잎을 주사전자현미경(scanning electron microscope, SEM) 관찰을 위해 서울대학교 농생명과학공동기기원(NICEM) 전자현미경 연구실로 옮겨 광학현미경(FESEM, AURIGA, Carl Zeiss, Genmany)을 이용하여 관찰하였다. 기공밀도(700 ×700µm)와 기공의 크기(7,000×7,000µm)를 관찰하여 측정하였다.
시스테인(Cysteine), 감마 글루타밀 시스테인(γ-glutamylcysteine)과 글루타치온(GSH) 함량 측정
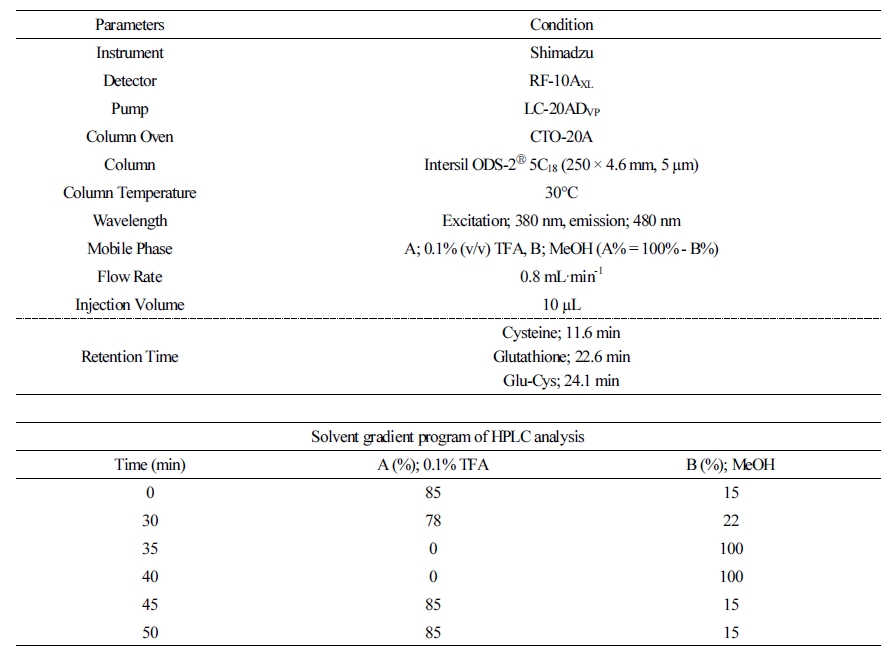
시스테인(Cysteine), 감마 글루타밀 시스테인(γ-glutamylcysteine)과 글루타치온(GSH) 측정은 mBBr(monobromobimane) 형광 유도체화법을 이용하여 HPLC로 분석했다(Kocsy et al., 2000; Kim et al., 2010). 시료 0.2g을 0.1M HCl(1mM Na2EDTA) 5mL를 첨가한 후 균질화 한 후 centrifuge tube에 옮겨16,000 × g에 4°C에서 15분간 원심분리했다. 원심분리한 상등액 400µL에 0.2M CHES[2-(cyclohexylamino) ethane sulfonic acid] pH 9.3, 600µL를 더하고 400mM NaBH4 100µL를 첨가하여, voltex한 후 얼음 위에서 20분간 반응시킨다. 혼합물에서 660µL를 덜어내어 15mM mBBr 15µL를 첨가한 후 암소에서 15분간 반응시킨다. 반응 후 5%(v/v)acetic acid 500µL를 더하여 유도체화 반응을 중지시킨 후, 16,000 × g에 4°C에서 15분간 원심분리하고, 0.45µm syringe filter에 여과한 후 분석용 시료로 사용했다. HPLC(shshimad, Tokyo, Japan) 측정조건은 Table 2과 같다. 결과값은 생체중으로 환산하여 µg·g-1 FW로 표시하였다.
통계분석
모든 결과는 통계프로그램 SPSS(SPSS, Chicago, IL, USA)를 이용하여 95% 신뢰수준에서 독립표본 t-test로 검증하였으며, 처리간 유의성(* p < 0.05; ** p < 0.01)을 분석하였다.
결과 및 고찰
광합성률
SO2 50µg·kg-1 농도 처리에 따른 고추와 가지의 생리 활성의 변화를 알아보고자 광합성을 측정하였다. 고추와 가지의 광합성률을 측정한 결과 대조구와 SO2 처리구 모두 광도 증가에 따라서는 광합성률도 증가하는 것으로 나타났다. 그러나 SO2 처리구에서 대조구보다 고추와 가지 두 작물 모두 광합성률이 감소하였다(Fig. 1A and B). 가지의 경우 광도가 증가할수록 대조구에 비해 SO2 처리구에서 광합성률이 현저히 낮아지는 경향을 보였으며, 처리구 간 통계적으로 큰 유의적 차이를 발견할 수 있었다(Fig. 1B). 반면, 고추의 경우 SO2 처리구에서 광합성률의 감소를 나타냈지만, 대조구와 유의한 차이는 없는 것으로 나타나 온실 내 가온환경에서 가지보다 고추가 SO2에 대한 적응능력이 상대적으로 우수한 것으로 판단되었다(Fig. 1A).
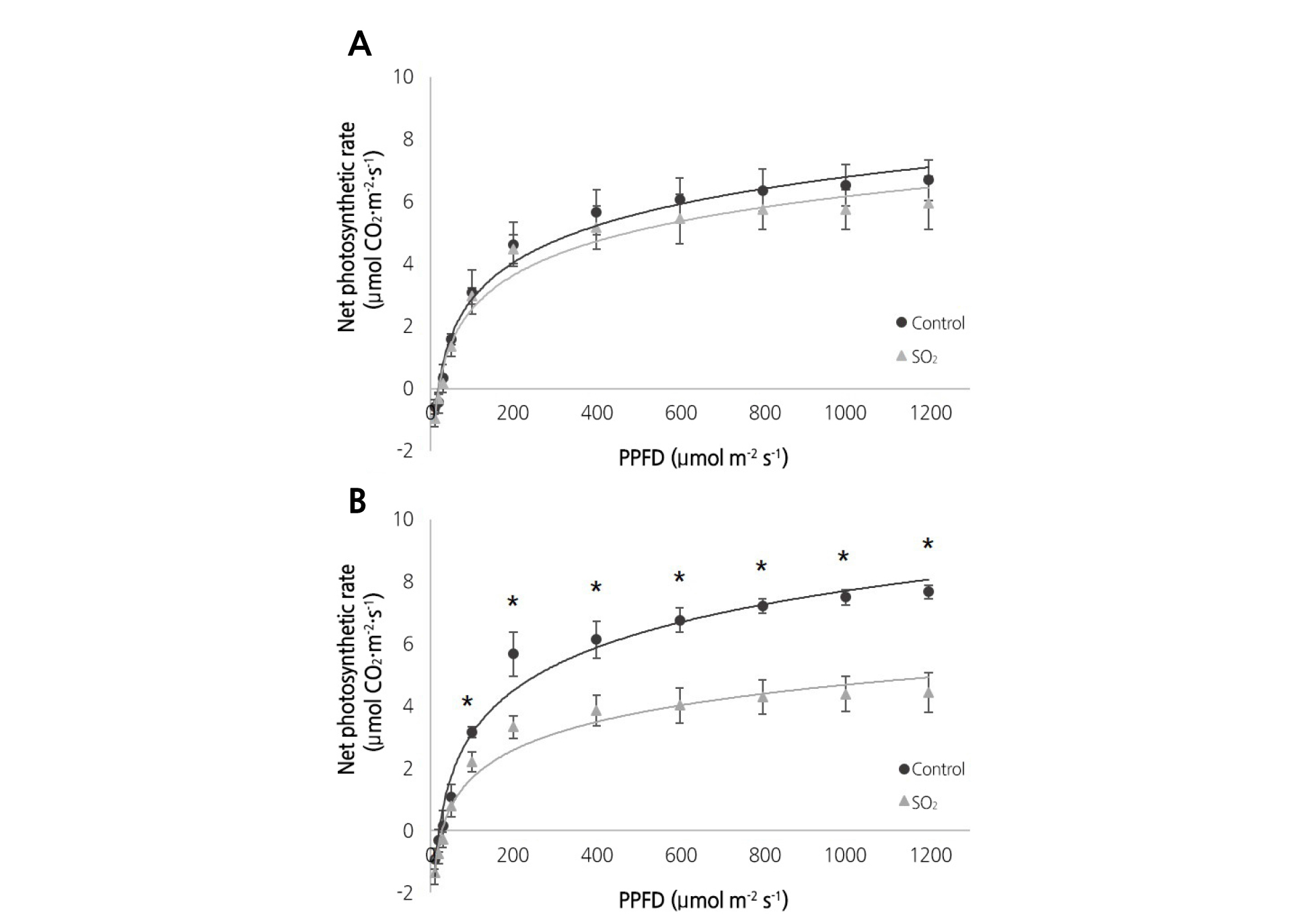
Fig. 1. Net photosynthetic rate of pepper (A) and eggplant (B) exposed to 50 µg·kg-1 SO2. Control (●) and 50 µg·kg-1 SO2 treatment (▲). Mean values are presented with vertical error bars that represent standard deviations calculated from three independent samples (n = 3). Asterisks (*) indicate statistically significant differences between control and SO2 treatment (* p < 0.05 by independent t-test).
일반적으로 대기오염에 노출된 식물은 광합성이 감소한다(Lee et al., 2001; Woo et al., 2003; Wali and Iqbal, 2004; Cheng et al., 2010; Choi et al., 2014). SO2와 같은 대기오염물질이 기공을 통해 식물체 내로 유입되면 산화과정을 거치며 활성산소를 생성하여 엽록체를 파괴하고, 기공수준에서 탄소 흡수를 억제하거나 Calvin cycle에 관련 있는 효소의 활성이 저해된다(Winner et al., 1985; Lee et al., 2003; Swain and Padhi, 2015). 결과적으로, 광합성 기구에 피해를 유발함으로써 광합성 능력을 저하시키고, 기공전도도 또한 감소하며 수분이용효율의 증가를 불러 일으키는 것으로 알 수 있다(Heyneke et al., 2012). 따라서, 지속적인 온실 내 가온처리에 따른 SO2 발생은 대표적인 겨울철 시설원예 작물인 고추와 가지의 광합성률 감소와 광합성 관련 기구를 손상시켜 기존의 도심지역 가로수종의 대기오염에 따른 광합성 저해현상(Woo et al., 2003)과 같은 양상을 보이는 것으로 나타났다. 고추와 가지 등 시설원예작물은 겨울철 지속적인 가온으로 인한 온실 내 대기환경에서 정상적인 작용을 행하지 못하는 것으로 볼 수 있으며, 이는 수분이용효율의 증가와 엽록소 함량의 감소로 이어지게 되고, 결국에는 작물 생장을 저하시켜 생산성 감소의 결과를 불러올 수 있다.
수분이용효율
SO2 50µg·kg-1 농도로 처리 후 고추와 가지의 수분이용효율을 조사한 결과, 두 수종 모두 대조구에 비해 SO2 처리구의 수분이용효율이 높게 나타났다(Fig. 2A and B). 식물은 일반적으로 스트레스 조건 하에서 수분이용효율이 증가하는 것으로 알려져 있다(Ashraf and Harris, 2013; Lee et al., 2013). 이 실험에서 SO2 처리한 실험구의 수분이용효율이 증가함을 보였는데, 이는 SO2 유입으로 인해 식물이 부분적으로 기공을 닫아 광합성보다 증산속도를 감소시켜 수분이용효율이 증가한 것으로 생각된다. 그러나 장기적으로는 기공폐쇄로 인한 탄소 유입을 제한함으로써 광합성에 부정적인 영향을 미치는 것으로 알려져 있다.
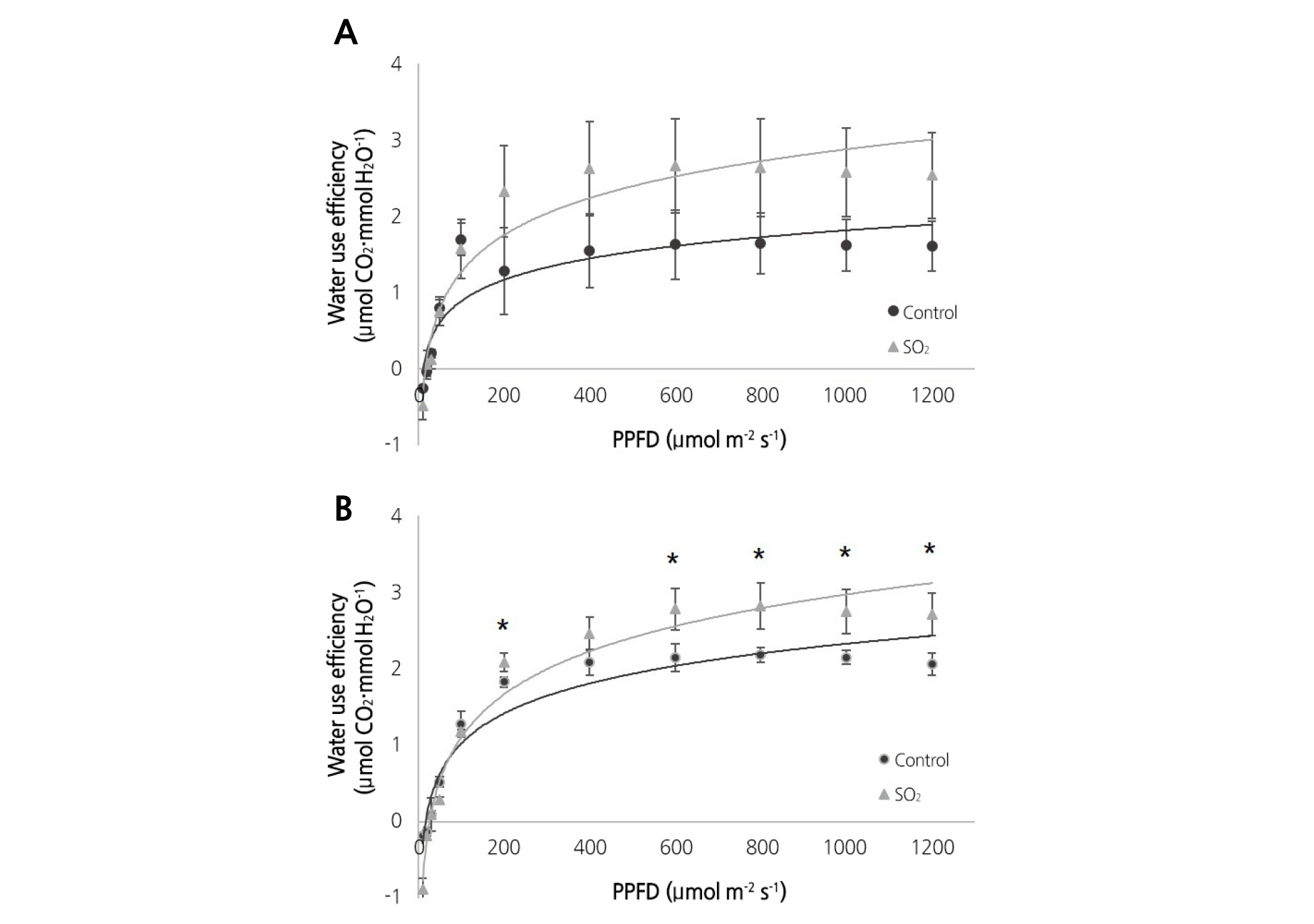
Fig. 2. Water use efficiency (WUE) of pepper (A) and eggplant (B) exposed to 50 µg·kg-1 SO2. Control (●) and 50 µg·kg-1 SO2 treatment (▲). Mean values are presented with vertical error bars that represent standard deviations calculated from three independent samples (n = 3). Asterisks (*) indicate statistically significant differences between control and SO2 treatment (* p < 0.05 by independent t-test).
수분이용효율은 식물의 증산과 광합성을 제대로 하는지를 평가하는 중요한 척도이다(Hetherington and Woodward, 2003; Medrano et al., 2015). 식물은 기공을 통해 탄소 흡수와 수분 방출을 동시에 하며, 탄소 흡수를 더 많이 하기 위해 증산을 억제하려는 특징이 있다(Je et al., 2006; Cheng et al., 2013). 이러한 결과로 고추와 가지는 SO2 노출 조건에서 기공을 통한 SO2의 유입을 막기 위하여 기공을 닫아 탄소를 얻는 것보다 수분손실을 최소화시켜 수분이용효율이 증가한 것으로 생각된다. 하지만 온실 내 가온 조건에서 시설원예작물이 SO2에 장기간 노출되면 광합성률이 더욱 감소되어 생장 및 생산량 저하가 클 것으로 판단된다. 따라서, 지속가능한 겨울철 작물생산을 위해서는 적절한 난방온도 설정 및 가온 횟수 조절을 통한 생리장해 예방이 필요하다.
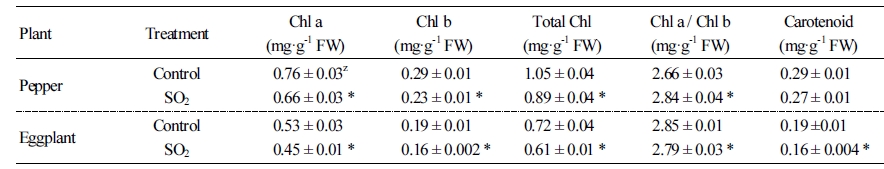
엽록소와 카로티노이드 분석
엽록소 a, b 및 총 엽록소 함량, 그리고 카로티노이드 함량 모두 대조구에 비해 50µg·kg-1 SO2 처리구에서 감소되는 경향을 보였다(Table 3). 고추의 경우 SO2 처리에 따라 엽록소 a 함량이 대조구에 비해 13% 정도 감소되었고, 엽록소 b 함량도 대조구에 비해 20% 정도 감소되었다. 또한 총 엽록소 함량은 15% 감소하였다. 가지에서는 대조구에 비해 SO2 처리구에서 엽록소 a 함량은 15%, 엽록소 b 함량은 15% 감소되었고, 총 엽록소 함량 역시 15% 감소되었다. 또한 스트레스 지표로써 나타나는 보조색소인 카로티노이드 함량은 SO2 처리구에서 각각 고추는 6%, 가지는 15% 감소되는 결과가 나타나 SO2 처리에 따른 식물의 엽록소 함량 변화를 확인할 수 있었다. 이러한 결과는 50µg·kg-1의 SO2 노출에 의해 잎 내 엽록소가 파괴되었음을 나타내며, 일반적으로 대기오염 스트레스에서 생장한 식물은 엽록소 함량을 감소시킨다는 결과와 일치하는 것으로 나타났다(Mcainsh et al., 2002; Haworth et al., 2012; Upreti et al., 2015).
엽록소는 광합성에 있어 빛 에너지를 일차적으로 수확하는 색소로 식물의 광합성능력을 나타내는 지표가 된다. 엽록소 함량은 식물이 광합성을 하는데 필수적인 색소로, 광합성 능력과 비례하는 것으로 알려져 있는데, 식물은 SO2와 같은 대기오염에 노출되면 황화나 백화현상과 같이 가시적으로 엽록소가 붕괴되는 현상을 보여준다. 이러한 엽록소 함량의 감소는 이전의 연구에서 다양한 작물들을 통해 연구가 진행되어 왔다(Lauenroth and Dodd, 1981; Kropff, 1987; Dhir et al., 2001; Joshi et al., 2009). 특히, 엽록소 a의 감소는 노화와 스트레스의 지표가 되는 엽록소a/b의 비율을 감소시킨다(Hikosaka and Terashima, 1995; Kitajima and Hogan, 2003).
카로티노이드는 대기오염과 같은 비생물적 스트레스에 의한 광합성 저하를 막기 위해 광보호를 하는 데 주요한 역할을 하는 색소이며, 산화스트레스로부터 막을 보호하는 데 쓰이기도 한다(Verma and Mishra, 2005). 이 실험에서는 SO2에 따라 엽록소 함량과 카로티노이드 함량의 감소가 나타났는데, 이는 SO2 50µg·kg-1 농도에 의해 색소체가 영향을 받아 엽록소 합성 과정에 손상이 일어나 나타난 결과로 보인다. 또한, SO2 처리구에서의 광합성 감소는 이 같은 엽록소 함량 감소와 관련이 있을 수 있는데, SO2 처리는 활성산소를 형성시켜 산화스트레스를 유발하여 광합성을 억제시키는 것으로 판단되며, 이러한 광합성 감소가 엽록소 합성을 억제시킴으로써 엽록소 함량이 더욱 감소된 것으로 판단된다.
가시적 피해증상 관찰
SO2 50µg·kg-1 처리에 의한 가시적인 피해는 고추의 경우 처리 14일째, 가지는 처리 후 18일째 처음 나타났다(Fig. 3). 고추의 경우 잎 표면에 황색 및 백색 반점이 엽맥 사이에서 관찰되었으며, 시간이 지날수록 탈색 및 괴사 현상이 나타났다(Fig. 3A and C). 가지는 잎 표면에 백색 반점 및 백화현상이 나타나며, 잎 가장자리가 말리는 현상이 나타나고 결국에는 두 작물 모두 20일째에 조기낙엽 현상이 관찰되었다. 식물은 SO2와 같은 대기오염 노출에 의해 엽록소가 파괴되어, 가시적으로 백화 및 황화 현상, 황색, 백색 반점, 탈색, 괴사 등이 나타난다(Heather, 2003; Brychkova et al., 2007; Baek and Woo, 2010; Yunus et al., 2013). 이러한 현상은 이 실험에서도 나타났다. 이를 통해 SO2 50µg·kg-1 농도에도 장기간 노출 시, 가지와 고추의 광합성률이 감소하고 엽록소 함량이 감소한 것을 가시적인 피해증상으로 더불어 설명할 수 있다. 겨울철 온실 내 가온 조건에서 적절한 농도조절이 이루어지지 않을 경우 생리적 피해와 더불어 가시적인 피해가 나타나는 것으로 보아 고추와 가지의 생산량과 더불어 품질에도 부정적인 영향을 미치는 것으로 판단되었다.
잎의 형태학적 특성
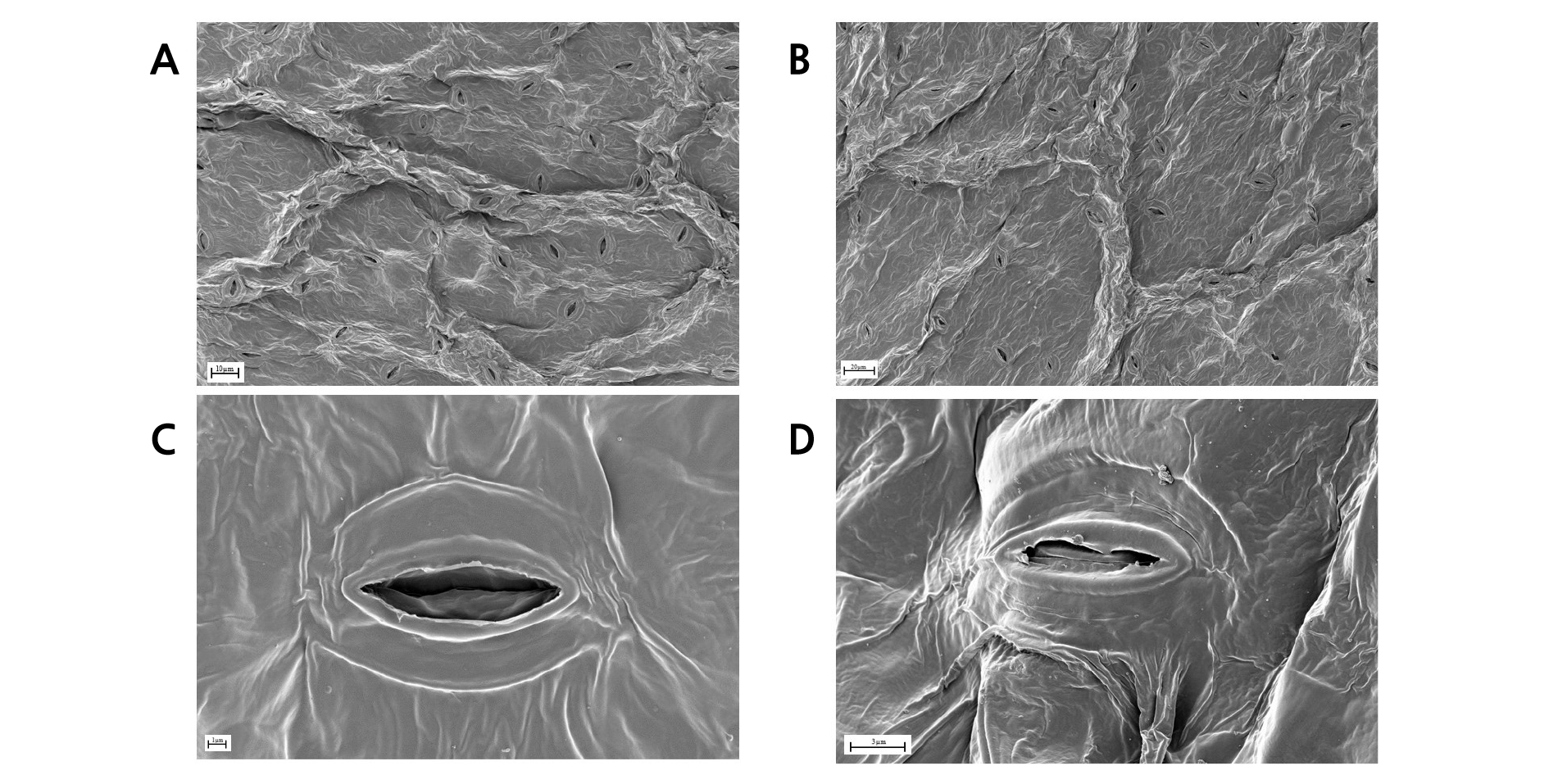
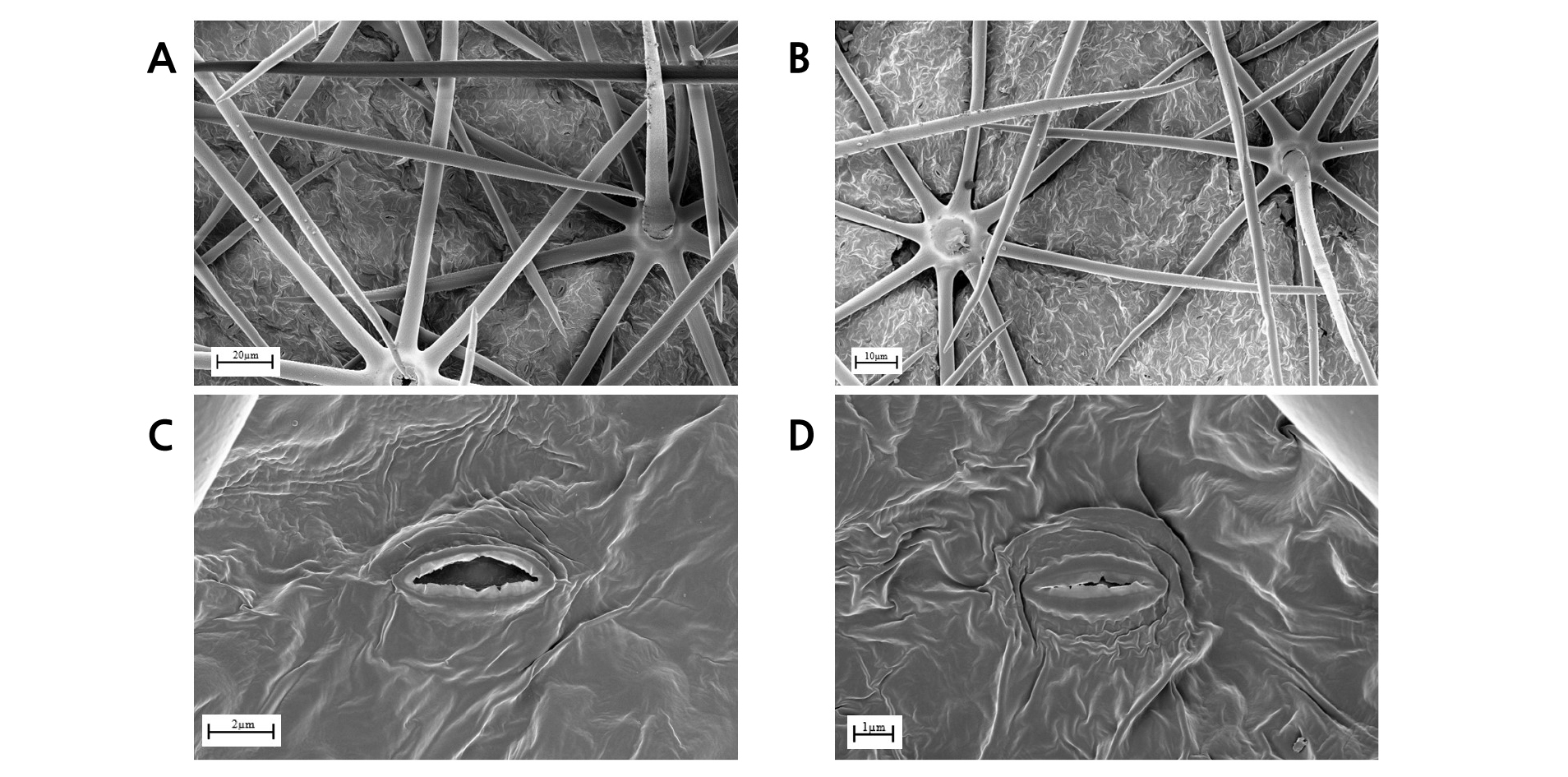
SO2는 식물체가 가스교환을 하는 과정에서 기공을 통해 식물체 내로 유입된다(Govindjee, 2012). 기공은 탄소 유입을 제한할 수 있기 때문에 식물의 생장과정에서 주요한 역할을 한다. 따라서 기공의 손상은 광합성률의 감소로 이어지게 되고, 식물 생장을 저해하며 결과적으로 생산량이 감소된다(Khan and Khan, 1993). 이 실험에서 SO2 50µg·kg-1 농도 처리 후 기공 형태를 관찰한 결과, 고추와 가지의 기공이 닫혀 있고, 기공 주변의 표피세포가 부풀어 오르며 파괴된 것을 관찰할 수 있었다(Figs. 4A-D and 5A-D). 이를 통해 SO2 50µg·kg-1 농도에 노출되면 기공의 개폐능력을 상실하게 되어 기공이 폐쇄되는 현상으로 볼 수 있으며, 이는 기공이 정상적인 기능을 수행하지 못하는 것으로 판단할 수 있다. Black and Black(1979) 연구에 따르면 SO2와 같은 대기오염물질에 노출 시 기공이 폐쇄되는 현상은 식물의 SO2에 대한 방어 작용으로 식물체내로 SO2가 유입되는 것을 차단한 것으로 해석할 수 있다고 보고하였다(Knabe, 1976; Gupta, 2016). 또한, SO2 노출시간이 증가할수록 기공은 기능을 상실하여 개폐작동이 원활하지 않게 된다고 하였다(Guderian, 2012).
SO2 처리 후 기공의 크기와 수가 두 수종 모두에서 통계적으로 유의한 차로 감소하는 경향을 보였다(Table 4). 기공의 크기는 스트레스를 받은 경우 작아지는데, 이 실험에서 단위면적(700×700µm)당 기공의 크기는 고추와 가지 모두 SO2 처리구에서 통계적으로 유의한 차이를 보이며 감소하였다.
시스테인(cysteine), 감마-글루타밀시스테인(γ-glutamylcysteine)과 글루타치온(glutathione, GSH) 함량
시스테인(cysteine), 감마-글루타밀시스테인(γ-glutamylcysteine)과 글루타치온(glutathione, GSH) 함량을 측정한 결과, 고추와 가지 두 수종 모두 SO2 처리구에서 높은 함량을 보였다(Fig. 6A, B and C), (Fig. 7A, B and C). 시스테인은 황화합물 대사에 있어 핵심이 되는 물질로서, 글루타치온의 중요한 전구체이며, 황 동화 과정 중 합성의 마지막 단계이다(Njålsson, 2005). 시스테인의 부족은 글루타치온 함량의 감소로 이어진다(Nikiforova et al., 2006). 이 실험 결과에서, 고추의 경우 시스테인 함량이 높게 나타났지만 감마-글루타밀시스테인 함량이 낮았다(Fig. 6A and B). 하지만 글루타치온 함량은 높게 나타난 것을 미루어보아 글루타치온으로 빠른 합성이 이루어진 것으로 생각된다(Fig. 6C). 가지에서도 역시 SO2 처리구에서 높은 시스테인 함량이 나타났으며, 통계적으로 유의한 차는 없으나 감마-글루타밀시스테인의 함량이 대조구에 비해 SO2 처리구에서 높았다(Fig. 7A and B). 이는 시스테인으로부터 합성이 많이 이루어진 결과로 보여지며 더불어 글루타치온 함량도 SO2 처리구에서 증가함을 보였다(Fig. 7C).
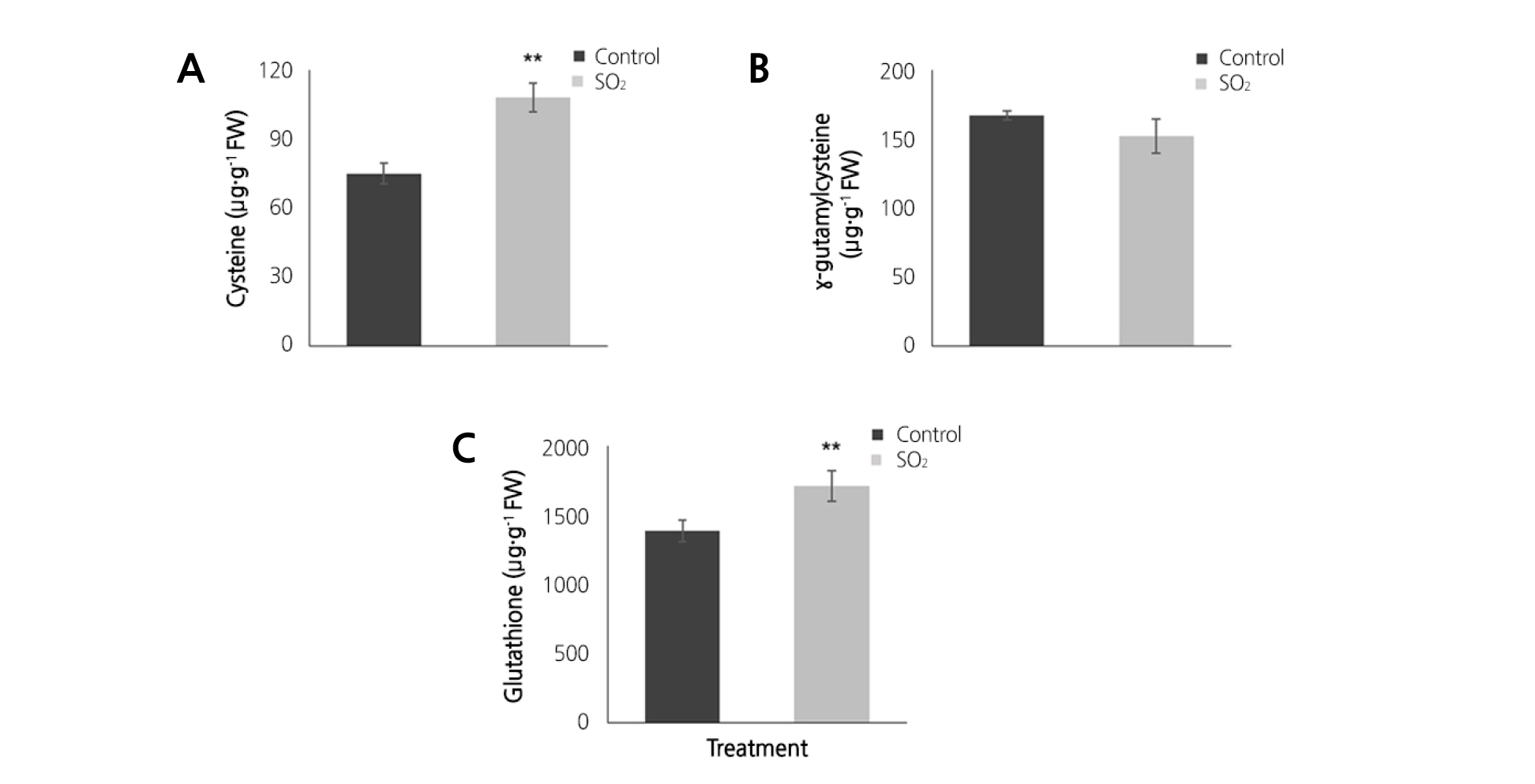
Fig. 6. Changes in cysteine (A), γ-glutamylcysteine (B) and GSH (C) contents in pepper under control (■) and 50 µg·kg-1 SO2 (■) conditions. Mean values are presented with vertical error bars that represent standard deviations (n = 3). Asterisks (*) indicate statistically significant differences between control and SO2 treatment (** p < 0.01 by independent t-test).
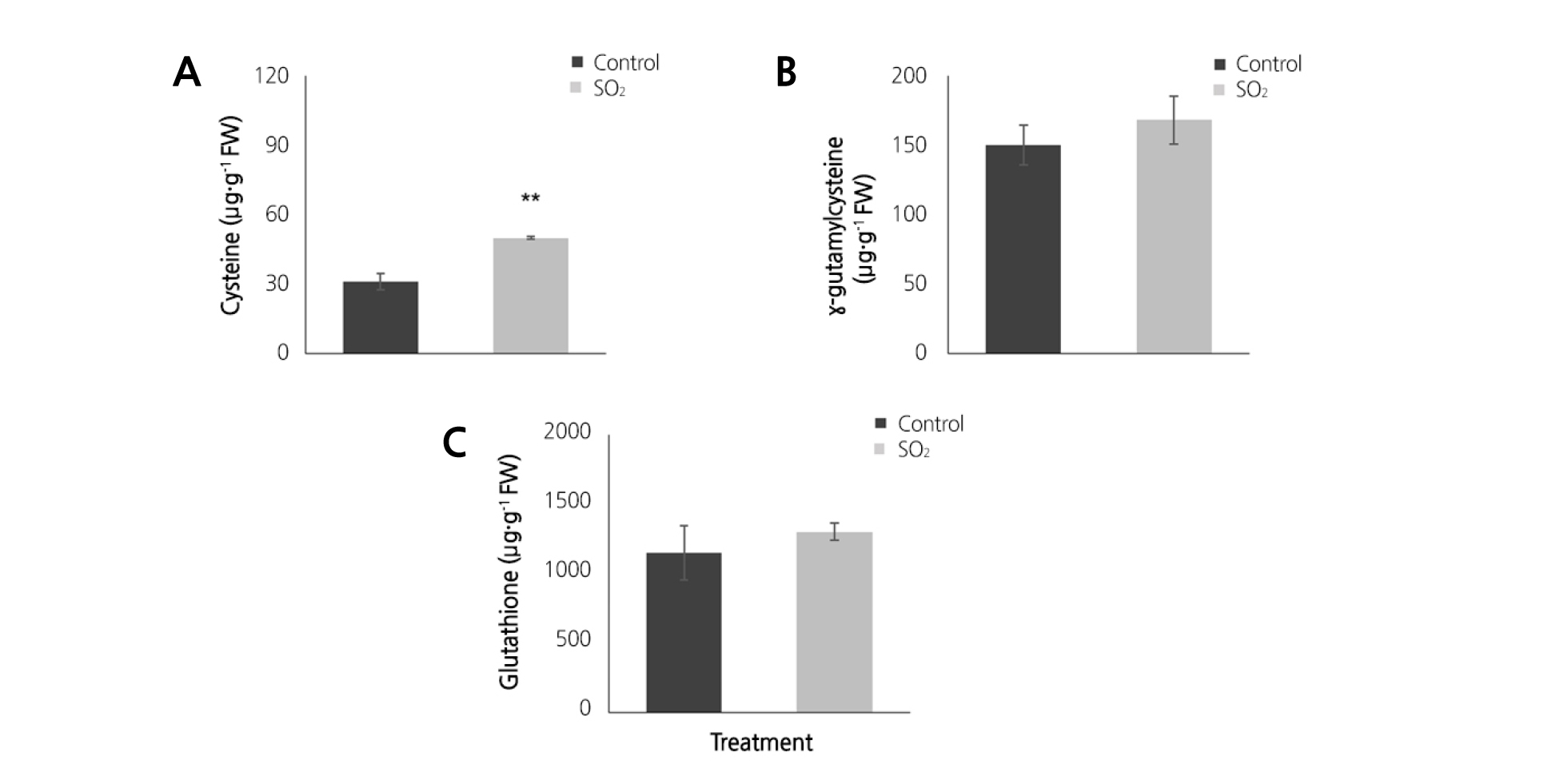
Fig. 7. Changes in cysteine (A), γ-glutamylcysteine (B) and GSH (C) contents in eggplant under control (■) and 50µg·kg-1 SO2 conditions (■). Mean values are presented with vertical error bars that represent standard deviations (n = 3). Asterisks (*) indicate statistically significant differences between control and SO2 treatment (** p < 0.01 by independent t-test).
글루타치온은 일반적으로 황 대사에 주요한 물질로서, 시스테인으로부터 감마-글루타밀시스테인을 거쳐 글루타치온으로 합성되며 특히, 글루타치온은 항산화 시스템에 중요한 역할을 하기도 한다(Noctor et al., 2012). 가온조건에서 발생되는 SO2 농도에 따른 고추와 가지의 적응능력에서 차이가 발생함을 알 수 있었는데, 고추의 글루타치온 함량이 가지의 함량보다 높게 나타났으며, 같은 SO2처리 조건에서 고추의 광합성능력이 가지보다 높은 결과와 일치하였다. 따라서 겨울철 가온에 따른 온실환경관리에 고추가 유리한 것으로 판단된다. 일반적으로 대기오염과 같은 환경적 스트레스를 받을 때 식물체 내 글루타치온 함량이 증가하는데(Hirase and Molin, 2003), 이 연구에서 온실 내 SO2 처리에 노출된 고추와 가지는 엽내 시스테인, 감마-글루타밀시스테인과 글루타치온 함량을 증가시켜 환경스트레스에 대한 항산화능이 향상되는 것을 확인하였다.