서 언
재료 및 방법
용매
시료
글루코시놀레이트(GSL) 추출
HPLC에 의한 글루코시놀레이트(GSL) 분석
LC-ESI-MS 분석에 의한 DS-GSL 동정
통계분석
결과 및 고찰
케일의 생장
GSL 분리 및 동정
생장단계에 따른 GSL 함량
품종 간 GSL 함량 비교
서 언
배추과(Brassicaceae) 채소는 350개의 속, 13개의 족으로 구분되어 있으며, 약 3,200종이 있다(Goncalves et al., 2012). 배추과 채소들은 글루코시놀레이트(glucosinolates, GSL), 비타민C(ascorbic acid), 비타민U(S-methylmethionine), 카로티노이드(carotenoids), 토코페롤(tocopherol), 폴리페놀(polyphenols)과 같은 기능성 성분 및 다양한 무기질 등의 함량이 풍부하다고 알려져 있다(Choi et al., 1995; Podsędek, 2007). 배추과 채소 중 Brassica oleracea는 백양배추(B. oleracea var. capitata f. alba), 적양배추(B. oleracea var. capitata f. rubra), 브로콜리(B. oleracea var. italica), 컬리플라워(B. oleracea var. botrytis), 싹양배추(Brussel sprouts, B. oleracea var. gemmifera), 케일(B. oleracea var. acephala) 등을 포함하고 있다(Hagen et al., 2009; Lee et al., 1997). 케일은 유럽 서북부가 원산지로 양배추 변종 중의 하나로서(Choi et al., 1995), 배추과 채소 중 항산화 활성이 가장 높은 것으로 보고되어 있다(Halvorsen et al., 2002).
|
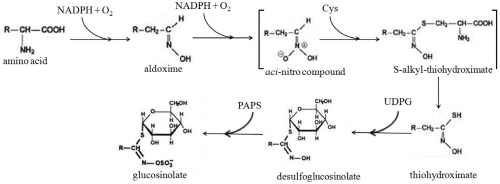
Fig. 1. Biosynthesis of glucosinolates (modified from Fahey et al., 2001; Halkier and Du, 1997; Lim, 2002). |
GSL는 질소와 황을 함유하고 있는 2차 대사산물로 배추과 채소에 널리 분포한다. GSL는 독특한 향기와 매운 맛을 내고 주로 종자에 많이 존재하며, 발아 후 생장하면서 그 농도가 줄어드는 것으로 보고되어 있다(Fahey et al., 2001; Lim, 2002). 현재까지 약 200종류 이상이 알려져 있으며 이 중 30여종이 생리 활성을 가진 것으로 알려져 있다(Clarke, 2010). GSL는 일반적으로 낮은 생리 활성을 갖지만 분해산물(isothiocyanates)은 항암 효과가 뛰어난 것으로 알려져 있다(Fahey et al., 2001; Zhang and Talalay, 1994). GSL는 화학적으로 안정한 상태로 존재하지만, 식물체 조직이 손상을 입으면 myrosinase(thioglycoside glucohydrolase, EC 3.2.3.1)에 의해 빠르게 가수분해되어 불안정한 중간체 thiohrdroxamate- O-sulfonate를 형성하며, 이 물질은 isothiocynates, oxazoldine- 2-thiones, indole-3-cabinol, nitriles, epithionitrile, thiocynates등과 같은 안정한 물질로 전환된다(Fahey et al., 2001; Halkier and Du, 1997; Higdon et al., 2007; Keck and Finley, 2004; Zhang et al., 2006). 특히 isothiocyanate는 주로 무독화효소 활성을 증가시키고, 세포자멸사(apoptosis) 및 세포주기 억제 기전을 통하여 방광암, 대장암, 폐암 등 항암효과가 뛰어나다고 보고되어 있다(Cartea et al., 2008; Hwang et al., 2012).
GSL는 그 전구체인 L-amino acid(methionine, tryptophan, phenylalanine) 종류에 따라 각각 aliphatic, indolyl, aromatic GSL 3그룹으로 구분된다(Lim, 2002; Sun et al., 2011). GSL 생합성 과정은 L-amino acid의 산화에 의해 aldoxime를 생성하고, 재산화를 통해 aci-nitro compound를 생성한다. 이 때 cysteine에 함유되어 있는 황으로부터 전자를 제공받아 thio기(-S)가 결합(conjugation)하여 S-alkylthiohydroximate가 된다. 이 물질은 glutathione-S-transferase에 의하여 촉매되어 thiohydroximate(C-S cleavage)가 생성되며, thiohydroximate glucosyltransferase(UDPG)에 의해 당화(glucosylation)과정이 일어나 desulfo(DS)-GSL이 생성된다. 마지막 단계에서 DS-GSL는 3'-phosphoadenosine-5'-phosphosulphate(PAPS)의 sulfate를 가져와(sulfation) GSL가 합성된다(Fig. 1)(Fahey et al., 2001; Halkier and Du, 1997; Lim, 2002).
이러한 GSL의 생리활성능력 때문에 식물체 내 GSL 총 함량 및 각 성분 측정은 매우 중요하고, 최근에는 배추과 작물 품종 개발뿐만 아니라 수확 적기 판단, 병충해 방제 등 다양한 분야에서 GSL분석 자료가 요구된다. 그렇지만 GSL 함량은 작물의 재배방법이나 기후조건, 작물의 영양상태, 유전적, 식물학적 특성에 따라 많은 영향을 받는다. 따라서 본 연구에서는 ‘케일 주스’로 많이 소비되고 있는 케일 잎을 생장 단계(35, 63, 91, 105, 119, 133 days after sowing, DAS)에 따라 수확하여 케일 잎의 GSL 함량을 평가하는 데 그 목적이 있다.
재료 및 방법
용매
HPLC-grade acetonitrile(CH3CN)과 methanol(CH3OH)은 J.T Baker chemical Co.(Phillipsburg, NJ, USA)를 사용하였다. Sodium acetate(NaC2H3O2・3H2O)은 Samchun Pure Chemical Co., Ltd.(Pyeongtaek, Korea) 것을 사용했으며, DEAE-Sephadex A-25는 GE Healthcare Bio-Sciences AB(Uppsala, Sweden)를 사용하였다. Sinigrin(2-propenyl GSL), aryl sulfatase(type H-1, EC 3.1.6.1)는 Sigma-Aldrich Chemical Co.(St Louis, MO, USA) 것을 사용하였다.
시료
케일 종자(Brassica oleracea var. acephala)는 2품종(‘Manchoo Collard’, ‘TBC’) 모두 아시아종묘(Asia seed Co., Ltd, Seoul, Korea)에서 구입한 것으로 2012년 2월 20일 충남대학교 농업생명과학대학 소재 부속 농장 유리 온실에 파종하였다. 72공-플러그 트레이(72 hole-plug tray)에 원예용 상토(High, Punong bed soil, Gyeongju, Korea)를 가볍게 담고 평평하게 한 후에 물을 적시고 케일 종자를 심은 다음 다시 상토로 복토를 하여 손가락으로 눌러 주었다. 햇볕을 차단하고, 수분의 증발을 막기 위하여 신문지로 덮고 그늘진 곳에 놓고 싹을 틔운 다음 삼일 후에 신문지를 걷어내고, 햇빛이 잘 비치는 곳으로 옮겨두었다. 5주 동안 지하수로 재배한 다음에 재배상태가 좋은 묘를 골라 상토(900g 사용)를 채운 포트(23 × 18cm)에 이식하였다.
재배기간은 총 133일로 각 시료는 이식 후 28일 간격(35, 63, 91, 119 days after sowing, DAS)과 14일 간격(91, 105, 119, 133 DAS)으로 3반복으로 수확하였다. 88, 101DAS에는 총 2회에 걸쳐 분말화한 비료(N-P-K, 22-12-12)를 각 1, 2g씩 추비하였다. 수확한 잎 시료는 -70°C 급속 초저온 냉동고(SFDSF 12, Samwon Freezing Engineering Co., Busan, Korea)에 보관하여 순차적으로 동결건조한 후에 막자와 막자사발로 분말하였다.
글루코시놀레이트(GSL) 추출
건조된 분말 시료 100mg을 칭량하여 2.0mL-Eppendorf tube에 넣고 끓는(endogenous myrosinase activity의 불활성화) 70%(v/v) methanol(1.5mL)를 첨가하여 진동혼합(vortex) 하였다. 항온수조(70°C)에서 5분간 조(crude) GSL를 추출하는 동안 2분 30초 후 진동혼합을 한 번 더 해주었다. 원심분리(12,000g, 10min, 4°C) 후에 상층액은 수거하고, 나머지는 동일한 과정으로 총 3회 추출하여 각 상층액을 모두 합하였다. 미니 칼럼 충진용 DEAE Sephadex A-25(30g)는 초순수에 녹여 분액여두에 넣은 다음 거의 빠져나가면 sodium acetate 0.5M(68g・L-1)를 넣어 H+ 형태로 활성화시켰다. 탈지면으로 1,000μL pipet tip 끝을 막은 mini-column에 상기의 활성화된 DEAE Sephadex A-25(약 78mg dry weight, DW)를 넣은 후 GSL 조 추출물(crude extract)을 pasteur pipette으로 로딩하였다. 로딩시킨 조 추출물이 다 빠지면 증류수 2mL를 로딩하여 칼럼을 세척하고, 세척 후 paraffin film로 칼럼 아래 부분을 막고 aryl sulfatase solution(115mg・5mL-1) 75μL를 넣은 후 칼럼 윗 부분을 paraffin film으로 막아서 16시간 동안 상온에서 정치하였다. Aryl sulfatase solution을 넣을 때 수평으로 로딩하여 벽에 붙지 않도록 주의하여야 한다. 16시간이 지난 후 초순수(0.5mL × 3회)로 2.0mL-Eppendorf tube에 DS-GSL를 용출하였다. 용출시킨 시료(DS-GSL)는 0.45μm hydrophilic PTFE syringe filter(직경 13mm)로 여과한 후, HPLC용 vial병에 넣어 냉장 보관하였다(modified from Kim et al., 2007).
HPLC에 의한 글루코시놀레이트(GSL) 분석
DS-GSL의 분석은 1200 series HPLC system(Agilent Technologies, CA, USA)를 사용하였고, 분석 칼럼은 Inertsil ODS-3 column(150 × 3.0mm I.d., particle size 3μm), 가드 칼럼은 Inertsil ODS-2 Cartridge Guard column E(10 × 2.0mm I.d., particle size 5μm)(GL Science, Tokyo, Japan)를 사용하였다. 칼럼 온도는 40°C, 검출 파장은 227nm, 유량은 0.2mL・min-1로 설정하였다. 시료는 automatic injector를 사용하여 10.0μL 주입하였다. 용매 A(초순수)와 용매 B(acetonitrile)를 이동상 용액으로 사용하였다. 용매 B를 18분까지는 7 → 24%로 증가시키고, 32분까지는 24%를 유지시키고 32.1분에 24 → 7%로 감소, 40분까지 7%를 유지시켰다. 각 GSL 성분의 정량은 외부표준물질인 sinigrin(0.1mg・mL-1, DS-sinigrin의 분자량 279)의 HPLC 피크 면적과 각 성분의 면적을 비교하고 그 값에 response factor(Clarke, 2010; ISO 9167-1, 1992.)를 곱하여 정량화(μmol・g-1 DW)하였다.
LC-ESI-MS 분석에 의한 DS-GSL 동정
각 DS-GSL 성분은 4000 QTrap LC-ESI-MS/MS system (Applied Biosystems Instrument)를 사용하여, positive ion mode([M+H]+)로 동정하였다. LC-ESI-MS/MS의 분석 조건은 다음과 같다. 분석 칼럼은 Inertsil ODS-3 column(150 × 3.0mm I.D., particle size 3μm)을 사용하였으며, 가드 칼럼은 Inertsil ODS-2 Cartridge Guard column E(10 ⨯ 2.0mm I.D., particle size 5μm)(GL Science, Tokyo, Japan)를 사용하였다. 칼럼 온도는 40°C, 검출 파장(detection wavelength)은 227nm, 유량(flow rate)은 0.2mL・min-1로 설정하였다. 시료는 자동 시료주입기(automatic injector)를 사용하여 10.0μL 주입하였다. 스캔범위(scan spectra)는 m/z 100–800로 설정하였고, 스캔시간(scan time)은 1.0s로 하였다.
통계분석
HPLC 분석 결과는 Microsoft Office Excel 2010을 이용하여 각 성분에 대한 함량의 평균값과 반복(n = 3)의 표준편차(SD, standard deviation)를 구하였다.
결과 및 고찰
케일의 생장
91DAS에서 ‘Manchoo Collard’는 가장 큰 잎의 길이가 평균 33.8cm, ‘TBC’는 34.2cm이었다. 잎의 수는 119DAS에서 ‘Manchoo Collard’가 평균 26.7장, ‘TBC’가 26.3장으로 가장 많았으며, 91, 105, 133DAS에는 ‘Manchoo Collard’가 18.7, 20.0, 21.0장, ‘TBC’가 23.0, 23.3, 26.3장이었다. 전체적으로 91DAS 이후에는 케일의 생장에서는 큰 변화가 나타나지 않았다(Fig. 2 and Table 1).
|
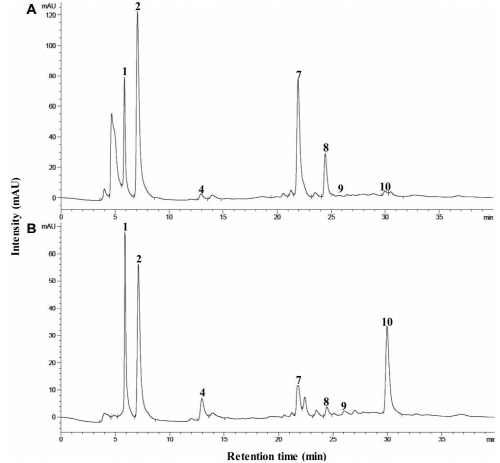
Fig. 2. HPLC chromatograms of glucosinolates separated from (A) ‘Manchoo Collard’, (B) ‘TBC’ cultivars at 133 DAS. Peak numbers refer to the glucosinolates shown in Table 1. |
GSL 분리 및 동정
HPLC를 통하여 케일을 분석한 결과, ‘TBC’에서는 총 10종의 GSL(progoitrin, sinigrin, glucoalyssin, gluconapin, glucoiberverin, 4-hydroxyglucobrassicin, glucobrassicin, 4- methoxyglucobrassicin, gluconasturtiin, neoglucobrassicin)가 분리되었으나 ‘Manchoo Collard’에서는 glucoiberverin을 제외한 9종의 GSL가 분리되었다. 10종류의 GSL 중 aliphatic GSL는 5종(progoitrin, sinigrin, glucoallysin, gluconapim, glucoiberverin), indolyl GSL는 4종(4-hydroxyglucobrassicin, glucobrassicin, 4-methoxyglucobrassicin, neoglucobrasscin), aromatic GSL는 1종(gluconasturtiin)으로 나타났다.
‘Manchoo Collard’와 ‘TBC’ 두 품종 모두 주요 GSL는 aliphatic GSL인 progoitrin과 sinigrin이었고 나머지 aliphatic, indolyl, aromatic GSL류는 적었다. 이는 GSL 생합성에 이용된 아미노산과 유전적 요인이 영향을 미쳤다고 판단된다(Agerbirk and Olsen, 2012; Magrath et al., 1994). Sinigrin과 progoitrin의 생합성에 이용되는 homo-methionine, di-homo- methionine은 GSL 생합성에 이용되었으나 glucoalyssin, indolyl GSL, gluconasturtiin를 생성하는 tri-homo-methionine, tryptophan, homo-phenylalanine(Agerbirk and Olsen, 2012; Halkier and Du, 1997; Sun et al., 2011)은 GSL 생합성에 많이 이용되지 않은 것으로 보여진다. 같은 아미노산으로부터 생합성되는 sinigrin, progoitrin의 함량은 높게 검출되었으나 glucoiberverin과 gluconapin의 함량이 낮게 검출된 이유는 GSL 생합성에 관여하는 유전자 GSL-OX(methylsulfinyl), GSL-ALK(alkenyl), GSL-OH(hydroxyalkenyl)에 의한 것으로 보인다. GSL-OX는 황을 산화시키는 역할을 하며, GSL-ALK는 methylthio기를 제거하고 이중결합을 만든다. 이때 생성되는 GSL가 sinigrin이다. GSL-hydroxyalkyl은 GSL의 곁사슬에 -OH기를 첨가시킨다(Halkier and Du, 1997; Sun et al., 2011). 이때 생성되는 GSL가 progoitrin으로 이들 유전자들의 작용결과로 중간 GSL인 glucoiberverin과 gluconapin이 많이 검출되지 않은 것으로 생각된다.
생장단계에 따른 GSL 함량
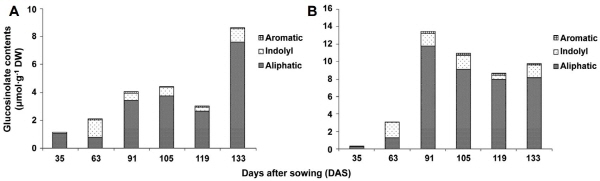
생장단계에 따른 케일 내 GSL 함량 범위는 ‘Manchoo Collard’(1.16–8.64μmol・g-1 DW), ‘TBC’(0.31–13.41μmol・g-1 DW)로 나타났다(Table 1). 이식 직후 수확한 묘(35DAS)의 GSL 함량은 ‘Manchoo Collard’(1.16μmol・g-1 DW), ‘TBC’(0.31 μmol・g-1 DW)로 모든 생장단계에서 가장 낮았다. ‘Manchoo Collard’는 133DAS에서 8.64μmol・g-1 DW, ‘TBC’는 91DAS에서 13.41μmol・g-1 DW로 가장 높았다. 133DAS에서 ‘Manchoo Collard’ 내 총 GSL 함량 중 가장 높은 비율을 나타낸 성분은 sinigrin으로 전체의 57%를 차지하였으며, progoitrin이 29%로 그 다음으로 높은 비율을 차지하였다. 91DAS에서, ‘TBC’ 내 총 GSL 함량 중 가장 높은 비율을 나타낸 성분은 sinigrin으로 전체의 43%를 차지하였으며, progoitrin이 33%로 그 다음으로 많은 비율을 차지하였다. Sinigrin과 progoitrin은 전체 생장단계 중 91DAS에서 가장 높게 나타났다. ‘Manchoo Collard’의 aliphatic GSL 함량은 119DAS와 133DAS사이에서 크게 증가하였다(Fig. 3). Indolyl GSL 함량은 35와 63DAS사이에 크게 증가하였다가 이후로 다시 감소하였다. Aromatic GSL인 gluconasturtiin은 63DAS에 처음 검출되었고, 133DAS까지 함량이 크게 변하지 않았다. ‘TBC’의 경우 aliphatic GSL 함량은 63DAS와 91DAS사이에 크게 증가하였다가 이후에 점점 감소하였다. Indolyl GSL 함량은 35DAS와 63DAS사이에 크게 증가하였다가 119DAS에서 크게 감소하였다. Aromatic GSL인 gluconasturtiin은 91DAS에 처음 검출되었고, 133DAS까지 함량이 크게 변하지 않았다. GSL 총 함량으로 비교했을 때 ‘Manchoo Collard’는 119, 133DAS 사이에서, ‘TBC’는 63와 91DAS 사이에서 함량 변화가 크게 나타났다. 이렇게 함량 변화가 크게 나타나는 이유는 시료 채취일(수확일)에서의 케일의 생육 정도를 보면 알 수 있다(Fig. 5 and 6). ‘Manchoo Collard’의 경우 119DAS의 케일 잎보다 133DAS 케일의 잎 크기가 확연히 크고 ‘TBC’의 경우 63DAS의 케일보다 91DAS 케일의 잎 수와 크기가 크게 달라진 것을 확인할 수 있다. 한편, ‘TBC’의 경우 91DAS 이후로는 GSL 전체 함량이 크게 달라지지 않았는데 이는 그에 해당하는 사진을 보면 알 수 있듯이 케일의 잎이 더 이상 크게 자라지 않았다. 이로 미루어 볼 때 케일 내 GSL 함량은 잎의 체적과 수량에 크게 영향을 받는 것으로 생각 되며 생육이 어느 정도 완성된 이후에도 주변 환경의 온도, 습도나 영양 상태에 따라 GSL 함량은 달라질 수 있으나 그 변화는 생장 정도에 비해 미미한 것으로 사료된다.
품종 간 GSL 함량 비교
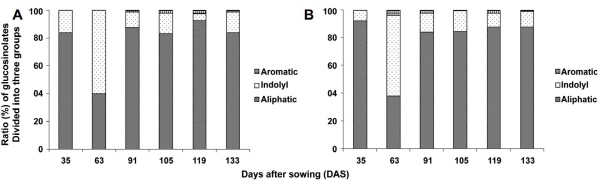
‘Manchoo Collard’와 ‘TBC’ 두 품종에서 동정된 GSL는 glucoiberverin을 제외한 9가지 GSL가 같은 종류의 GSL였다. 하지만 함량에서는 ‘Manchoo Collard’와 ‘TBC’가 최대 함량을 나타낸 133DAS, 91DAS기준으로 ‘TBC’가 ‘Manchoo Collard’보다 1.55배 높게 나타났다. 35DAS를 제외한 모든 수확시기에 ‘TBC’가 ‘Manchoo Collard’보다 1.13-3.33배 높게 나타났으며, 35DAS에서는 ‘Manchoo Collard’가 ‘TBC’보다 3.7배 높게 나타났다. ‘Manchoo Collard’의 총 GSL 함량 중 aliphatic GSL가 83%로 가장 높게 나타났으며, 다음으로 indolyl GSL가 15%, aromatic GSL가 2%로 나타났다. ‘TBC’의 총 GSL 함량 중 aliphatic GSL가 82%로 가장 높게 나타났으며, 다음으로 indolyl GSL가 16%, aromatic GSL가 2%로 나타났다(Fig. 4).
동정된 GSL 중 progoitrin, sinigrin, glucobrassicin, glu-conasturtiin은 ‘Manchoo Collard’와 ‘TBC’의 총 GSL 함량 중 각각 94%, 78%를 차지하였다. 이 중 progoitrin과 sinigrin은 aliphatic GSL로서 각각 분해산물로 nitrile과 isothiocyante인 crambene과 allyl isothiocyanete을 생성한다. glucobrassicin은 indolyl GSL, gluconasturtiin은 aromatic GSL로 분해산물로 indole-3-cabinol과 Phenethyl isothiocynate를 가진다. 이들 분해산물은 사람 또는 동물의 세포를 발암으로부터 보호해주는 물질로 알려져 있다(Fahey et al., 2001; Keck and Finley, 2004; Kim and Milner, 2005; Zhang and Talalay, 1994). 선행 연구 결과에 따르면 총 GSL 함량 중 Progoitrin, sinigrin, glucobrassicin, gluconasturtiin의 함량이 17.37, 66% (Cartea et al., 2008); 2.82, 35%(Kushad et al., 1999); 1.66, 26%(Kushad et al., 1999); 6.3, 43%(Kushad et al., 2004); 2.49, 28%(Sun et al., 2011)로 본 연구에서 나타난 GSL 함량이 가장 높게 나타났다. 따라서 ‘Manchoo Collard’와 ‘TBC’ 두 품종 모두 항암 효과를 가질 것으로 기대된다. 최근 케일 내 GSL에 관한 연구는 케일의 생육이 이미 끝난 상태에서의 GSL 함량, GSL의 항산화 활성, 관상용 케일 품종에 따른 GSL 함량 분포에 대한 연구 등이 있는데 케일의 생육정도에 따른 GSL 함량 변화에 대한 연구는 미미한 실정이다. 따라서 본 연구는 생육단계별 GSL 함량이 최대가 되는 생육 단계를 보여줌으로써 케일 활용에 있어서 더욱 유용한 정보를 제공할 수 있다.