서 언
재료 및 방법
식물 재료 및 온도 처리
RNA 분리 및 real-time PCR 분석
결과 및 고찰
온도 처리에 따른 온주밀감 ‘하례조생’ 과실의 유전자 발현 분석
온도 처리에 따른 ‘부지화’ 과실의 유전자 발현 분석
서 언
국내의 감귤류는 대부분이 제주지역에서 생산되고 있으며, 만다린에 속하는 온주밀감(Citrus unshiu)이 주로 재배되고, ‘금감’과 ‘부지화’(‘Shiranuhi’) 등의 만숙종 만다린 잡종이 시설에서 생산되고 있다(Song et al., 2011). 제주도의 감귤 재배면적은 21,300ha(2013년)이며, 노지 과원을 폐원하고 ‘부지화’ 등 만감류의 시설재배 면적은 꾸준히 증가하고 있다(KOSTAT, 2014).
온주밀감의 과실 품질은 과실 발달 2~3단계의 성숙과정에서 형성되는데, 품종, 수분 관리와 영양 상태, 전정, 착과 부위 및 형태, 과실의 크기, 토양 조건, 온도 및 광과 같은 기후 조건 등의 영향을 받아 과실의 물리적 특성과 화학적 조성을 갖추게 된다(Davies and Tucker, 2006; Iglesias et al., 2007; Zekri, 2011). 극조생 감귤류는 가을철의 이상 고온에 의해 10월 중순까지의 주간온도가 20°C 이상으로 유지되면 과실의 착색이 지연되어 감귤의 품질이 저하된다. ‘부지화’(‘Shiranuhi’)에서는 고온에 의한 생육기간 연장은 개화 불안정, 격년 결과 등을 초래하고, 과피 착색 불량 등의 상품성 저하를 유발하는 요인이 된다(Song et al., 2011). 이와 같이 온주밀감(극조생 감귤류)과 ‘부지화’에서 고온은 상품성을 크게 저하시키는 원인이 되고 있으나, 온주밀감은 성숙기의 온도가 낮은 조건 또는 개화기의 고온에 의해 착색이 촉진되고(Iwagaki and Hirose, 1980; Utsunomiya et al., 1982), 온도가 높은 수관외부 쪽의 과실이 착색이 양호하며 당함량은 높고 산함량은 낮다는 연구 보고(Izumi et al., 1990)도 있다. 수확 후의 과실에 단시간의 고온 처리를 하면 저온에 대한 내성이 증가하고(Holland et al., 2002; Lurie, 1998), 저장 기간이 연장되며(Sanchez-Ballesta et al., 2003), 산함량이 감소한다(Lee et al., 2007)는 연구 결과도 보고되어 있다.
지구온난화에 따른 기후변화는 원예작물의 생육기 온도변화를 야기하여 생물계절의 변화, 생산량과 과실 품질 등에 영향을 미치며, 특히 영년생 작물인 과수에서는 수체 생육이 불충실하게 누적되면서 과피의 착색이나 당 함량 등이 저하될 가능성이 제기되고 있다(Florides and Christodoulides, 2009; Son et al., 2014; Sun et al., 2012). 일본에서는 기후변화에 따른 품목별 대책을 수립하여 농가에서 실제 활용할 수 있는 기술을 개발하고 있으며, 감귤의 착색기 고온에 의한 착색 불량 및 부피과 발생에따른 피해를 최소화하기 위한 연구를 수행하고 있다K(im and Moon, 2012). 그러나 우리나라에서는 이에 관한 연구가 미흡한 실정이므로 감귤류의 생산과정에서 온도상승에 따른 성숙기 과실의 생리학적 변화와 피해 구명에 관한 분자생물학적인 연구가 필요한 실정이다.
따라서 본 연구에서는 감귤 생육기의 기온 상승에 따른 과실 성숙 불량의 원인 구명과 전사체 수준에서의 유전자 발현 분석에 요구되는 정보를 제공하기 위하여, ‘하례조생’과 ‘부지화’ 과실을 성숙기에 따라 3단계로 구분하여 고온에 노출 시킨 후 성숙과 관련된 유전자들의 발현 양상을 분석하고자 하였다.
재료 및 방법
식물 재료 및 온도 처리
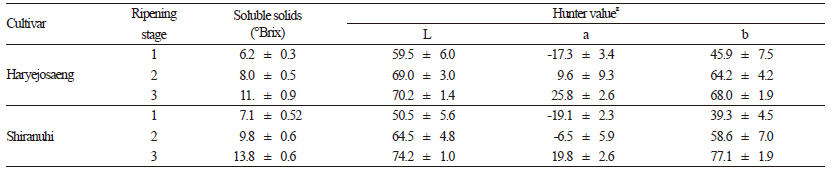
농촌진흥청 국립특작원예과학원 감귤연구소 시험포장에 재식 된 조생 온주밀감(C. unshiu)인 ‘하례조생’ 8년생과 만숙종 만다린 잡종인 ‘부지화’(C. reticulata) 8년생의 성목에서 과실을 각각 2014년 10월과 11월 중순에 수확하였고, 가용성 고형물 함량과 색도를 측정한 후(Table 1), 성숙단계를 3단계로 구분하여 실험에 사용하였다(Fig. 1). 가용성 고형물 함량은 과육의 손상없이 껍질을 벗기고 착즙하여 거즈로 거른 후 굴절당도계(Digital Refractometer PAL-1, Atago, Japan)로 측정하였고, 과피의 색도는 색차계(Chroma Meter CR-300, Minolta, Japan)를 이용하여 ‘하례조생’과 ‘부지화’ 과실을 적도 부위 4군데로 나누어 Hunter L, a 및 b 값을 각각 측정하였다. 온도처리를 위한 생장상의 온도 조건은 25 ± 1°C, 30 ± 1°C, 35 ± 1°C, 상대습도 60±10%, 광조건은 16시간/8시간(광/암)이 유지되도록 하였으며, 처리 0, 6, 12, 24, 48시간 후에 각각 과실을 채취하였다. 채취한 과실은 바로 8-16조각으로 자르고 고루 섞어 초저온 냉동고에 보관하고, 유전자 발현을 분석하기 위한 RNA 추출에 사용하였으며, 각 처리는 3반복으로 실시하였다.
RNA 분리 및 real-time PCR 분석
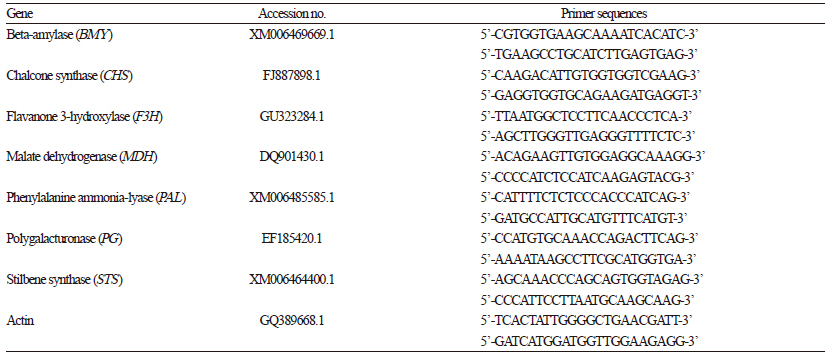
각 처리별로 채취한 과실 조각(1-2g)은 막자 사발에서 액체질소를 충분히 유지하면서 완전히 마쇄하였고 50mL 코닝 튜브에 넣어 다음 단계로 진행하였다. RNA 분리는 Chang et al.(1993)의 소나무 RNA 추출 방법에서 1, 2차 추출 단계의 원심분리 조건을 3,200rpm, 30분으로 바꾸고, 2-mercaptoethanol의 넣는 양을 수정하여 사용하였다. 분리한 RNA(500ng)는 GoScriptTM Reverse Transcription System (Promega, USA)을 이용 하여 1st cDNA를 합성하고 PCR 반응을 위한 주형으로 사용하였다.Quantitative real-time PCR 반응은 SYBR Premix Ex TaqTM(TaKaRa Bio Inc., Japan) 제조사의 방법대로 20μL 반응액을 조제하고, C1000TM Thermal Cycler(CFX96TM Real-Time System, BioRad, USA)를 이용하였으며, 사용한 7개의 primer set은 Table 1에 나타내었다. 반응 조건은 95°C에서 30초 후, 95°C에서 5초, 60°C에서 30초 반응을 40회 반복하였다. 발현 분석은 증폭량에 따른 형광 강도를 각 cycle 마다 측정하였고, 실험에 이용한 primer는 Table 2에 나타내었으며, 각각의 primer에 의한 발현값은 감귤 actin 유전자의 발현값에 비례하여 상대적으로 계산하였다.
결과 및 고찰
온도 처리에 따른 온주밀감 ‘하례조생’ 과실의 유전자 발현 분석
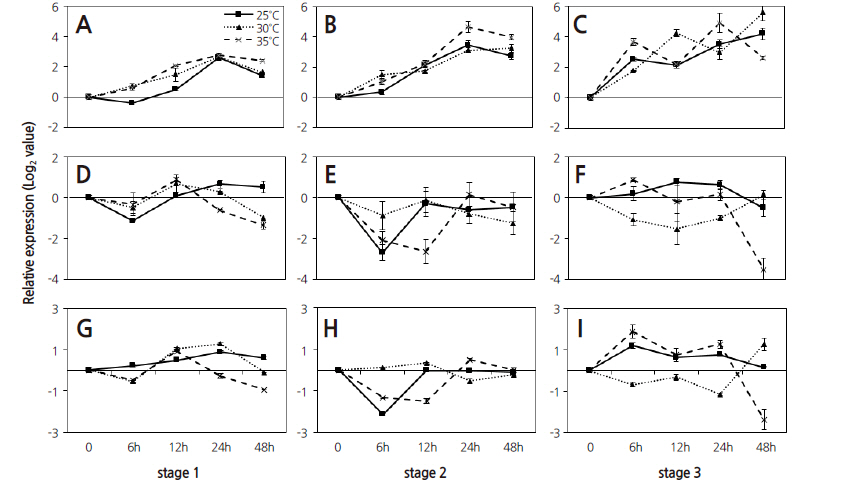
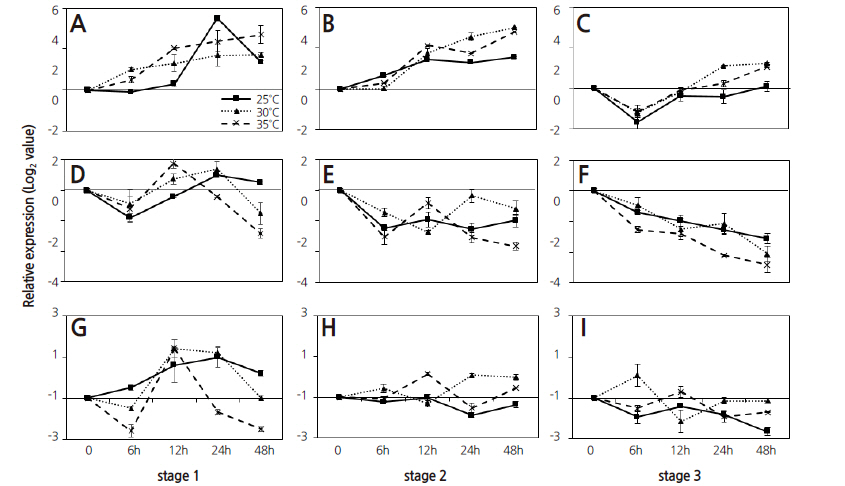
감귤(‘하례조생’) 과실을 성숙 3단계로 나누어 수확하여 온도에서 유지하면서 quantitative real-time PCR을 이용하여 betaamylase(BMY), polygalacturonase(PG), malate dehydrogenase(MDH) 유전자의 발현양상을 분석하였다(Fig. 2). BMY 유전자는 모든 단계에서 발현이 유도되었으며, 성숙 3단계에서는 1-2단계에 비해 모든 온도 처리에서 6시간이 경과한 후의 유전자 발현이 더 많이 유도되었다. 그러나, 25°C에 비해 30-35°C에서는 발현량이 증가하는 경향이었다. PG와 MDH 유전자는 비슷한 발현 양상을 나타내었다. PG 유전자는 1단계에서는 시간이 경과할수록 30-35°C에서 발현이 감소하는 경향이었으며, 2단계에서는 12시간이 경과한 후 발현이 저하되고 3단계에서는 25°C에 비해 30-35°C에서 발현이 억제되었으며, 특히 35°C에서는 발현이 현저하게 억제되었다. MDH 유전자는 초기 성숙단계인 1-2단계의 과실에서는 35°C에서 발현이 억제되었으며, 성숙이 진행되면서 3단계에서는 25°C에 비해 30-35°C에서 48시간이 경과한 후 현저히 감소하였다.
감귤 과실의 발달 단계별 flavonoid 생합성 및 stilbene 합성 관련 유전자들의 온도 처리에 따른 발현 양상을 분석하였다(Fig. 3). Phenylalanine ammonia-lyase(PAL) 유전자는 1단계에서는 모든 온도 처리에서 발현이 서서히 유도되는 양상이었으나, 25°C에 비해 35°C에서 억제되었다. 성숙이 진행된 2-3단계에서 30-35°C 처리구는 25°C에 비해 유전자의 발현이 증가하였다. Chalcone synthase(CHS) 유전자는 모든 온도 처리구에서 과실의 성숙이 진행됨에 따라 발현이 유도되었다. 2단계의 과실에서는 25°C에 비해 30°C에서 유전자의 발현이 증가하였으나, 성숙이 진행된 3단계에서는 30-35°C에서 발현이 감소하는 경향을 나타내었다. Flavanone 3-hydroxylase(F3H) 유전자의 발현은 1-2단계에서는 각 온도 처리구들이 비슷한 발현 양상으로 시간이 경과하면서 증가하였다. 성숙 3단계에서는 30°C에서는 12시간까지 발현이 증가하였다가 24시간에 감소하고, 48시간에 다시 증가하는 경향을 나타내었고, 35°C 처리구는 6시간과 24시간에서 2개의 정점을 보이고 48시간에서 발현이 크게 감소하였다. 3단계에서는 25°C보다 30-35°C에서 발현이 감소하는 경향이었다. Stilbene synthase(STS) 유전자의 발현양상은 성숙단계에 따라 1, 2, 3단계에서 각기 다른 발현 양상을 나타내었다. 성숙 1단계의 과실에서는 25°C에 비해 고온에서 유전자의 발현이 증가하였고, 35°C에서는 높은 수준의 발현이 유지되었으나, 30°C에서는 24시간이 경과하면서 발현이 현저히 감소하였다. 그러나, 성숙이 진행됨에 따라, 2-3단계의 과실에서는 25°C에 비해 30-35°C의 고온에서 발현이 증가하였다.
온도 처리에 따른 ‘부지화’ 과실의 유전자 발현 분석
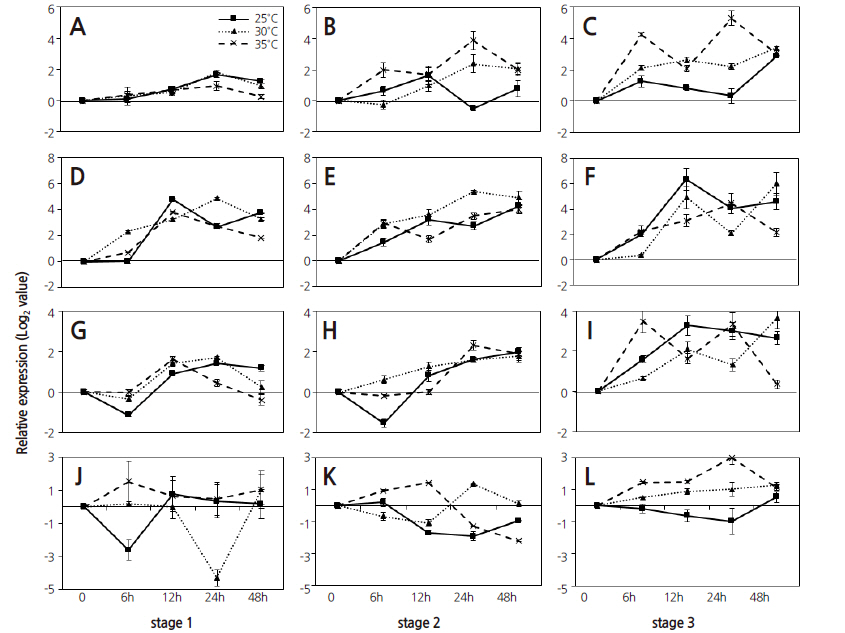
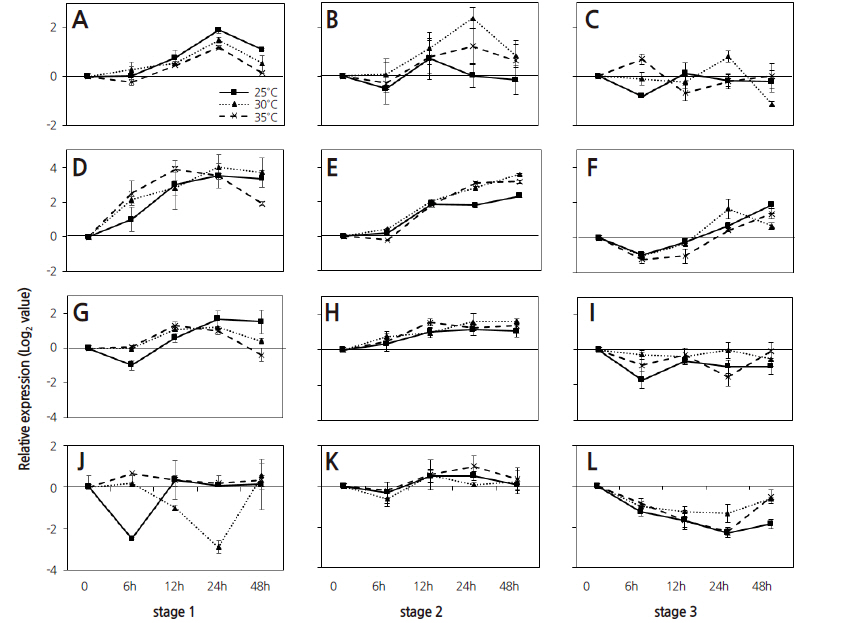
성숙 단계에 따라 3단계로 구분하여 수확한 ‘부지화’ 과실을 이용하여 온도에 대한 성숙과 관련된 유전자의 발현 양상을 분석하였다(Figs. 4 and 5). BMY 유전자의 경우, 1-2단계의 과실은 모든 온도에서 ‘하례조생’ 감귤 과실의 결과와 비슷한 경향을 보였으나 성숙이 진행된 성숙 3단계의 경우에는 ‘하례조생’ 감귤에서와는 달리 초기에는 감소하였다가 차츰 증가하는 경향이었다. 성숙 초기인 1단계 과실에서와 다르게 성숙이 진행되는 2-3단계의 모든 과실에서 25°C보다 30-35°C에서 유전자의 발현이 증가하였다. ‘부지화’ 과실에서 PG 유전자의 발현은 1, 2단계에서는 ‘하례조생’ 감귤 과실과 비슷한 경향이었고, 성숙이 진행됨에 따라 3단계에서는 모든 온도에서 유전자 발현이 현저히 저하되었다. 과실의 성숙이 진행되면서 고온에서 유전자의 발현이 억제되었으며 3단계에서는 고온인 35°C에서 발현이 크게 억제되었다. MDH 유전자는 25°C 처리구가 1단계에서는 유전자의 발현이 상승하다가 48시간에서 감소하였으나 2-3단계에서는 모두 감소하는 경향이었다. 1단계의 과실에서는 25°C보다 30-35°C에서 유전자의 발현이 감소하였으나, 유전자의 발현 양상은 비슷하였으며 성숙이 진행됨에 따라 25°C에 비해 고온(30-35°C)에서 유전자의 발현이 증가하는 경향이었다.
‘부지화’ 감귤 과실을 성숙 단계별로 고온에 유지하여 flavonoid 생합성 관련 및 STS 유전자의 따른 발현 양상을 조사하였다(Fig. 5). 성숙 1단계 과실에서의 PAL과 F3H 유전자의 발현 양상은 성숙 2단계 과실의 CHS와 F3H 유전자의 발현 양상과 각각 비슷한 경향을 나타내었다. PAL 유전자의 발현은 모든 온도에서 1단계에서는 대체적으로 서서히 증가하였으나, 25°C에 비해 30-35°C에서의 발현은 감소하였다. 그러나, 2단계의 과실에서는 25°C에 비해 고온에서 유전자의 발현은 증가하였고, 성숙 3단계에서는 온도에 따른 유전자 발현의 일정한 경향은 나타나지 않았다. CHS 유전자는 모든 온도에서 1-2단계에서는 계속 증가하는 경향이었고, 3단계에서는 초반에 감소하였다가 다시 증가하는 경향을 나타내었으나, 1-2단계의 과실에서는 고온에서 발현이 증가하였다. F3H 유전자는 25°C 처리구의 1단계에서는 초반에 감소하였다가 증가하고, 2단계에서는 처음부터 서서히 증가하는 경향이었다. 1단계의 30°C와 35°C 처리구에서 F3H 유전자의 발현양상은 24시간 이후에는 25°C에 비해 감소하였다. 3단계의 과실에서는 30-35°C에서 모두 발현이 저하되었지만, 25°C에 비해 발현은 많은 것으로 나타났다. ‘부지화’의 1단계 과실에서 STS 유전자의 발현은 모든 온도에서 감귤(‘하례조생’) 1단계 과실에서의 발현양상과 유사하였다. 감귤(‘하례조생’) 과실에서와 마찬가지로 초기에는 고온에서 발현이 많았지만 30°C에서는 급격히 감소하였다. 2단계의 과실에서도 모든 온도 처리구에서 초기에 발현이 억제되었다가 25°C와 35°C 처리구는 점차 증가한 후 서서히 감소하였다. 25°C에 비교하여 30°C에서는 발현양의 차이가 없었으나 35°C에서는 발현이 증가하였다. 3단계에서는 모든 온도 처리구에서 STS 유전자의 발현이 모두 저하되었으나, 고온에서는 시간이 경과할수록 발현이 증가하였다 .
Beta-amylase나 beta-mannosidase 등은 전분 분해 과정에 있어서 중요한 효소들이다(Mishra and Dubey, 2013). 황룡병에 감염된 mandarin의 전사체 분석 연구 논문(Xu et al., 2015) 결과를 보면, 차등 발현된 유전자들 중에서 발현이 억제된 대부분의 유전자들은 전분 대사 과정과 관련된 분해 효소 기능을 가지는 유전자들이며, 당대사와 관련된 4개의 beta-amylase, alcoholacyl transferase, glycosyl transferase family 8 유전자 등이 포함되었고, 발현이 유도되는 유전자들에는 ADP-glucose pyrophosphorylase, α-amylase, β-glucosidase, starch synthase 등 9종의 유전자가 포함되었다. Monroe et al.(2014)은 애기장대를 연구한 논문에서 온도나 수소이온농도 등의 다양한 스트레스 조건에 따라 BAM1과 BAM3 유전자가 서로 다른 발현 양상을 나타낸다고 하였는데, BAM1은 고온(35-45°C)에서, BAM3는 저온(10°C)에서 발현이 강하게 유도된다고 하였다. 본 연구의 결과에서 ‘하례조생’과 ‘부지화’의 BMY 유전자는 애기장대의 BAM1 유전자와 비슷하게 30-35°C 처리구에서 발현이 유도되는 경향을 나타내었다.
고온에 의한 세포벽의 변성은 에틸렌에 의해 조절되는 펙틴 분해효소에 의해 이루어지며(Lurie et al., 1996), PG의 mRNA 축적과 전사, 효소 활성 등은 에틸렌 의존적이라고 알려져 있다(Brummell and Harpster, 2001). 감귤류의 과실의 경우, 펙틴 중 합체의 변성에 중요 효소인 exopolygalacturonase의 활성은 매우 낮은 편이나(Riov, 1975), 펙틴 가용화에 있어서 이러한 효소들의 역할은 고온에 의한 것인지 또는 저온에 의한 것인지 확실하게 설명되어 있지 않다(Holland et al., 2012). 이러한 보고와 유사하게 본 연구에서도 PG 유전자의 발현은 두 품종 모두에서 전체적으로 감소되는 경향이었고, 시간이 경과할수록 25-30°C에서 보다 35°C의 고온에서 크게 감소하였다. 이러한 PG 유전자의 발현은 사과 과실(Kim et al., 2015a)과 포도 과실(Kim et al., 2015b)에서도 비슷한 경향을 나타내었다.
MDH 유전자는 세포에서 다양한 분자 형태로 존재하며, 미토콘드리아 MDH와 세포질 MDH로 식물에서 확인할 수 있다(Shannon, 1968; Yang and Scandalios, 1974; Yudina, 2012). 감귤류의 MDH 유전자에 대한 연구는 저온이나 dehydration에 의해 발현이 조절되고(Hara et al., 1999; Porat et al., 2002), 저온에 민감한 mandarin 외피에서 dehydrin을 encode하는 Crcor15가 과피에서 2°C나 12°C에서는 발현이 유지되었는데 37°C에서는 저하되었다고 보고 되어 있다(Sanchez-Ballesta et al., 2004). 본 연구에서 MDH 유전자는 1단계에서는 ‘하례조생’과 ‘부지화’에서 증가하는 경향이었으나, 성숙이 진행되면서 2, 3단계에서 두 품종에서 서로 다른 반응을 나타내었다 .
플라보노이드 생합성 과정은 phenylpropanoid 합성경로를 통해 일어나며, 여기에는 PAL, CHS, CHI, F3H, dihydroflavonol 4-reductase(DFR) 등 다양한 효소들이 관여하고 있다(Bogs et al., 2006; Boss et al., 1996; Ford et al., 1998). 플라보노이드 생합성과 관련된 유전자들의 발현은 사과의 착색에서 안토시아닌의 축적에 영향을 끼치며, 과실의 안토시아닌 함량과도 일치하는 발현 양상을 나타낸다(Honda et al., 2002). 감귤류에서 PAL의 활성 유도는 저온에 의한 증상 발달(Sanchez-Ballesta et al., 2000b), 감마선에 의한 과피 손상(Riov et al., 1968), 기계적 손상 후 발생하는 치유 과정(Ismail and Brown, 1979) 등과 함께 일어난다고 보고되어 있다. Sanchez-Ballesta et al.(2000a)은 고온 전처리(37°C)에 의해 감귤류의 PAL 유전자 발현과 효소 활성은 4시간 만에 가장 활발하고, 그 후 서서히 감소하는 경향을 보였으며, 이들은 저온 저장에서 내성을 나타냈다고 보고하였다. 사과 과실에서는 안토시아닌 함량과 PAL 활성은 15-20°C 정도에서 효과적으로 유도된다(Lee, 1999; Noro et al., 1991). 과실착색과 관련하여 CHS 유전자의 발현은 다양한 과실에서 보고(Cotroneo et al., 2006; Wang et al., 2010)되어 있는데, 빛과 UV-B 조사(Feng et al., 2010; Ubi et al., 2006), 저온(Crifo et al., 2011; Lo Piero et al., 2005) 등에 의해서 발현이 유도되며, 과수에 따라 다르게 조절되는 것으로 여겨진다(Xie et al., 2011). Crifo et al.(2011)은 blood orange에서 저온 스트레스는 유전자의 발현을 통해 안토시아닌 생합성을 증가시키며, 이와 관련된 PAL과 CHS 등 유전자의 발현이 증가되었다고 보고하였다. 사과나 포도 과실에 관한 연구에서는 30-35°C의 고온이 안토시아닌 함량을 감소시키고 안토시아닌 생합성 관련 유전자들의 발현도 저하되었다는 보고도 있다(Azuma et al., 2012; Lin-Wang et al., 2011). F3H 유전자는 저온에 의해 발현이 증가한다고 보고(Ban et al., 2007)되어 있는데, Ubi et al.(2006)은 사과 과피에서 UV-B와 온도에 따라 MdF3H와 pDFR 유전자는 모든 처리구에서 발현 되었고, MdCHS, MdANS, pUFGluT 등의 유전자는 고온(27°C)과 UV-B 처리 유무에 따라 약하게 발현되었다고 하였다. 본 실험에서 ‘하례조생’에서는 PAL 유전자는 35°C(2, 3단계)에서, ‘부지화’에서는 30°C(2단계)에서 발현이 크게 유도되는 경향을 보였다. 또 CHS 유전자의 경우에는 3개의 온도 조건에서 유전자의 발현이 유도 되는 경향이었으나 성숙 2단계의 ‘부지화’에서는 CHS 유전자의 발현이 감소하였다가 증가하는 경향을 보였다. ‘하례조생’의 경우, 특히 CHS와 F3H 유전자는 3단계의 25°C 처리구에서 발현이 크게 증가하는 경향이었다S. TS 유전자 또한 과실 착색과 관련이 있으며C, HS 유전자와 같은 기질을 이용하는 경쟁 관계에 있다(Ahn et al., 2015; Park et al., 2010; Richter et al., 2006). Kim et al.(2015b)은 성숙 단계의 ‘거봉’ 포도에서 STS 유전자의 발현은 35°C에서 강하게 유도되었다고 보고 하였는데, 본 연구에서도 3단계의 ‘하례조생’은 35°C에서 발현이 크게 유도되었으나 ‘부지화’는 3단계의 모든 온도에서 감소하는 경향을 나타냈다.
‘하례조생’과 ‘부지화’의 온도처리에 의한 유전자 발현 양상을 비교해 볼 때, 유전자의 발현양은 ‘하례조생’에서 더 크게 나타났으며, 1, 2단계에서 유전자의 발현 양상은 대체적으로 비슷한 경향이었는데, ‘부지화’ 과실에서 3단계의 유전자 발현은 ‘하례조생’과는 다르게 감소하는 경향을 나타내었다. 만숙종인 ‘부지화’는 온주밀감에 비해 온도에 더 민감하며 내한성이 약하고 고온 적응성이 좋은 특성(Moon, 2006; Moon and Kim, 2001)과 재배 환경 조건에 따라 수체 생육이나 과실의 품질이 크게 차이가 나는(Han and Kang, 2011; Moon et al., 2008) 등의 생육 특성을 가진다. 본 연구의 온주밀감과 ‘부지화’에서 나타나는 유전자들의 다른 발현 양상은 아마도 위에 언급한 ‘부지화’와 온주밀감의 생육특성의 차이, 즉 수체 생장이나 과실 성숙, 성숙 단계에 따른 성분이나 효소 활성 변화 등과도 관련이 있을 것으로 생각된다 .
기후변화 시나리오에 따르면, 21세기말 우리 나라 평균온도는 약 6.0°C 정도 상승할 것이라고 하며(NIMS, 2011), 이러한 기후변화로 인한 온도 상승과 이에 따른 과실의 수량 및 품질 등에 미치는 영향은 전세계적으로 여러 과수에서 부정적인 문제로 작용할 것이다(Easterling et al., 2007; Sugiura and Yokozawa, 2004; Sugiura et al., 2012). 본 연구에서는 ‘하례조생’과 ‘부지화’ 과실을 성숙 단계별로 구분하고 고온 스트레스에 노출시켜 여러 유전자들의 발현양상을 분석하였다. 이러한 연구 결과는 고온 스트레스와 관련된 다양한 생리현상을 전사체 분석을 통한 유전자 발현 수준에서 구명하고, 전사체 기반의 유용 유전자들을 대량 발굴하여 분자생물학적 연구에 도입함으로써 기후변화에 대응할 수 있는 재배법을 확립하고 고온에 내성인 신품종을 육성하는 데 중요한 자료로 활용할 수 있을 것으로 생각된다