서 언
재료 및 방법
식물 재료 및 전체 게놈 DNA 추출
엽록체 trnL-trnF 및 ITS 영역의 PCR 증폭 및 산물 정제
엽록체 trnL-trnF 및 ITS 영역의 염기서열 및 유연관계 분석
결과 및 고찰
엽록체 및 ITS 영역의 PCR 분석
엽록체 trnL-F 영역의 유전적 유연관계분석
ITS 영역의 유전적 유연관계분석
시판 품종의 저항성
서 언
감귤은 운향과(Rutaceae) 감귤아과(Aurantioideae)에 속하는 작물로써 전 세계적으로 중요하게 재배되고 있는 작물 중 하나이며(Coletta-Filho et al., 1998), 16종으로 구분한 Swingle and Reece(1967)과 162종으로 구분한 Tanaka(1977) 분류법에 의하여 분류되고 있는데(Barkley et al., 2006; Federici et al., 1998; Jung et al., 2005), 종 속간 유성교잡 및 높은 빈도의 가지변이 발생 등에 따른 번식, 그리고 널리 분포되어 있는 야생종들 때문에 계통을 분류하는 것은 쉽지가 않다(Cameron and Frost, 1968; Federici et al., 1998; Pang et al., 2007).
제주도내 재래감귤은 서기 476년 22품종이 재배된 것으로 고문서에 보고되고 있으나(Kim et al., 2001), 정확한 기원에 대한 연구는 미흡한 실정이다(Jung et al., 2005). 또한, 이들 품종들 중 맛이 없고 품질이 떨어지는 품종들은 차차 개량되어(Kim et al., 2001) 왔기 때문에 형태학적(Barrett and Rhodes, 1976; Scora 1975) 방법으로는 품종간 유연관계를 분류하는 것은 쉽지가 않았다(Jung et al., 2005).
초창기에는 감귤 품종간 유연관계를 분석하기 위하여 형태학적 생화학적 기술을 이용한 Isozyme(Herrero et al., 1996; Moon et al., 1992) 방법이 사용되었으나, 이 방법은 돌연변이에 의해 발생되는 품종들간 구별에는 적합하지 않았다(Rahman et al., 2001; Roose, 1988). 최근 분자 생물학이 발달하면서 식물들의 분류학적 연구에 RAPD(random amplified polymorphic DNA)(Deng et al., 1995, Oh, 1996), RFLP(restriction fragment length polymorphism)(Federici et al., 1998), ISSR(inter simple sequence repeat)(Fang et al., 1998; Gulsen and Roose, 2001), SSR(simple sequence repeat)(Barkley et al., 2006; Hong et al., 2016; Luro et al., 2008), 세포질 내 엽록체(Cheng et al., 2005; Deng et al., 2007; Jung et al., 2005; Penjor et al., 2013)와 미토콘드리아(Froelicher et al., 2011) 게놈에서 분리된 유전자와 스페이서 영역을 이용한 연구(Jung et al., 2005; Olmstead and Palmer, 1994), 그리고 핵 리보솜 DNA내 ITS 영역(Hynniewta et al., 2014; Jin et al., 2016; Sun et al., 2015)을 이용한 분자마커 기술이 광범위하게 사용되고 있다(Abkenar and Isshiki, 2003; Hazarika et al., 2014; Tingey and Tufo, 1993; Whitkus et al., 1994).
재래감귤은 선사시대부터 제주도에서 재배된 품종(Jung et al., 2005; Kim et al., 2001; Sun et al., 2015)으로서 유성교잡에 의한 종자번식(Chae et al., 2012; Song et al., 2011)으로 오랜 기간 동안 재배되어 오면서 품종들 간 유전적으로 안정화된 것으로 추측되고 있으나(Penjor et al., 2013), 재래감귤에 대한 연구는 미흡한 상태이다. 따라서, 이 연구에서는 양친의 유전자 확인에 사용하는 핵 리보솜 DNA내 ITS(ITS1-5.8S-ITS2) 전체 영역의 염기서열과 모계유전과 관련된 세포질 내 엽록체 영역의 염기서열을 이용하여 제주도 내 재래감귤 품종들 간의 계통관계 분석을 위한 기초자료로 사용하기 위하여 유연관계를 조사하였다.
재료 및 방법
식물 재료 및 전체 게놈 DNA 추출
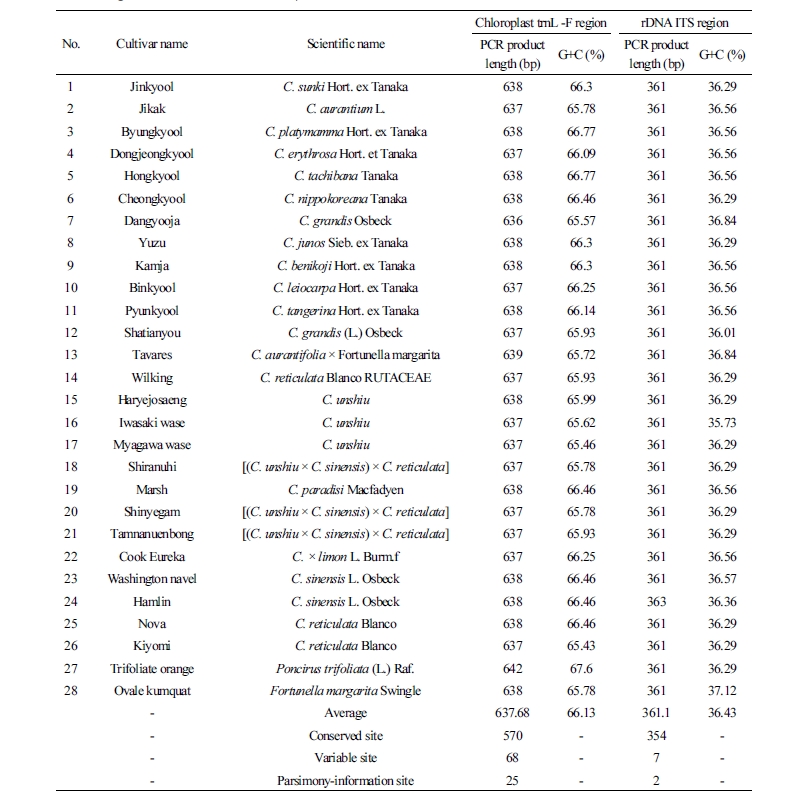
이 연구에 사용된 제주도 재래감귤 11품종[‘진귤’(‘Jinkyool’: C. sunki Hort. ex Tanaka), ‘지각’(‘Jikak’: C. aurantium L.), ‘병귤’(‘Byungkyool’: C. platymamma Hort. ex Tanaka), ‘동정귤’(‘Dongjeongkyool’: C. erythrosa Hort. et Tanaka), ‘홍귤’(‘Hongkyool’: C. tachibana Tanaka), ‘청귤’(‘Cheongkyool’: C. nippokoreana Tanaka), ‘당유자’(‘Dangyooja’: C. grandis Osbeck), ‘소유자’(‘Yuzu’: C. junos Sieb. ex Tanaka), ‘감자’(‘Kamja’: C. benikoji Hort. ex Tanaka), ‘빈귤’ (‘Binkyool’: C. leiocarpa Hort. ex Tanaka), ‘편귤’(‘Pyunkyool’: C. tangerina Hort. ex Tanaka)]과 감귤속 15품종[문단(‘Shatianyou’: C. grandis (L.) Osbeck), 라임(‘Tavares’: C. aurantifolia × Fortunella margarita), ‘윌킹’(‘Wilking’: C. reticulata Blanco RUTACEAE), ‘하례조생’(‘Haryejosaeng’: C. unshiu), ‘암기조생’(‘Iwasaki wase’: C. unshiu), ‘궁천조생’(‘Myagawa wase’: C. unshiu), ‘부지화’(‘Shiranuhi’: [(C. unshiu × C. sinensis) × C. reticulata]), 자몽(‘Marsh’: C. paradisi Macfadyen), ‘신예감’(‘Shinyegam’: [(C. unshiu × C. sinensis) × C. reticulata]), ‘탐나는봉’(‘Tamnanuenbong’: [(C. unshiu × C. sinensis) × C. reticulata]), 레몬(‘Cook Eureka’: C. × limon L. Burm.f.), ‘워싱톤 네블’(‘Washington navel’: C. sinensis L. Osbeck), ‘햄린’(‘Hamlin’: C. sinensis L. Osbeck), ‘노바’(‘Nova’: C. reticulata Blanco), ‘청견’(‘Kiyomi’: C. reticulata Blanco)] 탱자속 1품종[‘탱자’(‘Trifoliate orange’: P. trifoliata (L.) Raf.)] , 금감속 1품종[‘장실금감’(‘Ovale kumquat’: F. margarita (Lour.) Swingle)]들 총 28품종들은 2015년 9월 14일 감귤 연구소 내 보존 재배되고 있는 품종들을 수집하였고, Automatic Nuclear extraction(MX 16, Promega, Madison, WI, USA)을 이용하여 전체 게놈 DNA를 추출하였다. 추출한 전체 게놈 DNA는 -70°C에 보관하여 실험에 사용하였다.
엽록체 trnL-trnF 및 ITS 영역의 PCR 증폭 및 산물 정제
엽록체 TrnL-F 영역에 대한 PCR은 trnL3’ exon과 trnF5’ exon 지역이 포함되도록 제작(Sang et al., 1997)한 Jung et al.(2005)의 방법에 따라서 trnLF(5’-AAAATCGTGAGGGTTCAAGTC-3’)와 trnFR(5’-GATTTGAACTGGTGACACGAG-3’) 영역 프라이머 조합을 이용하여 PCR를 수행하였으며, 핵 Ribosomal DNA의 전체 ITS 영역에 대한 PCR 증폭 산물을 얻기 위하여, Jin et al.(2016) 의 연구결과에 따라서 18S rDNA와 ITS1 영역을 포함하도록 ITS1F1 프라이머(5’-GAAGGATCATTGTCG ACCTGCCAGCAGACG-3’)와 ITS2, 그리고 28S rDNA 영역을 포함하도록 ITS2R2 프라이머(5’-GACCTGGGGTCGCAA TGCGAGCGCCGCTT-3’) 조합을 제작하여 사용하였다.
엽록체 TrnL-F 영역과 5.8S rRNA 유전자 영역을 포함한 ITS 전체 영역(ITS1-5.8S-ITS2)이 포함된 증폭산물을 얻기 위하여, PCR 반응액은 AccuPower® Multiplex PCR PreMix(Bioneer, Corp., Daejeon, Korea)[250µM dNTP, 1.5mM MgCl2, 1.0 unit Taq DNA polymerase, 10mM Tris-HCl(pH 9.0), 40mM KCl]에 주형 25-50ng DNA, 그리고 0.5µM의 프라이머를 첨가하여 20µL로 조정하여 사용하였으며 PCR 반응은 Takara PCR Thermal cycle(Takara, Bio Inc., Japan)을 이용하여 35cycle 실시하였다. PCR 반응조건은 95°C에서 30초 동안 denaturation, 58°C에서 30초 동안 annealing, 그리고 72°C에서 40초간 extension을 수행하였다. 증폭된 PCR 생성물은 1.2% agarose gel에서 100V로 30분 동안 전기영동하여 나타나는 밴드로 확인하였고, agarose gel에서 확인된 증폭 산물은 GgenAll® Gel 정제 kit(GgenAll Biotechnology, Co., Seoul, Korea)을 이용하여 정제하였으며, 정제된 ITS 증폭산물은 pLUG-Prime® TA-Cloning Vector kit(iNtRON, Korea)를 사용하여 클로닝 하였다(단, 정제된 엽록체 TrnL-F 영역이 포함된 증폭산물은 클로닝하지 않고 바로 염기서열 분석을 의뢰하였다). 클로닝된 PCR 산물은 ㈜솔젠트(Solgent, Co., Daejeon, Korea)에 의뢰하여 염기서열을 결정하였다.
엽록체 trnL-trnF 및 ITS 영역의 염기서열 및 유연관계 분석
재래감귤 11품종들을 포함한 총 28종의 감귤류에 대한 계통학적 유연관계 분석을 위하여, 엽록체 trnL-F 및 ITS 영역의 염기서열은 Bioedit(Hall, 1999)을 이용하여 편집하였으며 no gap으로 한 후 multi Clustal W로 정렬하여 저장하였다. 계통학적 분석은 MEGA 5.0 프로그램으로 사용하였고, 유전적 거리 계산은 Just-control model를 이용하였으며. Maximum Likelihood(ML) 기법으로 계통수 분석을 실시하여 유연관계를 작성하였다. 그리고, Bootstrap 값은 1,000회 반복하여 수행하였다.
결과 및 고찰
엽록체 및 ITS 영역의 PCR 분석
재래감귤 11품종과 감귤속 15품종, 그리고 탱자속과 금감속 각각 1품종씩 총 28종에 대한 계통학적 유연관계분석을 위하여 전체 엽록체 trnL-F와 ITS(ITS1-5.8S-ITS2) 영역의 프라이머를 이용하여 PCR를 수행하였다. 그 결과 Fig. 1에서 보는 것처럼 엽록체 trnL-trnF 영역(프라이머 조합을 포함한 영역)은 약 390-400bp(Fig. 1A), ITS 영역(프라이머 조합을 포함한 영역)은 약 600-700bp(Fig. 1B)의 증폭산물을 얻었다.
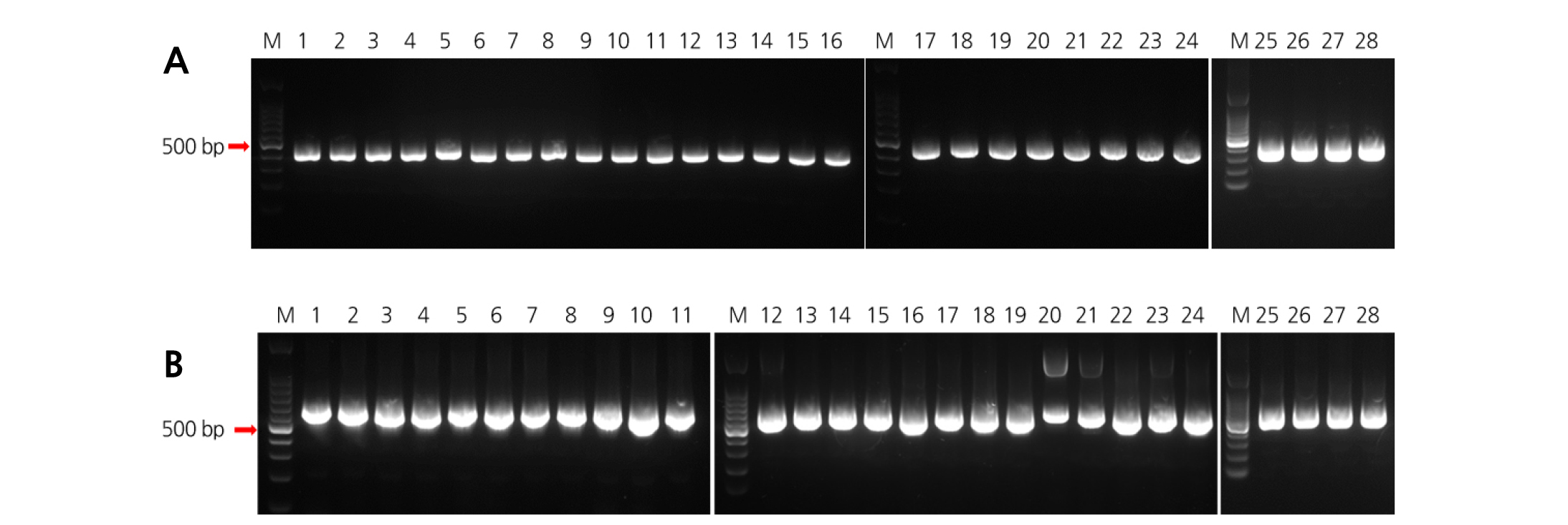
Fig. 1. PCR amplification of 28 Citrus and related species using the chloroplast trnL-F and rDNA ITS (containing 5.8S rDNA region) region: PCR amplification of chloroplast from trnL3’ exon to trnF5’ exon region (trnLF and trnFR primer pairs use) (A); PCR amplification of region from ITS1 to ITS2 (ITS1F1 and ITS2R2 primer pairs use) (B). M; 100 bp Takara marker, lane 1; ‘Jinkyool’ (C. sunki Hort. ex Tanaka), lane 2; ‘Cheongkyool’ (C. nippokoreana Tanaka), lane 3; ‘Hongkyool’ (C. tachibana Tanaka), lane 4; ‘Jikak’ (C. aurantium L.), lane 5; ‘Kamja’ (C. benikoji Hort. ex Tanaka), lane 6; ‘Binkyool’ (C. leiocarpa Hort. ex Tanaka), lane 7; ‘Dangyooja’ (C. grandis Osbeck), lane 8; ‘Byungkyool’ (C. platymamma Hort. ex Tanaka), lane 9; ‘Pyunkyool’ (C. tangerina Hort. ex Tanaka), lane 10; ‘Yuzu’ (C. junos Sieb. ex Tanaka), lane 11; ‘Dongjeongkyool’ (C. erythrosa Hort. et Tanaka), lane 12; ‘Tamnanuenbong’ ([(C. unshiu × C. sinensis) × C. reticulata], lane 13; ‘Cook Eureka’ (C. limon L. Burm.f.), lane 14; ‘Iwasaki wase’ (C. unshiu), lane 15; ‘Ovale kumquat’ (Fortunella margarita (Lour.) Swingle), lane 16; ‘Kiyomi’ (C. reticulata Blanco), lane 17; ‘Shinyegam’ ([(C. unshiu × C. sinensis) × C. reticulata], lane 18; ‘Shiranuhi’ ([(C. unshiu × C. sinensis) × C. reticulata], lane 19; ‘Wilking’ (C. reticulata Blanco RUTACEAE), lane 20; ‘Trifoliate orange’ (Poncirus trifoliata (L.) Raf.), lane 21; ‘Tavares’ (C. aurantifolia x Fortunella margarita ), lane 22; ‘Shatianyou’ (C. grandis (L.) Osbeck), lane 23; ‘Marsh’ (C. paradisi Macfadyen), lane 24; ‘Myagawa wase’ (C. unshiu), lane 25; ‘Haryejosaeng’ (C. unshiu), lane 26; ‘Nova’ (C. reticulata Blanco), lane 27; ‘Hamlin’ (C. sinensis L. Osbeck), lane 28; ‘Washington navel’ (C. sinensis L. Osbeck).
ITS와 trnL-F 영역 증폭산물에 대한 염기서열을 분석한 결과, trnL-F 영역을 포함한 염기서열은 평균적으로 361.1bp(정제한 PCR 산물에 대하여 염기서열을 분석함)였으며, G(구아닌)와 C(시토신)의 함량은 36.43%였다(Table 1). 게다가, 염기의 변이가 없이 보존되는 site는 354개로 나타났으며, 염기의 변이를 보이는 site는 7개 중 계통학적으로 2개의 염기가 유효한 것으로 확인되었다(Table 1). 위 결과는 이전연구자들(Jung et al., 2005; Li et al., 2010)의 연구 결과와 달리 염기 변이가 거이 없었다. 이와 같은 결과는 분석한 염기서열이 짧은 차이점(Huh et al., 2011)과 오랜 기간 동안 동일 모계 품종(Bang et al., 2004) 및 종속간 교잡(Li et al., 2010) 등의 진화과정으로 인하여 유전적으로 비슷해진 것으로 판단된다.
엽록체 trnL-F영역 염기서열의 분석결과를 통하여 얻어진 재래감귤 중 ‘동정귤’, ‘편귤’ 품종의 염기서열은 GenBank에 등록된 동일 품종과 유전적으로 상동성을 보이지 않았으나 ‘홍귤’, ‘지각’과는 100% 일치하는 경향을 보였다(자료 미제시). 식물에서 엽록체 DNA는 모계유전과 관련이 있는데(Daniell et al., 2002; Wang et al., 2008) 대립형질(Allelomorphic character)로 인하여 오랜 기간 진화 과정 중 돌연변이가 발생한 것으로 판단된다(Carbonell-Caballero et al., 2015). 따라서, 이들 품종들과 본 연구소에서 선발한 신품종 감귤류[‘신예감’, ‘하례조생’ 그리고 ‘탐나는봉’(‘부지화’ 주심배실생 품종)] 등 총 28품종들에 대해서도 차후 GenBank에 등록할 예정이다.
또한, ITS 영역의 염기서열 길이는 636-642bp였으며 ‘당유자’가 636bp로 가장 짧았고, ‘탱자’가 642bp로 가장 길었다(Table 1). 평균적인 ITS 전체 영역의 염기서열 길이는 637.68bp였고 G(구아닌)과 C(시토신)의 함량은 66.13%였다(Table 1). 더불어, 염기의 변이가 없이 보존되는 site는 570개로 나타났으며, 염기의 변이를 보이는 site는 68개, 그 중 계통학적으로 25개의 염기가 유효한 것으로 확인되었다(Table 1). 위 결과처럼 재래감귤을 비롯한 본 연구에 사용된 품종들간 ITS 전체 영역의 염기서열 길이는 Sun et al.(2015)의 연구 결과와 같이 비슷하였고 유효 염기 변이 또한 다른 식물들(Lee et al., 2010) 및 감귤 종(Li et al., 2010)에 비하여 변이가 심하게 나타나지 않았다(자료 미제시). 즉, 재래감귤들은 임성이 높은 주변 품종들과의 화분수정에 의하여 많은 종자를 생산할 수 있는 자가합성 품종들(Chae et al., 2012; Song et al., 2011; Yun et al., 2007)로써 고립된 지역 내에서(Jung et al., 2005) 오랜 기간 동안 느린 속도로 진화되어 오는 과정 중 유전적 안정화로 인하여(Penjor et al., 2013) ITS 전체 영역의 유전자가 비슷해진 것으로 판단 할 수 있다.
위 연구결과들을 바탕으로 28S rRNA 유전자 부위를 포함하는 ITS1 전체 영역에 대한 염기서열이 GenBank에 등록되어 있지 않은 ‘편귤’과 ‘홍귤’은 18S rRNA 유전자와 ITS1 부위 유전자를 포함하도록 제작된 ITS1F1 프라이머와 ITS2 및 28S rRNA 유전자 부위를 포함하도록 제작된 ITS2R2 프라이머 조합을 이용하여 ITS1 전체 영역 염기서열을 각각 획득하였고(Fig. 2A and B), GenBank에 등록되지 않은 ‘소유자’의 ITS 전체 영역 또한 확보하였다(Fig. 2C). 확보한 ‘편귤’과 ‘홍귤’의 전체 염기서열은 GenBank에 등록된 ‘편귤’(JQ990181), ‘홍귤’(JQ990178)과 99%의 상동성을 나타내었다(자료 미제시). 위 결과로 현재까지 GenBank에 등록되지 않은 ‘편귤’과 ‘홍귤’의 ITS1 전체 부위에 대한 염기서열을 확보할 수 있었다. 또한, 확보된 ‘소유자’의 염기(Fig. 2C)는 GenBank에 등록된 ‘소유자’(AB456114) 염기서열과 99% 상동성을 나타내었다. 그러나 이 결과는 28S RNA 부위가 아닌 26S RNA 부위 유전자 염기와 상동성을 보인 점에서 현재까지 GenBank에 등록되지 않은 유전자임을 알 수 있었다. 따라서, 이들 품종들을 포함한 총 28종의 전체 ITS 영역에 대한 염기서열은 GenBank에 등록할 예정이다.
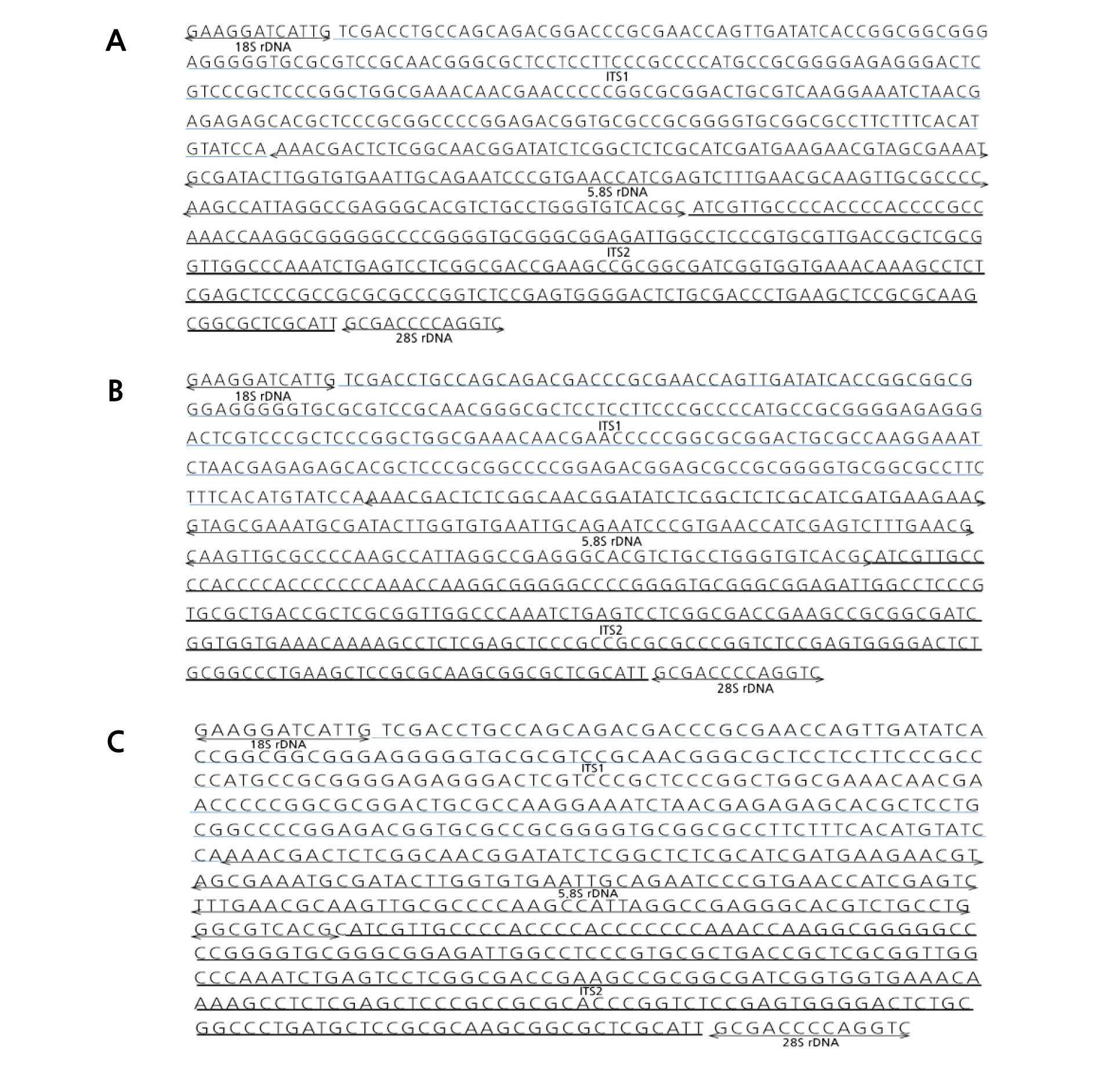
Fig. 2. Sequences of the rDNA ITS region (containing 5.8S rDNA region) isolated from Citrus and related species. ‘Pyunkyool’ (A); ‘Hongkyool’ (B); ‘Yuzu’ (C). ITS1 and ITS2 spacer region was underlined and ITS2 region was represented by the bold underline. 18S, 5.8 and 28S rDNA regions were expressed by double arrow.
엽록체 trnL-F 영역의 유전적 유연관계분석
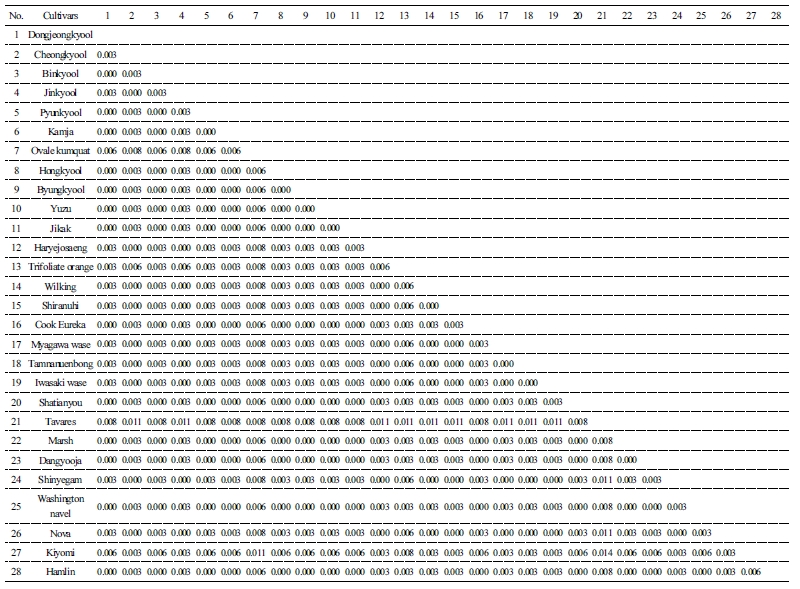
감귤류의 엽록체 trnL-F 영역에 대한 염기서열 분기값(Sequence divergency)은 0-0.011까지로 다양하게 나타났으며, 재래감귤 품종들간에는 0-0.003로 다른 감귤류와 비교하여 염기서열 다양성 정도가 낮았다. 즉, 이들 품종들간에 염기 다양성 정도가 낮다는 것은 유전적으로 근연관계에 있다는 것이며 동시에 동일 모계로부터 유전된 것으로 판단된다(Table 2). 식물의 모계 기원을 판별하는 데 있어서 엽록체 trnL-F, rcbL, 그리고 matK 유전자 영역을 이용한 분석 방법들이 사용되고 있는데(Kim et al., 2008; Oh, 2015), 이 중 trnL-F 유전자 영역은 감귤류의 기원 및 유연관계 분석에 주로 이용되었다(Huh et al., 2011; Jung et al., 2005; Li et al., 2010). 감귤 품종들간 분기값이 가장 높게 확인된 품종은 0.008-0.014로 가장 높게 나타난 라임 품종이었으며, ‘탱자’, ‘장실금감’순으로 각각 0.003-0.011, 0.006-0.011로 높게 나타났다(Table 2). 즉, 재래감귤류는 이들 품종들과 염기 구성이 거의 상이하다는 것을 보여주며 근연관계가 멀다는 것을 알 수 있었다.
엽록체 trnL-F 영역 염기서열을 이용하여 감귤 품종간 유연관계를 ML기법으로 조사한 결과 감귤속(Group I), 탱자속(Group II) 그리고 금감속(Group III) 3개의 분류군으로 나눌 수 있으며 감귤속(Group I)은 다시 3개(Clade I, Clade II 그리고 Clade III)의 분계조로 나누어지며, ‘당유자’, ‘워싱톤 네블오렌지’, 자몽, 문단, 레몬, ‘지각’, ‘소유자’ 품종으로 구성되어 있는 Gp1, ‘동정귤’, ‘빈귤’, ‘편귤’, ‘감자’, ‘홍귤’, ‘병귤’로 구성된 Gp2로 구성되어 있는 Clade I 분계조와 ‘노바’, ‘청견’으로 구성된 Gp3, ‘청귤’, ‘진귤’, ‘하례조생’, ‘부지화’, ‘궁천조생’, ‘탐나는봉’, ‘암기조생’, ‘신예감’으로 구성된 Gp4로 구성된 Clade II 분계조 그리고 독립된 단일 품종인 ‘햄린’(Gp5) 개체로 구성된 Clade III 분계조로 구성되어 있다(Fig. 3A). 위 결과에서 ‘햄린’은 문단류에 기원된 것으로 알려진 이전 연구(Barkley et al., 2006; Li et al., 2010)와는 달리 감귤 속에는 속하지만 독립된 개체로써 존재하였다. USDA(www.citrusvariety.ucr.Edu/citrus/Hamlin.hyml) 품종 자료에 따르면 ‘햄린’ 대한 정확한 기원은 알려져 있지 않은 상태인데 본 연구 결과를 통하여 ‘햄린’은 문단과 만다린 품종보다도 이전에 분류된 것으로 알 수 있다. Fig. 3A에서 보는 것처럼 모든 재래감귤 품종들은 감귤속인 Group I에 속하며, Clade I과 Clade II 분계조로 크게 나눌 수 있으며 대다수 재래감귤 품종들은 문단과 만다린 품종의 교잡종인 것으로 추측할 수 있었다. 이전 연구자들(Jung et al., 2005; Nicolosi et al., 2000)의 연구결과에 따르면 ‘홍귤’과 ‘편귤’은 만다린 품종에서 기원되었고, ‘당유자’와 ‘지각’은 문단으로부터 기원한 것이라고 하였는데, 본 연구에서도 이와 비슷한 결과를 얻었다. 하지만 이전 연구자(Jung et al., 2005)의 결과와는 달리 이 연구에서의 ‘병귤’, ‘동정귤’, 그리고 ‘소유자’은 독립적인 개체로 분류된 것이 아니라 대다수 재래감귤 품종처럼 문단과 만다린 품종과의 자연교잡을 통하여 얻어진 개체라는 것을 판단할 수 있었다.
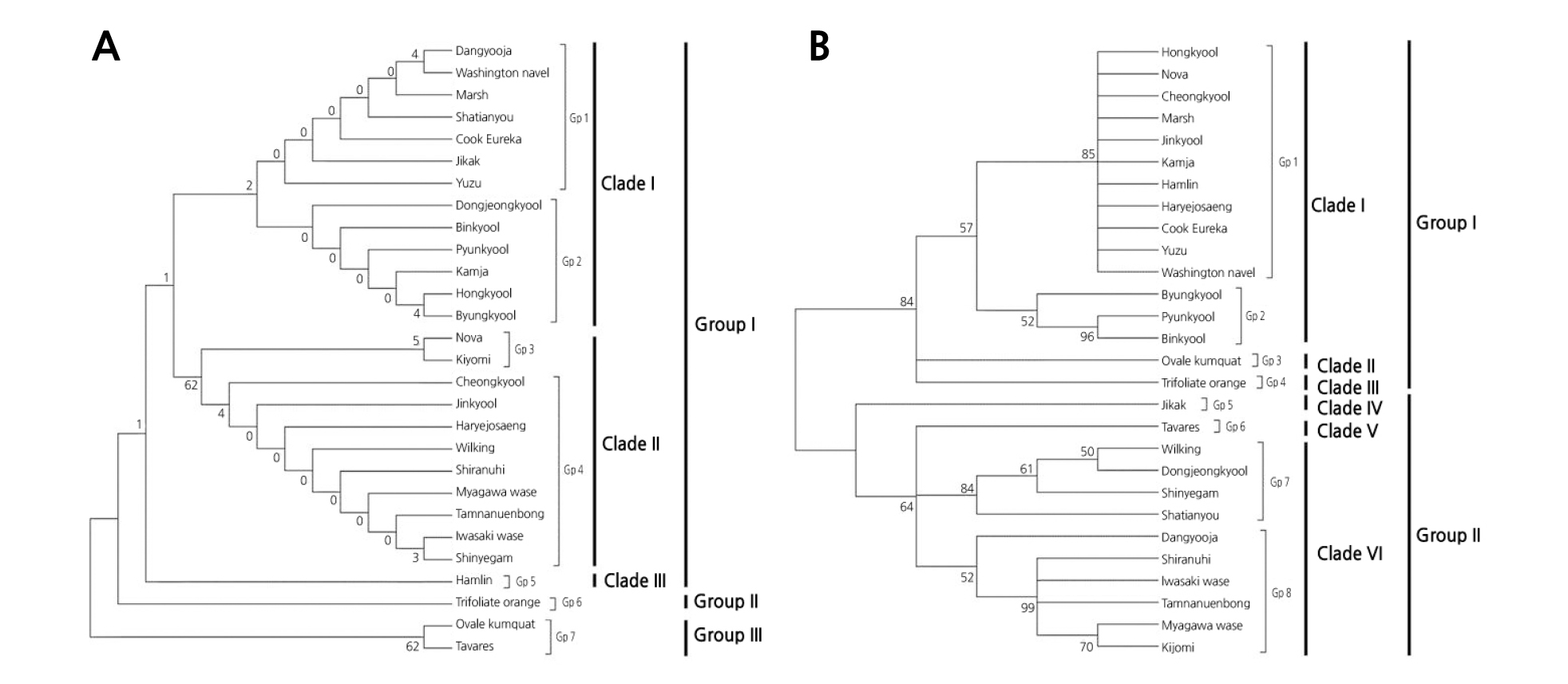
Fig. 3. Phylogenic tree of a total of 28 genotypes, including 11 cultivars native to Jeju, and 17 Citrus genotypes containing Poncirus and Fortunella by Maximum Likelihood (ML): Phylogenic tree constructed using sequences of the chloroplast trnL-F region (A); Phylogenic tree constructed using sequences of the rDNA internal transcribed spacer region (containing the 5.8S rDNA region) (B).
ITS 영역의 유전적 유연관계분석
감귤류의 전체 ITS 영역에 대한 염기서열 분기값은 0-0.039, 재래감귤은 0-0.032까지 다양하게 나타났다(Table 3). 대부분의 감귤 품종들은 ‘탱자’ 품종과의 분기값이 0.014-0.039로 전반적으로 가장 높았고 라임 품종과는 0.019-0.036으로 두 번째로 높게 나타났다(Table 3). 즉, 재래감귤은 이들 품종들과 염기 구성이 거의 상이하며 유전적으로 멀다는 것을 알 수 있었다. 특히, 재래감귤 품종 중 ‘홍귤’과 ‘청귤’간 분기값은 0으로 다른 재래감귤 품종들과 비교하여 염기서열 다양성 정도가 가장 낮았다(Table 3). 즉, 이들 품종들 간에는 염기 구성이 거의 동일한 것으로 나타났다. 게다가, 이 두 품종들은 자몽 품종과도 유전적으로 가장 근접한 유연관계를 얻었다(Table 3). 반면에, ‘당유자’은 ‘탱자’과의 분기값이 0.039로 다른 감귤류와 비교하여 유전적으로 가장 상이하게 나타났다(Table 3). 위 결과로 보았을 때 ‘탱자’은 형태학적으로나 분류학적으로 감귤속과는 다르기 때문에 감귤 품종 간 염기서열이 상이한 것으로 판단된다(Huh et al., 2011).
Table 3. Sequence divergences in the rDNA ITS region (containing the 5.8S rDNA region) of 28 Citrus and related species |
또한, ITS 영역에 대한 염기들을 이용하여 품종간의 유연관계를 ML기법으로 계통수를 조사하였다. 그 결과 Group I과 Group II의 2개 분류군으로 나눌 수 있었으며, 다시 6개의 분계조와 8개의 하위그룹으로 나눌 수 있었다(Fig. 3B). Group I은 ‘홍귤’, ‘노바’, ‘청귤’, 자몽, ‘진귤’, ‘감자’, ‘햄린’, ‘하례조생’, 레몬, ‘소유자’, ‘워싱톤 네블 오렌지’ 품종으로 구성되어 있는 Gp1, ‘병귤’, ‘편귤’, ‘빈귤’의 Gp2 하위그룹으로 구성된 분계조 Clade I와 독립된 개체로 구성된 분계조 Clade II, Clade III 내 각각 ‘장수금감’(Gp3)과 ‘탱자’(Gp4)으로 구성되어 있다(Fig. 3B). 또한, Group II는 독립된 개체로 구성된 Clade IV 내 ‘지각’(Gp5), Clade V에 속하는 라임(Gp6), 그리고 Gp7(‘윌킹’, ‘동정귤’, ‘신예감’)과 Gp8(‘당유자’, ‘부지화’, ‘암기조생’, ‘탐나는봉’, ‘궁천조생’, ‘청견’) 하위그룹 품종들이 포함되도록 구성된 Clade VI 분계조로 되어 있다(Fig. 3B).
Group I 내 Clade I에 속하는 재래감귤 품종들로는 ‘홍귤’, ‘청귤’, ‘진귤’, ‘소유자’을 포함하는 Gp1과 ‘병귤’, ‘편귤’, ‘빈귤’을 포함하는 Gp2 하위그룹으로 구성되어 있으며, 이들 재래감귤 품종들은 이전 연구자(Jung et al., 2005; Nicolosi et al., 2000)의 결과와 같이 문단과 만다린 품종의 잡종에 의하여 얻어진 품종이라고 추정할 수 있다. 특히, Gp2의 하위그룹에 속하는 ‘병귤’, ‘편귤’, ‘빈귤’은 독립적인 개체로 분리되었으며, ‘편귤’, ‘빈귤’은 동일 자매에 속하며 ‘병귤’과도 유전적으로 가장 근연관계에 있음을 알 수 있다(Fig. 3B). 게다가, ‘병귤’은 ‘빈귤’과 ‘편귤’ 품종 이전에 분류되었는데 이 결과는 ITS 영역을 이용하여 재래감귤 근연관계를 분석한 연구자들(Jin et al., 2016; Sun et al., 2015)의 결과와 비슷하였다. 또한, Group II에 속하는 재래감귤 품종들로는 독립적인 개체로써 Clade IV에 속하는 ‘지각’(Gp5)과 ‘윌킹’과 유전적으로 가장 근연관계에 있는 ‘동정귤’(Gp7), 그리고 Gp8에 속하며 문단 품종에서 유래된 것으로 추정되는 ‘당유자’(Jung et al., 2005; Nicolosi et al., 2000)들로 구성된 Clade VI 분계조가 있다. 이 중 ‘지각’은 독립적인 개체로써 다른 재래감귤 품종들에 비하여 오래 전에 분류된 것으로 확인되었으며(Fig. 3B), Citron의 변종 품종(C. medica var. sarcodatylis) 및 재래감귤인 ‘당유자’과 가장 유전적으로 근연관계에 있는 개체(Sun et al., 2015)로써 계통분류상 시트론, 문단, 만다린 품종으로 분류되는 연구결과(Caballero-Caballero et al., 2015)처럼 시트론과 문단 품종의 잡종 감귤로부터 기원한 것으로 추정할 수 있다. 따라서, Group II내 Clade IV에 속하는 재래감귤 ‘당유자’, ‘동정귤’은 시트론과 문단 품종의 잡종 감귤로부터 기원된 품종들과 만다린 품종간에 교잡을 통하여 얻어진 감귤들이라 추정할 수 있었다.
본 연구 결과들을 바탕으로 종속간 계통학적 유연관계 분석에 유용하게 이용되고 있는 엽록체 trnL-trnF와 ITS 영역(Cronn and Wendel, 2003)을 통하여 재래감귤들에 대한 유전적 근연관계를 비교 분석한 결과, 대부분의 품종들은 문단과 만다린 품종의 교잡종으로부터 얻어진 것임을 확인할 수 있었다. 특히, 그 중에서 ‘병귤’은 엽록체 DNA(cpDNA) trnL-F 영역의 염기서열을 이용하여 분석한 Jung et al.(2005)의 결과처럼 독립된 개체로 분류되지 않았으며, 단지 만다린 품종인 ‘홍귤’과 자매 품종에 속하며 문단과 만다린 품종의 교잡에 의한 품종임을 알 수 있었다(Fig. 3A-Gp2).
반면에, ITS 영역을 이용한 결과는 Sun et al.(2015)의 결과처럼 독립된 재래감귤 품종들로 구성되어 있음을 볼 수 있었지만 품종간 근연관계 분석 결과는 상이하게 나타났다(Fig. 3B-Gp2). 이전 연구자(Jin et al., 2016; Sun et al., 2015)의 결과에 따르면 ‘병귤’은 ‘청귤’과 가장 근연관계가 가까운 품종이라고 하였으나 본 연구에서는 ‘빈귤’ 또는 ‘편귤’과 가까운 결과를 얻었으며, ‘청귤’은 ‘병귤’과는 다른 Gp1 하위그룹에 속하며 유전적으로 근연관계가 멀다는 것이 확인되었다. 위 두 결과로 ‘병귤’은 문단(‘당유자’ 등)과 만다린(‘홍귤’ 등) 품종들과의 오랜 시간 동안 수분 수정 등(Dhillon et al., 1993)을 통한 종자번식으로 고립된 지역 내에서 선사시대부터 재배되어 왔기 때문에(Chae et al., 2012; Song et al., 2011; Yun et al., 2007) 이전 연구자들의 연구 결과와 유전적인 차이를 보인 것이라 판단되었다(Jin et al., 2016).
또한, 감귤연구소 내 재래감귤 품종들 간 엽록체 trnL-F와 ITS 영역의 염기서열을 이용하여 분석한 결과(자료 미제시) 염기의 변이가 없이 보존되는 site는 각각 360, 606개, 염기의 변이를 보이는 site는 각각 1개와 32개로 나타났으며 그 중 계통학적으로 유효한 염기수는 각각 1개와 15개로 확인되었다. 반면, 이전연구자들(Jung et al., 2005; Sun et al., 2015)의 연구결과를 기초로 하여 GenBank에 등록된 재래감귤의 trnL-F 와 GenBank에 등록된 유자(AB456114)의 ITS 영역 염기서열들을 가지고 동일한 조건하에서 조사한 결과(자료 미제시), 염기의 변이가 없이 보존되는 site는 각각 350개와 545개였고 변이를 보이는 site는 각각 22개와 84개였으며, 그 중 계통학적으로 유효한 염기수는 각각 7개와 14개로 나타나 본 연구결과와 상이한 염기 변이 차를 확인할 수 있었다. 이와 같은 결과는 동일 재배지역 내에서 수집한 시료가 아닐 뿐만 아니라 주변 품종들과의 교잡을 통한 유전자 삽입 및 결실에 의한 유전적 차이에 따른 것으로 추정되었다(Huh et al., 2011; Jin et al., 2016; Moon et al., 2010; Moon et al., 2015; Sun et al., 2015).
현재까지 재래감귤에 대한 연구는 미흡한 상태이며 비록 Jung et al.(2005)이 chloroplast DNA(cpDNA) 염기의 trnL-F를 이용하여 재래감귤에 대한 근연관계를 비교분석하였지만, 오랜 기간 동안 수분 수정을 통하여 종자번식된 재래감귤 품종들의 근연관계를 분석함에 있어 오류가 발생할 수 있으며(Hirai et al., 1986; Jung et al., 2005), 양친으로부터 유전되는 특성을 갖고 있는 ITS 영역의 염기서열을 이용하여 재래감귤의 유연관계를 분석한 결과(Sun et al., 2015) 역시 모든 품종의 염기서열 정보가 없는 관계로 본 연구소 내 재배 보존되고 있는 재래감귤 품종들과 제주도 내 재래감귤 품종들 간 ITS 영역의 연구결과를 비교 분석하는 것은 쉽지 않다. 따라서, 이 연구 결과는 제주도 내 재래감귤 품종들의 계통학적 유연관계 분석함에 있어서 중요한 기초자료가 될 것이다.