서 언
재료 및 방법
광처리 시간에 따른 A. brassicicola 7균주의 포자 형성량 조사
식물 재배
접종원 준비
접종 및 병조사
결과 및 고찰
A. brassicicola 7균주의 광처리 시간에 따른 포자 생산량 및 병원성
시판 무 61품종의 저항성
무 유묘의 생장 정도에 따른 검은무늬병 발생
접종원 농도에 따른 검은무늬병 발생
재배 온도에 따른 검은무늬병 발생
서 언
Alternaria에 의한 식물병은 전세계적으로 다양한 기주에서 발생하고 있으며, Alternaria병에 의한 경제적인 손실은 어떤 식 물병원균에 의한 것보다 높은 비율을 차지하고 있다(Agrios, 2005). 또한, 각종 작물의 잎, 줄기뿐만 아니라 농산물을 감염하거 나 종자를 오염시켜 피해를 주고 있으므로 농업환경 내에서 발생 분포가 매우 넓다고 하겠다(Lee and Yu, 1995). 세계적으로 배추과 작물(Brassicaceae)에 병을 일으키는 Alternaria로는 A. brassicae, A. brassicicola, A. japonica 그리고 A. alternata가 보 고되었다(Nowicki et al., 2012). 이 중 무(Raphanus sativus L.)에 발생하는 검은무늬병은 A. brassicicola, A. brassicae 그리고 A. japonica (= A. raphani)에 의해 발생한다(Yu et al., 1991; KSPP, 2009).
무에 Alternaria 검은무늬병균이 감염되면 초기 잎에 진한 갈색-검정색의 점무늬를 나타내다가 점차 둥근형 또는 타원형으 로 병반이 확대되면서 연한 갈색–회갈색의 윤문을 형성하고 병반 가장자리에 검은색의 둥근 테두리가 형성되거나 주위에 황 색–녹황색의 무리가 생기기도 한다. 결국 심하게 병든 잎은 여러 개의 병반이 합쳐지며 병반 주위가 회갈색–회황색으로 변 하고 잎이 말라 죽게 된다(Yu et al., 1991).
배추과 작물의 검은무늬병은 기주 범위와 포자의 비산 범위가 넓어 방제가 어려운 균이다(King, 1994). 이 병을 방제하는 가 장 일반적인 방법으로 합성 살균제가 사용되고 있지만(Mora and Earle, 2001; Iacomi-Vasilescu et al., 2004), 인체와 동물 그 리고 환경에 대한 독성 화학 농약 사용에 대한 우려가 증가하고 있다(Muto et al., 2005). 그러므로 이 병을 방제하기 위한 가장 친환경적이고 경제적인 방법은 저항성 품종의 재배일 것이다I(acomi-Vasilescu et al., 2004).
King(1994)에 의해 A. brassicicola에 저항성인 Brassica napus와 B. oleracea의 유전자형이 보고되었다. 그리고 배추과 작물 인 Camelina sativa와 Capsella bursapastoris가 Alternaria 병원균에 대하여 높은 저항성을 나타내는 것으로 알려졌다(Conn et al., 1988; King, 1994). 그러나 Tewari and Mithen(1999)는 거의 모든 상업적인 Brassica들은 A. brassicicola와 A. brassicae에 감수성이고, B. rapa와 B. juncea는 A. brassicae균주에 대해 B. napus와 B. carinata보다 더 감수성이라고 보고하였다. 이와 같 이 검은무늬병에 대한 저항성이 보고된 배추과 작물이 있음에도 불구하고 상업적으로 저항성을 나타내는 품종이 판매되지 못 하고 있는 실정이다(Iacomi-Vasilescu et al., 2004; Muto et al., 2005).
따라서 검은무늬병에 대한 저항성 품종을 개발하기 위해서는 신규 저항성 유전자원 발굴, 저항성 유전자의 규명, 저항성 유 전 양식 및 저항성 품종 육성을 위한 분자 표지 개발 등에 대한 연구가 시급하다(Bae et al., 2015; Kim et al., 2016). 이들 연구 를 위해서는 효율적이고 신뢰할 수 있는 무 검은무늬병 저항성 검정 방법의 확립이 필요하다. B. napus, B. juncea 또는 B. rapa에 서는 식물 생장단계, 습도 기간, 접종 농도, 접종 방법, 재배 온도 등의 주요 요인과 A. brassicicola와 A. brassicae에 의한 검은 무늬병 발생에 관한 연구가 수행되었다(Mridha and Wheeler, 1993; King, 1994; Hong and Fitt, 1995; Hong et al., 1996; Doullah et al., 2006). 하지만, 우리나라의 5대 채소 중 하나인 무에 큰 피해를 주고 있는 무 검은무늬병에 대해서는 거의 연구 가 이루어지지 못하였다.
본 연구에서는 효율적인 무 검은무늬병 저항성 검정법을 확립하고자, 광 조사기간에 따른 A. brassicicola 균주들의 포자 형 성량과 병원성을 조사하여 저항성 검정에 사용할 균주를 선발하고, 이 검은무늬병균에 대한 시판 중인 무 61개 품종의 저항성 정도를 조사하고, 저항성 정도가 다른 4개의 무 품종을 선발하여 생육 정도, 접종원 농도 및 재배 온도 등의 발병 조건에 따른 이 들 품종의 A. brassicicola에 의한 검은무늬병 발생을 조사하였다.
재료 및 방법
광처리 시간에 따른 A. brassicicola 7균주의 포자 형성량 조사
농촌진흥청 농업유전자원센터(KACC)로부터 무 검은무늬병균 A. brassicicola 7균주(KACC 40034, 40036, 40857, 43923,44415, 44877, 44878)를 분양받아 실험에 사용하였다.
A. brassicicola 7개 균주들의 광처리 기간에 따른 포자 형성량을 조사하고자 각각의 균주를 potato dextrose agar(PDA; Becton, Dickinson and Co.) 배지에 접종하고 25°C에서 7일간 전배양하여 형성된 균총으로부터 균사조각을 떼어내 직경 8.5cm Petri dish의 V-8 juice agar[V8 agar; V-8 Juice (V8 Campbell Soup Co.) 200mL, CaCO₃3g (Samchun Chem. Co., Ltd.), Agar (Junsei Chemical Co., Ltd.) 18g, distilled water 800mL] 배지 중앙에 1조각씩 올려놓고 알루미늄 호일로 싸서 암 상태가 되도록 한 후에 25°C에서 7일 동안 배양 하였다. 배양한 검은무늬병균 plate의 뚜껑을 열고 25°C 항온항습실(상대습도 80%)에서 하루에 12시간씩 광(55μmol·m-2·s-1)을 처리하면서 1일 또는 2일간 배양한 후에 배지에 멸균수 20mL를 넣고 멸균 한 붓으로 긁어 포자를 수확하였다. 그리고 4겹의 거즈로 걸러서 균사체를 제거하고 광학현미경 하에서 hemocytometer를 이 용하여 mL 당 포자의 수를 조사하고 이를 각 배지p late에 형성된 포자의 수로 환산하였다. 실험은 처리 당3 개의 plate를 사용 하였으며, 각 실험은 2회 반복하여 실시하였다.
식물 재배
시판중인 무 품종 61개(‘금봉’, ‘백춘’, ‘가을김장’, ‘새롬’, ‘전무후무’, ‘하우스청옥’, ‘백동’, ‘명산’, ‘장생’, ‘보석알타리’, ‘태창’, ‘청 풍명월’, ‘한농알타리’, ‘강성’, ‘알파인’, ‘극동’, ‘빛고은열무’, ‘명가가을1호’, ‘제일슈퍼시래기’, ‘아우리월동’, ‘슈퍼길조’, ‘우정알 타리’, ‘평강김장’, ‘백옥’, ‘초롱’, ‘YR챔피온열무’, ‘비바리월동’, ‘태광’, ‘백자’, ‘산나리열무’, ‘백세1호’, ‘청운플러스’, ‘참조아열무’, ‘슈퍼모델’, ‘제일건강시래기1호’, ‘송백’, ‘제일보라’, ‘미농조생’, ‘선봉알타리’, ‘초비’, ‘길조’, ‘시래기’, ‘만사형통’, ‘동하’, ‘박자’, ‘ 대박’, ‘청일품’, ‘아시아가을저장’, ‘관동여름’, ‘토광’, ‘여름춘향이열무’, ‘대들보’, ‘청두’, ‘청수궁중’, ‘태청’, ‘청운’, ‘대동’, ‘탐스런’, ‘강추’, ‘장형봄’, ‘대평여름’)의 종자를 시중에서 구입하여 실험에 사용하였다.
A. brassicicola 7개 균주들의 무에 대한 병원성 실험은 ‘한농알타리’(동부팜한농)와 ‘미농조생’(아시아종묘)을 그리고 발병 조건에 따른 무 품종 등의 검은무늬병 발생 실험은 ‘금봉’(권농종묘), ‘새롬’(신젠타), ‘토광’(동부팜한농), ‘대평여름’(신젠타) 네 품종을 사용하였다.
무의 생육 정도에 따른 검은무늬병 발생 실험을 제외한 모든 실험에서는 무 종자를 5 × 8 육묘용 연결 포트(70mL/pot, 범농 사)에 원예용상토 5호(부농사)를 넣고 포트 당 2립씩 파종하고 온실(25 ± 5°C)에서 재배하였다. 종자가 발아한 후 생장이 고 른 개체로 포트 당 1주씩 남기고 솎아 주었다. 파종 후 13-16일 동안 재배한 유묘를 실험에 사용하였다. 그리고 무의 생장 정도 에 따른 검은무늬병 발생 실험은 앞에서와 동일한 방법으로 파종하고 온실(25 ± 5°C)에서 10, 13, 16, 19일 동안 재배한 유묘 를 실험에 사용하였다.
접종원 준비
A. brassicicola 7개 균주들의 무에 대한 병원성 실험을 위해서는 ‘A. brassicicola 7균주의 광처리 시간에 따른 포자 형성량 조사’ 실험에서 수확한 포자를 사용하여 포자 농도가 5.0 × 105spores·mL-1인 포자현탁액을 준비하였다. 그리고 A. brassicicola KACC 40036을 다양한 포자 농도로 접종하여 병원성을 조사하는 실험을 위해서는 포자현탁액의 포자 농도가 각각 3.7 × 103, 1.1 × 104, 3.3 × 104, 1.0 × 105, 3.0 × 105spores·mL-1이 되도록 조정하였다.
A. brassicicola 균주들의 병원성 실험을 제외한 나머지 실험은 A. brassicicola KACC 40036 균주를 PDA 배지에 접종하고 25°C에서 7일간 배양한 균총으로부터 균사조각을 떼어내어 직경 8.5cm Petri dish의 V-8 juice agar 배지에 3조각씩 올려놓 고 25°C에서 7일 동안 배양하였다. 그리고 이 Petri dish의 뚜껑을 열고 25°C 항온항습실(상대습도 80%)에서 하루에 12시간 씩 광(55μmol·m-2·s-1)을 조사하면서 1일간 배양한 후에 ‘광처리 시간에 따른 A. brassicicola 7균주의 포자 형성량 조사’ 실험 과 동일한 방법으로 포자를 수확하고 포자 농도를 측정하였다
A. brassicicola 균주들의 병원성 실험과 접종원 농도에 따른 4개 품종들의 저항성 정도 실험을 제외한 모든 실험은 포자현탁 액의 포자 농도를 2.0 × 105spores·mL-1로 조정하여 사용하였고, 접종원 농도에 따른 검은무늬병 발생 실험을 위해서는 포자 현탁액의 포자 농도가 각각 2.5 × 104, 5.0 × 104, 1.0 × 105, 2.0 × 105 spores·mL-1 가 되도록 준비하였다
접종 및 병조사
A. brassicicola 7개 균주의 병원성과 재배 온도에 따른 무 검은무늬병 발생 실험을 제외한 모든 실험은 A. brassicicola KACC 40036의 포자현탁액을 무 유묘가 충분히 젖도록 분무 접종한 후에 25°C 습실상에서 암상태로 24시간 동안 배양하였다. 습실 처리한 유묘는 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광(55 μmol·m-2·s-1)을 처리하며 재배하여 병 발생을 유도하였고, 접종 2일 후에 잎에 발생한 검은무늬병의 병반면적율(%)을 달관조사 하였다.
A. brassicicola 7개 균주의 병원성 실험은 앞에서 같이 동일한 방법으로 접종하고 25°C 습실상에서 48시간 배양한 후에 항 온항습실(25°C, 상대습도 80%)에서 1일 동안 재배한 후에 병조사 하였다. 그리고 재배온도에 따른 무 검은무늬병 발생 실험은 A. brassicicola KACC 40036을 앞에서와 같은 방법으로 접종하고 각각 20, 25, 30°C 습실상에 넣고 48시간 동안 배양한 후에 검은무늬병 발생 정도를 조사하였다.
시판 중인 무 61개 품종의 A. brassicicola에 대한 저항성 정도 실험은 10반복씩 2회 수행하였으며, 나머지 모든 무 검은무늬 병 발생 실험은 5반복으로 2회 수행하였다. 그리고 SAS(SAS 9.1, SAS Institute Inc., USA) 프로그램을 이용하여 ANOVA 분 석을 하였으며, 처리 평균간 비교를 위하여D uncan’s multiple range test(p = 0.05)를 실시하였다.
결과 및 고찰
A. brassicicola 7균주의 광처리 시간에 따른 포자 생산량 및 병원성
광(55 μmol·m-2·s-1)을 조사한 기간에 따른 A. brassicicola 7개 균주(KACC 40034, 40036, 40857, 43923, 44415, 44877, 44878)의 포자 형성량을 실험한 결과, 7균주 모두 암상태에서 7일 동안 배양하였을 때에는 hemocytometer로 포자 형성량을 조사하기 어려울 정도로 적은 양의 포자가 형성되었으나(결과 미제시), 광을 처리하였을 때에는 실험한 균주 모두 포자 형성량 이 크게 증가하여 6.0 × 106개부터 1.4 × 108개의 많은 포자가 형성되었다(Table 1). 하지만 광을 하루에 12시간씩 1일 또는 2 일 처리에 의한 포자 형성량은 통계적으로 유의성 있는 차이를 보이지 않았다. 따라서 A. brassicicola 의 포자 형성을 위한 광 (55μmol·m-2·s-1) 조사는 1일이면 충분하다고 생각되었다
실험한 균주 중 KACC 40036와 KACC 43923은 가장 많은 포자를 형성하였는데 1일 광처리후에 각각 plate 당 1.1 × 108, 1.4 × 108개의 포자를 형성하였다(Table 1). 그리고 KACC 44878은 포자 형성이 가장 적었으며 1일 광처리에 의해 plate 당 6.0 × 106개를 생산할 뿐이었다
A. brassicicola 7개 균주들의 무에 대한 병원성 검정을 검정하고자 2개 무 품종(한농알타리, 미농조생)에 병원균을 분무 접 종하고 검은무늬병 발생을 실험한 결과, 실험한 균주 모두는 무 유묘에 분무접종하고 3일 후에 유묘 전체가 고사하였다(Table 1, Fig. 1). 따라서 7균주의 병원성 실험에서 접종한 유묘가 모두 고사한 것은 다른 실험들이 24시간 습실처리한 것과 달리 48시 간 동안 습실처리하여 검은무늬병이 심하게 발생한 것으로 생각되었다. 그리고 KACC 40036 균주의 포자현탁액을 5가지 농 도로 하여 두 품종의 무 유묘에 접종하고 24시간 습실처리하고 2일 후에 발병 정도를 조사한 결과, 두 품종 모두 접종한 포자 농 도 의존적으로 검은무늬병이 발생하였다(Fig. 2). 비병원성 균주는 습실처리 시간을 길게 하여도 병이 발생하지 않으므로, 실험 한 A. brassicicola 균주는 모두 무에 대하여 강한 병원성이 있다는 것을 알 수 있었
Table 1. Spore production of Alternaria brassicicola isolates by light treatment and pathogenicity of the fungus on two radish cultivars 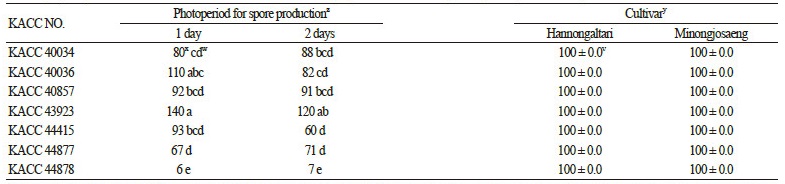 |
zEach isolate inoculated on aV -8 juice agar plate was incubated in darkness at 25°C for 7 dasy, and then the plates were cultured under a fluorescent lamp (55 μmol·m-2·s-1, 12 h/day) in a growth chamber (25°C, RH 80%).
ySeedlings at the three-leaf stage were inoculated by spraying a spore suspension of the fungus at a concentration of 5.0 × 105 spores·mL-1. The infected plants were incubated in a humidity chamber at 25°C for 48 hr and then transferred to a growth chamber at 25°C and 80% RH with a 12-h light/dark cycle. The percent diseased leaf area was scored 3 days after inoculation.
xEach value represents the mean number (× 106) of spores per plate of two runs with three replicates each.
wValues labeled with the same letter are not significantly different based on Duncan’s multiple range test atp = 0.05.
vEach value represents the mean disease severity ± standard devaition of two runs with five replicates each.
Fig. 1
Disease development on seedlings of radish cultivars ‘Hannongaltari’ (left) and ‘Minongjosaeng’ (right) caused by Alternaria brassicicola KACC 40036. (A) Two-week-old radish plants prior to inoculation; (B) Photograph of plants taken 3 days after inoculation.
Fig. 2
Effects of spore concentration on the occurrence of black spot on seedlings of radish cultivars ‘Hannongaltari’ and ‘Minongjosaeng’. Thirteen-day-old seedlings were inoculated with various concentration of spore suspension by the spray method: (A) 3.0 × 105; (B) 1.0 × 105; (C) 3.3 × 104; (D) 1.1 × 104; (E) 3.7 × 103 spores·mL-1 of Alternaria brassicicola KACC 40036; (F) control. The inoculated plants were incubated in a humidity chamber at 25°C for 24 h and then transferred to a growth chamber at 25°C and 80% RH with a 12-h light/dark cycle P. hotograph were taken two days after inoculation
많은 연구자들은 A. brassicicola의 포자 형성을 위해 암상태에서(Otani et al., 1998; Iacomi-Vasilescu et al., 2004; Doullah et al., 2006) 혹은 연속적인 광처리에서(Pedras et al., 2009) 혹은 하루에 12시간 광처리(Babadoost and Gabrielson, 1979; Muto et al., 2005; Köhl et al., 2010)를 하는 등 다양한 방법으로 A. brassicicola를 배양하였다. 하지만 대량시료의 무 검은무늬병 저 항성 검정을 위해서는 효율적으로 A. brassicicola의 포자를 생산하는 것이 중요하다. 이를 위해서는 기존의 포자 형성 방법들 을 비교하여 가장 효율적으로 A. brassicicola의 포자를 대량생산할 수 있는 방법을 선발하는 것이 필요하다. 기존 연구자들의 포자 형성 방법을 실험을 통해 비교한 결과, A. brassicicola를 암상태에서만 배양하였을 때에는 거의 포자가 형성되지 않았고, 대량의 포자를 생산하기 위해 병원균을 접종한 많은 plate를 펼쳐서 연속적으로 광상태에서 배양하는 것은 공간적으로 많은 제 약이 따랐다. 이와 달리 plate를 쌓아서 공간을 적게 사용하면서 암상태에서 7일 동안 배양한 후에 이들을 펼쳐서 하루에 12시 간씩 1일 혹은 2일 광을 처리하였을 때에는 용이하게 많은 양의 포자가 형성되었다
따라서 무 검은무늬병 저항성 검정을 위한 A. brassicicola의 포자 형성을 효과적으로 유도하는 방법으로 V-8 juice agar 배 지에 접종하고 7일 동안 배양한 후에 하루에 12시간씩 1일 동안 광(55 μmol·m-2·s-1)을 처리를 하는 방법을 확립하였다. 한편, A. brassicicola의 race 분화는 아직 보고된 바 없으므로 실험한 균주 중 A. brassicicola KACC 40036가 포자의 형태가 균일하 고 다른 균주보다 많은 포자를 형성하였으므로, 이 균주를 무 검은무늬병 저항성 검정법을 확립을 위해 선발하였다. 그리고 향 후 보다 정확한 무 검은무늬병 저항성 검정을 위해 다양한 저항성 유전자원을 확보한 후에 A. brassicicola의 race 분화에 관한 연구를 수행할 예정이다.
시판 무 61품종의 저항성
시판 중인 61개 무 품종의 A. brassicicola KACC 40036에 대한 저항성 정도를 조사하기 위하여 실험한 결과, 실험한 품종 중 높은 저항성을 나타내는 품종은 없었다. 하지만 ‘대평여름’ 등이 95% 이상의 병반면적율을 보이는 반면에 ‘금봉’, ‘백춘’, ‘새 롬’ 등은 54-66%의 병반면적율을 보여 이들이 A. brassicicola에 대해 약간의 저항성을 나타낸다고 생각되었다(Table 2).
이들 품종 중 종자회사에서 검은무늬병에 대한 저항성으로 공시한 품종은 없었고 우리의 저항성 검정 결과에서도 강한 저항 성 품종은 없었으므로, 무 검은무늬병 저항성 검정 체계확립을 위한 발병조건에 따른 무 검은무늬병 발생 실험을 위해 실험한 품종 중 높은 감수성을 보인 ‘토광’과 ‘대평여름’ 그리고 약한 저항성을 보인 ‘금봉’과 ‘새롬’을 선발하였다
무 유묘의 생장 정도에 따른 검은무늬병 발생
무 4품종의 파종 시기를 다르게 하여 10, 13, 16, 19일 동안 재배한 유묘에 병원균 접종하고 무 유묘의 생육 시기에 따른 검은 무늬병의 발생을 조사한 결과, 16일 재배한 유묘의 경우에는 ‘금봉’, ‘새롬’, ‘토광’, ‘대평여름’ 각각 82, 82, 95, 98%의 평균 병반 면적율을 보였다(Fig. 3). 하지만 10일 또는 13일 재배한 유묘는 실험한 품종 모두에서 91% 이상의 높은 병반면적율을 보였으 며, 19일 재배한 유묘는 감수성 품종인 ‘토광’과 ‘대평여름’이 각각8 6%와 75%의 다소 낮은 병반면적율을 나타냈다(Fig. 3).
Doullah et al.(2006)은 A. brassicicola에 대한 저항성 B. rapa 품종은 30일 재배한 유묘의 잎에서는 강한 저항성을 나타내었 지만 40일 재배한 식물의 잎에서는 경계선 상의 저항성을 나타냈으며, 감수성 품종도 생장 단계에 따라 서로 다른 병 발생 정도 를 보이며 나이든 잎이 어린 잎에 비해 더 감수성을 나타낸다고 보고하였다. 하지만 본 실험에서는 10, 13, 16, 19일 동안 재배 한 무 유묘의 검은무늬병 발생을 실험한 결과, 무 4품종의 평균 발병도는 각각 99, 96, 89, 74%로 무가 성장할수록 검은무늬병 발생은 감소하였다(Fig. 3). 이는 실험에 사용한 무 식물의 생장 정도가 서로 다르기 때문인 것으로 생각되었다. 본 실험은 저항 성 품종 육성을 위한 대량검정법 개발을 목표로 실험하였기 때문에 유묘를 사용하였고, Doullah et al.(2006)은 30-40일 재배 한 성숙한 식물을 사용하여 실험한 결과이다
저항성 정도가 다른 그룹으로 나누어 살펴보면 비교적 약한 저항성을 보인 ‘금봉’과 ‘새롬’ 두 품종에 대한 10, 13, 16, 19일 재 배한 유묘의 평균 병반면적율은 각각 98, 93, 82, 67%을, 그리고 감수성 품종 ‘토광’과 ‘대평여름’ 두 품종은 각각 100, 99, 97, 81%의 병반면적율을 보였다(Fig. 3). 따라서 품종의 저항성 정도와 관계없이 무가 생장할수록 검은무늬병 발생이 감소하는 것을 알 수 있었으며, 실험한 4가지 생육 시기 중 16일 재배한 유묘는 품종간 검은무늬병에 대한 저항성 차이가 가장 뚜렷하여 검 은무늬병 저항성 검정에 적합한 무의 생육 시기로 생각되었다.
Table 2. Resistance degree of 61 commercial radish cultivars to Alternaria brassicicola causing black spotz. 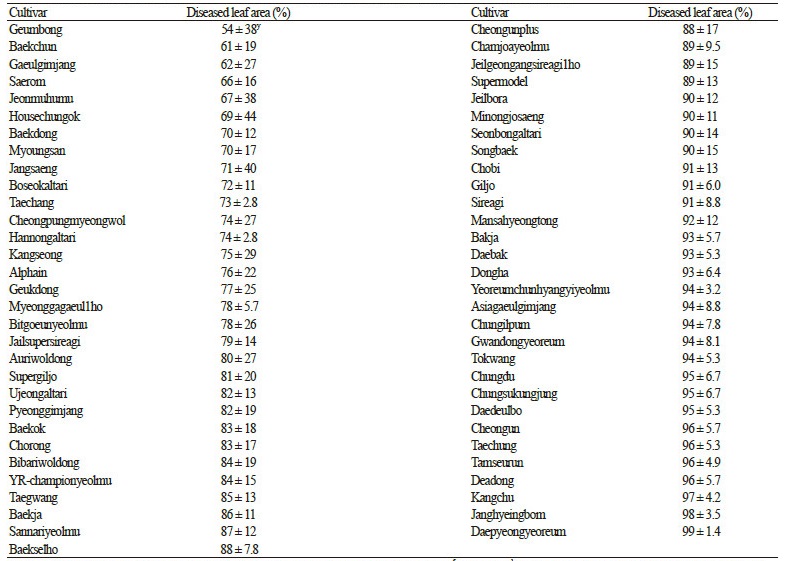 |
zThirteen-day-old seedlings of radish cultivars were inoculated with a spore suspension (2.0 × 105 spores·mL-1) of A. brassicicola KACC 40036 by the spray method.The plants were incubated in a humidity chamber at 25°C for 24 h and then transferred to a growth chamber at 25°C and 80% RH with a 12-h light/dark cycle. Two days after inoculation, the percent diseased leaf area of each plant was scored.
yMean ± standard deviation of two runs with ten replicates each.
Fig. 3
Fig. 3. Development of black spot on four radish cultivars at different plant growth stages. Spore suspension (2.0 × 105 spores·mL-1) of Alternaria brassicicola KACC 40036 was inoculated onto 10-, 13-, 16-, and 19-day-old seedlings of four radish cultivars were inoculated with by the spray method. The inoculated plants were incubated in a humidity chamber at 25°C for 24 h and then transferred to a growth chamber at 25°C and 80% RH with a 12-h light/dark cycle. Disease severity was measured two days after inoculation, and is represented as percentage of infected leaf area. The data were obtained from five replicates with two repetitions.
접종원 농도에 따른 검은무늬병 발생
접종원 농도(2.5 × 104, 5.0 × 104, 1.0 × 105, 2.0 × 105spores·mL-1)에 따른 4개 무 품종의 검은무늬병 발생을 실험한 결과,실험한 모든 품종들은 모두 접종 농도가 증가할수록 검은무늬병 발생이 증가하였다(Fig. 4). 감수성 품종인 ‘토광’과 ‘대평여름’ 은 1.0 × 105spores·mL-1 이하에서는 71% 이하의 다소 낮은 병반면적율을 보였으나, 2.0 × 105spores·mL-1 에서는 88% 이상의 높은 병반면적율을 보였다(Fig. 4).
King(1994)은 양배추(Brassica oleracea var. capitata)와 유채(B. napus)에 A. brassicicola 균주를 2.3 × 104, 3.7 × 104, 그리고 5 × 104conidia·mL-1 농도로 접종하고 검은무늬병 발생을 조사한 결과, 처리 간의 발병도 차이를 확인할 수 없었다고 보고 하였다. 하지만 본 실험에서 무 4품종에서 접종원 농도에 따른 검은무늬병 발생을 조사한 결과에서는 2.5 × 104, 5.0 × 104, 1.0 × 105, 2.0 × 105spores·mL-1 농도로 접종하였을 때 각각 16, 30, 48, 74%의 평균 발병도를 나타내며, 접종한 포자 농도가 높아 질수록 실험한 무 품종들의 검은무늬병의 발생은 증가하였다(Fig. 4). 이와 같은 경향은 모든 품종에서 확인되었는데, 이것은 무 검은무늬병에서 뿐만 아니라 대부분 균류병에서의 감수성 품종과 고추 역병 및 수박 덩굴쪼김병 등에서 고도의 질적저항성 품종이 아닌 중도저항성 품종에서는 일반적으로 발생하는 것으로(Jo et al., 2014; Jo et al., 2015) 본 실험에 사용한 무 품종들 중에 고도의 저항성 품종이 포함되지 않았기 때문으로 생각되었다. 본 결과로부터 A. brassicicola에 의한 무의 검은무늬병 저 항성 검정을 위해서는 2.0 × 105spores·mL-1농도로 접종하여 실험하는 것이 효과적이라 생각되었다
Fig. 4
Fig. 4. Effects of inoculum concentration on the occurrence of black spot on four radish cultivars. Sixteen-day-old seedlings were inoculated with various concentration (2.5 × 104, 5.0 × 104, 1.0 × 105 and 2.0 × 105 spores·mL-1) of Alternaria brassicicola KACC 40036 spore suspension by the spray method. The inoculated plants were incubated in a humidity chamber at 25°Cfor 24 hr and then transferred to a growth chamber at 25°C and 80% RH with a 12-h light/dark cycle. Disease severity was measured two days after inoculation, and is represented as percentage of infected leaf area. The data were obtained from two runs with five replicates each.
재배 온도에 따른 검은무늬병 발생
접종 후 재배온도(20, 25, 30°C)에 따른 네 가지 무 품종들의 검은무늬병 발생을 실험한 결과, 25°C의 경우에는 ‘금봉’, ‘새롬’, ‘토광’, ‘대평여름’에서 각각 74, 75, 89, 89%의 병반면적율을 보였다(Fig. 5). 즉, 감수성 품종들에서는 검은무늬병이 심하게 발 생하였고, 감수성 및 약한 저항성 품종 간의 발병 정도 차이 또한 효과적으로 나타났다. 하지만 20°C와 30°C에서는 감수성 품 종을 비롯한 모든 품종에서 58% 이하의 낮은 병반면적율을 보였을 뿐만 아니라, 감수성 및 약한 저항성 품종간의 차이도 거의 없었다(Fig. 5).
그리고 유묘에 병원균을 접종하고 20, 25, 30°C에서 재배하였을 때 무 4품종의 평균 발병도는 각각 27, 82, 47%를 나타내 25°C에서 검은무늬병이 가장 효과적으로 발생하고 있음을 알 수 있었다(Fig. 5). A. brassicicola를 접종한 식물은 25°C에서 검 은무늬병이 가장 빠르게 병징을 나타내지만, 병원균이 이미 감염되어 있는 종자로부터 재배된 유묘는30 °C에서 더 빠르게 병 징을 나타낸다고 하였다(Bassey and Gabrielson, 1983; Kumar et al., 2014). 본 연구는 건전 종자로부터 재배한 유묘에 병원균 을 접종한 경우이므로 검은무늬병 발생 최적온도가2 5°C라는 점에서 유사한 결과이다.
이상의 결과로부터 무 검은무늬병의 저항성 검정을 위한 효과적인 방법으로 종자를 파종하고 온실(25 ± 5°C)에서 16일 동 안 재배한 무 유묘의 잎에 A. brassicicola의 포자현탁액(2.0 × 105 spores·mL-1)을 충분히 분무하여 접종하고, 25°C 습실상에 서 24시간 동안 습실처리한 후에 25°C의 항온항습실(상대습도 80%)로 이동하여 하루 12시간씩 광을 조사하면서 재배하고, 접종 2일 후에 잎에 발생한 검은무늬병의 병반면적율(%)을 달관조사 하는 것을 제안하고자 한다.
Fig. 5
Effects of incubation temperature on the development of black spot on four radish cultivars. Sixteen-day-old seedlings were inoculated with spore suspension (2.0 × 105 spores·mL-1) of Alternaria brassicicola KACC 40036 by the spray method. The inoculated plants were incubated at 20, 25, and 30°C in a controlled humidity chambers. Disease severity of the plant was measured two days after inoculation, and is represented as percentage of infected leaf area. The data were obtained from five replicates with two repetitions


