서 언
박과(Cucurbitaceae) 식물은 118개 속(genera), 약 800종(species)으로 이루어져 있으며 대부분 1년생 초본과로 온화한 기후나 열대지방에서 생육한다(Jeffrey et al., 1980). 박과에 속하는 주요 작물로는 수박(Citrullus lanatus(Thunb.) Matsum. & Nakai.), 호박(Cucurbita spp.), 오이(Cucumis sativus L.), 멜론(Cucumis melo L.)이 있다. 이들 작물들의 2013년 전세계 생산량은 수박(1억 9백만 톤), 오이(7천 1백만 톤), 멜론(2천 구백만 톤), 호박(2천 2백만 톤)의 순으로 전체 채소 생산량의 약 30%를 차지함으로서(FAO, 2013), 생산에 따른 농가의 수익뿐만 아니라 종자산업에도 큰 수익을 창출해 내는 작물들이다.
이러한 작물들의 유연관계 및 유전적 다양성에 대한 분석은 유전적 범위에 대한 정보와 계통발생, 작물의 기원지 분석, 다양한 육종 재료 확보 측면에서 F1 잡종 품종이 주를 이루는 육종 사업에서 넓은 유전적 배경을 파악할 수 있는 중요한 연구 분야이다. 과거 시설의 필요와 많은 시간이 투자되고 환경적인 영향에 의해 유전적 판별에 오류가 발생할 수 있는 표현형(phenotype)의 차이를 이용하였다. 그러나 유전자형(genotype)을 통하여 표현형을 판별하는 방법인 분자표지(molecular marker)는 시간과 장소의 구애를 받지 않고 좀 더 정확한 유전정보를 얻을 수 있다. 분자표지는 유전적 다양성 연구, 품종판별(cultivar identification), 유전자 지도(genetic map) 작성 및 주요 형질의 분자표지를 이용한 선발(marker-assisted selection) 등 넓은 분야에 이용되고 있다(Hwang et al., 2011). 식물의 유전적 다양성 및 유연관계 분석을 위해 활용되어 온 분자표지로서는 isozyme(Akashi et al., 2002; Knerr et al., 1989), restriction fragment length polymorphsim(RFLP)(Dijkhuizen et al., 1996; Yi et al., 2006), random amplified polymorphic DNA(RAPD)(Ferriol et al., 2003b; Horejsi et al., 1999; Lee et al., 2003; Levi et al., 2001; Zhuang et al., 2004), amplified fragment length polymorphism (AFLP)(Ferriol et al., 2003a; Garcia-Mas et al., 2000), simple sequence repeat(SSR)(Chung et al., 2006; Katzir et al., 1996; Kwon et al., 2010; Ritschel et al., 2004) 등의 사례들이 있다. 특히 최근에 많이 사용되고 있는 expressed sequence tags (ESTs)은 발현된 유전자 부위에서 나타난 mRNA의 역전사를 통해 염기서열이 밝혀진 cDNA의 한 부분으로서 가지(Nunome et al., 2009), 고추(Yi et al., 2006), 토마토(D’Agostino et al., 2007), 장미(Park et al., 2010)에서뿐만 아니라 많은 수의 작물에서 EST의 염기서열이 분석되어 있고 데이터화되어 있다.
박과의 경우 International Cucurbit Genomics Initiative(ICuGI) database(http://www.icugi.org) 내에 멜론, 오이, 수박, 호박에 대한 ESTs 정보가 게시되어 있다. 이러한 EST의 정보를 통하여 유전자 전사체 기반의 분자표지 개발이 가능한데, EST-SSR의 경우 EST 내에 존재하는 초위성 염기서열(microsatellite) 또는 단순반복서열(simple sequence repeat)를 이용할 수 있는 분자표지의 한 형태이다. 초위성 염기서열은 DNA 내에 비교적 풍부하게 존재하며 재현성이 뛰어난 공우성 표지로 이용 가능하다. 따라서 기존 EST 정보를 이용한 EST-SSR 개발은 새로운 SSR을 찾는데 소비되는 비용을 절감할 수 있고, 이들 표지들이 유전자에 기반한 것이라는 측면에서 발현되는 유전자-특이적(gene-specific)라 할 수 있다. 또한 유전자의 종속간 상동성에 기인함으로서 분자표지의 종내 또는 근연종 간 이동성(transferability)이 (Ellis and Burke, 2007; Gupta et al., 2003) 종 간 비교유전체 연구에 활용성이 높다(Park et al., 2010). 이러한 EST-SSR을 이용하여 유전적 다양성을 연구한 사례는 멜론(Kong et al., 2006), 호박(Kong et al., 2007), 수박(Levi et al., 2009)이 있으나 4가지 박과 주요 작물의 유연관계분석에 이용된 사례는 드물다.
따라서 본 연구에서는 ICuGI DB에 공시되어 있는 수박의 EST-SSR에 대한 PCR Primer 염기서열을 선발하여 수박 EST-SSR 마커의 타 박과 주요 작물(오이, 참외, 멜론, 호박)에 적용 가능성을 알아보고, 박과 종의 F1 품종과 계통 간 유연관계를 분석하고자 수행되었다.
재료 및 방법
식물재료
합성된 EST-SSR primer의 PCR 검정용 1차 DNA 분석 시료로 수박 F1 1 품종(Citrullus lanatus var. vularis Schrad.)과 야생종 1 계통 Citrullus lanatus var. citroides Mats. & Nakai.), 호박 F1 3 품종[(Cucurbita moschata(Duch. ex Lam.) Duch. & Poir, Cucurbita maxima Duch., Cucurbita pepo L.)], 멜론 F1 1 품종(Cucumis melo var. cantalupensis Naudin.), 참외 F1 1 품종(Cucumis melo var. conomon Makino.), 오이 F1 1 품종(Cucumis sativus L.) 등 총 8점의 식물시료를 사용하였다(Table 1). 박과 작물 간 유연관계 분석을 위한 2차 DNA 분석 시료로는 수박 3 야생종 계통, F1 6 품종 총 9점, 호박 F1 4 품종, 오이 F1 5 품종, 멜론 F1 2 품종과 2 육성계통, 참외 F1 2 품종 등 총 24점의 식물시료가 사용되었다(Table 2).
Table 1. Eight accessions of Cucurbitaceous crops used as the first plant sample panel for evaluation of the watermelon EST-SSR primer sets. |
Species | Scientific name | Cultivar | Provider |
Watermelon | Citrullus lanatus var. citroides Mats. & Nakai | Gongdae | - |
Citrullus lanatus var. vulgaris Schrad | Speedggul | Nongwoo-Bio. |
Squash/Pumpkin | Cucurbita moschata (Duch. ex Lam.) Duch. & Poir | Nongwoojosengpoot | Nongwoo-Bio. |
Cucurbita maxima Duch. | Dambibamhobak | Jingheung Jongmyo |
Cucurbita pepo L. | Saeronzuccine | Hyundai Jongmyo |
Melon | Cucumis melo var. cantalupensis Naudin. | Earl’s Elite | Syngenta |
Oriental melon | Cucumis melo var. conomon Makino | Geummadalggul | Mirae Jongmyo |
Cucumber | Cucumis sativus L. | Janghyeongnakhab | Nongwoo-Bio. |
Table 2. Twenty-four accessions of Cucurbitaceous crops used as the second plant sample panel for genetic relationship study based on watermelon EST-SSRs. |
ENz. | Species | Scientific name | Cultivar | Provider |
1 | Watermelon | Citrullus lanatus var. citroides Mats. & Nakai. | Gongdae | - |
2 | Citrullus lanatus var. vulgaris Schrad. | Charleston Gray | Subaeunico |
3 | Citrullus lanatus var. vulgaris Schrad. | Augusta | Syngenta |
4 | Citrullus lanatus var. vulgaris Schrad. | Orangeking | Nongwoo-Bio |
5 | Citrullus lanatus var. vulgaris Schrad. | Vasko | Elite zaden |
6 | Citrullus lanatus var. vulgaris Schrad. | Hwabo | Nongwoo-Bio |
7 | Citrullus lanatus var. vulgaris Schrad. | Speedggul | Nongwoo-Bio |
8 | Citrullus lanatus var. citroides Mats. & Nakai | PI189225 | - |
9 | Citrullus lanatus var. citroides Mats. & Nakai | PI494817 | - |
10 | Squash/ Pumpkin | Cucurbita moschata (Duch. ex Lam.) Duch. & Poir | Nongwoojosengpoot | Nongwoo-Bio |
11 | Cucurbita maxima Duch. | Danbam | Nongwoo-Bio |
12 | Cucurbita pepo L. | Taeyangzuccine | Nongwoo-Bio |
13 | Cucurbita ficifolia Bouche. | Heukjong | Nongwoo-Bio |
14 | Melon | Cucumis melo var. cantalupensis Naudin. | Earl’s Elite | GARESy |
15 | Cucumis melo var. cantalupensis Naudin. | Charentais | GARES |
16 | Cucumis melo var. cantalupensis Naudin. | JC-23 | Jangchun Jongmyo |
17 | Cucumis melo var. cantalupensis Naudin. | JC-24 | Jangchun Jongmyo |
18 | Oriental melom | Cucumis melo var. conomon Makino. | Keumssaragi | GARESy |
19 | Cucumis melo var. conomon Makino. | Seonghwan | GARESy |
20 | Cucumber | Cucumis sativus L. | Janghyeongnakhab | Nongwoo-Bio |
21 | Cucumis sativus L. | Gangryeoksamcheok | Nongwoo-Bio |
22 | Cucumis sativus L. | Ganghobaekchim | Nongwoo-Bio |
23 | Cucumis sativus L. | Dynersity | K.S.I |
24 | Cucumis sativus L. | Mashya | Syngenta |
zEN, Entry number of 24 accessions of Cucurbitaceous crops. yGARES, Gyeongsangnam-do Agricultural Research & Extension Services. |
DNA 추출
DNA 추출은 발아 후 3주된 유엽을 사용하였다. 각 식물 시료에서 얻은 잎 0.5-2g을 1.5µL micro-centrifuge tube에 넣고 steel bead와 600µL DNA extraction buffer을 넣어준 뒤 TissueLyser(QIAGEN, Netherlands)를 이용하여 분쇄시키고 45분간 65°C에 waterbath를 이용하여 반응시켰다. 그 다음 200µL 7.5 M ammonium acetate를 넣고 15분 동안 4°C에 반응 시킨 후 10분간 14,240 × g으로 원심분리 시켰다. 새로운 1.5µL micro-centrifuge tube에 5µL glycogen solution (5mg・mL-1)과 600µL isopropanol을 넣은 후 원심분리시킨 tube의 상층액을 덜어서 새로운 튜브에 넣어주고 잘 혼합해 준 뒤 10분간 14,240 × g으로 원심분리시켜 주었다. 원심분리가 끝난 뒤 상층액을 버리고 300µL 70% EtOH 용액을 넣어주고 10분간 14,240 × g로 원심분리 시켜 세척하여 준 다음 pellet을 완전히 건조시켜 주었다. Pellet이 완전히 건조되면 0.1 M Tris 200µL를 넣어 용해시키고 추출한 DNA는 Nano- drop 1000(Thermo Scientific, USA) 분광광도계로 정량분석을 하였다.
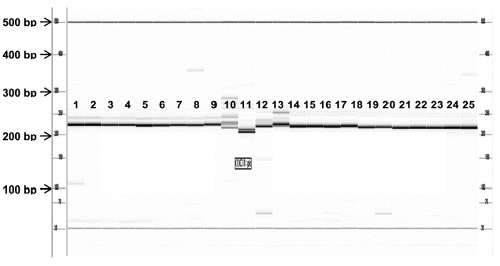
|
Fig. 1. Fragment Analyzer (capillary electrophoresis system) image of PCR products amplified by WMU 14110 primer set and polymorphic in 24 accessions of Cucurbitaceous crops. The numbers from 1 to 24 refer to the list of plant sample panel in Table 2. |
EST-SSR Primer 합성 및 선발
실험에 사용된 EST-SSR primer의 염기서열 정보는 Inter-national Cucurbit Genomics Initiative database(ICuGI, http:// www.icugi.org)에 공시된 수박의 WMU unigene을 토대로 총 650개의 primer set를 대상으로 선발하였으며, 이 중 120개의 primer set을 합성(Bioneer, daejeon, Korea)하였다. 합성한 primer set 중 1차 DNA 분석을 통해 대립유전자 특이적 PCR 증폭이 가능하고 식물 시료 간 다형성(polymorphism)을 보이는 primer set을 선발하였다. 선발된 primer set을 이용하여 2차 DNA 분석을 통해 보다 다양한 박과 식물시료의 유전자형 분석 및 유연관계 분석을 수행하였다.
PCR 및 전기영동
마커 검정을 위한 PCR용액의 조성은 genomic DNA 20ng, forward와 reverse primer 각각 0.5µM, 10X PCR buffer, 0.2µM dNTPs, 0.6 U Taq polymerase(Solgent, Korea), 그리고 나머지는 3차 증류수를 충당하여 총 반응 용액량을 20µL로 하였다. PCR 조건은 95°C에서 15초간, 60°C에서 30초간(2-10cycle 동안 각 cycle 간 0.5°C 감소), 72°C에서 30초간 10cycle, 95°C에서 15초간, 55°C에서 30초간, 72°C에서 1분간 35cycle의 touch-down PCR 단계를 거쳐 반응시켰다.
EST-SSR primer set의 PCR 증폭 산물들은 1차적으로 아가로스젤 전기영동을 통해 확인하였다. 전기영동은 2.5% 아가로스젤을 이용하여 TAE buffer 내에서 100V로 2시간 실시하였고, 분리된 PCR 생성물은 ethidium bromide를 이용하여 염색한 후 UV light 하에서 관찰하였다.
아가로스젤 전기영동을 통해 PCR 증폭이 확인된 PCR 산물들에 대해서는 Fragment Analyzer™(Advanced Analytical Technologies, USA)을 이용하여 보다 정밀한 유전자형 분석을 수행하였다(Fig. 1). 유전자형의 분석은 PROSize™ 2.0 version 1.2.1.1 프로그램을 이용하였다. PCR 증폭 산물의 크기 ± 2 bp 오차 범위 내에 있을 경우 동일한 유전자형으로 간주하고 증폭 산물이 명확한 것만 판독하였다. 각 시료 간 대립유전자(allele)는 유무(present/absent)에 따라 ‘1(present)’과 ‘0(absent)’으로 scoring 하였다.
마커 다형성 및 유연관계 분석
유전자형 분석에 사용된 primer set의 polymorphic information content(PIC) value는 다음 식을 사용하여 구하였다.
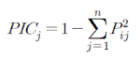
PICj는 EST-SSRi의 polymorphic information content value를 뜻하며 Pij는 n개의 패턴 중 EST-SSRi에 대한 j번째 패턴의 빈도를 나타낸다(Botstein et al., 1980). 짝유사행렬(Pairwise similarity matrix)은 Nei-Li similarity index(Nei and Li, 1979)를 이용하였으며 다음과 같다:
|
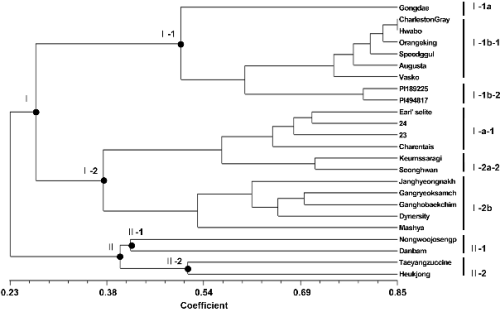
Fig. 2. A dendrogram showing the genetic relationship among 24 accessions of Cucurbitaceous crops based on 49 watermelon EST-SSR primer sets. |
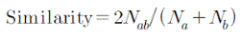
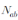 는 두 개의 유전자형에 공통으로 나타나는 단편의 수를 뜻하며
는 두 개의 유전자형에 공통으로 나타나는 단편의 수를 뜻하며 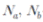 는 각각의 유전자형에서 나타나는 단편의 총 개수를 의미한다. 군집분석(cluster analysis)은 Nei-Li similarity 값을 기반으로 비가중 산술 결합법(UPGMA, unweighted pair group method on arithmetic averages) 방법을 이용하여 분석하였다. 모든 통계 분석에는 NTSYS-PC version 2.02k (Rohlf, 2002)를 이용하였다.
는 각각의 유전자형에서 나타나는 단편의 총 개수를 의미한다. 군집분석(cluster analysis)은 Nei-Li similarity 값을 기반으로 비가중 산술 결합법(UPGMA, unweighted pair group method on arithmetic averages) 방법을 이용하여 분석하였다. 모든 통계 분석에는 NTSYS-PC version 2.02k (Rohlf, 2002)를 이용하였다.
결과 및 고찰
EST-SSR Primer 선발 및 유전자형 분석
총 8개의 1차 검정 시료에 대해 120개 수박 EST-SSR primer set의 PCR 검정 결과, 51개(49.17%) primer set은 모든 식물시료에서 PCR 증폭이 가능하였으며, 이 중 식물시료 간 대립유전자 특이적 증폭산물(EST-SSR 마커) 크기에 따른 다형성을 보인 primer set은 총 49개(40.8%)였다. 선발된 49개의 primer set을 24개의 2차 식물시료에 대해 PCR 검정과 Fragment Analyzer를 이용한 전기영동 및 유전자형 분석 결과, 총 382개의 PCR 밴드가 확인되었다. 가장 많은 수와 가장 적은 수의 다형성 PCR 밴드를 나타낸 primer set는 WMU15338과 WMU15818로 각각 16개와 2개였으며, 한 primer set당 평균 다형성 PCR 밴드 수는 7.8개였다. 각 primer set의 PIC 값은 다양하였는데, 이 중 46개의 primer set이 0.5 이상의 값을 보였다(Table 3). 사용된 49개 primer set의 평균 PIC 값은 0.754였으며, 가장 높은 PIC 값을 보인 primer set은 WMU2826으로 0.904, 가장 낮은 PIC 값을 보인 primer set은 WMU15818로 0.100이었다.
Table 3. List of the watermelon EST-SSR primer sets used for the evaluation of genetic relationship among 24 accessions of Cucurbitaceous crops. Tm, EPS, and An indicate melting temperature, expected product size, and allele number, respectively. |
EST-SSR | Putative protein | Putative fucntion | E-value | SSR motif | Primer sequence | Tm | EPS | PIC value | AN |
WMU0003 | AAL27560 | abscisic acid response protein [Cucumis melo] | 4E-10 | (CCA)6 | F: AAAGCCATGGCAGAAGAAGA | 59.955 | 225 | 0.806 | 7 |
| | | | | R: CTTGTGTTCATGGCTGTGCT | 59.905 | | | |
WMU0029 | XP_002517606 | lactoylglutathione lyase, putative [Ricinus communis] | 2E-78 | (GCA)11 | F: TACCGGTGATTCCATTAGGC | 59.784 | 159 | 0.803 | 7 |
| | | | | R: TTAATTTCTCCCGTGGGTTG | 59.795 | | | |
WMU0129 | XP_002331872 | predicted protein [Populus trichocarpa] | 1E-41 | (TC)6 | F: TGCTTCCATTTTTGGAGACC | 60.051 | 265 | 0.842 | 8 |
| | | | | R: CAAGCACCTAGCTCTGACTCAA | 59.819 | | | |
WMU0155 | ABC69274 | putative DnaJ protein [Camellia sinensis] | 2E-51 | (TTC)10 | F: GCTTCCGTTGCTACTTCTGG | 60.015 | 280 | 0.651 | 4 |
| | | | | R: GCACGCCACAATTACTTCCT | 60.14 | | | |
WMU0535 | ABK96555 | unknown [Populus trichocarpa x Populus deltoides] | 9E-25 | (TTA)5 | F: TATCCCTGACCAACCTGAGC | 60.073 | 236 | 0.781 | 7 |
| | | | | R: ACCAACTTCTGTGACTCCTAAAAA | 59.646 | | | |
WMU0542 | XP_002277651 | predicted: hypothetical protein [Vitis vinifera] | 4E-15 | (AGA)5 | F: TGAGAAAGCAGCATTGTTGG | 59.988 | 241 | 0.662 | 5 |
| | | | | R: ATTATGGATTGCAAGACCGC | 59.929 | | | |
WMU0597 | BAA08094 | AOBP (ascorbate oxidase promoter-binding protein) [Cucurbita maxima] | 2E-32 | (CT)6 | F: GCATGAAGTGGAGACAAGCA | 59.992 | 171 | 0.753 | 6 |
| | | | | R: AGGATGGCTAGCAGATTCCA | 59.797 | | | |
WMU0823 | XP_002310274 | predicted protein [Populus trichocarpa] | 1E-70 | (TG)9 | F: ACGGGCTCAAATGGAGAAAT | 60.826 | 268 | 0.790 | 8 |
| | | | | R: TAGGGACCAATGGACAGTCG | 60.913 | | | |
WMU0850 | XP_002516559 | protein transporter, putative [Ricinus communis] | 6E-40 | (CAG)5 | F: CTCCTGCATCGGATCAAAAT | 60.036 | 225 | 0.808 | 12 |
| | | | | R; CCATGTTCATGACATTCCCA | 60.177 | | | |
WMU0857 | XP_002314149 | predicted protein [Populus trichocarpa] | 6E-45 | (TG)8 | F: GTGCACTCTTCCACCCATTT | 59.973 | 242 | 0.821 | 8 |
| | | | | R: ATGGAATGAATCCCAGTGCT | 59.366 | | | |
WMU0995 | CAN83645 | hypothetical protein [Vitis vinifera] | 3E-36 | (CAG)7 | F: TGGTTTGGGACAAAGGCTAC | 59.971 | 126 | 0.716 | 7 |
| | | | | R: GGGTGACTGAGAGAAGGCTG | 59.986 | | | |
Table 3. Continued. |
EST-SSR | Putative protein | Putative fucntion | E-value | SSR motif | Primer sequence | Tm | EPS | PIC value | AN |
WMU1066 | No hits found | - | - | (CCA)6 | F: AAAGCCATGGCAGAAGAAGA | 59.955 | 270 | 0.717 | 7 |
| | | | | R: CTGCGAGAGCGAAAGAAAAC | 60.27 | | | |
WMU1167 | XP_002277383 | predicted: hypothetical protein [Vitis vinifera] | 4E-21 | (CAC)5 | F: GACCACAATCACCAACTCCC | 60.223 | 270 | 0.698 | 5 |
| | | | | R: GCATGGTTTTATCATCAGCG | 59.14 | | | |
WMU1192 | XP_002273467 | predicted: hypothetical protein [Vitis vinifera] | 2E-39 | (GCC)5 | F: TTGACTCTGATTCTCCCGGT | 59.655 | 141 | 0.826 | 11 |
| | | | | R: AGGGGAGAAGAATTGGGAAA | 59.875 | | | |
WMU1502 | XP_002303301 | AP2/ERF domain-containing transcription factor [Populus trichocarpa] | 1E-38 | (GGA)6 | F: CCTTATGCATCAAAGGCGAT | 60.06 | 238 | 0.878 | 9 |
| | | | | R: TCGTTCAGCGACACAGTACC | 59.905 | | | |
WMU1508 | XP_002285195 | predicted: hypothetical protein [Vitis vinifera] | 8E-45 | (CTT)5 | F: CGCTAGGTTGAGGAAACAGG | 59.869 | 216 | 0.694 | 5 |
| | | | | R: ATATTTAAGGGGGTGGAGGG | 59.023 | | | |
WMU1957 | XP_002280404 | predicted: hypothetical protein [Vitis vinifera] | 3E-70 | (TA)7 | F: GAGCTGAACAAAAGCATCCC | 59.82 | 204 | 0.858 | 13 |
| | | | | R: GATTCACAGAAGCCTTTGCC | 59.82 | | | |
WMU2124 | No hits found | - | - | (TC)6 | F: ACCCAGCCACATCTACCAAA | 60.375 | 102 | 0.763 | 4 |
| | | | | R: CCACCATTAAGGGATGATACTTTC | 59.975 | | | |
WMU2175 | NP_196680 | SHN3 (shine3); DNA binding / transcription factor [Arabidopsis thaliana] | 1E-07 | (CTT)6 | F: TAATGGCCAACCCCATTAAA | 60.012 | 247 | 0.870 | 13 |
| | | | | R: GCTGCCTGACTCCTCTGAAC | 60.143 | | | |
WMU2282 | XP_002281427 | predicted: hypothetical protein [Vitis vinifera] | 2E-52 | (TGA)6 | F: TTCCAATCCGCTCTACTGCT | 59.978 | 221 | 0.627 | 5 |
| | | | | R: TCATCATCCACTTCACCAGC | 59.637 | | | |
WMU2376 | XP_002298707 | predicted protein [Populus trichocarpa] | 2E-16 | (AG)10 | F: CCAAAATGGGGCATGTCTAC | 60.192 | 236 | 0.896 | 12 |
| | | | | R: TTTCTTATGGGTCAGCCAGC | 60.214 | | | |
WMU2504 | XP_002284829 | predicted: hypothetical protein [Vitis vinifera] | 9E-39 | (GCA)6 | F: GCCTACAGATTGGTGGCATT | 59.962 | 245 | 0.722 | 5 |
| | | | | R: CTTGCATCTCTCCCTTGAGC | 60.096 | | | |
WMU2562 | No hits found | - | - | (TC)6 | F: TTGTTGTGAGCATTTGGAAAA | 59.192 | 131 | 0.834 | 7 |
| | | | | R: TCAGAACCACCCATCATCAA | 59.893 | | | |
Table 3. Continued. |
EST-SSR | Putative protein | Putative fucntion | E-value | SSR motif | Primer sequence | Tm | EPS | PIC value | AN |
WMU2826 | ACI15344 | NAC domain protein NAC3 [Gossypium hirsutum] | 2E-29 | (ATT)6 | F: CCGATTTCAGTGCCGATTAT | 59.923 | 251 | 0.904 | 15 |
| | | | | R: TGAACCGTTTGGGTACTTCC | 59.83 | | | |
WMU3858 | XP_002514762 | transcription factor, putative [Ricinus communis] | 6E-29 | (ATC)8 | F: TGATGAAGAAACGTCAAGTAGTAGTG | 58.994 | 211 | 0.658 | 6 |
| | | | | R: GAGCCTTCTTCACCAGTTGC | 59.997 | | | |
WMU4058 | XP_002319204 | predicted protein [Populus trichocarpa] | 7E-24 | (ATT)5 | F: ATCGGAGGAAATCCTTTTGC | 60.399 | 234 | 0.825 | 12 |
| | | | | R: TGACATTGCTATGCAGATTGAA | 59.329 | | | |
WMU4222 | No hits found | - | - | (TTC)7 | F: TCCAAGTGGCTTGCTCTTTT | 59.993 | 185 | 0.651 | 5 |
| | | | | R: TCTCAACCTCAAATTCCGAGA | 59.799 | | | |
WMU4232 | CAN67544 | hypothetical protein [Vitis vinifera] | 4E-46 | (AG)6 | F: GGCCACCAGATGAAAGAGAA | 60.195 | 251 | 0.874 | 9 |
| | | | | R: CCCTTCCCAAGCTTTCCTAT | 59.549 | | | |
WMU11952 | No hits found | - | - | (ATG0)7 | F: TCAATGGTGGTGAGAGCTGA | 60.402 | 136 | 0.853 | 10 |
| | | | | R: AACCCCTGTTAAAATTGCCA | 59.315 | | | |
WMU12236 | No hits found | - | - | (CT)6 | F: TGGCCGTTCTTCAAGCTTAC | 60.386 | 149 | 0.460 | 3 |
| | | | | R: GTGGAGAGCCAGTAGCGAAC | 60.02 | | | |
WMU12270 | XP_002276078 | predicted: hypothetical protein [Vitis vinifera] | 3E-09 | (CT)6 | F: CCCACCATTGAAAAATGCTT | 59.801 | 248 | 0.801 | 6 |
| | | | | R: GCTCGGTACGGTTGAAATGT | 60 | | | |
WMU12334 | ACU13810 | unknown [Glycine max] | 4 | (ATA)8 | F: CTTCCTGCACTTTTCAAGCC | 59.993 | 198 | 0.711 | 6 |
| | | | | R: CAGCAAATACAGATCGCTAACAA | 59.459 | | | |
WMU12911 | NP_00110572 | 9 signal recognition particle 9 kDa protein [Zea mays] | 2E-09 | (TCT)5 | F: CCTAACCCCGAAGAAATCAA | 59.016 | 209 | 0.863 | 10 |
| | | | | R: ATCTCTTGGTACCGCACACC | 59.997 | | | |
WMU13711 | No hits found | - | - | (TAT)5 | F: AAGCAGGTGGAAGTTAGCGA | 60.015 | 149 | 0.820 | 10 |
| | | | | R: CATCTCAACCGTGAAGGAAAG | 59.72 | | | |
WMU13715 | No hits found | - | - | (TC)7 | F: CTCCTTCTCCCACAAACCAA | 60.081 | 183 | 0.836 | 9 |
| | | | | R: AGGATGTAAAGGCGGGAAAT | 59.799 | | | |
WMU13866 | No hits found | - | - | (GGT)6 | F: CTTGTGTTCATGGCTGTGCT | 59.905 | 231 | 0.724 | 6 |
| | | | | R: AAAGCCATGGCAGAAGAAGA | 59.955 | | | |
WMU14110 | No hits found | - | - | (TGG)7 | F: TGTTCGTCAAAGCAATAGCG | 60.014 | 230 | 0.801 | 10 |
| | | | | R: GAGTGGCCCACGATAGAAGA | 60.218 | | | |
Table 3. Continued. |
EST-SSR | Putative protein | Putative fucntion | E-value | SSR motif | Primer sequence | Tm | EPS | PIC value | AN |
WMU14129 | No hits found | - | - | (TGG)5 | F: GGCGGAGCAGAGATGTTAAG | 59.978 | 232 | 0.753 | 5 |
| | | | | R: CCTTTTAAAACGCCCTGTGA | 60.103 | | | |
WMU14987 | No hits found | - | - | (CCT)5 | F: GGGATGAAACAAAACCACTGA | 59.822 | 187 | 0.746 | 5 |
| | | | | R: TGCAACAATGGAGAAGAGGA | 59.369 | | | |
WMU15045 | XP_002298266 | predicted protein [Populus trichocarpa] | 7E-16 | (TTCTCC)6 | F: GATGAAGCAGTCATCGCAAA | 59.955 | 280 | 0.850 | 11 |
| | | | | R: CCGTCGCTACTGCTCTGTAA | 59.245 | | | |
WMU15338 | ABV25901 | 3-hydroxy-3-methylglutaryl- coenzyme A reductase [Antirrhinum majus] | 1E-10 | (TCT)7 | F: TGCAATTTCAGCAGGACATC | 59.805 | 195 | 0.861 | 16 |
| | | | | R: ATTGATTCGAAAGTCACCGC | 60.081 | | | |
WMU15818 | XP_002265394 | predicted: hypothetical protein [Vitis vinifera] | 4E-17 | (AGA)5 | F: CATCGAAAAGTTCGACGACA | 59.84 | 129 | 0.100 | 2 |
| | | | | R: GTCATCCTTCTTCTCAGCCG | 59.95 | | | |
WMU16077 | No hits found | - | - | (GTC)5 | F: CTCCTCCATGTCGGAACTGT | 60.112 | 153 | 0.744 | 8 |
| | | | | R: AATCCTCCTCACAACGCATC | 60.081 | | | |
WMU16225 | No hits found | - | - | (GGA)5 | F: CAAAGTTTCAATGGCGGAAT | 59.938 | 175 | 0.370 | 3 |
| | | | | R: TTTCCACGACCACAACTCAA | 60.128 | | | |
WMU16230 | XP_002523973 | brg-1 associated factor, putative [Ricinus communis] | 1E-12 | (CCG)5 | F: GCTCTCTTAGCTCCGTCCAA | 59.717 | 207 | 0.760 | 7 |
| | | | | R: AGGAGAAACCTGGGTGACCT | 59.968 | | | |
WMU16339 | No hits found | - | - | (AT)6 | F: AACTGAATGCTCCCTGCATC | 60.226 | 261 | 0.853 | 10 |
| | | | | R: CAGGGACCAACCCTACAGAA | 59.959 | | | |
WMU16643 | XP_002521470 | RNA binding protein, putative [Ricinus communis] | 1E-15 | (GAG)5 | F: ATGATATGGGCATTGGCACT | 60.185 | 201 | 0.869 | 11 |
| | | | | R: GGACCTGGGACTTATCAGCA | 60.073 | | | |
WMU16698 | XP_002517624 | DNA binding protein, putative [Ricinus communis] | 3E-51 | (AT)11 | F: ATTGGAACTGCCCTCTTCCT | 60.074 | 258 | 0.861 | 11 |
| | | | | R: TCCCAAGTCCCATAAACAGC | 59.933 | | | |
WMU16703 | AAD47346 | ribosomal protein S26 [Pisum sativum] | 4E-22 | (TC)6 | F: GCATTTCCCACAAAACCCTA | 59.801 | 143 | 0.567 | 5 |
| | | | | R: AGCACCGGATGAACTTAACG | 60.132 | | | |
짝유사행렬(Pairwise Similarity Matrix) 및 계통도 (Dendrogram)
증폭된 384개 PCR 밴드와 Nei-Li similarity index를 이용하여 짝유사행렬(Pairwise similarity matrix)을 작성하였다(Table 4). 작성된 짝유사행렬에서 보여진 유사도의 범위는 0.10에서 0.84이었다. 가장 높은 유사도를 보인 것은 크림슨계 수박 품종인 ‘Charleston Gray’와 무지계 수박 품종인 ‘화보’로 0.84의 값을 나타내었으며, 반면에 가장 낮은 유사도를 보인 것은 대목계 호박 F1인 ‘흑종’과 무지계 수박 품종인 ‘화보’로 0.10의 값을 나타내었다.
Table 4. Pairwise similarity matrix of 24 accessions of Cucurbitaceous crops evaluated by using watermelon EST-SSRs. |
EN.z | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
1 | 1.0000 | | | | | | | | | | | | | | | | | | | | | | | |
2 | 0.4845 | 1.0000 | | | | | | | | | | | | | | | | | | | | | | |
3 | 0.4615 | 0.8000 | 1.0000 | | | | | | | | | | | | | | | | | | | | | |
4 | 0.4720 | 0.8235 | 0.8000 | 1.0000 | | | | | | | | | | | | | | | | | | | | |
5 | 0.4968 | 0.7831 | 0.7205 | 0.7590 | 1.0000 | | | | | | | | | | | | | | | | | | | |
6 | 0.4654 | 0.8452 | 0.7485 | 0.8214 | 0.7195 | 1.0000 | | | | | | | | | | | | | | | | | | |
7 | 0.4575 | 0.8025 | 0.7516 | 0.8025 | 0.7342 | 0.8000 | 1.0000 | | | | | | | | | | | | | | | | | |
8 | 0.5443 | 0.6467 | 0.5802 | 0.5749 | 0.6135 | 0.5697 | 0.5660 | 1.0000 | | | | | | | | | | | | | | | | |
9 | 0.6087 | 0.6471 | 0.5818 | 0.6000 | 0.6265 | 0.6071 | 0.6049 | 0.7904 | 1.0000 | | | | | | | | | | | | | | | |
10 | 0.1961 | 0.2222 | 0.2038 | 0.1852 | 0.2025 | 0.1625 | 0.1818 | 0.2138 | 0.2099 | 1.0000 | | | | | | | | | | | | | | |
11 | 0.2237 | 0.2236 | 0.2179 | 0.2236 | 0.2038 | 0.1635 | 0.1438 | 0.2152 | 0.2236 | 0.4183 | 1.0000 | | | | | | | | | | | | | |
12 | 0.2338 | 0.1963 | 0.2152 | 0.1963 | 0.2013 | 0.1491 | 0.1806 | 0.2250 | 0.2086 | 0.4129 | 0.4156 | 1.0000 | | | | | | | | | | | | |
13 | 0.2119 | 0.1500 | 0.1677 | 0.1625 | 0.1538 | 0.1013 | 0.1316 | 0.2038 | 0.2375 | 0.4211 | 0.3576 | 0.5098 | 1.0000 | | | | | | | | | | | |
14 | 0.2038 | 0.2892 | 0.2609 | 0.3012 | 0.2716 | 0.2317 | 0.2152 | 0.2822 | 0.2289 | 0.2278 | 0.2548 | 0.3019 | 0.2308 | 1.0000 | | | | | | | | | | |
15 | 0.1963 | 0.2674 | 0.2635 | 0.2558 | 0.2619 | 0.2235 | 0.2073 | 0.2722 | 0.2209 | 0.2073 | 0.2331 | 0.2303 | 0.1852 | 0.7024 | 1.0000 | | | | | | | | | |
16 | 0.2000 | 0.2642 | 0.2727 | 0.2642 | 0.2323 | 0.2420 | 0.2384 | 0.2692 | 0.2264 | 0.2384 | 0.2533 | 0.3026 | 0.2685 | 0.6839 | 0.5963 | 1.0000 | | | | | | | | |
17 | 0.2745 | 0.3086 | 0.3057 | 0.2716 | 0.3038 | 0.2625 | 0.2468 | 0.2893 | 0.3086 | 0.2727 | 0.2484 | 0.3355 | 0.2632 | 0.7089 | 0.6380 | 0.6755 | 1.0000 | | | | | | | |
18 | 0.2424 | 0.2874 | 0.3077 | 0.2874 | 0.3176 | 0.2674 | 0.2410 | 0.2924 | 0.2989 | 0.2651 | 0.3152 | 0.2275 | 0.2195 | 0.5765 | 0.5341 | 0.5890 | 0.6145 | 1.0000 | | | | | | |
19 | 0.2405 | 0.3114 | 0.2840 | 0.2635 | 0.2945 | 0.2909 | 0.2767 | 0.3171 | 0.2515 | 0.2893 | 0.2911 | 0.2500 | 0.2548 | 0.5644 | 0.5325 | 0.5641 | 0.5409 | 0.7135 | 1.0000 | | | | | |
20 | 0.2038 | 0.2651 | 0.2733 | 0.2892 | 0.2469 | 0.2683 | 0.2658 | 0.2577 | 0.2169 | 0.2405 | 0.2293 | 0.2390 | 0.1795 | 0.3704 | 0.3452 | 0.4000 | 0.4177 | 0.3647 | 0.3190 | 1.0000 | | | | |
21 | 0.2237 | 0.2981 | 0.3205 | 0.3354 | 0.2675 | 0.3145 | 0.2614 | 0.3038 | 0.2609 | 0.2222 | 0.2368 | 0.1818 | 0.1457 | 0.4331 | 0.3804 | 0.4000 | 0.4575 | 0.4000 | 0.3671 | 0.6752 | 1.0000 | | | |
22 | 0.2360 | 0.2824 | 0.2667 | 0.3294 | 0.2651 | 0.2857 | 0.2593 | 0.2994 | 0.3176 | 0.2716 | 0.3230 | 0.2945 | 0.2375 | 0.4217 | 0.3721 | 0.3899 | 0.4198 | 0.4253 | 0.3952 | 0.5783 | 0.6957 | 1.0000 | | |
23 | 0.2436 | 0.2909 | 0.3250 | 0.3294 | 0.2733 | 0.2945 | 0.2675 | 0.2840 | 0.2545 | 0.2675 | 0.2821 | 0.2911 | 0.2323 | 0.3975 | 0.3234 | 0.4026 | 0.4459 | 0.3669 | 0.3333 | 0.5839 | 0.6667 | 0.6424 | 1.0000 | |
24 | 0.2128 | 0.2667 | 0.2483 | 0.2400 | 0.2466 | 0.2297 | 0.2394 | 0.2177 | 0.2133 | 0.2676 | 0.2979 | 0.2657 | 0.2286 | 0.3151 | 0.3026 | 0.3022 | 0.3239 | 0.3247 | 0.3265 | 0.5068 | 0.5248 | 0.5467 | 0.5241 | 1.0000 |
zEN, Entry number of 24 accessions of Cucurbitaceous crops shown in Table 2. |
짝유사행렬을 토대로 UPGMA를 통해 계통도(dendrogram)를 분석한 결과, 유사도 0.23에서 크게 2개의 clade(Clade I 과 Clade II)로 구분되었다. Clade I에는 수박, 멜론, 오이의 모든 품종들이 군을 이루었으며, Clade II에는 호박의 모든 품종들이 군을 이루었다. 이는 박과의 족(tribe)에 따른 분류와 일치한다고 볼 수 있는데, 박과(Cucurbitaceae)는 Benincaseae, Cucurbiteae, Sycyeae, Momodiceae의 4가지 족으로 이루어져 있으며 그 중 수박, 멜론, 오이는 Benincaseae 족, 호박은 Cucurbiteae 족에 속하는 작물이다(Schaefer et al., 2009).
Clade I는 다시 0.27의 유사도에서 2개의 clade(Clade I-1, Clade I-2)로 구분되었는데, Clade I-1은 수박(Citrullus lanatus L.), I-2는 오리엔탈 멜론(참외)를 포함한 멜론(Cucumis melo L.)과 오이(Cucumis sativus L.)의 모든 품종이 군을 이루었다. Clade I-1은 유사도 0.50에서 다시 수박 대목용 야생종 품종인 ‘공대’가 I-1a, 그 외 8개 품종이 I-1b의 독립된 군으로 구분되었다. I-1b는 유사도 0.61에서 다시 두 개의 clade (Clade I-1b-1와 I-1b-2)로 재배종과 야생종 품종이 구분되었는데 clade I-1b-1에는 모두 재배종(Citrullus lanatus var. vulgaris Schrad.)인 6개 품종(‘Charleston Gray’, ‘Augusta’, ‘오렌지킹’, ‘Vasko’, ‘화보’, ‘스피드’)이 위치하였으며, 유사도 범위는 0.72-0.85로서 ‘Charleston gray’계 품종인 ‘Charleston Gray’와 무지계 품종인 ‘화보’가 0.85의 유사도로 가장 가까웠으며, 반면에 무지계 품종 ‘화보’와 크림슨계 품종 ‘Vasko’는 0.72의 유사도로 가장 멀었다. Clade I-1b-2는 야생종(Citrullus lanatus var. citroides Mats. & Nakai.)에 속하는 2 계통(PI189225, PI494817)이 위치하였으며 유사도는 0.79 였다. C. lanathus var. vulgaris(Clade I-1b-1)는 전 세계적으로 분포하는 재배종 수박이나, C. lanatus var. citroides(Clade I-1b-2)는 주로 남아프리카에 분포하는 야생종으로 분류된다. 과의 특성 또한 차이가 나는데 C. lanathus var. vulgaris는 적색이고 단맛의 과육을 가지는 반면 C. lanatus var. citroides는 흰색 또는 녹색의 과육색을 지니며 당도함량과 풍미 또한 다양하게 분포되어 있다. 또한 I-1b-1의 품종들이 비교적 유사도 범위가 좁고 평균 유사도가 높은 것은 재배종 수박들로서 비교적 좁은 유전적 배경과 제한된 유전적 다양성을 지니고 있기 때문으로 판단된다. 반면에, I-1a와 I-1b-2의 품종들간 유사도는 개체간 유전적 다양성 및 특성형질의 차이가 재배종에서보다 야생종에서 보다 클 것이라는 예상을 뒷받침 해 주고 있으며, 특히 C. lanatus var. citroides의 재료로 쓰인 PI189225는 탄저병(anthracnose)의 race 2와 덩굴마름병(gummy stem blight)에 저항성을 보이는 재료이며(Levi et al., 2001) PI494817은 과실썩음병(bacterial fruit blotch)의 저항성 보이는 재료로서(Hopkins et al., 2008) 병 저항성 육종의 소재로서 이용될 수 있다.
Clade I-2의 멜론과 오이는 모두 Cucumis 속의 종들이며, 오이(Cucumis sativus L., 2n = 2x = 14)는 멜론(C. melo L.) (2n = 2x = 24)과 같이 24개 염색체를 가지는 조상 종으로부터 진화하는 과정에서 염색체 융합(chromosome fusion)을 통하여 분화된 종으로 알려져 있다(Li et al., 2011). 멜론과 오이의 비교 유전자지도와 총 게놈 염기서열을 비교한 연구에서 오이의 염색체가 멜론의 염색체 위에 조각으로 산재하거나 혹은 온전하게 보전되어 있음을 보고한 바 있다(Li et al., 2011). 이와 같이 오이와 멜론은 수박과 호박 등 타 종에 비하여 유전적으로 매우 유사한 종임을 본 연구에서도 확인할 수 있었다. 멜론과 오이 품종군은 유사도 0.37에서 두 개의 독립된 군으로 나누어졌으며, 멜론군(I-2a)은 다시 유사도 0.57에서 일반 멜론(Cucumis melo var. cantalupensis) (I-2a-1)과 오리엔탈 멜론(참외, Cucumis melo var. conomon) (I-2a-1)으로 구분되었다. Silberstein 등(Yi et al., 2006)은 14개의 멜론 종을 RAPD와 RFLP를 이용하여 분석한 결과 멜론과 참외가 다른 집단을 이룬다는 결과를 보였으며, Lee 등(Lee et al., 2003)도 RAPD를 이용하여 50종의 멜론 종의 유연관계를 분석한 결과 참외와 멜론의 유전적 차이가 있다는 것을 보였다. 일반 멜론 품종군(I-2a-1)에는 ‘Earl’s Elite’, ‘Charentise’, JC-23, JC-24이 속하였는데, 얼스엘리트계 F1 품종 ‘얼스엘리트’와 녹육계 계통 JC-24가 0.71의 유사도를 나타내어 가장 높은 유사도를 보였으며 JC-24와 유럽계 품종 ‘Charentise’가 0.64으로 가장 낮은 유사도를 보였다. 오리엔탈 멜론군(I-2a-2)에서는 ‘금싸라기’, ‘성환참외’가 0.71의 유사도로 그룹을 이루었다. 오이(Cucumis sativus L.) 품종들로 구성된 하위그룹 I-2b에는 ‘장형낙합’, ‘강력삼척’, ‘강호백침’, ‘다이너시티’, ‘마샤’의 5개의 품종이 속하였으며 이 중 가시오이계 품종인 ‘강력삼척’과 반백다다기계 품종인 ‘강호백침’이 0.70로 가장 높은 유사도를 보였고 취청계 품종인 ‘장형낙합’과 피클용 품종인 ‘마샤’가 0.51로 가장 낮은 유사도를 보였다.
Clade II는 ‘농우조생풋’[Cucurbita moschata(Duch. ex Lam.) Duch. & Poir.], ‘단밤’(Cucurbita maxima Duch.), ‘태양쥬키니’(Cucurbita pepo L.), ‘흑종’(Cucurbita ficifolia Bouche.)로 구성되었으며 동양계 품종인 ‘농우조생풋’과 서양계 품종인 ‘단밤’이 0.42의 유사도를 보이며 하위그룹 II-1을 이루었고 쥬키니계 품종인 ‘태양쥬키니’와 대목계 품종인 ‘흑종’이 0.51의 유사도를 보이며 하위그룹 II-2를 이루었다. C. moschata, C. pepo, C. maxima는 중생식물(mesophytic)의 일년생식물로 알려져 있으며, C. ficifolia는 중생식물이며 다년생 식물로 알려져 있다(Bisognin, 2002). 이와 같은 생물학적 분류로 미루어 볼 때 C. moschata, C. pepo, C. maxima와 C. ficifolia가 유전적 거리가 동떨어지게 그룹 지어질 것으로 예상하였지만 결과는 다르게 나왔다. 또한 Sanjur 등(Schaefer et al., 2009)의 실험에 따르면 미토콘드리아의 nad I 탈수소효소 유전자의 exon B와 C 사이에 있는 intron 2 지역을 이용하여 65개의 호박 종간의 유연관계를 분석한 결과 C. moschata와 C. pepo가 가장 가까운 거리를 나타내었으며 그 다음으로 C. maxima가 가까운 거리를 보이며, 가장 먼 거리를 나타낸 것은 C. ficifolia였다. 이러한 결과는 본 연구에서 보여지는 유연관계와 차이가 있다. 이는 실험에 사용된 수박 EST-SSR primer set의 수가 Cucurbiteae 족에 속하는 호박을 명확히 분류하기에 충분치 못하였거나, 사용된 시료가 계통이 아닌 품종으로서 품종 개발 시 종간교잡 등을 통해 유전적 특성의 조합이 일어났기 때문일 수 있다.
이상의 결과를 통하여 수박 EST-SSR 마커들이 타 박과 종의 유전체 및 마커 개발 연구분야에 적용될 수 있음을 확인하였다. 특히 이들 마커를 이용한 유연관계 분석 결과가 Cucurbiteae 족의 호박을 제외한 Benincaseae 족에서 기존의 종명법에 따른 분류법과 종간 유연관계와 일치한다는 사실은 선발된 수박 EST-SSR 마커들이 타 박과 작물의 유전적 다양성 분석뿐만 아니라 유전자 지도 작성 및 박과작물 간 비교유전체 분석에 활용 가치가 있음을 보여준다. 또한 육종분야에 있어서도 다양한 박과작물의 형질선발용 분자마커 개발 및 F1 순도검정과 품종식별 마커개발(Choi et al., 2012)에 활용이 가능할 것으로 기대된다.
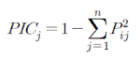
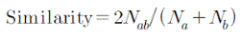
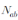 는 두 개의 유전자형에 공통으로 나타나는 단편의 수를 뜻하며
는 두 개의 유전자형에 공통으로 나타나는 단편의 수를 뜻하며 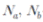 는 각각의 유전자형에서 나타나는 단편의 총 개수를 의미한다. 군집분석(cluster analysis)은 Nei-Li similarity 값을 기반으로 비가중 산술 결합법(UPGMA, unweighted pair group method on arithmetic averages) 방법을 이용하여 분석하였다. 모든 통계 분석에는 NTSYS-PC version 2.02k (Rohlf, 2002)를 이용하였다.
는 각각의 유전자형에서 나타나는 단편의 총 개수를 의미한다. 군집분석(cluster analysis)은 Nei-Li similarity 값을 기반으로 비가중 산술 결합법(UPGMA, unweighted pair group method on arithmetic averages) 방법을 이용하여 분석하였다. 모든 통계 분석에는 NTSYS-PC version 2.02k (Rohlf, 2002)를 이용하였다.



