서 언
재료 및 방법
과실의 종류, 품종 및 실험구 배치
하우스의 온도관리 및 재배조건
과실의 가용성 고형분 측정 및 시료 전처리
총 페놀화합물 분석
DPPH 활성산소 소거활성 검정
총 flavonoid 분석
Mangiferin 분석
결과 및 고찰
서 언
최근에 우리의 삶에 있어 건강지향이 높아지면서 식생활에 대한 관심이 높아짐과 동시에 청과물이 갖고 있는 항산화 기능에 주목을 하고 있다. 특히, 과실류에는 암, 관절염, 심장병, 염증, 뇌기능장애, 노화촉진과 같은 증상완화를 돋는 항산화 물질이 풍부하다F(eskanich et al., 2000; Gordon, 1996; Halliwell., 1996).
많은 열대과수에서 각기 다른 방법으로 항산화 물질 및 활성에 대해 조사되어 왔다(Jimenez-Escrig et al., 2001; Leong and Shui, 2002; Someya et al., 2002). 특히, 말레이시아의 Meiean and Mohamed(2001)은 시식용 열대식물에 대해 flavonoid 함량을 조사했다. Suda et al.(2005)은 오키나와산 과실류 및 채소류에 대해 polyphenol 함량과 활성산소 소거활성(free radical scavenging activity)을 조사 한 바가 있는데 과실에 대한 1,1-diphenyl-2-picrylhydrazyl(DPPH) 활성 산소제거 능력을 조사한 결과, 열대원산인 sapoilla, sanistel, guava와 starfruit가 614.7, 57.4 및 17.0μmol(trolox equivalents·g·FW-1)순으로 나타냈다(Suda et al., 2005).
망고(Mangifera indica L.)는 옻나무(Anacardiaceae)과에서도 중요한 과실로 영양과 의료적인 면에서 가치가 높은 열대과실이다. 망고에는 여러 종류의 polyphenol 화합물 중에 mangiferin이 다량으로 함유되어 있다(Luo et al., 2012). 이 물질은 소염, 항당뇨, 면역 조절기능, 항종양, 항산화작용 등의 다양한 생물활성을 가지고 있는 식물성 화학물질이다(Carvalho et al., 2009; Dar et al., 2005; Guha et al., 1996; Muruganandan et al., 2005; Noratto et al., 2010; Rajendran et al., 2008).
제주도에서는 최근 지구온난화에 따른 기후변화 대응으로 비닐 하우스를 이용한 새로운 고소득 작물인 열대과수 재배에 대한 관심이 높아짐에 따라 망고가 재배되고 있다. 제주의 망고재배 농가에서는 생산량을 높이기 위해 가온 하우스 내 고수고 밀식 재배방법으로 착색과 품질이 문제시 되고 있는 반면에 오키나와 재배농가는 저수고 유인재배로 착색상태가 양호한 고품질 과실을 생산하고 있다. 또한 제주에 위치한 온난화 대응 농업연구소(IRCA)에서는 몇 년 전부터 오키나와의 저수고 유인재배를 도입해 시험재배를 행하고 있다.
따라서 본 논문에서는 망고 ‘Irwin’ 과실에 대한 품질 및 기능성을 비교 평가 하기 위해 IRCA, 제주 및 오키나와 농가에서 재배되는 망고를 대상으로 가용성 고형분, 총 페놀화합물, 활성산소 소거활성, 총 플라보노이드 함량과 mangiferin 성분의 변화 양상 등을 조사하였다.
재료 및 방법
과실의 종류, 품종 및 실험구 배치
공시품목과 품종은 Table 1에서 표시 한 바와 같이 제주 및 오키나와에서 재배가 되고 있는 망고 ‘Irwin’을 공시품목으로 이용했다. 실험구 배치는 나무 한 구루를 1반복으로 하우스 중앙부에 무작위로 6반복 구를 설정했다. 과실품질 및 기능성 성분을 분석하기 위해 나무 한 구루 당 상부, 중부 및 하부에 착과된 3개의 과실을 수확기에 18개를 채취했다. 채취한 시료는 과피와 과육으로 분류한 다음 각각에 대하여 과실품질 조사 및 기능성물질 분석에 이용했다.
Table 1. Mango fruit used in the present experiment
| |
zResearch Institute of Climate Change and Agriculture in Jeju | |
하우스의 온도관리 및 재배조건
제주에서 재배된 망고는 2013년 여름철에 IRCA에 저수고 유인재배로 유인된 과실 및 고수고 유인재배로 유인된 과실을 채취해 실험용 시료로 이용했다. 하우스의 가온 관리는 후기가온 재배로 1월초에 가온을 시작해 최저기온 20°C를 유지시켰다.
1월말부터 3월말까지 화아 분화기에는 최저기온을 10°C로 변화를 시켰고 그 후에 개화, 과실비대기 및 수확기인 4월 초부터 7월 말까지도 최저기온 20°C유지시켰다. 서귀포시에 위치한 농가하우스는 조기 가온 재배로 연구소보다 2개월 조기 가온을 시작해 5월 중순에 수확을 했다.
오키나와 농가에서 재배된 망고는 재배지역인 나고시에서 IRCA처럼 후기 가온재배 및 저수고 유인재배를 하였으며, 적과기에 병충해방제 및 안정된 착색을 위해 과실에 봉지 씌우기를 행했다. 수확은7월 말부터 8월 중순까지 하였다.
과실의 가용성 고형분 측정 및 시료 전처리
제주 및 오키나와에서 재배되는 망고 시료는 만개 후 약 100일째에 완전착색이 된 후 수확기에 과실을 채취한 다음 착즙하여 디지털 당도계(digital refractometer, PR-101, ATAGO, America)로 가용성 고형분 함량을 측정했다. 그 후에 과피 및 과육을 동결건조 하였으며, 제주산 건조시료는 국제우편을 통해 오키나와현 건강 바이오센터 내 오키나와 연구센터로 보내졌다. 또한 오키나와에서 생산된 과실시료도 오키나와 건강 바이오센터에서 동결건조를 행했다. 동결건조 된 시료는 분석하기 전까지 −20°C 냉동고에 보관하였다.
동결건조 시료를 mortar와 pestle 및 믹서기로 균질화 시킨 후에 50ml 튜브에 100mg의 시료를 칭량했다. 그 튜브에 80% 에탄올 20mL를 채우고 그 혼합물을 60°C의 항온수조에서 shaking을 하면서 하루 밤 동안 알코올 가용성물질을 추출을 행했다. 그 추출물을 여과를 시킨 후에 10mL씩 원심분리용 튜브에 분주를 했다. 분주된 10mL의 추출액을 40°C로 조정된 원심형 진공 농축기(miVac Duo LV system, England)로 완전히 건조될 때까지 농축을 시켰다 .
총 페놀화합물 분석
총 페놀화합물 함량은 Singleton과 Rossi(1965), Folin-ciocalteau 방법을 조금 변경해 분석을 행했다. 완전 건조된 알코올 추출물을 에탄올 2mL로 용해시킨 다음에 100μL의 시료액을 취한 후에 300μL 20% sodium carbonate와 50μL Folin-ciocalteau 를 넣고 15분간 실온에서 반응시킨 후에 1mL의 증류수를 첨가한 한 다음에 UV/Vis 분광광도계(Jasco V-570, Japan)로 725nm에서 흡광도를 측정했다. 총 페놀함량은 gallic acid를 이용해 검량선을 작성하여 GAE(gallic acid equivalents)로 표시했다.
DPPH 활성산소 소거활성 검정
각 시료의 에탄올 추출물의 전자 공여능은 Blois(1958)의 방법을 변형하여 검정하였다. Methanol 400μL를 농도별로 각각의 시료에 첨가한 후 0.15mM 1,1-diphenyl-2-picrylhydrazyl (DPPH) 100μL를 혼합하여 실온에서 30분간 안정화시킨 다음 UV/vis 분광광도계(Jasco V-570, Japan)로 517nm에서 흡광도를 측정하였다. Sample 첨가구와 무첨가구의 흡광도 차이를 백분율(%)로 표시하여 전자공여능을 측정하였으며, 아래와 같이 계산하였다.
EDA (%) = (1 - ABSsample/ABScontrol) × 100
ABSsample: Absorbance of the experimental sample
ABScontrol: Absorbance of the control
총 flavonoid 분석
총 flavonoid 함량은 Muhammad et al.(2011)의 방법을 변형하여 분석하였다. 완전 건조된 알코올 추출물을 에탄올 2mL로 용해한 다음 100μL를 취한 후에 300mL의 5% NaNO2 를 첨가한 후에 실온에서 10분간 방치했다. 그 후에 다시 300μL의 10% Al(NO3)3 넣고 10분간 실온에 두었다가 400μL의 1% NaOH를 첨가해 30분간 실온에서 발색을 시키고 UV/Vis 분광광도계 (Jasco V-570, Japan)로 500nm에서 흡광도를 측정하였다. 총 flavonoid 함량은 catechin을 이용해 검량선을 작성하여 계산하였다.
Mangiferin 분석
동결건조 된 과육 및 과피의 시료를 분쇄기로 균질화 시켰다. 균질화 시킨 시료 2g을 추출 플라스크에 넣은 후 85% Methanol 300mL을 가하여 85°C에서 5시간 동안 환류 냉각장치를 부착하여 추출하였다. 추출액을 정용한 다음 0.1% formic acid을 함유하는 85% 메탄올로 적정 분석범위에 알맞도록 조절한 후 0.2μm membrane filter(Ministart RC 15, Satrius stedim, Germany) 로 여과시켜 기기분석용 검액을 조제하였다.
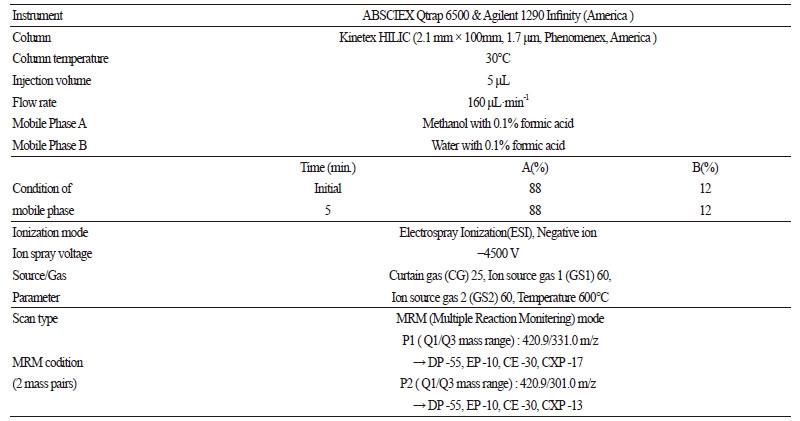
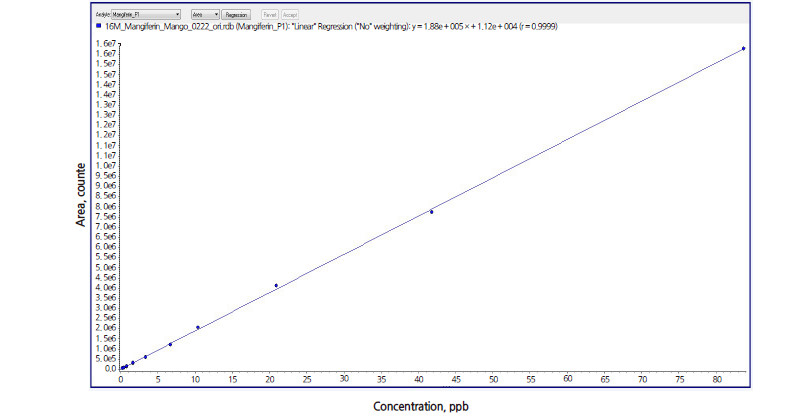
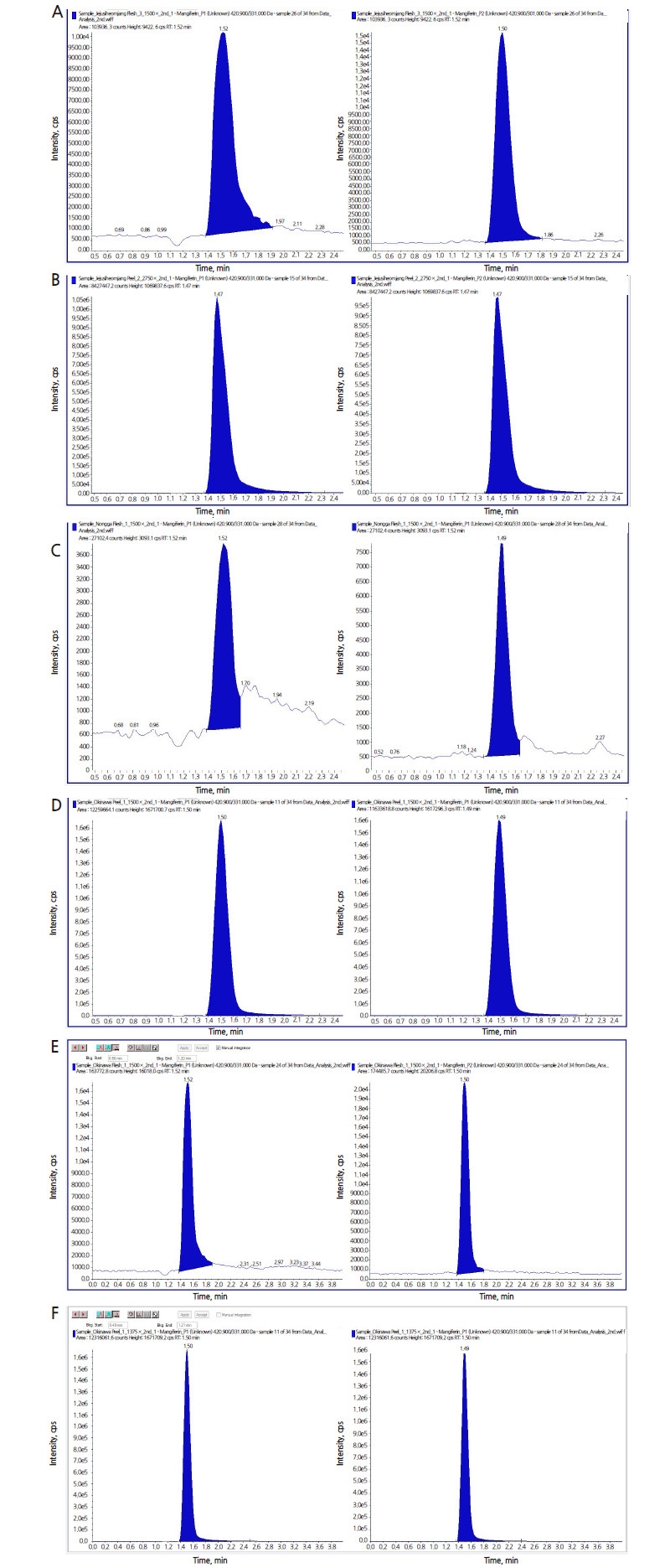
정밀 여과시킨 시료 검액을 액체질량분석기(UPLC-MS/MS, Agilent 1290 Infinity, UPLC/AB Sciex Qtrap 6500, Triple Quadrupole Mass Spectrometry, America)를 사용하여 Table 2의 분석조건에서 정성적 확인과 외부표준 물질법으로 Fig. 1과 같이 P2(Q1/Q3, 420.9/301.0 m/z) chromatogram의 peak면적과 mangiferin 표준용액의 농도를 기준하여 검량선(calibration curve)을 작성하여 mangiferin 함량을 정량 하였다. 또한, ESI(Electrospry Ionization)법으로 이온화하여 negative mode에서 mangiferin의 질량스펙트럼(mass spectrum)을 토대로 Table 2의 multiple reaction monitoring(MRM) mode의 모분자(precusor ion, Q1)와 딸분자(product ion, Q3)의 이온쌍을 설정한 다음 분석하였다. mangiferin 표준용액은 0.1% formic acid을 함유하는 85% 메탄올로 0.2-83.7μg·L-1 수준이 되도록 조제하였다. 그리고 대표적인 시료의 mangiferin 성분의 질량 크로마토크램을 Fig. 3에 나타내었다. Mangiferin 표준품은 Wako(Japan)에서 메탄올은 Burdick & Jackson에서 formic acid 등 분석 시약은 Sigma-Aldrich(St. Louis, Mo, USA)에서 구입하여 사용하였다.
결과 및 고찰
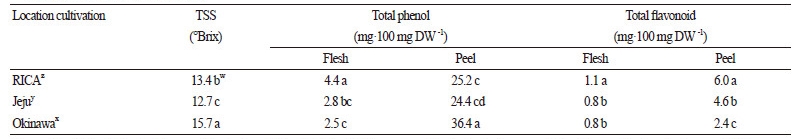
제주산 및 오키나와산 망고 ‘Irwin’에 대한 과실 수확기에 있어 가용성 고형분, 총 페놀함량, 활성산소 소거능 및 총 flavonoid 함량을 분석하여 Table 3에 나타냈다. 가용성 고형분 함량은 제주산에 있어 저수고 유인재배를 하고 있는 IRCA 하우스와 고수고 유인재배를 하는 농가와 비교해 보았으며, 또한 저수고 유인재배는 하는 오키나와의 농가와도 비교를 했다. 제주산에서 는 IRCA 하우스와 농가와도 차이가 있으며, 또한 IRCA 하우스 보다 오키나와 농가 하우스가 그 함량이 높았다. 총 페놀함량은 과육과 과피의 그 함량이 비슷한 값을 나타냈으며 과육에서 IRCA가 높은 값을 보였으나 과피에서는 오키나와산이 높은 값을 보였다.
총 flavonoid 함량은 과피가 과육보다 높은 함량을 나타냈다. 과육에 있어 IRCA가 제주산 및 오키나와산보다 높은 함량을 보였으며, 과피에서도 제주산이 오키나와산보다 그 함량이 높았다 .
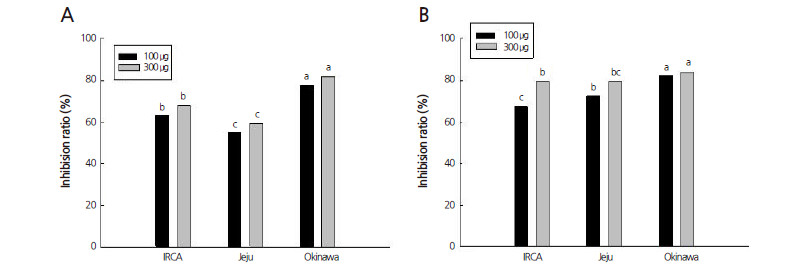
활성산소 소거능 비교는 건물시료 과육 및 과피(100μg과 300μg)에 대한 DPPH 활성산소 소거능력을 비교해서 Fig. 2에 나타냈다. 과육의 시료함량에 관계없이 유의적인 차이를 나타냈는데 오키나와산이 제주산보다 높았으며, IRCA가 제주 농가보다 높은 활성을 보였다. 한편, 과피에서도 시료함량에 따른 차이는 없었으나, 시료함량이 높은 쪽이 높은 활성을 보였으며, 과육과 비슷한 활성을 보였다.
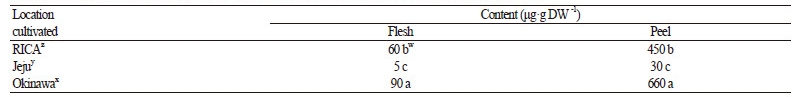
Fig. 3에 mangiferin에 대한 정량 및 정성분석을 위해 제주산 및 오키나와산 mango 과육과 과피에 대한 UPLC-ESI-MS/MS로 분석된 P1과 P2의 mass chromatogram을 그림 왼쪽과 오른쪽에 표시했다. 시료의 P1과 P2의 peak가 표준용액과 동일시간대(retention time)에 나타났으며, 또한 그 비율(P1/P2 ratio)이 같은 패턴을 보여 이들 peak가 mangiferin peak임이 확인 되었다. 감도가 높은 P2 chromatogram의 면적으로 그 함량을 정량하였다. 그 함량을 Table 4에 건물 중 1g 당 함유된 량을 μg단위로 나타냈다. 오키나와산이 과육은 90μg으로 제주산보다 그 함량이 많았으며, 제주산에서는 IRCA 하우스가 60μg으로 농가하우스 5μg 보다 높았다. 또한, 과피는 각각 660, 450 및 30μg으로 과피가 과육보다 그 함량이 높았다. Luo et al.(2012)은 중국 망고 11 품종에 대한 mangiferin 함량을 분석했는데 과육이 2-200μg, 과피는 40μg-7.49mg으로 보고했으며, 또한, mangiferin 이 L-ascorbic acid와 trolox보다 DPPH 활성산소 소거능력이 강하다고 하였다.
Phenol 화합물은 많은 식물에서 항산화 물질로 중요한 위치를 차지하고 있다. Mahattanatawee et al.(2006)은 Florida에서 재배된 열대과수에 대한 총 페놀함량을 조사한 바가 있는데 생과실을 1g 당 함량으로 나타낸‘Keitt’ 망고는 0.5mg이었는데 건물중으로 환산하면 5mg으로 오키나와산보다 2.5mg이나 높았다. 그것은 열대와 아열대 기후에 따른 차이라고 생각이 되었다. Suda et al.(2005)도 또한 오키나와산 망고의 과육과 과피의 총 페놀함량을 조사했는데 우리 조사한 함량과 비슷한 함량을 보였다. 항산화 활성에 대해 주로 DPPH free radical 소거법으로 조사를 했는데 Mahattanatawee et al.(2006)은 열대 과수류와 총 phenol함량과 항산화 활성간에 상관관계를 보고 한 바가 있다. 본 실험에서 조사 된 항산화 활성은 Mahattanatawee et al.(2006)의 보고와는 달리 그 함량이 대부분은 높을수록 항산화 활성이 높았으나 일부는 일치하지 않은 것도 있었다. Kondo et al.(2002)은 사과품종 별 과실생장에 따른 과육과 과피의 에탄올 추출물에 대해 superoxide(O2-)와 DPPH free radical 소거법에 의한 항산화 활성을 조사한 바가 있다. 생체중당 과피의 그 함량이 과실 성숙기에 3배나 감소했지만 그 농도는 수화기의 과육에 비해 항산화 활성은 3-8배나 높았다. 항산화 활성은 생육초기부터 수확기 전까지는 거의 비슷해 과실의 항산화 활성은 특정의 polyphenol 농도에 의해 유지가 가능한 것으로 고찰을 했다. Häkkinen et al.(1999)은 19종의 소과류의 과실에 대한 선택된 flavonoid류와 phenolic acid류에 대해서 스크린을 한적이 있다. 본 실험에서도 열대 과수류의 항산화 활성에 연관된 mangiferin 함량을 분석감도와 특이성이 뛰어난 액체 질량분석기로 정량분석을 했다. 항산화 활성이 높았던 오키나와산은 과육과 과피에서 총 flavonoid 함량은 낮은 반면에 액체 질량분석기로 정량된 mangiferin 함량은 제주산보다 높았다. Häkkinen et al.(1999)도 강한 항산화 활성을 갖고 있는 소과류의 총 phenol 함량 중에 품목에 따라서 flavonoid와 phenolic acid류의 조성이 다르다고 보고했다. 그러므로 항산화 활성에는 flavonoid류의 물질보다 강력한 항산화 물질이 관여한다고 사료되었다.
본 실험에서 오키나와 후기 가온 하우스재배 농가의 ‘Irwin’ 망고와 똑같이 저 수고 유인을 하는 IRCA와 조기 가온 하우스 재배에 고수고 유인을 하는 제주농가보다 가용성고형물 함량도 많았으며, 또한, 과육과 과피의 항산화 활성이 높게 나타났다. 과실품질 및 항산화 활성이라는 기능성의 차이를 재배환경적인 측면에서 생각을 해보았다. Oe et al.(2014)은 매실 ‘남고’에 대한 홍색의 착색요인과 매실주에 미치는 영향에 대한 연구에서 자외선 제거구가 무처리에 비해 항산화 활성이 낮게 나났타다.
Simizu et al.(2005)은 복숭아 ‘Akatsuki’의 고당도 과실생산 요인에 대해 수관내의 상대조도가 높은 과수원일수록 과실의 당도가 높았다. 본 실험에도 저수고유인 재배를 하고 있는 IRCA와 오키나와 농가가 고수고 유인재배의 제주농가보다 과실의 당도가 높은 것은 저수고 유인인 경우 수관내의 상대조도에 의한 것으로 사료가 되었다.