서 언
재료 및 방법
식물재료
실험기간과 육묘환경
매개변수 평가
광화학 지수 측정
통계처리
결과 및 고찰
식물체 크기, 무게, 엽록소 수치, 엽색 분석
식생지수와 엽록소 형광 매개변수 분석
서 언
채소는 수분, 미네랄, 항산화 성분 및 식물성 화합물(phytochemical)이 풍부하며(Lampe, 1999; Slavin and Lloyd, 2012; Jideani et al., 2021), 현대인의 건강증진을 위해 채소가 포함된 식사가 권장된다. 건강한 삶에 대한 욕구가 증가함에 따라 건강식품 소비가 증가하고 있으며 기능성 건강식품산업에 대한 수요도 확대되고 있다(Woo et al., 2017; Choi et al., 2022). 이에 따라 인위적으로 합성된 물질에 비해 천연색소나 폴리페놀, 미네랄, 비타민 등 식물성 유래 성분에 대한 수요는 지속적으로 늘어나고 있는 추세다(Han et al., 2004; Rho et al., 2013; Kim et al., 2020; Choi et al., 2022).
치커리(Cichorium intybus)는 국화과(Asteraceae)에 속한 엽채소류의 일종으로, 지중해, 중앙아시아, 북아프리카에서 기원한 것으로 알려져 있다(Wang and Cui, 2011). 역사적으로 치커리는 약 4000년 전부터 그리스인과 로마인들로부터 채소작물로 이용되었으며(Plmuier, 1972; Muñoz, 2004), 고대 이집트인들에 의해 채소작물, 약용식물, 동물사료 등의 목적으로 재배되었다(Grieve, 1971; Plmuier, 1972; Muñoz, 2004).
기능성 측면에서 치커리는 항염증(Ripoll et al., 2007), 항미생물(Tursunay et al., 2009), 항바이러스(Ni et al., 2005; Ren et al., 2008), 항노화(Qi et al., 2008), 항암(Pool-Zobel, 2006) 등에 효과가 있는 것으로 보고되었다. 치커리는 에스쿨레틴(esculetin), 치커린(cichoriin), 락투코피크린(lactucopicrin)이 풍부하여 간을 해독하고 담낭을 조절하며 피로를 완화시키는데 도움을 주는 것으로 나타났다(Wang and Cui, 2009a, 2009b). 그뿐만 아니라 치커리는 미네랄과 아미노산 함량이 풍부하여 건강관리에 도움을 줄 수 있으며(Yin et al., 2008), 치커리에 포함된 다량의 식이섬유는 장 기능을 개선시키고 배변활동을 원활히 할 수 있도록 도움을 주는 것으로 알려져있다(Shin et al., 2014). 이처럼 치커리는 제약산업 및 건강기능식품산업에서의 활용 가능성이 열려있으며 수요가 높은 것이 특징이다(Mona et al., 2009; Perović et al., 2021).
폐쇄형 육묘시설은 개방형 온실이나 개방형 식물공장에 비해 병해충의 유입을 쉽게 차단할 수 있다(Jemai et al., 2022). 시간이 지나 오래된 비닐하우스, 온실, 개방형 식물공장은 햇빛에 의한 구조물의 부식, 누수, 노후화 등의 문제가 발생하기 쉬운데, 폐쇄형 시설의 경우 일사량이 통제되기 때문에 시설 내부 구조물의 수명이 개방형 시설에 비해 상대적으로 길고, 온실 내부의 온도, 습도, 이산화탄소 농도 조절이 용이하고 에너지가 절약이 쉬우며 동시에 작물의 생산 및 품질제어 측면에서 유리하다(Al-Jamal, 1994; Gale, 1981; Jemai et al., 2022). 그러나 폐쇄형 육묘시설은 닫혀 있는 공간이라는 점에서 열 발생량이 상대적으로 많은 고압나트륨등이나 할로겐등의 사용이 어렵기 때문에 주로 발광 다이오드(light-emitting diode, LED)와 같이 열 발생량이 낮고 에너지 효율이 높은 인공광원이 사용되고 있다(Tadahisa et al., 2004; Kozai, 2007).
LED는 광질의 조절이 쉽기 때문에 분광분포를 달리하여 채소의 품질을 높이는 용도로 사용되고 있다(Choi et al., 2013). 과거 연구에서 육묘시설에서 청색 LED를 조사할 때 적색 LED에 비해 오이와 토마토 묘의 엽록소 수치와 건물중을 저하시킨다고 보고하였으며(Kim et al., 2008), 접목된 토마토는 적색 파장을 기반으로 청색 파장을 10% 혼합 조사할 경우 묘의 저장성이 증대된다는 보고가 있었다(Fujiwara et al., 2003). 한편, 과거 백색광 LED를 활용한 연구에서는 백색 LED의 색온도에 따라 다육식물의 생장수준이 유의미하게 변화하였다는 보고도 있었다(Kim et al., 2022; Lee and Nam, 2022; Lee et al., 2022b). 이처럼 식물과 LED의 종류에 따라 상이한 결과를 나타내기 때문에 식물 종 별로 생육에 적합한 LED 광질을 찾는 것은 중요한 과제다. 치커리 재배실험의 경우 적색과 청색 LED를 활용한 다양한 연구들이 수행되었으나(Pennisi et al., 2019; Montefiori et al., 2021; Orlando et al., 2022), 백색 LED를 활용한 연구는 아직 제한적인 실정이다.
분광분포의 차이는 식물의 생육과 대사작용 그리고 광화학 반응에 다양한 영향을 미치는 것으로 알려져 있다(Seo et al., 2022; Guo et al., 2023; Shang et al., 2023). 이때, 엽록소 형광(chlorophyll fluorescence) 분석기법을 통해 비파괴적인 방법으로 식물의 광화학적 생리상태를 손 쉽게 평가할 수 있으며(Park et al., 2023), 이 분석기법은 과거 여러 연구들을 통해 다각도로 적용되어 왔다(Lee and Kim, 2022; Yang et al., 2022; Yoon et al., 2022; Kang et al., 2023; Zheng et al., 2023).
이에 본 연구에서는 폐쇄형 육묘시설에서 치커리의 재배생산 품질을 향상시키기 위해 백색 LED를 포함한 다양한 분광분포를 나타내는 일곱 가지 LED를 적용하였으며, LED 광질의 영향을 받은 치커리묘의 생육과 식생지수 및 광합성에 대한 다양한 기초자료를 제시하였다.
재료 및 방법
식물재료
폐쇄형 육묘시설에서 LED 광질의 영향을 받은 치커리묘의 생육과 식생지수 및 광합성 수준을 조사하기 위해 종묘회사(Asia Seed, South Korea)로부터 ‘아시아슈가’(Cichorium intybus cv. Asia Sugar)와 ‘로사이탈리아나’(C. intybus cv. Rossa Italiana) 품종의 종자를 구입해서 사용하였다. 이때, 배지는 원예용 유비상토(Hanareumsangto, Shinsung Mineral, South Korea)를 사용하였다. 종자는 가로 × 세로 × 높이의 길이가 각각 6.5 × 6.5 × 6.5cm인 화분에 3립씩 파종하였다. 파종된 종자는 25% 차광수준과 평균온도와 상대습도가 각각 21.3 ± 3.4°C, 54.7 ± 14.7%인 실험온실에서 발아할 때까지 관리되었다. 종자가 발아된 후 첫 번째 본엽이 완전히 전개되기 직전에 하나의 묘만 남기고 모두 솎아내었으며, 직후 폐쇄형 육묘시설에 배치하였다.
실험기간과 육묘환경
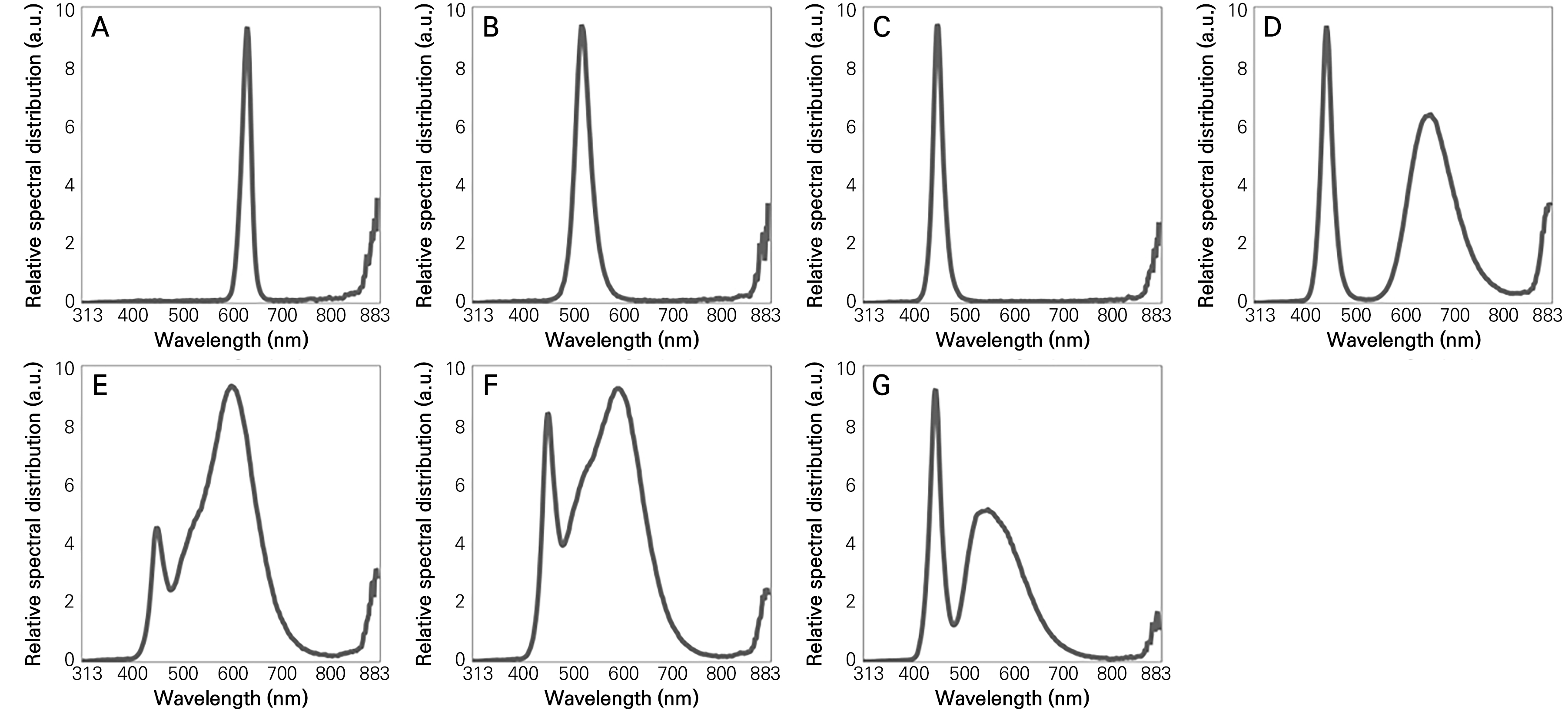
실험은 총 30일 동안 서울특별시 노원구에 위치한 삼육대학교 환경원예학과 실험온실 뒷편에 위치해 있는 가로 × 세로 × 높이가 각각 6.4 × 5.2 × 2.4m 크기인 폐쇄형 육묘시설(37°38′41″N 127°06′24″E )에서 수행되었다. 발광 다이오드(light-emitting diode; LED)(T5 LED, Zhong Shan Jinsung Electronic, China)는 적색(630nm), 녹색(520nm), 청색(450nm)의 단색광 LED, 보라색(450, 650nm)을 띄는 복합광 LED 그리고 각각 3000(455, 600nm), 4100(455, 590nm), 6500K(450, 545nm)의 색온도를 나타내는 백색 LED를 적용하였다(Fig. 1 and Table 1). 이때, 보라색 LED는 적색 LED와 청색 LED가 혼합 배치된 것이 아닌, 개별 다이오드에서 보라색의 복합 분광분포를 나타내었으며, 추가적으로 적외선 파장이 일부 포함되어 있었다. 실험에 사용된 LED는 1.2m의 크기, 20W의 소비전력을 나타내었으며, 명기와 암기는 각각 14시간과 10시간으로 설정하였다. 광도는 휴대용 분광복사계(SpectraPen mini, Photon Systems Instruments, Czech Republic)를 활용하여 350–800nm 범위의 광량자속밀도(photon flux density, PFD)가 총 100µmol·m-2·s-1이 되도록 식물과 LED 사이의 거리를 조절하였다. 각 처리구가 배치된 구간 사이에 광의 교섭을 방지하기 위해 흑색 폴리에틸렌 암막을 설치하였다. 온도는 20 ± 1°C로 냉난방장치를 이용하여 일정하게 유지시켰으며, 상대습도는 48.3 ± 11.8%였다. 관수는 매주 1회 저면관수 하였다. 이때 관수는 침전필터(sediment filter), 프리카본필터(free carbon filter), UF멤브레인필터(UF membrane filter), 포스트카본필터(post carbon filter)의 네 단계 정수처리를 거친 물을 사용하였으며, 실험 3주차에는 정수처리한 물로 저면관수 하는 대신 양액관주용 제4종 복합비료(High Grade S, HYPONeX, Japan) 희석액 1000ppm을 저면관수 방식으로 급비 하였다.
Table 1.
Photon flux density (PFD) and photosynthetically active radiation (PAR) of monochromatic, composite, and white light-emitting diodes (LEDs)
매개변수 평가
LED 광질의 영향을 받은 치커리묘의 생육과 식생지수 및 광합성 수준을 알아보기 위해 생육 매개변수인 초장, 초폭, 줄기의 직경, 근장, 피복면적, 엽수, 엽장, 엽폭, 지상부와 지하부의 생체중과 건물중, 지상부와 지하부의 수분함량을 측정하였으며, 식생지수(vegetation indices)와 관련된 매개변수인 정규식생지수(normalized difference vegetation index, NDVI), 광화학 반사율지수(photochemical reflectance index, PRI), 수정된 엽록소 흡광량지수(modified chlorophyll absorption ratio index, MCARI)를 측정하였다. 추가로 치커리 묘의 광합성 수준과 엽록소 농도 및 엽색을 조사하기 위해 Fv/Fm, ΦDo, ABS/RC, DIo/RC, PIABS, 엽록소 수치(SPAD units) 및 CIELAB L*, a*, b* 값을 조사하였다. 이때, 식물체 크기의 측정은 Park et al. (2023)의 측정방식을 참조하였으며 다음과 같다. 초장은 지면으로부터 묘가 가장 높게 솟아있는 부분을 기준으로 측정하였으며, 초폭은 묘를 위에서 바라볼 때 가장 넓은 부분을 기준으로 측정하였다. 근장은 묘의 뿌리 중 가장 긴 뿌리를 기준으로 측정하였다. 정규식생지수(Rouse et al., 1973) (1), 광화학 반사율지수(Gamon et al., 1992; Gamon et al., 1997) (2), 수정된 엽록소 흡광량지수(Daughtry et al., 2000) (3)는 휴대용 식물생리지수 측정계(PolyPen RP410, Photon Systems Instruments, Czech Republic)를 활용해 측정하였으며 그 식은 다음과 같다.
엽록소 수치는 휴대용 엽록소계(SPAD-502Plus, Konica Minolta, Japan)를 활용하여 측정하였다. CIELAB 값의 측정은 Lee et al. (2022a)의 엽색 측정 방법을 참조하여 분광광도계(CM-2600d, Konica Minolta, Japan)를 CIELAB D65/10°로 설정한 뒤 정반사광(specular component included, SCI)이 포함된 CIELAB L*, a*, b* 값을 얻었다. 이때, 정규식생지수, 광화학 반사율지수, 수정된 엽록소 흡광량지수, 엽록소 수치, CIELAB L*, a*, b* 값은 공통적으로 치커리 묘의 엽 중앙부에서 엽맥이 지나지 않는 부분을 무작위로 선별하여 8회씩 총 3반복 측정하였다. 생체중은 식물을 세척하고 3시간 동안 밀폐된 공간에서 자연건조 시킨 후 측정하였으며, 건물중은 열풍건조기(HK-DO135F, HANKUK S&I, South Korea)를 이용하여 85°C로 12시간 동안 건조시킨 후 측정하였다. 추가적으로 생체중과 건물중을 대조하여 수분함량을 대조하여 분석하였으며 그 식 (4)은 다음과 같다.
(는 수분함량, 는 생체중, 는 건물중을 나타낸다)
광화학 지수 측정
폐쇄형 육묘시설에서 LED 광질의 영향을 받은 치커리묘의 광화학 지수를 알아보기 위해 OJIP 엽록소 형광(OJIP chlorophyll fluorescence) 분석을 수행하였으며, 휴대용 엽록소 형광 측정기(FluorPen FP 110/D, Photon Systems Instruments, Czech Republic)를 사용하여 완전히 전개된 잎의 중앙부 중 엽맥이 지나지 않는 부분을 기준으로 측정하였다. 이때, 엽록소 형광지수를 측정하기 전에 제조사의 가이드라인에 따라 암적응용 리프클립(dark-adaptation leaf clips)을 활용하여 식물체를 약 15분간 암적응 시켰으며(PSI, 2023), 실험 종료일에 8회씩 총 3반복 측정하였다. 이때, 엽록소 형광의 측정은 휴대용 엽록소 형광 측정기를 455nm 파장으로 설정한 후 최대 형광단계인 Fm을 유도하기 위해 슈퍼펄스(super pulse)의 50% 강도인 1,500µmol·m-2·s-1 강도로 설정하였으며, 기기의 측정부를 암적응용 리프클립의 측정부에 관통시킨 뒤 광을 조사시켜 잎의 엽록소 형광 매개변수를 측정하였다. 여기서 식물의 스트레스 지표로 활용이 가능한 다섯 가지 형광 매개변수를 선정하여 분석하였다. 광계II의 최대 양자 수율(maximum quantum yield)을 나타내는 Fv/Fm (5), 흡수된 광자가 소멸될 확률(probability of photon dissipated)을 나타내는 ΦDo (6), 반응중심(reaction center, RC)당 흡광량(absorption flux)을 나타내는 ABS/RC (7), 반응중심당 소산되는 에너지의 양(dissipated energy flux)을 나타내는 DIo/RC (8), 흡광량 기준(absorption basis)의 성능지수(performance index, PI)를 타내는 PIABS (9)는 아래와 같은 수식을 사용하여 산출하였다(Stirbet and Govindjee, 2011; PSI, 2023).
통계처리
실험 결과의 분석은 SAS 9.4(SAS Institute, USA)를 사용하여 분산분석(ANOVA)을 수행하였다. 평균간 비교는 p < 0.05 수준의 던컨의 다중검정(Duncan’s multiple range test)으로 통계분석 하였다. 이때, 치커리 묘는 각 품종별로 8개체 3반복 완전임의배치법(completely randomized design)으로 배치하였다.
결과 및 고찰
식물체 크기, 무게, 엽록소 수치, 엽색 분석
폐쇄형 육묘시설에서 발광 다이오드(light-emitting diode, LED) 광질의 영향을 받은 두 치커리품종의 묘 크기 변화에서 다양한 결과를 나타내었다(Fig. 2 and Table 2). 결과에서 ‘아시아슈가’(Cichorium intybus cv. Asia Sugar)와 ‘로사이탈리아나’(C. intybus cv. Rossa Italiana) 묘의 초장은 각각 6500, 3000K 백색 LED 처리구에서 가장 높은 것으로 나타났다(각각 9.66, 14.23cm) 이때, ‘아시아슈가’의 초장은 단색광(monochromatic light) 처리구 내에서 적색 LED 처리구에 비해 상대적으로 청색 LED 처리구에서 낮았던 경향을 보였는데, 이는 광수용체인 크립토크롬(cryptochrome)이 청색 파장에 의해 자극될 때 브라시노스테로이드(brassinosteroids)나 옥신(auxin)의 분비를 감소시켜 식물의 줄기 신장을 억제시킨다고 보고된 결과와 유사하였다(Keuskamp et al., 2011; Song et al., 2019). 한편, 페튜니아(Petunia)는 청색 LED에 비해 적색 LED 하에서 약 60% 더 높은 초장을 나타내는 것으로 보고되었다(Fukuda et al., 2009). 초폭은 ‘아시아슈가’의 경우 던컨의 다중검정(Duncan’s multiple range test) 결과에서 3000, 4100K 백색 LED 처리구가 동등한 유의수준을 가지는 것으로 나타났으며(각각 16.86, 16.68cm), ‘로사이탈리아나’는 3000K 처리구에서 20.36cm로 가장 넓게 나타나 초폭의 증가율은 백색의 분광분포 내에서 청색 파장에 비해 적색 파장의 분포도가 상대적으로 높을 때 유리한 것으로 보인다. 한편, 줄기의 직경은 두 품종 모두 3000K 처리구에서 각각 0.56, 0.52cm로 가장 두꺼웠던 것으로 나타나 초폭과 마찬가지로 줄기의 직경 역시 적색파장의 분포가 상대적으로 큰 영향을 미치는 것으로 판단된다. 근장의 결과에서 ‘아시아슈가’는 보라색 LED 처리구에서 17.90cm로 가장 길었으며, ‘로사이탈리아나’는 3000K 백색 LED 처리구 하에서 23.22cm로 가장 긴 것으로 나타나 초장, 초폭, 근장의 결과와 유사하였다. 카네이션(Dianthus caryophyllus)(Manivannan et al., 2017)과 국화(Chrysanthemum)(Im et al., 2013)는 적색 LED하에서 식물체 뿌리의 생장이 촉진되는 것으로 알려져 있으나, 지황(Rehmannia glutinosa)(Manivannanet al., 2015)과 상추(Lactuca sativa)(Son et al., 2012)는 청색 LED 하에서 재배될 때 뿌리의 생장이 상대적으로 더 좋았던 것으로 나타나 식물 종에 따른 광질의 영향이 다름을 알 수 있었다. 한편, 고구마(Ipomoea batatas)의 기내 무병묘에서 청색 LED에 비해 상대적으로 적색 LED에서 더 높은 근장을 나타내는 경향이 있었으며 혼합광 처리시에는 적색 파장의 비율이 상대적으로 높아짐에 따라 근장도 비례하여 늘어나는 것으로 보고되었다(Yoo and Lee, 2017).
Table 2.
Plant sizes of Cichorium intybus cv. Asia Sugar and C. intybus cv. Rossa Italiana seedlings as affected by LED light qualities in a closed nursery facility for thirty days
| Cultivars | LED lights | Plant sizes (cm) |
Plant area (cm2) |
No. of leaves | Leaf sizes (cm) | ||||
|
Shoot height |
Shoot width |
Stem diameter |
Root length | Length | Width | ||||
| Asia Sugar | Red | 8.70 abcz | 15.38 ab | 0.43 d | 8.67 d | 265.1 a | 5.2 c | 10.96 a | 4.13 c |
| Green | 7.26 c | 13.42 bc | 0.35 e | 6.50 d | 195.5 bc | 4.7 d | 9.98 ab | 3.06 d | |
| Blue | 7.01 c | 11.57 c | 0.37 e | 9.43 cd | 136.9 c | 4.3 d | 8.25 c | 3.30 d | |
| Purple | 7.70 bc | 14.83 ab | 0.52 ab | 17.90 a | 235.8 ab | 6.0 b | 10.21 a | 4.86 b | |
| 3000 K white | 9.07 ab | 16.68 a | 0.56 a | 12.28 bc | 291.1 a | 6.8 a | 10.56 a | 5.35 ab | |
| 4100 K white | 9.26 ab | 16.86 a | 0.51 b | 12.89 b | 291.4 a | 6.7 a | 8.83 bc | 5.43 a | |
| 6500 K white | 9.66 a | 15.01 ab | 0.48 c | 12.97 b | 227.2 ab | 7.0 a | 9.75 ab | 5.16 ab | |
| Rossa Italiana | Red | 10.23 c | 16.62 bc | 0.46 bc | 20.17 ab | 307.6 bc | 5.7 d | 15.35 a | 2.56 a |
| Green | 7.48 d | 17.27 bc | 0.40 d | 9.41 d | 319.5 bc | 5.6 d | 13.60 b | 1.91 b | |
| Blue | 9.73 c | 16.82 bc | 0.35 e | 15.42 c | 298.6 bc | 5.1 e | 11.11 c | 1.66 c | |
| Purple | 14.23 ab | 15.17 c | 0.50 ab | 20.32 ab | 237.2 c | 6.5 c | 13.76 b | 2.67 a | |
| 3000 K white | 14.95 a | 20.36 a | 0.52 a | 23.22 a | 440.8 a | 7.3 b | 13.37 b | 2.78 a | |
| 4100 K white | 12.92 b | 19.43 ab | 0.45 c | 21.36 ab | 389.8 ab | 7.8 a | 13.23 b | 2.68 a | |
| 6500 K white | 12.87 b | 14.91 c | 0.46 bc | 17.96 bc | 247.3 c | 7.5 ab | 11.90 c | 2.62 a | |
| Significancey | Cultivar (A) | *** | ** | NS | *** | ** | ** | ** | *** |
| Treatment (B) | ** | *** | ** | *** | *** | *** | ** | ** | |
| (A) × (B) | ** | * | ** | ** | * | NS | NS | ** | |
피복면적은 ‘아시아슈가’의 경우 3000, 4100K 백색 LED 처리구 하에서 동등한 유의수준으로 나타났으며(각각 291.1, 291.4cm2), ‘로사이탈리아나’는 3000K 백색 LED 처리구에서 440.8cm2으로 가장 넓었다. 특히나 ‘아시아슈가’와 ‘로사이탈리아나’ 두 품종 모두 공통적으로 단색광 처리구 내에서 청색 LED에 비해 적색 LED 하에서 피복면적이 더 넓어지는 것으로 나타났으며, 백색 LED 처리구 중에서 상대적으로 적색 파장의 분포가 높은 3000, 4100K 백색 LED 처리구의 피복면적이 넓었던 것으로 보아 치커리 묘의 피복면적 증가에는 청색 파장에 비해 적색 파장의 영향이 상대적으로 크다는 것을 알 수 있었다. 과거 연구에서 패트로세덤 루페스트레(Petrosedum rupestre)와 ‘안젤리나’(P. rupestre cv. Angelina) 품종은 6500K 백색 LED에 비해 상대적으로 적색광 파장의 분포가 높은 4100, 3000K 백색 LED에서 더 높은 피복면적을 나타내어 본 실험의 결과와 유사하였다(Kim et al., 2022). 엽수는 ‘아시아슈가’가 3000, 4100, 6500K 백색 LED 처리구에서 많았던 것으로 나타났으며(각각 6.7, 7.0, 6.8개), ‘로사이탈리아나’는 4100K 백색 LED 처리구에서 7.8개로 가장 많았다. 단색광 처리구 내에서는 청색 LED에 비해 적색 LED에서 더 많은 엽수를 관찰할 수 있었으며 앞서 언급된 백색 LED 처리구와 일부 상반된 결과를 나타내었다. 과거 적색광 하에서 재배된 상추는 더 많은 엽수, 엽면적, 엽중량을 가지는 것으로 보고되었으며(Lee et al., 2014), 이와 유사하게 페튜니아는 청색 LED에 비해 상대적으로 적색 LED 아래에서 더 많은 엽수를 나타내어(Fukuda et al., 2009), 본 실험의 결과와 유사하였다.
엽장은 ‘아시아슈가’가 적색, 보라색, 3000K 백색 LED 처리구 하에서 길게 나타났으며(각각 10.96 10.21, 10.56cm), ‘로사이탈리아나’의 경우에는 적색 LED 처리구 하에서 엽장이 15.35cm로 가장 길었다. 이전 연구에서 심비디움(Cymbidium) 기내묘의 엽 크기는 청색광 파장에 비해 적색광 파장에서 증대되는 경향이 있는 것으로 나타났다(Tanaka et al., 1998). 한편, 본 연구에서 엽폭은 ‘아시아슈가’가 4100K 백색 LED 처리구에서 5.43cm로 가장 넓었으며, ‘로사이탈리아나’는 녹색과 청색 이외의 모든 처리구에서 2.56–2.78cm 범위에서 동등한 유의수준으로 나타났다. 과거 연구에서 상추는 청색 파장의 비율이 증가함에 따라 잎의 크기가 감소하였으며 식물체 크기가 줄어든다는 보고가 있었으나 반대로 청색광이 완전히 배제되었을 때에는 식물이 그늘 회피 반응(shade avoidance response)과 유사한 반응을 나타내어 상품가치가 현저히 떨어져(Kang et al., 2016), 적절한 청색광 비율을 설정하는 것이 중요함을 알 수 있었다. 한편, 대두(Glycine max)의 경우에도 백색광 내에서 청색 파장의 비율이 증가함에 따라 엽면적이 선형적으로 감소하는 것으로 나타났다(Cope and Bugbee, 2013). 치커리와 동일하게 국화과(Asteraceae)에 속하는 상추는 상대적으로 청색 파장의 비율이 높아질수록 식물체 크기와 관련된 매개변수에서 부정적인 결과를 나타내었으나, 총 페놀, 항산화력, 플라보노이드 함량과 같은 유효성분에 관한 매개변수는 청색 파장의 비율이 높아질 때 비례하여 높아지는 것으로 나타났다(Son and Oh, 2013).
다양한 LED 처리의 영향을 받은 치커리묘의 생체중과 건물중 그리고 수분함량에서 다양한 결과가 나타났다(Table 3). 지상부 생체중의 결과에서 ‘아시아슈가’는 3000, 4100K 백색 LED 처리구에서 각각 3043.8, 3022.5mg으로 무겁게 나타났으며, ‘로사이탈리아나’는 3000K 백색 LED 처리구에서 2566.1mg으로 가장 무거웠다. 이와 유사하게 단색광 처리구 내에서 적색 LED 하에서 재배된 치커리는 청색 LED 하에서 재배된 치커리에 비해 상대적으로 더 무거운 지상부 생체중을 나타내었다. 이와 관련하여 바나나(Musa × paradisiaca)의 경우 3000K 백색 LED의 적색과 청색 비율과 비교적 유사한 8:2의 적색과 청색 파장의 비율에서 생체중이 가장 무거웠던 것으로 나타났다(Nhut et al., 2000). 한편, 지상부 건물중의 경우에는 ‘아시아슈가’의 경우 3000, 4100, 6500K 백색 LED 처리구에서 무거웠던 것으로 조사되었으며(각각 213.7, 216.3, 210.0mg), ‘로사이탈리아나’의 경우에는 상대적으로 3000, 4100K 백색 LED 처리구에서 무거웠던 것으로 나타났다(각각 185.0, 181.2mg). 추가로 단색광 처리구에서 지상부 건물중은 상대적으로 청색 LED 처리구에 비해 적색 LED 처리구에서 더 무거웠던 것으로 나타나, 적색 파장 하에서는 동화산물의 축적이 보다 촉진되는 것으로 보인다. 지하부 생체중은 ‘아시아슈가’와 ‘로사이탈리아나’ 모두 3000K 백색 LED에서 각각 332.5, 547.5mg으로 가장 무거웠던 것으로 나타나 백색광 내에서 적색의 분광분포가 상대적으로 높은 경우 건실한 지하부 생육을 유도할 수 있는 것으로 판단된다. 지하부 건물중의 경우에는 ‘아시아슈가’가 보라색 LED와 세 가지 백색 LED 모두 동일한 유의수준으로 높게 나타났으며, ‘로사이탈리아나는 3000, 4100K 백색 LED 처리구에서 각각 40.2, 36.2mg으로 무거웠다. 마지막으로 수분함량에서 ‘아시아슈가’의 경우 지상부와 지하부가 각각 녹색, 적색 LED 처리구에서 가장 높게 나타났으며(각각 94.5, 93.9%), ‘로사이탈리아나’는 지상부와 지하부 모두 청색 LED 하에서 가장 높게 나타났다(각각 93.2, 93.5%). 치커리의 크기 및 생체중의 결과와 비교하였을 때 치커리가 우수한 생육수준을 나타내었을 때, 치커리의 수분함량은 상대적으로 감소하는 경향을 나타내었다. 과거 연구에서 바위솔(Orostachys japonica)은 녹색 LED 처리구에서 가장 높은 수분함량을 나타내었는데 이는 ‘아시아슈가’의 지상부 수분함량의 결과와 유사하였다(Lee et al., 2022b). 한편, Lee and Nam (2023)의 연구결과에서 6500K 백색 LED 하에서 재배된 상록바위솔 ‘블랙탑’(Sempervivum cv. Black Top) 품종은 높은 수분함량을 나타냄과 동시에 건실한 생장수준을 나타낸 것으로 보고되었으나, 본 실험에서는 녹색 LED 처리구에서 높은 수분함량과 낮은 생육수준 동시에 나타내어 이전 연구 결과와 상반되었다. 단색광 LED 처리구에 비해 상대적으로 다양한 분광분포를 나타내는 보라색 및 백색 LED 처리구에서 두 치커리 품종은 높은 묘 크기와 무게를 나타내었으며, 특히 보라색 LED 처리구에 비해 상대적으로 백색 LED 처리구에서 우수한 생육 결과를 나타내었다. 한편, ‘아시아슈가’와 ‘로사이탈리아나’ 두 품종 모두 보라색 LED 처리구에 비해 상대적으로 백색 LED 처리구에서 높은 생체중을 나타내었으며, 이는 녹색 파장의 분포 비율이 극도로 낮았던 것이 원인이었던 것으로 추정된다. 단일 녹색 LED 처리구에서 치커리는 식물체 크기와 생체중 모두 낮은 값을 나타내어 녹색 LED를 단용으로 사용하는 것은 치커리의 재배생산에 비효율적인 것으로 평가되나, 보라색 LED의 결과에 비해 상대적으로 백색 LED 처리구에서 생육수준이 높았던 것으로 미루어 보아 백색 LED 내에서 녹색파장을 일정 비율 이상으로 유지할 때 치커리 묘의 생육에 전반적으로 긍정적인 영향을 미치는 것으로 보인다.
Table 3.
Plant weights and relative moisture content of C. intybus cv. Asia Sugar and C. intybus cv. Rossa Italiana seedlings as affected by LED light qualities in a closed nursery facility for thirty days
| Cultivars | LED lights | Shoot weights (mg) | Root weights (mg) | Relative moisture content (%) | |||||
| Fresh weight | Dry weight | Fresh weight | Dry weight | Shoot | Root | ||||
| Asia Sugar | Red | 1898.7 cz | 108.8 c | 107.5 c | 6.9 b | 94.3 ab | 93.9 a | ||
| Green | 1085.0 d | 57.5 d | 65.3 c | 5.1 b | 94.5 a | 92.3 d | |||
| Blue | 1085.0 d | 68.7 d | 118.1 c | 7.6 b | 93.5 bc | 93.2 b | |||
| Purple | 2526.2 b | 172.5 b | 265.0 b | 20.6 a | 93.2 c | 92.5 c | |||
| 3000 K white | 3043.8 a | 213.7 a | 332.5 a | 24.2 a | 92.9 c | 92.5 c | |||
| 4100 K white | 3022.5 a | 216.3 a | 301.2 ab | 19.6 a | 92.8 c | 92.9 bc | |||
| 6500 K white | 2867.4 ab | 210.0 a | 292.5 ab | 21.7 a | 92.7 c | 92.7 c | |||
| Rossa Italiana | Red | 1778.6 d | 123.7 c | 262.5 d | 15.9 c | 92.8 b | 94.1 ab | ||
| Green | 1120.1 e | 71.2 d | 128.7 e | 8.6 d | 93.2 b | 93.5 b | |||
| Blue | 860.0 e | 43.7 e | 138.7 e | 7.6 d | 94.8 a | 94.6 a | |||
| Purple | 2191.3 bc | 148.6 b | 351.2 c | 24.4 b | 93.2 b | 92.9 c | |||
| 3000 K white | 2566.1 a | 185.0 a | 547.5 a | 40.2 a | 92.7 b | 92.5 c | |||
| 4100 K white | 2385.0 ab | 181.2 a | 506.2 ab | 36.2 a | 92.3 b | 92.4 c | |||
| 6500 K white | 2081.2 c | 153.8 b | 446.2 b | 29.3 b | 92.2 b | 93.6 b | |||
| Significancey | Cultivar (A) | ** | ** | *** | *** | * | ** | ||
| Treatment (B) | *** | *** | *** | *** | *** | *** | |||
| (A) × (B) | * | ** | * | ** | * | ** | |||
LED 광질의 영향을 받은 치커리묘의 엽록소 수치(SPAD units)와 CIELAB 색공간 분석에서도 다양한 결과를 나타내었다(Fig. 3). 엽록소 수치의 결과에서 ‘아시아슈가’는 3000, 4100, 6500K 백색 LED 처리구에서 높게 나타났으며(각각 26.67, 27.91, 27.46 SPAD units), ‘로사이탈리아나’는 보라색, 3000, 4100, 6500K 백색 LED에서 동등한 유의수준으로 나타났다(Fig. 3A). 이때, 앞서 설명한 초폭과 피복면적에서 ‘아시아슈가’는 3000, 4100K, ‘로사이탈리아나’는 3000K 백색 LED 처리구에서 가장 높은 것으로 나타났는데, 엽록소 수치의 결과와 비교했을 때 스파티필름(Spathiphyllum wallisii)과 무늬호야(Hoya carnosa var. variegata)(Lee et al., 2021a), 자주꿩의비름(Hylotelephium telephium)(Nam et al., 2022), 속리기린초(Sedum zokuriense)(Lee et al., 2021b)에서 식물이 넓은 수광면적을 나타낼 때 엽록소 수치 또한 함께 높아졌다는 연구결과와 유사하였다. CIELAB 색공간(color space)에서 명도(lightness)를 나타내는 매개변수인 CIELAB L*은 ‘아시아슈가’가 적색 LED 처리구에서 55.29로 가장 높게 나타났으며, ‘로사이탈리아나’는 적색, 녹색, 청색 LED 처리구에서 높게 나타나(각각 55.29, 53.78, 54.44), 단색광 조건 하에서는 상대적으로 잎의 명도가 높아지는 것으로 평가되었다(Fig. 3B). 이러한 결과는 엽록소 수치, 생체중, 건물중, 수분함량의 결과와 상반되는 경향을 나타내었으며, 위 결과를 종합적으로 판단할 때 백색의 분광분포에 비해 상대적으로 단색광 조건 하에서는 세포의 크기가 비대해지고 동일 면적 대비 엽록소의 밀도가 낮아지는 것으로 추정된다. 적색과 녹색을 나타내는 매개변수인 CIELAB a*는 ‘아시아슈가’의 경우 적색, 녹색, 청색 LED 처리구에서 높게 나타났으며(각각 ‒9.67, ‒9.54, ‒9.50), ‘로사이탈리아나’는 4100K 백색 LED 처리구에서 ‒10.23으로 가장 높게 나타났다(Fig. 3C). a*가 음의 수를 나타낼수록 엽색이 녹색에 가까워지는 것을 의미하며, 해당 수치와 엽록소 수치의 결과를 비교 분석했을 때 a*의 값이 높아질수록 엽록소 수치가 낮아지는 경향이 나타나 단색광 하에서 재배한 치커리의 경우 동일 면적 대비 엽록소 밀도가 낮아지는 것으로 보인다. 마지막으로 황색과 청색을 나타내는 매개변수인 CIELAB b*는 ‘아시아슈가’가 적색 LED에서 32.96으로 가장 높게 나타났으며, ‘로사이탈리아나’는 녹색, 청색 LED 내에서 높게 나타났다(각각 28.46, 28.25)(Fig. 3D). 과거 연구에서 L*과 b*의 증가는 식물의 생장수준과 음의 상관관계를 가지는 것으로 분석되었는데(Lee et al., 2021b; Lee et al., 2022a, 2022b), 적색, 청색 등의 단색광과 백색 LED하에서 재배된 치커리 묘의 생육수준을 비교하였을 때 이와 유사한 결과를 나타내었다. 이에 낮은 명도와 황색도를 나타내는 묘를 얻기 위해서는 백색 LED 하에서 재배하는 것이 상대적으로 유리한 것으로 판단된다.
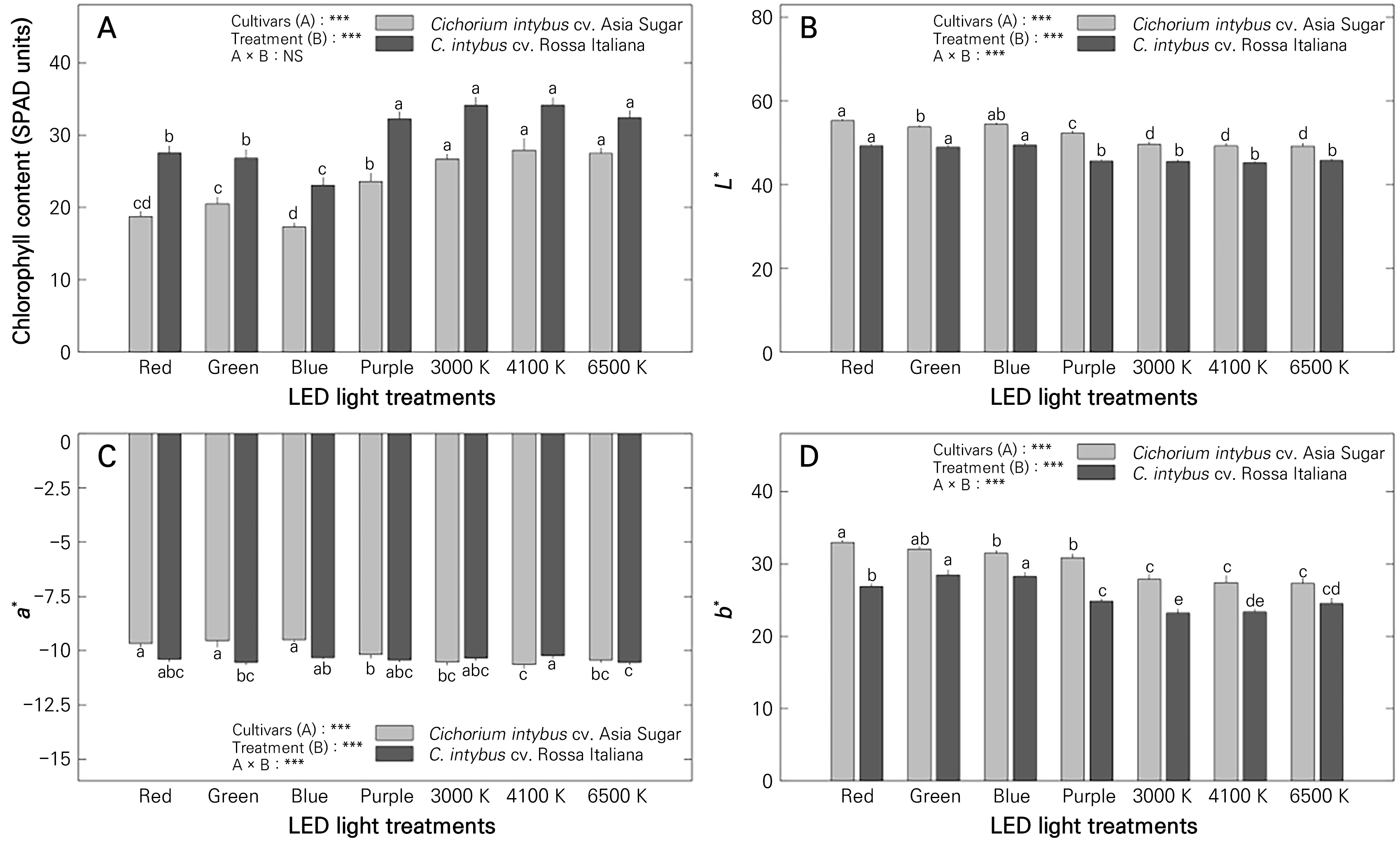
Fig. 3.
Chlorophyll content (SPAD units) and leaf color reading values of CIELAB (L*, a*, and b*) of C. intybus cv. Asia Sugar and C. intybus cv. Rossa Italiana seedlings as affected by LED light qualities. The units indicated in color temperature (K) are white LED treatments (3000, 4100, and 6500 K). Vertical bars indicate the standard error, and asterisks (***) indicate significance at p < 0.001. Different lowercase letters indicate significant differences at p < 0.05 based on Duncan’s multiple range test, and NS indicates no significant difference (n = 3).
결론적으로 식물체 크기, 무게, 엽록소 수치, 엽색 분석을 종합적으로 판단할 때, 두 품종의 치커리 묘는 상대적으로 높은 적색 파장의 분포를 선호하는 것으로 보인다. 이러한 결과에 따라 ‘아시아슈가’ 품종은 백색의 분광분포 내에서 적색 파장의 분포가 상대적으로 높은 3000, 4100K 백색 LED에서 재배하는 것이 보다 유리할 것으로 판단되며, ‘로사이탈리아나’ 품종은 3000K 백색 LED에서 재배하는 것이 건실한 묘를 얻는데 유리할 것으로 판단된다.
식생지수와 엽록소 형광 매개변수 분석
서로 다른 LED 광질의 영향을 받은 치커리는 다양한 식생지수와 엽록소 형광 매개변수의 변화를 나타내었다(Table 4). 정규식생지수(normalized difference vegetation index, NDVI)는 ‘아시아슈가’와 ‘로사이탈리아나’ 두 품종 모두 백색 LED 처리구에서 높게 나타났으며, 추가적으로 ‘로사이탈리아나’의 경우 보라색 LED 처리구에서도 정규식생지수가 0.632로 높게 나타났다. 광화학 반사율 지수(photochemical reflectance index, PRI)는 광합성 효율을 저해시키는 메커니즘인 크산토필 색소 상호전환 역학(xanthophyll pigment interconversion)을 비파괴적인 측정방식으로 추정하기 위해 사용된다(Magney et al., 2016). 광화학 반사율 지수는 두 품종 모두 4100K 백색 LED 처리구에서 각각 0.027, 0.031로 높게 나타났다. 한편, 단색광 처리구 간의 비교에서는 ‘아시아슈가’의 경우 적색 LED에 비해 청색 LED에서 더 높은 광화학 반사율 지수를 나타내었다. 수정된 엽록소 흡광량 지수(modified chlorophyll absorption ratio index, MCARI)는 적색 LED 처리구에서 두 품종 모두 가장 높게 나타났다(각각 0.609, 0.464). 위 지수는 잎의 엽록소 농도와 지면 반사율(ground reflectance)에 반응하며, 일반적으로 식물의 엽록소 함량과 반비례한다(Nagler et al., 2000). 이때, ‘아시아슈가’와 ‘로사이탈리아나’ 품종 모두 3000–6500K 범위의 백색 LED 처리구에서 해당 매개변수가 낮게 나타나 단색광 처리구에 비해 상대적으로 엽록소 함량이 높았던 것을 추정할 수 있었다.
Table 4.
Normalized difference vegetation index (NDVI), photochemical reflectance index (PRI), modified chlorophyll absorption ratio index (MCARI), and chlorophyll fluorescence parameters (Fv/Fm, ΦDo, ABS/RC, DIo/RC, and PIABS) of C. intybus cv. Asia Sugar and C. intybus cv. Rossa Italiana seedlings as affected by LED light qualities in a closed nursery facility for thirty days
| Cultivars | LED lights | Vegetation indices | Chlorophyll fluorescence parameters | |||||||
| NDVI | PRI | MCARI | Fv/Fm | ΦDo | ABS/RC | DIo/RC | PIABS | |||
| Asia Sugar | Red | 0.486 cz | 0.019 b | 0.609 a | 0.79 b | 0.20 b | 2.51 a | 0.50 b | 2.59 cd | |
| Green | 0.506 c | 0.022 ab | 0.577 a | 0.78 c | 0.21 a | 2.65 a | 0.56 a | 2.18 d | ||
| Blue | 0.529 bc | 0.023 ab | 0.551 a | 0.80 a | 0.19 c | 2.29 b | 0.43 c | 3.26 b | ||
| Purple | 0.576 ab | 0.025 a | 0.544 a | 0.80 a | 0.19 c | 2.30 b | 0.44 c | 2.88 bc | ||
| 3000 K white | 0.590 a | 0.024 ab | 0.379 b | 0.80 a | 0.19 c | 2.22 b | 0.42 c | 3.17 b | ||
| 4100 K white | 0.616 a | 0.027 a | 0.444 b | 0.81 a | 0.18 c | 2.13 b | 0.39 c | 4.03 a | ||
| 6500 K white | 0.589 a | 0.025 a | 0.419 b | 0.81 a | 0.18 c | 2.18 b | 0.41 c | 3.81 a | ||
| Rossa Italiana | Red | 0.590 ab | 0.026 abc | 0.464 a | 0.80 b | 0.19 b | 2.29 b | 0.44 b | 3.19 cd | |
| Green | 0.568 b | 0.024 bc | 0.446 a | 0.79 c | 0.20 a | 2.44 a | 0.49 a | 2.62 d | ||
| Blue | 0.572 b | 0.027 abc | 0.445 a | 0.82 a | 0.17 c | 1.94 d | 0.35 d | 4.75 ab | ||
| Purple | 0.632 a | 0.030 ab | 0.436 a | 0.81 ab | 0.18 bc | 2.11 c | 0.39 c | 3.58 c | ||
| 3000 K white | 0.627 a | 0.023 c | 0.326 b | 0.81 ab | 0.18 bc | 2.01 cd | 0.37 cd | 4.38 b | ||
| 4100 K white | 0.638 a | 0.031 a | 0.320 b | 0.82 a | 0.17 c | 1.98 d | 0.35 d | 4.86 ab | ||
| 6500 K white | 0.619 a | 0.029 abc | 0.354 b | 0.82 a | 0.17 c | 1.95 d | 0.34 d | 5.14 a | ||
| Significancey | Cultivar (A) | *** | *** | *** | *** | *** | *** | *** | *** | |
| Treatment (B) | *** | *** | *** | *** | *** | *** | *** | *** | ||
| (A) × (B) | NS | NS | NS | NS | NS | NS | NS | NS | ||
Fv/Fm는 엽록소 형광 매개변수 중 하나로 스트레스를 받지 않은 고등식물의 경우 0.78–0.84의 수준을 나타내며 광계II의 최대 양자 수율(maximum quantum yield)을 나타내는 매개변수로 활용되고 있다(Butler and Kitajima, 1975; Paillotin, 1976; Björkman and Demmig, 1987; Genty et al., 1989; Govindjee, 1995; Govindjee, 2004; Yoo et al., 2012). 본 연구에서 매개변수 Fv/Fm는 0.78–0.82의 범위로 나타나 처리구나 품종에 상관없이 최대 양자 수율은 정상범위 내에 있는 것으로 분석되었다. 한편, 흡수된 광자가 소멸될 확률(probability of photon dissipated)을 나타내는 ΦDo는 녹색 LED 처리구에서 두 품종 모두 0.20–0.21 범위로 나타나 광자의 소멸 확률이 다른 처리구에 비해 상대적으로 높은 것으로 분석되었으나, 종합적으로 볼 때에는 정상 범위 내에 있는 것으로 평가되었다. ABS/RC는 광계II에서 비활성 상태로 존재하는 반응중심의 수의 증감 정도를 나타낸다(Spoustová et al., 2013). 반응중심(reaction center)당 흡광량(absorption flux)을 나타내는 ABS/RC는 앞서 언급된 스트레스 지표인 ΦDo와 마찬가지로 두 품종 모두 녹색 LED 처리구에서 가장 높게 나타났으며, 백색 LED 처리구에서는 상대적으로 낮은 범위에 속하는 것으로 나타나 백색 LED 하에서는 반응중심의 활성도가 비교적 높았던 것으로 보인다. 반응중심당 소산되는 에너지의 양(dissipated energy flux)을 나타내는 매개변수 DIo/RC는 ΦDo 및 ABS/RC와 마찬가지로 두 품 종 모두 녹색 LED 처리구에서 가장 높게 나타났다(각각 0.56, 0.49). PIABS는 흡광량을 기반(absorption basis)으로 한 성능지수(performance index)다(Srivastava et al., 1999). 이때, PIABS는 ‘아시아슈가’의 경우 4100, 6500K 백색 LED에서 높은 값을 나타냈으며(각각 4.03, 3.81), ‘로사이탈리아나’는 6500K 백색 LED 처리구에서 5.14로 가장 높게 나타나 단색 LED에 비해 백색 LED 하에서 상대적으로 더 높은 광합성 효율을 가졌음을 알 수 있었다.
결과적으로 치커리 ‘아시아슈가’와 ‘로사이탈리아나’ 품종의 식물체 크기, 무게, 엽록소 수치 분석, 엽색 분석, 식생지수, 엽록소 형광 매개변수 분석의 결과를 종합적으로 평가한 결과, 두 품종 모두 단색광 LED와 보라색 LED 처리구에 비해 상대적으로 백색 LED 처리구 하에서 더 우수한 식물체를 얻을 수 있었다. 특히 적외선 파장이 포함되었던 보라색 LED에 비해 백색 LED 처리구에서 보다 건실한 식물체를 생산할 수 있었던 것으로 미루어 보아 적외선의 영향 보다 분광분포 내에서 녹색 파장의 유무가 치커리 묘의 생육과 광화학 반응에 더 큰 영향을 미치는 것으로 판단된다. 따라서 이후 적외선과 녹색광 파장의 비율을 달리하여 적용한 후속실험이 필요할 것으로 판단된다. 위와 같은 결과들을 종합할 때, 두 품종의 치커리 묘 크기와 무게를 유의미하게 증대시키기 위해서는 ‘아시아슈가’와 ‘로사이탈리아나’ 모두 적색 파장이 상대적으로 더 많이 분포해 있는 3000, 4100K의 백색 LED를 사용하여 재배하는 것이 유리할 것으로 판단되며, 청색 파장이 상대적으로 더 많이 분포해 있는 6500K 백색 LED의 경우 치커리 묘의 크기는 3000, 4100K 백색 LED에 비해 상대적으로 작은 편이었으나, 식생지수 및 엽록소 형광 매개변수의 결과는 상대적으로 우수하였다.