서 언
재료 및 방법
실험재료
추출물의 제조
활성물질의 분리 및 동정
세포배양
MTT assay
Nitric oxide(NO) 측정
iNOS, COX-2 및 p65 단백질 expression 측정
Cytoplasmic과 nuclear의 분획
TNF-α, IL-1β, IL-6, MCP-1, PTGES2의 Real-time PCR 측정
통계처리
결과 및 고찰
활성 물질의 분리 및 구조분석
Isoorientin의 Raw 264.7 cell에 대한 MTT assay
Isoorientin의 NO 생성 억제 효과
Isoorientin의 p65, iNOS 및 COX-2 protein expression 억제 효과
Isoorientin의 pro-inflammatory cytokine 및 chemokine 발현 억제효과
서 언
약용식물자원 및 폐기 식물자원으로부터 분리한 천연물질에 대해 질병의 예방과 치료를 위한 새로운 소재 개발이 시도되고 있다(Jhoo 2008). 식물이 생산하는 2차대사산물인 페놀성 화합물은 식물체에서는 자신을 방하기 위한 용도로 쓰이지만, 인간에게 있어서는 항산화, 항암, 항당뇨, 항염증, 성인병 예방 및 치료 등에 다양하게 적용되고 있어 매우 유익한 물질군으로 분류되고 있다(Joo et al. 2007; Cho et al. 2008). 오늘날 우리들의 먹거리문화가 서구화 되면서 다양한 고혈압, 당뇨 같은 성인성 질환과 스트레스 등으로 인한 염증성 질환이 증가하고 있는 현실에서 식물이 함유하고 있는 페놀성 물질들은 이러한 질환들을 예방 및 치료에 이용할 수 있는 건강기능성 자원으로 각광받고 있다.
염증은 인체에서 물리적 외상, 화학물질, 미생물학적 감염 등에 의해 정상적으로 돌아가려는 항상성기전으로 면역세포에 의해 발생하는 복합적인 면역반응으로 발생하는 순기능에 해당된다. 그러나 염증반응이 오래 지속되게 되면 다양한 성인병에 해당하는 병리적 현상들이 나타나게 된다(Moncada et al. 1991; Ryu et al. 2011; Lee et al. 2016a).
박테리아 내독소인 lipopolysaccharide(LPS)는 macrophage를 자극하여 염증반응을 일으키는 주요한 인자이다. 염증반응이 활성화되게 되면 세포 내부의 여러 신호전달 과정 중 활성화된 NF-κB가 핵내로 진입하여 tumor necrosis factor-α, interleukin1β, interleukin6 등의 염증성 cytokine과 cyclooxygenase2, inducible NOS와 같은 염증에 관여하는 효소단백질의 expression을 높여주고 NO와 PGE2를 만들게 됨으로서 미리 생성된 염증성 cytokine과 함께 통증, 부종, 발열 등 염증반응을 유발하는 것으로 알려져 있다(Tak and Firestein 2001; Kang et al. 2011; Kim et al. 2014). 현재 우리들이 이용하고 있는 약물인 합성 항염증제는 aspirin, indomethacin, arachidonic acid 등이 있는데, 주로 cyclooxygenase2 효소단백질 expression 억제를 통하여 염증억제 효과를 나타내게 된다(Dangne et al. 2006). 그러나 합성 항염증제는 위산분비 증가, 혈소판 응집감소 등 부작용이 알려져 있어 보다 안전이 확보될 수 있는 천연 염증억제제의 개발이 필요하다(Makins and Ballinger 2004; Jeong et al. 2013).
털주름풀이라 불리는 주름조개풀(Oplismenus undulatifolius)은 다년생 초본으로 일반적으로 산에 널리 퍼져서 야생하며, 우리나라의 중부이남, 유럽의 지중해 연안, 중앙아시아, 인도북부 등 극동 지방에 주로 분포되어 자생한다(Lee 1999). 주름조개풀은 가축의 사료로 이용되고 있으나 약용으로서의 효능 검정 등에 관한 연구 보고는 거의 없으며, 현재까지 Oplismenus 속에 존재하는 화합물들의 성분연구에서 isoarborinol, cylindrin, triedelin 등의 triterpenoid 성분을 분리, 동정하여 보고된 것이 유일하며(Ohmoto and Ikuse 1970), 최근 주름조개풀이 가지는 생리활성 등에 관심을 가지고 이 등(Lee et al. 2017)이 주름조개풀이 가지는 생리활성에 대한 연구 보고를 한 것이 가장 최근의 연구 보고인데 이 연구에서 주름조개풀의 생리활성 중 염증억제효과가 있음을 보고하였다.
그중 isoorientin은 폴리페놀 계열의 수용성 플라보노이드 배당체이다. 대부분의 플라보노이드와 같이 isoorientin의 구조 중간에 강한 산소 염기의 화학적 특성을 가지고 있으며(Singh et al. 2014) 물과 에탄올에 잘 용해된다. 게다가, ascorbic acid, quercertin 등과 같이 널리 알려진 항산화제와 같이 높은 항산화력을 보여준다(Watanabe 2007). 또한 간세포에서도 isoorientin의 효과가 간 손상 예방은 물론 항산화, 항염증, 침해 방지 활동 등 간암의 증식을 억제하는 것으로 나타났다(Li et al. 2016).
따라서 본 연구에서는 염증억제효과가 있다고 보고된 주름조개풀로부터 isoorientin을 분리 동정하고 isoorientin이 LPS에 의해 자극된 Raw 264.7 cell에서 나타내는 염증억제 효과를 측정하기 위해서 염증발현인자인 NO와 PTGES2 m-RNA생성, iNOS 및 COX2 발현제어, 염증성 cytokine 및 chemokine인 TNF-α, IL-6, IL-1β와 MCP-1의 발현억제를 확인하여 천연 염증 치료제로써 개발하고자 하였다.
재료 및 방법
실험재료
실험소재인 주름조개풀은 경북소재의 팔공산 위도 : 35.9774057, 경도 : 128.7328101 지점의 야산에서 2021년 8월에 직접 채취하여 뿌리를 제외한 전초를 실험에 이용하였으며, 채취한 주름조개풀(Fig. 1)은 50°C의 항온건조기에서 4일간 건조 후, 40mesh로 분쇄하고 진공 포장하여 4°C의 냉장고에 저장하며 실험에 사용하였다.
추출물의 제조
추출물의 제조는 건조된 주름조개풀 건조분말 5g에 10배의 70% 에탄올을 용매로 첨가하여 120rpm으로 24시간 동안 추출하였다. 추출이 끝난 용액은 Whatman No. 1 여과지로 찌꺼기를 여과, 제거한 후 회전증발농축기(Eyela NE, Tokyo, Japan)로 농축 공정을 통해 에탄올을 모두 제거하였으며, 농축액은 Folin과 Denis의 방법(1921)에 따라 total phenolic 함량을 측정하여 50에서 200µg/mL의 phenolic 농도로 효소 실험을 진행하였으며, cell 실험은 추출물로부터 분리 동정한 isoorientin을 사용하여 진행하였다.
활성물질의 분리 및 동정
시료에 10배 이상의 70% 에탄올을 넣고 4°C에서 24시간 동안 2회 교반해 추출하였다. 추출액은 Whatman No.1 여과지로 여과한 후 회전식감압농축기(IKA RV 8, IKA, Germany)로 농축하여 냉장 보관하였다(58g). 제조한 분말(40g)은 10% 메탄올에 현탁하여 여과한 후 MPLC(Buchi, Sepacore 50, Swiss)를 이용하여 ODS-SM-50B(50µm, Yamazen, Japan) resin을 충진한 컬럼에 H2O-MeOH을 0–100%까지 농도를 높여 분리하였으며, 분리물은 silica gel 60(Merck, Darmstadt, Germany)을 사용한 TLC를 실시한 후 분리여부를 확인하였다. 1H-NMR 및 13C-NMR spectra는 Avance III HD NMR기기(600 MHz, Bruker Biospin GmbH, Rheinstetten, Germany)로 spectrum을 측정하였다.
세포배양
한국세포주은행(Korean Cell Line Bank)에서 구입한 Raw 264.7 cell의 배양은 37°C, 5% CO2 incubator의 조건에서 DMEM에 fetal bovine serum(FBS)을 10%, 100U/mL penicillin 및 100µg/mL streptomycin 1%를 혼합하여 조제한 배지를 사용하여 72시간 동안 세포배양 하였다. 5% CO2 조건에서 세포배양 접시에 세포의 밀도가 2–3×106 cell/mL정도가 되게 배양, 유지하였다. 실험과정의 모든 세포는 80% 정도의 밀도일 때 계대배양하였고, 세포는 20 passages를 넘지 않은 건강한 세포를 사용하여 실험하였다.
MTT assay
MTT assay는 Carmichael의 방법(1987)으로 48 well plate를 이용하여 Raw 264.7 cell을 5×103 cells/mL의 농도로 분주하여 5% CO2의 조건으로 24시간 동안 배양하였다. 배양 후 농도별 시료를 첨가하고 다시 동일한 조건에서 24시간 2차 배양하였다. 2차 배양 후 3mg/mL 농도의 MTT 용액 0.5mL를 처리하고 다시 4시간 배양 후 배양액을 제거하였다. 각 well 마다 0.5mL의 dimethyl sulfoxide를 가하고 10분간 상온에서 반응시켰다. 세포 생존율 계산을 위한 흡광도 측정은 540nm의 파장으로 ELISA reader로 측정하였다. 세포 생존율은 시료 용액의 무첨가군과 첨가군의 흡광도 감소율로 나타내었다. 대조군은 동일한 조건에서 시료와 동일한 양의 DMEM 배지를 첨가하였다. 세포생존율(cell viability, %)는 (시료첨가군의 흡광도/대조군의 흡광도)×100으로 나타내었다.
Nitric oxide(NO) 측정
NO 측정은 griess reagent System(Promega, USA)으로 수행하였으며, 96 well plate에 세포의 농도가 5×104 cells/mL이 되게 분주하고 37°C, 5% CO2 조건에서 24시간 배양하였다. 배양 후 Phosphate buffer solution으로 세척하고 상등액을 제거한 뒤 무혈청 배지를 분주하였다. 이때 Normal군을 제외한 모든 well에 대해 LPS 1µg/mL을 첨가해 세포자극을 유도하였다. 세포 자극 후 시료를 농도별로 첨가하고 37°C, 5% CO2 incubator에서 24시간 2차 배양시켰다. 배양 후 상등액은 griess reagent로 반응시키고 540nm에서 흡광도를 측정하였다. 측정한 흡광도값은 NO 생성율(%)로 환산하여 나타내었다. 세포생존율이 80% 이상인 농도 구간을 설정 후 실험 진행하였다.
iNOS, COX-2 및 p65 단백질 expression 측정
Raw 264.7 cell 양을 counting하여 6 well plate에 5×105 cells/mL의 농도로 주입하고 37°C, 24시간 동안 5% CO2의 조건에서 incubation한 뒤, phosphate buffer solution으로 세척하고 무혈청 배지와 LPS 1µg/mL을 normal군을 제외한 모든 well에 처리하여 세포를 자극시켰다. 자극 후 시료를 농도별로 첨가하여 37°C, 18시간 동안 5% CO2 조건에서 배양시켰다. 배양 후 상등액을 제거하고 차가운 PBS로 2번 세척한 뒤 M-PER buffer를 넣은 후 스크레퍼를 사용해 단백질을 용출시켰다. 용출된 단백질은 20분 동안 4°C, 13,000rpm에서 원심 분리하였으며, 상층액만 모은 뒤 BCA protein assay Kit로 단백질양을 계산하여 western blot 실험에 사용하였다. 단백질 sample은 전기영동 system으로 10% SDS-PAGE로 1시간 30분 동안 120V로 단백질을 분리하였고, 분리된 단백질은 transfer 기기를 이용해 PVDF membrane으로 60V에서 2.5시간 동안 transfer하였다. Transfer된 단백질 band를 확인하기 위해 2분 정도 ponceau S에 담궈 확인한 후, TBST로 3번 세척하고 1시간동안 blocking buffer로 배경을 탈색시켰다. iNOS나 COX-2 발현을 위한 primary antibody는 1 : 1,000으로 희석하여 붙인 후 TBST로 3번 세척하고, 1시간 30분 동안 mouse anti-rabbit IgG HPR(secondary antibody)를 1 : 1,000으로 붙인 다음 TBST로 3번 세척하였다. Band의 현상은 ECL Kit와 반응시켜 image analyzer(C300, Azure biosystems, Dublin, USA)로 현상하였으며, 면적을 계산하여 양을 계산하였다(Park et al. 2018).
Cytoplasmic과 nuclear의 분획
LPS로 자극한 Raw 264.7 cell은 2×106 cells/mL 농도가 되도록 분주하고 37°C에서 24시간 5% CO2 조건에서 배양하였다. 배지에 1µg/mL LPS와 isoorientin을 차례로 처리하고 60분간 배양하였다. 배양 후, 원심분리하여 세포를 모으고 cold PBS를 이용해 3회 세척하였다. Cytoplasmic과 nuclear 단백질의 추출은 NE-PER(Thermo Fisher Scientific.)을 사용하여 준비하였다.
TNF-α, IL-1β, IL-6, MCP-1, PTGES2의 Real-time PCR 측정
TNF-α, IL-1β, IL-6, MCP-1 및 PTGES2 mRNA의 측정은 100×20mm 배양접시에 Raw 264.7 cell을 5×106 cells/mL의 농도로 분주하고 24시간 배양한 후 1µg/mL의 LPS로 세포를 자극하고 농도별 isoorientin을 처리한 후 다시 24시간 배양하였으며, phosphate buffer solution으로 3회 세척하였다. mRNA 발현량을 비교하기 위해 total RNA는 GeneAll®Ribospin RNA 추출 Kit(GeneAll Biotechnology Co.)로 RNA를 추출하였으며, cDNA 합성은 qPCRBIO cDNA synthesis Kit(PCR Biosystems.)을 이용하여 합성하였다. 합성된 cDNA는 PCRmax Eco 48 real-time PCR system을 이용하여 mRNA 발현을 측정하였으며, PCR operating 조건과 primer sequence는 Tables 1 and 2와 같다.
Table 1.
Primer sequences of Real-time PCR for Proinflammatory-related gene mRNA expression levels
Table 2.
Real-time PCR operating conditions to test Proinflammatory-related gene mRNA expression levels
통계처리
본 실험의 결과는 3회 반복 측정한 값을 평균±표준편차의 형식으로 나타내었다. 유의성 분석은 SPSS 22 for windows(Statistical Package for Social Science, Chicago, IL, USA) 프로그램으로 통계분석 하였으며, ANOVA test로 유의성(95%)을 검정하였다.
결과 및 고찰
활성 물질의 분리 및 구조분석
저자는 Lee et al.(2017)의 논문에서 주름조개풀 ethanol 추출물의 항염증 효과를 보고한 바 있으며, 본 연구에서는 주름조개풀에 존재하는 천연물 중 염증억제 효과를 가지는 물질을 동정하고, 분리된 천연물의 세포생물학적 염증억제 활성정도를 밝히고자 하였다.
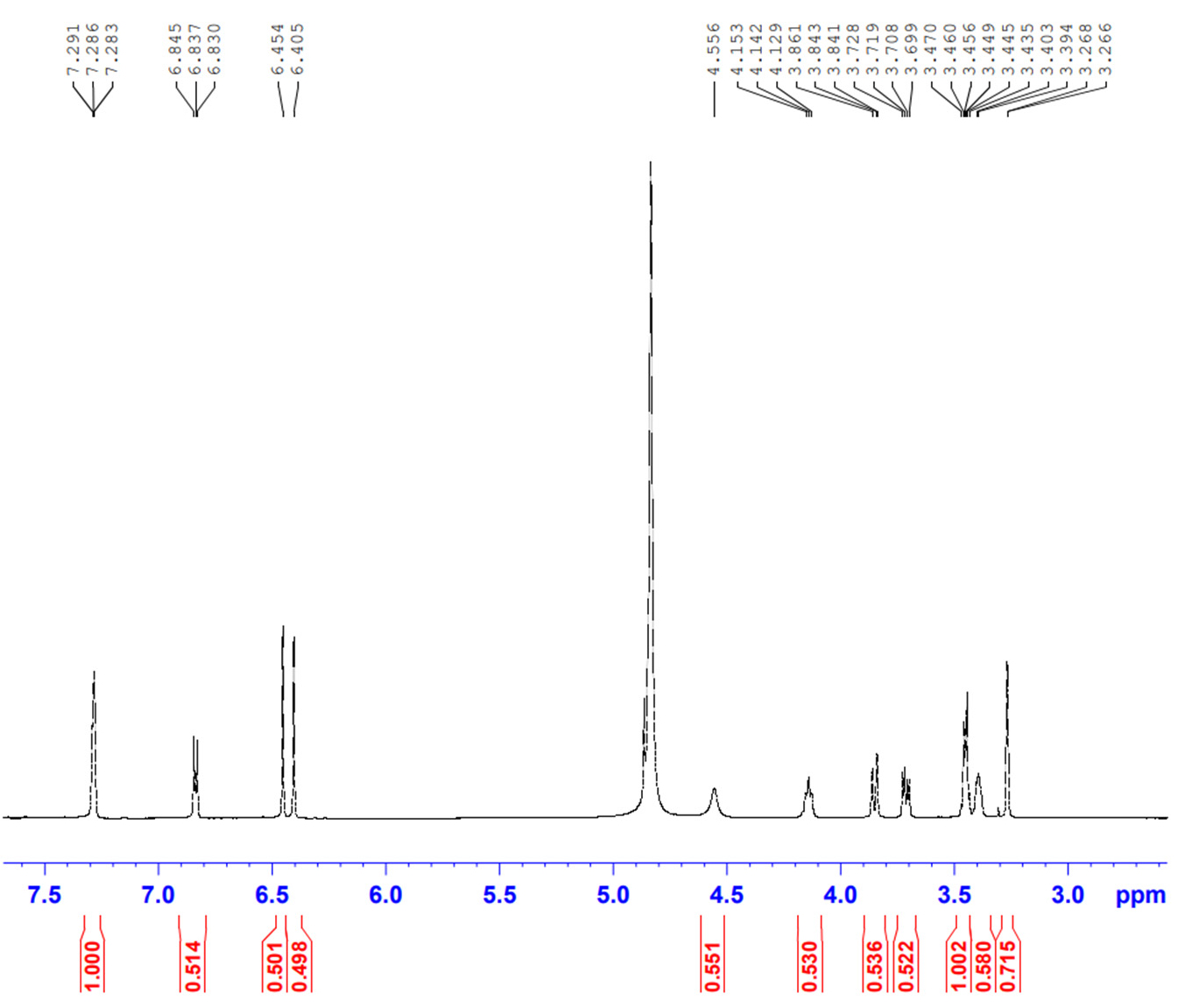
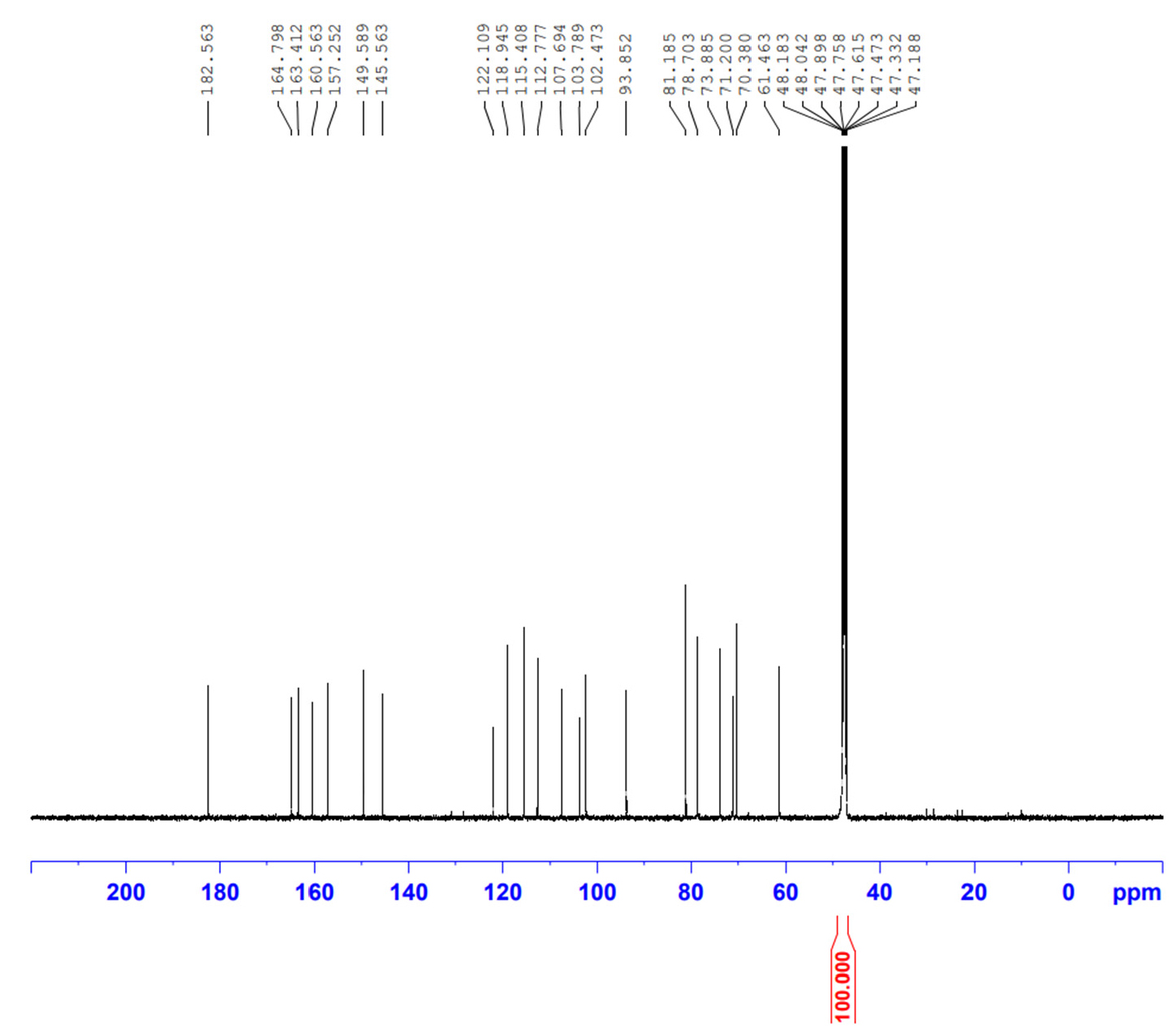
분리된 단일 화합물의 색깔은 노란색 무결정 분말로 nucleamagnetic resorurcenance(1H-NMR, 600 MHz, MeOD) spectrum은 Fig. 2에서와 같이 δ : 6.45(1H, s, H-3), 6.40(1H, s, H-8), 7.28(1H, brs, H-2'), 6.84(1H, d , J = 9.0Hz, H-5'), 7.29(1H, brd, J = 9.0Hz, H-6'), 4.55(1H, s, H-1''), 4.14(1H, dd, J = 6.6, 7.8Hz, H-2'')로 나타났다. 13C-NMR(150MHz, MeOD)는 Fig. 3에서와 같이 δ : 163.4(C-2), 102.5(C-3), 182.6(C-4), 160.6(C-5), 107.7(C-6), 164.8(C-7), 93.9(C-8), 157.3(C-9), 103.8(C-10), 122.1(C-1'), 73.9(C-1''), 112.8(C-2'), 71.2(C-2''), 145.6(C-3'), 78.7(C-3''), 149.6(C-4'), 70.4(C-4''), 115.4(C-5'), 81.2(C-5''), 118.9(C-6'), 61.5(C-6'')으로 나타나 이상의 결과는 Joshi et al.(2015)이 보고한 문헌과 비교한 결과, isoorientin으로 동정하였다.
Isoorientin의 Raw 264.7 cell에 대한 MTT assay
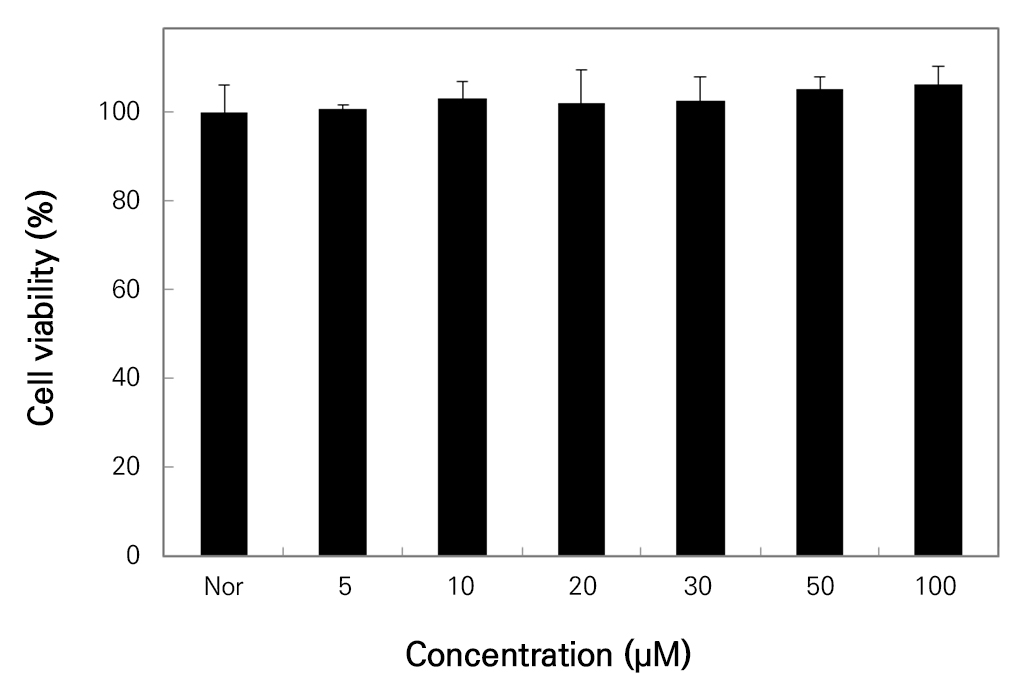
Macrophage cell에서 일어나는 염증반응에서 isoorientin이 나타내는 염증억제 효과는 Raw 264.7 cell에 대한 isoorientin의 세포독성과 세포생존율을 측정하였다. Isoorientin을 5, 10, 25, 50, 100µg/mL의 농도로 가하여 MTT assay를 측정한 결과 Fig. 4에서와 같이 isoorientin은 100µg/mL까지 독성 효과가 나타나지 않아 독성이 거의 없는 것으로 관찰되었다. 따라서 위의 결과를 바탕으로 본 연구에서는 생존율이 높은 100µg/mL 이하의 농도로 실험을 진행하였다.
Isoorientin의 NO 생성 억제 효과
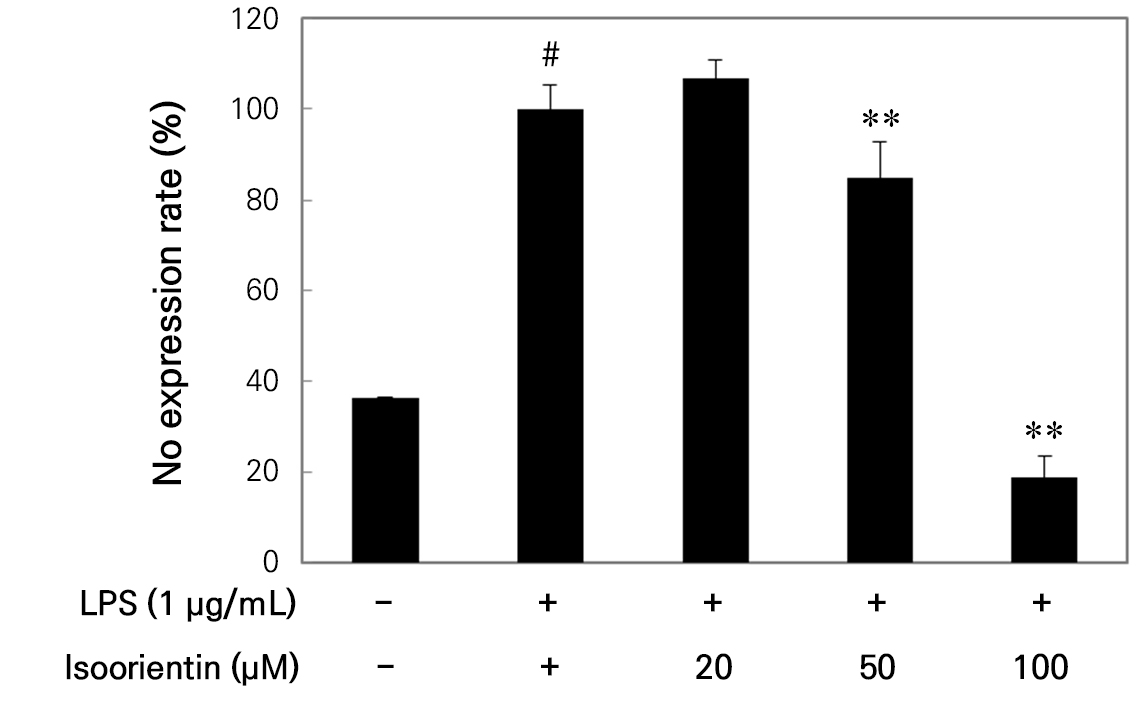
iNOS에 의해 발현되는 NO는 면역기능을 수행하지만, 과량으로 생성된 NO는 오히려 체내에 염증을 일으켜 유전자 변이나 조직 및 신경의 손상을 유발할 수 있다(Kim and Kim 2015). 본 연구에서 isoorientin에 의한 NO 발현억제 효과를 측정한 결과 Fig. 5에서와 같이 LPS만으로 세포를 자극한 대조구와 LPS 자극과와 함께 isoorientin을 처리하였을 때, NO 발현 억제효과는 농도 의존적으로 유의성 있는 감소 경향을 나타내었고, 100µg/mL 농도에서 약 80% 정도의 NO 생성억제를 나타내었으며, normal군보다 낮은 수치를 나타내었다. Yoon et al.(2011)은 50µg/mL 농도의 황금 물추출물에서 NO 생성억제율이 약 50%를 나타내었으며, Nam(2014)은 산짚신나물 에탄올 추출물 25, 50µg/mL 농도에서 각각 8.00%, 31.50%의 NO 생성억제 효과를 나태내었다고 보고하였다. 이상의 결과와 비교했을 때 isoorientin은 더 우수한 NO 생성억제를 나타내어 염증질환의 치료 및 예방을 위한 agent로 사용가능성을 크게 기대할 수 있었다.
Isoorientin의 p65, iNOS 및 COX-2 protein expression 억제 효과
LPS 자극한 Raw 264.7 cell에 isoorientin을 20, 50, 100µg/mL의 농도로 처리하여 NF-κB 복합체 중 인산화된 p65 단백질의 발현량을 western blotting으로 측정하였다. 그 결과 Fig. 6A에서와 같이 처리된 isoorientin의 농도에 의해 인산화된 p-p65 발현량이 농도의존적으로 유의성 있게 억제되었으며, 이러한 결과는 염증매개체인 iNOS나 COX-2 발현량에도 영향을 미칠 것으로 판단하였다. Isoorientin에 의한 iNOS와 COX-2 발현 억제효과를 확인한 결과 Fig. 6B와 C에서와 같이 LPS 단독 처리구인 대조구에 비해 LPS와 함께 isoorientin을 처리하였을 때 20µg/mL 정도의 농도에서 iNOS와 COX-2 단백질 expression의 억제효율이 높게 측정되었으며, 농도의존적으로 억제되는 경향을 확인하였다. iNOS 단백질 발현량은 Fig. 6B에서와 같이 isoorientin 100µg/mL의 처리농도에서 LPS 단독 처리구에 비해 약 80% 이상의 저해효과를 나타내었고, COX-2 발현량은 Fig. 6C에서와 같이 100µg/mL의 농도에서 약 65% 정도의 저해효과를 나타내었다. 이러한 결과는 NO와 PTGES2 m-RNA 생성율 저해양상과 유사한 pattern으로, NO와 PTGES2의 생성에 관여하는 iNOS와 COX-2 단백질 expression도 농도의존적 감소경향을 나타내어 이들의 상관관계가 입증되었다.
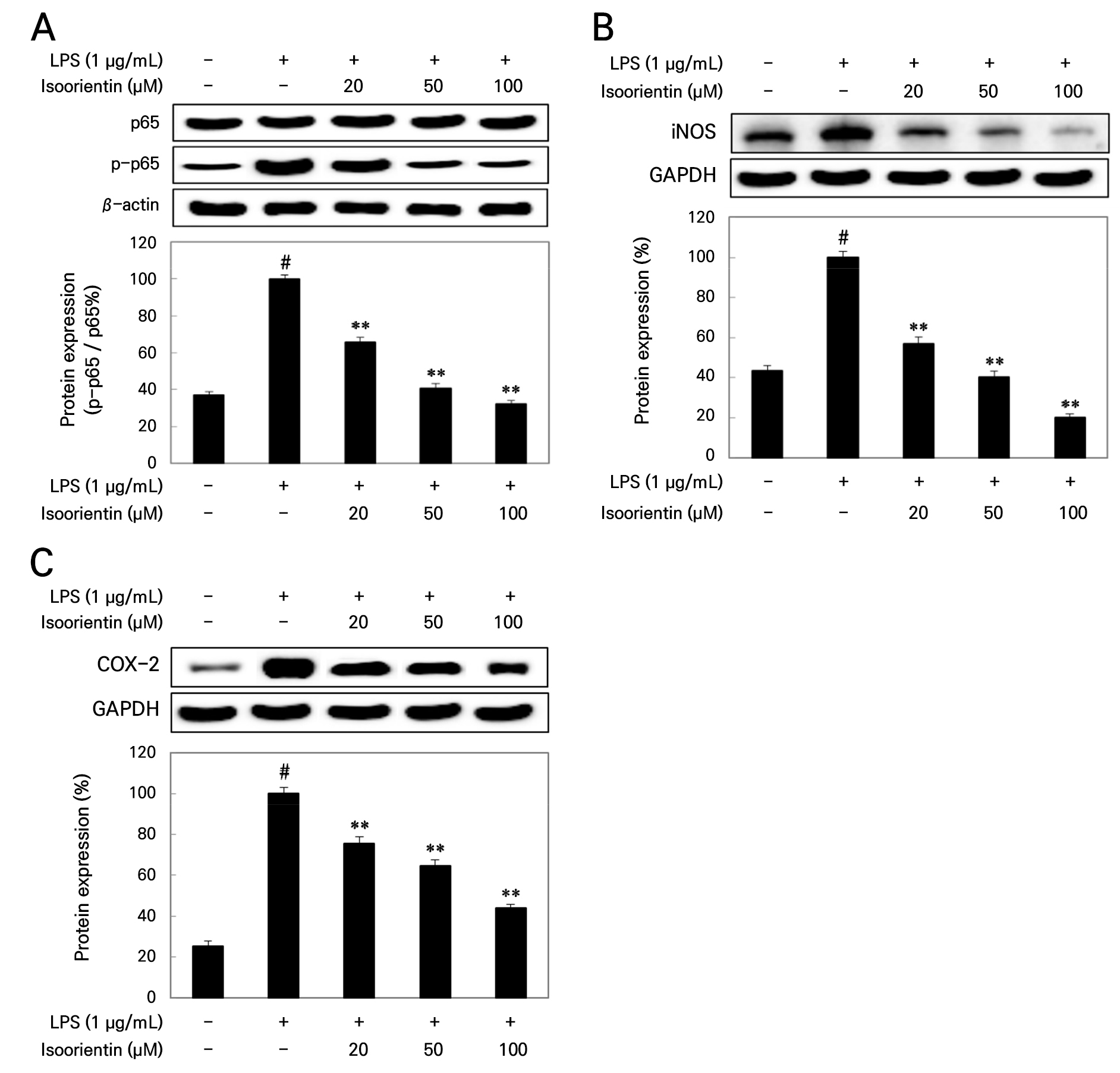
Fig. 6.
Inhibitory effects of isoorientin against p65 (A), iNOS (B) and COX-2 (C) expression levels, where raw 264.7 cells were stimulated with LPS (1 µg/mL) for 18 hr. Mean±standard deviation (n = 3); #p < 0.05, compared with the LPS non-induced group (Nor); and **p < 0.05, compared with the only LPS-induced group (Con).
외부 자극에 의해 NF-κB 경로로 염증반응이 조절되는데, NF-κB는 면역조절 및 염증반응 조절 등에 관여하는 단백질그룹으로 세포 내에서 신호전달 인자이다(Shin et al. 2012). NF-κB 복합체는 핵에서 iNOS나 COX-2 효소단백질을 생성하고, 염증성 cytokines 생성을 관장하는 유전자 promoter와 결합하여 cytokine의 생성을 촉진한다(Rehman et al. 2012). NF-κB 복합체 중 인산화된 p65 단백질은 염증매개물질인 iNOS와 COX-2의 발현량을 증가시키게 된다. 이때 대식세포의 자극으로 생성되는 iNOS는 과량 발현되면 cytokine 태풍 현상으로 인해 관절염, 다발성 경화증, 천식, 당뇨병 및 심혈관 질환 등 염증성 질병을 유발하는 것으로 알려져 있다(Lee et al. 2016b). 또한 Prostaglandin을 생성하는 COX-2 효소는 cytokine에 의해 염증 발생부위에서 감염, 혈관 확장, 암 발생에 관여한다. 따라서 isoorientin이 염증억제의 작용기전에서 prostaglandin 합성억제는 염증이 억제되는 효과를 나타내며, 이러한 COX-2의 생성 및 저해에 의해 조절되는 것(Jeong et al. 2013)을 iNOS와 COX-2 효소 단백질 expression을 억제하여 생성물인 NO와 PTGES2 m-RNA 발현을 효과적으로 억제하는 작용기전을 나타내는 것을 확인하였으며, 이를 통해 isoorientin이 항염증효과가 우수함을 확인하였다.
Isoorientin의 pro-inflammatory cytokine 및 chemokine 발현 억제효과
LPS 자극에 의한 염증반응의 주요 매개체인 TNF-α는 분비량이 많아져 염증반응을 일으키고 추가적으로 생성이 지속되면 NF-κB 활성화에 의해 염증을 발생시키고, 만성염증을 유발하는 것으로 보고하였다(Byun 2005). IL-6는 면역반응, 생체방어기작 등의 중요한 기능을 하는 인자로 LPS, cytokines 등에 의한 자극, virus 감염 등에 의해 생성이 많아지게 되면 악성종양 및 감염성 질환 등을 일으킨다(Hibi et al. 1696; Van 1990). IL-1β는 염증반응 시 생성되는 cytokine으로 염증반응에 중요한 역할을 한다. 생체내에서 IL-1β의 적절한 농도를 유지하면 항상성 유지가 가능하지만 과량 생산되면 T-cell이 활성화화 되고, B-cell이 성숙함으로서 염증증상을 악화시킨다(Kim et al. 2015). 본 연구에서 isoorientin의 cytokine의 생성억제 효과를 real-time PCR로 확인한 결과, Fig. 7에서와 같이 LPS 단독 처리구에 비해 LPS와 함께 isoorientin을 처리하였을 때 염증반응에서 농도의존적으로 cytokines의 생성을 저해하는 결과를 나타냈으며, TNF-α의 mRNA 발현량 저해효과는 Fig. 7A에서와 같이 isoorientin 100µg/mL의 농도에서 LPS 단독 처리구에 비해 약 30% 정도의 저해효과를 나타내었다. IL-1β의 mRNA 발현량 억제 효과는 Fig. 7B에서와 같이 100µg/mL 농도에서 LPS 단독 처리구에 비해 약 45%의 억제효과를 나타내어 isoorientin이 우수한 항염증 효과를 나타내는 것으로 판단되었다. IL-6의 mRNA 발현량 억제 효과는 Fig. 5C에서와 같이 100µg/mL 농도에서 LPS 단독 처리구에 비해 약 40% 정도의 억제효과를 나타내었다. 만성적인 염증반응 인자인 chemokine 중 monocyte chemoattractant protein(MCP)-1은 IL-1β, TNF-α 등에 반응하는 인자이다. MCP-1의 mRNA 발현량 억제 효과는 Fig. 7D에서와 같이 cyclooxigenase(COX)-2에 의하여 100µg/mL 농도에서 LPS 단독 처리구에 비해 70% 정도의 높은 억제효과를 나타내었다. PTGES2는 염증성 질환뿐만 아니라 생체반응에서 각종 질병을 유발시키거나 질병의 진행에도 관여하는 것으로 알려져 있다(Kim et al. 2010). Isoorientin의 PTGES2의 mRNA 발현량 저해 효과를 측정한 결과 Fig. 7E에서와 같이 isoorientin을 처리하였을 때, 농도 의존적으로 PTGES2 발현이 유의성 있게 감소하는 경향을 보였으며, 20–100µg/mL 농도에서 농도 의존적으로 억제효과를 나타냄을 확인하였다. Yun and Lee(2012)의 보고에 따르면 200µg/mL 농도의 금은화 물과 에탄올 추출물에서 각각 15.95%와 7.46%로 PTGES2 발현이 억제된다고 보고하였다. 상기의 금은화와 비교했을 때 isoorientin은 매우 높은 PTGES2 발현 저해효과를 나타내어 우수한 항염증 효과를 나타낼 것으로 판단되었다. Kim(2016)은 압척초 에탄올 추출물 500µg/mL 농도에서 39.54%의 억제 효과를 나타내었다고 보고한 것에 비하면 주름조개풀의 isoorientin은 상대적으로 매우 우수한 염증억제 효과를 나타내었다.
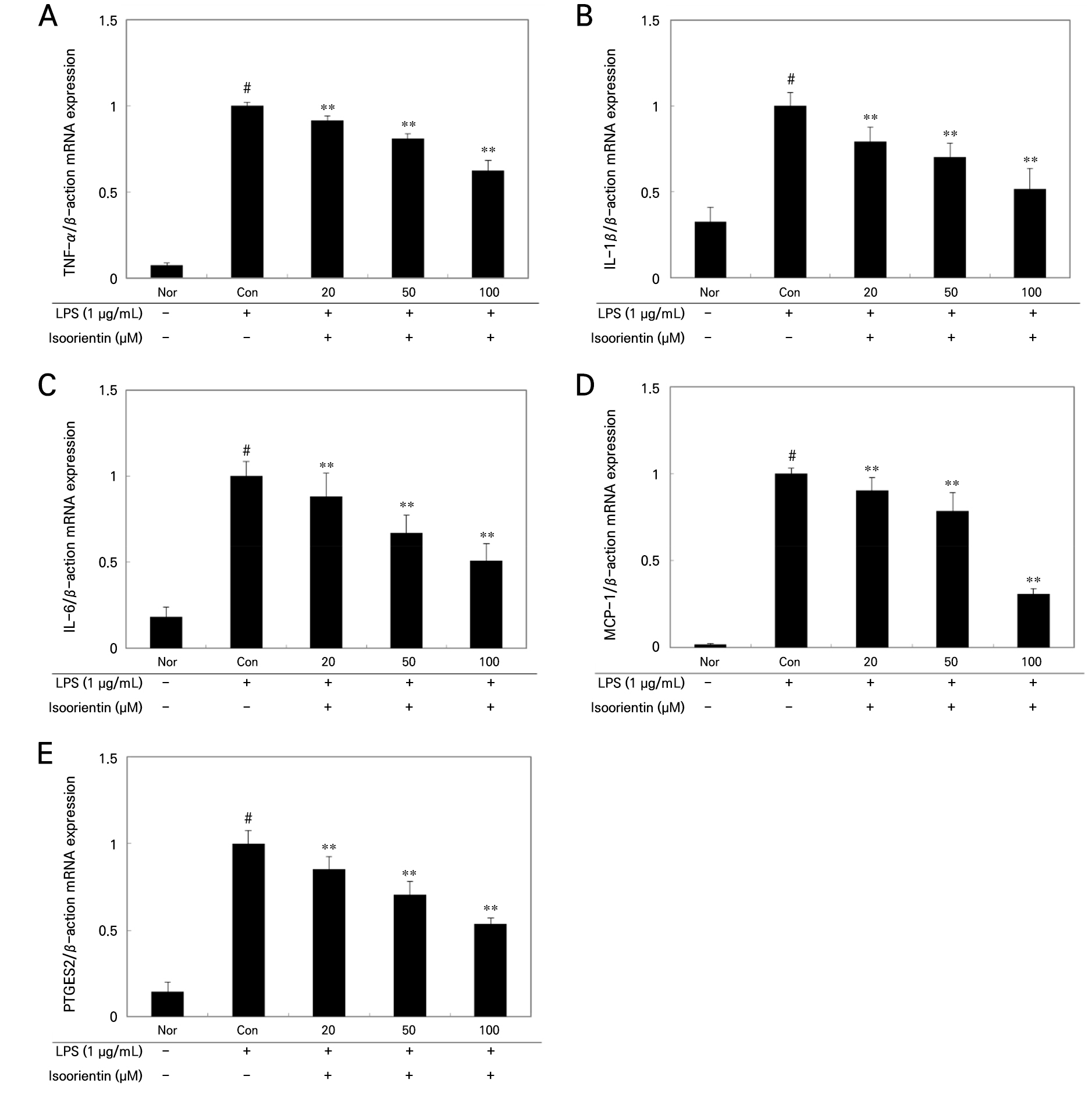
Fig. 7.
Inhibitory effects of isoorientin against the production of cytokines, where raw 264.7 cells were stimulated with LPS (1 µg/mL) for 18 hr. (A) TNF-α, (B) IL-1β, (C) IL-6, (D) MCP-1 and (E) PTGES2. Mean±standard deviation (n = 3); #p < 0.05, compared with the LPS non-induced group (Nor); and **p < 0.05, compared with the only LPS-induced group (Con).
이상의 결과에 따라, LPS로 자극된 Raw 264.7 cell에서 염증매게체인 iNOS, COX-2와 염증성 cytokine의 발현은 주름조개풀에 존재하는 isoorientin의 첨가 농도가 증가할수록 억제력이 높아지는 것을 확인하였다. 즉, isoorientin은 iNOS와 COX-2 단백질의 발현 억제 기작으로 인해 염증 반응에 관련된 NO, PTGES2, TNF-α, IL-6, IL-1β 및 MCP-1 생성을 억제하는 mechanism을 통하여 염증억제가 일어나는 것으로 확인되었다.