서 언
재료 및 방법
시험재료
포도의 소포자 또는 수 배우체 발달 단계 조사
포도의 꽃 발달 단계 조사
결 과
포도의 소포자 형성과 수 배우체 발달 단계
포도의 꽃 발달 단계 결정
특정 꽃 발달 단계를 갖는 화서와 포도나무의 잎 수
고 찰
서 언
상업적으로 재배되고 있는 거의 모든 포도 품종은 생식능력이 있는 수 기관(male organ)과 암 기관(female organ)을 모두 가진 꽃을 피운다. 포도 꽃은 5개의 수술, 1개의 암술, 5개의 꽃잎(petal)이 융합된 구조인 화관(flower cap; calyptra), 그리고 융합된 형태의 꽃받침(calyx) 구조를 가진다(Dokoozlian, 2000). 포도의 꽃 발달에 대한 연구는 꽃 발달을 조절하는 분열조직 정체성 유전자(meristem identity genes)나 꽃기관 정체성 유전자(floral organ identity genes)와 관련하여 MADS- box 도메인을 갖는 유전자를 중심으로 연구가 이루어져 왔으나(Boss et al., 2002; Fernandezl et al., 2013; Poupin et al., 2007) 꽃 발달과 관련된 해부학적 연구는 많이 보고되지 않았다. 포도의 잠아(latent bud) 출현을 0단계로 하고 화관이 떨어지기 직전의 꽃봉오리까지를 11단계로 나눈 보고가 있다(Srinivasan and Mullins, 1981). 이 연구에서는 화서에서 꽃받침이 발달하는 시기를 9단계, 화관이 출현하는 시기를 10단계, 개약 직전의 꽃봉오리를 갖는 시기를 11단계로 구분하였다. 즉 화관 출현부터 개화직전의 발달 단계를 두 단계로만 구분하였다. 포도 꽃 내부의 소포자(microspore) 또는 수 배우체(male gametophyte)의 발달은 ‘Pinot noir’와 ‘Gerwurztraminer’의 두 품종을 대상으로 특정 발달 단계에서 보고된 바 있다(Lebon et al., 2008).
포도나무의 발달 단계는 전체 나무 발달을 47단계로 나눈 ‘수정된 E-L 시스템’이 많이 사용되는데(Coombe, 1995), ‘Pinot noir’와 ‘Gerwurztraminer’의 두 품종에서는 ‘수정된 E-L 시스템’ 12단계에서 소포자를 형성할 포자성 조직(sporogenous tissue)이, ‘수정된 E-L 시스템’ 21단계에서는 성숙한 화분(mature pollen)이 발달하였다. 그러나 ‘수정된 E-L 시스템’ 15-17단계에서의 두 품종은 소포자 또는 화분의 발달 단계가 달랐다. 그러나 이 보고에서는 꽃밥(anther)의 절편을 이용하여 광학현미경으로 소포자 또는 화분을 관찰하였기 때문에 소포자 내 핵(nucleus)이나 액포(vacuole)의 존재, 생식핵(generative nucleus), 영양핵(vegetative nucleus)을 구분할 수 없었다. 한편 ‘Loureiro’ 품종의 경우 다양한 현미경을 사용하여 화분립의 외관, 꽃밥 내 화분발달, 화분 내 생식핵과 영양핵의 구분, 화분의 활력(viability), 화분관의 신장 등이 보고되었다(Abreu et al., 2006). 그러나 현재까지 포도 꽃 발달 단계를 세분화하거나 포도 꽃 발달 단계에 따른 소포자 또는 수배우체의 상세 구조에 대한 보고는 거의 없다.
완전화(perfect flower)를 갖는 식물 중에서 꽃 구조와 꽃 발달 과정이 잘 연구된 예는 애기장대가 있다. 애기장대의 꽃은 꽃받침 4장, 꽃잎 4장, 수술 6개, 암술 1개로 이루어져 있다. 꽃 발달은 꽃 원기(flower primodia)가 출현하는 시기부터 종자가 떨어질 때 까지를 20단계로 구분한다(Bowman et al., 1991; Müller, 1961; Smyth et al., 1990). 특히 개화시기인 13단계 이전의 꽃 발달 시기가 특히 잘 연구되어 있다. 꽃 발달의 지표로는 꽃 기관의 상대적인 길이, 구조나 색 변화 등을 사용한다. 꽃 발달 단계에 따른 배우체의 발달도 잘 보고되어 있는데, 비교적 분석이 쉬운 소포자 또는 수 배우체의 경우, 꽃 발달 단계에 따른 화분 발달과 수술의 전반적인 구조에 대해 잘 알려져 있다. 즉 꽃 발달 9단계에서는 화분모세포(pollen mother cell; microspore mother cell) 부터 4분포자(tetrad)까지 분포하고 꽃 발달 10단계에서는 단세포성 소포자(unicellular microspore)가, 꽃 발달 11단계부터 12단계까지는 2번의 유사분열이 일어나 3세포성 화분(tricellular pollen)이 만들어진다(Bowman et al., 1991; Regan and Moffatt, 1990; Borg et al., 2009). 수 배우체에서의 많은 돌연변이체 연구는 화분 발달이나 꽃 발달 단계에 대한 상세한 연구의 토대 위에 수행되었다(Berger and Twell, 2011; Twell, 2011). 그러나 애기장대의 꽃 발달 단계를 포도 꽃에 그대로 적용하기에는 두 종의 꽃 구조나 특징이 달라서 한계가 있다.
본 연구에서는 포도 ‘캠벨얼리(Vitis laruscana)’와 ‘탐나라(V. spp.; Park et al., 2004)’ 품종의 꽃 발달 단계를 결정하기 위하여 비교적 발달 단계 측정이 용이한 소포자 또는 수 배우체의 발달 과정을 관찰하고, 소포자 또는 수 배우체 발달 단계가 동일한 꽃에서 공통적인 형태적 특징을 찾고자 했다. 포도 꽃의 발달 단계 구분은 애기장대를 기준으로 수 배우체의 발달이 시작되는 꽃봉오리(flower bud)부터 화관이 탈락하는 시기까지만 세분화하였다. 또한 포도 화방(rachis)을 구성하는 개별적 꽃의 외형적인 특징을 보고 꽃 발달 단계를 판정할 수 있는 기준도 마련하였다. 본 연구 결과는 ‘캠벨얼리’와 ‘탐나라’ 품종의 세분화된 꽃 발달 기준이 필요할 때 유용하게 이용될 수 있을 것이다.
재료 및 방법
시험재료
시험재료는 농촌진흥청 국립원예특작과학원의 비가림 시설이 설치된 포장에서 재배 중인 유핵포도 ‘캠벨얼리’와 ‘탐나라’를 사용하였다. 실험재료의 채취는 2013년 여름과 2014년 여름, 2년에 걸쳐 수행하였다.
포도의 소포자 또는 수 배우체 발달 단계 조사
소포자 또는 수 배우체 발달 단계를 조사하기 위해 화관이 탈락하기 이전의 꽃봉오리로부터 꽃밥을 분리하였다. 소포자 또는 수 배우체 발달 정도에 따라 꽃밥을 잘게 찢거나 꽃밥 안쪽 조직에서 화분을 긁어낸 후 화분을 슬라이드 글라스에 얇게 펼쳐 염색하였다. 핵 발달을 확인하기 위해 DAPI (4',6-diamidino-2-phenylindole; Sigma, USA) staining solution (0.1 M sodium phosphate, pH 7, 1mM EDTA, 0.1% Triton X-100, 0.5μg・mL-1 DAPI)을 처리하였다. 화분의 전반적인 형태와 핵 발달 상태는 광학과 형광 조건에서 각각 현미경(BX53F-32S, Olympus, Japan)으로 관찰하였다.
포도의 꽃 발달 단계 조사
포도 꽃봉오리와 꽃의 형태적 특징은 해부현미경(Stemi SV11, ZEISS, Germany)과 주사전자현미경(Scanning Electron Microscope, SEM; S-4800, HITACHI, Japan)으로 관찰하였다. 포도 꽃의 발달 단계는 애기장대의 연구를 근거로 하여 포도 꽃에서 소포자발생(microsporogenesis) 부터 화관이 탈락하는 시기에 한정하여 결정하였다. 시험재료인 두 품종 ‘캠벨얼리’와 ‘탐나라’의 꽃 발달 단계를 기술할 수 있는 기준을 마련하고자 각 꽃 발달 단계에 해당하는 꽃봉오리에서 꽃 기관별 길이와 폭 등을 측정하였다. 정확한 기관의 길이 측정을 위해 각 꽃봉오리는 1% agar 배지에 올려두고 해부현미경으로 촬영한 후, 각 기관의 길이를 ImageJ 프로그램(1.47v, National Institutes of Health)을 사용하여 측정하였다. 또한 꽃 발달 단계 동안 각 기관의 색깔과 형태도 조사하였다. 형태분석에는 최소 10개 이상의 꽃봉오리를 사용하였다. 실험에 사용한 두 품종 ‘캠벨얼리’와 ‘탐나라’의 기관별 길이와 크기에 대한 측정값과 분산에 대한 차이는 T-test와 F-test로 검정하였다.
결 과
포도의 소포자 형성과 수 배우체 발달 단계
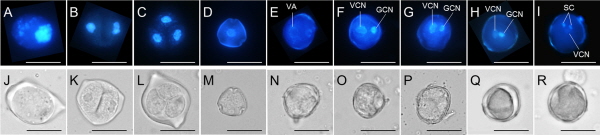
포도에서 꽃 발달 단계를 명확하게 구분하기 위해 수 배우체의 발달 과정을 조사하였다(Fig. 1). 그 결과, 생식세포로의 분열이 개시되는 화분모세포(Fig. 1A, J), 제1 감수분열(meiosis I)이 일어난 2핵 상태인 2분포자(Fig. 1B, K), 제2 감수분열(meiosis II)까지 일어난 반수체인 4개의 4분포자(Fig. 1C, L)를 관찰할 수 있었다. 4분포자는 4개의 소포자가 각각 분리되어 하나의 핵을 가지는 단세포성 소포자(Fig. 1D, M)와 핵과 커다란 액포를 가진 극성 소포자(polarized unicellular microspore)로 분화하였고(Fig. 1E, N), 이후 첫 번째 유사분열(mitosis I)이 일어나서 불균등한 크기의 핵 2 개를 가진 2세포성 화분(bicellular pollen)으로 분화하였다. 2세포성 화분은 초기(Fig. 1F, O), 중기(Fig. 1G, P), 말기(Fig. 1H, Q)의 3단계로 나눌 수 있었는데, 초기는 큰 영양핵이 중앙에 위치하고 상대적으로 크기가 작은 생식핵이 세포막 쪽으로 위치하여 두 핵 사이의 거리가 멀었다. 중기에는 생식핵이 세포의 중앙으로 이동했고, 말기에는 생식핵과 영양핵 사이의 거리가 가까워져서 거의 붙어 있는 것처럼 보였다. 생식핵이 유사분열(mitosis II)을 하여 두 개의 정세포(sperm cell)가 형성됨으로써 3개의 핵을 가진 3세포성 화분(Fig. 1I, R)으로 발달하였다. 3개의 핵은 일정 간격으로 위치하다가 성숙한 화분(muture pollen)이 되면 핵들이 중앙에 집중되었다.
포도의 꽃 발달 단계 결정
포도의 꽃 발달 단계는 소포자 형성과 수 배우체의 발달 과정을 기준으로 결정하였다. 애기장대의 경우 반수체인 소포자가 출현하는 시기가 꽃 발달 9단계이고 개화하여 꽃밥이 터지는 시기가 꽃 발달 13단계이다. 따라서 포도 꽃의 발달 단계 결정은 애기장대의 꽃 발달 9단계부터 13단계에 해당하는 수 배우체 발달에 의해 추정할 수 있는 꽃 발달 단계로 한정하였으며 특정 발달 단계의 수 배우체를 70% 이상 갖는 애기장대의 꽃 발달 단계를 기준으로 하여 포도의 꽃 발달 단계를 결정하였다. 즉 4분포자가 나타나는 시기를 꽃 발달 9단계, 단세포성 소포자와 극성 소포자가 나타나는 시기를 꽃 발달 10단계, 초기와 중기 2세포성 화분이 나타나는 시기를 꽃 발달 11단계, 말기 2세포성 화분과 3세포성 화분, 성숙한 화분이 혼재하는 시기를 꽃 발달 12단계, 화관이 떨어지고 꽃이 개화한 시기를 꽃 발달 13단계로 결정하였다.
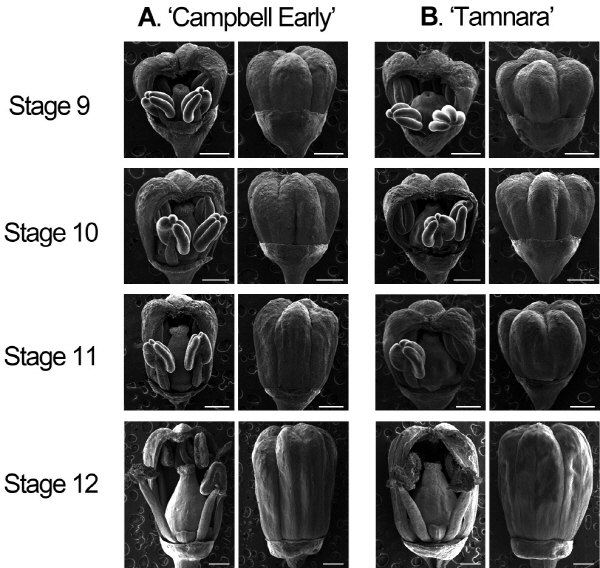
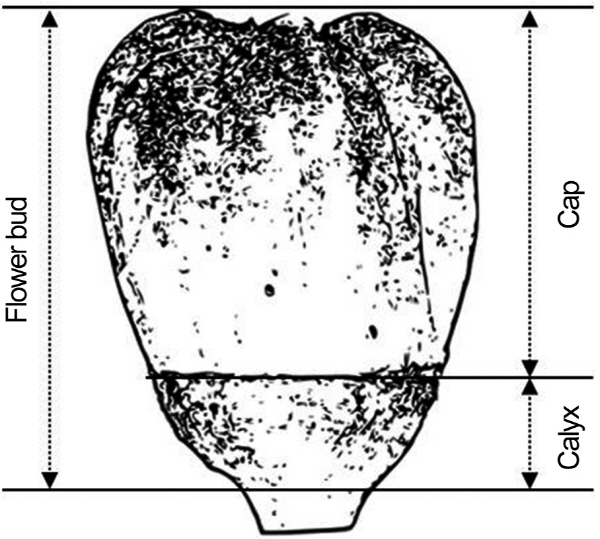
‘캠벨얼리’와 ‘탐나라’의 두 품종에서 꽃 발달 단계별 꽃봉오리를 내부구조가 보이는 상태와 외관만 보이는 상태로 각각 주사전자현미경으로 관찰하였다(Fig. 2). Table 1에는 각 꽃 발달 단계에서 포도의 두 품종에 대한 꽃 기관의 특징을 애기장대의 꽃 발달 단계의 특징과 함께 정리하였다. 즉 포도의 두 품종에서 꽃의 각 발달 단계에 따른 소포자 또는 수 배우체의 발달 단계, 꿀샘(nectary)의 출현, 암술머리의 특징, 꽃밥 색 변화 등을 정리하였다. 꽃 발달 9단계와 10단계의 꽃봉오리는 화방에서 화축(primary branch) 1/3상단과 어깨송이(shoulder)를 제외한 나머지 부분에서 채취하였으며, 꽃 발달 11단계 이상 되는 꽃봉오리는 화축과 어깨송이 모두에서 상단 1/3부분을 제외한 부분에서 채취하였다. 어깨송이란 화방의 주축(main axis)에서 돌출된 가지를 일컫는다(Fig. 3).
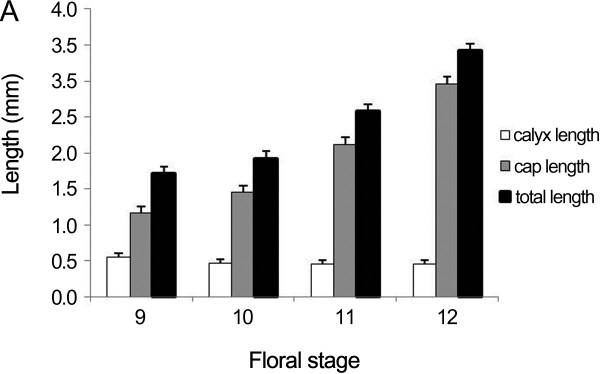
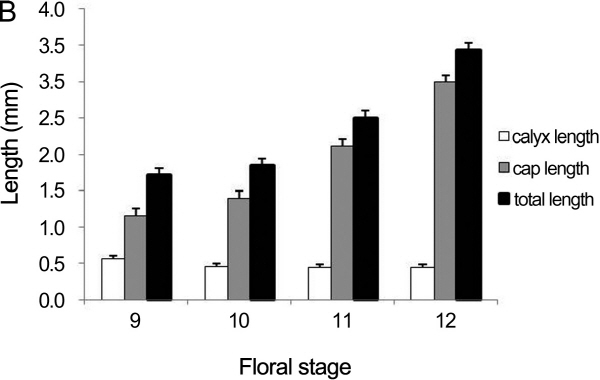
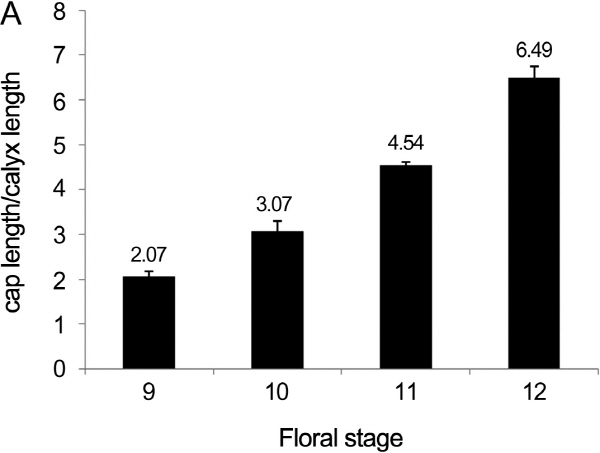
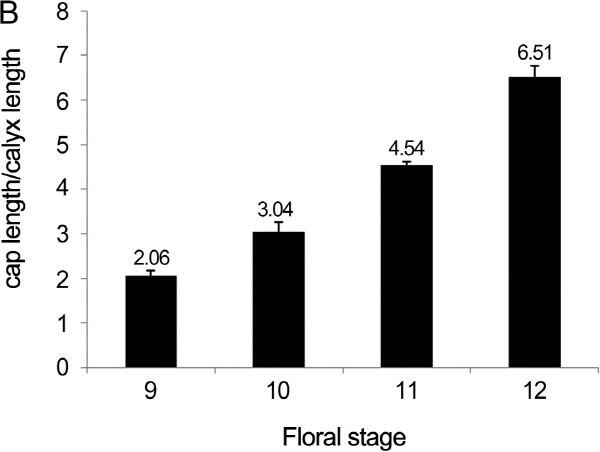
꽃의 외관으로 꽃 발달 단계를 판별할 수 있는 지표를 마련하고자 각 발달 단계별로 꽃봉오리에서 화관의 길이와 꽃받침의 길이를 측정하였다(Fig. 4). 그 결과, 꽃받침 길이는 꽃 발달 단계 변화 동안 거의 변하지 않은 반면, 화관의 길이는 꽃 발달 동안 지속적으로 증가하였다(Fig. 5). 두 품종 사이에는 전체적인 꽃 길이, 화관, 그리고 꽃받침의 길이가 유사하였다. 두 품종 간에 화관의 길이와 꽃받침의 평균 길이와 분산에 차이가 있는지 판단하기 위해 T-test와 F-test를 수행하였다. T-test(p > 0.05) 결과 각 꽃 발달 단계에서 측정한 화관과 꽃받침의 평균 길이는 ‘캠벨얼리’와 ‘탐나라’의 두 포도 간에 통계적 차이가 없었으며 F-test(p > 0.05) 결과 두 포도 간에 화관과 꽃받침의 길이에 대한 분산도 통계적으로 유의한 차이는 없었다(Table 2). ‘꽃받침 길이에 대한 화관 길이의 비율’을 보면, 꽃 발달 9단계에서는 2.0, 꽃 발달 10단계에서는 3.0, 꽃 발달 11단계에서는 4.5, 꽃 발달 12단계에서는 6.5였다(Fig. 6).
‘꽃받침 길이에 대한 화관 길이의 비율’을 기준으로 꽃 발달 단계를 나누었을 때, 각 꽃 발달 단계가 특징적인 소포자 발달 단계를 갖는지를 확인하였다. ‘꽃받침 길이에 대한 화관 길이의 비율’이 동일한 꽃봉오리 2개를 채취하여 소포자 발달 단계를 조사하였다(Table 3). 꽃 발달 단계별 소포자는 각 꽃봉오리에서 90개 이상을 관찰한 결과, 꽃 발달 9단계에서는 4분포자의 비율이 95%, 꽃 발달 10단계에서는 단세포성 소포자의 비율이 100%, 꽃 발달 11단계에서는 중기 2세포성 소포자의 비율이 80%, 꽃밥이 터지지 않았던 꽃 발달 12단계에서는 말기 2세포성 소포자의 비율이 91.7%였다. 따라서 ‘꽃받침 길이에 대한 화관 길이의 비율’로 꽃 발달 단계를 결정할 수 있고, 이때 꽃 발달 단계에 따른 화분 발달 단계도 일치함을 확인하였다. 따라서 두 품종에서 꽃 발달 단계를 판별하는 기준으로 ‘꽃받침 길이에 대한 화관 길이의 비율’을 적용할 수 있는 것으로 나타났다.
특정 꽃 발달 단계를 갖는 화서와 포도나무의 잎 수
‘캠벨얼리’와 ‘탐나라’ 두 품종의 특정 꽃 발달 단계를 갖는 화서의 특징과 이때 포도나무의 잎 수와의 관계를 분석하였다. 포도의 ‘수정된 E-L 시스템’에 따르면 첫 번째 화서를 볼 수 시기가 12단계이며, 이때 잎 수는 5번째 잎과 6번째 잎이 완전히 펴지지 않은 상태이다. 그러나 2013년과 2014년도 첫 번째 화방을 조사한 바에 따르면 꽃 발달 9단계를 갖는 화방이 출현할 때, 포도나무의 잎 수는 년도에 따라 차이가 있었지만 3-5장만을 가졌다. 꽃 발달 10단계는 4.5-6.5장, 꽃 발달 11단계는 7-9장, 꽃 발달 12단계는 9-11장을 가졌다. 이러한 결과는 포도 품종과 생육환경에 따라 잎 수가 달라질 수 있기 때문에 화방 내 꽃 발달 단계를 판정할 때는 ‘꽃받침 길이에 대한 화관 길이의 비율’로 개별적인 꽃 발달 단계를 파악하는 것이 더 정확할 것으로 사료된다(Table 4).
고 찰
대부분 포도 재배종의 꽃은 수 배우체와 암 배우체를 모두 갖는 완전화이다. 본 연구에서는 완전화를 갖는 포도 중 ‘캠벨얼리’와 ‘탐나라’ 두 품종의 꽃 발달 단계를 세분화하기 위해 비교적 분석이 용이한 소포자 또는 수 배우체 발달 과정을 관찰하고 이에 근거하여 꽃 발달 단계를 설정하였다. 또한 각 꽃 발달 단계를 외관상으로 구분할 수 있게 하는 형태적 특징들을 조사한 결과, 화관과 꽃받침의 상대적인 길이를 이용하면 꽃 발달 단계를 정확하게 결정할 수 있음을 확인하였다. 본 연구 결과는 ‘캠벨얼리’와 ‘탐나라’의 두 품종에서 꽃 발달 단계별 형태적 특징이 통계적으로 일치함을 보였다. 본 연구에 쓰인 ‘탐나라’의 경우 자방친이 ‘캠벨얼리’이기 때문에 두 품종에서 측정된 생육 지표의 유사성은 이들 품종이 유전적으로 가깝기 때문에 나타난 결과일 수 있다. 포도의 외형적인 형태적 발달과 배우체 발달은 품종마다 차이가 있는 것으로 알려져 있는데(Lebon et al., 2008), 이러한 현상이 잎 수에 근거한 ‘수정된 E-L 시스템’의 발달 단계의 한계 때문인지, 동일한 ‘꽃받침 길이에 대한 화관 길이의 비율’ 지표를 적용했을 때도 차이를 보이는지에 대해서는 추가 연구가 필요하다.
다양한 포도 품종을 대상으로 많은 해부학적 연구들이 보고되었고, 형광현미경을 이용한 화분의 활력 연구도 많이 수행되었지만 소포자 형성이나 수 배우체 발달에 대해 핵과 소기관의 배열과 같은 상세한 발달 단계 연구가 이루어진 바 없다. 따라서 본 연구가 비록 두 품종에서의 소포자 형성과 수배우체 발달에 대한 보고이지만 관련 연구에 좋은 기초자료가 될 것으로 기대한다.
포도나무의 발달 단계 측정을 위한 지표로는 1977년 Eichhorn and Lorenz에 의해 발표된 ‘E-L 시스템’을 사용한다. 그러나 현재 더 많이 사용되는 것은 1995년 Coombe에 의해 발표된 ‘수정된 E-L 시스템’이다. ‘수정된 E-L 시스템’ 역시 처음 발표된 ‘E-L 시스템’처럼 포도나무의 발달을 47단계로 나누었다. 그러나 ‘수정된 E-L 시스템’은 포도나무 전반적인 발달 단계를 나누는 기준이기 때문에 포도 화방 내의 꽃 발달 단계를 측정하기 위해서는 세분화한 꽃 발달 단계의 기준이 필요하다. 특히 포도의 소포자 배양(microspore culture)이나 무핵 유도를 위한 개화 이전의 GA 처리 등을 위해서는 정확한 꽃 발달 시기가 중요하다. Srinivasan and Mullins(1981)는 화방에서 개별적인 꽃을 구분할 수 있는 시기를 2단계로만 구분하였다. 본 연구에서는 꽃 발달 단계를 훨씬 세분화하여 꽃봉오리를 꽃 발달 9단계부터 12단계의 4단계로 구분함으로써 체계적인 꽃 발달 단계를 적용할 수 있게 하였다. 일반적으로 소포자 배양은 단세포성 소포자 시기부터 초기 2세포성 화분 시기에서 수행하는데(Seguí-Simarro and Nuez, 2008), 본 연구 결과를 적용한다면 이는 꽃 발달 10단계부터 꽃 발달 11단계 초반에 해당한다. 또한 무핵 유도를 위한 GA 처리는 경험적으로 꽃 피기 14일 전에 수행하는데 ‘수정된 E-L 시스템’에 따르면 15단계에 처리한다(Jung et al., 2014). ‘수정된 E-L 시스템’의 15단계의 잎 수는 8장이며, 화방의 특징은 개개의 꽃을 구분할 수 있는 시기이다. 본 연구의 결과를 적용해보면 이 시기는 소포자 배양 최적시기와 유사한 꽃 발달 10단계부터 꽃 발달 11단계 초기에 해당되는 것으로 판단된다. 따라서 본 연구에서 제시한 꽃 발달 단계의 지표인 ‘꽃받침 길이에 대한 화관 길이의 비율’을 이용한다면 ‘캠벨얼리’와 ‘탐나라’의 두 품종에서의 소포자 배양에 유용하게 활용될 수 있으며, ‘탐나라’ 품종의 경우 무핵화 처리에도 응용할 수 있을 것으로 사료된다.