서 언
재료 및 방법
식물재료 및 재배
광계II 활성 분석
항산화효소 활성 분석
생육특성 및 생산성
통계분석
결 과
마늘의 초기 생육
마늘 잎의 광계II 활성
마늘의 생산성
마늘의 항산화효소 활성
고 찰
서 언
마늘(Allium sativum L.)은 백합과 파속에 속하는 인경채소작물로 향신료자원으로 세계적으로 널리 재배되고 있다. 더군다나, 항암, 혈중 콜레스테롤 저하, 혈압 강하 등 다양한 기능성이 밝혀지면서 약용자원으로도 활용되고 있을 뿐만 아니라 세계 10대 건강식품으로 선정되어 소비량이 꾸준히 증가하고 있다. 마늘은 생육초기 일정기간의 저온기를 거친 후 고온과 장일 조건에서 인경비대가 시작되는 특성을 가지고 있기 때문에(Bandara et al., 2000; Rahim and Fordham, 2001), 우리나라에서는 가을에 파종하여 겨울의 저온기를 거친 후 이듬해 초여름에 수확을 하고 있다(Song et al., 2001). 마늘의 출하시기가 계절적으로 여름철에 집중되다 보니 계절에 따라 가격차가 크고, 마늘을 수확하여 저장하는 동안의 고온다습으로 중량 감소나 부패 등으로 인한 손실이 큰 것으로 알려져 있다(Cho and Lee, 2008). 따라서 일부 지역에서는 출하시기를 조절하기 위하여 비닐하우스 내에서 재배하거나 멀칭하여 조기재배를 시도하기도 한다(Hwang and Tae, 2000). 그러나 멀칭하여 재배하였을 때 조기수확이 가능하고 수확량이 많아지는 잇점이 있지만 지온 상승으로 인해 고온 장해나 벌마늘이 발생하는 문제점이 제기되고 있다(Choi et al., 2009). 따라서 마늘의 안정적 생산을 위해서는 재배관리 측면에서 고온장애가 일어나지 않으면서 조기수확이 가능한 저온기의 적정 재배온도를 규명할 필요가 있다.
한편, 온도는 식물의 생장과 발달에 있어 중요한 환경인자이며, 생육적온을 벗어난 고온이나 저온은 작물의 생산성과도 직결된다. 일례로서 고온은 광계II(photosystem II)와 같은 광합성기구에 직・간접적으로 손상을 줄 수 있어(Takahashi and Murata, 2008; Yoshioka et al., 2006), 고온에 노출된 작물은 광합성량의 감소로 인해 생산량이 감소, 품질의 저하 등이 초래될 수 있다. 즉, 고온에서 틸라코이드 라멜라에서의 광화학적 반응과 엽록체 스트로마에서 탄소대사는 고온 장해의 주요 부위이며, rubisco 활성과 캘빈회로의 주요 효소 활성을 감소시킨다. 고온이 식물체에 미치는 악영향은 물질대사, 광합성 능력, 광화학적 효율의 저하로 나타나며, 식물의 생장은 광합성과 탄소 획득의 감소로 영향을 받는다. 더욱이 광계II 활성은 환경 스트레스에 민감하여 식물 스트레스 분석을 위한 지표로 사용되고 있다(Ball et al., 1994; Oh et al., 2014; Strasser and Strasser, 1995). 특히, 식물의 잎에 빛을 조사하여 방출되는 형광의 시간대별 밀도를 나타내는 OKJIP 곡선(OKJIP transient curve)의 분석으로 광계II에서의 에너지 흐름의 변화와 전자수용체의 환원 등 다양한 정보를 정량적으로 얻을 수 있다(Strasser et al., 2000). 그리고, 식물이 스트레스를 받으면 생체내 산소는 반응성이 높은 독성의 활성산소종(reactive oxygen species)으로 변하며(Alscher and Hess, 1993), 이들은 강한 산화력을 가지고 있어 핵산, 단백질, 지질 등의 변성과 광합성 억제 등 심각한 생리적 장애를 일으키고, 결국 식물체를 고사시킨다(Alscher and Hess, 1993; Asada, 1999). 고온 스트레스 하에서의 광계II 활성의 감소, 엽록체 효소의 불활성화, 엽록소 함량의 감소 또한 활성산소종에 의한 산화적 스트레스에 의해 야기되는 것으로 알려지고 있다(Kumar et al., 2013). 그러나 스트레스에 의해 과다하게 생성되는 활성산소종은 peroxidase, catalase, superoxide dismutase 등의 항산화효소의 작용으로 제거되며 스트레스 하에서 식물의 생존 또는 내성과 관련이 있음으로 항산화효소 활성의 분석은 환경 스트레스의 지표로 사용될 수 있으며 식물의 생존 가능한 한계 범위를 파악하는데 이용될 수 있다(Foyer et al., 1991).
따라서, 본 연구에서는 마늘의 초기생장 시 고온 스트레스의 영향을 밝히고 적합한 재배온도 범위를 알아보기 위하여 온도를 달리한 조건에서 재배하여 생육 특성과 광계II 활성, 그리고 항산화효소 활성을 조사하였다.
재료 및 방법
식물재료 및 재배
본 실험에 사용한 마늘(A. sativum L.)은 한지형인 단양종(‘Danyang’)이며, 3-4g 정도의 크기가 중간 정도인 건전한 인편을 종구로 사용하였다. 상토가 들어있는 포트에 인편을 하나씩 파종한 후, 10°C의 온도와 100μmol・m-2・s-1의 광량으로 14h/10h 명암의 주기로 10일간 재배하여 발아시켰다. 맹아가 일정하게 나온 유식물체를 10-30°C의 범위에서 온도를 5°C 단위로 설정한 생장상 형태의 밀폐형 시스템(Cold bank, Samwon Technique & Research Co., Korea)에서 각 온도별로 유식물 30주씩 3반복으로 재배하였다. 재배 후 15일째에 마늘의 생육특성, 광계II 활성, 항산화효소 활성 등을 조사하였으며, 30일째에는 마늘의 각 부위별 건중량을 조사하였다.
광계II 활성 분석
광계II 활성은 엽록소형광분석기(Plant Efficiency Analyzer, Hansatech Instrument Ltd., King’s Lynn, UK)를 이용하여 분석하였다(Strasser and Strasser, 1995). 15분간 광을 차단하여 암적응시킨 마늘의 잎에 1,500μmol・m-2・s-1의 광량을 5초간 조사하여 OKJIP곡선을 유도하였다. Time scale은 10μs에서 1s의 범위로 설정하고, 10μs에서 2ms까지는 1μs단위로, 2ms에서 1s까지는 1ms 단위로 인식하도록 하였으며, 50μs(O-단계), 300μs(K-단계), 2ms(J-단계), 30ms(I-단계), 500ms (P-단계)에서 엽록소형광 밀도를 분석하였다(Srivastava et al., 1997). OKJIP 곡선의 분석으로 기본적 형광변수(Fo, Fm, Fv/Fo, Fv/Fm)들과 광계II의 활성 상태의 반응중심의 밀도(RC/CSm), 반응중심을 통한 에너지 흐름의 변화(ABS/CSm, TRo/CSm, ETo/CSm, DIo/CSm) 등을 정량적으로 산출하여 제시하였다.
항산화효소 활성 분석
식물체의 잎과 뿌리를 1.0g씩 취하여 0.1M Tris-HCl 완충용액(pH 8.0; 1mM phenylmethylsulfonyl fluoride, 25μM polyvinyl-pyrrolidone, 0.1mM ethylenediamine tetraacetic acid, 0.5% Triton X-100) 10mL와 함께 얼음 위의 막자사발에서 마쇄한 후, 4°C에서 10,000×g으로 30분간 원심분리하여 얻은 상징액을 조효소액으로 사용하였다. 전기영동은 Laemmli (1970)의 방법을 변형하여 native gel 조건에서 실시하였다. 전기영동 시료는 효소액을 동량의 시료용 완충용액(125mM Tris-HCl, pH 6.8; 0.005% bromophenol blue, 40% glycerol, 5% β-mercaptoethanol)과 혼합하여 사용하였다. 전기영동 시 superoxide dismutase(SOD)는 10% running gel을, catalase (CAT)와 peroxidase(POD)는 7.5%의 running gel을 사용하였으며, stacking gel은 3% gel을 사용하였다. 시료를 vertical slab gel에 loading하여 stacking gel에서는 50V, running gel에서는 100V로 전개하였다. POD 활성은 50mM potassium phosphate 완충용액(pH 7.8; 10mM H2O2)에 전기영동이 끝난 겔을 10분 동안 담근 후 염색액(1.4mM 3,3′-diaminobenzidine tetrahydrochloride)에 담가 어두운 곳에서 반응시켜 나타나는 밴드로 조사하였다(Rao et al., 1996). SOD 활성은 riboflavin/ nitro blue tetrazolium 염색 방법을 사용하여 조사하였다(Beauchamp and Fridovich, 1971). 전기영동이 끝난 겔을 2.45mM nitro blue tetrazolium 용액에 넣어 어두운 곳에 20분간 둔 후, 반응용액(36mM potassium phosphate, pH 7.8; 28mM TEMED, 28μM riboflavin)에 넣어 암상태에서 15분간 진탕하고, 빛을 조사하면서 5-10분간 반응시켜 나타나는 밴드를 조사하였다. SOD isoenzyme 특성을 분석하기 위해서는 전기영동이 끝난 겔을 3mM H2O2 또는 2mM KCN 용액에 담가 30분간 진탕한 후 동일한 방법으로 SOD를 검출하였다. CAT 활성은 ferricyanide 염색법을 사용하여 조사하였다(Woodbury et al., 1971). 전기영동이 끝난 겔을 3.27mM H2O2가 함유된 증류수에 넣어 암상태에서 10분간 반응시킨 후 반응용액(3.7mM ferric chloride, 3mM potassium ferricyanide)에 넣어 5-10분 후에 나타난 밴드를 조사하였다.
생육특성 및 생산성
생육조사는 각 처리당 10주를 무작위로 선발하여 지상부 길이, 엽초경, 엽수, SPAD 값 등 마늘의 생육특성과 각 부위(지상부, 인경, 뿌리)별 건중량을 조사하였다. 지상부의 길이는 잎을 길게 늘어뜨렸을 때 인경 바로 윗부분에서부터 잎의 끝부분까지의 길이를 측정하였으며, 엽초경은 버니어캘리퍼스를 이용하여 맹아엽 하단부의 직경을 측정하였다. 엽수는 맹아엽을 제외한 주당 모든 엽수로 나타내었으며, SPAD 값은 엽록소계(SPAD-502, Minolta Co., Osaka, Japan)를 사용하여 2번째 잎의 중앙부위를 측정하였다. 건중량은 지상부, 인경, 뿌리로 구분하여 60°C 건조실에서 5일간 건조시켜 측정하였다. 또한 부수적으로 60일 동안 재배하면서 잎의 노화 여부와 녹색 상태의 엽수의 변화를 조사하였다.
통계분석
모든 통계분석은 SPSS 통계 패키지 18.0(SPSS, Chicago, IL, USA)를 이용하여 수행하였으며, Duncan의 다중검정(p < 0.05)으로 평균치간의 차이에 대한 유의성을 검정하였다. 그리고 재배온도, 식물체의 건중량과 엽록소형광 변수들 간의 관계는 Pearson 상관분석을 통하여 분석하였다.
결 과
마늘의 초기 생육
온도(10-30°C)를 달리하여 15일간 재배하였을 때, 지상부 길이는 25°C 조건에서 34.0cm로 가장 크게 자랐으며, 엽초경과 엽수는 15-25°C에서 각각 5.8-6.2mm, 4.4-5.0매로 엽초경이 더 굵고 엽수 또한 더 많았다(Table 1). SPAD값도 지상부 길이와 유사하게 25°C 조건에서 55.8로 그 이하 또는 이상의 온도에서보다 더 높았다.
마늘 잎의 광계II 활성
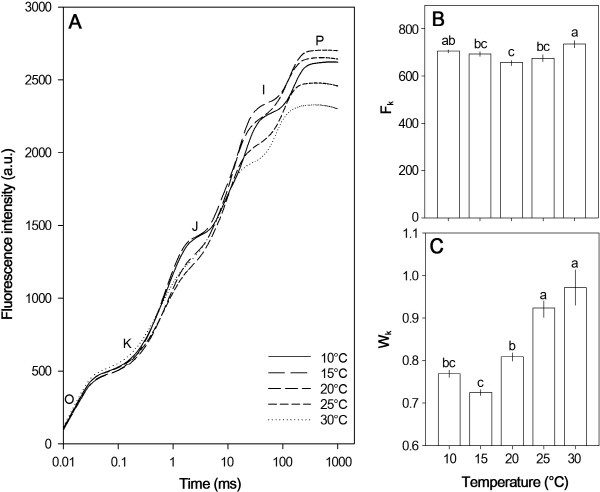
OKJIP 곡선의 변화를 보면, 15-20°C 온도에서 I와 P 단계에서의 형광밀도 Fi, Fp가 25-30°C 보다 높았다(Fig. 1A). 그리고 K 단계에서의 형광밀도 Fk는 20°C를 전후하여 다소 감소하였으나 30°C에서 다소 높았다(Fig. 1B). Wk 값은 15°C에서 가장 낮았으며 그보다 낮거나 높은 온도에서는 확연하게 증가하였다(Fig. 1C).
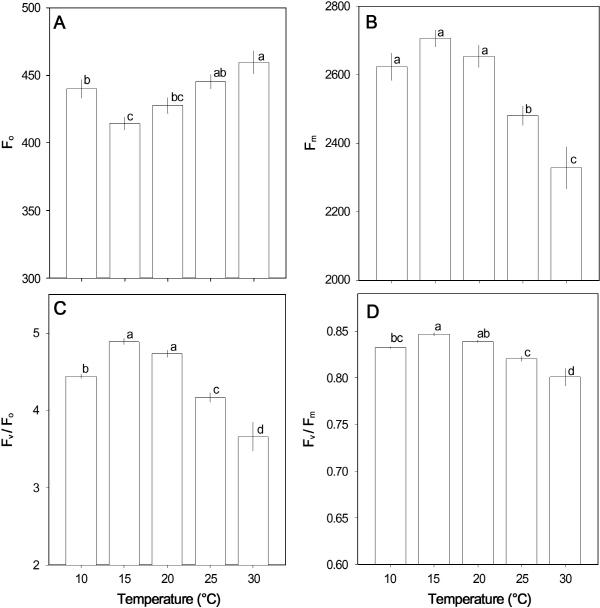
초기형광수율(Fo)은 15°C에서 가장 낮고 10°C 조건이나 20°C 이상에서는 크게 증가하였다(Fig. 2A). 최대형광수율(Fm)은 10-20°C 조건에서는 높았으나 25°C 이상의 온도에서는 낮았으며(Fig. 2B), 광계II의 잠재적 광합성능(Fv/Fo)과 광계II의 최대 광화학적 효율(Fv/Fm)은 15-20°C 조건에서 높았다(Figs. 2C and 2D).
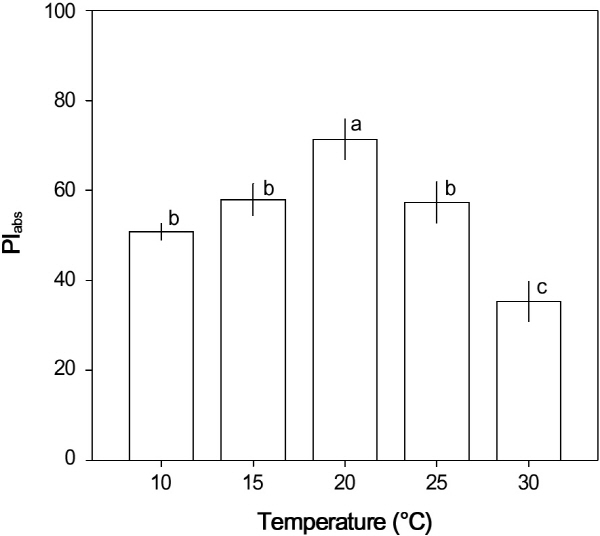
광계II의 활성 상태의 반응중심의 밀도(RC/CSm)와 에너지 흐름의 변화(ABS/CSm, TRo/CSm, ETo/CSm, DIo/CSm)를 나타내는 형광변수들 중에 RC/CSm, ABS/CSm, TRo/CSm은 10-20°C에서 높고, 그 보다 온도가 높아졌을 때 점차 감소하였다(Table 2). 그리고, ETo/CSm은 15-20°C에서 높았으며, DIo/CSm은 온도가 높아짐에 따라 점차 증가하여 30°C에서 가장 높았다. PIabs는 20°C에서 가장 높고 그 보다 온도가 낮거나 높아지면 감소하였다(Fig. 3).
마늘의 생산성
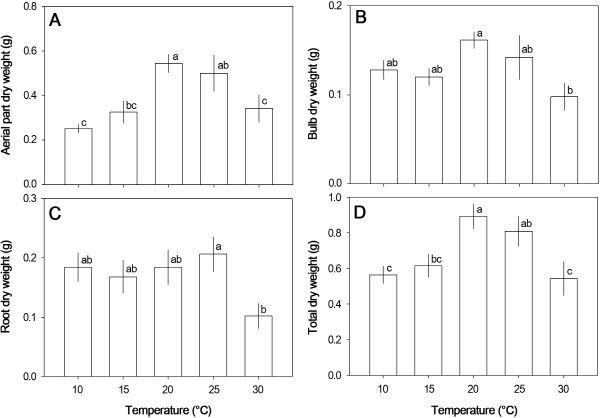
지상부 건중량은 20°C에서 가장 높았으며(Fig. 4A), 인경과 뿌리의 건중량은 각각 20°C와 25°C에서 가장 높았으나 10-25°C 조건에서 처리 온도간에 큰 차이를 보이지는 않았으며, 30°C에서는 크게 감소하였다(Figs. 4B and 4C). 그리고 마늘의 전체 무게는 20-25°C에서 높았다(Fig. 4D).
마늘의 항산화효소 활성
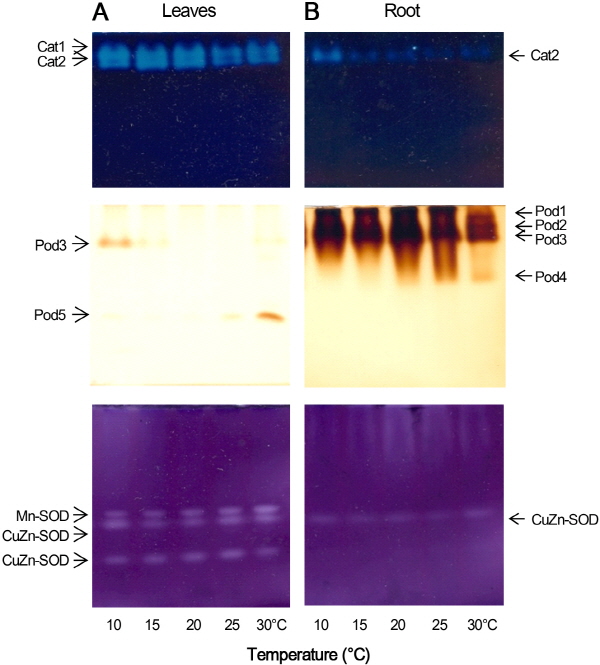
잎에서 항산화효소의 발현양상을 보면, CAT와 POD는 각각 2개의 밴드를 확인할 수 있었다. 그리고, SOD는 3개의 밴드가 확인되었으며, 그 중 1개는 Mn-SOD이고 2개는 CuZn-SOD로 구분되었다(Fig. 5A). 잎에서 CAT 활성은 25°C 이상의 온도에서 점차 감소하였다. POD는 2개의 밴드 중에 POD3는 10°C에서, POD5는 30°C에서 미약하지만 특이적으로 검출되었다. Mn-SOD는 20°C 이상의 온도에서 미약하게 발현되고 CuZn-SOD1, CuZn-SOD2 또한 20°C 이상의 온도에서 그 활성이 다소 높았으나 30°C에서는 다시 감소하는 것으로 관찰되었다. 뿌리에서 항산화효소의 발현양상을 보면, CAT는 1개의 밴드가, POD는 4개의 밴드가 확인되었다. SOD는 1개의 밴드이며, CuZn-SOD로 구분되었다(Fig. 5B). CAT 활성은 대체로 낮았으나 온도가 높을수록 다소 높았으며, POD는 25°C까지 서서히 증가하나 30°C에서 감소하였다. SOD 활성은 20°C 이상의 온도에서 미약하게 검출되었다. 그리고, CAT와 SOD는 뿌리에서보다 잎에서 그 활성이 더 높고, POD는 잎에서보다 뿌리에서 더 높았다.
고 찰
본 연구에서 마늘은 25°C까지는 온도가 높을수록 크게 자랐으나 재배기간이 30일 이상 길어짐에 따라 고온 조건에서 잎의 노화가 빨리 진행되고 잎 끝부분이 점차 황백화되면서 고사하여 고온이 마늘에 스트레스로 작용함을 알 수 있었다(Table 1 and Fig. 6). 고온이 마늘의 생장에 비우호적으로 작용한다는 사실은 광계II의 잠재적 광합성능과 최대 광화학적 효율을 나타내는 Fv/Fo와 Fv/Fm의 변화로도 알 수 있는데(Fig. 2), 이들 형광변수들은 15-20°C에서 높았으나 25°C 이상의 온도에서 크게 감소하였다. 이러한 결과는 25°C 이상의 온도에서 불활성상태의 반응중심이 증가하고(Kriedemann et al., 1985) 광계II의 반응중심이 손상되고 있음을 나타낸다(Oh et al., 2014). 이는 마늘을 30°C에서 재배하였을 때 지상부의 생장과 엽수가 크게 감소하고(Table 1), 식물의 생산성과 관련된 지상부, 인경, 뿌리의 건중량 또한 크게 감소하는 것으로도 알 수 있다(Fig. 4). 재배 온도에 따라 CAT와 POD의 활성 또한 확실한 차이를 보였는데(Fig. 5), CAT는 뿌리에서보다 잎에서 더 높은 활성을 보이고 25°C 이상의 온도에서 그 활성이 점차 감소하는 양상을 보였으며, POD는 POD1, POD2, POD3가 잎에서 보다 뿌리에서 더 높은 활성을 유지하며 20-25°C에서 높고 30°C에서 크게 낮아졌다. SOD도 역시 CAT와 마찬가지로 뿌리에서보다 잎에서 더 높은 활성을 보였는데 20-25°C에서 다소 높고 30°C에서는 감소하였다. 이러한 결과는 20-25°C의 온도가 마늘의 초기 생육에 우호적으로 작용하고 30°C 이상의 온도는 고온 스트레스로 작용하고 있음을 보여주고 있다(Lima et al., 2002; Meloni et al., 2003; Shim et al., 2003). 한지형 잔디인 켄터키 블루그래스(Poa pratensis L.)에서도 생육적온(20/15°C, 주간/야간)에서와는 달리 고온(35/30°C, 주간/야간)에 노출되었을 때 Fv/Fm 값의 감소, 품질 저하와 함께 CAT와 SOD 등 항산화효소 활성이 감소한다(Wang and Huang, 2004). 밀(Triticum aestivum L.)의 유묘를 온도를 달리하여 배양하였을 때에도, 잎에서 CAT와 SOD 활성이 25°C에서 보다 30°C에서는 증가하고 35°C에서는 크게 감소하는데, 이때 지상부와 뿌리의 생장과 Fv/Fm 값이 35°C에서 크게 저해되어 고온 스트레스의 영향을 받는 것으로 보고되었다(Kumar et al., 2013). 더군다나, ascorbate, glutathione, proline 등의 비효소적 항산화물질들도 30°C에서는 증가하는데 반해 35°C에서는 크게 감소하고, 35°C 고온과 α-tocopherol를 동시에 처리하였을 때에 항산화효소와 비효소적 항산화물질의 함량이 대조구와 유사하면서 밀의 생장에 영향을 덜 미치는 것으로 보고되었다. 따라서 생육적온을 벗어난 높은 온도에서는 항산화효소나 비효소적 항산화물질들이 원활하게 합성되지 못하여 고온에 대한 대응이 원활하지 못하여 생육에도 영향을 미치고 있음을 알 수 있다. 본 연구에서 잎에서는 CAT와 SOD가, 뿌리에서는 POD가 높은 활성을 보이고 있어 잎과 뿌리가 산화적 스트레스에 대응하는 메커니즘이 서로 다른 것으로 보인다. 그리고, POD의 경우 미약하지만 잎에서는 10°C 조건에서 POD3가, 30°C 조건에서는 POD5가 검출되어, 저온과 고온에서 스트레스에 대처하는 항산화 메커니즘이 다소 다른 것으로 판단된다.
고온 스트레스의 영향은 OKJIP 곡선의 변화로도 확인할 수 있는데, 25°C 이상의 온도에서 Fi, Fp가 크게 감소하였으며, Fk는 30°C에서, Wk 값은 25°C 이상의 온도에서 확연하게 증가하여(Fig. 1B and 1C) 고온에서 불활성 상태의 반응중심이 많아져 전자전달이 원활하게 일어나지 않음을 알 수 있다(Srivastava et al., 1997). 밀(Tritium aestivum L.)에서도 25°C에서 생육한 잎에서는 Fk가 나타나지 않지만 37.5°C 이상의 온도에서 Fk가 점차 증가하는 것으로 보고된 바 있다(Lu and Zhang, 2000; Mathur et al., 2011). Fig. 1A의 OKJIP 곡선으로부터 산출된 RC/CSm은 20°C까지는 일정하나 온도가 증가함에 따라 점차 감소하여(Table 2) 높은 온도에서 활성상태의 반응중심의 수가 감소함을 나타내 주고 있다. 그리고, ABS/CSm, TRo/CSm, ETo/CSm도 25°C 이상의 높은 온도에서 점차 낮아져(Table 2) 엽면적당 흡수되는 빛에너지 양과 광계II의 반응중심에 포획되는 에너지, 전자전달로 전해지는 에너지가 모두 감소하고 있음을 알 수 있다. 이에 반해 DIo/CSm은 온도가 높아짐에 따라 점차 증가하였으며, 특히 30°C에서 높았다(Table 2). 이는 고온에서는 흡수된 빛에너지가 상당량 광합성에 이용되지 못하고 소실되고 있음을 알려주고 있다. 이러한 결과는 본 연구에서 사용한 마늘이 한지형 품종이기 때문에 기인하는 것으로 보이는데, 호냉성 채소로 잘 알려진 배추(Brassica campestris ssp. napus var. pekinensis)를 봄철 대기온도보다 4°C 또는 7°C 더 높은 조건에서 재배하였을 때(Oh et al., 2014), 그리고 보리(Hordeum vulgare L.), 수수(Sorghum bicolor)와 밀(T. aestivum L.)을 고온에서 재배하였을 때에도 이와 유사한 결과를 나타내는 것으로 보고된 바 있어(Kalaji et al., 2011; Mathur et al., 2011; Yan et al., 2012) 저온내성 작물들에 있어서 공통적인 특성인 것으로 보인다. PIabs 또한 온도가 높아짐에 따라 점차 감소하여 저온성 작물인 마늘이 높은 온도에 노출되었을 때 고온에 민감하여 활력이 저하되었음을 나타내 주고 있다(Strasser et al., 2000).
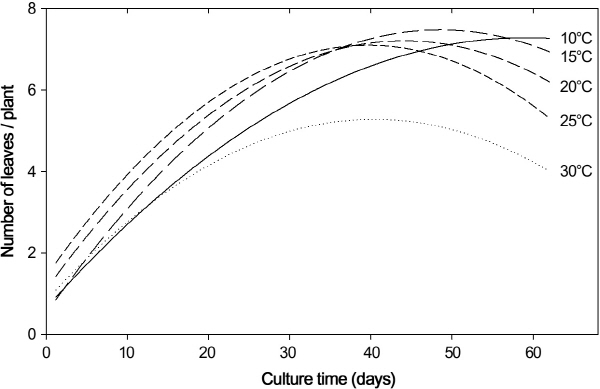
마늘의 생산성을 예측하는 데 있어 식물체당 엽수 또한 중요한 요소이며, 특정 시점까지는 녹색 상태의 건전한 잎이 증가하고 이후 점차적으로 시들면서 녹색 상태의 잎이 감소하는 양상을 보인다(Moravčević et al., 2011). 본 연구에서도 이러한 특성을 잘 보여주고 있다(Fig. 6). 잎의 발생 시기는 온도가 높을수록 빨라졌으나 엽수는 10-25°C 범위에서 재배하였을 때 7개 정도로 유사하였다. 그러나 30°C에서는 엽수가 5개 이하로 가장 적었으며 잎의 발생시기 또한 가장 늦었다. 40일이 경과한 이후부터는 잎이 노랗게 변하여 녹색 상태의 엽수가 점차 감소하였는데, 온도가 낮을수록 노화가 진행되는 시기가 늦춰졌으며, 30°C에서는 잎이 밑으로 쳐지면서 노화가 빨리 이루어졌다. 따라서 20°C에서 재배하는 것이 마늘의 초기 지상부 영양생장과 인경의 발달이 좋을 뿐만 아니라(Fig. 4) 잎의 발달이 비교적 빠르고 노화가 늦게 진행되어(Fig. 6), 저온기 마늘의 재배를 위한 적정 온도로는 20°C 전후가 적절할 것으로 판단된다. 그리고, 풋마늘로 이용하기 위해서는 30일 전후부터 50일 이내에 수확하는 것이 바람직한 것으로 보인다(Fig. 6).
작물수확량은 온도에 의해 크게 영향을 받으며, 이는 광계II 활성과 직접적으로 관련이 있다. 본 연구에서도 광계II의 엽록소형광변수인 Fo, Wk는 온도와 1% 수준에서 정의 상관을, Fm, Fv/Fo, Fv/Fm, RC/CSm, ABS/CSm, TRo/CSm은 온도와 1% 수준에서 음의 상관을 나타내었다(Table 3). 이러한 결과는 엽록소형광 변수들이 고온 스트레스에 의한 영향이 육안으로 관찰되기 전에 고온 스트레스의 영향을 조기에 파악하는데 유용하게 이용될 수 있음을 나타내 주고 있다. 특히, Fv/Fo, Fv/Fm, Fk, ETo/CSm, PIabs는 전체 건중량과도 의미있는 상관을 보여, 마늘 생산성을 조기예측하는데 있어서 유용한 변수로 활용될 수 있을 것으로 보인다.