서 언
식물은 광 신호전달 기작에 의해서 개화, 굴광성, 기공 개폐 및 안토시아닌 합성 등과 같은 광형태형성 변화를 나타낸다(Wang et al., 2012). 이 가운데 안토시아닌 합성은 광환경 스트레스에 따른 식물의 전형적인 반응에 해당한다(Scott, 1999). 식물에게 광환경 스트레스를 부여하는 자외선은 파장에 따라 UV-A (315-380nm), UV-B (280-315nm), UV-C (100-280nm)의 3 영역으로 구분된다. 태양복사에 포함된 UV-A와 일부 UV-B는 지표면에 도달하나, UV-C는 오존층에 의해 차단되어 지표면에 도달하지 못한다. 때문에 지표면에 도달한 자외선 가운데 UV-A가 95% 정도를 차지한다. 한편 온실 내에서는 자외선을 흡수하는 피복재의 특성으로 인하여 투과되는 자외선의 강도가 급격하게 줄어든다(Moan, 2001).
파장은 짧으나 높은 에너지를 지닌 자외선은 식물 생장 특성에 커다란 영향을 미칠 뿐만 아니라 DNA, RNA 및 단백질에 물리적 손상을 초래한다(Britt et al., 1993; Frohnmeyer and Steiger, 2003; Jansen et al., 1998). 한편, 낮은 강도의 자외선은 형태적 변화 또는 플라보노이드 생성을 유도하는 것으로 알려져 있다. 즉 낮은 강도의 UV-B를 조사시켰을 때 토마토(Brandt et al., 1995), 옥수수(Piazza et al., 2002), Arabidopsis (Suesslin and Frohnmeyer, 2003), 고추(Mahdavian et al., 2008)에서 안토시아닌의 축적이 보고된 바 있으나, 청색 또는 적색의 단색광 LED에 UV-A LED를 부가하여 조사할 경우에 안토시아닌 축적을 증대시키는 적정 광주기와 광강도에 관한 보고는 이루어지지 않고 있다.
파이토케미컬(phytochemicals)의 한 종류에 해당하는 안토시아닌의 발현 기작은 매우 복잡하여, 유전적 요소뿐만 아니라 여러가지 환경 조건에 의해서도 크게 좌우된다(Lee and Gould, 2002; Oren-Shamir, 2009). 한편 아스코르빈산은 대사 과정에서 조효소로서 작용하나, 인체 내에서 스스로 생성되지 않는다. 최근 들어 안토시아닌과 아스코르빈산의 항산화 작용(Lila, 2004; Kong et al., 2003)이 알려지면서 이것들이 기능성 물질로 주목받고 있다. 때문에 상추류의 기능성 물질에 미치는 인공광원의 조명 효과가 부분적으로 보고되고 있으나(Son et al., 2012), 안토시아닌과 아스코르빈산의 함량을 증진시키는데 효과적인 UV LED의 조사 효과에 관한 연구는 미흡한 실정이다(Brazaityte et al., 2015; Wang et al., 2012).
전력소모가 작고, 수명이 길며, 광합성속도에 영향을 미치는 광질 선택과 펄스 조사가 가능한 발광다이오드(light-emitting diodes, LED)를 작물생산용 인공광원으로 활용하기 위한 연구 결과가 지속적으로 보고되고 있다(Goins et al., 1997; Johkan et al., 2010; Lee and Kim, 2013). 이러한 연구 결과들은 작물의 생산 과정에서 LED의 활용 가능성을 탐색하는 것으로서의 의미를 지니고 있으나, 대부분이 광합성 작용에 효과를 보이는 청색광 또는 적색광 영역에서 피크파장을 갖는 LED를 이용한 것이기에 파이토케미컬 함량의 증진을 포함하여 작물의 영양성을 높이는 데 한계가 있을 수 밖에 없다.
지금까지 작물에 대한 광환경 스트레스를 분석하고자 자외선 램프 또는 자외선 투과 필름을 이용한 사례가 다수 보고된 바있으나(Erkan et al., 2008; Lercari et al., 1989; Wenke and Qichang, 2012), 작물생장용 인공광원으로서 UV LED의 이용은 최근에 이루어지고 있다. 본 연구의 목적은 상이한 광주기를 갖는 청색 및 적색 LED 하에서 생장된 상추의 생장, 안토시아닌 및 아스코르빈산의 함량 변화에 미치는 UV-A LED의 조사 효과를 분석하는 데 있다.
재료 및 방법
광처리 및 식물생장 조건
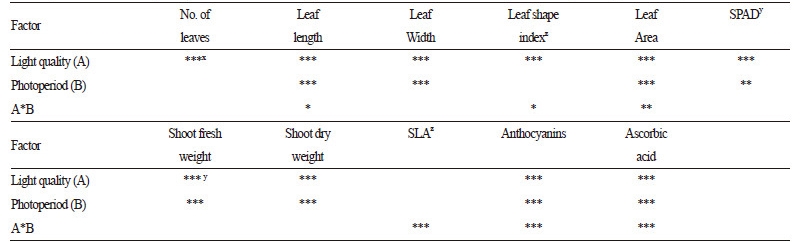
본 연구에서는 피크파장이 각각 450nm, 660nm, 365nm인 청색 LED(KLBB1203-1, KODENSHI AUK, Iksan, Korea), 적색 LED(KLRR1203-1, KODENSHI AUK, Iksan, Korea), UV-A LED(KLUV1203-1, KODENSHI AUK, Iksan, Korea)를 이용하여 4개의 처리구를 구성하였으며, 백색형광등(DULUX L55W/840, OSRAM, Munich, Germany)을 대조구로 사용하였다(Table 1). 또한 광주기(명기/암기)는 3수준(12/12h, 16/8h, 20/4h)으로 설정하였다. 이때 광원의 분광특성을 분석하고자 분광광도계(LI-1800, Li-Cor Inc., Lincoln, NE, USA)를 이용하였으며(Fig. 1), 광강도는 광양자 센서(SKP 215, SKYE, Powys, UK)를 사용하여 측정하였다.
| |
Fig. 1. Spectral characteristics of (A) blue LED, (B) red LED, (C) UVA- LED, and (D) white fluorescent lamps used in this study. | |
적치마상추(Lactuca sativa L. ‘중생종’, 흥농씨앗) 종자를 파종한 후 본엽이 4매일 때 폐쇄형 식물 생산시스템(이하 ‘폐쇄형 시스템’) 내에 설치된 담액수경 재배베드에 각 처리구당 27주씩 정식하였다. 양액 처방은 서울시립대 엽채류 배양액(N-P-KCa-Mg=0.8-2.0-6.0-3.0-2.0mg·L-1, pH 5.5-6.0, EC 1.5-1.8dS· m-1)으로서, 양액 온도를 22°C로 조절하였다. 폐쇄형시스템내의 환경조건은 기온 22/18°C, 습도 70%, CO2 농도 800μmol· moL-1로 설정하였다. LED조명에 연결된 SMPS(SP-320-48, Mean Well, New Taipei City, Taiwan)를 이용하여 광강도를 조절한 결과 광원으로부터 25cm 떨어진 재배베드 표면에서의 평균 광합성유효광양자속(photosynthetic photon flux, PPF)이 230 ± 11μmol·m-2·s-1로 나타났으며, 동일한 지점에서 UV-A 센서(SKU 420, SKYE, Powys, UK)로 측정된 UV-A LED의 평균 조사강도는 80 ± 3mW· m-2로 나타났다.
생장조사
MATLAB(R2011b, MathWorks Inc., Natick, MA, USA)의 랜덤함수를 이용하여 처리구 당 5주씩 임의로 선택된 상추를 대상으로 정식 후 28일째에 생장조사를 수행하였다. 처리구별 상추의 생장 특성으로 엽수, 엽장, 엽폭, 엽면적, 엽록소 함량, 지상부 및 지하부의 생체중 및 건물중 을 조사하였다. 하단부로부터 3번째 본엽에 대한 엽록소함량은 휴대용 엽록소 측정기(SPAD 502, MINOLTA Co., Osaka, Japan)를 사용하여 측정하였고, 엽면적은 CCD 카메라(VK-C370, HITACHI, Tokyo, Japan) 로 측정된 상추 잎의 영상에 기지의 물체 면적과 화소수 사이의 회귀관계를 적용하여 계산하였다. 지상부와 지하부로 구분된 상추의 생체중과 건물중의 측정에 전자저울(SBA51, SCALTEC INSTRUMENTS, Goettingen, Germany)을 이용하였다. 건물중의 측정에 사용된 시료는 기온이 70°C로 유지되는 오븐(ON-21, JEIO TECH, Seoul, Korea)에서 3일간 건조되었다.
안토시아닌 및 아스코르빈산 함량 분석
상추 잎의 안토시아닌 추출을 위하여 정식 후 28일째에 각 처리구 당 생체 시료 5g을 3반복으로 채취하였다. 채취된 상추를 동결 건조후 분쇄기(HMF-3000s, Hanil Electric, Seoul, Korea)를 이용하여 마쇄한 후 시료 500mg을 채취하여 95% ethanol과 1.5N HCL을 85:15(v/v)로 혼합하였다. 혼합한 추출액을 4°C 암조건 하에서 16시간 shaking 한 후 22,000g에서 20분간 원심분리하였다. 원심분리기(AVANTI J-26XP, Beckman Coulter, Brea, CA, USA)로 얻은 상징액을 흡광도계(SpectraMax M2, Molecular Devices, Sunnyvale, CA, USA)를 사용하여 530nm와 680nm에서 흡광도를 산출하였으며, 이것에 기초하여 안토시아닌 함량을 산출하였다(Fuleki and Francis, 1968).
상추의 아스코르빈산 함량을 분석하고자 생시료 10g 에 10% 메타인산용액(73160-1201, Junsei Chemical Co., Tokyo, Japan)을 넣고 균질기(IKA DI25, Wilmington, NC, USA)를 이용하여 균질화하였다(Korea Food and Drug Administration, 2008). 균질화된 검체를 10% 메타인산용액으로 100mL 를 정용하여 0.22μm의 membrane filter로 여과한 후 HPLC(Ultimate 3000, Thermo Fisher Scientific, Sunnyvaly, CA, USA)로 분석하였다. 이때 5μm와 4.6 × 250mm의 제원을 갖는 컬럼(INNO C18, Youngjin Biochrom, Seongnam, Korea)을 사용하였고, 오븐온도 30°C, UV검출기 파장 254nm, 이동상은 A: 0.05 M KH2PO4, B: 메탄올 gradient grade로 분석하였다. 1.0mL·min-1의 유속을 갖는 이동상 A와 B의 gradient는0-5min에서 각각 100, 0%이었고, 8-13min에서는 각각 20, 80% 이었으며, 15-20min에서는 100, 0%이었다.
통계처리
상추의 생장 특성, 안토시아닌 및 아스코르빈산 함량에 미치는 광질과 광주기의 영향을 분석하고자 SAS 프로그램(V9.3, SAS Institute Inc., Cary, NC, USA)을 이용하여 이원분산분석을 하였으며 최소유의차 검정으로 5% 수준에서 각 처리간의 유의성을 검증하였다.
결과 및 고찰
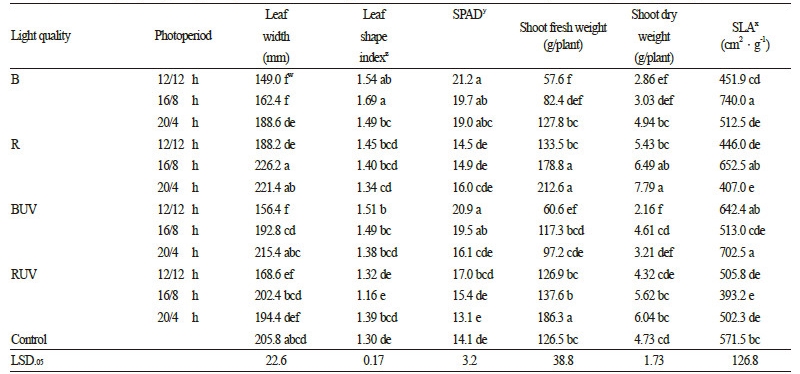
본 연구에서 적용된 광질은 정식 후 28일째에 측정된 상추의 엽수, 엽장, 엽폭, 엽형지수, 엽면적, 비엽면적(specific leaf area), 지상부 생체중 및 건물중, 엽록소 함량 등 생장 특성에 커다란 영향을 미쳤다. 또한 엽수, 엽형지수 및 비엽면적을 제외한 생장특성은 광주기의 영향을 크게 받았다. 한편 안토시아닌과 아스코르빈산 함량은 광질과 광주기의 영향을 크게 받을 뿐만 아니라 이들의 교호작용 효과가 존재하였다(Table 2). 이밖에 엽면적과 비엽면적에서 광질과 광주기의 교호작용 효과가 나타났다.
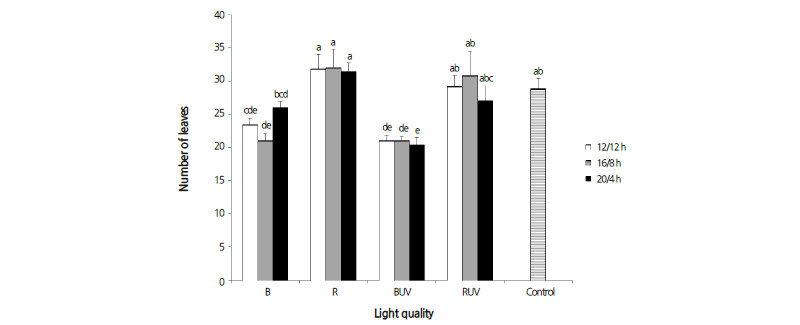
엽수는 적색광 단독의 R 처리구 또는 적색광에 UV-A가 부가적으로 조사된 RUV 처리구에서 높게 나타났다. 반대로 청색광 단독의 B 처리구 또는 청색광에 UV-A가 부가된 BUV 처리구에서 엽수가 적었으며, 대조구에 비해서 적게 나타났다(Fig. 2). 엽장은 적색광 하에서 광주기가 늘어날수록 증가한 가운데 R 처리구의 16/8h의 광주기에서 최대치가 나타났다. 한편 적색광에 UV-A가 부가된 RUV 처리구에서의 엽장은 대조구 뿐만 아니라 R 처리구에 비해서 크게 줄어들었는데, 이러한 결과는 12/12h과 16/8h의 광주기에서 분명하게 나타났다(Fig. 3). 엽폭에 미치는 광질 또는 광주기의 영향은 엽장과 비슷하게 나타났다. 특히 12/12h의 광주기를 갖는 청색광 단독의 B 처리구 또는 UV-A가 부가된 처리구에서의 엽폭은 대조구에 비해서 49.4-56.8mm 작게 나타났다(Table 3). 엽장을 엽폭으로 나눈 값에 해당하는 엽형지수는 B 처리구와 BUV 처리구에서 높게 나타났고, 나머지 처리구에서는 대조구와 비슷한 수준이었다. 이러한 결과는 청색광이 많이 포함된 처리구에서 엽폭이 작게 나타났기 때문인 것으로 판단된다. 엽면적은 적색광 단독의 R 처리구에서 높게 나타난 가운데, 16/8h의 광주기 처리구에서 4,018.4cm2의 최대치가 나타났다. 이러한 결과는 적색광 처리구에서의 엽수와 엽장이 늘어났기 때문인 것으로 판단된다. 한편 UV-A가 부가된 RUV 처리구에서 엽면적의 감소가 분명하게 나타났다(Fig. 4). 결과적으로 UV-A의 조사가 잎의 신장을 억제한 것으로 판단된다. SPAD 값으로 측정된 엽록소함량은 청색광 또는 UV-A가 부가된 BUV 처리구에서 비슷한 수준으로 나타났다(Table 3). 한편 적색광 또는 UV-A가 부가된 RUV 처리구에서의 엽록소함량은 대조구와 비슷한 수준으로 나타났다. 지상부생체중은 광질과 광주기의 영향을 받는 가운데 적색광의 R 처리구와 UV-A가 부가된 RUV 처리구에서 높게 나타났다. 이러한 결과는 광주기가 길수록 분명하게 나타났다. 한편 청색광 단독 또는 UV-A가 부가된 청색광 처리구에서의 생체중이 줄어들었다. 그러므로 청색광 또는 UV-A가 잎의 신장을 억제하였을 뿐만 아니라 바이오매스를 감소시켰음을 알 수 있다. 지상부 건물중은 지상부 생체중의 결과와 유사하게 나타났다. 상추 잎의 건물중에 대한 엽면적의 비, 즉 비엽면적은 광주기가 16/8h인 B 처리구와 R 처리구에서 높게 나타났다.
| |
Fig. 2. Effects of LED light quality and photoperiod on the number olfe aves of lettuce. The data indicate the means ± S.E. (n = 5). | |
| |
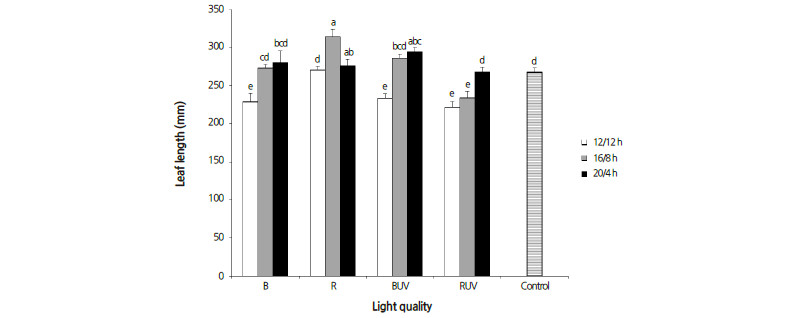
Fig. 3. Effects of LED light quality and photoperiod on the leaf lenght of lettuce. The data indicate the means ± S.E. (n = 5). | |
| |
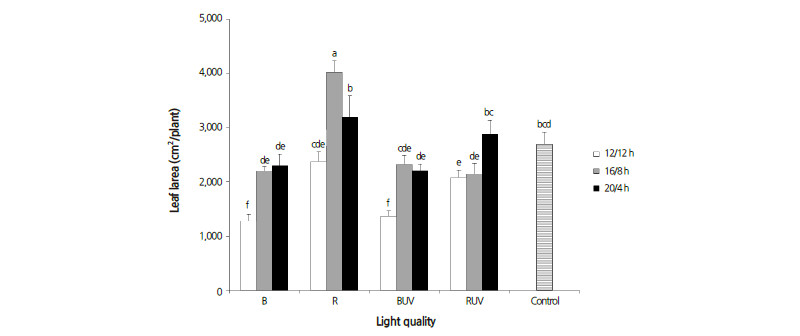
Fig. 4. Effects of LED light quality and photoperiod on the leaf areao f lettuce. The data indicate the means ± S.E. (n = 5). | |
이전 연구에서 명기가 증가할수록 상추의 엽장, 생체중 및 건물중이 증가하였으며(Park et al., 2012), 감자 플러그묘의 생장도 크게 증가하였다(Kim et al., 2006). 기존의 연구 결과와 유사하게 본 연구에서도 명기 시간이 길어질수록 상추의 잎 관련 생장 특성, 생체중 및 건물중이 높게 나타났다. 본 연구에서 상이한 광주기를 갖는 청색 및 적L색E D 하에서 생장된 상추의 생장 특성은 Lee and Kim(2014)의 연구 결과와 일치한다. 즉 적색광은 상추의 엽수, 엽장, 엽폭, 엽면적, 지상부 생체중 및 지상부 건물중은 증가시키는 데 효과적이었다. 한편, 청색광은 잎의 신장을 억제하는 대신에 엽록소함량을 증가시키는 데 기여하였다.
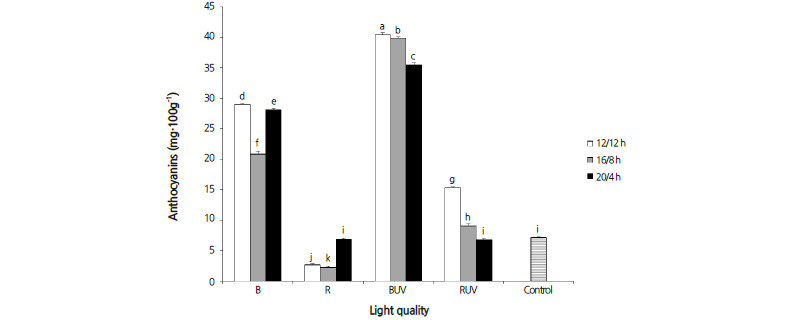
안토시아닌의 축적에 미치는 광질 효과가 분명하게 유의차를 나타낸 가운데 B 처리구에서의 안토시아닌 함량을 R 처리구와 비교하면 광주기가 12/12h, 16/8h, 20/4h일 때 각각 10.7배, 9.2배, 4.1배 높게 나타났다(Fig. 5). 상기 결과로부터 안토시아닌의 축적이 청색광 조건에서 많이 이루어지거나, 명기가 짧아질수록 상대적으로 많이 이루어짐을 알 수 있다. 광질, 광강도 및 광주기 등 광환경 뿐만 아니라 작물의 종류에 따라 안토시아닌의 합성은 다르게 나타났다(Zoratti et al., 2014). 명기가 짧아질수록 브로콜리(Steindal et al., 2013)에서 안토시아닌이 축적되었으나, 감자(Reyes et al., 2004), 고구마(Carvalho et al., 2010), 베리류(Uleberg et al., 2012)에서는 안토시아닌 함량이 낮았다. 한편 청색광과 UV-A의 광수용체로서 작용하는 크립토크롬(cryptochrome)은 안토시아닌의 생합성과 관련된 유전자의 발현을 촉진하는 것으로 알려져 있다(Giliberto et al., 2005; Ninu et al., 1999). 12/12h, 16/8h, 20/4h의 광주기를 갖는 UV-A LED의 부가 조사로 말미암아 BUV 처리구에서의 안토시아닌 함량은 B 처리구에 비해서 1.3-1.9배 높게 나타났다. Wang et al.(2012)은 UV-A LED 하에서 생장된 순무 싹의 배축 위치에 따른 안토시아닌 함량의 변화를 제시하면서 청색 LED에 UV-A LED를 부가한 조사에서 안토시아닌 함량의 상승 효과를 보고한 바 있다. 한편 RUV 처리구의 안토시아닌 함량은 R 처리구에 비해서 1.0-5.6배 증가하였다. 결과적으로 청색 또는 적색 LED와 같은 단색광 조건에 UV-A LED를 부가한 조사에서 상추 잎에 안토시아닌의 축적이 많이 이루어짐을 알 수 있다. 특히, 대조구와 비교한 R 처리구에서의 안토시아닌 함량이 32-95%에 불과하였으나, RUV 처리구에서는 1.0-2.1배로 증가하여 UV-A LED의 부가 조사 효과가 높게 나타났다.
| |
Fig. 5. Effects of LED light quality and photoperiod on the anthocyanins in lettuce leaf. The data indicate the means ± S.E. (n = 3). | |
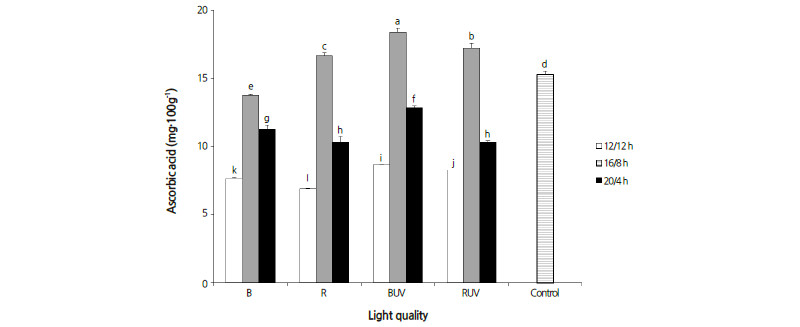
LED의 광질에 비해서 광주기가 아스코르빈산 함량에 미치는 영향이 높게 나타났다(Fig. 6). 대조구와 비교한 B 처리구에서 의 아스코르빈산 함량은 12/12h, 16/8h, 20/4h의 광주기에서 각각 50, 90, 74%로 나타났고, R 처리구에서는 45, 109, 68%으로 나타났다. 특히, 광주기가 16/8h 일 때 아스코르빈산 함량이 가장 높게 나타났으며, 다음으로 20/4h, 12/12h의 순서로 나타났다. 12/12h, 16/8h, 20/4h의 광주기를 갖는 UV-A LED의 부가 조사로 말미암아 BUV 처리구에서의 아스코르빈산 함량은 B 처리구에 비해서 1.1-1.3배 높게 나타났고, RUV 처리구는 R 처리구에 비해서 1.0-1.2배 높게 나타났다. 이러한 결과로부터 청색 또는 적색 LED에서 UV-A LED의 부가 조사에 따른 아스코르빈산 함량의 증가는 최대 20-30% 정도로 추정된다. UV-A LED의 부가 조사에 의해서 청경채의 아스코르빈산 함량이 증가하였으며(Brazaityte et al., 2015), 청색 LED 하에서 생장된 배추의 비타민 C와 엽록소함량은 유의차가 인정될 만큼 크게 증가하였다(Li et al., 2012), 또한 16h의 명기에서 생장된 상추의 아스코르빈산과 글루코스 함량 사이에 높은 상관관계가 있는 것으로 보고되었다(Samuoliene et al., 2012).
이전 연구 결과에서 630-670nm 영역의 적색 LED는 엽채류의 생장을 촉진하고, 430-470nm의 청색 LED는 안토시아닌 함량을 높이는 데 효과적인 것으로 나타났다(Lee and Kim, 2014). 그런데 400-700nm의 가시광 영역에 해당하는 LED를 작물재배용 인공광원으로 사용할 경우 자외선을 포함하고 있지 않기 때문에 작물의 형태형성이 제대로 이루어지지 않거나, 영양성이 저하될 수 있다. 때문에 폐쇄형 시스템에서 적정 강도의 UV-A를 인위적으로 조사시킬 경우 엽채류의 영양성과 경제적 가치가 향상될 것으로 기대된다 (Basahi et al., 2014; Lee et al., 2014; Li and Kubota, 2009; Tsormpatsidis et al., 2008).
본 연구에서는 피크파장이 365nm이며, 조사강도가 80 ± 3mW· m-2인 UV-A LED가 인공광원으로 사용되었다. 연구 결과 UV-A LED 조사로 인하여 상추의 생장이 억제되었으나, 엽록소함량, 안토시아닌 및 아스코르빈산 함량의 증가에 효과적이었다. 그러므로 안토시아닌 및 아스코르빈산 함량에 미치는 UV-A LED의 부가 조사 효과는 인공광하에서 생산된 엽채류의 영양성을 높이는 데 기여할 것으로 판단된다. 최근 들어 UV-A LED의 대량생산 체계 구축으로 작물의 형태형성 또는 파이토케미컬 함량을 증진시키는 데 UV-A LED의 활용 가능성이 높아졌으나, 여전히 UV-A LED의 가격은 청색 또는 적색 LED의 3.5-5배 수준으로 알려져 있다. 한편 가시광 영역의 LED 효율은 20% 정도이나, 피크파장이 365nm인 UV-A LED 효율은 5-8%에 불과하다. 그러므로 폐쇄형 시스템에서 UV-A LED 도입의 실용성을 높이려면 UV-A LED의 부가 조사에 따른 엽채류의 영양성 향상 효과, 조명효율, 가격 등을 종합적으로 검토해야 할 것이다. 아울러 UV-A LED의 적정 조사강도와 조사 시간을 제시할 수 있는 추가적인 연구가 필요할 것으로 판단된다.