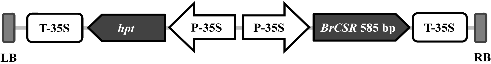서 언
재료 및 방법
신규 저온 저항성 유전자 동정
과발현 Vector, pSL101 제작 및 담배 형질전환
Genomic DNA 추출
PCR 및 Southern Hybridization 분석
형질전환체의 저온 저항성 분석
Total RNA 추출
도입유전자, BrCSR의 발현 분석
결과 및 고찰
신규 저온 저항성 유전자 동정
BrCSR 유전자 기능 분석
서 언
고농도 염 집적, 건조, 저온과 같은 비생물적 스트레스는 대부분의 작물에서 생장 및 생육형태 변화, 생리적・생화학적 변화, 수확량의 저하를 일으키는 중요한 요인이다(Wang et al., 2001, 2003). 이 중 저온 스트레스는 효소활성 저하 및 에너지 대사의 불균형 등을 초래하고 transcriptome, proteome, metabolome의 변화를 동반하게 되므로(Guy et al., 2008), 최근 다양한 작물에서 저온 저항성 유전자를 찾아내는 연구들이 활발히 진행되고 있다(Dubouzet et al., 2003; Fowler and Thomashow, 2002; Jaglo et al., 2001; Lee et al., 2012; Qin et al., 2004; Seki et al., 2002; Yang et al., 2005; Zhang et al., 2006). 예를 들어, 벼에서는 GPAT(arabidopsis glycerol- 3P-acyltransferase)(Yokoi et al., 1998), OsCDPK7(rice calcium- dependent protein kinase)(Saijo et al., 2000), OsDREB1(rice DRE-binding protein 1)(Ito et al., 2006), HvCBF4(barley C- repeat binding factor)(Oh et al., 2007), OsCIPK03(rice calcineurin B-like protein-interaction protein kinase 03)(Xiang et al., 2007), 및 OsTPP1(trehalose-6-phosphate phosphatase)(Ge et al., 2008) 등이 있으며, 옥수수에서는 NPK1(nicotiana protein kinase)(Shou et al., 2004), 애기장대에서는 MYB15(MYB-like transcription factor)(Agarwal et al., 2006) 등이 대표적인 저온 저항성 유전자들이다. 실제로 GPAT의 경우에는 벼에 GPAT가 도입되어 28%까지 불포화 지방산이 증가하였으며 17°C에서 광합성 효율이 20%까지 증가되는 결과를 가져와 저온 환경에서 벼의 생육저하를 최소화하였다(Yokoi et al., 1998). 그리고 애기장대에서 MYB15의 억제가 저온 저항성과 관련 있는 CBF(C-repeat binding factor) 유전자들의 발현을 증가시켜 저온 저항성을 높였다고 보고하였다(Agarwal et al., 2006).
따라서 본 연구는 비생물적 스트레스인 저온이 처리된 내혼계배추(Brassica rapa ssp. pekinensis inbred line ‘Chiifu’)를 대상으로 microarray 분석을 통하여 저온 저항성 유전자로 추정되는 유전자를 선발・동정하였다. 분리된 유전자는 이를 과발현(over-expression)시킨 형질전환 담배를 생산 및 분석하여 저온 스트레스 처리 시 해당 유전자의 저온 저항성을 확인하였고 BrCSR(B. rapa Cold Stress Resistance)로 명명하였다.
재료 및 방법
신규 저온 저항성 유전자 동정
내혼계배추(B. rapa ssp. pekinensis inbred line ‘Chiifu’)를 3주간 생장상(광도 290µmol・m-2・s-1, 광주기 명처리 16시간/암처리 8시간, 생육온도 25°C, 생육습도 40-70%)에서 재배하고 저온(4°C)을 48시간까지 처리한 후, 생육단계별로 total RNA를 추출하고 cDNA library를 이용한 127,144개의 배추 EST 분석을 수행하였으며 KBGP-24K oligo chip을 이용하여 각 유전자들의 발현 변화를 비교・분석하였다. 분석 후 저온 처리에 따른 배추에서의 발현 분석 결과를 BrEMD(B. rapa EST and Microarray Database, www.brassica-rapa.org/BrEMD)에 등록하였다(Lee et al., 2008). 이에 따라 본 연구에 이용할 저온 저항성 관련 유전자는 이 BrEMD 정보를 활용하여, 저온 스트레스 처리 시 반응하는 유전자들 중 발현이 강하게 증가한 유전자들을 분류하고 완전장을 갖추고 있으며 기능이 알려지지 않은 대상유전자 중에서 선발하였다.
유전자 동정은 RT-PCR 방법을 이용하였으며 이를 위해 585bp ORF(Open Reading Frame) 및 애기장대(Arabidopsis thaliana)에서 상동성을 가지는 cDNA 염기서열(AT1G02870)과 NCBI에 등록된 B. rapa subsp. pekinensis clone KBrB030F10 염기서열(AC189302)을 바탕으로 primer(BrCSR-F: 5'-ATG GCG AGG TCA AGG AGG A-3', BrCSR-R: 5'-TCA GAA TGG AAC TAA AAC AGG-3')를 제작하였다. 증폭된 PCR product는 pGemT-easy vector에 클로닝 후 염기서열을 확인하고(Macrogen Co., Seoul, Korea) National Center for Bio-technology Information(NCBI) database(www.ncbi.nlm.nih.gov)를 이용하여 상동성을 분석하였다.
과발현 Vector, pSL101 제작 및 담배 형질전환
동정한 BrCSR 유전자를 과발현(over-expression) 시키기 위하여 pH2GW7(VIB-Ghent University, Belgium)에, 클로닝한 585bp의 BrCSR 유전자를 삽입하여 형질전환용 vector인 pSL101를 제작하였다(Fig. 1). 제작된 pSL101 vector를 이용한 담배 형질전환은 무균 상태로 기내 배양된 담배(Nicotiana tabacum ‘SR1’) 잎을 이용하였다. 절단한 잎은 pSL101 vector를 포함하는 Agrobacterium LBA4404 strain 용액에 1분 동안 침지시키는 방법으로 접종하고, 공동배양배지[Murashige & Skoog(MS) 기본배지, 3% sucrose, 0.8% plant agar, BA 1.5mg・L-1, pH5.8]에 치상하였다. 치상 후 21 ± 2°C, 암조건에서 3일 동안 공동배양한 절편체는 cefotaxime 200mg・L-1이 포함된 MS 기본액체배지에서 3회 반복하여 Agrobacterium을 제거해 주고 hygromycin 5mg・L-1가 첨가된 선발배지(MS 기본배지, 3% sucrose, BA 1.5mg・L-1, 0.8% plant agar, cefotaxime 200mg・L-1, pH5.7)에 치상하였다. 절편체에서 발생된 신초는 발근배지(MS 기본배지, 3% sucrose, 0.8% plant agar, pH5.8)로 옮겨 발근시킨 후 순화하였다. 생산된 T0 담배 형질전환체들은 형질전환 유무를 PCR 방법으로 확인하고 자가수분시켜 T1 세대로 세대진전하였다. 본 연구에서는 T1 세대 담배 형질전환체를 이용하여 분석을 수행하였다.
Genomic DNA 추출
T1 형질전환체로 추정되는 담배의 잎을 채취하여 액체질소를 이용해 분쇄한 후 DNA 추출 buffer(0.5M NaCl, 0.1M Tris-HCl, 50mM EDTA, 1.25% SDS)를 넣고 65°C에서 30분간 처리하였다. 그 후 phenol, chloroform, isoamyl alcohol를 사용하여 genomic DNA를 추출하였다(Lee et al., 2004).
PCR 및 Southern Hybridization 분석
담배 형질전환체들의 도입유전자 전이 유무는 도입된 T- DNA 상의 선발마커인 hygromycin 저항성 유전자를 대상으로 HPT-F: 5’-TTT CCA CT GCG AGT AC-3’와 HPT-R: 5’-TGT CGA GAA GTT TCT GAT CGA-3’ primer set을 이용한 PCR 분석법으로 확인하였다.
PCR 분석으로 확인된 T1 형질전환체를 대상으로 Southern hybridization 분석을 수행하여 도입유전자의 copy 수를 확인하였다. Southern hybridization 분석은 genomic DNA 30μg을 제한효소 HindIII를 첨가하여 37°C에서 18시간 동안 반응시킨 후 1× TBE buffer를 사용하여 1% agarose gel 상에서 30V로 15시간 전기영동 하였다. 이 gel을 0.25N HCl로 depurination시키고 0.4N NaOH로 denaturation시킨 후, 0.4N NaOH에 18시간 처리하여 Hybond-N+ nylon membrane(Amersham Biosciences, UK)으로 옮겼다. 이후 도입된 pSL101 vector의 hygromycin 저항성 유전자를 탐침하는 [32P]-dCTP로 labeling된 960bp의 probe로 18시간 동안 혼성화[(NaH2PO4(mono- basic) 1M, Na2HPO4(di-basic) 1M,10% BSA, 20% SDS, EDTA 0.5M, 32P-dCTP, 65°C)] 반응된 nylon membrane은 2× SSC, 0.1% SDS와 0.1× SSC, 0.1% SDS로 각각 65°C에서 15분간 처리하였다. 그 후 nylon membrane을 -80°C에서 24시간 동안 X-ray 필름에 노출시키고 필름현상용 developer와 fixer를 이용하여 X-ray 필름을 현상하였다(Lee et al., 2004).
형질전환체의 저온 저항성 분석
PCR과 Southern hybridization 분석을 통해 형질전환체로 확인된 담배를 대상으로 저온 자극 시 도입유전자의 발현량 변화와 저항성 여부를 분석하기 위해 저온 스트레스를 처리하였다. 저온 자극은 본엽이 7-9매가 된 비형질전환 대조군과 형질전환체들을 저온처리가 진행되는 동안 다른 어떠한 비생물적 자극(수분, 온도, 빛 등)이나 생물적 자극(병원균 감염, 해충 피해 등)이 발생하지 않는 제한된 조건(광도 250 µmol・m-2・s-1, 광주기 16시간 명처리/8시간 암처리, 처리온도 4°C, 습도 30-50%)에서 표현형적으로 명확한 차이를 보이는 시기(생장 멈춤, 엽색 변화, 도복 여부)까지 실시하였다.
Total RNA 추출
저온(4°C) 처리 후 100mg의 잎을 채취하여 RNeasy® Plant Mini Kit(QIAGEN, Germany)를 이용하여 total RNA를 추출하였다. 7µL의 ß-mercaptoethanol이 첨가된 세포 용해용 RLT buffer 700µL를 넣고 상온에서 5분간 반응시킨 후 1차 column을 이용하여 수용층 용액을 분리하였다. 분리된 용액을 2차 column에 넣고 원심분리한 후, membrane에 결합된 RNA를 세척하는 RW1 buffer 700µL와 RPE buffer 500µL를 차례로 넣어 column을 세척한 후 RNase-free water로 total RNA를 추출하였다.
도입유전자, BrCSR의 발현 분석
형질전환이 확인된 개체들에서 BrCSR 유전자의 발형 양상을 확인하기 위해 quantitative real-time RT-PCR과 Northern blot hybridization 분석을 수행하였다. Quantitative real-time RT- PCR은 Rotor-Gene 6000(Corbett, Australia)과 SensiMix One- Step Kit(Quantace, USA)를 이용하였으며, 사용한 primer set은 CSRreal-F: 5’-ATG GCG AGG TCA AGG A-3’과 CSRreal-R: 5’-TCA GAA TGG AAC TAA AA-3’이었다. 방법은 2× SensiMix one-step(reaction buffer, reverse transcriptase, heat- activazted DNA polymerase, dNTP, 6mM MgCl2), 50× SYBR green solution, RNase inhibitor, 5μM forward and reverse primers, 500ng total RNA로 조합된 20μL의 반응용액을 먼저 42°C에서 30분간 cDNA 합성 후 95°C에서 10분간 denature 시켰다. 그 후 95°C에서 10초, 56°C에서 15초, 72°C에서 20초 반응을 35회 반복하였다. 발현 분석 방법은 증폭량에 따른 형광강도수치(fluorescence intensity data)를 각 cycle의 종료 시마다 측정하였고, 측정치는 분석 소프트웨어에 의해 분석하였다. 각 형질전환체의 BrCSR 발현값은 actin 유전자의 발현값에 비례하여 상대적으로 계산하였다. 사용한 actin primer set은 Actin56-F: 5’-TCA GTC CAA GAG AGG TAT TC-3’과 Actin56-R: 5’-TAG CAG GGA CAT TGA AAG-3’이었다. Northern blot hybridization 분석은 10µg의 RNA를 formaldehyde와 MOPS 용액을 이용하여 전기영동한 후, 0.4N NaOH로 18시간 처리하였고, Hybond-N+ nylon membrane (Amersham Biosciences, UK)으로 옮기는 단계부터는 Southern hybridization 방법과 동일하게 수행하였다.
결과 및 고찰
신규 저온 저항성 유전자 동정
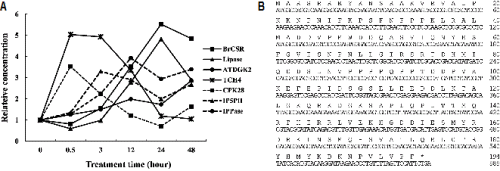
BrEMD의 저온(4°C) 스트레스가 처리된 ‘Chiifu’를 대상으로 한, 2반복의 KBGP-24K oligo chip 자료를 분석한 결과 23,929개의 unigene들 중 저온 처리 시 대조군 대비 5배 이상 발현이 증가하는 417개(1.7%)의 저온 반응 유전자를 1차 선발하고, 이들 중 기능이 정확히 알려지지 않았으나 완전장을 갖춘 유전자를 최종 선발하여 BrCSR로 명명하였다. 선발된 BrCSR과 저온 저항성 관련 유전자로 알려진 6개[IPPase(AT5G63990), GDSL-like lipase(AT3G48460), ATDGK2 (AT5G63770), CPK28(AT5G66210), IP5PII(AT4G18010), TCH4(AT5G57560)]의 유전자들의 시간대별 발현 변화를 분석한 결과, 우선 BrCSR은 기존의 저항성 관련 유전자들과 유사하게 대조군 대비 발현량이 최대 5.5배까지 증가됨으로써 저온 자극과 관련된 유전자임을 추정하였고, 저온 자극 초기에 발현되는 TCH4(AT5G57560)(Purugganan et al., 1997)와 CPK28(AT5G66210)(Lee et al., 2005)과는 달리, GDSL-like lipase(AT3G48460)(Jiang et al., 2012)와 ATDGK2 (AT5G63770)(Gómez-Merino et al., 2004)처럼 초기(1차) 자극에 의해 유발되는 2차 신호로 발현되는 저온 저항성 관련 유전자들 중의 하나임을 확인할 수 있었다(Fig. 2A). 이 BrCSR의 KBGP-24K chip seqID는 “BRAS0001S00015792”이고, 5’ end EST clone 이름은 “KFSD-035C01”이며, TAIR ID는 “AT1G02870”이다. BrEMD에 공개된 777bp의 cDNA 염기서열에서 585bp의 ORF와 194개의 아미노산을 확인할 수 있었으며(Fig. 2B) 이 정보를 바탕으로 RT-PCR 방법을 이용하여 순계배추의 잎에서 BrCSR를 동정하였다. 동정된 BrCSR의 염기서열을 이용한 BlastX 분석을 수행한 결과, 애기장대(A. thaliana)를 비롯하여 검은시나무(Populus trichocarpa), 피마자(Ricinus communis), 포도(Vitis vinifera) 등과 98% 이상의 아미노산 상동성을 보였으나 이들 작물에서도 그 기능은 아직 밝혀져 있지 않았다(Fig. 2C).
한편, BrCSR의 게놈 내 위치를 확인하기 위하여 529Mbp 전체 배추 게놈 중에 현재 공개되어 있는 2,026개 BAC clone 염기서열을 바탕으로 분석을 한 결과, BrCSR은 VCS3M_DH genetic map에서 10번 염색체(A10)의 40.242cM 위치에 있는 KBrB030F10(B030F10-2) BAC clone에 하나가 존재하고 있음을 확인하였다(Brassica rapa Genome Project, www.brassica- rapa.org)(Fig. 2D).
BrCSR 유전자 기능 분석
In silico 분석을 통해 BrCSR의 기능을 유추하기 위해, 먼저 NCBI의 conserved domain 분석을 한 결과 동정된 585bp 내 10-546bp(179개 아미노산)까지 “NOP16”으로 추정되는 도메인이 존재하는 것을 확인하였다. 이 도메인은 효모(Saccharomyces cerevisiae)와 인간(Homo sapience)을 대상으로 한 연구에서 ribosome biogenesis의 기능을 하는 NOP16 단백질의 과발현이 유방암 환자의 치료 효율(생존율)을 높이는데 관여한다고 보고하였다(Butt et al., 2008; Kundel et al., 2012). 이에 따라 효모 및 인간에서처럼 식물에서도 NOP16 도메인은 리보솜 합성과 관련된 기능을 할 것으로 예측하였다. 식물에서 리보솜 합성과 저온 스트레스의 관련성에 대한 연구로서, Lee et al.(2005)은 애기장대 연구에서 저온 자극 시 리보솜 합성을 포함한 RNA 대사 관련 유전자[Nuclear transport factor 2(AT1G69250), RNA and export factor binding protein(AT5G59950), CCR4-associated factor 1(AT3G44260) 등]들의 발현이 크게 증가함을 보고하였다. 한편 애기장대 기관 발달 과정에서의 리보솜 합성은 auxin 호르몬이 중요 조절 인자로 연관되어 있고(Rosado et al., 2010), 다양한 리보솜 합성에 관여하는 뉴클레올린(nucleolin)이라는 RNA 결합 단백질의 활성 정도가 식물의 생장과 조직형태 결정에 매우 중요한 요소라는 연구결과도 보고되었다(Petricka and Nelson, 2007). 한편 애기장대 데이터베이스를 기반으로 BrCSR과 관련된 유전자들을 분석한 결과, 총 19개의 유전자가 BrCSR의 발현 변화에 영향을 받는 것으로 확인되었고, 이 중 10개의 유전자가 리보솜 합성과 관련된 것으로 확인되었다(GENEMANIA, www.genemania.org)(Table 1). 특히 BrCSR과 밀접한 관련성이 있는 것으로 분석된 저온 저항성 관련 유전자인 Arabidopsis glycine-rich RNA- binding protein 2(ATGRP2, AT4G13850)는 애기장대 연구에서 ATGRP2의 발현 향상이 저온 스트레스 환경에서 abscisic acid(ABA) 호르몬과 관계없이 종자 발아와 어린 식물의 생장을 촉진했다는 연구결과도 보고되었다(Kim et al., 2007). 또한 “Arabidopsis eFP Browser(www.bar.utoronto.ca)”(Winter et al., 2007)를 이용한 분석에서 BrCSR은 호르몬 관련 비교에서 ABA, zeatin, indole-acetic acid(IAA), methyl jasmonate, gibberellic acid 3(GA3), brassinosteroids이 처리된 어린 애기장대 모든 조직에서 처리농도 및 시간에 관계없이 일정한 발현 수준을 보였으며, 조직별 발현 비교에서는 정단분열조직에서, 식물 발달 단계별 비교에서는 24시간 동안 수분을 흡수한 종자에서 상대적으로 강하게 발현됨을 확인할 수 있었다. 이에 따라 BrCSR는 식물 호르몬과는 독립적으로 정단분열조직 및 발아 초기의 종자에서 리보솜 합성 촉진 기능과 밀접한 관련이 있으며, 저온 스트레스 조건 하에서는 식물의 생장 및 조직형태 유지에 관여하여 저온 저항성을 부여하는 기능을 하는 것으로 추정할 수 있다.
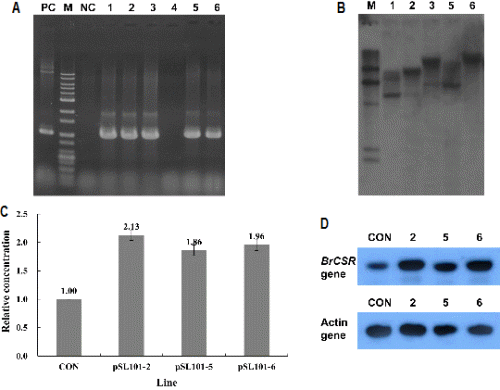
현재까지 명확한 기능이 밝혀지지는 않았으나, 선행 연구 결과로 배추의 저온 저항성 관련 유전자로 추정되는 BrCSR 유전자의 기능을 알아보기 위해 모델 식물인 담배(N. tabacum ‘SR1’)에 BrCSR의 과발현을 유도하였다. BrCSR 과발현용 pSL101 vector를 Agrobacterium을 이용한 형질전환 방법으로 담배에 도입한 결과, 총 6개체의 추정 담배 형질전환체를 생산하였으나 이 중 1개체는 hygromycin 저항성 유전자(hpt)를 대상으로 한 PCR 증폭 시 hpt 유전자의 존재가 확인되지 않아 이 개체를 제외하고 최종 5개체의 담배 형질전환체를 선발하였다(순서대로 pSL101-1, -2, -3, -5, -6으로 명명함)(Fig. 3A). 또한 5개체의 PCR product의 염기서열 분석으로 hpt 유전자임을 확인하여 pSL101 vector가 정상적으로 도입된 형질전환체임을 증명하였다. 아울러 Southern hybridization 분석으로 이들의 T-DNA 도입 수를 확인한 결과, 3개체(pSL101-2, -5, -6)에서 1 copy의 T-DNA가 도입되었음을 알 수 있었다(Fig. 3B). 선발된 형질전환체들을 대상으로 저온 스트레스 환경 시 내부 BrCSR 유전자의 발현 수준을 분석하기 위해 4°C에서 5일 동안 처리하였다. 저온 처리된 pSL101 담배 형질전환체들을 대상으로 BrCSR 유전자의 발현 수준을 quantitative real-time RT-PCR과 Northern blot hybridization 분석으로 확인하였으며, 내부 대조 유전자인 action 유전자의 일정한 발현을 통해 실험의 신뢰성을 확인하였다(Figs. 3C and 3D). Quantitative real-time RT-PCR과 Northern blot hybridization 분석에서 대조군에서 약하게 유전자의 발현이 확인되는 것은 도입한 BrCSR과 유사한 염기서열을 가진 유전자가 담배에도 존재하며 그것이 발현된 것으로 추측된다. Quantitative real-time RT-PCR과 Northern blot hybridization 분석에서 동일한 결과로 3개의 형질전환체들 모두 대조군 대비 발현량이 약 2배 정도 증가한 것으로 나타났다.
BrCSR 유전자가 도입된 형질전환 T1 세대 담배와 대조군인 비형질전환체의 저온 처리 시 표현형을 비교한 결과 1 copy의 BrCSR가 도입되어 대조군 대비 발현량이 증가한 3개의 담배 형질전환체들은 저온 처리 5일째가 되었을 때 명확하게 대조군과 다른 표현형을 보였다. 대조군인 비형질전환체의 담배는 잎과 줄기의 탄력을 잃고 힘없이 쓰러졌으며 엽색이 점차 연해지고 더 이상 생장하지 못하는 모습을 보인 반면, 형질전환된 3개체는 모두 저온 처리 전과 동일한 모습으로서 표현형상의 차이를 보여 주지 않았다(Fig. 4). 저온 스트레스는 CO2의 흡수율을 2배 이상 감소시키고 광합성 전자 수송을 억제하여 광합성 효율을 급격히 저하시키며(Foyer et al., 2002; Savitch et al., 2009), 동시에 활성산소종(reactive oxygen species, ROS)을 발생시켜 광합성에서의 광저해(photoinhibition) 작용을 유발하여(Greer, 1990; Savitch et al., 2011) 작물의 생육을 크게 저해시킨다는 보고들이 있다. BrCSR과 연관이 있는 유전자들을 제시한 Table 1에서 리보솜 합성과 밀접히 관련된 것으로 확인된 10개의 유전자를 제외한 10개 유전자 중에 AT3G06790(Takenaka et al., 2012)와 AT1G71260(Desveaux et al., 2005)은 엽록체 관련 단백질이며, AT5G11630(Vellosillo et al., 2007), AT2G20940 (Jen et al., 2006) 및 AT4G13850(Kim et al., 2007)은 스트레스에 대한 방어기작 관련 유전자들이다. 실제로 저온 처리된 배추의 BrEMD 분석결과에서도 AT1G71260, AT5G11630 및 AT2G20940의 발현이 1.7-3.1배까지 증가한 것으로 나타나, 이들이 저온 스트레스에 저항성과 밀접한 관련이 있는 것으로 추정된다(Desveaux et al., 2005; Jen et al., 2006; Vellosillo et al., 2007).
결론적으로 내혼계배추(‘Chiifu’)의 저온 자극 시 5배 이상의 발현량 증가 및 저온 스트레스 관련 유전자들과의 발현 비교 분석(BrEMD의 KBGP-24K microarray 분석), NOP16 domain 분석, 애기장대에서의 생장과 기관발달 관련 연구보고 및 실제 담배 형질전환체의 저온 자극 시 표현형 비교를 종합하여 볼 때, BrCSR 유전자는 저온 스트레스 발생 시 발현량의 증가를 통해 식물의 생장 및 발달을 유도하여 저온 저항성을 부여하는 유전자일 것으로 판단된다.