서 언
재료 및 방법
배추 형질전환체 확보
Genomic DNA 추출 및 형질전환체 선발
T-DNA 삽입 위치 분석
Semi-quantitative RT-PCR 분석
BrSSR의 체내 발현 수준 및 염 저항성 분석
cDNA 칩 분석
결과 및 고찰
체내 BrSSR 발현 수준 및 염 저항성 분석
게놈 내 T-DNA 도입 위치 분석
염 스트레스 반응 유전자 선별
염 저항성 관련 유전자 발현 패턴 분석
서 언
다양한 비생물적 스트레스 중에서 토양의 염 집적은 거의 대부분의 작물에서 생장 및 생존을 위협하는 큰 요인 중의 하나이다. 이러한 염 스트레스는 100개국 이상의 국가에서 농업작물의 수확량을 감소시키고 있는 것으로 보고되었다(Flowers and Yeo, 1995; Munns, 2002, Rengasamy, 2006). 토양에서 상대적으로 높은 농도의 염이 집적되면 식물체가 토양에서 수분을 흡수하는 것을 제한하게 되어 식물 세포의 죽음으로 이어진다(Munns, 2002). 또한 삼투성 스트레스(osmotic stress)와 이온 유독성(ion toxicity)으로 잘 알려진 Na+ 이온의 세포 내 증가는 산화적 스트레스(oxidative stress)로 이어져 식물체 생육에 불리하게 작용하지만, 작물의 염 저항성 획득이 산화적 스트레스에 대한 내성을 향상시켜 주었다는 보고도 있다(Hernandez et al., 2001).
2000년도 전・후로 염 저항성과 관련된 활발한 연구들이 수행되어 다양한 유전적, 생리적 연구 결과들이 보고되었다. 그 예로 식물의 salt overly sensitive(SOS) 유전자군 중 특히, SOS1, SOS2, SOS3가 세포 내 이온항상성(ion homeostasis)과 염 저항성을 조절하는 신호 전달 체계에서 중요한 역할을 담당함을 보고하였고(Bertorello and Zhu, 2009; Gong et al., 2001; Halfter et al., 2000; Liu et al., 2000; Shi et al., 2003; Wu et al., 1996; Yang et al., 2009; Zhu, 1998, 2003), 벼의 OsCDPK7(rice calcium-dependent protein kinase) 유전자가 과발현된 형질전환 벼의 생장성 개선 연구(Saijo et al., 2000)와 보리의 late embryogenesis abundant(LEA) 단백질 유전자인 HVA1이 도입된 벼에서 염 저항성이 크게 향상되었다는 보고(Xu et al., 1996) 등이 있다. 한편, 이들 저항성 유전자들의 연구를 활용한 염 스트레스 저항성 작물의 개발은 농업 생산량의 유지 및 증가를 위해 계속적으로 요구되고 있다.
이에 본 연구팀은 2013년에 B. rapa ssp. pekinensis ‘Chiifu’를 대상으로 한 “KBGP-24K microarray chip”을 분석하여 DUF581 도메인을 보유하고 있는 BrSSR 유전자를 내혼계 배추 ‘CT001’(시원씨드, 경기도 평택)에서 동정하였으며, 담배(Nicotiana tabacum)에서 과발현을 유도하여 BrSSR의 과발현이 염 저항성 획득에 기여함을 확인하였다(Yu and Park, 2013). 따라서 본 연구는 염 저항성 유전자로 추정되는 BrSSR (Brassica rapa Salt Stress Resistance) 유전자를 과발현(over- expression) 시킨 형질전환 배추(B. rapa ssp. pekinensis)를 이용하여 BrSSR 유전자의 염 저항성 기능 검정을 수행하였다. 또한 microarray 데이터를 이용한 배추의 염 저항성 관련 유전자들의 발현 네트워크를 비교・분석하여 BrSSR과 밀접하게 연관된 유전자들을 밝혀 내었다.
재료 및 방법
배추 형질전환체 확보
배추의 환경 스트레스 저항성 관련 전사체(transcriptome) 분석용 KBGP-24K 올리고 칩 데이터를 분석한 결과(Lee et al., 2008), 아직 기능이 알려지지 않았으며 염 스트레스 발생 시 대조군 대비 5배 이상 발현이 증가한 것으로 확인된 BrSSR 유전자를 이용하여 과발현용 형질전환 vector인 pSL94 vector를 제작하였다. 본 연구는 실제 내혼계 배추(B. rapa ssp. pekinensis inbred line ‘CT001’)에서도 BrSSR이 염 저항성 획득에 관여하는지를 확인하고, 아울러 microarray 분석을 수행하여 염 스트레스에 반응하는 저항성 관련 유전자들의 발현 양상을 분석하기 위해, Lee et al.(2004)에 의해 보고된 배추 형질전환 방법을 이용하여 pSL94 vector를 내혼계 배추에 도입하였다. 형질전환이 확인된 배추계통들은 뇌수분 방법으로 T1 세대로 진전시킨 후 본 연구에 이용하였다.
Genomic DNA 추출 및 형질전환체 선발
배추 형질전환체의 잎을 이용한 genomic DNA 추출은 Lee et al.(2004)에 제시된 방법과 동일하게 수행하였다. 또한 형질전환체들을 선발하기 위한 hygromycin 저항성 유전자(hpt) 대상 PCR 분석 및 삽입된 T-DNA 개수의 확인을 위한 DNA blot 분석은 Yu and Park(2013)에 제시된 방법과 동일하게 수행하였다.
T-DNA 삽입 위치 분석
10µg의 gDNA를 SacI 제한효소로 18시간 동안 처리한 후, phenol-chloroform-isoamyl alcohol(25:24:1) 용액을 이용하여 정제하였다. 그 후, thermocycler(Biometra, USA)를 사용하여 50µL 반응액으로 inverse PCR을 수행하였다(Yu et al., 2010). 증폭된 PCR 산물은 pGemT-easy vector(Promega, USA)에 삽입 후 염기서열을 분석(Macrogen Co., Korea)하였다. 확인된 flanking DNA 염기서열은 “Flanking Sequence Tag Validator(FSTVAL)” 프로그램(GreenGene Bio Tech Inc., Korea)을 이용하여 배추 게놈 내 삽입 위치를 분석하였다(Kim et al., 2012).
Semi-quantitative RT-PCR 분석
Microarray 데이터를 활용하여 구축된 네트워크상의 유전자들을 대상으로 대조군(CON) 대비 형질전환체에서의 발현량의 차이를 분석하기 위해 semi-quantitative RT-PCR을 수행하였다. Yu et al.(2012)에 제시된 방법으로 대조군과 형질전환체에서 RNA를 추출한 후, Maxime RT-PCR premix (iNtRON Biotechnology, Korea)를 이용하여 cDNA 합성 및 PCR 증폭을 수행하였다. PCR에 사용된 primer 정보는 Table 1에 제시하였으며, 증폭은 94°C에서 5분간/1회 predenaturation한 후 94°C에서 30초간 denaturation, 60°C에서 30초간 annealing, 72°C에서 30초간 extension 과정을 진행하였으며, 증폭 회수는 대조군 대비 형질전환체에서 4가지 유전자(ERD15, PAM2, GABA-T, BrSSR)의 발현량의 차이가 현저하게 나타나는 25cycle로 수행하였다. 증폭된 PCR 산물은 1× TBE buffer를 사용하여 1% agarose gel 상에서 100V, 30분간 전기영동하여 ethidium bromide (EtBr)로 염색한 후, UV illuminator를 이용하여 반응산물을 확인하였다.
BrSSR의 체내 발현 수준 및 염 저항성 분석
염 스트레스 발생 시 BrSSR 유전자의 발현 양상을 확인하기 위해, 바로커 상토(원예범용, 서울바이오)에서 생장하여 본엽이 6-8매가 된 비형질전환 대조군(CON)과 형질전환체들을 3일(유전자 발현 수준 분석용), 15일(표현형 분석용) 동안 250mM NaCl 용액으로 건조하지 않게 처리하였다. 생육조건은 생물적・비생물적 변수가 최대한 억제된 공간에서 진행되었으며 광도 250µmol・m-2・s-1, 광주기 16시간 명처리/8시간 암처리, 온도 22 ± 2°C, 습도 30-50%로 유지해 주었다. 3일 처리된 개체들에서 total RNA를 추출하였으며, 추출된 RNA를 이용하여 quantitative real-time RT-PCR을 수행하여 체내 BrSSR의 발현 수준을 분석하였다(Yu and Park, 2013). Quantitative real-time RT PCR 분석 결과로 체내 BrSSR가 과발현된 형질전환 배추와 대조군인 비형질전환 배추(CON)를 대상으로 15일간 염 스트레스 발생 시 표현형의 변화를 관찰하였다.
cDNA 칩 분석
염 저항성을 보인 형질전환 배추를 대상으로 염 스트레스를 처리한 후 RNA를 추출하여 “B. rapa genome 135K cDNA 칩”을 제작 및 분석하여 형질전환체 내 BrSSR 유전자 및 관련 유전자들의 발현 패턴을 분석하였다. B. rapa genome 135K cDNA 칩(Nimblegen, Madison, WI, http:// www.nimblegen.com)은 41,173개의 unigene을 포함하고 있으며, 한 유전자당 3개의 probe로 발현이 탐지되도록 제작되었다. 추출된 RNA를 이용한 혼성화 단계는 Yu et al.(2012)에 제시된 방법과 동일하게 수행하였다. 발현 시그널은 GenePix scanner 4000B(Axon Instrument, NY)로 수집하고, NimbleScan v2.5 software(Nimblegen, WI)를 통해 수치화하였다. 획득한 데이터 값을 바탕으로 우선 MultiExperiment Viewer(http://www.tm4.org) 프로그램을 이용하여 발현 수준에 따라 유전자들을 분류하고, 높은 유의성을 가지는 false discovery rate(FDR)값의 주요 유전자들은 TAIR gene ontology annotation(http://www.arabidopsis.org), MapMan(http://mapman. gabipd.org), cytoscape(http://www.cytoscape.org) 분석 프로그램들을 이용하여 BrSSR과 염 저항성 관련 유전자들의 발현 패턴을 비교・분석하였다.
결과 및 고찰
체내 BrSSR 발현 수준 및 염 저항성 분석
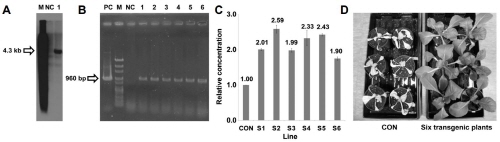
BrSSR 유전자의 배추 내 염 저항성 여부를 알아보기 위해 내혼계 배추(‘CT001’)를 이용하여 BrSSR 과발현 vector인 pSL94 vector로 형질전환하였다. 생산된 T0 배추 형질전환체들 중 hygromycin 저항성 유전자(hpt)를 대상으로 DNA blot 분석을 수행하여 1 copy의 T-DNA가 삽입된 계통을 선발하고(Fig. 1A), 삽입이 확인된 계통의 종자를 파종하여 PCR분석 및 염기서열 분석을 통해 6개의 T1 형질전환체를 확보하여 S1, -2, -3, -4, -5, -6으로 명명하였다(Fig. 1B). 선발된 T1 형질전환체들을 대상으로 염 스트레스 환경 시 내부 BrSSR 유전자의 발현 수준을 분석하기 위해 3일간 염 처리를 수행하였다. 스트레스가 처리된 비형질전환체(CON)와 형질전환체들(S1-S6)에서 각각 total RNA를 추출하였고, 이를 이용하여 quantitative real-time RT-PCR 분석을 수행하였으며 내부 대조 유전자인 actin 유전자의 발현량을 이용하여 BrSSR의 발현값을 보정하였다. 그 결과, 6개체들 모두에서 체내 BrSSR의 발현량이 대조계통(CON) 대비 1.90-2.59배까지 증가한 것으로 분석되었다(Fig. 1C).
한편, 15일간 염 스트레스 처리 후 이루어진 표현형 분석에서 대조군인 비형질전환체들은 처리 5일 후, 성숙잎부터 엽색이 점차 노란색으로 변한 후 급격히 수분을 모두 잃어 갔으며 중륵 부위도 더 이상 생장하지 못하며 고사하기 시작하였다. 반면, BrSSR이 과발현된 것으로 확인된 6개의 형질전환 배추들은 모두 염 처리 전과 동일한 모습을 유지하여 표현형상의 뚜렷한 차이를 보여 주었다(Fig. 1D). 또한 ‘Chiifu’ 배추를 대상으로 하여 염 처리 48시간까지의 시간대별 발현 변화를 분석한 B. rapa KBGP-24K microarray 분석 결과에서, BrSSR은 대표적인 염 저항성 유전자로 알려진 SOS 유전자군보다 더 민감하게 반응하는 것으로 분석되었다(Lee et al., 2008; Yu and Park, 2013). 즉, 아직까지 명확한 기능이 알려지지 않았던 BrSSR 유전자는 염 스트레스 환경 조건 시 식물의 염 저항성 향상 기작에 있어 중요한 역할을 하고 있는 것으로 판단된다.
게놈 내 T-DNA 도입 위치 분석
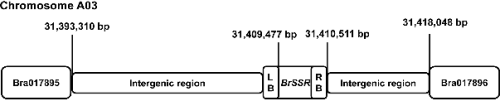
염 저항성을 보인 배추 형질전환체를 대상으로 전이된 T-DNA의 염색체 내 삽입 위치를 확인하기 위하여 inverse PCR 분석을 수행하였다. PCR산물의 염기서열을 확인하고 이를 “Flanking Sequence Tag Validator(FSTVAL)” 프로그램(GreenGene Bio Tech Inc., Korea)을 이용하여 배추 게놈 내 T-DNA 삽입 위치를 분석하였다. 그 결과, pSL94 vector의 T-DNA가 A03염색체의 intergenic region에 삽입되어 있는 것으로 확인되었다(Fig. 2).
염 스트레스 반응 유전자 선별
T-DNA가 intergenic region에 삽입된 것으로 확인된 형질전환체를 이용하여 도입한 BrSSR 유전자의 과발현과 관련하여 염 저항성과 관계될 것으로 추정되는 유전자들의 선발 및 발현 패턴을 분석하기 위해 “B. rapa genome 135K cDNA microarray 데이터”를 분석하였다. 우선 microarray 데이터를 MultiExperiment Viewer 프로그램으로 분석한 결과, 분석된 총 4,009개의 유전자 중 대조군 대비 발현이 증가한 유전자는 2,103개이고, 발현이 감소한 유전자는 1,906개로 분석되었다. 이들 중 4배 이상 발현이 변화한 유전자 선별 결과, 총 710개이며 498개는 발현이 4배 이상 증가하였고, 212개는 발현이 4배 이상 감소한 것으로 나타났다. 이 분석 데이터를 바탕으로 대조군 대비 발현이 크게 변화하고 높은 유의성을 가지는 유전자들을 재차 분석하여[false discovery rate(FDR) < 0.05], 발현 증가 유전자 집단에서 265개, 발현 감소 유전자 집단에서 109개로 총 374개 유전자들을 선별하였다. 이들 주요 유전자들을 각각 TAIR gene ontology annotation을 이용하여 3가지 기능 범주(biological process, cellular component, and molecular function) 중 어느 범주에 속하는 지를 확인하여 체내 유전자들의 변화를 분석하였다. 분석 결과, cellular component에서는 “Chloroplast”, “Nucleus”에 속한 유전자들이 많이 발현하며, molecular function에서는 “Transferase activity”, “Hydrolase activity”에 속한 유전자들이 많이 발현되었다. Biological process에서는 “Response to stress”, “Response to abiotic or biotic stimulus”에 속한 유전자들 중 발현이 증가한 유전자들이 많이 분석되었는데, 특히 “Calcineurin B-like protein-interacting protein kinases (CIPKs, CBL-interacting protein kinases)” 관련 유전자들의 발현이 크게 증가한 것으로 확인되었다. CIPKs 중 CIPK24는 SOS2와, CIPK4는 SOS3과 서로 상호작용하여 식물체 내의 Na+ 항상성을 유지하며, CIPK6와 CIPK23은 염 자극 시 발행하는 활성산소류(reactive oxygene sprecies, ROS)들의 포집 및 소거 및 K+/Na+ 항상성을 조절하는 것으로 보고되어 있다(Deng et al., 2013; Martinez-Atienza et al., 2007; Qiu et al., 2002; Tang et al., 2010; Xiang et al., 2007; Zhao et al., 2009; Zhu, 2003). 또한 FDR값으로 선별된 유전자들을 대상으로 MapMan 프로그램을 이용하여 식물 호르몬 및 비생물적 스트레스와 관련된 유전자들의 발현 수준을 분석하였다(Table 2). 식물 5대 호르몬(옥신, 사이토키닌, 지베렐린, 앱시스산, 에틸렌)과 jasmonic acid, salicylic acid 합성 및 작용 경로 관련 분석에서, 특히 앱시스산 및 에틸렌, jasmonate 관련 반응 유전자들의 발현량이 큰 차이를 보였다. 또한 비생물적 스트레스 반응 기작과 관련된 분석 결과, 염 스트레스에 반응하고 salicylic acid 대사 과정을 조절하는 “Calmodulin binding protein of 25kDa”의 변화가 가장 크게 발현됨을 알 수 있었다(Perruc et al., 2004). 한편, 대표적인 저온 스트레스 반응 유전자로 보고된 “Low-temperature- induced 78”(Mantyla et al., 1995; Nordin et al., 1993)의 발현 수준이 대조군과 유사하게 분석되었다. 이는 염 저항성과 관련된 BrSSR의 발현 변화가 염 집적과 같은 비생물적 스트레스 중 하나인 저온에 반응하는 유전자들의 발현 변화에도 영향을 미칠 것이라는 예상과는 다른 결과였다. 즉, BrSSR은 염 스트레스에만 특이적으로 반응하는 저항성 기작과 연관이 있을 것으로 판단된다.
염 저항성 관련 유전자 발현 패턴 분석
도입한 BrSSR 유전자와 관련된 유전자들의 발현 패턴을 분석하기 위해 우선 Lee et al.(2008)에서 보고된 “KBGP-24K 올리고 칩” 데이터와 PlantArrayNet(GreenGene Bio Tech Inc., Korea)의 “Brassica 300K microarray” 데이터를 분석하여 배추 내 염 저항성 관련 유전자들의 발현 네트워크를 구축하였다. 구축된 유전자 발현 네트워크는 multi-edge node pair와 self-loop node를 분석하여 총 1,853개의 node와 5,740개의 edge로 구성되었다. 구축된 네트워크의 connected component의 수가 142개를 이루고 있어 높은 상호 관계를 이룬 네트워크만이 구축되어 있음을 보이고 있으며, 이들 하위 connected component 중 가장 크게 차지하고 있는 그룹은 1,398개의 node와 5,375개의 edge를 포함하고 있어, 전체 네트워크의 node 중 75.44%를 차지하고, 총 edge의 93.64%를 차지하고 있었다. 또한 네트워크 내에 연결된 2개의 node의 거리를 나타내는 characteristic path length 값은 18.304로 구축된 네트워크가 밀접한 연관관계로 이루어져 있는 것으로 판단된다(자료 미제시).
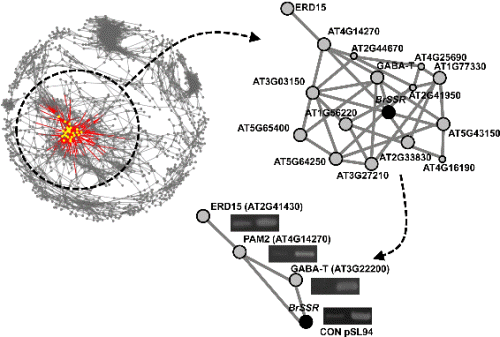
구축된 발현 네트워크와 “B. rapa genome 135K cDNA 칩” 데이터를 이용하여 과발현된 BrSSR 유전자의 발현 네트워크를 분석하였다(Fig. 3). BrSSR 유전자와 발현 네트워크상에서 직접적으로 연결된 주요 유전자로는 polyadenyl 결합 단백질의 PABC domain과 반응하는 “Protein containing PAM2(AT4G14270)”과 “gamma-aminobutyrate transaminase (GABA-T)(AT3G22200)”가 확인되었다. GABA-T는 “succinic semialdehyde dehydrogenase(SSADH)”와 함께 GABA를 TCA-cycle에 필수적인 succinate로 합성하는 역할을 하고 있다. Krasensky and Jonak(2012) 보고와 Fait et al.(2008) 보고에 따르면 succinate는 식물의 비생물적 스트레스 저항성에 필수적인 요소로써 GABA-T의 발현이 억제될 경우 스트레스 저항성이 약해진다고 보고하였다. 이에 따라 BrSSR의 경우 네트워크로 밀접히 연결되어 있는 GABA-T의 발현과 밀접한 상호 관계를 가지고 있을 것으로 판단된다. 또한 BrSSR은 PAM2 motif를 가진 unknown 유전자와 밀접한 네트워크를 가지고 있는 것으로 분석되었다. PAM2 motif를 가진 PABC domain을 보유한 유전자 중 대표적인 유전자로는 “early responsive to dehydration 15(ERD15)(AT2G41430)”가 있다. Ziaf et al.(2011)의 연구에 따르면 ERD15를 과발현 시키면 식물체의 Photosystem II(PSII)의 quinone 수용체를 부분적으로 산화적 형태로 유지시킴으로써 PSII의 효율을 증가시킨다고 보고하였다. 또한 이러한 PSII의 효율 증가는 삼투압을 조절하는 세포 내에 이면성 용질(compatible solute)의 양을 증가시키고, 지질 과산화(lipid peroxidation)를 억제하여 염 등의 비생물적 스트레스의 내성을 비약적으로 증가시켜 준다고 보고하였다. 즉, BrSSR은 PAM2 motif를 가진 unknown 유전자들을 매개로 GABA-T와 함께 succinate의 발현을 유지하고 ERD15의 발현을 촉진하여 PSII의 효율을 증진시키는 것으로 염 저항성을 부여하는 것으로 추정된다. 실제로 염 처리된 형질전환체와 대조군을 대상으로 BrSSR을 포함한 3개의 유전자의 발현량을 semi-quantitative RT-PCR로 분석한 결과, 모두 대조군보다 높은 발현 수준을 보여 줌으로써 4개의 유전자가 서로 연결되어 있음을 확인할 수 있었다.
결론적으로 본 연구에서의 배추의 염 저항성 표현형 분석 및 발현 네트워크 결과를 종합해 볼 때, BrSSR 유전자는 기존에 보고된 염 저항성 관련 유전자들과 네트워크적으로 연결되어 있으며 실제 염 스트레스 처리 시에도 뚜렷한 저항성을 보여줌으로써 배추의 염 스트레스 발생 시 발현량의 증가를 통해 염 저항성 향상에 기여하는 것으로 판단된다.