서 언
재료 및 방법
토양시료 채취
토양의 화학성 분석
산, 고형물함량 및 pH 측정
무기성분 분석
알리인, 알리신 및 총 피루베이트산 함량 분석
총 페놀, 플라보노이드 및 환원당 함량 측정
α-Glucosidase 억제활성 측정
항균활성 측정
통계분석
결과 및 고찰
토양의 물리적 및 화학성
산, 고형물함량 및 pH 측정
무기성분 분석
알리신, 알리인 및 총 피루베이트산 함량 분석
총 페놀, 플라보노이드, 환원당 및 α-glucosidase 저해활성 측정
항균활성 측정
서 언
중앙아시아나 지중해 연안이 원산지로 알려진 마늘(Allium sativum L.)은 파를 비롯한 양파, 삼채, 부추 및 달래 등과 함께 백합과(Liliaceae), 파속(Allium)에 속하는 초본성 식물이다(Shin et al., 2004). 일찍이 김치문화가 발달한 우리나라는 주요 조미채소로 마늘(25,062ha, 353,761ton)을 많이 이용하고 있으며 실질적으로 노지채소 중 고추(36,120ha, 85,068 ton), 배추(28,301ha, 2,120,393ton) 다음으로 많이 재배하고 있다(http://www.kosis.kr). 이러한 마늘은 한지형과 난지형의 두 가지 생태형으로 분류되는데 제주에서 재배되는 품종들은 대부분 난지형에 속한다. 난지형 마늘은 한지형 마늘에 비하여 휴면기간이 짧고 파종 후 어느 정도 자란 상태에서 월동하며, 단위면적당 수확량이 많은 것이 특징이다.
남도마늘은 1970년대 중국 상해지역에서 재배되던 ‘가정백’이란 품종을 국내로 도입한 후 국내 적응시험 및 재배특성을 통과하여 재배되기 시작하였으며(Kim et al., 2009), 제주도내 재배마늘의 90% 이상을 차지하고 있다. 이러한 남도마늘의 연구동향은 주아재배의 기계화 체계를 확립하기 위해 시비량, 지온과 파종시기에 대한 연구(Ahn et al., 2008, 2010; Choi et al., 2009; Kim et al., 2009), 품종별 마늘의 생장량과 수확량의 변화(Hwang et al., 2009; Ra and Park, 1987; Song et al., 2001), 마늘의 향기성분과 항산화활성 분석(Jeong et al., 2007; Kwon et al., 2014; Shin et al., 2011a,b) 및 토양과 마늘 성분 함량간 상관관계(Kim et al., 2015)에 대한 연구가 주를 이루고 있다.
식물은 재배지의 자연환경(기후, 토양이나 지형)이나 재배방법(재배방식이나 기술, 시비법 등) 및 품종에 따라 생육이나 체내 함유 성분들의 차이를 나타내게 된다. 따라서 어떤 지역에 재배하느냐에 따라 그 작물의 유용성분 함량을 최대한 높일 수 있는 전략이 되며 그 지역이 그 작물의 주산지가 되기도 하는데 마늘 또한 그러하다. 제주는 남도마늘의 대표적 재배지로, 특히 동부와 서부에서 재배되는 마늘의 토양 및 함유 성분들을 비교하면 지역에 따른 차이를 확인할 수 있으며 향후 재배농가의 홍보자료 및 특정 성분을 목적으로 한 맞춤형 재배가 이루어 질 수 있으리라 기대된다. 본 연구는 제주의 동부와 서부 마늘 재배지역의 토양 및 생산된 마늘을 이용하여 다양한 성분분석을 실시하였기에 보고한다.
재료 및 방법
토양시료 채취
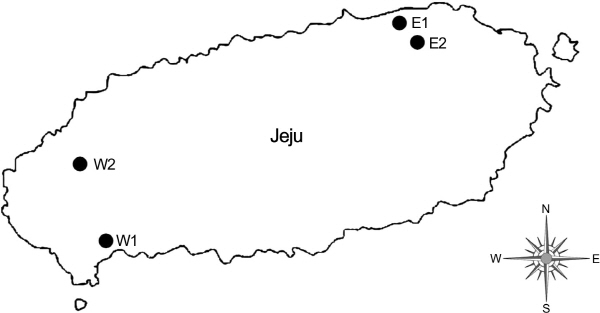
토양시료는 2013년 8월부터 9월에 마늘을 파종하여 재배한 곳으로 동부와 서부 각각 2개지점을 선정하여 채취하였다(Fig. 1). 토양 색에 따라 분류하였을 때 농암갈색 화산회토 구좌통이었다.
토양의 화학성 분석
토양의 화학적 성질을 조사하기 위하여 마늘을 수확한 농지로부터 토양을 채취하여 풍건시킨 후에 2mm 체를 통과시켜 농촌진흥청 농업과학기술원 토양 및 식물체 분석법(RDA, 2000)에 준하여 분석하였다. 토양 pH는 토양:증류수의 비를 1:5로 하여 토양 5g에 증류수 25mL를 첨가한 다음 진탕하여 pH meter(Orion Star A211, Thermo Scientific, UK)를 이용하여 측정하였다. 전기전도도는 pH와 동일하게 제조된 시료를 전기전도도계(Orion Star A329, Thermo Scientific, UK)를 이용하여 측정하였다. 토양 유기물함량은 Walkley and Black법을 이용하여 측정하였다. 질소함량은 토양시료를 황산으로 분해한 다음 Kjeldahl법으로 자동증류장치(K9840, Jinan Hanon, China)로 증류한 후 0.1N HCl 적정용액으로 적정하였다. 교환성 양이온은 토양 5g에 1N ammonium acetate용액(pH 7.0) 50mL를 첨가하여 30분간 진탕한 다음 여과하여 얻어진 여액을 ICP(JY 138 Ultrace, Jobin Yvon, France)를 이용하여 분석하였다. 토양 Fe, Mn, Zn 및 Cu 함량은 토양 5g에 0.1N HCl 중금속 추출액 25mL를 첨가한 후 30°C에서 1시간동안 진탕하여 여과한 용액을 ICP를 이용하여 분석하였다. 유효황은 토양 10g을 침출액(Calcium phosphate monohydrate; 500ppm P용액) 100mL를 가해 30분동안 진탕한 후 여과하고, 여과된 시료액 10mL를 시험관에 넣고 25% nitric acid 2.5mL, acetic-phosphoric acid 2mL 및 증류수를 가하여 22mL가 되도록 섞었다. Barium sulphate seed 현탁액 0.5mL를 넣고, barium chloride crystals 0.2g을 첨가하여 섞어준 후 20분 동안 반응시켰다. 반응액에 gum acacia-acetic acid액 1mL를 첨가하고 30분 후에 UV/Vis Spectrometer (Lambda 25, PerkinElmer, USA)를 이용하여 440nm에서 분석하였다. 유효인산은 Lancaster법을 이용하여 토양 5g에 인산침출액 20mL를 첨가하고 10분간 진탕한 다음 여과하여 몰리브덴 청법(molybdenum blue method)으로 발색시켜 UV- spectrophotometer로 분석하였다. 유효규산은 토양 5g에 1N NaOAc(pH 4.0)용액 50mL을 첨가하여 항온 수평 진탕기(60°C, 125rpm)로 90분간 반응시킨 후 5분 동안 차가운 물로 식혀서 여과하였다. 여과 후 시험관에 여과액 5mL를 넣고 0.6N HCl을 5mL, 10% ammonium molybdate을 5mL 넣고 3분 후에 17% sodium sulfite를 10mL 첨가하여 30°C에서 20분간 발색시킨 다음 UV-spectrophotometer를 이용하여 700nm에서 측정하였다.
산, 고형물함량 및 pH 측정
마늘 착즙액 2mL에 증류수 8mL를 첨가하여 교반한 뒤 4°C, 17,000rpm에서 10분간 원심분리(1730MR, Cyrozen, Korea)하여 상층액을 분리하였고, 산/당도 분석장치(NH-2000, Horiba, Japan)를 이용하여 마늘 착즙액의 산도 및 고형물함량을 분석하였으며 고형물함량은 °Brix, 산도는 %로 표시하였다. pH는 위와 동일하게 처리하여 얻어진 시료 10mL를 이용하여 pH meter로 측정하였다.
무기성분 분석
남도 마늘을 수돗물로 세척하여 70°C에서 건조시킨 다음 식용부위인 인편을 분쇄하여 분석용 시료로 이용하였다. 분말화된 시료 0.5g을 분해플라스크에 넣고 왕수(염산 3mL:질산 1mL) 분해법으로 분해시킨 후 P, K, Ca, Mg, Na, Fe, Mn, Zn, Cu 및 S 함량을 ICP를 이용하여 정량하였다. 전질소 함량은 위와 동일하게 처리된 시료 0.5g을 켈달플라스크에 정확히 취하고 H2SO4-H2O2법으로 분해시킨 후 Kjeldahl법으로 정량하였다.
알리인, 알리신 및 총 피루베이트산 함량 분석
알리인 함량 분석은 각각의 시료 1g에 20% 에탄올 30mL을 가하고 30분간 sonication으로 추출하였으며, 추출액은 원심분리기(Combi-514R, Hanil, Korea)를 이용하여 3,000rpm에서 10분간 원심분리하였다. 원심분리 후 상층액을 0.45µm syringe filter로 여과하여 HPLC-DAD(Agilent 1260, Agilent Technologies, Waldbronn, Germany)로 분석하였다. Analytical column은 Agilent Zorbax SB-C18(4.6 × 250mm, 5µm)를 사용하였고, 이동상은 (A) 0.1% formic acid containing water와 (B) 0.1% formic acid containing acetonitrile을 시간에 따라 gradient로 용리하여 분석하였다. 이동상의 속도는 1.0 mL/min, 시료 주입량은 10µL, UV 검출 파장은 210nm에서 검출하였다.
알리신 함량 분석은 각각의 시료 1g에 3차 증류수 30mL을 가하여 30분간 교반하여 추출하여 측정하였다. 칼럼 및 이동상 조건은 알리인 분석조건과 동일하며, 이동상의 속도는 0.7mL/min, 시료 주입량은 20μL, UV 검출기 파장은 254nm에서 검출하였다.
총 피루베이트산 함량은 Schwimmer and Weston(1961)의 방법을 일부 변형하여 실시하였으며 시료 1g에 10% trichloroacetic acid 10mL를 첨가하여 균질화하고 1시간 동안 방치한 후 여과하였다. 여과액 0.2mL에 0.0125% 2,4-dinitrophenylhydrazine 0.2mL를 가하여 37°C에서 10분간 반응한 후 0.6N NaOH 1mL를 혼합하여 UV-spectrophotometer(UV-1800, Shimadzu, Japan)를 이용하여 420nm에서 흡광도를 측정하였다. Sodium pyruvate를 사용하여 얻은 표준검량 곡선으로 총 피루베이트산 함량을 산출하였다.
총 페놀, 플라보노이드 및 환원당 함량 측정
총 페놀 함량은 Kim 등(2010)의 방법을 일부 수정하여 사용하였다. 마늘 착즙액 100µL・mL-1에 50µL Folin-Ciocalteu reagent를 첨가하고 5분간 실온에서 반응시킨 후 0.3mL 20% sodium carbonate를 첨가하였다. 그리고 UV-spectrophotometer를 사용하여 725nm에서 흡광도를 측정하였다. 총 페놀 함량은 gallic acid를 표준품으로 사용하였으며, 검량선으로부터 얻어진 방정식(y = 174.59 × -0.5589, R2 = 0.9998)을 이용하여 추출물 g당 gallic acid의 정량(GAE)으로 표현하였다.
총 플라보노이드는 Moreno 등(2000)의 방법을 일부 수정하여 사용하였다. 시료 200µL에 100µL 10% aluminium nitrate를 섞고, 100µL 1M potassium acetate를 혼합하였다. 그 후 4,600µL의 80% 에탄올을 넣고, 40분 뒤 UV-spectrophotometer 415nm에서 흡광도를 측정하였다. Quercetin을 표준품으로 사용하였고 검량선으로부터 얻어진 방정식(y = 325.46 × -0.3754, R2 = 0.9999)을 사용하여 추출물 g당 quercetin equivalents(QE)로 계산하였다.
환원당 정량법인 DNS법(Miller, 1959)을 변형하여 마늘 착즙액의 환원당 함량을 측정하였다. 각 시료액 200µL에 DNS 시약(7.5g DNS, 14.0g NaOH, 126.1g Rochelle 염, 5.4mL phenol, 5.9g Na2S2O5/L)을 200µL 혼합하여 95°C heating block(HD-96D, Daihan, Korea)으로 15분간 반응시키고 발색된 반응액을 5분간 4°C에서 반응을 정지시킨 후 증류수 600µL를 첨가하여 UV-spectrophotometer 546nm에서 흡광도를 측정하였다.
α-Glucosidase 억제활성 측정
α-Glucosidase 억제활성은 Hyun 등(2014)의 방법에 따라 실험하였다. 각각의 샘플 50µL에 0.5U/mL α-glucosidase 효소액 50µL, 200mM potassium phosphate buffer(pH 6.8) 50µL를 혼합하여 37°C에서 15분간 배양한 후 3mM p-nitrophenyl α-D-glucopyranoside(pNPG) 100µL를 첨가하여 37°C에서 10분간 반응시켰다. 0.1M sodium carbonate 750µL로 반응을 정지시키고 405nm에서 흡광도를 측정하였다. α-Glucosidase의 활성을 50% 억제하는데 필요한 농도를 IC50으로 나타내었다.
항균활성 측정
본 연구에 사용된 균주는 한국농업미생물자원센터(Korean Agricultural Culture Collection, KACC, Suwon, Korea)에서 분양 받았으며 Kim 등(2010)의 방법에 따랐다. 마늘 착즙액의 항균활성을 측정하기 위하여 3종의 그람음성균 Escherichia coli(KACC 14818), Klebsiella pneumonia(KACC 14816), Salmonella enterica subsp. Enterica(KACC 10769)과 4종의 그람양성균 Staphylococcus epidermidis(KACC 14822), Micrococcus luteus(KACC 14819), Kocuria rhizophila(KACC 14744), Bacillus subtilis subsp. Spizizenii(KACC 14741)을 사용하였다. 품종별 마늘 착즙액은 임계희석법을 이용하여 최저저해농도(Minimum Inhibitory Concentration; MIC)로 표시하였다.
통계분석
본 연구의 실험 데이터는 평균 ± 표준편차로 나타내었다. 실험군간의 통계학적 분석은 SPSS(Statistical package for social science, Ver 20)를 사용하여 one-way analysis of variance(ANOVA) 분석을 실시하였으며 유의적 차이가 있는 항목에 대해서는 Duncan’s Multiple Range Test(DMRT)로 p < 0.05의 수준에서 통계학적 유의성을 검정하였다. 또한, 측정 변인간의 관련성을 알아보기 위하여 Pearson 상관분석을 실시하였다.
결과 및 고찰
토양의 물리적 및 화학성
제주의 마늘 재배지를 동부와 서부로 나누어 토양분석을 실시하였다. 제주 지역 토양 특성상 미사와 점토 성분이 66-89% 정도를 차지하였다. 남도 품종이 재배되었던 제주지역의 토양 pH는 6.39-8.20 범위였다(Table 1). 서부지역의 토양 pH는 6.64로 중성을 나타냈고, 동부지역의 pH는 8.14로 알카리성을 나타냈다. 서부지역 토양의 전기전도도는 0.61ds・m-1이었고 동부지역 토양은 1.18ds・m-1을 나타내어 동부지역이 서부지역의 1.9배 높은 전기전도도를 보였다. 남도 마늘을 재배하는 서부지역의 유기물 함량은 7.75%를 나타내었고 동부지역의 토양은 5.88%이었다.
마늘이 재배되었던 서부지역 토양의 유효인산 함량은 373.02ppm이었고, 동부지역은 233.80ppm이었다. 유효황 함량은 서부지역 토양에서 15.18ppm을 나타냈고, 동부지역 토양에서는 3.83ppm으로 서부지역이 4배나 높았다. 유효규산 함량은 서부지역 토양에서 567.02ppm이었고, 동부지역에서는 838.44ppm이었다. 제주도 내 마늘재배 농가에서는 산성토양 개량이나 작물수량 증수 목적으로 규회석 비료를 많이 시용하고 있는데 동부지역이 규회석 과다시용으로 인한 토양 내 칼슘과 규산 성분의 과다축적으로 인하여 토양의 pH가 서부지역보다 높게 나타난 것으로 추측이 된다.
남도 품종이 재배되었던 제주도의 화산회토에 존재하는 교환성 양이온 함량은 칼슘 > 마그네슘 > 칼륨 > 나트륨 순이었다(Table 2). 남도 품종이 재배되었던 서부지역의 칼륨 함량은 1.45cmol+・kg-1을 나타내었고 동부지역에서는 1.96 cmol+・kg-1을 나타냈다. 칼슘 역시 칼륨과 비슷한 경향을 보였다. 서부지역에서의 함량은 13.14cmol+・kg-1을 나타내었고 동부지역은 32.83cmol+・kg-1으로 서부지역보다 2.5배 높았다. 마그네슘 함량을 비교한 결과, 서부지역에서는 2.65cmol+・kg-1을 나타내었고 동부지역은 1.91cmol+・kg-1을 나타내었다. 서부지역의 나트륨 함량은 0.06cmol+・kg-1을 나타내었고 동부지역은 0.16cmol+・kg-1으로 서부지역보다 2.7배 높았다. 제주지역에서 발생하는 바람은 대체로 남동풍의 바람이 부는데 이로 인하여 동부지역이 서부지역보다 토양 내 나트륨 함량이 높은 것이 아닌가 생각한다. 또한 해안 근처에 위치한 마늘 재배지역임에도 불구하고 나트륨 함량이 많지 않은 것은 바닷바람에 의한 토양의 나트륨 집적이 적거나 제주 지역의 다우로 인한 용탈이 이루어진 것으로 생각된다. 제주도 내 마늘 재배지역의 미량원소인 철, 망간, 구리 및 아연 함량을 측정하였다. 토양 내 미량원소의 함량은 망간 > 철 > 아연 > 구리 순으로 나타났으며 서부지역이 동부지역보다 미량원소 함량이 높게 나타났다. 남도 마늘이 재배되었던 서부지역에서는 12.00ppm, 동부지역에서는 1.01ppm을 나타내었다. 서부지역의 망간 함량은 44.21ppm이었고 동부지역은 2.46ppm으로 서부지역이 동부지역보다 18배나 높게 나타났다. 서부지역의 구리 함량은 1.44ppm이었고 동부지역 망간 함량은 0.12ppm이었다. 서부지역 아연 함량은 11.61ppm을 나타냈으나 동부지역에서는 검출이 되지 않았다.
산, 고형물함량 및 pH 측정
제주도 동부와 서부지역에서 생산된 남도 마늘의 산, 고형물함량 및 pH의 결과를 Table 3으로 정리하였다. 서부에서 재배된 남도 품종은 7.18°Brix를, 동부지역에서 재배된 마늘은 7.53°Brix를 나타내었다. 서부에서 자란 마늘의 산도는 0.42%를 나타내었고 동부지역에서는 0.48%를 나타내었다. 마늘 착즙액의 pH는 비슷하였다. 서부에서 자란 남도 품종의 pH는 5.97을 나타내었고 동부지역에서 자란 품종은 5.94를 나타냈다.
무기성분 분석
무기물은 총 10종을 분석하였으며 총량을 기준으로 서부지역의 마늘에서는 26,451ppm, 동부지역에서는 29,188ppm을 함유하고 있었다(Table 4). 무기물 성분 중 칼륨이 전체의 48%(13,413ppm)를 차지하였으며 다음으로 황이 29% (8,150ppm), 인이 18%(4,933ppm)를 차지하였다. 칼륨이나 황, 인과 유사하게 칼슘 성분 역시 동부지역이(400ppm) 서부지역보다(350ppm) 높게 분포하였다. 마그네슘과 나트륨 역시 비슷한 경향을 보였다. Shin 등(2004)과 Jeong 등(2009) 등도 국내 산지별 마늘의 무기물 함량을 분석한 결과 칼륨과 인 성분이 가장 많이 함유되어 있다고 보고하였으며 이는 본 연구결과와 일치하였다. 미량원소의 함량을 측정하였다(Table 4). 다량원소의 경우 서부지역보다 동부지역에서의 함량이 높게 나타났으나 미량원소는 반대로 동부지역보다 서부지역에서 함량이 높았다. 미량원소 중 철(49.1ppm) 함량이 가장 많았으며 다음으로 아연(19.9ppm), 망간(5.5ppm), 구리(2.9ppm) 순이었다. 남도 품종을 화산회토양에서 재배하였을 경우 서부지역 철 함량은 71.60ppm이었고, 동부지역은 26.60ppm이었다. 아연과 망간 역시 철과 비슷하게 서부지역에서 함량이 높았다. 이와 같이 철이나 망간의 함량이 동부지역에서 낮은 것은 높은 토양 pH로 인하여 이들 성분의 용해도가 낮아져서 마늘로의 흡수가 저해된 것이 아닌가 생각을 한다(Lee 등, 2008).
마늘을 재배하였던 토양의 무기물 분석과 생산된 마늘의 무기물 분석결과 토양 내 무기물 함량이 높을수록 재배된 마늘에서의 무기물 함량도 높게 나타났다. 비료의 성분들은 토양에 존재할 때, 각 성분간의 관계에 따라 식물체로의 흡수를 서로 도와주거나 방해하기도 한다. 인 성분의 경우 칼륨(r = 0.794, p < 0.01)과 마그네슘(r = 0.916, p < 0.001)과의 상승작용에 의한 양의 상관관계를 보였으며 칼슘 역시 나트륨(r = 0.960, p < 0.001)과 양의 상관관계를 보였다. 한편, 미량원소의 경우 서로 길항작용을 보였다. 철의 경우 칼륨(r = -0.722, p < 0.05)과, 망간의 경우 인(r = -0.776, p < 0.05), 철, 마그네슘 및 나트륨과, 아연의 경우 칼륨 및 황(r = -0.807, p < 0.01)과, 구리의 경우 황 및 철(r = -0.728, p < 0.05)과 음의 상관관계를 보였다(Table 8).
알리신, 알리인 및 총 피루베이트산 함량 분석
마늘의 황 함유 화합물의 함량을 조사하였다(Table 5). 화산회토양에서 남도품종을 재배하였을 경우, 서부지역의 알리인 함량은 10.05mg・g-1이었고, 동부지역은 7.48mg・g-1으로 서부지역에서 재배하였을 때 높게 나타냈다. 알리신 함량은 동부지역에서 재배한 마늘에서 높게 나타났다. 서부지역 토양에서 재배하였을 경우 2.18mg・g-1을 나타내었고 동부지역에서는 2.71mg・g-1을 나타내었다. Hyun 등(2008)은 제주 대정지역 마늘의 알리신 함량을 측정하였는데 303-357 mg・100g-1의 범위라고 보고하였으며 본 연구의 결과값이 낮은 것은 마늘품종이 다르거나 재배환경의 차이에 의한 것으로 생각된다. 총 피루베이트산의 함량은 알리신과 비슷한 경향을 보였다. 서부지역 토양에서는 90.26µM・g-1, 동부지역에서는 127.52µM・g-1으로 동부지역에서 마늘을 재배하였을 때 총 피루베이트산 함량이 높았다. 마늘체내의 무기물과 알리신, 알리인과의 상관관계를 분석한 결과 알리인은 망간(r = 0.800, p < 0.01)과, 알리인은 구리(r = 0.820, p < 0.01)와 양의 상관관계를 보였다(Table 8).
총 페놀, 플라보노이드, 환원당 및 α-glucosidase 저해활성 측정
화산회토양에서 재배된 남도마늘의 총 페놀, 플라보노이드, 환원당의 함량 및 α-glucosidase 저해활성을 측정하였다(Table 6). 화산회토양에서 남도 마늘을 재배시 서부지역에서의 총 페놀 함량은 91.68mg GAE/100g을 나타냈고 동부지역에서는 86.01mg GAE/100g을 나타내어 서부지역의 마늘에서 함량이 높게 나타났다. 특히, W1(119.08 ± 4.01mg GAE/100g)의 마늘에서 높게 나타냈다. 총 플라보노이드 함량은 총 페놀함량과 다르게 나타났는데, 서부지역 마늘에서 19.69mg QE/100g을, 동부지역에서 30.00mg QE/100g의 함량을 보였다. 환원당 역시 서부지역보다(23.78mg GE/g) 동부지역(25.04mg GE/g) 마늘에서 높은 함량을 보였다. 총 페놀 및 플라보노이드와 마늘 무기물과의 상관관계에서는 페놀의 경우 아연(r = 0.915, p < 0.001) 및 구리와, 플라보노이드의 경우 인, 칼슘(r = 0.784, p < 0.05), 나트륨 및 구리와 양의 상관관계를 보였다(Table 8).
체내로 흡수된 탄수화물은 α-amylase에 의해 이당류로 분해가 된 후 α-glucosidase에 의해 단당류로 분해되어 혈관 내로 흡수된다(van de Laar et al., 2005). 이렇게 흡수된 단당류는 식후 혈당농도를 상승시키게 된다. 마늘 추출물이 식사 후 혈당이 상승하는 것을 제어할 수 있는지를 알아보기 위하여 α-glucosidase의 저해활성을 측정하였다(Table 6). 서부지역 남도마늘의 α-glucosidase 저해활성은 IC50 = 15.01µL를 나타냈고 동부지역은 IC50 = 11.86µL를 나타내어 동부지역의 마늘이 서부지역보다 α-glucosidase 저해활성이 우수함을 나타내었다. 특히 E1(IC50 = 8.79 ± 0.01µL) 샘플에서 α-glucosidase 저해활성이 가장 좋게 나타났다. α-Glucosidase 저해활성과 마늘 성분간의 상관관계를 분석한 결과, 인(r = -0.918, p < 0.001), 칼륨, 칼슘, 마그네슘, 나트륨 및 총플라보노이드 함량과 음의 상관관계를 보여 이들 성분들이 마늘에 많이 함유될수록 α-glucosidase 저해활성이 높아짐을 알 수 있었다(Table 8).
항균활성 측정
마늘 착즙액의 항균활성은 그람음성균 3종과 그람양성균 4종을 이용하여 측정하였다(Table 7). 남도 마늘의 그람음성균 3종에 대한 항균활성은 병원성 대장균인 Escherichia coli에 대하여 0.63-1.25%(v/v)의 농도에서 저해를 하였으며 Klebsiella pneumonia에 대해서는 1.25-2.50%(v/v), Salmonella enterica subsp. enterica에 대해서는 0.63-1.25%(v/v)의 농도에서 저해활성을 나타냈다. 4종의 그람양성균에 대해서는 Staphylococcus epidermidis에 대하여 0.63-2.50%(v/v), Micro-coccus luteus에 대해서는 0.31-1.25%(v/v), Kocuria rhizophila에 대해서는 0.63-1.25%(v/v), Bacillus subtilis subsp. spizizenii에 대해서는 0.63%(v/v)의 농도에서 생육저해를 나타냈다. 서부지역의 마늘 착즙액은 동부지역보다 그람양성균인 Micrococcus luteus에 대한 높은 생육 저해 활성을 보였으며, 동부지역 마늘은 Klebsiella pneumonia와 Kocuria rhizophila에 대하여 서부지역 마늘보다 우수한 억제활성을 보였다. 마늘에 0.3-0.4% 존재하는 알리신은 항균활성이 있다고 보고되어 있는데(Yamada and Azuma, 1997), 그람 음성균 및 양성균에 모두 생육 저해 활성을 보이는 것은 세포벽의 두께와 상관없이 영향을 주는 것으로 보여지며, 지역별로 강한 항균활성을 지니는 대상 균주가 상이함을 보이는 이유는 재배 지역의 자연 환경이 다르기 때문이라 사료된다.