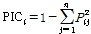서 언
재료 및 방법
공시품종 및 DNA 추출
Microsatellite 분석
결과 및 고찰
Microsatellite 분석
품종식별력 검정 및 유전적 유사도 분석
서 언
재배종 딸기(Fragaria × ananasa Duch)는 장미과에 속하는 초본성 다년생 식물로서 8배체(2n = 8x = 56)로 알려져 있다. 우리나라 딸기의 재배면적은 2012년 현재 6,435ha(시설, 6,290ha; 노지, 145ha)이고 생산량 192톤(시설, 189톤; 노지, 3톤)에 이르며 토마토와 더불어 매년 10% 내외의 생산량이 증대될 정도로 우리나라 농업에서 차지하는 비중이 큰 원예작물의 하나이다(http://www.mafra.go.kr). 딸기는 영양번식 작물이기 때문에 국내 민간 종자회사에서 품종을 육성하는 예는 거의 없는 실정이며 주로 국가기관이나 지방자치단체, 개인육종가에 의해 다수의 신품종이 육성되어 2014년 5월 현재 품종보호출원 및 등록된 50품종과 생산 수입판매 신고된 130품종이 국내 종자시장에서 유통되고 있다(http://www.seed.go.kr). 우리나라에 재배되고 있는 딸기는 2000년대 초반만 하더라도 일본 품종인 ‘Akihime’와 ‘Redpearl’이 전체 재배면적의 90% 정도를 점유하였으나 신품종에 대한 지식재산권의 중요성이 날로 증대되면서 국내에서도 이를 대체할 수 있는 품종개발에 박차를 가하여 온 결과 2013년 현재 우리나라에서 육성된 ‘Seolhyang(설향)’, ‘Maehyang(매향)’, ‘Manhyang(만향)’ 품종이 국내 딸기 재배면적의 78%를 점유할 정도로 큰 연구성과를 거두고 있다(http://www.krei.re.kr). 딸기의 품종 육성은 교잡육종법에 의하여 실생묘를 얻고 이를 영양번식에 의해 우수한 형질을 가진 개체를 선발하여 영양번식에 의해 증식하는 방법을 주로 이용한다. 따라서 형태적 특성에 의한 품종의 확인과 유전자원의 특성평가 방법은 단순하지 않기 때문에 일본, 영국, 미국 등의 국가에서는 주로 DNA 검정 방법을 활용하고 있다. 일본의 경우 자국에서 육성된 딸기의 품종을 보호하기 위하여 25개의 cleavage amplified polymorphic sequence(CAPs) 마커를 활용하여 117품종을 식별하는 체계를 구축하였으나(Kunihisa et al., 2005), 이 분석 방법은 간편하지 않고 데이터베이스 구축에 어려움이 있어 최근에는 75개의 딸기 유전자원 및 품종을 대상으로 4개의 microsatellite 마커를 이용한 품종식별 체계 구축을 발표한 바 있다(Honjo et al., 2011). 영국에서도 딸기 60개 품종을 microsatellite 마커에 의해 분석한 결과를 보고한 바 있으며(Govan et al., 2008), 최근 미국에서는 219개의 딸기 유전자원 및 품종을 대상으로 8개의 microsatellite 마커를 활용하여 분석한 결과를 보고한 바 있다(Chambers et al., 2013). 우리나라의 경우는 amplified fragment length polymorphism(AFLP) 및 microsatellite 마커를 이용한 50개의 딸기 유전자원 및 품종의 유전적 다양성 분석(Cho et al., 2007), CAPS 마커를 이용한 국내 및 일본에서 육성된 19품종의 판별 체계 구축에 대한 연구결과가 보고되고 있다(Cho et al., 2008). 그러나 일본, 미국, 영국 및 국내에서 수행한 연구결과를 종합해 볼 때 자국에서 육성된 품종 및 유전자원을 중심으로 품종식별 체계를 구축하였기 때문에 이 결과를 활용하여 정밀도 높은 DNA profile 데이터베이스 구축에 직접 활용하기에는 어느 정도 한계가 있는 것으로 판단되었다. 따라서 국내에서 최근에 육성된 품종과 일본, 미국 등의 국가에서 재배되고 있는 품종을 추가하여 우리나라 고유의 딸기 품종별 microsatellite profile 데이터베이스 구축이 필요할 것으로 사료되었다. 이러한 연구 결과는 품종보호 출원품종 재배심사의 정밀도 제고, 우리나라 농업 생산물의 보호 및 지식재산권이 확보된 딸기 묘의 무단 증식 방지 등과 같은 다양한 방면에 활용도가 높을 것으로 판단된다.
따라서 본 연구에서는 microsatellite 마커를 활용하여 딸기 100 품종에 대한 품종식별용 마커의 선정 및 이를 활용한 DNA profile 데이터베이스 구축에 대한 일련의 연구를 수행하여 얻어진 결과를 보고하는 바이다.
재료 및 방법
공시품종 및 DNA 추출
본 연구에서는 국립종자원 서부지원과 농촌진흥청 국립원예특작과학원 및 경상북도농업기술원 성주과채류시험장에서 수집하여 보존되고 있는 딸기 100 품종을 공시하여 microsatellite 마커를 이용한 품종별 데이터베이스 구축에 활용하였다(Table 1). 공시 품종의 엽조직을 액체질소를 이용하여 마쇄한 다음 NucleoSpin®PlantII(Macherey-Nagel Cat. 740 770.250, Germany) 키트를 이용하여 게놈 DNA를 분리하였다. 추출된 DNA는 1.5% 아가로스젤에서 전기 영동하여 DNA 농도를 확인한 후 μL당 10ng의 농도로 정량하여 PCR 분석에 이용하였다.
Microsatellite 분석
딸기 품종식별에 효과적인 microsatellite 마커를 선발하기 위하여, ‘Kurume 52’, ‘Seolhyang(설향)’, ‘Maehyang(매향)’, ‘Akihime’, ‘Redpearl’, ‘Jumbo’, ‘Chodong’, ‘Donner’, ‘Sukyoung(수경)’, ‘Santa(싼타)’, ‘Daeun(대운)’, ‘Albion’, ‘Black Monte’, ‘Flether’, ‘Eyehime’, ‘Solar’, ‘Ca51 Sr-1’, ‘Jaspan’, ‘Lihn’, ‘Marshall’, ‘Everberry’ 품종과 국제장미과 게놈프로젝트(http://www.rosaceae.org)에서 제시된 microsatellite 프라이머의 염색체상 위치와 반복 염기서열 정도 등을 고려하여 최종 274개를 선정하고 이들 프라이머와 21품종의 다형성 정도를 조사하였다. PCR 반응을 통한 증폭 산물은 6% 아크릴아마이드 젤에 2시간 전기영동한 다음 silver sequenceTM staining reagents(Promega, USA)로 염색하여 polymorphism 여부를 확인하였다. 그리고 microsatellite primer 선발과정에서 다형성을 보이면서 대립유전자의 수가 많은 45개를 1차 선발하여 프라이머의 정방향에 FAM, VIC, NED, PET (Applied Biosystems, USA)으로 형광 표지한 다음 딸기 100 품종(Table 1)에 대한 DNA profile 데이터베이스 구축에 이용하였다.
PCR 반응은 딸기 게놈 DNA 30ng, 0.1μM의 SSR primer, 2.0μL dNTP mixture(2.5mM), Taq polymerase 1.0U, 2.5μL의 10 × PCR buffer(50mM KCl, 20mM Tris-HCl, pH 8.0, 2.0mM MgCl2)에 증류수를 첨가하여 전체 부피를 25μL로 조절하였다. PCR(C1000, BioRad, USA) 증폭은 94°C에서 30초간 denature 한 후, 55°C에서 30초 annealing, 72°C에서 45초간 extension을 40cycle 수행하였다. PCR이 완료된 후 3.0μL의 증폭산물을 2.5% 아가로스 젤에서 전기 영동하여 증
Table 1. Strawberry cultivars used for genetic characterization using microsatellite markers. |
No. | Cultivar name | Parentage | Origin | Reference |
1 | Nonsan 1 | Tochinomine × Toyonoka | Korea | http://www.seed.go.kr |
2 | Daehak 1 | Unpublished | Korea | http://www.seed.go.kr |
3 | Danmi | Maehyang × Amaou | Korea | http://www.seed.go.kr |
4 | Seonhong | Johong × Maehyang | Korea | http://www.seed.go.kr |
5 | Suhong | Hokowase × Harunoka | Korea | http://www.seed.go.kr |
6 | Shinyeobong | Tissue culture | Korea | http://www.seed.go.kr |
7 | Sancheonwang | Hikarigobuyaka × Maehyang | Korea | http://www.seed.go.kr |
8 | Sinmyeong | Maehyang × Geumhyang | Korea | http://www.seed.go.kr |
9 | Sindaebong | Geumhyang × Seolhyang | Korea | http://www.seed.go.kr |
10 | Sinseolmae | Seolhyang × Maehyang | Korea | http://www.seed.go.kr |
11 | Okhyang | Johong × Akihime | Korea | http://www.seed.go.kr |
12 | Santa | Maehyang × Seolhyang | Korea | http://www.seed.go.kr |
13 | Hanun | Seolhyang × Maehyang | Korea | http://www.seed.go.kr |
14 | Daeun | Akihime × Redpearl | Korea | http://www.seed.go.kr |
15 | Manhyang | Nyoho × Akanekko | Korea | http://www.seed.go.kr |
16 | Keumhyang | Akihime × Tochiotome | Korea | http://www.seed.go.kr |
17 | Seolhyang | Akihime × Redpearl | Korea | http://www.seed.go.kr |
18 | Maehyang | Tochinomine × Akihime | Korea | http://www.seed.go.kr |
19 | Jukhyang | Redpearl × Maehyang | Korea | http://www.seed.go.kr |
20 | Damhyang | Akihime × Maehyang | Korea | http://www.seed.go.kr |
21 | Sukyoung | Johong × Maehyang | Korea | http://www.seed.go.kr |
22 | Chodong | Harunoka × Yachiyo | Korea | http://www.seed.go.kr |
23 | Johong | Nyoho × Akihime | Korea | http://www.seed.go.kr |
24 | Daewang | Maehyang × Wongyo 3111 | Korea | http://www.seed.go.kr |
25 | Josaenghongsim | Benizuru × Usosio | Korea | http://www.seed.go.kr |
26 | Eyeberry Busan | Unpublished | Korea | - |
27 | Sagyeojeol | Unpublished | Japan | - |
28 | Kunowase | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
29 | Kurume 49 | Toyonoka × Nyoho | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
30 | Derunoka | Unpublished | Japan | - |
31 | Tochinomine | Kei511 × Nyoho | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
32 | Rowang | Unpublished | Japan | - |
33 | Beni hoppe | Akihime × Sachinoka | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
34 | Morioka 16 | (Fairfax × Ettersburg) × Chiyoda | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
Table 1. Continued. |
No. | Cultivar name | Parentage | Origin | Reference |
35 | Morioka 17 | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
36 | Akanekko | [(Aiberry × Hokowase) × Toyonoka] × (Aiberry × Hokowase) | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
37 | Amaou | Fukuoka S6 | Japan | http://www.scielo.cl/fbpe/img/ejb/v15n2/a06/t1.html |
38 | Asuka Ruby | Asuka Wave × Nyoho | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
39 | Asuka Wave | [Uzushio × {(Kurume Sokusei-3 × Hokowase) × (Donner × Hokowase)}] × [(Kurume Sokusei-3 × Hokowase) × {Donner × (Kobe-1 × Hokowase)}] | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
40 | Reiko | Harunoka-s × Fukuba-s | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
41 | Himesodachi | Unpublished | Japan | - |
42 | Chizuru | [(Donner-s)-s × (Harunoka-s)-s]-s × Harunoka-s | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
43 | Benizuru | (Miyazaki × The Sun) × Fukuba | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
44 | Takane | Unpublished | Japan | - |
45 | Kurume 103 | (Miyazaki × The Sun) × Fukuba | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
46 | Syuko | Shizutakara × Haruyoi | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
47 | Kofuku | Unpublished | Japan | - |
48 | Everberry | Oishishikinari2 × Haruyoi | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
49 | Harunoka | Kurume103 × Donner | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
50 | Nagoya-oomi | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
51 | Okitsu | Unpublished | Japan | - |
52 | Akihime | Kunowase × Nyoho | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
53 | Nyoho | Kei210 × Reiko | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
54 | Redpearl | Aiberry × Toyonoka | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
55 | Sachinoka | Toyonoka × Aiberry | Japan | http://www.tulips.tsukuba.ac.jp/limedio/dlam/B28/B2869562/1.pdf |
56 | Fujisaki 068 | Dorsett × Ettersburg | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
57 | Tonami | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
58 | Tonami-zairai- shikinari | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
59 | Touhoku 13 | Selection of F. × ananassa | Japan | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
60 | Jumbo | Unpublished | Japan | - |
61 | Chunseong | Unpublished | China | - |
62 | Chuncho | Unpublished | China | - |
63 | Taiwan Farmer | Unpublished | Taiwan | - |
64 | Albion | Diamante × Cal94.16-1 | USA | http://strawberryplants.org/2010/05/strawberry-varieties/ |
65 | Blakemore | Missionary × Howard 17 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
66 | Ca51 Sr-1 | Lassen × self | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
Table 1. Continued. |
No. | Cultivar name | Parentage | Origin | Reference |
67 | Jaspan | Unpublished | USA | - |
68 | Sweet Charlie | FL80-456 × Pajaro | USA | http://strawberryplants.org/2010/05/strawberry-varieties/ |
69 | Summerberry | Titan × MDUS2856 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
70 | Columbia | WA157 × WA175 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
71 | Donner | CAL222 × CAL145.52 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
72 | Marshall | Unpublished | USA | - |
73 | Carmine | Losa linda × FL93-53 | USA | http://hortsci.ashspublications.org/content/39/6/1496.full.pdf |
74 | Cruz | Cal. 37.20-45 × Sequoia | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
75 | Darrow | MdUS2713 × MdUS2787 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
76 | Douglas | Tufts × 64.57-108 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
77 | Earlidawn | Midland × Tennessee Shipper | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
78 | Earliglow | MDUS 2359 (Fairland × Midland) × MDUS2713 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
79 | EarliMiss | Albritton × Tennessee Shipper | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
80 | MDUS 3839 | Earlidawn × MDUS2713 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
81 | Midland | Howard17 × Redheart | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
82 | Pelican | 82-1556 P × Louisiana | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
83 | Prelude | Titan × NC 2967 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
84 | Red Cross | Ettersburg No. 216 × Trebla | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
85 | Solana | CAL177-19 × CAL 103-22 | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
86 | Sunrise | USMD4152 × Stelemaster | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
87 | Titan | NC1767 × Albritton | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
88 | Toro | Unpublished | USA | - |
89 | To-wan | Unpublished | USA | - |
90 | Vesper | Sparkle × Valentine | USA | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
91 | Eastern Pine | Cultivar grown since the late 1700s, original species from United States but grown in Europe since then. | UK | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
92 | Amelia | Includes Pandora, Marmolada, Kent, and Providence | UK | http://strawberryplants.org/2010/05/strawberry-varieties/ |
93 | Flamenco | Evita × EMR77 | UK | http://strawberryplants.org/2010/05/strawberry-varieties/ |
94 | Jucunda | Selection of cultivated strawberry from England | UK | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
95 | Bolero | Selva × LA988 | UK | http://strawberryplants.org/2010/05/strawberry-varieties/ |
96 | Pink Panda (Frel) | Fragaria × Comarum hybrid involving Fragaria chiloensis | UK | http://strawberryplants.org/2010/05/strawberry-varieties/ |
97 | Blomidon | K72-4 × [Micmac × (Guardsman × Tioga)] | Canada | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
98 | Cornwallis | Earliglow × Kent | Canada | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
99 | Rabunda | Redgauntlet × Repita | Netherlands | http://www.bordeaux.inra.fr/eustrawberrydb/accession/206 |
100 | Tango | Rapella × Selva | Netherlands | http://www.ars.usda.gov/SP2UserFiles/Place/53581500/catalogs/fracult.html |
폭 여부를 확인한 다음, 초순수 150μL에 PCR 산물 1.5μL를 희석하였다. 희석된 PCR 증폭 산물 1.5μL는 탈이온된 포름아마이드(deionized formamide) 10μL, size marker(LIZ500 size standard) 0.25μL를 혼합한 다음 94°C에서 2분간 변성시켰다. 변성시킨 PCR 증폭 산물은 자동염기서열분석기(Genetic Analyzer 3130XL, Applied Biosystems, USA)를 활용하여 전기 영동한 다음 GeneMapper(version 3.7) 컴퓨터 프로그램(Applied Biosystems, USA)을 이용하여 마커별 대립 유전자의 크기를 결정하였다.
Microsatellite 마커의 다형성 정도를 조사하기 위하여 아래의 공식을 이용하여 polymorphism information content(PIC) 값을 산출하였다. 아래 식에서 n은 마커당 분석되어지는 대립유전자의 수, Pij는 마커 i의 밴드들 중에서 j번째 공통 밴드 패턴의 빈도수이다(Anderson et al., 1993).
|
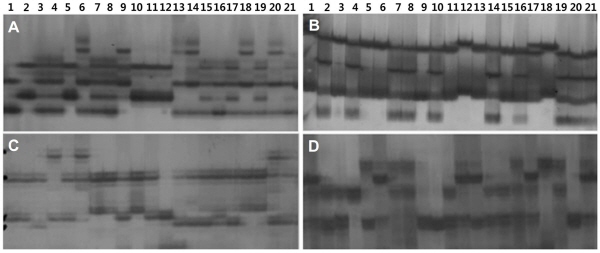
Fig. 1. Polymorphism of four microsatellite markers, EMFvi179 (A), EMFvi109 (B), FAC-013 (C) and EMFv021 (D). The PCR products were separated on 6% polyacrylamide gel. Lane 1, ‘Kurme 49’; 2, ‘Seolhyang’; 3, ‘Reiko’; 4, ‘Redpearl’; 5, ‘Akihime’; 6, ‘Jumbo’; 7, ‘Chodong’; 8, ‘Donner’; 9, ‘Sukyoung’; 10, ‘Santa’; 11, ‘Daeun’; 12, ‘Albion’; 13, ‘Blakemore’; 14, ‘Flether’; 15, ‘Eyehime’; 16, ‘Solar’; 17, ‘Ca51Sr-1’; 18, ‘Jaspan’; 19, ‘Lihn’; 20, ‘Marshall’; 21, ‘Everberry’. |
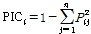
Microsatellite 분석을 통하여 재현성이 높고 다형성을 보이는 대립유전자를 마커로 선발하여 대립유전자의 유무(dominant marker scoring; present = 1, absent = 0)에 따라 NTSYSpc(version 2.10b)(Rohlf, 2000) 컴퓨터 프로그램에 입력하고 Jaccard 방법에 준하여 유전적 유사도 값을 계산한 다음 unweighted pair-group method with arithmetical average (UPGMA) (Sneath and Sokal, 1973) 방법으로 집괴 분석하고 계통도를 작성하여 microsatellite 마커의 품종 식별력을 비교 분석하였다.
결과 및 고찰
Microsatellite 분석
딸기 품종식별에 효과적인 microsatellite 마커를 선정하기 위하여, ‘Seolhyang(설향)’외 20품종을 활용하여 국제 장미작물 게놈프로젝트에서 염기서열 정보가 공개되어 있는 microsatellite primer 274개와 다형성 정도를 6% 아크릴아마이드 젤 전기영동에 의해 조사한 바(Fig. 1), 총 274개 중에서 229개는 대립유전자의 다형성을 보이지 않거나 특정 품종에서만 다형성을 보이는 양상을 보였고, 다형성을 나타내더라도 대립유전자의 양상이 복잡하였다. 그러나 나머지 45개는 대립유전자의 수가 많을 뿐만 아니라 밴드의 패턴이 양호한 것으로 나타났다. 따라서 45개의 microsatellite 정방향 프라이머의 5’-말단에 형광물질인 FAM, VIC, NED, PET를 각각 표지하여 딸기 100품종의 genomic DNA와 PCR하고 증폭산물을 자동염기서열분석기를 이용하여 전기영동 한 바, 45개 중 25개는 GeneMapper 컴퓨터 프로그램에서 검출되어진 피크가 깨끗하여 품종별 fingerprinting에 용이하였으나 나머지 20개는 아크릴아마이드 젤 분석에서 검출되지 않았던 대립 유전자가 검출되어 fingerprinting 하기에 적합하지 않은 것으로 나타나 이를 제외시켰다.
딸기 품종식별용 마커의 선발과정에서 최종 선정된 25개의 microsatellite 프라이머와 딸기 100품종에 대한 다형성 정도를 조사한 바(Table 2), microsatellite 프라이머에 따른 검출된 대립유전자의 개수는 3-13개로 다양하게 나타났으며 총 195개의 대립유전자가 검출되었고, 마커당 평균 대립유전자의 개수는 7.50개로 나타났다. 한편 각 마커별 공시 품종의 유전적 다형성 정도를 나타내는 지수인 PIC 값은 0.333-0.841까지 다양한 범위에서 분포하였으며, 평균값도 0.706으로 높은 경향을 보였다. 그리고 25개의 microsatellite 프라이머 가운데 17개가 0.70 이상의 높은 PIC 값을 나타내어 본 연구에서 선발된 microsatellite 마커는 딸기 품종의 식별에 충분히 활용될 수 있을 것으로 나타났다.
Table 2. Repeat motif, no. of alleles, and PIC value of microsatellite markers selected for genetic characterization of strawberry. |
Microsatellite designation | Primer sequence | Repeat motif | Annealing temp | Product size (bp) | No. of alleles | PIC value |
ARSFL_092 | F: VIC-TCCGGTGACGAATCTAAAGG R: GAAGAACAAGCACCACCACA | (CT)8(GA)13-1 | 55 | 170-188 | 8 | 0.759 |
ARSFL_099 | F: FAM-GATTAGGGAGAGGCAACGTG R: GCTTCAAGCAAAATGCATCA | (AC)13 | 55 | 163-183 | 7 | 0.668 |
ARSFL_100 | F: PET-TGATGTATTGCATTTCGTGCT R: CTATCTCCCGGTGCTTTGAC | (AT)7 | 55 | 242-264 | 5 | 0.553 |
ARSFL_101 | F: NED-CAGCTAAAACCCTGCTCTCG R: GTGACGATAGGCCGTGAAAC | (AGG)6 | 55 | 164-219 | 7 | 0.740 |
CFVCT016 | F: VIC-CACAACGGAGTACACGGCTA R: TCAGATTCACCTCGGACCTC | - | 55 | 120-134 | 7 | 0.622 |
EMFn160 | F: VIC-GCATCCTTGGGAAATTAATGC R: TTGGGAAGGATCATAAAAACC | (CT)24 | 55 | 135-195 | 13 | 0.764 |
EMFn185 | F: NED-GTAACGACGGCTGCTTCTCC R: CGCTCGCTCTTATAAACTTCC | (GA)11 | 55 | 196-215 | 6 | 0.752 |
EMFv013 | F: PET-CGGTGCGGCGGTGCAACTC R: GGTTTGATGGCCCTTTGCTGGATG | Perfect trinucleotide | 55 | 206-218 | 4 | 0.711 |
EMFv016 | F: NED-AGCGCTTTAAACAACTTTCACAC R: ATTTAGCCACACGACCATTTTC | Imperfect dinucleotide | 55 | 211-256 | 9 | 0.790 |
EMFv021 | F: FAM-TCATTTTTCAGGGCCACGGGTAGA R: GTGGTGGTTGAGGCAGTGGAGGAT | Perfect dinucleotide | 55 | 191-221 | 9 | 0.759 |
EMFvi025 | F: FAM-TTGTGATCTCGTAGAAGGAGCA R: GGGTTCCGTGAAACTAAACTTG | (TG)8 | 55 | 244-256 | 8 | 0.631 |
EMFvi108 | F: PET-GGACCCCAAAACATTGAATAAA R: GAAGAGGGGAGGAGCAATAAAT | (AG)29 | 55 | 172-198 | 8 | 0.741 |
EMFvi109 | F: VIC-CTGCAACTTGTTTCCCGTTATT R: AATTGCAGCAGTAGCAGCAG | (TC)4/(TC)7 | 55 | 251-275 | 7 | 0.801 |
EMFvi146 | F: NED-ACGAAAAACAGCATACACATCG R: TACCGCCCCTTAAGTTTGAGTA | (AC)8 | 55 | 191-198 | 4 | 0.651 |
EMFvi179 | F: FAM-GGGAATCAAATCTGAAATGAGC R: GGATCCAATTTAAATGCTGGTT | (AG)36 | 55 | 133-155 | 7 | 0.721 |
FAC-003a | F: PET-AAGCTAATTCTCAGGCCACAAG R: TTCATTGCCAGTTTGAATTACG | (TA)7 | 55 | 167-210 | 3 | 0.333 |
FAC-003b | F: VIC-TCGACCTCACTCTAAGCATCAA R: AGATAAGCTTCTTGTGGCCTGA | (GAA)5 | 55 | 301-327 | 10 | 0.779 |
FAC-013 | F: VIC-TGTTTGAAAAGTGCTGGAC R: GATATCAATATCAATACTAGATAACAG | (AAG)10 | 55 | 178-219 | 6 | 0.775 |
UDF017 | F: VIC-GGACGTTCCACATCCGTAGA R: CGGTGGAGATGTGATTTTATGA | - | 55 | 176-202 | 11 | 0.789 |
UFFa02H04 | F: FAM-ATCAGTCATCCTGCTAGGCACT R: TACTCTGGAACACGCAAGAGAA | (TCG)6 | 55 | 197-213 | 6 | 0.750 |
UFFa11G07 | F: VIC-TCTCTGTGTCTTCTCCGAAACT R: CTACTGCTCCAACTTCAAATCG | (AT)8 | 55 | 164-178 | 7 | 0.698 |
UFFa11A11 | F: NED-ACGAGGCTCCAATAGAGTTCTG R: CTGAGCAGAAGCCATAGTATCAC | (TC)11 | 55 | 220-278 | 11 | 0.841 |
UFFa13C07 | F: PET-GGAGTCAACAGTAGTGCAGGTAA R: GGTTTTCTTGCAGTTGGAGTAG | (CAG)6 | 55 | 163-184 | 5 | 0.621 |
UFFa18H04 | F: FAM-CCTTCGTTACTCTAGTAGCTCCA R: GTGATGAAGACGATGATGAGGT | (CT)14 | 55 | 133-168 | 11 | 0.726 |
UFFa20H10 | F: FAM-GATGTGCTAGGACTCATACTTGG R: TAAAAGACGAGGCCATCTGA | (AT)7 | 55 | 211-236 | 9 | 0.709 |
Total | | | | | 195 | 18.347 |
Mean | | | | | 7.50 | 0.706 |
Microsatellite 마커를 활용한 딸기 품종별 fingerprinting 및 유전자원의 다양성 평가를 하였을 때 각 마커의 평균 대립유전자 개수는 Govan et al.(2008)은 영국과 미국 등에서 육성된 60품종을 8개의 microsatellite 마커로 분석 시 대립유전자의 개수가 24-64개까지 분포함을 밝혔으며, Honjo et al.(2011)도 일본 등에서 육성된 75품종을 대상으로 4개의 microsatellite 마커로 검정하였을 때 마커당 대립유전자의 개수가 20-34개로 높게 나타남을 보고하였다. 그러나 본 연구에서는 대립유전자 개수가 3-13까지 나타나 이들 연구자들과 상이한 결과를 나타내었는데 이러한 이유는 마커의 선발과정에서 복잡한 대립유전자 형태를 나타내는 마커는 실용적 활용 과정에서 문제점을 야기할 수 있기 때문에 이러한 마커를 제외하고 피크의 패턴이 단순하면서 반복 재현성이 높은 마커를 fingerprinting에 활용했기 때문에 나타난 결과라고 사료된다. 한편, 본 연구에서는 Yoon et al. (2012)이 우리나라, 독일, 미국, 영국 및 일본에서 유래된 품종 및 유전자원 59점을 18개의 microsatellite 마커로 분석한 PIC 값(평균 0.454)과 대립유전자의 개수(5.6)보다 높은 경향을 나타내었는데 이는 분석재료의 유전적 다양성이 높거나 품종식별이 높은 마커를 1차 선발했기 때문에 나타난 결과로 판단된다. 본 연구에 최종 선정된 microsatellite 마커 25개는 지금까지 국내외에 연구자들이 품종식별에 활용하지 않았던 새로운 마커 세트로서 국외의 연구자에 의해 개발된 품종식별용 마커에 비해 대립유전자의 수는 작으나 반복 재현성이 높고 자동염기서열 분석기로 분석 시 피크의 패턴이 복잡하지 않기 때문에 향후 품종의 진위 확인과 관련된 다양한 분야에 매우 유용하게 활용될 수 있을 것으로 판단되었다.
품종식별력 검정 및 유전적 유사도 분석
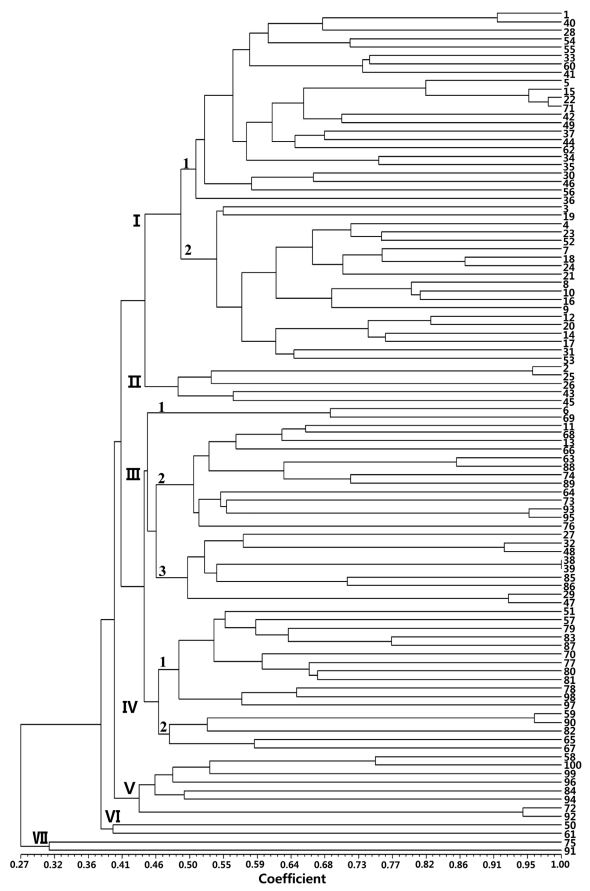
25개의 microsatellite 마커를 이용하여 검출된 대립유전자의 크기를 근거로 딸기 100품종에 대한 유전적 다양성을 조사한 바(Fig. 2), 공시품종의 전체 유사도 지수는 0.27-1.00의 범위에 속하였고, microsatellite 마커의 유전자형에 의해 7개의 대그룹으로 구분됨을 확인할 수 있었다. I 그룹은 우리나라에서 육성된 ‘Seolhyang(설향)’ 등 20품종, 일본에서 육성된 ‘Akihime’ 등 20품종, 중국에서 재배되고 있는 1품종을 포함하여 42품종이 분포하였다. I 그룹은 유전적 유사도 지수 0.40에서 2개의 소그룹으로 다시 구분되었다. I-1 소그룹에 속하는 23품종 중에서 우리나라에서 육성된 품종은 ‘Nonsan 1(논산1)’, ‘Suhong(수홍)’, ‘Manhyang(만향)’, ‘Chodong (초동)’ 4개의 품종뿐이었고 나머지는 일본에서 육성된 ‘Beni hoppe’ 등 17품종과 중국에서 수집된 유전자원인 ‘Chuncho’, 미국 유전자원 중 교배모본으로 널리 활용되고 있는 ‘Donner’ 품종이 속하였다. I-1 그룹에 속하는 품종 중에서 우리나라에서 육성된 ‘Chodong(초동)’ 품종과 미국에서 육성된 ‘Donner’ 품종이 95% 이상의 높은 유사도를 나타내었다. ‘Chodong’ 품종의 경우 일본에서 육성된 ‘Harunoka’와 ‘Yachio’가 교배된 조합에서 선발된 것인데 ‘Harunoka’ 품종의 육성 계보도를 볼 때 ‘Donner’ 품종을 부계로 활용했기 때문에 나타난 결과라고 추정된다. I-2 그룹은 최근에 우리나라에서 육성된 품종인 ‘Seolhyang(설향)’, ‘Maehyang(매향)’, ‘Santa(싼타)’ 등 16품종과 일본에서 육성된 ‘Tochinomine’, ‘Akihime’, ‘Nyoho’ 3품종이 포함되었는데 모든 품종이 마커의 유전자형에 의해 뚜렷하게 구분되는 양상을 나타내었다. 우리나라에서 육성된 대부분의 딸기 품종 대부분이 I-2 그룹에 분포하는 이유는 교배모본으로 활용된 품종이 주로 우리나라에서 육성된 ‘Maehyang(매향)’과 일본에서 육성된 ‘Tochinomine’, ‘Akihime’, ‘Nyoho’를 주로 활용했기 때문에 나타난 결과라고 판단된다. II 그룹은 ‘Daehak 1(대학1)’, ‘Eyeberry Busan(아이베리 부산)’, ‘Josaenghongsim(조생홍심)’, ‘Benizuru’, ‘Kurume103’ 5품종이 그룹화되었으며 1940년대 우리나라에서 선발 육종된 ‘Daehak 1(대학1)’은 ‘Josaenghongsim(조생홍심)’ 품종의 유전적 유사도가 90% 이상 높은 것으로 분석되었고 주로 ‘Benizuru’가 교배모본으로 활용된 품종들이 분포하였다. III 그룹은 유전적 유사도 0.46에서 3개의 소그룹으로 구분할 수 있었으며, III-1은 우리나라에서 조직배양 기법으로 육성된 ‘Shinyeobong(신여봉)’ 품종과 미국에서 육성된 ‘Summerberry’ 품종이 속하였다. III-2는 미국에서 육성된 품종인 ‘Albion’ 등 8품종, 영국에서 육성된 ‘Flamenco’와 ‘Bolero’, 대만에서 육성된 ‘Taiwan Farmer’, 우리나라의 성주과채류 시험장에서 육성된 ‘Okhyang(옥향)’과 ‘Hanun(한운)’ 품종이 분포하였다. ‘Okhyang(옥향)’과 ‘Hanun(한운)’ 품종의 경우 양친으로 활용된 품종이 I-2 그룹에 분포하는 ‘Johong(조홍)’, ‘Seolhyang(설향)’, ‘Maehyang(매향)’, ‘Akihime’ 품종이 활용되었음에도 불구하고 III-2 그룹에 속한 이유는 이들 품종의 선발을 주로 중국의 운남성 원예연구소에서 수행하였는 바, 이 지역에 적합한 계통을 선발하였기 나타난 결과라고 추정되며, 향후 이들 품종에 대해서는 마커의 수와 품종별 시료를 다양화하여 정밀도 높은 분석이 필요할 것으로 사료된다. III-3은 일본 유래의 ‘Kurume 49’ 등 7품종과 미국에서 육성된 ‘Solana’, ‘Sunrise’ 품종이 속하였으며, ‘Asuka Ruby’와 ‘Asuka Wave’는 본 연구에서 활용된 마커에 의해서는 식별이 불가능하였는데 ‘Asuka Ruby’는 ‘Asuka Wave’와 ‘Nyoho’ 품종의 교배조합에서 육성된 품종이기 때문에 나타난 결과라고 판단된다.
|
Fig. 2. A dendrogram depicting the classification of 100 strawberry cultivars constructed using unweighted pair-group method with arithmetical average (UPGMA) based on microsatellite markers. The numbers (1 to 100) at right side refer to the list of cultivars in Table 1. The scale at the bottom is Jaccard’s coefficient of similarity. |
IV 그룹은 유사도 지수 0.47에서 2개의 소그룹으로 나누어졌는데 IV-1은 미국에서 재배되고 있는 ‘Columbia’ 등 8품종, 일본에서 육성된 ‘Okitsu’ 등 2품종과 캐나다에서 개발된 ‘Blomidon’과 ‘Cornwallis’ 2품종이 속하였다. IV-2 그룹은 ‘Blakemore’ 등 5품종이 그룹화되었고 ‘Tohoku 13’과 ‘Vasper’ 품종이 95% 이상의 높은 유전적 유사도를 나타내었다. V 그룹은 ‘Marshall’ 등 8품종이 분포하였으며 미국에서 재배되고 있는 ‘Marshall’과 ‘Amelia’ 품종의 유전적 유사도가 높은 경향을 보였다. VI 그룹은 ‘Nagoya-oomi’와 ‘Chunseong’, VII 그룹은 ‘Darrow’와 ‘Eastern Pine’ 품종이 각각 속하였다. 이상의 결과를 종합해 볼 때 본 연구에 공시된 딸기 100품종에 대하여 25개의 microsatellite 마커를 이용하여 분석할 경우 대부분의 딸기 품종 식별이 가능하였을 뿐만 아니라 품종 육성 계보도와 각 국가별로 재배되고 있는 품종들이 마커의 유전자형에 의해 뚜렷하게 그룹화되는 경향을 보여, 본 연구에서 선정된 마커들은 품종간 유연관계 설정을 통한 유전자원 특성 평가와 품종의 진위성 확인 및 조직배양 기술을 이용한 딸기의 무병묘 증식 시 변이체의 확인 등 다양한 분야에 활용될 수 있을 것으로 판단된다.
마커를 이용한 품종별 데이터베이스 구축은 유럽품종보호사무소에서 국가별 컨소시엄을 구축하여 토마토(Bredemeijer et al., 2002), 밀(Röder et al., 2002), 장미(Esselink et al., 2003), 감자(Reid et al., 2011) 등의 작물에 대하여 연구결과를 발표한 이후 중국에서는 옥수수(Wang et al., 2011), 우리나라에서는 고추(Kwon et al., 2013), 오이(Kwon and Choi, 2013)의 시판품종에 대하여 데이터베이스 구축에 대한 연구결과가 보고되고 있다. 이들 연구결과를 종합해 볼 때 여러 가지 유전자 분석방법 중에서 microsatellite 분석을 주로 활용하고 20-30개 내외의 microsatellite를 활용하여 100품종 이상에 대한 정밀도 높은 데이터베이스를 구축하였다는 점이다. 본 연구에서도 딸기의 품종별 DNA profile 데이터베이스 구축에 microsatellite 마커가 효과적이라는 측면에서 기존의 연구결과를 확인할 수 있었다. 한편, 본 연구에서 구축된 정밀도 높은 딸기 품종별 microsatellite 데이터베이스는 품종보호 출원 시 DNA 검정을 먼저 실시하고 이 데이터베이스에 구축된 품종과 유전적 유사도를 비교하여 근연도가 가까운 품종을 대조품종으로 선정한다면 재배심사의 정밀도 향상에 크게 기여할 수 있을 것이다. 실제로 이러한 방법을 오이, 벼 등과 같은 작물에 활용한 결과 품종의 구별성이 인정되지 않은 경우도 있어 품종보호 등록이 거절된 사례가 3건 이상 있다. 또한 재배시험 과정 중에 출원품종의 구별성, 균일성 및 안정성이 의심될 경우 본 연구에서 선정된 마커로 DNA 검정을 수행하고 검정 시료간 동일성 여부를 확인한다면 심사의 보조자료로 유용하게 이용될 수 있을 것이다. 향후, 본 연구에서 선정된 딸기 품종식별용 microsatellite 마커 세트를 활용하여 실험실 및 분석기기간 교차 분석 및 블라인드 테스트를 통한 검정 기술의 표준화는 신품종 육성 시 유전거리의 사전 예측이 가능하여 육종효율을 향상시킬 뿐만 아니라 국가간에 발생하는 품종보호 침해 및 딸기묘의 무단 증식의 사전 예방 등과 같은 분야에 활용도가 높을 것으로 판단된다.