서 언
재료 및 방법
식물 재료
스틸벤 추출 및 HPLC 분석
총 페놀 함량 분석
총 플라보노이드 함량 분석
항산화능 측정
통계 처리 및 다변량 해석
결과 및 고찰
스틸벤 화합물 함량
총 페놀 및 총 플라보노이드 함량
항산화능 비교
서 언
포도는 지구상에서 재배되는 주요 과수 중의 하나로, 전 세계적으로 약 7,102천 ha에서 67,017천 톤이 생산되고 있다(FAO, 2014). 포도는 생과뿐만 아니라 와인, 건포도, 포도즙, 포도주스, 포도잼, 포도씨유 등으로 가공되어 소비되고 있다. 포도나무는 포도과(Vitaceae)에 속하는 덩굴성 식물로 전세계적으로 60
여 종이 분포한다. 포도속은 크게 진정포도아속(Euvitis, 2=38)과 머스카디니아속(Muscadinia, 2=40)으로 분류된다. 아시아에서는 우리나라와 일본, 중국 등지에서 왕머루(Vitis amurensis), 머루(V. coignetiae), 새머루(V. flexuosa), 까마귀머루(V. thunbergii) 및 V. davidii 등의 39종이 분포하고 있다(Reisch et al., 2012). 또한 북미지역에는 강변포도(V. riparia), 사막포도(V. rupestris), 동포도(V. berlandieri) 등이 분포하여 주로 대목 육종을 위한 소재로 활용되고 있다(Reisch et al., 2012).
포도 과실에는 안토시아닌, 플라보놀, 스틸벤 화합물과 같은 폴리페놀 성분이 풍부한데(Flamini et al., 2013), 그 중에서도 스틸벤 화합물인 resveratrol은 항산화능이 높아서 동물체에 있어서 항암, 항염증, 심혈관계 질환 감소의 효과를 나타내는 것으로 보고되어 있다(Baur and Sinclair, 2006). 식물에서는 병원균 및 해충의 침입과 같은 생물학적 요인과 자외선 조사와 같은 비생물학적 요인에 대한 방어 기작 중의 하나로 합성된다(Chong et al., 2009). 스틸벤 화합물은 phenylpropanoid 경로에서 스틸벤 합성효소에 의해 합성되어 다양한 형태로 존재하게 된다(Chong et al., 2009; Soleas et al., 1995). 대부분의 스틸벤 화합물은 과실의 종자(65%)와 과피(30%)에 많이 함유되어 있다(Contreras-Calderón et al., 2011; Kubola and Siriamornpun, 2011).
중국과 한국의 야생머루의 일부 계통에서 유럽종 포도에 비해서 resveratrol 함량이 높은 것으로 보고되었으며(Shi et al., 2014), 스틸벤 화합물 합성에 관여하는 다양한 유전자의 발현을 분석하는 연구도 진행되고 있다(Ahn et al, 2015; Chong et al., 2009; Shi et al., 2014). 왕머루(V. amurensis)를 비롯한 야생 머루는 포도 재배품종에 비해서 스틸벤 화합물 등의 기능성 성분의 함량이 높은 것으로 보고되어 있다(Ahn et al, 2015; Shi et al., 2014).
또한, 국내의 야생 머루는 내병충성, 기능성 성분 함량 등의 특성이 계통 간에 변이를 나타내기 때문에 유용한 육종 소재로 이용하기 위해서는 우수한 특성을 지닌 계통을 선발하는 것이 중요하다. 그러나 재배되고 있는 포도 품종을 대상으로 한 기능성 식품 개발 및 유전자 발현에 관한 연구는 보고되어 있으나(Kim et al., 2005; Kim et al., 2006; Kim et al., 2016; Kim et al., 2017), 국내 자생 머루를 대상으로 계통 간의 기능성 물질 함량을 비교하는 연구는 미흡하다.
따라서 본 연구에서는 국내에서 수집한 머루 계통을 대상으로 스틸벤 화합물, 페놀 및 플라보노이드 함량을 분석하였으며, ABTS+ radical scavenging, DPPH radical scavenging, hydroxy radical scavenging 등 항산화 활성을 분석하여 기능성 성분 함량이 많고 생리활성이 높은 자생자원을 육종 소재로 선발하고자 하였다.
재료 및 방법
식물 재료
머루 계통(13계통) 및 포도 품종(6품종)은 강원도농업기술원과 영남대학교의 유전자원포에서 보존하고 있는 포도나무에서 과실을 수확하여 실험재료로 사용하였다(Table 1). 모든 과실은 성숙기에 맞추어 8월 말경에서 9월 중순경에 걸쳐 수확하였고, 수확한 과실은 바로 과피와 과육으로 분리하여 스틸벤 추출 시 과피 부분만 시료로 사용하여 3반복으로 추출하였다. 총 페놀 및 플라보노이드 함량 분석과 항산화능 측정 실험에 사용된 과실은 동결하여 - 70°C에 보관한 후 3반복으로 추출하여 사용하였다. 모든 추출 및 분석은 머루 계통 및 포도 품종에서 각각 무작위로 선발한 과방 5개에서 5 - 15개의 과립을 다시 무작위로 선발한 후 3반복으로 추출하고 분석을 진행하였다.
Table 1. Korean wild and cultivated grapes used in this study 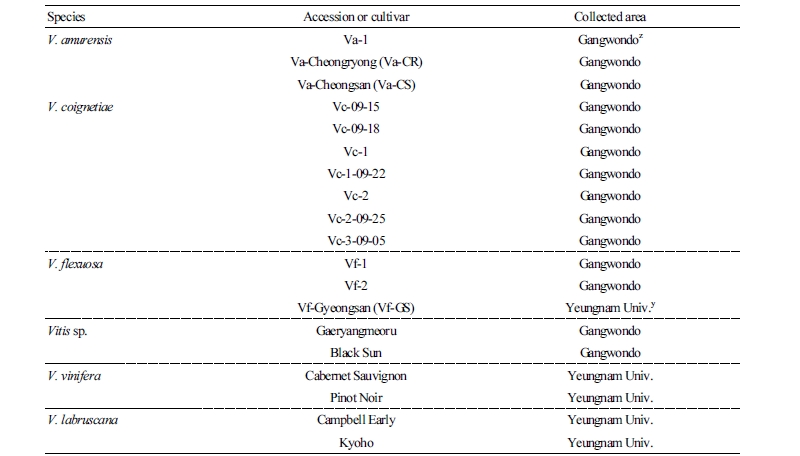 | |
zGangwondo Agricultural Research and Extension Service germplasm repository. yYeungnam University grapevine germplasm repository. | |
스틸벤 추출 및 HPLC 분석
스틸벤 추출 실험은 생체중 1g의 과피를 시료로 사용하였다. 막자사발에서 시료에 4mL의 80%(v/v) methanol을 가하여 마쇄한 후 암소에서 3분 동안 갈아 스틸벤을 추출하였다. 시료 추출액은 25,000xg에 20분간 원심분리하였고, 원심분리하여 얻은 상징액은 syringe(Norm-ject, HSW, Germany)와 0.45um syringe filter(PTFE filter media, Whatman, USA)를 이용하여 여과한 후 사용하였다. 시료 추출액은 high-performance liquid chromatography(HPLC) 분석 전까지 - 20°C에 보관하였고, HPLC 분석은 Choi(2011)의 방법에 따라 HPLC-mass spectrometer(LC-MS) (Model 2695 HPLC, Model 3100 MS, Waters, Woburn, MA, USA)를 이용하여 수행되었다.
총 페놀 함량 분석
머루 계통 및 포도 품종의 과피 시료를 80% methanol로 추출하여 총 페놀 함량 측정에 사용하였으며, Folin-Denis법(Folin and Denis, 1915)에 따라 분석하였다. 일정 농도의 시료 추출액 100µL에 2% Na2CO3 용액 2.0mL를 가한 뒤 2분 후에 50% Folin-Ciocalteu(2.0N) 시약 200µL를 넣고 혼합 후 암소에서 1시간 방치 후 750nm에서 반응액의 흡광도를 측정하였다. 표준물질로 gallic acid(Sigma, St. Louis, MO, USA)를 이용하여 표준곡선을 작성하고 총 페놀 함량을 계산하였다. 시료의 총 페놀 함량은 생체중 1g당 mg garlic acid equivalent(GAE/g FW)로 나타내었다.
총 플라보노이드 함량 분석
머루 계통 및 포도 품종의 과피 시료를 80% methanol로 추출하여 총 플라보노이드 함량 측정에 사용하였고, Moreno et al.(2000)의 방법을 일부 수정하여 측정하였다. 일정 농도의 시료 추출액 1mL에 10% 알루미늄질산염 100µL, 1M 초산칼륨 100µL를 넣고, ethanol 4.3mL를 혼합하고 실온에서 50분간 방치한 후 415nm에서 흡광도를 측정하였다. 표준물질로 quercetin(Sigma, St. Louis, MO, USA)를 이용하여 표준곡선을 작성하고 총 플라보노이드 함량을 계산하였다. 시료의 총 플라보노이드 함량은 생체중 1g당 mg quercetin equivalent(QE/g FW)로 나타내었다.
항산화능 측정
ABTS+ radical 소거능 측정
시료의 ABTS+ radical 소거능은 Re et al.(1999)의 방법에 따라 측정하였다. ABTS+(2,2’-azino-bis-3-ethylbenzothiazoline- 6-sulfonic acid, TCI, Japan) 7.5mM과 potassium persulfate 2.45mM을 혼합한 후 하루 동안 암소에 방치하여 ABTS+ radical cation(ABTS+)을 생성시켰고, 이 용액이 734nm에서 흡광도 값이 0.70 ± 02가 되도록 ethanol로 희석하였다. 일정 농도의 시료 추출물 100µL와 ABTS+ 용액 3mL를 첨가하여 6분 동안 방치한 후 734nm에서 흡광도를 측정하였다. 항산화능의 positive control은 ascorbic acid(Sigma, St. Louis, MO, USA)를 사용하였다. 시료의 항산화능은 다음과 같은 식으로 환산하였다.
ABTS+ radical 소거 활성(%) = (1‑시료의 흡광도/대조구의 흡광도) × 100
DPPH radical 소거능 측정
DPPH radical 소거능은 Blois(1958)의 방법에 따라 시료의 전자공여능으로 인한 DPPH radical의 감소 정도를 흡광도로 측정하였다. 일정 농도의 시료 추출물 1mL에 0.2mM DPPH 용액 500µL를 첨가하고 37°C에서 30분동안 반응시킨 후 517nm에서 흡광도를 측정하였다. 항산화능의 positive control은 ascorbic acid(Sigma, St. Louis, MO, USA)를 사용하였고, 시료의 항산화능은 다음과 같은 식으로 환산하였다.
DPPH radical 소거 활성(%) = (1‑시료의 흡광도/대조구의 흡광도) × 100
Hydroxy radical 소거능 측정
시료의 hydroxy radical 소거능은 Gutteridge(1994)의 방법에 따라 측정하였다. 1mM FeSO4, 1mM ethylenediamine-tetraaceticacid(EDTA), 10mM 2-deoxyribose와 일정 농도의 시료 추출액을 각각 200µL씩 혼합한 후, 0.1M phosphate buffer(pH 7.2) 1.2mL과 10mM H2O2 0.2mL를 첨가한 후 1시간 동안 37°C 수욕상에서 반응시켰다. 반응시킨 용액 500µL와 2.8% trichloroacetic acid 용액 1mL을 섞은 후, 1% thiobarbituric acid 용액 1mL를 가하여 10분간 100°C의 수욕상에서 반응시켜 급냉하여 532nm에서 흡광도를 측정했다. 항산화능의 positive control은 ascorbic acid(Sigma, St. Louis, MO, USA)를 사용하였으며, 시료의 항산화능은 다음과 같은 식으로 환산하였다.
Hydroxy radical 소거 활성 (%) = (1‑시료의 흡광도/대조구의 흡광도) × 100
통계 처리 및 다변량 해석
각 항목별 실험결과의 유의성은 SPSS 23.0 version을 통해 처리하였고, p<0.05 수준에서 Duncan’s multiple range test(DMRT)로 스틸벤 화합물 함량, 총 페놀 및 플라보노이드 함량, 항산화능 측정 등의 결과를 각 실험 항목별로 표준화하기 위하여 통계분석결과에 따라 모든 항목을 16개 등급으로 구분하였으며 등급별로 수치화하고, 수치화한 항목별 점수를 합산하여 총점을 계산하였다.
수치화된 데이터는 Poppr package(R 3.1) 프로그램을 이용하여 UPGMA(unweighted pair group method with arithmetic mean analysis) 방법으로 군집분석을 수행한 후, 사후검정으로 Tukey의 다중비교 검증을 통해 다변량 분산분석을 실시하였으며, 검증을 위한 유의수준은 5%(p < 0.05)로 설정하였다.
결과 및 고찰
스틸벤 화합물 함량
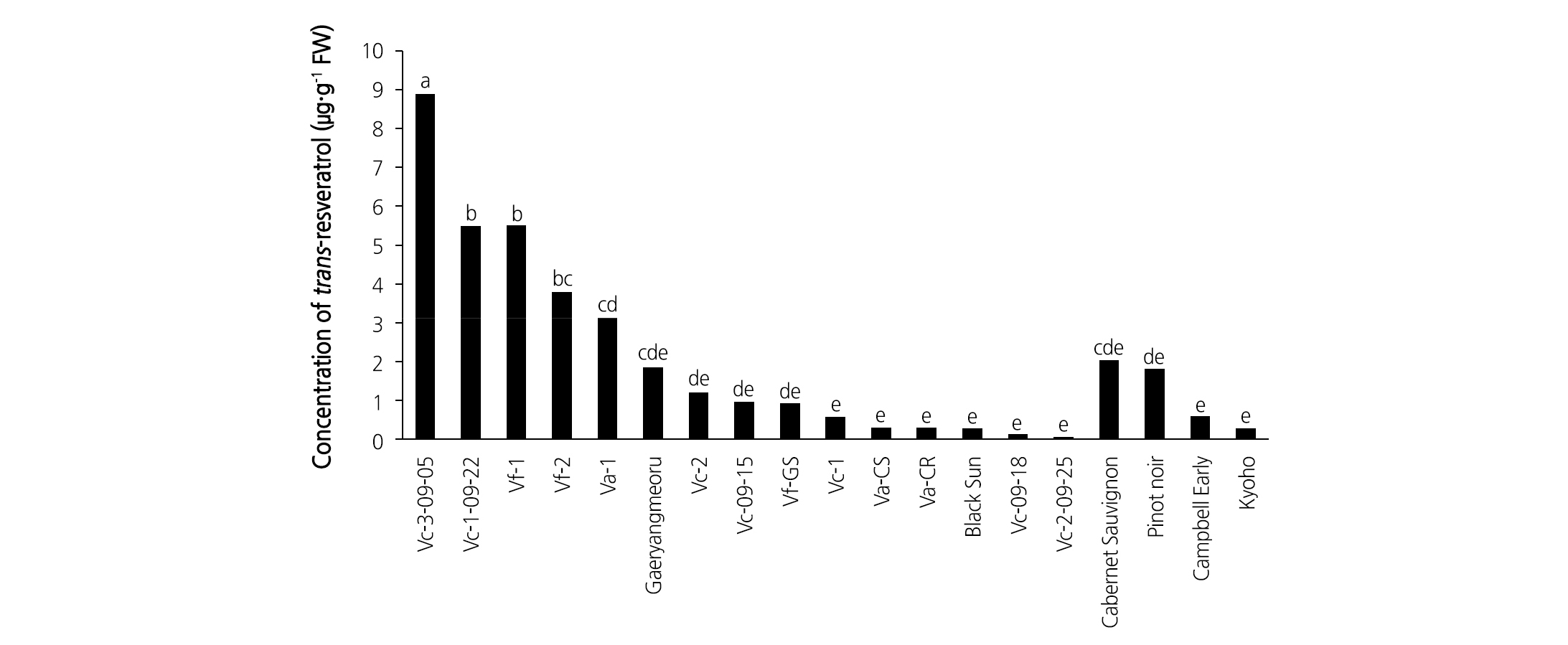
국내에서 자생하는 머루 계통(13계통)과 재배되고 있는 포도 품종(6품종)의 과피로부터 trans-resveratrol, cis-resveratrol, piceatannol, trans-Piceid, cis-Piceid 등의 총 5종류의 스틸벤 화합물의 함량을 조사하였다. 머루(V. coignetiae) 계통인 ‘Vc-3-09-05’, ‘Vc-1-09-22’와 새머루(V. flexsuosa) 계통인 ‘Vf-1’, ‘Vf-2’에서는 유럽종 ‘Cabernet Sauvignon’, ‘Pinot Noir’와 국내 주요 품종인 ‘Campbell Early’, ‘Kyoho’보다 함량이 더 높게 검출되었다(Fig. 1). 머루 계통인 ‘Vc-3-09-05’에서 trans-resveratrol의 함량은 2개의 국내 품종보다 약 15 - 30배, 2개의 유럽종보다 약 4.5 - 4.9배 정도 높았다. 왕머루(V. amurensis) 계통인 ‘Va-1’에서는 2개의 유럽종에 비해 trans-resveratrol의 함량에 큰 차이가 없었으나, 2개의 국내 품종보다 보다는 약 5 - 10배 더 높았다. 나머지 머루 계통에서는 유럽종 및 국내에서 재배되는 주요 품종들과 큰 차이가 나타나지 않았다.
Park et al.(2005a)은 왕머루인 ‘청산’ 품종의 과실 내의 resveratrol 함량이 0.212mg/100g FW으로 ‘Campbell Early’보다 2배 정도 높다고 보고하였다. 또한 Shi et al.(2014)은 중국 야생 머루종(V. quinquangularis)의 일부 계통들은 과립 내 trans-resveratrol 함량이 ‘Cabernet Sauvignon’, ‘Pinot Noir’보다 약 6 - 20배 많았다고 보고하였다. Kiselev et al.(2017)도 왕머루 과피의 trans-resveratrol 함량이 4 - 121µg·g-1(DW)로 유럽종 포도(V. vinifera)보다 높은 함량을 나타냈다고 보고하였다.
Cis-resveratrol은 스틸벤 화합물 추출 시 UV 조사로 인한 trans-resveratrol의 이성질화(isomerisation)에 의한 결과물이라고 알려져 있다(Soleas et al., 1995). 국내에서 재배되고 있는 포도의 과피에서는 미량으로 존재하고(Ahn et al., 2015), UV 조사에 의해 포도나무 잎과 과실에서 cis-resveratrol의 함량이 크게 증가한다고 보고되었다(Choi, 2011, 2012). 본 시험에서 조사된 모든 머루 계통과 재배 품종에서 cis-resveratrol은 검출되지 않았거나, 매우 낮은 농도 수준으로 검출되었다.
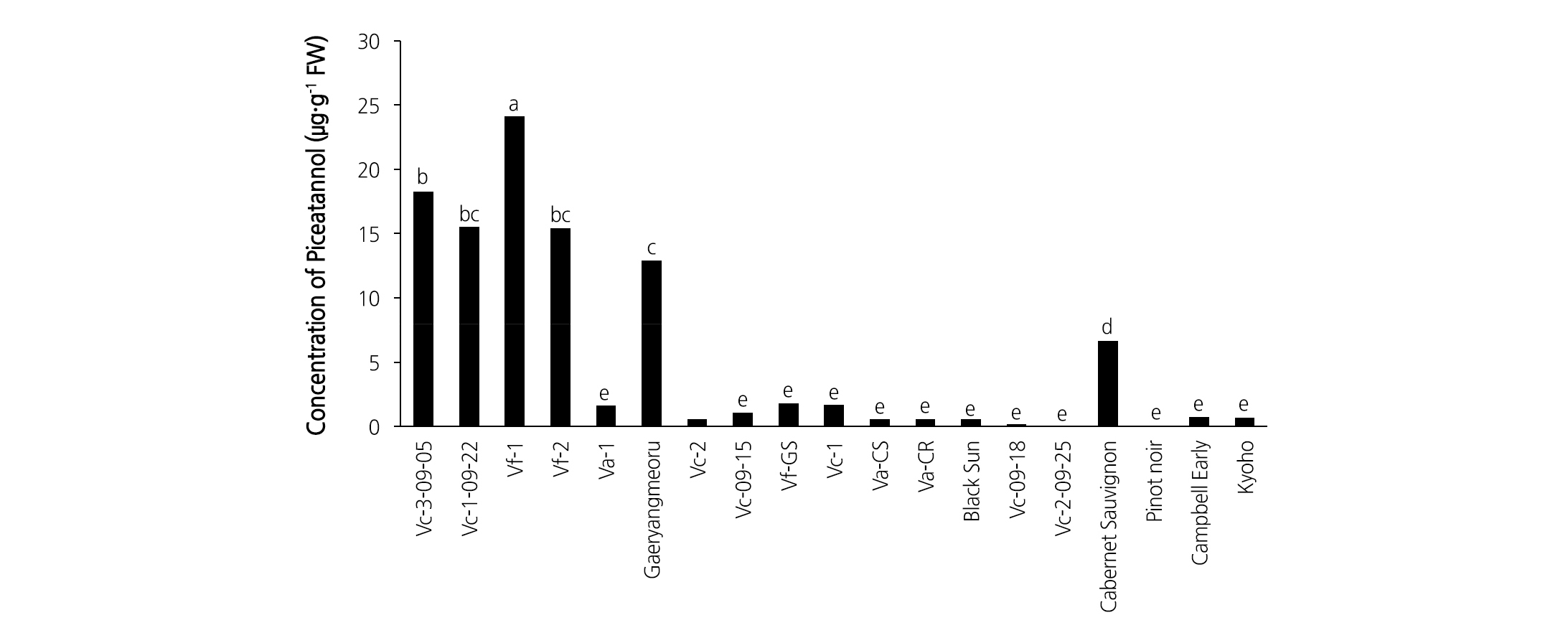
Piceatannol 함량 분석 결과는 trans-resveratrol 함량 분석 결과와 유사한 경향을 보였는데(Fig. 2), ‘Vf-1’, ‘Vc-3-09-05, ‘Vc-1-09-22’ ‘Vf-2’ 계통들이 재배되는 포도 품종보다 훨씬 높은 함량을 나타냈다. 특히 새머루 계통인 ‘Vf-1’에서 가장 높았으며 ‘Cabernet Sauvignon’에 비해 약 3.6배, ‘Pinot Noir’, ‘Campbell Early’, ‘Kyoho’보다는 약 34배의 높은 함량을 보였다. 그러나, 머루의 4계통과 ‘Gaeryangmeoru’를 제외한 나머지 머루 계통에서의 piceatannol 함량은 ‘Pinot Noir’, ‘Campbell Early’, ‘Kyoho’에 비해 큰 차이가 없었다.
Piceatannol은 화학 구조에서 hydroxyphenyl기가 추가적으로 붙어 있어 free radical 소거능이 뛰어나다고 알려져 있다(Chong et al., 2009). 저농도에서도 인체에 효과적이며 쥐실험에서 25µg·kg-1의 piceatannol이 부정맥 및 심장질환을 감소하는 효과를 보였다(Hung et al., 2001). Piceatannol은 resveratrol과 같은 항산화능이 뛰어나 기능성 측면에서 효과적이며, resveratrol 함량이 높은 자생머루 계통들에서 piceatannol의 함량도 높게 나타났으므로 향후 기능성 포도 품종 개발을 위한 육종 소재로 활용될 수 있을 것으로 생각된다.
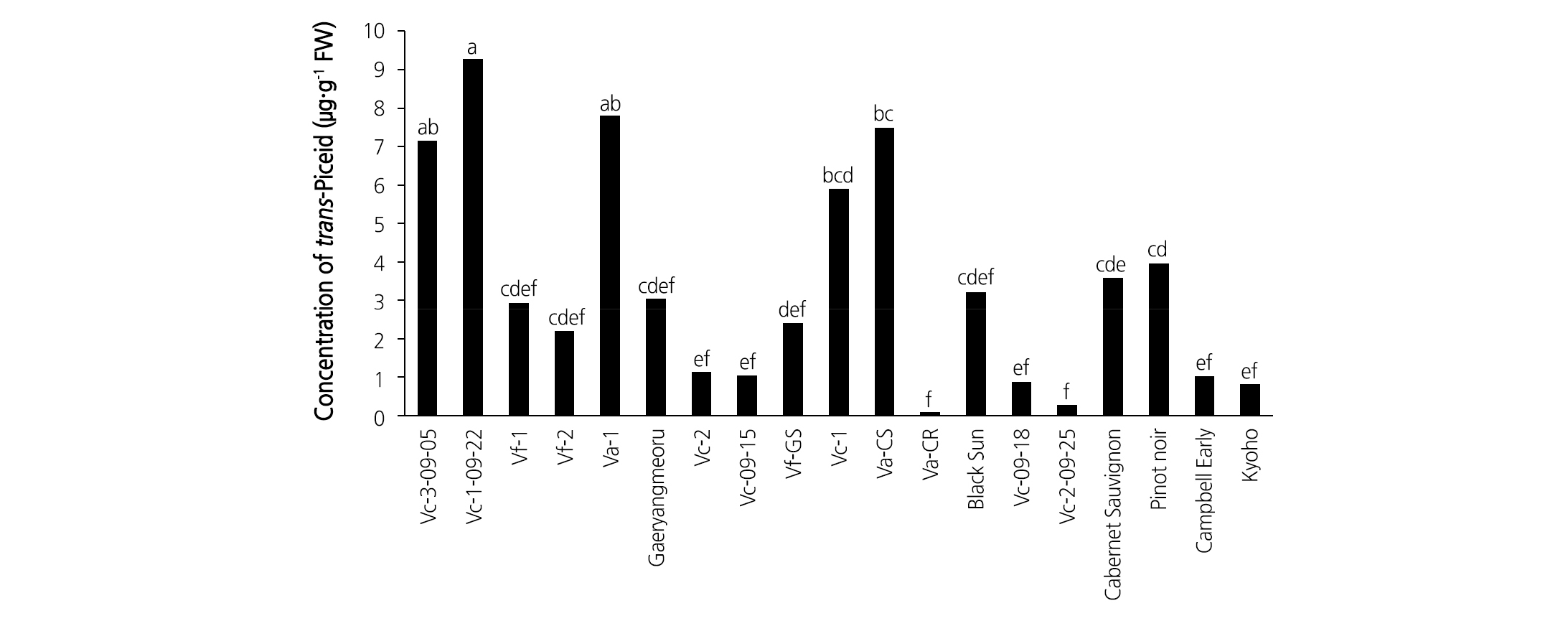
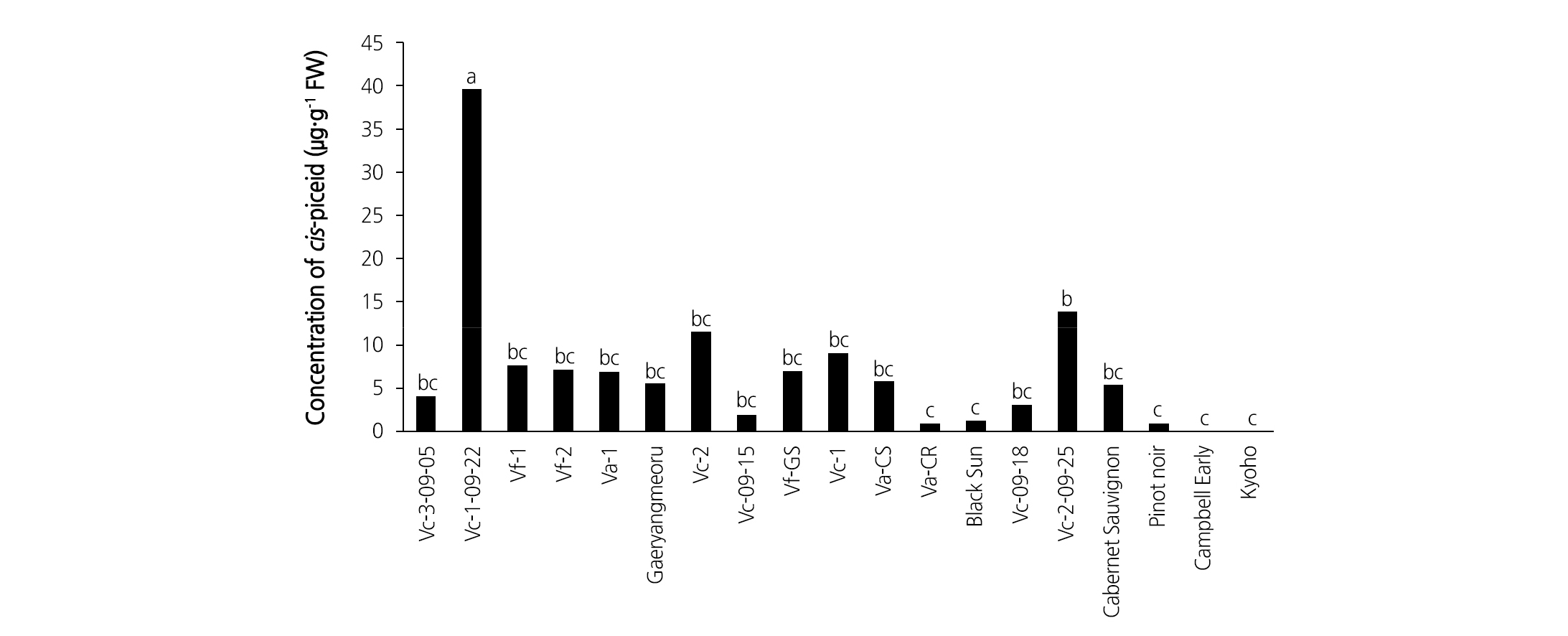
Piceid 함량을 분석한 결과, trans-piceid는 ‘Vc-3-09-05’, ‘Vc-1-09-22’, ‘Va-1’, ‘Va-CS’, ‘Vc-1’에서 포도 품종보다 더 높은 함량이 검출되었다. 특히 ‘Vc-1-09-22’에서 가장 높았으며 2개의 국내 품종보다 약 9.3 - 11.6배, 2개의 유럽종보다 약 2.3 - 2.6배 높게 나타났다. 반면 다른 머루 계통에서는 포도 품종과의 trans-piceid 함량에 큰 차이는 없었다. Cis-piceid의 함량은 머루 계통인 ‘Vc-1-09-22’, ‘Vc-2-09-25’에서 포도 품종보다 높게 나타났지만, 다른 머루 계통에서는 포도 품종과 유사하게 나타났다(Figs. 3 and 4).
일반적으로도 포도에서는 piceid 농도가 resveratrol보다 높다고 알려져 있으나(Romero-Perez et al., 2001; Sun et al., 2006), resveratrol이나 piceatannol과 비교하여 비교적 낮은 생리활성 및 항산화 효과를 보인다고 보고 되어 있다(Choi, 2012; Lorenz et al., 2003). Trans-piceid와 cis-piceid는 시판되는 포도 주스에서 검출되는 주요 스틸벤 화합물이며 특히 적포도 주스에서는 평균 3.8mg·L-1의 trans-piceid가 함유되어 있다고 보고되어 있다(Romero-Perez et al., 1999). 유럽종 포도(V. vinifera)의 과실과 와인에서는 trans-piceid와 cis-piceid 모두 검출되는데 품종에 따라 cis/trans 비율이 매우 다르게 나타나며, 이는 식물의 생리활성 및 대사작용에 영향을 미치는 것으로 보고되어 있다(Bavaresco and Fregoni, 2001; Waterhouse and Lamuela- Raventos, 1994). 식물에서 trans-piceid와 cis-piceid 등의 스틸벤 배당체들은 세포 내에서의 저장, 세포질에서 세포간극으로의 이동 등에 관여하며 세포를 산화적 분해로부터 보호해주는 역할을 한다(Morales et al., 1998).
본 시험에서 일부 머루 계통의 trans-piceid 함량이 포도 품종보다 높고 이들의 piceid 함량이 resveratrol보다 높으며, 머루 계통에 따른 cis/trans 비율에 차이가 있음을 확인할 수 있었으며, 이러한 차이에 따른 식물 생리활성에 관한 추가 연구가 필요할 것으로 생각된다.
총 페놀 및 총 플라보노이드 함량
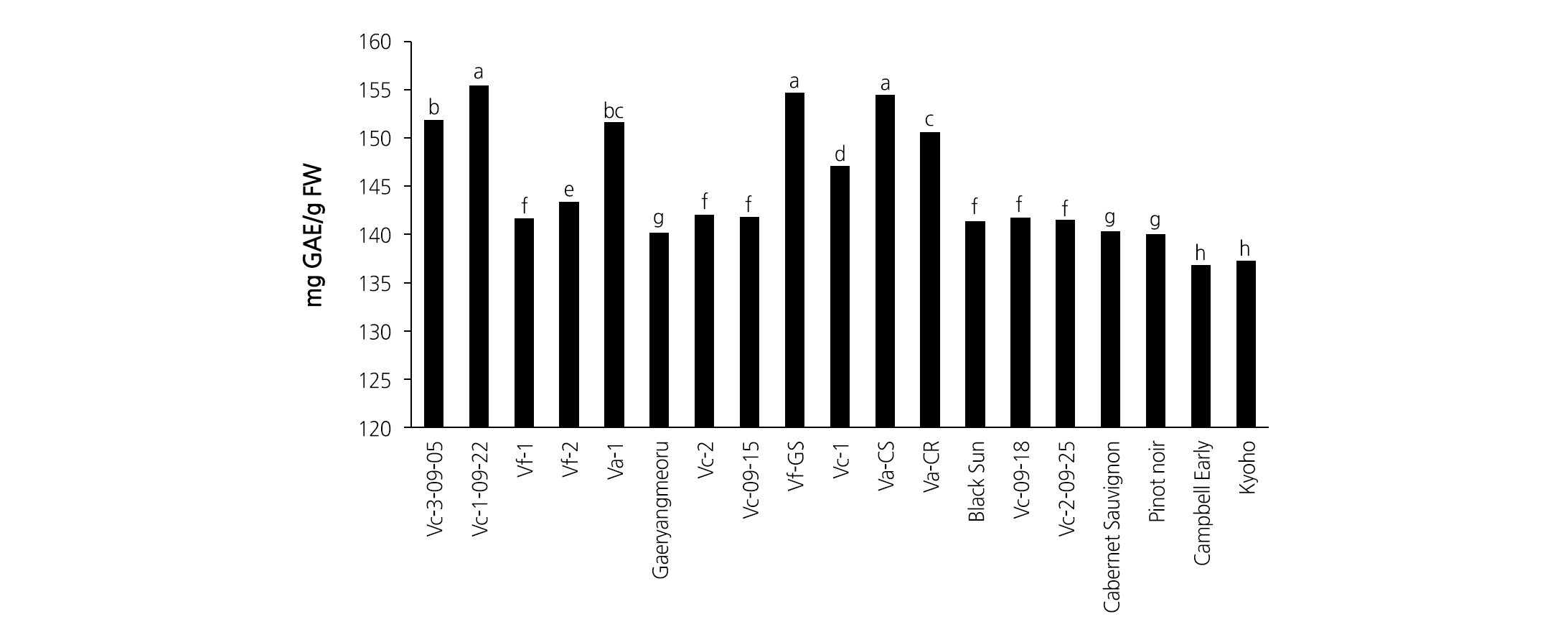
총 페놀 함량은 ‘Vc-1-09-22’(155.4mg GAE/g), ‘Vf-GS’(154.7mg GAE/g), ‘Va-CS’(154.5mg GAE/g)에서 유럽종 ‘Cabernet Sauvignon’(140.3mg GAE/g), ‘Pinot Noir’(140.2mg GAE/g)와 국내 품종인 ‘Campbell Early’(136.8mg GAE/g), ‘Kyoho’(137.3mg GAE/g)보다 높았다(Fig. 5). 반면, trans-resveratrol 함량이 높았던 ‘Vf-1’, ‘Vf-2’에서는 포도 품종보다 총 페놀 함량이 높게 나타났으나, ‘Vc-1-09-22’, ‘Vf-GS’, ‘Va-CS’에서는 포도 품종과 함량에 큰 차이가 나타나지 않았다.
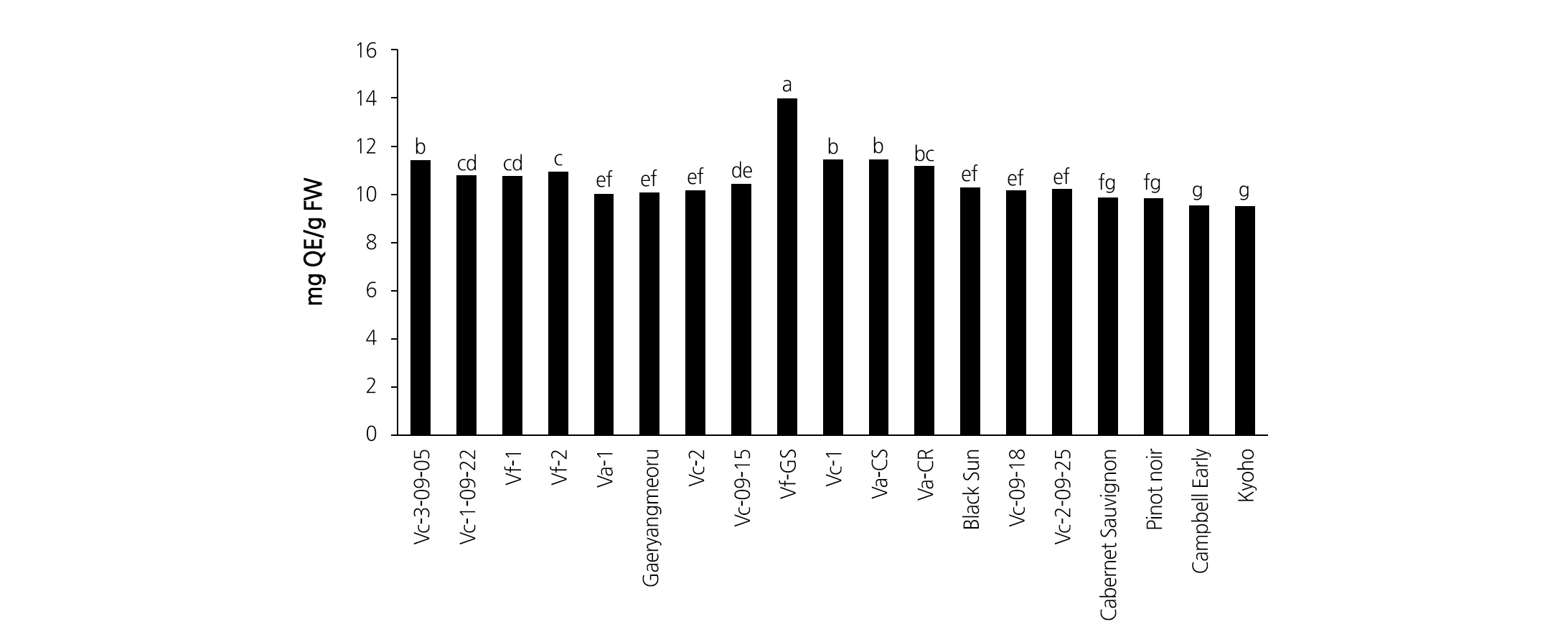
총 플라보노이드 함량을 비교한 결과(Fig. 6), ‘Vf-GS’(14.0mg QE/g), ‘Vc-3-09-05’(11.4mg QE/g), ‘Vc-1’(11.5mg QE/g), ‘Va-CS’(11.4mg QE/g)에서 2개의 유럽종(9.8 - 9.9mg QE/g)과 2개의 국내 품종(9.5mg QE/g)보다 높았다. 그 외의 ‘Vc-1-09-22’, ‘Vf-1’, ‘Vf-2’에서도 함량은 높은 경향이었다.
Kubola and Siriamornpun(2011)은 과실의 부위별로 총 페놀 및 플라보노이드 함량을 측정했을 때, 과육이나 종자보다 과피에서 3배 이상 높게 검출되었다고 보고하였다. Lee et al.(2012)은 유럽종 포도(V. vinifera) 과피의 총 페놀 함량은 107.4mg GAE/g(FW), 총 플라보노이드 함량은 35.9mg QE/g(FW)으로 보고하였다. 머루 과피 추출물의 페놀함량은 Won and Kim(2012)에 의해 5.98mg GAE/g(FW)으로 보고되었으나, Choi et al.(2006)은 54.4mg GAE/100g(FW)로 보고하였다. 이와 같은 다양한 시험 결과는 분석된 과실의 계통 간의 함량 차이, 재배 지역 및 환경에 따른 과실의 특성 차이, 과실의 분석 부위에 따른 함량 차이, 분석한 과실의 건물중과 생체중에 따른 차이에 의해 나타난 것으로 여겨진다.
식물체와 과실의 페놀 화합물은 병에 대한 저항성 역할을 할 뿐만 아니라 맛, 색 등 과실의 품질과 항산화 기능에 있어서 중요한 성분이다(Mnanach et al., 2005; Zhou et al., 2009). 본 시험에서 자생머루 중에서 총 페놀 및 플라보노이드 함량이 높은 계통을 확인하였으며, 내병성 및 기능성 포도 품종 육성을 위한 육종 소재로서 유용한 가치를 지닌 것으로 생각된다.
항산화능 비교
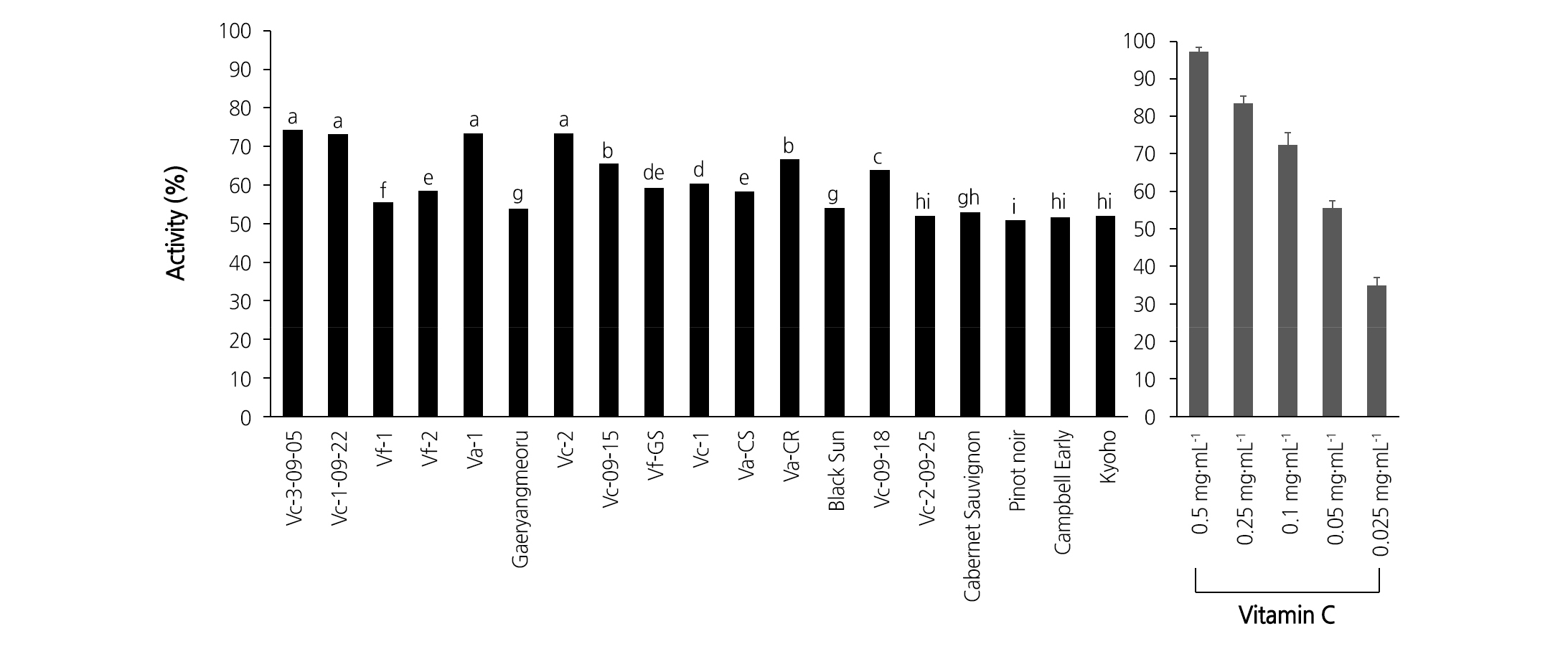
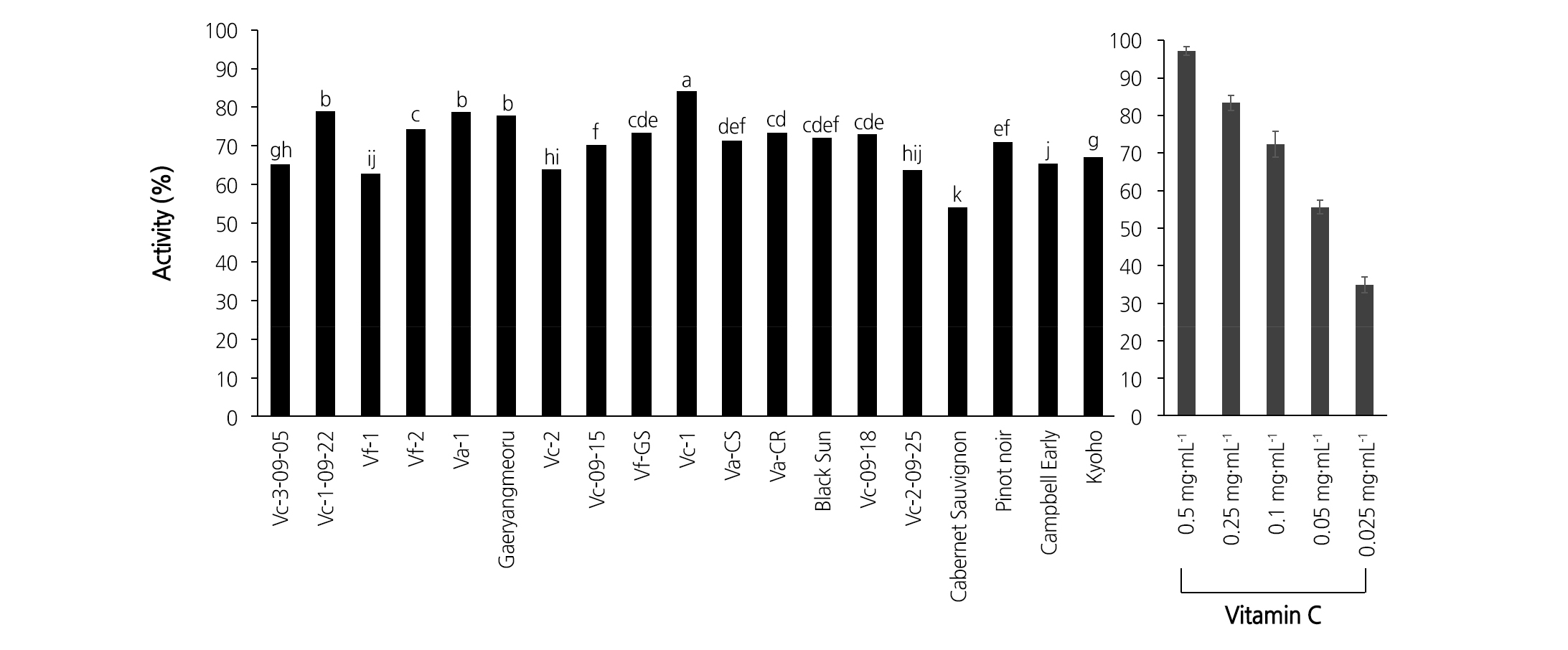
ABTS+ radical 소거능은 ‘Vc-3-09-05’, ‘Vc-1-09-22’, ‘Va-1’, ‘Vc-2’ 계통에서 포도 품종에서보다 항산화능이 뛰어났으며, ‘Vc-09-15’, ‘Va-CR’, ‘Vc-09-18’와 같은 머루 계통들의 과피 추출물도 높은 항산화능을 나타내었다(Fig. 7).
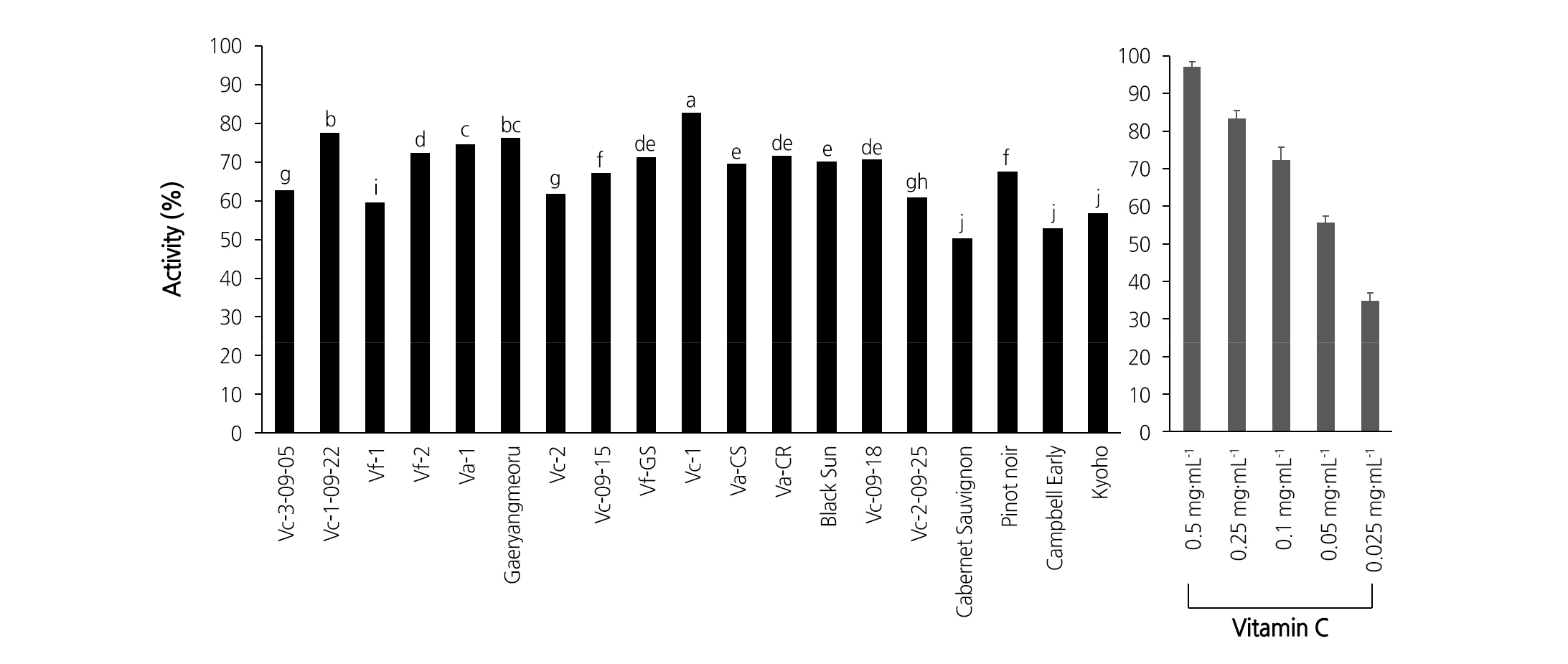
DPPH radical 소거능을 비교한 결과는 Fig. 8에 나타내었다. ‘Vc-1’계통에서 항산화능이 가장 좋았으며, 다음으로 ‘Vc-1-09-22’, ‘Gaeryangmeoru’, ‘Va-1’ 순서였다. 반면 ‘Vc-09-15’에서는 ‘Pinot Noir’와 항산화능에서 큰 차이를 보이지 않았고, ‘Vc-2’, ‘Vc-2-09-25’ 등은 ‘Pinot Noir’보다 오히려 항산화능이 낮았다.
Hydroxy radical 소거능은 ‘Vc-1’에서 가장 좋았고, ‘Vc-1-09-22’, ‘Va-1’, ‘Gaeryangmeoru’, ‘Vf-2’ 순으로 항산화능이 높게 나타났다(Fig. 9). ‘Pinot Noir’(71.0%)에서는 왕머루 계통인 ‘Va-CS’(71.4%), 머루 계통인 ‘Vc-09-15’(70.2%)와 유사한 항산화능이 확인되었으며, ‘Vc-2’, ‘Vc-2-09-25’에서는 ‘Kyoho’보다 항산화능이 낮게 나타났다.
유럽종 포도(V. vinifera)와 미국종 포도(V. labrusca)에서 trans-resveratrol 함량이 높았던 품종은 항산화능도 높은 것으로 보고되어 있으며(Burin et al., 2013), 왕머루(V. amurensis) 과피 추출물의 DPPH radical 소거능은 유럽종 포도(V. vinifera)보다 강하다고 보고 되었다(Chen et al. 2018). 본 연구에서는 ‘Vc-3-09-05’는 총 페놀 및 플라보노이드 함량과 ABTS+ radical 소거능이 높았고, ‘Vc-3-09-05’, ‘Vc-1-09-22’, ‘Va-1’의 경우, trans-resveratrol 함량과 ABTS+ radical 소거능이 높은 결과를 보였다. Trans-resveratrol과 같은 기능성 물질의 함량이 높은 자생머루 계통은 높은 항산화 활성을 나타낼 것으로 생각된다.
Trans-resveratrol은 생체 내에서 다양한 작용점을 지니고 있어서 직간접적으로 인체 내의 생리활성을 나타내며(Bollmann et al., 2014), 주요 작용점 중의 하나인 SIRT1을 활성화한다(Xia et al., 2017). 그러나, SIRT1은 다양한 요인에 의해서도 활성화되어, 다양한 유전자의 발현 조절 등을 통한 항산화 활성을 포함한 생리활성을 나타낸다. 순수한 trans-resveratrol의 처리뿐 아니라 다양한 성분을 함유한 추출물의 처리에 의해서 생리활성 효과가 나타난다(Xia et al., 2014; Zhang and Kraus, 2010).
포도 과실에는 안토시아닌, 플라보놀, 폴리페놀 성분이 풍부하여(Flamini et al., 2013), 포도 과실의 추출물에 의한 항산화능을 비롯한 생리활성이 높아서 동물체에 있어서 항암, 항염증, 심혈관계 질환 감소의 효과를 나타내는 것으로 보고되어 있다(Baur and Sinclair, 2006; Li et al., 2012). 비록 ‘Vf-1’은 trans-resveratrol의 함량이 높은 계통과는 다르게 항산화능은 높지 않은 것으로 나타났지만, 다른 계통의 포도 추출물에는 resveratrol 이외의 많은 성분이 존재하여 다른 기작을 통한 항산화 활성을 나타낸 것으로 사료된다.
왕머루 과실에 존재하는 높은 함량의 폴리페놀은 free radical을 소거함으로써 쥐의 심장 세포 손상을 억제한다고 보고되었으며(Shu-ping et al., 2008), H2O2를 소거하는 활성이 탁월하여 formazan 형성과 내피세포 손상을 방지하는 효과를 나타낸다(Gao and Zhang, 2006; Zhang et al., 2007). Jeong et al.(2007)은 머루(V. coignetiae) 계통 과립의 50% 에탄올 추출물과 증류수 추출물(1.6g·dL-1)의 산화능이 각각 101.4%, 99.4%로 0.1% L-ascorbic acid(97.7%)와 1% L-ascorbic acid(98.1%)보다도 뛰어나다고 보고하였다.
국내 산머루 종자 추출물의 DPPH radical 소거능은 ‘Campbell Early’보다 높으며(Park et al., 2003), Park et al.(2005b)은 머루 실생 계통의 수소공여능이 82.9%로 40 - 50%인 ‘Campbell Early’ 품종보다 매우 높다고 보고하였다. 또한 머루 에탄올 추출물 1,000µL·mL-1 농도에서 전자공여능은 94.8%로 대조구인 butylated hydroxytolune(95.6%)과 L-ascorbic acid(80.6%)보다 높게 나타났다(Park, 2010).
본 시험에서도 Fan et al.(2011)의 보고와 같이 자생머루 과피 내 스틸벤 화합물이나 페놀 화합물의 높은 함량이 수소원자의 전달이나 전자공여능 활성을 높여 불안정한 free radical을 소거함으로써 세포 내 DNA, 단백질 등과 같은 중요한 분자 화합물의 산화를 방지하는 것으로 생각된다. 따라서, 자생머루는 인체 내에서 강한 항산화 작용을 통해 당뇨병, 심장병, 노화 등을 억제하는 효과가 있을 것으로 기대된다. 이러한 스틸벤 화합물은 포도 및 머루의 과실에 많이 존재하며, phenylpropanoid 경로에서 스틸벤 합성효소에 의해 합성된 trans-resveratrol(3,5,4’-trilhydroxy-stilbene)을 기본 골격으로 하여 수산화(hydroxylation), 배당화(glycosylation), 메톡시화(methoxylation), 중합 등의 유도체화 반응을 거쳐 다양한 형태로 존재하며, 식물체 내에 수십 종류가 있다(Chong et al., 2009; Soleas et al., 1995).
활성산소는 hydrogen peroxide, superoxide radical, hydroxyl radical, peroxide 등이 있으며 지질 산화, 단백질 분해, DNA 변이 등을 유발하여 각종 질환을 일으킨다(Droge, 2001; Halliwell et al., 1995). 활성산소를 제거하는 항산화 능력은 마늘이나 여러 과수의 과실에서 우수하다고 보고되었다(Imai et al., 1994; Kubola and Siriamornpun, 2011; Lichtentha and Marx, 2005; Sun et al., 2002). 스틸벤 화합물은 항산화능이 뛰어나고, 스틸벤 화합물을 포함한 대부분의 폴리페놀 성분은 포도 과실의 종자(65%)와 과피(30%)에 많이 함유되어 있어(Contreras-Calderón et al., 2011; Kubola and Siriamornpun, 2011), 포도주나 과실의 종자와 과피에서 추출한 가공품의 이용은 인류 건강에 도움을 줄 수 있을 것으로 생각된다.
최근 포도속(Vitis spp.) 중에서도 왕머루(V. amurensis), 머루(V. coignetiae), 새머루(V. flexuosa), 까마귀머루(V. thunbergii)와 같은 야생 포도는 재배되는 포도 품종에 비해서 스틸벤 화합물 등의 기능성 물질이 높다고 보고되어 있다(Ahn, 2015; Shi et al., 2014). 야생종 머루 종자 내 항산화 물질 분석(Choi, 2011; 2012; Kim et al., 2005; Kim et al., 2006; Shi et al., 2014), 머루 과피의 항산화 활성 분석에 대한 연구도 많이 보고 되었다(Choi et al., 2006). 대부분의 야생 포도에는 스틸벤 화합물의 함량이 높으며 스틸벤 합성에 관여하는 유전자의 발현도 재배되는 품종에 비해 높은 것으로 보고되어 있다(Ahn et al., 2015; Chong et al., 2009; Moon et al., 2017; Shi et al., 2014).
본 연구에서도 국내에 자생하는 왕머루를 비롯한 야생 머루종은 포장에서 재배되는 포도 품종에 비해서 스틸벤 화합물 등의 기능성 물질의 함량이 높은 것으로 나타났기에 고품질 기능성의 포도 품종 육성을 위한 육종프로그램에 중요한 육종 소재로 이용될 수 있을 것이다.
국내에서는 기능성과 내병성을 가진 고품질 포도 품종 육종을 위해 머루가 육종 소재로 손꼽히고 있다. 그러나 국내에 자생하는 머루는 다양하고 종내 계통 간에도 기능성 및 내병성 등의 형질에 변이가 크다. 본 연구에서도 trans-resveratrol함량이 높은 머루 계통들이 총 페놀 및 플라보노이드 함량과 항산화능에 있어 차이를 보였다. 따라서, trans-resveratrol함량과 총 페놀 및 플라보노이드 함량이 높고 항산화능이 뛰어난 자생 머루를 육종 소재로 선발하기 위해서는 다양한 시험 분석 결과를 이용한 종합분석이 요구되었다. 그러나 다양한 형질을 이용한 머루 유전자원에 대한 포도 육종에 유용한 유용한 육종 소재를 선발하는 것은 시도가 거의 되지 않고 있다.
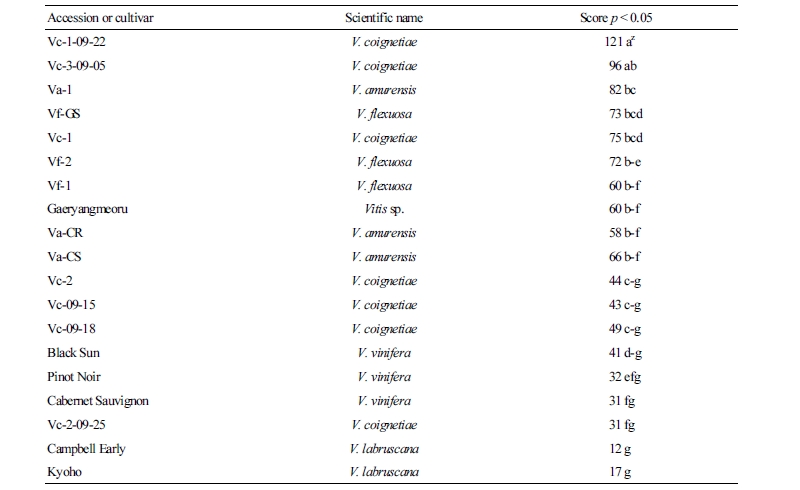
따라서 본 연구에서는 다변량 해석을 통해 유용한 육종 소재를 선발하고자 하였으며(Table 2), 유용한 형질을 지니고 있어 상위권에 속하는 머루 계통으로는 ‘Vc-1-09-22’, ‘Vc-3-09-05’, 왕머루 계통에서는 ‘Va-1’, 새머루 계통에서는 ‘Vf-2’ 등이 있으며, 현재 국내에서 재배되고 있는 포도 품종보다 생리활성 물질 함량 및 항산화능이 훨씬 더 효율적이었다. 이러한 분석을 근거로 머루(V. coignetiae) 계통인 ‘Vc-1-09-22’, ‘Vc-3-09-05’, 새머루(V. flexsuosa) 계통인 ‘Vf-2’, 왕머루(V. amurensis) 계통인 ‘Va-1’이 기능성 물질이 다량 함유된 국내 포도 품종을 육종하는 소재로 사용하기에 적합하다고 판단하였다.
작물의 신품종 육성에 있어 야생종의 특성 구명은 매우 중요하며(Ellstrand et al., 2010), 내병성 및 재해 저항성인 포도 품종 육성에 야생종 포도를 활용하기 위한 유전적 다양성에 관한 연구도 진행되어 왔다(Cambrolle et al., 2013; Coleman et al., 2009; Revilla et al., 2010). 야생종 및 재배 품종의 기원, 기능성 물질 함량 비교 및 특정 형질과 연관된 다양성에 관한 분자생물학적 특성 연구가 진행되고 있으나, 주로 개별 형질을 대상으로 한 연구들이다(Arroyo-Garcia et al., 2006; Duan et al., 2015; Emanuelli et al., 2010; This et al., 2006). 최근 Riaz et al.(2018)은 유럽의 지중해 인근과 아시아에 자생하거나 재배되는 1,378계통의 포도 유전자원을 대상으로 20종류의 SSR 표지를 이용하여 유전적 다양성과 유연관계를 밝히고 군집의 특성을 파악하였다. 유전자와 염색체의 특징, 고정 등의 특성을 이용하여 집괴 분석, 주좌표 통계분석, 구조 분석 등의 다변량 해석을 통한 유전적 다양성과 특성을 분석하여 내병성 및 내재해성 포도 신품종 육성에 관한 중요한 자료를 마련하였다.
수량 분류란 생물의 형질을 그 상태에 따라 분류하고 구성단위의 수적 표현에 의해서 그룹화 하는 분류 체계법으로, 주로 생물 형질에 대한 군집 분석(cluster analysis)과 같은 수적 알고리즘을 사용하여 분류하는데 이용된다. 이와 같이 향후에는 다양한 형질을 고려한 유용 유전자원을 선발하는데 있어서도 형질 특성을 객관화하여 분석할 수 있는 시스템 개발이 요구된다. 머루의 유전체 및 전사체 분석과 유전적 형질 특성을 연계한 비교분석이 이루어진다면 고품질의 포도 품종 육성 프로그램에 있어 중요한 정보를 제공할 것으로 생각된다.