서 언
토양과 물의 과도한 염은 식물의 생장과 발육을 저해하는 대표적인 비생물적 스트레스이다. 염은 토양의 삼투압을 낮추어 식물 뿌리의 수분흡수를 방해하고(Asish and Anath, 2005), 식물체내로 흡수된 후에는 세포의 Na+, Cl- 이온뿐만 아니라 K+, Ca2+ 이온 등의 항상성을 방해하여 세포 내 이온불균형을 유발한다(Hasegawa[21] et al., 2000; Rodriguez[40] et al., 2005). 세포 내 이온불균형 은 다양한 효소들의 활성을 억제하여(Dreyer et al., 1999) 미네랄 흡수와 광합성작용을 저해할 뿐만 아니라(Larcher, 1980; Fidalgo et al., 2004) 활성산소의 축적을 촉진하고(Davenport et al., 2005) 항산화 기작을 방해함으로써(Foyer and Noctor, 2003) 결 국 생육을 억제시키거나 심할 경우 식물체를 고사시킨다. 최근, 기후변화로 인한 세계적인 한발과 가뭄의 심화는 농경지와 농 업용수원의 염류화를 촉진시키고 있어서 염 스트레스는 전 세계적으로 농작물의 안정생산을 위협하는 주된 요인이 되고 있 다. 특히, 감자(Solanum tuberosum L.)는 식량과 가공원료를 목적으로 전 세계의 약 120여 국가에서 재배되고 있어 염 저항성에 대한 요구가 크다(Flowers and Yeo, 1995; Levy and Veilleux, 2007). 감자는 Maas and Hoffman (1977)에 의해 염 저항성이 약한 작 물로 분류된 바 있는데, 비교적 낮은 염 조건(EC 1-2 dS·m-1)에서도 수량에 부정적인 영향을 받는다(van Hoorn et al., 1993). 또 한, 염 스트레스에 노출될 경우, 엽 황화, tip burn, leaf burn, 줄기왜화, 괴경표피경화, 괴경열개 등이 발생한다고 알려져 있다 (Greenway and Munns, 1980; Feigin, 1988). 한편, 감자는 지구상에 약 2000여종 이상이 존재하며(Hanneman Jr., 1989), 염에 대한 감자의 민감성 또는 저항성은 타고난 유전적 소질에 따라 광범위한 차이가 있다고 보고된 바 있다(Kim et al., 1995; Jaarsma et al., 2013). 즉, 2배체인 근연야생종들이 4배체인 일반 재배종보다 염 저항성이 강한 경향이며(Martinez et al., 1996; Arvin and Donnelly, 2008), 4배체 상업적 재배종들 간에도 염 스트레스 조건에서 생장과 수량성에 큰 차이가 있음이 보고되었다(Elkhatib et al., 2004; Homayoun et al., 2011). 식물의 염 저항성 발현에는 osmolyte류가 관여하는 것으로 알려져 있는데, 아미노산의 일종 인 proline이 대표적이다(Nanjo et al., 1999; Hasegawa et al., 2000). Proline은 염 스트레스에 처한 식물에서 함량이 증가하는데, 세 포외부의 삼투압에 반응하여 세포내 삼투압을 조절하고, 세포막을 보호하며, 생체효소를 안정화시켜 염에 대한 저항력을 높 인다(Delauney and Verma, 1993; Nanjo et al., 1999; Hasegawa et al., 2000). 감자에서는 Martinez et al. (1996)이 다양한 Solanum species를 대상으로 염 스트레스를 처리한 결과, proline이 많이 축적된 species가 염 저항성이 강했다고 한 반면, Cano et al. (1996), Feitosa et al. (2001) 등은 이와 상반된 연구결과를 보고하여 proline 함량과 감자의 염 저항성 간 상관관계는 아직 명확하지 않은 실정이다. 우리나라의 경우 염은 일부 해안가 및 간척지를 제외하고는 감자 경작에 있어서 큰 문제가 되지 않아서 현재까지 감자의 염 저항성 관련 연구가 미미한 실정이다. 다만, 근래의 농산물 무역 자유화 추세에 따라 국산 감자의 해외 진출을 위한 연구가 활발하게 진행되면서, 수출 대상지역에서 가장 큰 제약요소인 염 스트레스에 대한 국내외 감자의 생육반응과 염 저항 성을 이해하는 것이 필요하게 되었다.
이에 따라, 본 연구는 국내외 주요 감자 품종의 염 스트레스에 대한 생육, 수량성 및 proline 함량 반응을 구명하고, 농업적 측 면에서 품종 간 염 저항성을 상호 비교함으로써 염 저항성 감자 품종 개발을 위한 기초자료로 활용하고자 하였다.
재료 및 방법
실험재료
본 연구에 공시된 실험재료는 국내 감자 장려품종인 ‘수미’(‘Superior’), ‘대서’(‘Atlantic’), ‘대지’(‘Daejima’), ‘고운’(‘Goun’), ‘하 령’(‘Haryeong’), ‘추백’(‘Chuback’), ‘두백’(‘Duback’)과 농촌진흥청 고령지농업연구소에서 유전자원으로 보유하고 있는 ‘파보 리타’(‘Favorite’), ‘LT-8’, ‘스푼타’(‘Spunta’), ‘레드라소다’(‘Redlasoda’), ‘러셋 버뱅크’(‘Russet burbank’), ‘크로다’(‘Kroda’), ‘로 마나’(‘Romana’), ‘레드스칼렛’(‘Redscarret’), ‘데지레’(‘Desiree’), ‘마르포나’(‘Marfona’), ‘그라놀라’(‘Granola’) 등 국내외 감자 18품종을 대상으로 하였다.
재배 및 염 스트레스 처리
균일한 생리적 조건의 씨감자를 위하여 강원도 대관령에 위치한 고령지농업연구소 망실포장에서 여름재배를 통하여 2014 년 9월 수확한 각 공시품종의 건전한 씨감자를 파종2 5일전에 산광최아하였다. 괴경 정단부에서 싹이0 .5cm 내외로 균일하게 출현된 괴경들을 골라 염수준 별로 다르게 조제된 염상토와 염수를 이용하여 강릉시 송정에 위치한 유리온실에서 3월 25일 파 종 및 봄재배하였다. 염처리를 위한 염상토 및 염수는 원예용 상토(쑥쑥이 2호, 농우바이오, 수원, 대한민국)와 수돗물에 순도 97% 이상의 국내산 천일염을 일정량 첨가하여 EC 1.0(대조구), 4.0, 8.0 dS·m-1 등 3수준으로 조제하였다. 먼저, 염상토는 염수 준 별로 쑥쑥이 상토(EC 0.42 dS·m-1) 50L당 천일염을 각각 8g, 45g, 86g 내외로 첨가하여 골고루 혼합 후 사용하였다. 염수는 실험온실에서 관수원으로 사용하는 수돗물(EC 0.67 dS·m-1) 100L당 천일염을 각각 11g, 130g, 265g 내외로 첨가 후 잘 저어서 완전히 녹여 염수준 별 관수 처리에 사용하였다. 파종을 위하여 플라스틱 포트(지름 20cm, 높이 25cm)에 염상토를 적당량 충 진 후, 포트당 괴경 1개씩을 10cm 깊이로 파종하였으며, 각 처리 당 품종 별 포트 5개씩을 3반복으로 하여 완전임의배치법으로 실험하였다. 비배관리를 위하여 포트 당 감자 전용 복비(N:P:K=10:8:9, 슈퍼감자, 남해화학, 포항, 대한민국) 15g씩을 전량 기 비로써 천일염 첨가 전 상토에 혼용하였으며, 관수는 염수준 별로 조제된 염수를 사용하여 생육초기(파종-파종후 30일)에는 7 일 간격으로, 생육중기부터 수확까지는3 -4일 간격으로 저면관수 및 식물체 상부관수를 동시에 실시하였다 .
생장 및 수량성 조사
염처리에 따른 감자 품종 별 생장반응을 알아보기 위하여 파종후 70일경 지상부 특성으로서 경수, 경장, 경두께, 지상부 무게 를, 뿌리 특성으로서 뿌리길이, 뿌리무게 및 TR율을, 그리고 엽 특성으로는 엽수, 엽면적(LAI), 엽중을 조사하여 ANOVA 분석 하였다. 또한, 총 chlorophyll, chlorophyll a(Chl a), b(Chl b) 함량 및 Chl a와 Chl b의 함량 비율을 분석하였다. 수량성은 파종후 90일경 최종 수확하여 괴경갯수, 평균괴경무게, 괴경수량을 조사 및 ANOVA 분석하였다. 또한, 염 저항성 비교 기준으로써 지 상부 무게와 괴경수량을 대상으로 염처리 수준별 대조구(EC 1.0 dS·m-1)에 대한 백분율로 환산하여 품종 간 비교 분석하였다.
Chlorophyll 분석
Chlorophyll 함량 분석은 AOAC(2003)의 방법에 준하여 실시하였다. 파종후 70일경 지상부 줄기 상단부로부터 5-7마디 아 래 부분에서 채취한 엽의 생체시료 1g에 85% acetone 10mL를 첨가한 후 마쇄 및 원심분리(10,000rpm, 10분)하였다. 잔사에 85% acetone 첨가 및 원심분리를 4회 반복 실시하였으며, 상등액 10mL에 ether 10mL, 증류수 5mL를 가한 후 진탕하였다. Ether 층에 소량의 sodium sulfate를 가하여 수분을 제거한 후, 3mL를 취하여 분광광도계(X-ma 2000, Human Corp., USA) 로 660.0nm와 642.5nm에서 흡광도를 측정하였다. 아래의 식으로 산출된 chlorophyll 함량 data를 ANOVA 분석에 사용하였다.
총 chlorophyll(μg·mL-1) = 7.12 O.D.(660.0nm) + 16.80 O.D.(642.5nm) Chl a(μg·mL-1) = 9.930 O.D.(660.0nm) - 0.777 O.D.(642.5nm) Chl b(μg·mL-1) = 17.60 O.D.(642.5nm) - 2.81 O.D.(660.0nm)
Proline 분석
Proline 함량 분석을 위하여 파종 후 70일경 채취한 엽을 동결건조하여 분쇄한 후 Bates et al. (1973)의 방법에 따라 분석하 였다. 엽 건조시료 1g에 10mL의 sulfosalicylic acid 용액(3%, w/v)을 첨가한 후 24시간 동안 상온에 보관한 다음, filter paper(Whatman No. 42)로 여과하였다. 여과액 1mL에 glacial acetic acid 1mL와 ninhydrin reagent 1mL를 첨가하였다. 시험 관 뚜껑을 막고 끊는 물(100°C)에서 1시간 동안 반응시킨 후 상온(21°C)에서 5분간 보관하였다. 여기에 toluene 2mL를 첨가하 여 20초 동안 교반 후 상등액을 취하여 분광광도계(X-ma 2000, Human Corp., USA)로 흡광도(520nm)를 측정하였다. 정량을 위하여 proline(Sigma-Aldrich Co., USA)을 표준물질로 사용하였으며, mM·g-1 DW로 나타내었다.
상관성 및 통계 분석
본 실험에서 도출된 data의 통계분석을 위하여 SAS enterprise guide 4.3(SAS Institute Inc, Cary, NC, USA) 통계프로그램 을 이용하여 ANOVA 분석(Analysis of variance)을 수행하였으며, DMRT(Duncan’s Multiple Range Test) 5% 수준에서 유의 성을 검정하였다.
결과 및 고찰
줄기, 엽, 뿌리 생장 분석
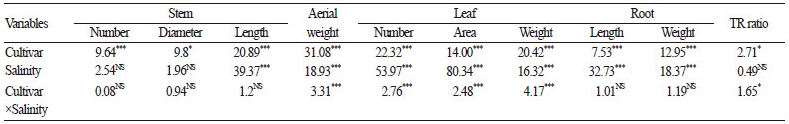
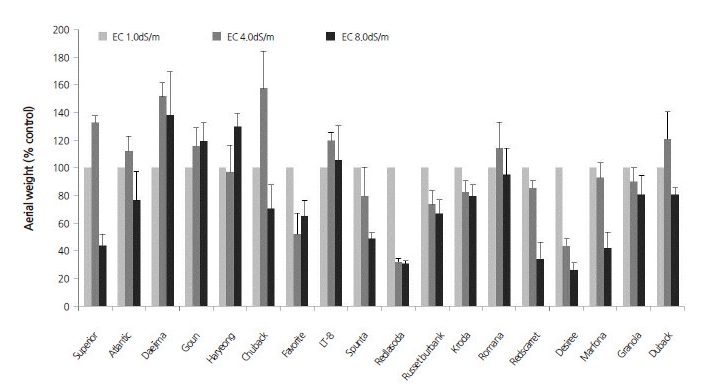
염처리에 따른 감자 품종별 줄기, 엽, 뿌리의 생장량을 조사하여 ANOVA 분석하였다(Table 1). 경수와 경두께는 품종에 따 른 유의적 차이가 있었으나 염에 의한 영향은 유의성이 없었다. 반면, 경장(F value = 39.37, p≤ 0.001)과 지상부 무게(F value = 18.93, p≤ 0.001)는 염에 대해 고도의 유의성을 나타내어 매우 민감하게 영향 받았음을 알 수 있었다. 특히, 지상부 무게의 경우, 품종×염의 교호작용에 따른 영향도 유의성이 높았으며(F value = 3.31, p≤ 0.001), 염 스트레스에 따른 품종 간 차이가 매우 큰 것으로 나타났다. 대조구에 대한 염 처리구의 지상부 무게 비율을 품종 간 비교한 결과(Fig. 1), 염 수준이 높을수록 대 부분 품종에서 감소하는 경향이었으나, 일부 품종의 경우 오히려 더 증가하였다. 즉, EC 4.0 dS·m-1에서 ‘수미’, ‘대서’, ‘대지’, ‘ 고운’, ‘추백’, ‘LT-8’, ‘로마나’, ‘두백’ 등 8품종이, EC 8.0 dS·m-1에서 ‘대지’, ‘고운’, ‘하령’, ‘LT-8’ 등 4품종이 대조구(EC 1.0 dS·m-1)보다 더 무거웠다.
배추, 콩 등에서 적당한 염은 작물의 생장을 촉진하지만, 고염은 생장억제 및 식물체의 무게 감소를 유발하며, 피해를 일으키 는 염 수준은 작물에 따라 다른 것으로 알려져 있다(Khan, 2001; Kim et al., 2010; Amira and Abdul, 2011). 또한, 동일 작물이 라 하더라도 유전적 형질에 따라 염에 대한 생장반응이 다르게 나타나며, 감자에서 품종 간 차이에 대한 여러 연구결과들이 보 고된 바 있다. Jaarsma et al. (2013)는 60mM NaCl을 양액처리한 감자의 수경재배에서 품종 간 생체중을 비교한 결과, ‘Russet burbank’, ‘Bintje’는 대조구(0mM NaCl)와 차이가 적었으나, ‘Mozart’와 ‘Monalisa’는 대조구의 60% 수준까지 감소되었다고 하였다. Kim et al. (2013)은 ‘수미’의 경우 EC 4.8 dS·m-1에서 식물체의 초장이 대조구와 차이가 없었던 반면, ‘추강’은 EC 1.6 dS·m-1에서도 초장이 감소되었으며, 일부 품종에서는 대조구보다 증가하였다고 하여 본 실험의 결과와 유사하였다 .
염처리에 따른 엽의 ANOVA 분석 결과, 엽수, 엽면적, 엽중 모두 염뿐만 아니라 품종×염의 교호작용에 대해서도 매우 높은 유의성(p≤ 0.001)을 나타냈다. 즉, 엽의 생장이 염 스트레스에 매우 민감한 것을 알 수 있었다. 이와 관련하여, Papp et al. (1983) 은 sugar beet의 NaCl 처리에서 엽수를 결정짓는 엽의 유기는 세포분열에 의하여 영향을 받으며, 염에 따른 영향은 적었다고 한 반면, 엽면적을 좌우하는 엽의 신장은 Ca 이온의 상태에 따라 달라지며, 염에 매우 민감하게 영향을 받았다고 하였다. Papp et al. (1983)의 연구결과는 본 실험의 엽면적 경향과 유사하였으나, 엽수에 대해서는 다소 차이가 있었다. 하지만, cowpea(Raul et al., 2003), 양배추(Jamil et al., 2005), 콩(Gama et al., 2007) 등 다양한 작물에서 NaCl 처리로 인한 엽수 감소가 보고된 바 있 는데, 이는 체내로 흡수된 염을 체외로 배출하기 위한 식물의 적극적인 대응기작 중 하나로써, 체내의 과도한 염을 늙은 하엽에 집적시킨 후 그 엽을 탈락시키기 때문인 것으로 밝혀진 바 있다(Munns, 2002). 엽중의 ANOVA 분석 결과는 지상부 무게의 경 향과 유사하였다.
한편, 뿌리는 전 생육기간에 걸쳐 토양에 함유된 염에 직접 접촉되는 기관으로서, 염 스트레스에 의해 양수분의 체내 흡수가 저해됨에 따라 뿌리 생장도 영향을 받게 된다(Larcher, 1980; Zidan et al., 1990). 이에 따라 뿌리 생장은 식물체의 염 저항성 평 가 시 주요 판단기준으로써 활용되기도 한다(Bilski et al., 1988; Kim et al., 1995; Im et al., 2015). 본 실험에서 염처리에 따른 뿌리길이와 뿌리무게의 ANOVA 분석에서도 두 항목 모두 품종 및 염에 대해 유의성이 매우 높았다(p≤ 0.001). TR율은 염에 대한 유의성은 없었던 반면, 품종×염의 교호작용에 따른 유의성(p≤ 0.05)이 인정되어, 염 스트레스 환경에서 지상부 및 뿌리 의 생장 비율에 품종 간 차이가 있음을 가늠할 수 있었다. 이는 앞서 지상부 무게에 대한 품종×염의 교호작용 결과와 연계된 것 으로 생각되었다.
Chlorophyll 함량 분석
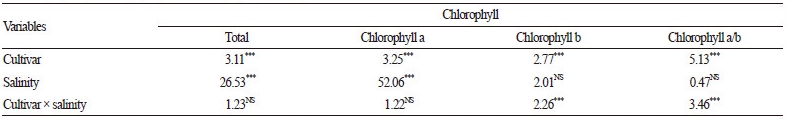
염처리에 따른 chlorophyll 함량의 ANOVA 분석 결과는 (Table 2)와 같았다. 총 chlorophyll 함량은 품종(F value = 3.11, p≤ 0.001)은 물론 염(F value = 26.53, p≤ 0.001)에 대해서도 고도의 유의성을 나타내어 매우 민감하게 반응하였음을 알 수 있었 다. 반면, 품종×염의 교호작용은 유의성이 없었다. Chl a와 Chl b의 염에 따른 영향은 다소 차이가 있었다. Chl a는 총 chlorophyll 의 ANOVA 분석 결과와 유사하였던 반면, Chl b는 염 단일요인에 따른 영향은 유의성이 없었으나, 품종×염의 교호작용(F value = 2.26, p≤ 0.001)에 대해서는 고도의 유의성을 나타냈다. 또한, Chl a와 Chl b의 함량비율은 Chl b의 ANOVA 경향과 유사하였다. 즉, 염 스트레스에 대해 Chl a보다는 Chl b에서 감자 품종 간 반응에 차이가 컸음을 알 수 있었다. 일반적으로 염은 thylakoid swelling이나 grana stacking의 감소를 일으켜 엽록체의 구조를 악화시키고, chlorophyll 함량을 감소시켜 결국 광합 성을 저해한다고 알려져 있다(Bruns and Hechtbuchholz, 1990; Ghosh et al., 2001; Fidalgo et al., 2004). 또한 토마토 (Khavarinejad and Mostofi, 1998), 보리(Tort and Turkyilmaz, 2004), 배추(Kim et al., 2010), 콩(Amira and Abdul, 2011) 등 대 부분 작물에서도 염 스트레스로 인한 총 chlorophyll과 Chl a, Chl b의 함량 감소가 보고된 바 있다. 특히, Kim et al. (2010)은 배 추에서 염 스트레스에 따른 Chl a와 Chl b의 함량비율 증가를 보고하여, 본 실험의 결과와 같이 염에 대한 Chl a와 Chl b의 반 응에 차이가 있음을 시사하였다.
수량성 및 Proline 함량 분석
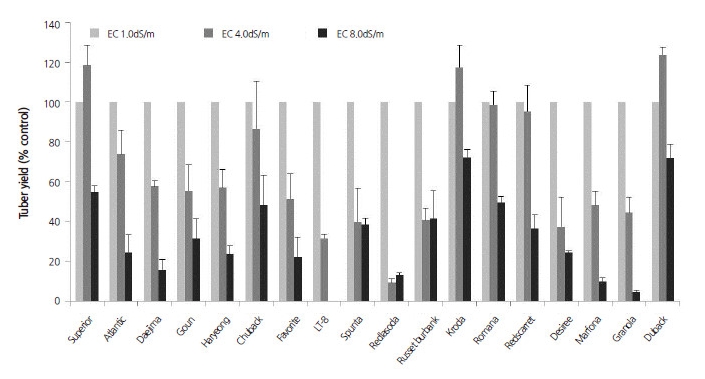
염처리에 따른 감자 품종 간 수량성의 ANOVA 분석 결과(Table 3), 괴경수, 평균괴경무게, 괴경수량 모두 품종과 염에 대해 고도의 유의성을 나타냈다. 평균괴경무게는 품종×염의 교호작용에 대해서는 유의성이 없었으나, 괴경수(F value = 1.7, p≤ 0.05)와 괴경수량(F value = 2.48, p≤ 0.001)의 경우, 유의적으로 나타나 다소간 영향을 받은 것으로 생각되었다. 특히, 괴경수 량에 있어 염에 대한 품종 간 반응 차이가 큰 것으로 나타났다. 괴경수량은 대부분 품종에서 염수준이 높을수록 감소하였는데 (Fig. 2), 앞서 지상부 무게에서의 품종 간 경향과는 차이가 있었다. ‘수미’, ‘크로다’, ‘로마나’, ‘두백’ 등은 EC 4.0 dS·m-1에서 괴 경수량이 대조구와 같거나 그보다 더 무거웠으며, EC 8.0 dS·m-1에서도 수량 감소율이 다른 품종들보다 더 낮았다. 이에 반해, 지상부 무게가 대조구보다 염 처리구(EC 4.0 dS·m-1 및 8.0 dS·m-1)에서 더 무거웠던 ‘대지’, ‘고운’, ‘하령’, ‘LT-8’ 등은 염처리 에 따른 수량감소가 심하였다. 특히, 고염 조건(EC 8.0 dS·m-1)에서 ‘LT-8’의 경우, 지상부는 번무하였으나 괴경이 아예 형성되 지 않았다. 즉, 감자에서 염 스트레스에 대한 식물체 자체의 생장반응과 괴경에서의 수량이 일치하지 않으며, 다소 상이함을 알 수 있었다. 또한, 농업적으로 중요한 수량성 측면에서 볼 때, 염 스트레스 환경에서 수량 감소가 적은 감자품종의 선발 및 재배 가 감자의 생산 안정성을 위해 가치가 있을 것으로 생각되었다.
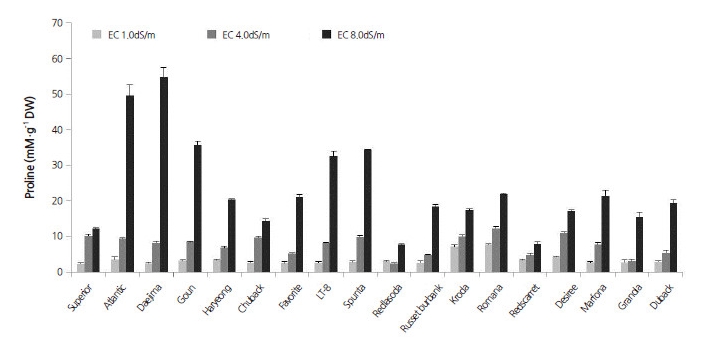
한편, proline은 염 스트레스에 처한 식물체에서 함량이 증가하여 세포내 삼투압 안정, 세포막 보호, 막단백질 안정화 등을 통 해 염 저항성을 높이는 대표적인 osmolyte로서 알려져 있다(Mansour, 1998; Nanjo et al., 1999; Szabados and Savoure, 2010). 본 실험에서 엽에 축적된 proline 함량은 품종(F value = 7.28, p≤ 0.001), 염(F value = 126.78, p≤ 0.001), 그리고 품종×염의 교호작용(F value = 6.21, p≤ 0.001) 모두에 의해서 매우 민감하게 영향을 받았다. 즉, 염 스트레스 조건에서 품종 간 그 생성량 에 차이가 컸음을 알 수 있었다. 이에 염처리에 따른 품종 간 proline 함량을 비교한 결과, Fig. 3에서와 같이 염수준이 높을수록 거의 모든 품종에서 증가하였다. 특히, 염처리구(EC 4.0 dS·m-1, 8.0 dS·m-1)에서 지상부 무게가 대조구와 유사하였거나 더 무 거웠던 ‘대지’, ‘고운’, ‘LT-8’ 등에서 proline의 함량 증가가 두드러졌다. 이에 반해, 고염처리구(EC 8.0 dS·m-1)에서 지상부 무 게는 대조구에 비해 다소 가벼웠으나, 수량 감소율이 다른 품종들보다 낮았던 ‘수미’, ‘크로다’, ‘로마나’, ‘두백’에서는 상대적으 로 낮은 경향이었다. Martinez et al. (1996), Feitosa et al. (2001), Jaarsma et al. (2013) 등 많은 연구자들도 감자 식물체에서 염 스트레스 처리로 인한 proline의 함량 증가와 축적의 품종 간 차이를 보고한 바 있다. 하지만 proline 함량과 감자의 염 저항성 간 상관성에 대해서는 서로 견해가 달랐다. Martinez et al. (1996)는 두 요인의 정의 상관을, Feitosa et al. (2001)은 부의 상관을 주장한데 반해, Jaarsma et al. (2013)은 상관성이 낮다고 하여 두 항목 간 상관성은 아직 명확하게 밝혀지지 않은 상황이다. 본 실험에서는 염 스트레스 조건에서 proline의 함량 증가가 많았던 품종들이 적었던 품종들보다 지상부 생장은 더 양호했던 반 면, 수량 감소는 더 큰 것을 관찰할 수 있었다. 또한, 염처리 조건에서 수량감소가 적었던 품종들은 염에 따른 proline의 함량 증 가가 적은 경향을 확인하였다. 즉, 염 저항성에 대한 평가기준을 감자 식물체의 생장반응에 둘 때와 괴경수량으로 할 경우, proline 함량과 염 저항성 간 상관성 결과가 서로 상반될 것으로 생각되었다 .
상관관계 분석
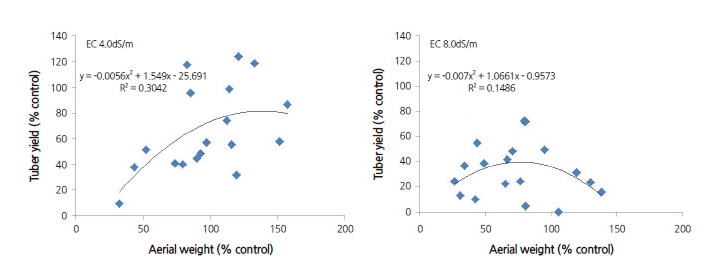
한편, 지상부 무게와 괴경수량의 관계는 Fig. 4와 같았다. EC 4.0 dS·m-1에서는 ‘y = -0.0056x2 + 1.549x – 25.691(R2 = 0.3042)’를, EC 8.0 dS·m-1에서는 ‘y = -0.007x2 + 1.0661x – 0.9573(R2 = 0.1486)’를 나타내어 염수준이 높을수록 지상부 무 게와 괴경수량 간 상관성이 낮아지는 경향이었다. 따라서, 감자의 염 저항성 평가 및 개체 선발 시, 지상부 생장이 왕성한 것만 을 단편적으로 선발하는 것은 농업적으로 중요한 수량성 측면에서는 오류가 발생할 수 있을 것으로 생각되었다.
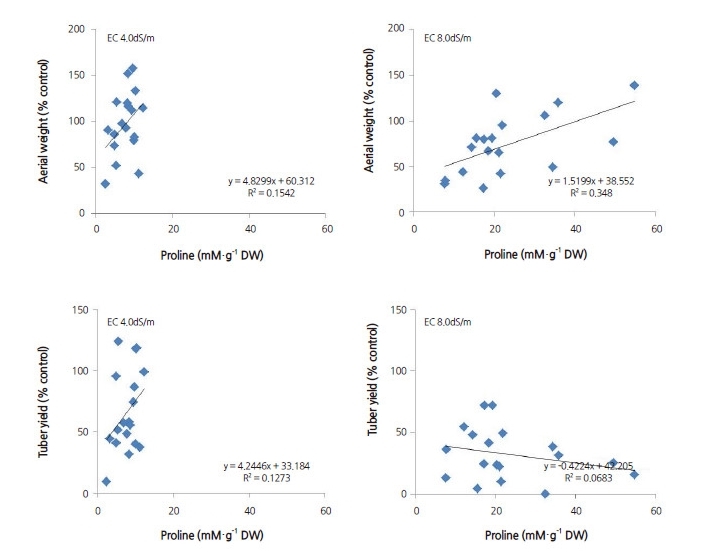
Proline 함량과 지상부 무게 및 괴경수량과의 관계를 분석한 결과, 염수준에 따라 경향이 달랐다(Fig. 5). 즉, EC 4.0 dS·m-1에 서는 지상부 무게(y = 4.8299x + 60.312, R2 = 0.1542)와 괴경수량(y = 4.2446x + 33.184, R2 = 0.1273) 모두 proline 함량과 정 의 상관성을 나타냈다. 한편, EC 8.0 dS·m-1에서는 지상부 무게는 정의 상관성을(y = 1.5199x + 38.552, R2 = 0.348), 괴경수량 은 부의 상관성을(y = -0.4224x + 42.205, R2 = 0.0683) 나타냈다. 지상부 무게가 괴경수량보다 proline 함량과의 정의 상관성 이 좀 더 높았으며, 괴경수량은 염수준이 높을수록 상관성이 낮았다. 이는 환경스트레스 조건에서 보다 더 잘 견디기 위하여 광 합성 산물을 괴경 내 축적보다는 proline 등 저항성 증진 관련 물질의 합성에 할애함으로써 엽과 줄기의 생장유지 또는 촉진 방 향으로 대사작용이 집중되었기 때문인 것으로 추정되나 이에 대한 연구결과들이 거의 없어 향후 좀 더 정밀한 연구가 필요할 것으로 보였다.
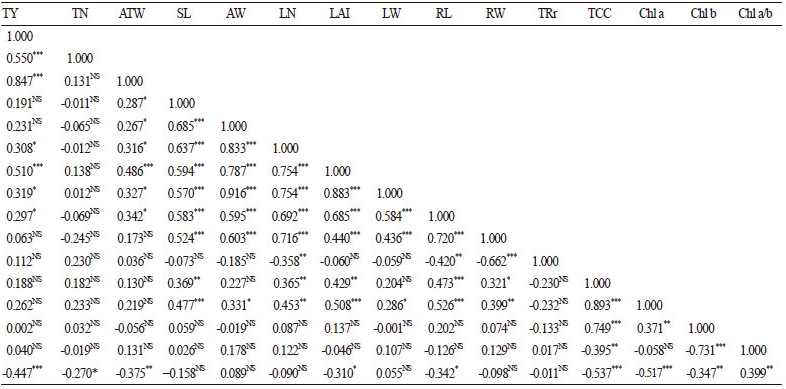
괴경수량을 중심으로 줄기, 엽, 뿌리, chlorophyll, proline 함량 등 본 실험의 조사항목 간 pearson 계수 및 상관성을 분석하였 다(Table 4). 괴경수량은 괴경갯수(Pearson’s r = 0.550, p≤ 0.001)보다는 괴경비대와 관련 있는 평균괴경무게(Pearson’s r = 0.847, p≤ 0.001)와 좀 더 높은 정의 상관성이 있었다. 또한 엽수(Pearson’s r = 0.308, p≤ 0.05), 엽면적(Pearson’s r = 0.510, p ≤ 0.001), 엽중(Pearson’s r = 0.319, p≤ 0.05) 및 뿌리길이(Pearson’s r = 0.297, p≤ 0.05)와도 정의 상관성을 나타낸 반면, proline 함량과는 고도의 부의 상관성(Pearson’s r = -0.447, p≤ 0.001)을 보였다. Poline 함량은 괴경갯수(Pearson’s r = -0.270, p≤ 0.05)보다는 평균괴경무게(Pearson’s r = -0.375, p≤ 0.01)와 좀 더 높은 부의 상관성이 있었다. 또한, 총 chlorophyll(Pearson’s r = -0.537, p≤ 0.001) 및 Chl a(Pearson’s r = -0.517, p≤ 0.001), Chl b(Pearson’s r = -0.347, p≤ 0.001)와도 부의 상관성을 나타냈다.
결론적으로, 본 실험에서 염 처리에 따른 감자 품종 간 생장양상과 수량요소의 반응에 차이가 있음을 알 수 있었다. 또한, 식 물체의 염 저항성 관련 지표로써 일반적으로 널리 알려져 있는 proline 함량의 효용성은 농업적 측면에서는 다소 낮은 것으로 확인되었다. 이는 지상부 생장과 괴경 수량성과의 연관성이 염수준이 높을수록 낮았기 때문이었다. 따라서, 감자의 염 저항성 판단 시 단편적인 기준 적용보다는 식물학적으로는 식물체의 생장량을, 농업적인 목적으로는 상대적인 수량감소율을 평가 기 준으로 활용하는 것이 보다 실용적일 것으로 생각되었다. 이러한 측면에서 볼 때, 고염조건에서 수량감소율이 다른 품종들보 다 상대적으로 낮은 ‘수미’, ‘크로다’, ‘두백’ 등은 염 저항성 감자 육성을 위한 교배재료로써 뿐만 아니라, 염이 문제되는 지역에 서 감자의 생산 안정성을 높이는데 유용한 품종들로 판단된다 .