서 언
재료 및 방법
실험재료 및 외생 에틸렌 처리
과실 품질 분석
세포벽 분해 및 에틸렌 생합성 관련 유전자 발현
결 과
외생 에틸렌 처리에 따른 ‘골드원’과 ‘제시골드’ 키위프루트의 과실품질 변화
외생 에틸렌 처리에 따른 ‘골드원’과 ‘제시골드’ 키위프루트의 유전자 발현 변화
고 찰
외생 에틸렌 처리에 따른 황육계 키위프루트 과실의 품질 변화
세포벽 분해와 에틸렌 관련 유전자 발현
서 언
에틸렌은 식물호르몬 중 하나로 망고, 바나나 등의 호흡급등형 과실의 후숙 과정을 촉진한다(Johnson et al., 1997; Prasanna et al., 2007). 또한 에틸렌은 다양한 원예작물 내의 화학적인 성분 변화와 더불어 물리적인 변화를 유도하는 것으로 알려져 있다(Kato, 1990; Johnson et al., 1997; Miller and McDonald, 1997; Bower et al., 2003; Prasanna et al., 2007). 원예작물 중 성숙 이후 추가적인 후숙이 필요한 대부분의 과실들은 외생 에틸렌 처리로 후숙이 촉진되고, 과실의 맛과 풍미가 증진되며 식용하기에 보다 좋은 상태로 변화한다(Kato, 1990; Johnson et al., 1997; Miller and McDonald, 1997; Saltveit, 1999; Bower et al., 2003; Prasanna et al., 2007: Lim et al., 2015). 이와 같은 과정에서 부적합한 외생 에틸렌 처리는 오히려 내적, 외적인 품질 저하를 유발하며 식미 가치를 빠르게 저하시키는 등 원예산물의 영양학적, 경제적 가치를 저하시키는 원인이 되기도 한다.
키위프루트(Actinidia chinesis)의 후숙 과정에는 호흡급등형 과실과 다른 몇 가지 특징이 있다. 일반적인 호흡급등형 과실은 수확후 과실의 호흡 증가가 발생하는 시기와 유사한 단계에서 자가촉매적 에틸렌 생합성으로 에틸렌 생성량이 증가하지만 키위프루트 과실은 외생 에틸렌의 자극 없이는 내생 에틸렌이 낮은 수준으로 유지된다(Antunes et al., 2000; Antunes and Sfakiotakis, 2002; Park et al., 2006; Antunes, 2007; Jabbar and East, 2016). 또한 외생 에틸렌을 처리하더라도 10°C 이하의 온도에서는 호흡비급등형 형태의 과실 특성을 보인다(Antunes et al., 2000; Antunes, 2007). 그리고 일반적으로 호흡과 에틸렌 생성이 동시에 이루어지는 호흡급등형 과실들과 다르게 과실의 호흡 증가와 에틸렌 생성이 분리되어 있는 것으로 보고되었다(Antunes and Sfakiotakis, 2002; Antunes, 2007).
현재 국내에서 유통되고 있는 키위프루트의 경우 수확후 및 저장 후 후숙처리를 하지 않은 단단한 상태의 과실들이 유통되고 있어서 소비자의 구매욕구에 도달하지 못하고 있는 실정이다. 또한 불완전한 후숙 과실들은 신맛이 강하고 과심이 단단하여 고품질 후숙과실의 생산과 유통을 위한 기술 개발이 절실하게 필요한 실정이다. 키위프루트에서 외생 에틸렌 처리는 최적의 가식 단계까지 과실을 빠르고 균일하게 후숙시키는 적절한 수확후 처리수단이며, 키위프루트에 대한 외생 에틸렌 처리의 필요성은 여러 연구 결과를 통해 확인되었다(Ritenour et al., 1999; Saltveit, 1999; Jabbar and East, 2016; Lim et al., 2017). 또한 키위프루트를 후숙시키기 위한 외생 에틸렌 처리농도와 처리시간은 종과 품종에 따라 상당히 다르다(Ritenour et al., 1999; Saltveit, 1999; Jabbar and East, 2016). 기존의 외국 육성 품종의 경우 적절한 외생 에틸렌 처리방법이 구명되어 과실 후숙에 이용되고 있지만, 최근 국내에서 육성된 품종에 대한 수확후 외생 에틸렌 처리 방법은 아직 구명되어 있지 않다. 따라서 본 연구는 국내에서 새롭게 육성된 황육계 키위프루트에 대해 외생 에틸렌 처리에 따른 과실의 후숙 특성을 이해하고, 우수한 품질의 후숙과실 생산을 위한 외생 에틸렌 처리방법을 구명하고자 실시하였다.
재료 및 방법
실험재료 및 외생 에틸렌 처리
키위프루트(Actinidia chinesis)는 ‘골드원(Goldone)’과 ‘제시골드(Jecy Gold)’ 두 품종으로 2015년 10월 31일에 경남 사천 소재의 과원에서 수확한 후 건전한 과실을 선별하여 실험에 사용하였다. 외생 에틸렌 처리는 과실을 밀폐용기에 넣고 20°C에서 24시간 동안 0, 10, 100µL·L-1 농도로 에틸렌 가스를 각각 주입하여 처리하였다. 처리 후 과실은 20°C에 저장하며 3일 간격으로 15일간 과실의 품질 변화를 조사하였으며, 처리 후 3일과 6일에 과실의 과심 부분을 이용하여 세포벽 분해와 에틸렌 생합성에 관련된 유전자 발현을 조사하였다.
과실 품질 분석
과실 품질 변화는 가용성 고형물 및 산 함량, 경도, 호흡률, 에틸렌 발생량을 조사하였다. 가용성 고형물 함량은 10개의 과실을 사용하여 cheese cloth로 감싸 착즙하여 과즙을 디지털 굴절 당도계(Pocket Refractometer, PAL-1, Atago, Japan)를 사용하여 측정하였다. 산 함량은 과즙 5mL에 증류수 35mL을 혼합하여 0.1N NaOH를 사용하여 pH 8.3까지 중화적정한 후 구연산으로 환산하여 표기하였고, 과실은 총 9개를 3개씩 3반복으로 측정하였다.
경도는 10개의 과실을 대상으로 2cm 두께로 횡단면을 잘라낸 후 경도계(RHEO TEX SD-700, Sun Scientific Inc., Japan)를 이용하여 8mm 원형 probe로 깊이 3mm로 과육 2회, 과심 1회를 측정하여 최대하중을 Newton(N) 값으로 환산하여 표기하였다.
과실의 호흡률과 에틸렌 발생량은 각 처리별 과실을 680mL 폴리프로필렌 밀폐용기(HPLC851, Locknlock, China)에 넣어 4시간 동안 밀폐시킨 후 상단부에서 가스 표본 1mL을 시험구당 3반복으로 포집한 다음 분석하였다. 에틸렌 가스분석은 HP PLOT Al2O3(Agilent, 50m×0.53mm, 15.00mm, CA, USA) 칼럼과 FID가 장착된 gas chromatograph(GC 7890B, Agilent Technologies, USA)를 사용하여 oven 100°C, injection 250°C, detector 250°C로 설정하여 측정하였고, 호흡률 측정은 Shincarbon-ST 50/80(Shinwa Chemical Industries LTD., 4.0m×3.0mm, Kyoto, Japan) 칼럼과 TCD를 장착한 gas chromatograph (GC 6890, Agilent Technologies, USA)를 이용하여 oven 100°C, injection 150°C, detector 150°C로 설정하여 측정하였다.
세포벽 분해 및 에틸렌 생합성 관련 유전자 발현
과실의 RNA 추출
과실의 RNA 추출은 CTAB(cetyl trimethyl ammonium bromide) 시약을 이용하였다. 마쇄 된 시료에 1mL의 CTAB을 넣고 68°C에서 1시간 용해시킨 후, 원심분리기를 이용하여 4°C, 15,000×g에서 15분간 원심분리 하였다. 상징액을 새 튜브에 옮긴 후 chloroform/isoamyl alcohol(24:1) 동량과 혼합하여 10분간 방치하였다. 원심분리기를 이용하여 4°C, 15,000×g에서 15분간 원심분리한 후, 상징액을 새 튜브에 옮긴 후 3M sodium acetate를 상징액의 1/10양을 첨가하고 isopropanol을 상징액의 7/10을 혼합한 뒤 4°C에서 20분간 침전시켰다. 다음으로 원심분리기를 이용하여 4°C, 15,000×g에서 20분간 원심분리하여, 침전된 찌꺼기를 제외한 용액을 제거하였다. 건조된 찌꺼기를 diethyl pyrocarbonate(DEPC)를 넣은 3차 증류수에 녹인 후 chloroform/isoamyl alcohol(24:1) 용액과 1:1로 혼합하여 10분간 방치하였다. 원심분리기를 이용하여 4°C, 15,000×g에서 15분간 원심분리하여, 상징액을 새 튜브에 옮긴 후 상징액의 1/10양의 sodium acetate와 상징액의 2배의 100% ethanol을 혼합하여 -20°C에서 16시간 침전시켰다. 침전 후 원심분리를 통해 튜브 안의 용액을 버린 후 70% ethanol을 튜브에 넣고 원심분리하여 찌꺼기를 세척한 후, 4°C, 15,000×g에서 5분간 원심분리하여, 최종적으로 찌꺼기를 얻게 되며, 상온에서 찌꺼기를 완전히 건조한 후 DEPC가 혼합된 3차 증류수 20µL에 녹여서 이후 실험에 이용하였다.
RNA 정량분석
RNA의 정량은 Colibri Microvolume Spectrometer(Dakara, Japan)를 사용하였다. 기기의 설정은 nucleic acid에서 sample type RNA-40, path lengths 자동으로 설정하였다. 정량을 위한 blank는 DEPC를 넣은 3차 증류수를 사용하였다. 추출한 RNA는 10%로 희석하여 측정하였다.
상보적 DNA의 합성
추출한 RNA에서 cDNA를 합성하기 위한 역전사 효소는 TOPscript™ RT DryMIX(Enzynomic, Korea)를 사용하였다. cDNA를 합성하기 위해 전체 RNA의 양은 시료당 1µg을 사용하였다. 1개의 튜브에는 총 20µL가 들어가며 1µg의 전체 RNA를 제외한 나머지 양은 DEPC가 포함된 3차 증류수를 넣었다. 역전사효소를 활성화하기 위한 반응은 42°C 5분, 역전사 반응은 42°C에서 60분, 반응 후 역전사효소를 불활성화하기 위한 반응으로 95°C, 5분을 설정하여 진행하였다.
프라이머 합성 및 중합효소연쇄반응 분석
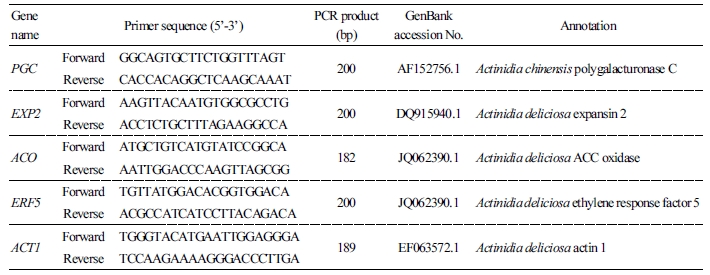
실험에 사용할 유전자들의 염기서열은 NCBI 웹사이트(https://www.ncbi.nlm.nih.gov/)를 이용하여 확인하였다. 특이적 프라이머의 제작은 Primer3Plus 웹사이트(http://primer3plus.com)를 이용하였다(Untergasser et al., 2012). 시료 mRNA 양을 보정하기 위한 내부 대조구로서는 actin의 유전자 발현량을 이용하였으며, 실험에 사용된 유전자 및 프라이머 정보를 Table 1에 정리하였다. PCR 분석은 Enzynomic사의 TOPsimple™ DryMIX-nTaq(10mM dNTP, Taq DNA 중합효소, 5mM MgCl2, 10×PCR 완충용액 포함)과 제작된 프라이머를 사용하여 각 cDNA를 주형으로 이용하여 실시하였다. PCR 반응액(총 20µL)에는 역전사된 cDNA 일정량(1µL)과 10pmole의 정방향 및 역방향 프라이머(각 0.5µL), 그리고 3차 증류수(18µL)를 포함시켰다. PCR 증폭은 94°C 5분을 개시로 94°C 30초 denaturation, 60°C 30초 annealing, 72°C 45초 extension의 조건으로 30 cycle 반복하였고, 최종산물은 1.2∼1.5% agarose gel 상에서 전기영동으로 확인하였다.
결 과
외생 에틸렌 처리에 따른 ‘골드원’과 ‘제시골드’ 키위프루트의 과실품질 변화
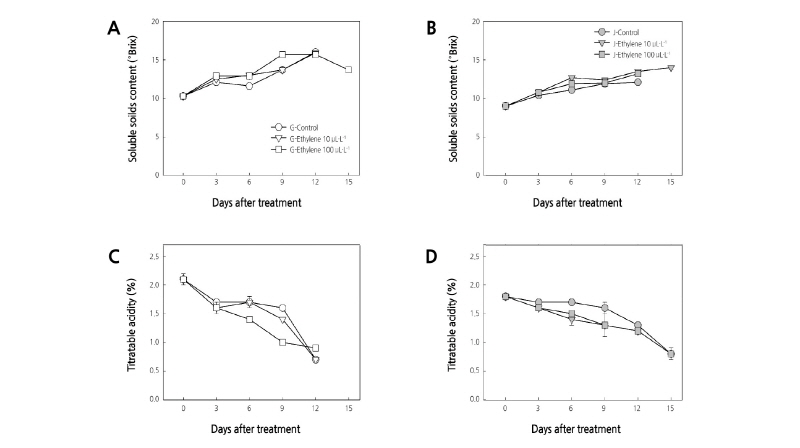
외생 에틸렌 처리에 따른 ‘골드원’과 ‘제시골드’ 과실의 가용성 고형물 함량과 산 함량은 외생 에틸렌 처리 과실에서 무처리 과실에 비해 빠르게 변화하였으며, 처리 농도가 높은 과실에 더욱 빠른 변화를 보였다(Fig. 1). ‘골드원’의 가용성 고형물 함량은 수확 당일 10.3°Brix에서 최대 16.0°Brix까지 증가하였고, ‘제시골드’는 9.0°Brix에서 최대 14.0°Brix까지 증가하였으며(Fig. 1A, 1B), ‘제시골드’ 과실에서 가용성 고형물 함량은 상대적으로 낮았다. 수확 당일 과실의 산 함량은 ‘골드원’이 2.1%로 ‘제시골드’의 1.8%보다 높았으나 과실 후숙이 진행됨에 따라 ‘골드원’ 과실에서 빠르게 감소하여 처리 후 12일에는 더욱 낮은 값을 보였다(Fig. 1C, 1D). ‘골드원’의 산 함량은 외생 에틸렌 처리 과실에서 무처리 과실보다 빠르게 감소하였으며, 특히 100µL·L-1 처리 과실은 처리 후 9일에 가식에 좋은 적정산도(1%) 이하로 빠르게 감소하였다. 반면 ‘제시골드’ 과실은 외생 에틸렌 처리 과실이 무처리 과실보다 산 함량이 빠르게 감소하였지만, 처리 과실과 무처리 과실 모두 처리 후 15일이 되어서야 산 함량이 1% 이하로 감소하였다. 그리고 ‘제시골드’ 과실은 외생 에틸렌 처리 농도에 따른 산 함량의 변화 속도에 차이를 보이지 않았다.
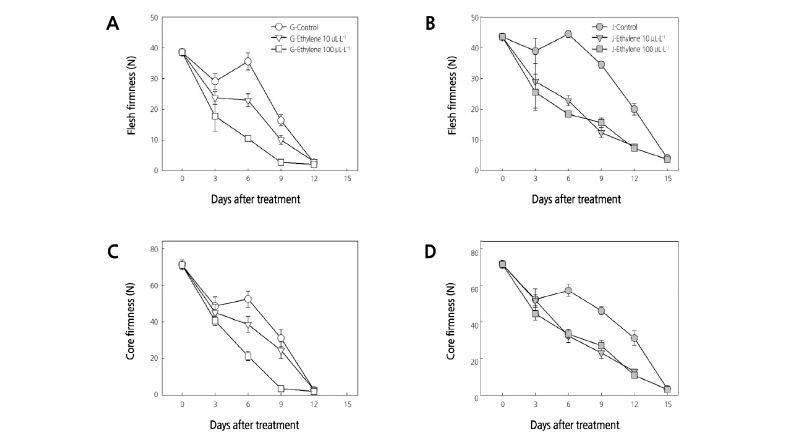
과실의 경도 변화는 두 품종 모두 외생 에틸렌 처리 과실에서 빠르게 감소하였으며 ‘골드원’이 ‘제시골드’보다 처리 농도에 따른 연화속도의 차이를 뚜렷하게 보였다(Fig. 2). ‘골드원’에 대한 외생 에틸렌 100µL·L-1 처리 과실은 수확 당일 과육은 38.6N, 과심은 71.3N이었으나 과육은 6일 후, 과심은 9일 후에 10N 이하로 연화되었고, 외생 에틸렌 10µL·L-1 처리는 그보다 각각 3일 늦은 시기에 10N 이하로 감소되어 연화되었다. ‘제시골드’ 과실에 대한 외생 에틸렌 100µL·L-1 처리는 수확 당일 과육 43.6N과 과심 71.7N에서 12일후에는 과육과 과심 모두 10N 이하로 감소하였다. 두 품종 모두 무처리 과실의 경도는 처리 후 6일까지 큰 변화가 없다가 이후 급격히 감소하였다.
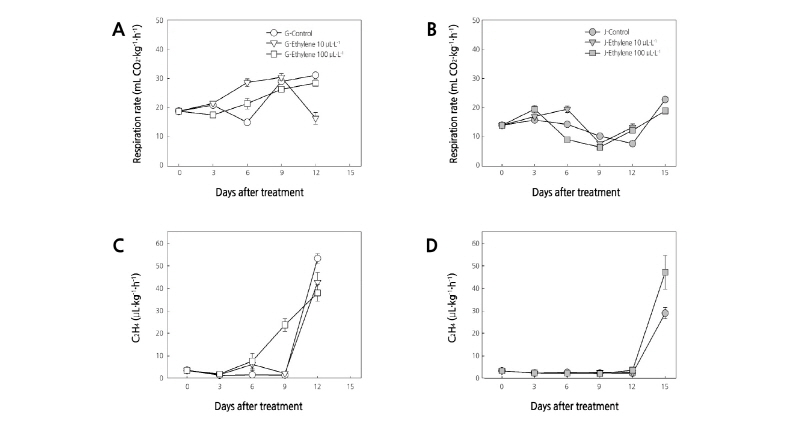
‘골드원’ 과실에 대한 외생 에틸렌 10µL·L-1 및 100µL·L-1 처리에 따른 과실의 호흡률은 처리 후 9일까지 계속해서 증가해 각각 44.0mL CO2·kg-1·h-1, 38.0mL CO2·kg-1·h-1을 보였다(Fig. 3A, 3B). ‘제시골드’ 품종의 호흡률은 외생 에틸렌 처리농도에 따른 차이가 뚜렷하지 않았다. 에틸렌 발생량은 ‘골드원’ 과실은 처리 후 6일에 외생 에틸렌 100µL·L-1 처리 과실에서 증가하기 시작하여 9일에는 34.3µL·kg-1·h-1로 무처리와 외생 에틸렌 10µL·L-1 처리 과실보다 발생량이 많았다(Fig. 3C, 3D). ‘제시골드’ 과실의 에틸렌 발생은 처리농도에 관계없이 모두 처리 후 15일부터 증가하였는데 외생 에틸렌 100µL·L-1 처리 과실은 68.3µL·kg-1·h-1로 무처리 42.0µL·kg-1·h-1보다 발생량이 많았다.
과실의 가용성 고형물 및 산 함량, 경도 그리고 과육색의 변화(Fig. 4)를 종합해보면 ‘골드원’, ‘제시골드’ 두 품종 모두 100µL·L-1 처리에서 빠르고 균일하게 후숙되었으며, 외생 에틸렌을 100µL·L-1로 처리하였을 때 각각 9일과 15일에 식용하기에 좋은 상태에 도달하였다.
외생 에틸렌 처리에 따른 ‘골드원’과 ‘제시골드’ 키위프루트의 유전자 발현 변화
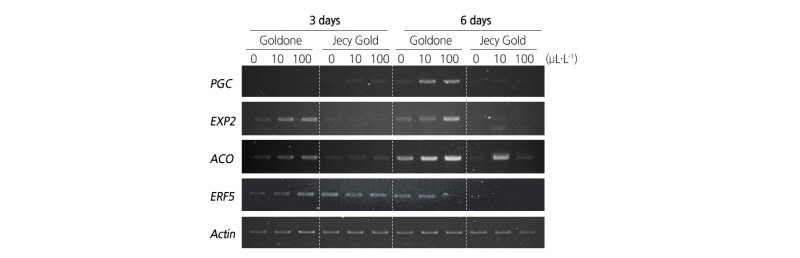
본 실험에서는 에틸렌 생합성 경로에서 최종적인 에틸렌 생합성량을 결정하는 ACO(ACC oxidase) 유전자와 에틸렌 신호절달에 관여하는 ERF5(ethylene response factor 5) 유전자, 세포벽 분해효소 중 세포 중층과 펙틴 분해에 관여하는 PGC (polygalacturonase C)와 펙틴 가용화를 유도하는 EXP2(expansin 2) 유전자 발현 정도를 비교하였다. 외생 에틸렌 처리 후 ‘골드원’과 ‘제시골드’ 과실의 유전자 발현을 분석한 결과, ACO, PGC, EXP2, ERF5에서만 유전자의 발현이 확인되었다(Fig. 5). 두 품종 간의 유전자 발현량은 ‘골드원’ 품종에서 더 높게 발현되었으며 외생 에틸렌 처리농도가 높은 과실에서 발현 수준이 높았다. 에틸렌 생합성과 관련된 ACO 유전자의 발현은 처리 후 3일보다 6일에서 증가하였고, 에틸렌 발생은 외생 에틸렌 100µL·L-1 처리가 10µL·L-1 처리보다 높았던 반면에, 유전자의 발현은 에틸렌 처리 농도와는 큰 차이가 없었다.
세포벽 분해와 관련된 PGC 유전자의 발현은 처리 후 3일까지 두 품종 모두 처리농도와 관계없이 낮은 수준을 유지하다가 외생 에틸렌 처리 6일후에 ‘골드원’ 품종의 과실에서만 증가하였다. PGC 유전자 발현은 다른 유전자보다 외생 에틸렌 처리농도에 따른 발현 수준 차이가 컸다. EXP2 유전자 역시 ‘골드원’ 품종에서만 발현 변화를 확인할 수 있었는데 무처리 과실의 경우 3일과 6일 사이에 큰 변화가 없었던 반면, 외생 에틸렌 처리 과실의 경우 처리 후 3일에서 6일까지 발현 수준이 증가하였다.
고 찰
외생 에틸렌 처리에 따른 황육계 키위프루트 과실의 품질 변화
본 연구는 외생 에틸렌 처리에 따른 키위프루트 과실의 후숙 특성을 이해하고, 국내 육성 품종에 적절한 외생 에틸렌 처리 농도를 구명하고자 수행하였다. 외생 에틸렌 처리에 따른 키위프루트 과실의 품질 변화는 외생 에틸렌 처리 과실이 무처리 과실보다 빠르게 변화하였으며 높은 처리농도에서 더욱 빠르게 변하였다. 외생 에틸렌 처리 농도에 따른 가용성 고형물 함량은 외생 에틸렌 처리 농도가 높은 과실에서 비교적 높은 가용성 고형물 함량을 보였다. 에틸렌 유사물질인 프로필렌을 처리한 ‘헤이워드’에서도 처리농도가 높은 과실에서 가용성 고형물 함량이 더욱 증가하였다고 보고되었다(Antunes et al., 2000).
과실의 산 함량 또한 두 품종 모두 외생 에틸렌 처리 과실에서 무처리 과실보다 빠르게 감소하였다. 프로필렌을 처리한 ‘사누키골드’, ‘홍양’ 역시 무처리 과실보다 처리 과실에서 산 함량이 빠르게 감소하였다(Mworia et al., 2011; Murakami et al., 2014). 키위프루트의 주요 유기산 구성은 구연산(40-50%), 퀸산(40-50%), 그리고 말산(10%)이며(Marsh et al., 2004), 후숙 과정 중 과실의 산 함량 감소는 구연산의 감소에서 기인하는 것으로 보고된 바 있다(MacRae et al., 1989; Marsh et al., 2004).
키위프루트에서 과실의 경도는 후숙 단계를 나타내는 지표로 사용되는데, 외생 에틸렌의 처리는 과실을 균일하고 빠르게 연화시킨다고 하였다(Redgwell et al., 1990; Redgwell et al., 1992; Redgwell et al., 1997; Schröder and Atkinson, 2006; Lim et al., 2017). ‘골드원’과 ‘제시골드’ 품종의 경도 역시 프로필렌을 처리한 다른 품종과 마찬가지로 외생 에틸렌을 처리한 과실에서, 그리고 처리농도가 높은 과실에서 빠르게 감소되었다(Antunes et al., 2000; Mworia et al., 2011; Murakami et al., 2014).
키위프루트는 외생 에틸렌 자극 없이는 자가촉매적 에틸렌 생합성이 유도되지 않으며(Antunes and Sfakiotakis, 2002; Park et al., 2006; Antunes, 2007; Jabbar and East, 2016) 외생 에틸렌 자극 없이 과실 내의 에틸렌이 대량 발생하게 되는 경우는 대부분 과실의 물리적인 손상과 병해충에 의한 것으로 알려져 있다(Jabbar and East, 2016; Asiche et al., 2017). 본 연구에도 대부분의 무처리 과실이 처리 과실보다 늦게 에틸렌 발생이 증가하거나 낮은 발생량을 보였다. 일반적인 호흡급등형 과실은 수확후 호흡과 내생 에틸렌 증가가 동시에 이루어지나 키위프루트는 호흡 증가 이후 자가촉매적 에틸렌 생합성이 증가한다(Antunes and Sfakiotakis, 2002; Antunes, 2007; Jabbar and East, 2016). 본 실험에서도 과실의 호흡 증가 후 에틸렌 증가를 확인할 수 있었다(Fig. 3).
대부분 호흡급등형 과실들은 외생 에틸렌 처리로 과실 후숙이 유도되며 과실의 맛과 풍미를 증가시킨다(Lim et al., 2017). 토마토를 비롯한 다양한 호흡급등형 과실에서 외생 에틸렌 처리는 과실의 감미와 풍미를 향상시키고, 경도와 산미를 감소시킨다(Saltveit, 1999). 또한 감, 카람볼라, 그리고 서양배 과실에서도 외생 에틸렌 처리를 통해 과실 연화, 가용성 고형물 함량의 증가, 탄닌의 분해 등의 풍미에 영향을 주는 생리·화학적 변화를 유도하여 식미 가치를 높인다(Kato, 1990; Miller and McDonald, 1997; Bower et al., 2003). 하지만 외생 에틸렌의 처리가 항상 긍정적인 변화만을 가져오는 것은 아니어서(Stern et al., 1994; Yamaguchi et al., 1997; Scriven et al., 1989) 멜론과 바나나의 경우 외생 에틸렌 처리 없이 자연적으로 후숙된 과실이 더 우수한 품질 상태를 보인다(Yamaguchi, et al.,1997; Scriven et al., 1989). 토마토 역시 외생 에틸렌 처리로 익힌 과실이 수체에서 자연적으로 익은 과실보다 휘발성 화합물 발생이 낮다고 한다(Stern et al., 1994). 하지만 키위프루트에서는 외생 에틸렌 처리가 과실 품질에 부정적인 영향을 주었다는 연구 결과는 아직 보고된 적이 없다(Lim et al., 2017). 최근의 연구 결과에 따르면 외생 에틸렌 처리 없이 저온 스트레스를 통해서도 키위프루트의 연화를 유도할 수 있다고 보고되었지만(Jabbar and East, 2016), 빠르고 균일한 과실 후숙을 위해서는 외생 에틸렌의 처리가 필요한 것으로 판단된다.
세포벽 분해와 에틸렌 관련 유전자 발현
본 연구에서는 외생 에틸렌 처리 후의 과실 품질 변화와 함께 세포벽 분해 관련 유전자와 에틸렌 관련 유전자발현을 조사한 결과, 후숙과정 중의 ACO(ACC oxidase), PGC(polygalacturonase C), EXP2(expansin 2), ERF5(ethylene response factor 5) 유전자의 발현 정도 변화를 확인할 수 있었다. 조사된 모든 유전자 발현은 ‘제시골드’ 과실에서 비교적 낮게 조사되었다.
키위프루트의 과실 후숙 과정 중 에틸렌은 매우 중요한 역할을 담당하고 있으며 에틸렌 생합성에 관련된 신호전달 효소 및 유전자 활성에 대한 다양한 연구들이 보고되었다(Antunes et al., 2000; Park et al., 2006; Murakami et al., 2014). Murakami et al.(2014)의 연구에서는 에틸렌 생합성과 관련하여 ACS1, ACO3유전자와 신호전달과 관련하여 EIL4(EIN-like), ERF14 (ethylene response factor) 유전자 발현을 함께 확인하였다. ACC oxidase는 에틸렌 생합성 경로에서 ACC를 에틸렌으로 산화시키는 효소로 외생 에틸렌을 처리한 ‘홍양’ 과실에서도 내생 에틸렌 발생 증가와 함께 ACO 유전자발현 수준이 증가하는 것을 확인할 수 있었다(Murakami et al., 2014). 또한 프로필렌을 처리한 ‘헤이워드’에서도 유사한 결과를 얻었다(Antunes et al., 2000).
세포벽 분해와 관련하여 PGC 유전자 발현은 ‘골드원’ 과실에서 처리 3일까지 매우 낮은 수준을 유지하다가 6일 후에 발현수준이 증가하였는데, 외생 에틸렌 처리농도가 높을수록 발현 수준이 높았다.
Wang et al.(2000)은 키위프루트 과실의 연화와 에틸렌 생합성 관계에서의 PG 유전자 발현을 조사하여 CkPGA, CkPGB, CkPGC의 3가지 유전자를 동정하였다. CkPGA와 CkPGB 유전자는 내생 에틸렌이 생합성되는 과실에서만 발현되었지만 CkPGC 유전자는 연화가 시작된 이후 지속적으로 강하게 발현되었다. 본 실험에서도 CkPGC와 함께 CkPGA와 CkPGB 유전자 발현을 조사하였으나, 연화 마지막 단계에서 발현되는 CkPGA, CkPGB 유전자의 발현을 확인할 수 없었다. 이는 실험에 사용된 과실의 연화 정도가 크지 않았기 때문으로 판단되었다.
‘제시골드’ 과실은 ‘골드원’ 과실과 비교하여 전체적으로 낮은 PGC 발현 수준을 보였으며, 그 결과 ‘제시골드’가 ‘골드원’보다 연화 속도가 늦게 진행되는 것으로 판단된다. Lee et al.(2014)에 따르면 ‘해향’과 ‘한라골드’ 과실에서는 PG 활성이 과실 연화에 미치는 영향이 제한적일 것으로 추정하였지만 ‘골드원’ 과실에서는 연화에 대한 PGC의 역할이 중요할 것으로 생각된다.
EXP2 유전자 발현은 ‘골드원’ 과실은 3일후보다 6일후의 과실에서 발현이 증가하였으며 외생 에틸렌 처리 농도가 높을수록 발현 수준이 증가하였다. Expansin은 직접적인 세포벽의 중층을 가수분해하지는 않으나 세포벽 중합체와의 결합을 도와 가수분해를 가속화하는 역할을 한다(Rose et al., 1997; Cosgrove, 1999; Mworia et al., 2011). ‘사누키골드’ 과실에서도 프로필렌 처리로 EXP 유전자발현이 증가하는 것이 확인되었다(Mworia et al., 2011).
이상의 결과를 종합해 보면, ‘골드원’, ‘제시골드’ 과실은 100µL·L-1 처리로 각각 9일과 15일에 식용 가능한 상태로 후숙되었다. ‘제시골드’ 과실은 상대적으로 ‘골드원’ 과실과 비교하여 외생 에틸렌 처리에 둔감한 반응을 보였다. 황색 과육 키위프르트와 달리 녹색과육 키위프루트 A. deliciosa ‘헤이워드’ 품종은 외생 에틸렌 1,000µL·L-1 처리 후 20°C에서 9일차에 먹기에 적절한 상태에 도달하였고(과심경도 < 10N), A. deliciosa ‘감록’ 품종의 경우는 동일 조건에서 6일이 걸리는 것으로 조사되었다(Shin et al., 2017). 현재 국내에서는 키위프루트 과실의 후숙을 위해 간이 에틸렌 발생제를 이용하고 있다(Lim et al., 2016). 그러나 새로운 품종의 고품질 후숙과실 생산을 위해서는 각 품종에 대한 적정한 외생 에틸렌 처리가 이루어질 필요가 있으며 외생 에틸렌 처리 이후의 품질 유지 기술에 대한 연구가 추가적으로 이루어져야 할 것으로 판단된다.