서 언
재료 및 방법
고춧가루 시료
ASTA-20 분석
Vis/NIR 초분광 분석
Vis/NIR 초분광 분석 스펙트럼 전처리
ASTA 값 예측 모델 개발
결과 및 고찰
ASTA-20 방법을 이용한 고춧가루 색도 측정
Vis/NIR 초분광 분석법을 이용한 ASTA 값 예측모델 개발
ASTA-20 방법 및 Vis/NIR 초분광 분석법 비교
서 언
고추(Capsicum spp.)는 전 세계적으로 가장 많이 소비되는 채소 중 하나로 한 해에 약 200억 달러가 생산되고 있다(FAO STAT, 2012). 고추는 과실 모양과 크기, 색이 다양하고 매운맛을 내는 물질인 capsaicin을 함유하고 있어 생과 및 건과가 식재료, 식품 첨가물, 양념 등의 용도로 활용된다. 특히 건고추는 아시아 국가의 각종 양념에 활용되고 있어 세계적으로 생산되는 31억 달러 중 약 65%가 아시아 지역에서 생산된다(FAO STAT, 2012). 한국에서는 건고추를 분쇄한 고춧가루를 각종 식품에 첨가하여 사용하고 있으며 맛, 색, 향 등이 품질을 결정하는 주 요인으로 알려져 있다. 고춧가루의 색도는 궁극적으로 식품의 외관에 큰 영향을 미치며, 이는 고춧가루에 포함된 카로티노이드에 의해 나타난다. 고추의 카로티노이드는 붉은 색을 띠는 capsanthin, capsorubin, 주황색인 β-carotene, 노란색인 zeaxanthin 등이 대표적이며 각 카로티노이드의 조합에 따라 과실 색이 결정된다(Rodriguez- Uribe et al., 2012; Wahyuni et al., 2011). 특히 capsanthin의 경우 고추에 가장 많이 포함되어 있는 물질로서 고추 과실의 색도에 가장 큰 영향을 미친다.
고추 과실의 색도를 측정하기 위해서 용매를 이용하여 카로티노이드 추출 후 high-performance liquid chromatography (HPLC) 또는 thin layer chromatography(TLC)로 분석하는 방법이 개발되어 사용되고 있다(Hernandez-Ortega et al., 2012; Lee et al., 2005; Minguez-Mosquera and Hornero-Mendez, 1993). HPLC와 TLC 방법은 성분 별 함량을 정확하게 분석할 수 있다는 장점이 있으나 전처리 과정이 복잡하고, 분석에 상당한 시간과 비용이 든다. 따라서 다수의 시료에 대한 색도를 상대적으로 비교할 때에는 ASTA-20 분석법이 많이 사용된다(Minguez-Mosquera et al., 1992; Mo et al., 2015; Tepic and Vujicic, 2004). ASTA-20 분석법은 카로티노이드 추출을 바탕으로 하는 분석법 보다 간단하며 HPLC로 측정한 카로티노이드 함량, 특히 capsanthin 함량과 높은 상관관계를 보인다(Lee et al., 2004). 하지만 하나의 시료를 분석하는 데 소요되는 시간이 16시간 이상이며, acetone을 사용하기 때문에 후드에서 색소를 추출해야 하며 분석 후 폐액이 발생한다.
최근에는 visible/near infrared(Vis/NIR) 초분광 영상 기술을 이용한 비파괴 측정기술이 원예작물, 곡물 등의 종자 발아율 확인, 당도 측정, 경도 측정, 성숙도 측정 등에 활용되고 있다(Ahn et al., 2012; Fox and Manley, 2014; Gowen et al., 2007). 이 기술은 분광기술과 영상기술이 융합된 기술로 일반적인 분광분석장비가 대상물 전체에 대한 평균적인 분광정보만을 제공하는 것과 달리 대상물의 세부 공간영역에 대한 물리, 화학적 정보를 획득하여 분석할 수 있다는 장점이 있다. 또한 기존의 분석법에서 사용하던 물질 추출 단계를 요구하지 않기 때문에 고춧가루 색도 측정에도 활용 가능하다.
본 논문에서는 ASTA-20 분석법에 요구되는 다량의 시약과 긴 분석 시간을 절약하고, 효율적으로 고춧가루 색도를 측정하는 방법을 개발하고자 하였다. 총 488점 샘플에 대한 ASTA-20 분석 결과와 Vis/NIR 초분광 분석 결과를 비교하여 Vis/NIR 초분광 분석법을 이용한 색도 측정 모델을 확립하였다. Vis/NIR 초분광 분석법으로 예측한 ASTA 값은 ASTA-20 분석 결과와 유의성 있는 상관관계를 보였으며, 분석 소요 시간을 획기적으로 시간을 절약하였다.
재료 및 방법
고춧가루 시료
국내 종자회사에서 육성한 451개의 육성 계통 및 6개 종자회사[㈜농우바이오, 한국다끼이㈜, 바이엘 크롭사이언스㈜, 사카타코리아㈜, 신젠타코리아㈜, ㈜코레곤, 아시아종묘㈜]의 시판 품종 시료 37점을 포함하는 488점의 고춧가루를 이용하였다(Table 1; Supplementary Table 1 and 2). 시판 품종은 주로 고춧가루를 생산하기 위해 재배되는 대과종 중 고색도 품종인 농우바이오의 ‘나잘난’과 색도 이외의 품질이 우수한 열한개의 품종을 선발하였다. 코레곤의 ‘PR 케이스타’와 농우바이오의 ‘PR 스마트’ 품종을 제외한 10개의 시판 품종의 경우 노지의 서로 다른 위치에서 반복 재배하여 고춧가루 색도를 측정하였다. 식물은 모두 태국에서 재배한 후 양건하였다. 이후 과실을 품종 당 3개씩 수확하여 종자를 제거한 후 과실자루가 붙어있는 과실 꼭지 및 과실 끝 부분을 자르고 가운데 부위만을 취하여 분쇄하였다. 고춧가루는 밀봉하여 4°C 냉장고에 밀봉하여 암소에 보관하였다.
ASTA-20 분석
고춧가루의 색도는 알려진 ASTA-20 분석법에 따라 다음과 같이 측정하였다(Minguez-Mosquera, Jaren-Galan and Garrido-Fernandez, 1992). 0.1g의 고춧가루 시료를 갈색 250 mL 병에 담고 100mL의 공업용 acetone(덕산과학, 서울, 대한민국)을 넣어 16시간 동안 상온에서 보관하였다. 처음 acetone을 넣었을 때와 16시간 후에 한번씩 병을 흔들어 주었다. 이후 UV-Vis spectrophotometer UV-2550(Shimadzu, Seoul, Korea)를 이용하여 460nm의 흡광도를 측정하였다. ASTA 값은 다음 식에 따라 계산하였다.
If값은 1로 보았으며 고춧가루 무게는 소수점 이하 셋째 자리까지 계산하였다.
Vis/NIR 초분광 분석
실험에 사용한 초분광 영상 시스템은 EMCCD(Electron multiplying charge-coupled device) 카메라(Luca RDL-604M, Andor Technology, USA), imaging spectrograph(VNIR/SWIR, Headwll photonics, Fitchburg, MA, USA), 그리고 시료 이송을 위한 linear travel translation stage(XNN10-0180-M02-21, VELMEX INC, USA)로 구성되어 있다. 광원은 100W 할로겐 램프 6개를 fiber optic을 이용하여 시료에 고르게 조명되도록 구성하였다. 제어 소프트웨어는 Visual Basic 6.0을 기반으로 운영되며, 카메라의 노출시간에 따라 step motor를 구동하여 측정하는 라인스캔 방식을 적용하였다. 획득된 초분광 영상 데이터는 502 × 1000 픽셀의 총 128개 파장별 영상으로 구성되었으며 파장은 400-1,000nm 범위였다. 약 0.5g의 고춧가루를 직경 2cm 플레이트에 놓은 후 위의 영상 시스템에서 초분광 영상을 획득하였다.
Vis/NIR 초분광 분석 스펙트럼 전처리
분광분석 장비로부터 획득된 원본 스펙트럼은 기기 및 외부 환경 조건의 변화에 따라 보정이 필요하다. 특히, 고춧가루를 비롯한 농산물과 같은 외부 형상이 고르지 못한 시료의 측정이나, 시간에 따른 광원의 세기 변화는 심한 스펙트럼의 편차를 발생시킨다. 따라서, 시료로부터 정확한 스펙트럼 정보를 얻기 위해 다양한 스펙트럼 전처리 통계분석 방법이 사용된다. 본 연구에서는 정규화 방법(mean, maximum, and range normalization), 광산란을 보정하기 위한 multiplicative scatter correction(MSC)와 standard normal variate(SNV), 스펙트럼의 미소변화 강조를 위해 savitzky-golay 방법을 적용한 Vis/NIR 초분광 스펙트럼을 활용하였다.
ASTA 값 예측 모델 개발
고춧가루의 ASTA 값을 예측하는 모델을 개발하기 위하여 회귀분석 방법인 부분최소자승법(PLS)을 사용하였다. 부분최소자승법은 다중회귀분석 방법 중 하나로 하나의 종속변수를 예측하기 위하여 여러 개의 독립변수를 활용하여 직선 모델을 개발하는데 활용한다(Wold et al., 2001). 초분광 영상 데이터로부터 추출한 스펙트럼 데이터와 ASTA-20 방법을 통해 획득한 고춧가루의 ASTA 값을 동시에 고려하여 모델을 개발하였다. 총 488개의 고춧가루 시료 중 366개의 시료를 이용하여 모델을 개발하였다. 모델 개발은 전처리를 하지 않은 스펙트럼 데이터와 여섯 가지의 전처리 방법을 거친 데이터 각각의 방법에 대해 이루어졌다. 데이터 분석은 MATLAB(version 7.0.4, Mathworks, Natick, MA, USA) 프로그램을 사용하였다. 부분최소자승법(PLS) 모델 개발에 사용한 식은 다음과 같으며, 각 파장대에서 획득한 이미지가 갖는 beta coefficient를 계산하여 모델을 개발하였다.
Expected ASTA value = 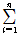 WiHi + constant
WiHi + constant
Wi : beta coefficient
Hi : the image at ith wavelength of a total of n spectral images
Constant: beta coefficients constant
그리고, 488개의 고춧가루 시료 중 모델 개발에 사용하지 않은 122개의 시료를 이용하여 개발한 모델을 검증하였다.
결과 및 고찰
ASTA-20 방법을 이용한 고춧가루 색도 측정
국내 고추 품종의 색도 분포를 확인하기 위하여 6개 종자 회사의 12개 시판 품종의 고춧가루 색도를 ASTA-20 방법으로 측정하였다(Table 1). 총 12개 품종 중 6개 품종의 ASTA 값이 100 이상으로 비교적 색소 함량이 높았다. 이 중 고색소 품종으로 판매되는 농우바이오 ‘나잘난’의 평균 ASTA 값이 124로 가장 높은 색도를 보였다. 색도의 변이가 가장 컸던 품종은 농우바이오의 ‘빅스타’로, ASTA 값이 57에서 138의 범위에서 나타났다. 이와 같은 동일 품종 내의 ASTA값 변이는 과실의 수확시기, 착과 위치, 시료의 햇빛 노출 시간 등에 의해 나타난 것으로 판단된다(Kim et al., 2002; Kim et al., 2008).
색도가 고춧가루의 중요한 품질 결정 요인임에도 불구하고 국내에서 판매되고 있는 고색도 품종이 많지 않으며 실제 ASTA-20 방법으로 측정한 시판 품종들의 ASTA 값도 46에서 147까지 넓게 분포하였다. 따라서 본 연구에서는 낮은 ASTA 값에서부터 높은 ASTA 값을 갖는 시료를 사용함으로써, 보다 넓은 범위에서 ASTA 값을 예측할 수 있는 새로운 분석 방법을 개발하고자 하였다. 이를 위하여 국내 종자 회사 육성 계통의 ASTA 값을 측정하였다(Supplementary Table 1 and 2). ASTA 값은 20-146에 분포하였으며 평균값은 66으로 나타났다. 따라서 Vis/NIR 초분광 분석법으로 ASTA 값을 예측하기 위한 모델식 개발은 시판 품종과 육성 계통의 고춧가루 시료를 모두 이용하여 ASTA 값 20-148 범위에서 이루어졌다.
Vis/NIR 초분광 분석법을 이용한 ASTA 값 예측모델 개발
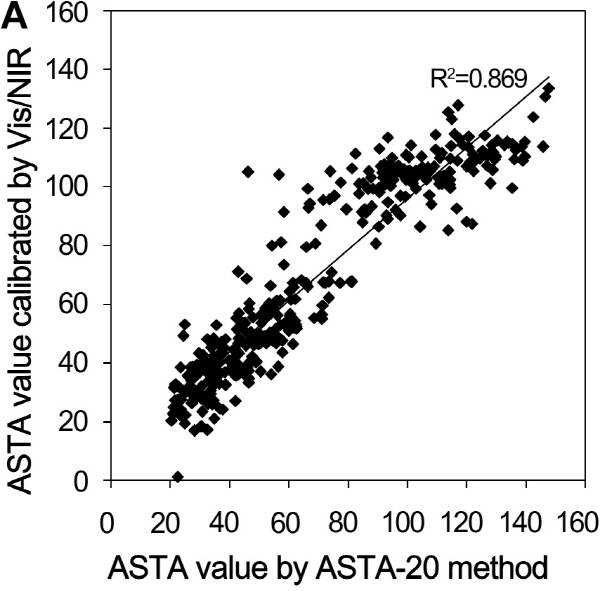
ASTA-20 방법과 Vis/NIR 초분광 분석법의 상관관계를 알아보기 위하여 488점의 시료 중 366점의 시료를 무작위적으로 선발하였다. 366점 시료의 ASTA 값은 최소 20에서 최대 148까지 연속적으로 분포하였다(Supplementary Table 1). 이후 Vis/NIR 초분광 분석법을 이용하여 선발한 시료의 스펙트럼 데이터를 획득하고, 스펙트럼 데이터에 6가지의 전처리 방법을 적용함으로써 두 분석법의 상관관계(Rc2) 및 보정오차를 전처리 전과 비교하였다(Table 2). 가장 낮은 상관관계와 가장 높은 상관관계 값은 maximum-normalization과 mean-normalization 전처리 방법을 통해 얻었으며 그 값은 0.853에서 0.869로 큰 차이를 보이지 않았다(Table 2). 이는 고춧가루 시료의 입자 표면, 광원의 세기 변화 등의 외부 조건이 Vis/NIR 초분광 분석법으로 스펙트럼 데이터를 획득하는 데에 큰 영향을 미치지 않았음을 보여준다. 한편, 두 분석법의 상관관계(Rc2)가 0.869로 가장 높고 보정오차 값이 12.647로 가장 낮은 mean-normalization 방법으로 전처리 후 각 파장대별 beta coefficient를 획득하여 최종적인 PLS 모델을 개발하였을 때(Supplementary Table 3), PLS 모델을 이용하여 보정된 ASTA 값과 ASTA-20으로 측정한 ASTA 값의 상관관계가 가장 높고, 값의 차이가 가장 적었다(Fig. 1A; Supplementary Table 1).
|
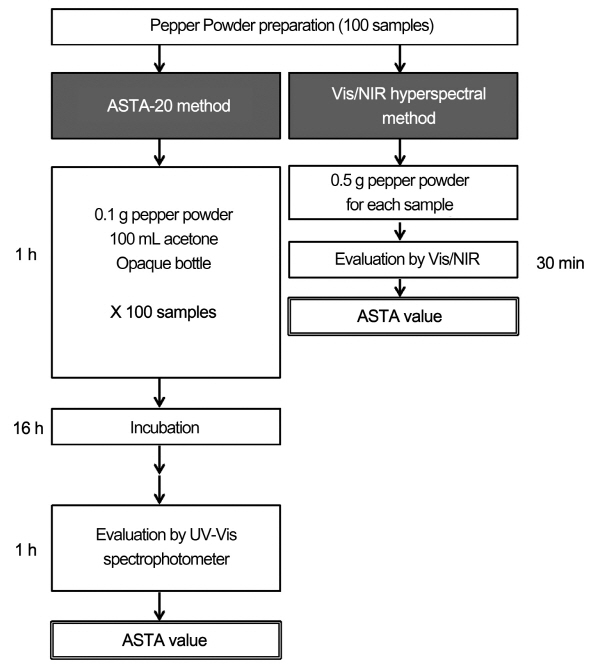
Fig. 2. Comparison of ASTA-20 and Vis/NIR hyperspectral methods. Time for each step is indicated beside a box. |
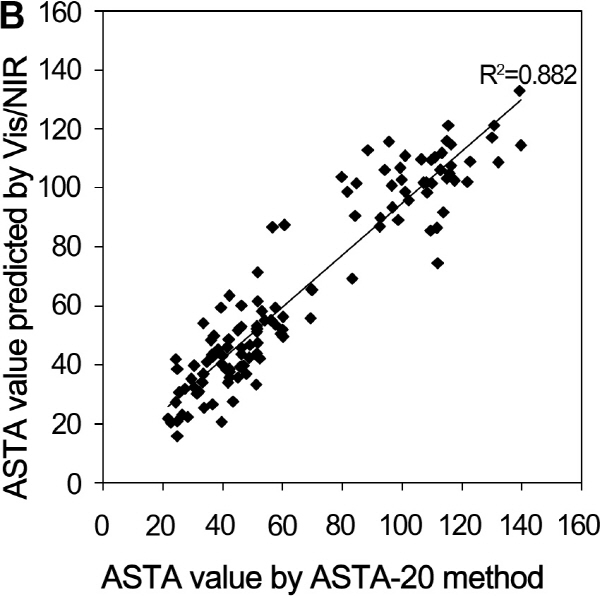
개발된 모델을 검정하기 위해 122개의 시료로부터 색도를 ASTA-20 방법과 Vis/NIR 초분광 분석법으로 각각 측정하였다. ASTA-20 방법에 의한 ASTA 값은 최소값 22에서 최대값 140 범위 내에 있었으며, Vis/NIR 초분광 분석법에 의해 획득된 시료의 스펙트럼 데이터는 모델식 개발에 이용한 mean-normalization 방법을 적용하여 ASTA 값을 얻었다(Supplementary Table 2). 그 결과 두 분석법으로 확인한 ASTA 값의 상관관계(R2)가 0.882로 높게 나타났다(Fig. 1B). 이는 본 모델이 저색도에서 고색도, 육성 계통 및 시판 품종의 ASTA 값 측정에 활용될 수 있음을 보여준다.
ASTA-20 방법 및 Vis/NIR 초분광 분석법 비교
Vis/NIR 초분광 분석 결과와 ASTA-20 방법으로 측정한 ASTA 값이 보인 유의성 있는 상관관계는 고춧가루 색도 측정에 Vis/NIR 초분광 분석법을 활용할 수 있음을 보여준다. Vis/NIR 초분광 분석법의 가장 큰 장점은 분석 시간이 짧다는 것이다. 한 명의 연구자가 100개의 시료에 대한 ASTA 값을 ASTA-20 방법으로 측정한다고 하였을 때 소요되는 시간은 약 18 시간이었던 반면 Vis/NIR 초분광 분석법의 경우 30분 내외에 분석을 마칠 수 있어 약 50배의 시간이 절약되었다(Fig. 2). ASTA-20 방법은 분석 시간이 길다는 점 이외에도 휘발성이 높은 아세톤을 처리하는 과정에 흄후드가 필요하고, 빛을 차단하는 불투명한 병이 100개 이상 필요하며, 전처리 시 이를 보관할 장소가 필요하다는 단점이 있다. 또한 분석 시간 이외에도 병의 재활용을 위해 폐액을 버리고, 병을 닦는 데 걸리는 시간과 노동력도 상당하다. 반면 Vis/NIR 초분광 분석법의 경우 흄후드, 불투명 병 등이 필요하지 않으며 폐시약이 발생하지 않는다는 장점이 있다.
본 연구는 보다 간편하고 빠르게 고춧가루의 색도를 다량으로 분석할 수 있는 새로운 방법을 제시하였으며, 개발한 Vis/NIR 초분광 분석법은 다수의 육성 계통 및 품종의 색도 분석에 유용하게 사용할 수 있다. 또한 넓은 ASTA 값 범위에 적용 가능하기 때문에 색도와 관련이 있는 새로운 품종을 개발하기 위해서도 활용할 수 있다.