서 언
재료 및 방법
식물 재료
RGEN(RNA-guided engineered nuclease)의 선정
CRISPR/Cas9 이용 벡터 구축
형질전환 토마토 육성 및 도입확인
Single Copy 선발 및 염기서열 분석을 통한 변이체 확인
에틸렌 생산량 측정
결과 및 고찰
sgRNA 디자인 및 CRISPR-Cas9 벡터 구축
형질전환체의 육성과 T-DNA 도입 확인 및 Single Copy 선발
유전자 편집 확인 및 에틸렌 생산량 분석
서 언
과실은 착과되어 시간이 경과됨에 따라 성숙에 따른 다양한 생리적 변화를 초래한다. 따라서 수확 후 과실의 신선도 및 품질을 유지하기 위한 기술개발이 다양한 측면에서 시도되어 왔다. 특히 과실 성숙에 관한
분자메커니즘, 세포벽 및 대사체 연구, 에틸렌 생합성 경로 및 응답반응 등에 대해 지난 20년간 많은 연구 성과를 보였다(Giovannoni, 2001). 식물을 위해 대기에서 활동하는 유일한 호르몬인 에틸렌(ethylene)은 식물의 생장과 분화, 환경응답에 중요한 역할을 담당하고 있다. 토마토, 사과, 바나나, 배 등과 같이 과실성숙을 위해 에틸렌이 반드시 필요한 것을 호흡급등형 과실(climacteric fruit)이라고 말하며, 이들은 에틸렌 생성이 과실 성숙개시 직전에 시작하여 과실성숙을 제어하며, 잎이나 꽃의 노화, 낙엽 및 낙과, 근모의 발생 등과 같은 생리적 요인에 관여하고 있다(Hiwasa et al., 2003). 또한 에틸렌은 과실성숙에 관련된 유전자 및 병원균의 감염 후 응답에 관여하는 유전자 등 다양한 유전자들의 발현을 제어하고 있다(Oeller et al., 1991). 과실성숙에 동반하여 생성한 에틸렌은 chlorophyll 분해관련 유전자, 카로티노이드 합성효소 등 색소합성에 관련된 유전자, 과육연화를 일으키는 세포벽 분해 관련 유전자 등의 발현을 유도 및 활성화시킨다고 보고되고 있다(Trebitsh et al., 1993; Alexander and Grierson, 2002; Hiwasa et al., 2003; Marty et al., 2005).
과실은 성숙을 동반하여 호흡량의 변화를 지표로, 성숙 이전에 특이적으로 호흡이 상승되는 호흡급등형(climacteric)과 호흡 및 에틸렌 생성이 상승하지 않는 호흡비급등형(non climacteric)으로 대별된다. 에틸렌 생합성 및 에틸렌 억제제를 이용한 호흡급등형 과실의 분석(Yang and Hoffman, 1984), 에틸렌 생합성 관련 유전자의 발현을 억제한 형질전환 식물에서의 분석(Klee et al., 1991; Oeller et al., 1991; Picton et al., 1993) 또는 에틸렌 수용체와 관련된 토마토 돌연변이 Never-ripe(Nr) (Tucker et al., 1984; Lanahan et al., 1994; Wilkinson et al., 1995; Yen et al., 1995) 등의 연구에서 과실 성숙이 현저하게 억제되며, 과실 성숙에 에틸렌의 작용이 필수적인 것으로 확인되었다. 호흡급등형 과실은 일정한 발달 단계에 도달하면 미숙한 단계에서 수확해도 시간이 경과하면 인공적으로 에틸렌 처리를 하지 않아도 스스로 에틸렌을 생산하고 성숙한다. 이러한 수확 후 성숙 현상은 maturation과 구별하여 ripening이라고 한다. 호흡급등형 과실은 성숙과 함께 호흡 활성이 일시적으로 급증한다. 이 급증하여 생성하는 에너지는 세포벽에 의한 연화, 착색, 향기 성분의 생성, 전분의 당으로 분해 및 유기산 감소 등의 다양한 성분 변화로 이루어진 과실의 성숙 현상의 진행에 사용된다고 생각되고 있다.
농산물의 숙성은 제품의 신선도와 품질에 큰 영향을 미친다. 숙성에 의한 변화는 과실의 품종에 따라 차이가 있지만 일반적으로 세포벽의 초미세 구조 및 조성이 변화하고 전분에서 설탕으로의 전환이 촉진되어 병원균에 대한 감수성이 높아져 질병에 감염되기 쉬운 상태가 된다(Seymour et al., 1993). 또한 색소의 생합성 변화 및 축적 또는 맛에 관련된 물질과 휘발성 방향족 화합물의 증가 등 큰 변화가 일어난다고 하였다(Rhodes, 1980; Seymour et al., 1993).
호흡급등형 토마토는 과실 발육 및 성숙에 대한 연구와 교배 및 종자 채취가 용이하여 모델식물로 많이 사용되고 있다(Yen et al., 1995; Chung et al., 2010). 특히 토마토의 성숙에 관련된 자연 돌연변이 rin 및 nor 토마토는 호흡급등형처럼 급격한 호흡 활성의 촉진이 일어나지 않고, 에틸렌 생합성도 일어나지 않는다. 이들 변이체를 이용하여 에틸렌 처리 후, 에틸렌 관련 유전자의 발현 유도(Tigchelaar et al., 1978; Yen et al., 1995) 및 rin과 nor 토마토에서 상해에 대한 반응으로 에틸렌 합성이 유도(Lincoln and Fischer, 1988) 된다고 알려졌다. 최근 들어 rin 및 nor 토마토의 성숙되지 않는 원인 유전자가 분리되었다. 토마토 rin 돌연변이는 MADS-box 전사인자에 속하는 LeMADS-RIN유전자의 exon 부분이 결실되어 있는 것으로 나타났다(Vrebalov et al., 2002; Giovannoni, 2004). nor 돌연변이체에서는 nor locus 내부에 하나의 전사 인자 구조의 특징을 가진 비 MADS-box 패밀리인 전사인자가 존재하고 있는 것으로 알려졌다(Alvarez-Buylla et al., 2000; Vrebalov et al., 2002).
토마토의 돌연변이체를 이용한 연구는 성숙에 관련된 유전자의 발현이 제어되어 형질로서 나타난 것으로부터 형질관련 유전자를 동정하고 열매 성숙 생리 연구에 상당한 기여를 하고 있다(Vrebalov et al., 2002; Manning et al., 2006 ; Giovannoni 2007; Matas et al., 2009; Wang et al., 2009; Chung et al., 2010; Nashilevitz et al., 2010; Karlova et al., 2011). 또한 최근의 토마토 연구로는 전사체 분석(Alba et al., 2005; Lemaire-Chamley et al., 2005; Carrari et al., 2006; Vriezen et al., 2008; Wang et al., 2009), 프로테옴 분석(Saravanan and Rose, 2004; Faurobert et al., 2007; Page et al., 2010), 및 대사체 분석(Roessner- Tunali et al., 2003; Carrari and Fernie, 2006; Fraser et al., 2007; Moco et al., 2007) 등에 따라 토마토의 생리적 현상들의 포괄적인 분석이 이루어져 다량의 데이터가 축적되고 있으며, 토마토 유전자 재조합 기술에 의해 ACC(1-aminocy-clo-propane- 1-carboxylic acid) 합성효소와 ACC 산화효소의 발현을 억제함으로써 에틸렌 생산량이 저하된 형질전환체를 육성하여 확인하였다(Chung et al., 2010; Ma et al., 2014; Wang et al., 2017). 따라서 토마토의 성숙시작에 에틸렌이 필수적인 것은 분명하지만, 개별 성숙 관련 유전자의 발현이 에틸렌을 직접 통제하거나 간접적인 제어에 의한 것인지는 분명하지 않다.
토마토 성숙 관련 돌연변이 rin과 nor의 분석에서 LeMADS-RIN 및 NOR 등 에틸렌 이외에도 성숙 현상에 필수인자도 알려져 있다(Wang et al., 2017). 다수의 성숙 관련 유전자가 에틸렌과 RIN 및 NOR 신호전달계에 의해 교묘하게 제어된 것으로 간주하고 있지만, 그 자세한 것은 아직까지 분명하지 않다. 따라서 본 연구에서는 토마토 과실 성숙 관련 LeMADS-RIN 유전자를 CRSPR/Cas9(Clustered Regularly-Interspaced Short Palindromic Repeats/CRISPR associated protein 9) 시스템을 적용하여 인위적으로 유전자를 편집하여 에틸렌 생산과의 관계를 구명하고자 하였다. 아울러 토마토에서 유전자 편집기술을 쉽고 빠르게 할 수 있는 방법을 함께 제공하고자 하였다.
재료 및 방법
식물 재료
토마토(Solanum lycopersicum L.) 품종은 TYLCV(Tomato Yellow Leaf Curl Virus)계 ‘마미리오(Mamirio)’와 β-caro-tene 함량이 높은 ‘골든벨(Golden Bell)’ 품종을 사용하였다. 토마토 종자는 70% ethanol과 2% 차염소산나트륨으로 소독한 후 멸균수로 3회 세척하여 MSR3배지에 파종하고, 23±2°C 배양실에서 10-14일간 무균배양 후 자엽을 잘라서 형질전환에 사용하였다. 재분화된 식물체는 포트로 이식하여 후대를 육성하였고, 토마토 잎은 잘라서 FavorPrepTM Plant Genomic DNA Extraction Mini kit(Favorgen Biotech Corp., Taiwan)를 이용하여 genomic DNA를 추출하였다.
RGEN(RNA-guided engineered nuclease)의 선정
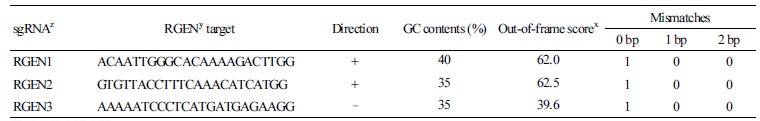
토마토 과실 성숙 관련 LeMADS-RIN(accession no. AF448522) 유전자의 편집을 위하여 http://ensembl.gramene.org/Sola num_lycopersicum/Info/Index사이트로부터 토마토 유전자의 게놈 정보를 확인하고(Gene: Solyc05g012020.2), CRISPR RGEN tools(http://www.rgenome.net/cas-designer/)을 이용하여 sgRNA(single guide RNA)를 디자인하였다(Park et al., 2015). RGEN은 CRISPR/Cas9 효소가 인식하는 PAM(Proto-Spacer Adjacent Motif) 영역인 5’-NGG-3’ 서열을 제외한 20bp 크기의 염기로 구성된다. 이렇게 얻어진 sgRNA들은 mis-match 1, 2에서 off-target이 제거된 list 1-0-0으로 나온 것과, 30-70% 사이의 GC 함량으로 구성되고, out-of-frame score가 높은 것 순으로 RGEN을 선정하였다(Table 1).
CRISPR/Cas9 이용 벡터 구축
토마토 형질전환을 위한 Ti-plasmid 벡터, pBAtC는 CRISPR/Cas9효소가 CaMV 35S 프로모터에 의해 제어되며, sgRNA는 AtU6 프로모터에 의하여 작동되도록 구축한 기본 벡터를 이용하였다(Kim et al., 2016). CRISPR RGEN tools로부터 선정된 3개의 RGEN은 유전자를 합성한 후 제한효소 AarI을 사용하여 pBAtC 벡터에 삽입하여 완성하였다(Jung et al., 2017). 구축된 Ti-plasmid 벡터는 각각 Agrobacterium tumefaciens LBA4404 균주에 형질전환하여 이용하였다. 토마토에 형질전환시켜 얻어진 식물체의 선발 마커는 Bar 유전자를 이용하였다.
형질전환 토마토 육성 및 도입확인
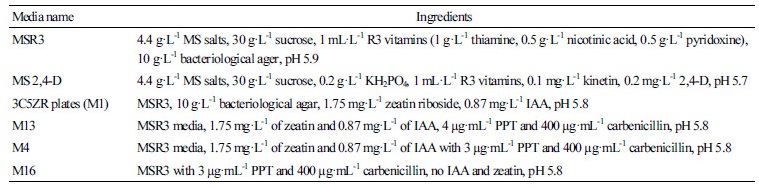
토마토 종자는 70% ethanol과 2% 차염소산나트륨으로 소독한 후 멸균수로 3회 세척하여 MSR3 배지에 파종하고, 23±2°C 배양실에서 10-14일간 무균배양한 후, 양끝 단면을 잘라버린 자엽을 MS 2,4-D 액체배지에 30-60분간 침적하였다. 그리고 M1 고체배지에 옮겨 24시간 배양하였다. Ti-plasmid vector가 도입된 A. tumefaciens cell은 OD600=1.8-2.0로 조정한 후, 24시간 M1 배지에서 배양된 자엽을 15분간 감염 후 M1 배지에 옮겨 2일간 공동 배양하였다. Agrobacterium에 의해 감염된 자엽은 M13 배지에 옮겨 캘루스가 형성될 때까지 배양한 후 M4 배지로 옮겨 신초를 형성시켰고, M16 배지에서 발근시킨 후 순화과정을 거쳐 포트에 이식하였다(Frary and Earle, 1996; Jung, 2013)(Table 2).
pBAtC 벡터의 도입을 확인하기 위하여 재분화된 개체의 잎으로부터 genomic DNA를 분리하여 nos-bar 유전자 특이 증폭용 primer set를 이용하여 PCR 분석을 수행하였다. 이때 사용한 유전자 프라이머는 bar-forward 5'-CGTCAACCACTACAT CGAGA-3', nos-reverse 5'-TTGCGCGCTATATTTTGTTT-3'로 제작하여 95°C에서 5분간 pre-denaturation시킨 후, 94°C에서 30초간 denaturation, 58°C에서 30초간 annealing, 72°C에서 1분간 extension 과정을 30 cycles로 수행하였으며, 마지막으로 72°C에서 5분간 extension을 실시하여 분석하였다.
Single Copy 선발 및 염기서열 분석을 통한 변이체 확인
PCR 분석을 통해 확인된 형질전환체(T0)로부터 single copy로 도입된 개체를 선발하기 위해 TaqMan PCR 분석을 수행하였다(Jung et al., 2017). 대조군으로 single copy 도입이 확인된 형질전환체 T2 homo 개체와 T2 hetero 개체의 DNA를 이용하였으며, TaqMan probe PCR 반응 조건은 95°C에서 10분간 predenaturation시킨 후, 95°C에서 20초 denuaturation, 56°C에서 1분 annealing을 40회 반복 실시하였고, annealing 반응 중에 Quencher로부터 분리된 fluorescein FAM이 활성화될 때마다 fluorescence를 탐지하고 처음 탐지된 cycle 수(ct)는 amplification plots로 표현하였다. TaqMan probe real-time PCR 검사로 복제된 증폭산물은 nos terminator의 특이적인 labeling한 probe primer를 이용하여 분석하였다. 선발된 single copy 개체들로부터 유전자 편집 여부의 확인은 유전자의 표적부위인 sgRNA 부분이 포함되며, 각각 362bp와 571bp의 PCR 산물을 얻을 수 있도록 각각의 표적부위마다 특이 증폭용 primer set를 작성하고, 잎으로부터 추출한 DNA를 이용하여 PCR 분석을 수행하였다. 사용된 RGEN1 primer set 정보는 forward 5'-TTGAAGCTTAAAACAAGAGTGGAA-3', reverse 5'-TGCCTCAATGAT-GAATCCAA-3'로 제작하였으며, RGEN2와 RGEN3 primer set 정보는 forward 5'-CTGAAATGAACAAATCTTTGAG-AA-3', reverse 5'-GGCCCTACTTGTGAGGTTACAC-3'로 제작하였다. Wild type과 각각의 형질전환 개체들의 PCR 산물은 ㈜바이오니아(www.bioneer.co.kr)로 의뢰하여 염기서열 분석을 수행하였다.
에틸렌 생산량 측정
CRISPR/Cas9 도입 형질전환 토마토 T0세대 중에서 RIN 유전자가 편집된 TG4, TG12 및 TG26 개체의 에틸렌 생산량을 측정하기 위하여 토마토를 1L의 밀폐 유리병에 담고 25°C 상온에 3시간 동안 배양한 후, ALUMINA F-1 column(Alltech Associates, Deerfield, IL, USA)과 FID가 장착된 gas chromatography(Model 3800, Varian Inc, Palo Alto, CA, USA)를 이용하여 에틸렌 생산량을 측정하였다(Chung et al., 2010).
결과 및 고찰
sgRNA 디자인 및 CRISPR-Cas9 벡터 구축
토마토 과실 성숙 관련 LeMADS-RIN 유전자는 5번 염색체에 위치하여 8개의 exon을 가지며, open reading frame(ORF)은 729bp이고, 242개의 아미노산으로 구성되어 있다(Vrebalov et al., 2002). 에틸렌 생합성은 LeMADS, LeACS 및 LeAOC 등 많은 유전자들의 발현 조절에 의해 과실 성숙에 관여한다고 알려져 있다(Giovannoni, 2004)(Fig. 1A). 최근 들어 LeMADS- RIN 유전자의 exon 부분이 결실되어 있는 돌연변이체(rin)가 발견되어 성숙에 관한 유전생리학적 연구가 많이 진행되었다(Vrebalov et al., 2002; Giovannoni, 2004). 따라서 LeMADS-RIN 유전자 부위의 CRISPR/Cas9 효소가 인식할 수 있는 sgRNA을 선정하기 위해 각 exon 영역을 CRISPR RGEN tools에 삽입하여 sgRNA(single guide RNA) 3개를 선발하였다(Table 1, Fig. 1B). 선발된 sgRNA는 Cas9 자체에 의해 인식되는 3bp의 트리뉴클레오티드(5’-NGG-3’) 영역을 제외한 20bp의 염기로 구성되며, GC 함량은 35-40%를 보였다. RGEN1과 RGEN2의 out-of-frame score는 62.0 및 RGEN3는 39.6이었으며, 게놈상 mismatches 영역이 1-0-0이므로 off-target 확률이 낮게 나타났다. sgRNA는 유전자를 합성한 후, AarI에 의해 소화한 후, Cas9 효소가 포함된 식물 발현 벡터인 pBAtC에 클로닝하였다(Fig. 1C). 이들 결과는 Kim et al.(2016)의 보고에서도 mis-matches 영역이 0bp는 1, 1bp와 2bp는 0인 경우에 목적 유전자 편집 영역 외의 off-target 영역의 변이가 발생할 확률이 낮다고 하였다. 또한 sgRNA 영역의 GC 함량이 30-70%이며, out-of-frame score가 높게 나온 것을 선정하는 것이 indel이 일어났을 때 frame-shift가 일어날 가능성을 예측하여 유전자 편집의 효율을 증대시킬 수 있다고 보고하였다. 따라서 본 연구에서 선정한 3개의 sgRNA는 기존에 제시한 조건을 모두 만족하였다(Kim et al. 2016).
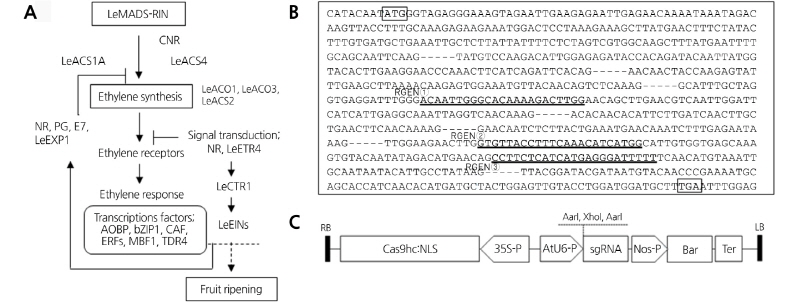
Fig. 1. Ethylene biosynthesis for fruit ripening, selection of sgRNA for gene editing and construction of Ti-plasmid vector. A: Model for the mechanism of fruit ripening in tomato. B: Three target sites for CRISPR/Cas9-mediated mutagenesis in the LeMADS-RIN gene. C: Ti-plasmid vector (pBAtC) construction of RGEN (sgRNA region) for gene editing in tomato. Cas9, human codon-optimized Cas9 expressing cassette; 35S, CaMV 35S promoter; AtU6, Arabidopsis U6-26 promoter driven single-guide RNA (sgRNA) cassette; Nos, Nos promoter; Bar, Basta resistance gene; Ter, Nos terminator; LB, left border; RB, right border; RGEN, RNA-guided engineered nuclease.
형질전환체의 육성과 T-DNA 도입 확인 및 Single Copy 선발
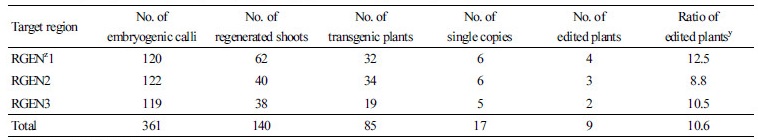
식물 발현 벡터에 sgRNA1-3을 각각 구축된 벡터(pBAtC-RGEN1-3)를 이용하여 ‘마미리오’와 ‘골든벨’ 품종에 형질전환하였다. 토마토 종자를 발아시킨 후 14일된 유묘에서 얻은 자엽 절편에 A. tumefaciens LBA4404를 이용하여 형질전환시켰다(Fig. 2A). 감염된 자엽은 M13 배지에서 캘루스를 형성시키고, 다시 M4 배지로 옮겨 신초를 형성시킨 다음 M16 배지에서 발근시킨 후에 최종적으로 순화과정을 거쳐 포트에 이식하였다(Fig. 2B). 형질전환실험에서 얻어진 재분화 식물체를 대상으로 유전자의 도입여부를 확인하기 위해 nos-bar 유전자 특이 증폭용 primer를 이용하여 PCR 분석을 수행한 결과 총 85개의 형질전환 식물체를 얻었다(Fig. 2, Table 3). 형질전환체에서 single copy 여부를 알기 위해 TaqMan PCR 분석을 실시한 결과, RGEN1 도입 형질전환체 32개체 중 6개체, RGEN2 도입 형질전환체 34개체 중 6개 및 RGEN3 도입 형질전환체 19개체 중 5개체 등 총 17개 T0 식물체에서 single copy로 확인하고 T1 종자를 채종하여 계통화하였다(Fig. 2C, D).
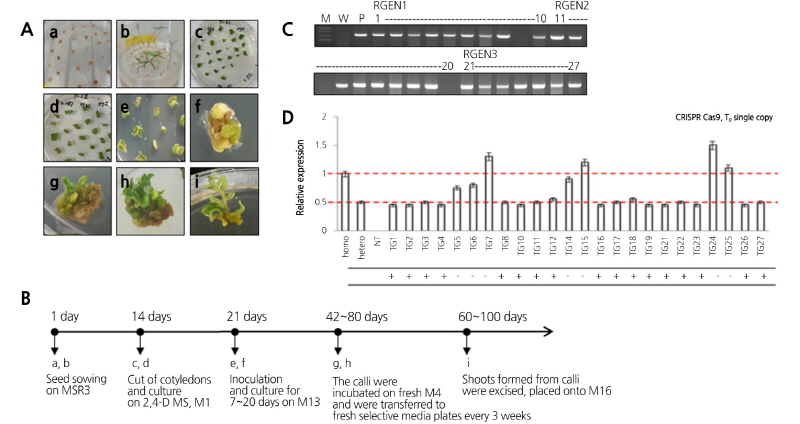
Fig. 2. Development of transgenic tomato and confirmation of transgene. A: Introduction of pBAtC-RGEN vector through Agrobacterium-mediated transformation in tomato plants. B: Schematic of tomato plant transformation for 100 days. C: PCR analysis of bar and nos terminator region. D: Selection of transgenic single copy plants using TaqMan PCR analysis. Lane 1, T2 Homo; Lane 2, T2 Hetero; Lane 3, Negative control and transgenic lines, TG1-10 for RGEN1; TG11-20 for RGEN2; TG21-27 for RGEN3. Each levels generated from the DNA template of independent T0 transgenic lines (target gene probe; 3'NOS, reference probe; tubulin1).
유전자 편집 확인 및 에틸렌 생산량 분석
도입유전자가 single copy로 삽입된 T0 개체들로부터 유전자 편집 여부의 확인은 LeMADS-RIN 유전자의 표적부분이 포함되도록 제작된 primer를 이용하여 PCR 증폭을 수행하고 염기서열을 분석하였다. 식물 발현 벡터에 각각 도입된 3개의 sgRNA (RGEN1, RGEN2, RGEN3) 중 RGEN1이 도입된 6개의 형질전환체 중 2개체는 변이가 없었다. TG2 변이체는 T/A로 치환되었고, TG4 변이체는 17bp가, TG8 변이체는 4bp가, 그리고 TG10 변이체는 1bp가 각각 결실되었다. RGEN2가 도입된 6개의 형질전환체 중 3개체는 변이를 보이지 않았으며, TG12 변이체는 28bp가, TG16 변이체는 2bp가, 그리고 TG17 변이체는 1bp가 각각 결실되었다. RGEN3가 도입된 5개의 형질전환체 중 3개체는 변이가 없었으며, TG23 변이체는 T/A로 치환되었고, TG26 변이체는 2bp가 결실된 것으로 확인하여 총 9계통을 선발하였다(Fig. 3A).

Fig. 3. CRISPR/Cas9-induced LeMADS-RIN gene modification in tomato. A: Nucleotide sequences of the target site in the 9 T0 edited tomato lines. The indel sequences of target locus are ranked as hyphens with deletion (-) and mismatched (m). B: Alteration of amino acid sequences with early stop codon after CRISPR/Cas9 cleavage in LeMADS-RIN gene.
이들 변이체로부터 아미노산 합성 여부를 조사한 결과는 Fig. 3B와 같이 ‘마미리오’ 품종으로부터 얻은 TG4 및 ‘골든벨’ 품종으로부터 얻은 TG12와 TG26 개체에서 종결 코돈이 형성되어 단백질 발현 및 아미노산 생성이 불활성화된 것을 확인할 수 있었다. 이와 같이 선발된 TG4, TG12와 TG26의 과실에서 에틸렌 생산량의 변화를 살펴본 결과 대조구에 비해 에틸렌 생산량이 현저히 감소하였다(Fig. 4). 이러한 결과는 과실 숙성을 저해하는 LeMADS-RIN 유전자가 knockout되어 RIN 단백질이 축적되지 않아 에틸렌 생산에 변화를 보인 것으로 생각된다. 최근 Ito et al.(2015)은 ‘Ailsa Craig’ 품종에 Agrobacterium법에 의해 유전자 편집을 시도하여 RIN 단백질이 축적되지 않는 knockout 토마토를 육성한 결과 불안정한 과색을 보인다고 하였다. 그러나 육성된 편집 식물체에서 에틸렌 생산량을 측정하지 않았다. 본 실험에서 사용한 ‘마미리오’ 및 ‘골든벨’ 품종은 세계적으로 유명한 적색계 품종으로 RIN 유전자 편집에 의해 다양한 과색 변이를 보여주었으며 아울러 에틸렌 생산량이 현저히 감소하는 결과를 보였다(Fig. 4). 따라서 이들 편집계통들은 과실의 저장성이 매우 좋을 것으로 기대된다.
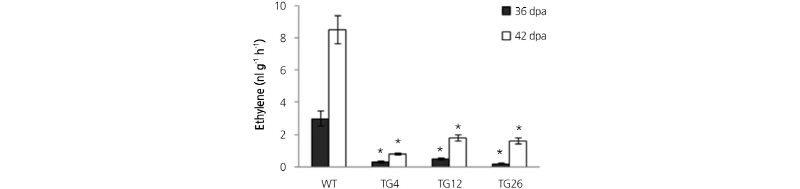
Fig. 4. Production of ethylene in transgenic tomato fruits at 36 and 42 days post-anthesis (dpa). WT: wild type, TG: transgenic plants. The values are shown as the means ±SD. Asterisks indicate significant differences (t-test p ≤ 0.05). TG4: RGEN1 transgenic ‘Mamirio’, TG12: RGEN2 transgenic ‘Golden Bell’, TG26: RGEN3 transgenic ‘Golden Bell’.
지금까지 보고된 에틸렌(ethylene) 생합성 과정은 methionine으로부터 S-adenosyl-L-Met(SAM)에서 1-aminocyclopropa ne-1-carboxylic acid(ACC)로, ACC가 에틸렌으로 전환되는 두 단계에서 에틸렌 생합성이 조절된다고 하였으며, LeMADS- RIN 유전자 발현을 통해 첫 번째 단계에서는 ACC synthase(ACS)에 의해, 두 번째 단계에서는 ACC oxidase(ACO)에 의해 이루어진다(Giovannoni, 2004). 토마토에서 ACS와 ACO는 multigene family를 이루고 있으며, 대표적으로 ACS에는 LE- ACSIA, LE-ACSIB와 LE-ACS2-7 등이 있으며, ACO에는 LE-ACO1-4가 존재한다. 에틸렌의 조절작용 시스템은 두 가지로 구분되는데, 이 중 과실 숙성과 노화에 관련된 시스템 작동 시 LE-ACS2와 LE-ACS4가 에틸렌 합성에 관여한 다음 LE-ACO3, Le-ACO4 유전자가 유도되면서 signal transduction과 transcription factor들의 작용으로 에틸렌 생합성이 조절되며 과실 숙성이 이루어진다고 알려져 있다(Giovannoni, 2004; Ito, 2016) (Fig. 1A).
따라서 본 연구에서 토마토 과실 성숙 관련 LeMADS-RIN 유전자를 CRSPR/Cas9 시스템을 적용하여 선발된 형질전환체는 이미 Adams-Phillips et al.(2004)이 보고한 rin 토마토 돌연변이 계통과 유사한 결과를 보여주었다. 따라서 이들 육성계통을 이용하여 과실 성숙에 관한 분자 메커니즘, 세포벽 및 대사체 연구, 에틸렌 생합성 경로 및 응답반응 등에 대한 연구 재료로써 활용 가능성도 시사된다. 이와 같이 정밀 유전자편집 기술인 CRISPR/Cas9 system을 이용하여 농업생산성 및 기능유전자가 편집된 개체를 확보하여 계통화하면 직접 육종에 활용할 수 있을 것으로 사료된다.