서 언
재료 및 방법
식물재료 및 VIGS, 표현형 분석
유전자 서열, 구조 및 진화 분석
RT-PCR
조직 특이적 및 병원균 상호작용 발현패턴 분석
결과 및 고찰
CaS17 유전자 동정
CaLOP 유전자의 구조 및 계통 분석
발현 패턴 분석
서 언
식물은 끊임없이 외부에서 비생물학적, 생물학적 스트레스의 영향을 받는다(Lee and Yeom, 2015). 식물이 생물학적 스트레스를 극복하기 위한 방법 중의 하나는 세포벽을 이용하여 세포 밖의 다양한 환경에 대항하는 것이다(Hugot et al., 2004). 특히, 식물은 병원균 침입 초기에 병원균의 분비 유도체를 인지하여 신호전달경로를 활성화하고, 세포벽 및 세포간극으로 분비단백질(secretome)을 내보내어 방어기제를 시작한다(Lee et al., 2004). 식물의 다양한 방어기제에 중요한 역할을 하는 것으로 알려진 분비단백질은 식물이 병원균에 공격을 받았을 때 세포 편광과 유두 형성을 통한 세포벽 비대에 관여하는 것으로 보고되었다(Schulze-Lefert, 2004). 또한, PR 단백질(pathogenesis-related protein)과 같은 분비단백질은 systemic acquired resistance (SAR)을 통한 식물의 저항성에 기여하는 것으로 보고되었고(Schmelzer, 2002; Yeom et al., 2012), 식물의 형태 변화, 조직 분화 및 생장과 같은 생육과 발달에도 중요한 역할을 한다고 알려져 있다(Yamane et al., 2005; Lee et al., 2011; Yeom et al., 2011; Seo et al., 2012).
선행 연구에서 고추(Capsicum annuum L.)와 고추 역병균(Phytophthora capsici)과의 상호작용을 통해 분비되는 유전자들을 효모 기반 분비단백질 분리 기법(yeast-based secretion trap screen)을 통해 고추 분비단백질(C. annuum secretome, CaS) 유전자를 대량 분리하였다(Yeom et al., 2011). 고추 역병균에 대해 저항성 고추와 감수성 고추에서 특이적으로 발현되는 분비단백질을 코딩하는 유전자들에 대한 발현 분석을 통해 후보 유전자들을 선별하고, 이들에 대해 바이러스 기반 유전자 침묵 기법(virus-induced gene silencing, VIGS)을 통해 저항성 기능 분석을 수행하였다. 또한, 병원균과 상호작용하는 CaS 유전자가 식물의 생육과 발달에도 중요한 역할을 할 것이라는 가능성도 제시하였다(Seo et al., 2012). 하지만, 그 유전자들의 다양한 환경 스트레스에 대한 상호작용과 식물의 생육 및 발달에 관한 생물학적 기능에 대해서는 제한적으로 연구가 진행되었다.
본 연구는 선행연구에서 분리된 CaS 유전자들 중에서 고추 lipoxygenase 유사 유전자인 CaS17(CaLOP)에 대한 식물 생육 및 발달에 관한 기능을 밝히고자 하였다. 이를 위해 RNA-seq 정보를 활용하여 다양한 조직에서의 발현 양상 분석 및 세균, 바이러스, 역병 등 다양한 병원균 침입 시의 발현 양상 분석 등을 통해 다양한 병원균과의 상호작용에 관한 식물 방어 기제 연관성을 추가 분석하였고, 바이러스 기반 유전자 침묵 기법을 이용한 유전자의 발현 억제를 유도하여 CaS17(CaLOP)의 생물학적 기능을 검정하였다. 또한, CaS17(CaLOP)과 동종 상동성 유전자인 CaS4와의 비교 분석을 통해 두 유전자 간의 생육과 발달에 관련된 기능적 차이를 확인하였다.
재료 및 방법
식물재료 및 VIGS, 표현형 분석
광 16시간, 암 8시간의 순환의 23°C 생장상(Kim et al., 2008)에서 키운 고추를 바이러스 기반 유전자 침묵 기법(VIGS)을 수행에 사용하였다. VIGS는 Yeom et al.(2012)에서 보고된 TRV-based VIGS 방법을 참조하여 다음과 같이 수행하였다. DNA 염기서열 특이적인 CaS4와 CaS17 유전자가 클로닝된 pTRV 벡터를 Agrobacterium tumefaciens sp. strain GV2260에 형질전환 후, Agrobacterium을 rifampicin 50mg·mL-1과 kanamycin 50mg·mL-1를 포함한 YEP 배지(yeast extract peptone media)에서 2일 동안 30°C에서 진탕배양하였다. 증식한 Agrobacterium을 원심분리기로 세포를 침전시켜 접종 버퍼(10mM MES, 10mM MgCl2, pH 5.5)에 풀어준 후, 배양액의 흡광도(optical density, O.D.)를 0.5로 정량하여 사용하였다. 이 후 고추의 떡잎에 배양액을 1mL 주사기로 접종한 후 24시간 동안 16°C 에서 저온배양 후에 광 16시간, 암 8시간 순환의 21°C 생장상(JSPC- 420C, JS Research Inc., Gongju, Korea)에서 키웠다. 표현형은 접종 후 5주차의 고추에서 관찰하였으며 각 개체의 초장과 엽면적을 측정하였다. 엽면적은 각각의 식물체의 3번째 본엽을 채취하여 측정하였다. 통계분석은 SPSS 프로그램(PASW statistics 18, Chicago, IL, USA)을 사용하여 분산분석(ANOVA)을 하였다. 분산분석 간에 평균의 비교는 Tukey의 다중비교법을 이용하였다.
유전자 서열, 구조 및 진화 분석
CaS4와 CaS17의 전체 염기서열은 고추 유전체 사이트(http://genome.pepper.snu.ac.kr/)에서 확보하였다. 단백질의 도메인 구조 분석은 SMART(http://smart.embl-heidelberg.de/)를 이용하였다. 고추 외의 토마토, 감자, 담배, 벼, 애기장대에서의 이종 상동성 유전자 서열은 Sol Genomic Network(https://solgenomics.net/, 토마토, 감자, 담배 서열), Rice Genome Annotation Project(http://rice.plantbiology.msu.edu/), Arabidopsis TAIR(https://www.arabidopsis.org)에서 각각 확보하였다. 유전자 서열분석(multiple sequences alignment, MSA)은 EMBL-EBI(http://www.ebi.ac.uk/)의 MUSCLE 프로그램을 사용하였다. 진화 계통수 분석은 Seo et al.(2016)에서 보고된 방법을 참조하여 다음과 같이 수행하였다. MEGA7(http://www.megasoftware.net/) 프로그램을 기반으로 계통분석 시 방법은 neighbor-joining을 사용하였고, bootstrap method로 100번 반복하였다. 치환모델은 Jones-Taylor-Thornton(JTT) model을 사용하고, 부분 간의 비율은 uniform rates를 사용하였다. 공백과 잘못된 데이터의 처리는 partial deletion을 사용하여 95% 이하로 겹치는 것은 제거하였다.
RT-PCR
RNA의 추출은 VIGS 수행 후 5주차의 식물체를 대상으로 하여 3-4번째 본엽에서 추출하였으며 Trizol(Invitrogen, Carlsbad, CA, USA)을 이용하여 제조회사의 지침에 따라 진행하였다. cDNA는 M-MLV Reverse Transcriptase(Promega, Madison, WI, USA)를 사용하여 합성하였다. RT-PCR에 사용된 프라이머는 CaTin1_C_F(5'-GGCAGTGGTTACGACTACTT-3'), CaTin1_C_R(5'-CATGATAGGACTGAGGATCG-3'), CaLOP_N_F(5'-ACTGCCATGGGAGTAGCTCAGGT-3'), CaLOP_ F_C_R(5'-GCCTACACAAATGATGAGATAACGT-3')을 사용하였다.
조직 특이적 및 병원균 상호작용 발현패턴 분석
고추 유전자의 조직 별 RNA-seq 정보는 선행연구 결과(Kim et al., 2014)를 기반으로 5개의 조직(잎, 줄기, 뿌리, 과피, 태좌)에서 7개의 과실 숙도에 따른 발달 단계인 수분 후 6일(6DPA, days post-anthesis), 16일(16PDA), 25일(25PDA), 과실의 녹색기(mature green, MG), 변색기(breaker, B), 변색기 후 5일(B5), 10일(B10)에서의 유전자 발현 패턴을 분석하였다. TMV-P0, TMV-P2, PepMoV, 고추역병과의 고추와의 상호작용 RNA-seq 정보 및 발현 분석은 Kang et al.(2016)에서 보고된 방법을 기반으로 병원균을 접종하지 않은 음성 대조군 값으로 정규화(normalization)한 후에 분석하였다. 각 유전자별 발현패턴은 RPKM(read per kilobase per million mapped reads) 값에 log2 값을 취하여 수행하였으며, heatmap은 정규화된 RNA-seq 정보를 heat-map R package(http://bioconductor.org/)를 이용하여 분석하였다.
결과 및 고찰
CaS17 유전자 동정
선행연구를 통해 분리한 분비단백질 유전자 CaS17와 CaS4의 특성 분석을 위해 두 유전자들의 클론을 시퀀싱하여 유전자의 서열을 확보하고, 이 서열들을 고추 유전체 데이타베이스에서 BLAST하여 전체 유전자를 검정하였다. 각 유전자의 확보한 서열 크기는 CaS4와 Cas17 유전자가 각각 UTR을 포함하여 804bp(179aa)와 730bp(184aa)였다. 이 후, 두 유전자들의 기능 및 특성을 예측하기 위하여 NCBI에 BLAST한 결과, CaS4 유전자는 단백질 수준에서 기존에 보고된 CaTin1 유전자(Shin et al., 2003)와 100%로 동일한 유전자였으며, CaS17 유전자는 기존에 보고된 CaTin1-2 유전자(Shin et al., 2003)와 84% coverage, 99% similarity를 가지고 있는 것을 확인하였다. 또한 CaS4와 CaS17 유전자를 비교했을 때는 서로 62% similarity를 가지는 것을 알 수 있었다. 이를 통해 CaS4와 CaS17은 서로 상동성이 높지만, 서로 다른 유전자인 것을 확인하였으며 유사한 기능을 가질 것으로 유추할 수 있었다. 기존에 보고된 선행 연구 결과를 살펴보면, CaTin1 유전자는 CaTin1-2 유전자와 동일한 프로모터를 사용하며, 두 유전자가 함께 Tobacco mosaic virus(TMV) 저항성과 에틸렌의 산화, 환원 반응에 관여한다고 알려져 있다(Shin et al., 2003; Shin et al., 2004). 그러나 다른 병원균에 대한 유전자의 발현 양상 등의 반응성과 작물의 생육과 발달에 대한 기능에 대해서는 연구 결과가 아직 보고되지 않았다. 그러므로 아직 그 기능이 보고 되지 않은 CaS17 유전자로 후속 연구를 진행하였다.
CaLOP 유전자의 구조 및 계통 분석
CaS17 유전자의 구조적 특징을 확인하기 위하여, SMART 프로그램으로 구조 분석을 수행하였다. 유전자의 5' 말단(1-26aa)에 signal peptide(SP), 중간 부분부터 3' 말단(33-160aa)에는 PLAT/LH2 구조를 가지고 있는 것을 확인하였다(Fig. 1A). 예측한 구조 중에서 PLAT(ploycystin-1, lipoxygenase, alpha-toxin) 도메인과 LH2(lipoxygenase homology) 도메인은 lipoxygenase와 관련된 것으로 CaS17도 lipoxygenase의 역할을 할 것으로 예측할 수 있었다. 이에 따라 CaS17 유전자를 C. annuum lipoxygenase homology protein(CaLOP)로 명명하였다.
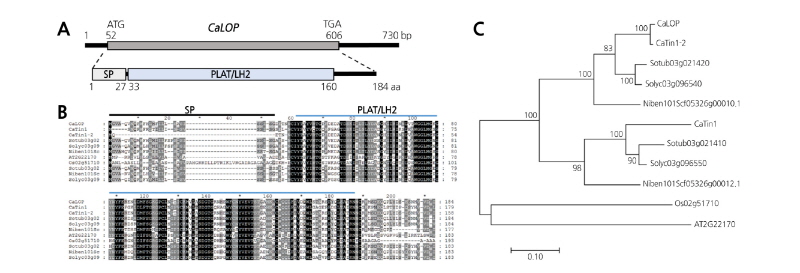
Fig. 1. Structural and phylogenetic analysis of CaLOP and its homologs. A Structure of CaLOP. The CaLOP gene comprises two exons and one intron. The CaLOP protein contains a signal peptide (SP) and lipoxygenase homology 2 (PLAT/LH2) domain. Numbers shown underneath the CaLOP structure represent the location of each domain on the gene. B Comparative analysis of predicted amino acid sequences of CaLOP and its homologs. Bars with SP and PLAT/LH2 above the sequence alignment indicate the signal peptide and lipoxygenase homology 2 domains, respectively. C Phylogenetic tree of CaLOP, and homologs of CaLOP. CaLOP was clustered with CaTin1-2 (Capsicum annuum), Sotub03g021420 (Solanum tuberosum), Solyc03g096540 (Solanum lycopersicum), and Niben101Scf05326g00010.1 (Nicotiana sylbestris). CaTin1 was clustered with three genes (Sotub03g021410 from Solanum tuberosum, Solyc03g096550 from Solanum lycopersicum, and Niben101Scf05326g00012.1 from Nicotiana sylbestris). Rice (Os02g51710) and Arabidopsis (AT2G221700) genes were clustered at the same clade. The tree is drawn to scale, with branch lengths measured in the number of substitutions per site.
CaLOP 유전자의 상동유전자 간의 진화 및 특징 차이를 분석하기 위하여 CaLOP 유전자와 동종 상동성 유전자인 CaTin1-2, CaTin1(CaS4)와 다른 작물의 이종 상동성 유전자들 간의 단백질 서열 비교 및 계통 분석을 하였다. CaLOP와 CaTin1의 서열을 바탕으로 감자(Sotub03g021410, Sotub03g021420), 담배(Niben101Scf05326g00010.1, Niben101Scf05326g00012.1), 토마토(Solyc03g096540, Solyc03g096550), 벼(Os02g51710), 애기장대(AT2G22170)에서 상동유전자를 확보하였다. 벼와 애기장대의 경우 두 유전자와 상동성이 높은 유전자가 각각 하나씩 확인되었다. 이들 유전자들은 CaLOP 유전자와 동일하게 모두 SP와 PLAT/LH2 도메인 구조를 가지고 있었고, 단백질 서열 간의 상동성이 높은 것을 확인하였다(Fig. 1B). 계통도 분석(phylogenetic analysis)을 통한 진화분석을 수행한 결과 총 3개의 그룹으로 분류할 수 있었으며, 가지과 작물끼리 그룹으로 나뉜 것이 2개, 벼와 애기장대가 함께 1개의 그룹으로 나뉘었다. 가지과 내에서는 CaLOP 유전자와 CaTin1 유전자를 중심으로 2개의 그룹으로 나뉘었다. CaLOP 유전자와 CaTin1-2, Sotub03g021420, Solyc03g096540, Niben101Scf05326g00010.1 유전자가 하나의 그룹으로 분류되었고, CaTin1 유전자와 Sotub03g021410, Solyc03g096550, Niben101Scf05326g00012.1 유전자가 다른 한 그룹으로 분류되었다(Fig. 1C). 이 결과를 통하여, CaLOP와 CaTin1은 가지과 작물이 종 분화되기 이전에 원시 기원 유전자에서 CaLOP와 CaTin1이 각각 생성되어 진화한 것으로 예측할 수 있었다. 또한, CaTin1-2 유전자와 CaLOP 유전자는 가지과 종분화 이후에 복제 기작에 의해 동종 상동성 유전자가 되었다는 것을 시사한다. CaLOP 유전자는 감자, 토마토, 담배에서 각각 이종 상동성의 유전자들의 유전자 구조가 잘 보존되어 있는 것을 알 수 있었다. 또한, 벼와 애기장대에서도 유사성이 높은 유전자가 있는 것으로 보아 식물체 내에서 보존된 기능을 수행하고 있을 것으로 보인다.
발현 패턴 분석
C. annuum cv. CM334의 RNA-seq 결과를 이용한 발현양상 분석을 통하여 CaLOP의 기능을 예측하고자 하였다. CaLOP 유전자의 발현 양상을 비교 분석하기 위해 CaTin1 유전자도 함께 분석을 수행하였다. CaLOP 유전자와 CaTin1 유전자의 고추 조직 별 및 과실의 발달 단계별 발현패턴을 분석한 결과, 두 유전자는 테스트한 조직 모두에서 비슷한 발현 패턴을 보였다(Fig. 2A). 두 유전자 모두 잎보다는 줄기, 줄기보다는 뿌리에서의 발현 양이 많았으며, 과실의 발달 단계에서는 과피(PR)보다는 태좌(PL)에서 발현이 더 많이 되는 것을 알 수 있었다. 또한 태좌에서 과실의 발달단계에 따른 발현양상을 살펴보면, 초기 발달 단계인 개화 후 6일(6DPA)부터 25DPA에서 발현이 많이 되고, 그 이후 후기 단계인 녹색기와(MG) 변색기(B)에서는 발현이 감소하는 것을 확인하였다(Fig. 2A). 이를 통해 CaLOP 및 CaTin1은 생식 생장에 관련된 조직보다는 영양 생장에 관련된 조직에서 발현이 증가하여, 영양 생장 조직의 형성 및 발달에 영향을 미칠 것으로 예측할 수 있었다.
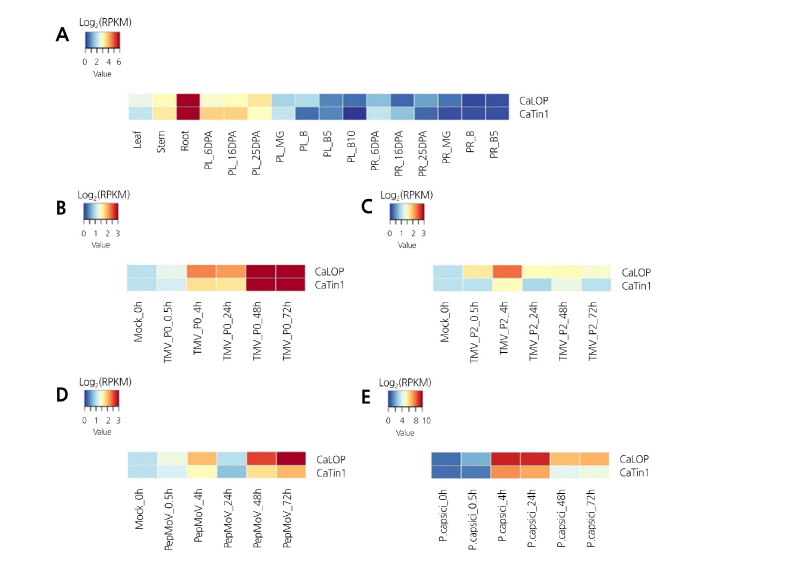
Fig. 2. Heat maps showing the expression patterns of CaLOP and CaTin1 in various tissues, and responses to pathogen infection in pepper. Tissue-specific expression profiles (A) were analyzed in various tissues and developmental stages in pepper. PR, pericarp; PL, placenta; MG, mature green; B, breaker stage; DPA, days post-anthesis; B5 and 10, 5 and 10 days post-breaker stage. The expression values were normalized by log2 (RPKM, Reads Per Kilobase of transcript per Million mapped reads). The expression patterns of CaLOP and CaTin1 were examined in response to TMV-P0 (B), TMV-P2 (C), PepMoV (D), and P. capsici (E). The RPKM expression values of responses to pathogen infection were normalized relative to expression values and transformed log2 values. Blue represents low expression; red represents high expression.
CaLOP와 원시유전자 및 동일 프로모터를 공유한 CaTin1과 상동 유전자 CaTin1-2는 TMV-P0에 대해 바이러스 접종 후 각각 36시간과 48시간부터 발현이 증가한다는 결과를 통해 CaTin1과 CaTin1-2는 TMV 저항성과 관련이 있는 것으로 보고되었다(Shin et al., 2003). 그러므로, CaLOP도 TMV를 포함한 다른 병원균에 대해서 저항성 반응과 관련이 있는지를 확인하기 위해, 3가지 바이러스[Tobacco mosaic virus(TMV)–Pathotype0(P0), TMV-P2, Pepper mottle virus(PepMoV)]와 고추 역병(Phytophthora capsici)을 접종한 RNA-seq 정보를 이용하여 발현양상을 분석하였다. 조직 발현 분석과 마찬가지로 CaTin1도 함께 분석하여 발현 양상을 비교하였다. 본 연구에서 사용한 RNA-seq 재료인 C. annuum cv. CM334는 TMV의 pathotype에 따라서 각기 다른 저항성 양상을 보이며, TMV-P0에는 대해서는 저항성으로, TMV-P2에 대해서는 감수성으로 보고되었다(Tomita et al., 2011; Yang et al., 2012).
CaLOP와 CaTin1은 TMV-P0를 접종하였을 때, 접종 후 30분(0.5h)부터 발현이 증가하기 시작하여, 시간이 지날수록 유전자의 발현이 점점 증가하는 양상을 보였다. 테스트한 시간 중 48hpi와 72hpi에서 유전자의 발현이 다른 시간대에 비해 매우 강하게 나타나는 것을 확인할 수 있었다(Fig. 2B). 이 결과를 통해서 CaTin1은 선행연구에서 보고된 것과 마찬가지로 48시간 이후부터 발현이 매우 높게 증가한다는 것을 확인하였으며, CaLOP는 CaTin1과 비슷한 양상을 보이면서, 48hpi부터 강하게 발현되는 것을 알 수 있었다. 그리고 TMV-P2를 접종한 샘플에서는 TMV-P0를 접종한 샘플처럼 CaLOP가 CaTin1보다 많은 발현량이 보였지만, 전체적인 발현 양상을 보면, TMV-P0를 접종했을 때보다 TMV-P2를 접종한 샘플에서의 두 유전자 발현이 상대적으로 모두 약하게 발현하는 것을 확인하였다(Fig. 2C).
CaLOP 유전자는 CM334가 감수성을 보인 TMV-P2보다 저항성을 보인 TMV-P0에서 강하게 발현하는 양상을 보였고, 이를 통하여 CaLOP 유전자도 TMV에 대한 저항성에 관여한다는 것을 유추할 수 있었다. 또한 PepMoV를 접종한 샘플에서도 CaLOP 유전자는 PepMoV 접종 전(0h)보다 접종 후에 발현이 증가하여 72hpi에서 가장 발현이 높았다(Fig. 2D). 고추 역병을 접종한 샘플에서는 접종 후 초기 단계인 6hpi와 24hpi에서 발현이 증가하였지만, 48hpi와 72hpi에서는 이전 시기에 비해 상대적으로 발현이 감소하였다. CaLOP 유전자뿐만 아니라 CaTin1 유전자에서도 비슷한 양상을 확인하였고, 고추 역병과 관련하여 접종 후 초기 단계에 저항성과 관련이 있는 것으로 생각되었다(Fig. 2E). 지금까지의 결과를 토대로, 생물학적 스트레스에 대한 CaLOP 유전자는 기존에 상동 유전자에서 보고된 TMV 이외에도 고추 역병과 PepMoV와 같은 다양한 생물학적 스트레스와의 상호작용에 관여한다는 것을 시사한다.
CaLOP 유전자의 식물의 발달 및 생육 관련 기능 분석
CaLOP 유전자의 식물의 발달 및 생육에 관련된 기능을 분석하기 위해 고추에서 VIGS를 이용하여 유전자의 발현을 억제하였다. CaLOP 유전자의 비교 분석을 위하여 CaTin1 유전자도 TRV 유래 벡터를 사용하여 VIGS를 수행하였다(Fig. 3A and 3B). 대조군으로는 green fluorescent protein(GFP)와 endogenous phytoene desaturase(PDS) 유전자에 대한 VIGS 실험을 수행하였다. 이 후, VIGS 수행 5주 후에 식물체의 표현형 변화를 관찰하였다. GFP를 이용하여 VIGS를 수행한 대조군(TRV-GFP)은 CaTin1의 발현을 억제한 식물(TRV-CaTin1)과 비교했을 때, 생육에서 차이를 보이지 않았다(Fig. 3C). 그러나 CaLOP 유전자의 발현을 억제한 식물(TRV-CaLOP)에서는 초기 생육단계에서 고사 또는 잎의 변형과 함께 초장의 단축을 보이거나 생육 저해로 인한 초장의 단축 현상만 보이는 3가지 형태의 표현형을 보였다(Fig. 3C). 동일한 CaLOP 유전자의 발현을 억제하였을 때, 생육이 억제되는 동일한 현상이 나타나지만, 그 안에서의 3종류의 다른 표현형이 나타나는 이유는 VIGS의 효율에 따라서 각기 다른 표현형을 보이는 것으로 예상할 수 있었다. VIGS를 수행한지 5주째 되는 식물에서 샘플링을 수행하여 각 유전자들의 발현 억제 유무를 확인하고자 RT-PCR을 수행하였다. 그 결과, 비교 유전자 CaTin1와 CaLOP의 발현을 억제한 식물체에서 각 해당 유전자만 특이적으로 발현이 억제된 것을 확인하였고, 이는 앞서 관찰한 표현형이 유전자 침묵현상으로 인해 관찰된 것임을 확인할 수 있었다(Fig. 3D).
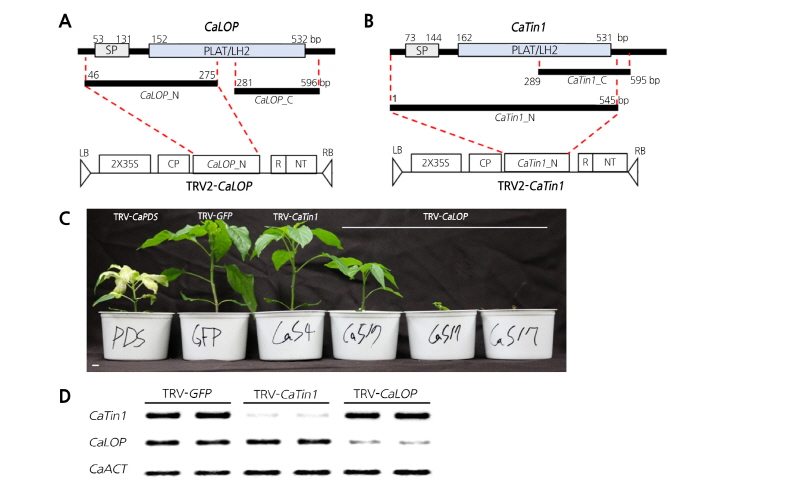
Fig. 3. Silencing effects of CaLOP and CaTin1 on pepper growth and development. A Diagram of the silencing construct TRV-CaLOP. CaLOP_N, targeting the N terminus of CaLOP, was designated TRV-CaLOP, which contains signal peptide (SP) and lipoxygenase homology 2 PLAT/LH2 domains. N, N-terminal region used for the Tobacco rattle virus (TRV)-based virus-induced gene silencing (VIGS) system. B Diagram of the silencing construct TRV-CaTin1. CaTin1_N was used as TRV-CaTin1, including the N-terminus of CaTin1. C Phenotype of CaLOP-silenced and CaTin1-silenced pepper. The picture was taken 5 weeks after silencing. TRV-CaPDS and TRV-GFP were used as controls. D Semi-quantitative reverse-transcription polymerase chain reaction expression analysis of CaLOP and CaTin1 in TRV-GFP, TRV-CaLOP (N-terminal) and TRV-CaTin1 (N-terminal)-infiltrated pepper. The CaACT gene was used as a control.
반복 실험을 통해 CaLOP 유전자의 발현 억제를 통한 식물체 생육과 발달의 변화 양상을 조사하였다. 여러 번의 반복실험을 통하여 총 135개체의 표현형을 관찰하였고, 135개체의 식물체 중 56%에 해당하는 75개체의 식물에서 초장이 매우 작고, 잎의 모양이 심하게 변형되는 표현형을 보였고, 27개체(20%)의 식물체는 CaLOP 유전자가 강하게 발현이 억제되면서 초기 생육 단계에서 고사하였다(Fig. 4A). 그리고 나머지 33개체(24%)의 식물체는 대조군과 비교하였을 때 초장의 길이 및 잎의 크기가 작아진 것으로 확인되었다(Fig. 4A). 식물체의 엽면적과 초장을 측정하여 대조군과 비교하였다. 그 결과 VIGS 5주차 식물체의 엽면적은 TRV-GFP는 평균 11.1cm2, TRV-CaTin1은 8.5cm2, TRV-CaLOP는 0.9cm2로 나타났으며, TRV-GFP와 비교하였을 때, TRV-GFP보다 TRV-CaTin1은 2.6cm2, TRV-CaLOP 10.2cm2가 작아진 것을 확인할 수 있었다(Fig. 4B). 초장에서는 TRV-GFP는 평균 11.3cm로 확인 되었고, TRV-CaTin1의 초장은 11.1cm로 확인되어 TRV-GFP와 비교하였을 때 유의한 차이를 보이지 않았다. 하지만 TRV-CaLOP 식물체에서는 평균 3.5cm로 TRV-GFP와 비교하였을 때 초장이 평균 7.8㎝ 더 작아진 것을 확인할 수 있었다(Fig. 4C). VIGS 수행 후 5주째 되는 식물을 샘플링을 하여 CaLOP 발현억제 시 3가지 표현형에 따른 유전자 발현을 확인하였다. 식물이 고사하는 표현형을 가진 식물체에서는 식물체의 고사로 인해 샘플링을 수행할 수 없었다. RT-PCR 결과, 초장이 단축과 잎이 작아지는 표현형(SG)을 가진 식물체보다 잎 모양이 심하게 변형되고 초장이 매우 작아진 식물체(SG + Ab)에서 CaLOP의 발현이 더 억제되는 양상을 보였다(Fig. 4D). 이 결과를 통하여, 동일한 CaLOP 유전자의 발현을 억제하였을 때, 각기 다른 표현형이 나타나는 이유는 VIGS의 효율에 의한 것임을 알 수 있었다.
이러한 결과들을 통하여, CaLOP은 CaTin1 유전자와 달리 식물의 생육과 발달에 핵심적인 기능을 수행한다는 것을 알 수 있었다. Fig. 4A의 표현형 조사결과에서 56%의 개체가 해당되는 많은 수의 식물체가 키가 매우 작아지고 잎의 모양이 정상적으로 발달하지 않는 표현형을 나타내는 것으로 보아, CaLOP 유전자는 식물의 생육에 깊은 관련이 있고, 동시에 발달에도 관여하여 초장 및 잎의 형태를 유지하는 데에 중요한 역할을 할 것으로 생각된다.
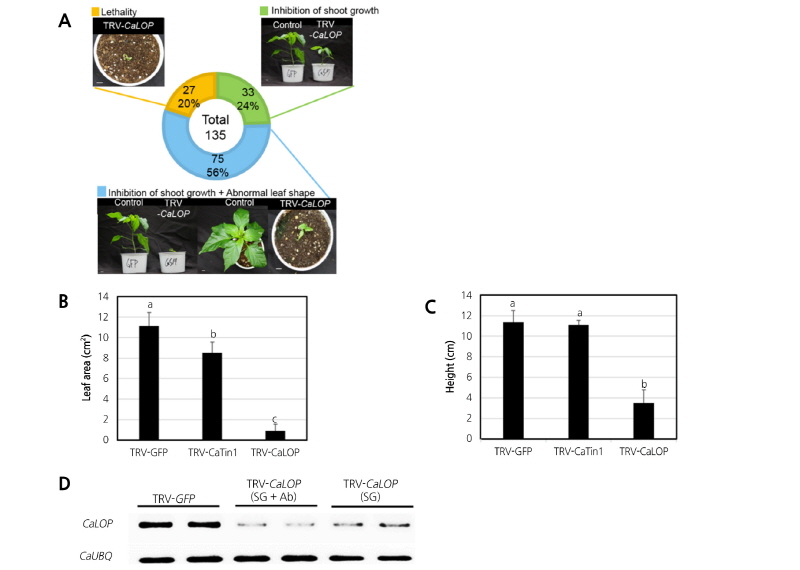
Fig. 4. Phenotype analysis of CaLOP-silenced pepper. A Phenotypic classification of CaLOP-silenced plants. CaLOP-silenced plants are categorized into three classes, each with a specifically colored square box on the left side of the class description. The circular diagram indicates the percentage of each class. Representative CaLOP described in each class is shown. The picture was taken 5 weeks after silencing. A total of 135 plants were silenced, with three independent experiments. A representative result is shown. Control (TRV-GFP) in this figure indicates GFP-silenced pepper. B, C Measurement of height and leaf area in silenced plants. The plant leaf area and height was measured 5 weeks after silencing each gene in pepper. Error bars represent standard deviation. Different letters above bars denote statistically different values according to Tukey’s honest significant difference test, p‹0.05]. D Semi-quantitative reverse-transcription polymerase chain reaction expression analysis of CaLOP in TRV-GFP, TRV-CaLOP (N-terminal) with inhibition of shoot growth phenotype and abnormal leaf shape (SG + Ab), and TRV-CaLOP (N-terminal) with inhibition of shoot growth phenotype (SG)-infiltrated pepper. The CaUBQ gene was used as a control. SG, inhibition of shoot growth; SG + Ab, inhibition of shoot growth and abnormal leaf shape.


