서 언
재료 및 방법
형질전환체 IGA 1번 계통의 T1 및 T2 세대 확보
도입된 전이유전자의 삽입위치 확인
T1 세대에서의 T-DNA 내부 구조 분석
T2 세대에서의 T-DNA 삽입 위치 확인 및 내부 구조 분석
IGA 1 계통의 세대별 PEITC 함량 분석
Quinone reductase(QR) 활성 측정
결과 및 고찰
형질전환체 IGA 1번 계통의 T1 및 T2 세대 확보
도입된 T-DNA 삽입위치 분석
도입된 T-DNA의 안정적 유전의 확인
PEITC 함량 조사와 암 예방 효과 확인
서 언
현재 유전자 변형(GM) 작물은 해충 및 제초제 저항성, 각종 스트레스 저항성, 그리고 기능성 물질 합성 증진 등을 위해 활발 히 개발되고 있으며 전 세계적으로는 옥수수, 밀, 콩, 면화 등의 여러 작물이 상업적으로 재배되고 있고 그 면적도 계속 증가하 고 있다(Bhalla, 2006; Chen et al., 2012; Stoger et al., 2005). 배추의 경우 2011년 배추게놈 프로젝트의 완료로 기존보다 더 좋 은 품질의 품종을 개발하기 위한 유전자 기능 연구가 가속화되었으며(Wang et al., 2011) 이를 기반으로 Agrobacterium을 이 용한 형질전환으로 다양한 저항성 증진 및 기능성 물질 다량 합성배추 등의 개발을 위한 연구가 진행되고 있다(Park et al., 2011; Yu et al., 2010, Yu et al., 2014). 특히 Park et al.(2011)은 glucosinolate의 2차 대사 산물 중 isothiocynate의 한 종류인 phenylethylisothiocyanate(PEITC)를 glutathione으로 전환해주는 glutathione S-transferase(GST) 유전자를 RNAi 벡터로 발현 억제시킴으로써 암 예방 물질인 PEITC의 양이 wild type 배추보다 2-3배 가량 증가한 형질전환 배추를 보고하였다. 이 와 같이 농업적 형질의 개선을 위해 개발된 GM 작물들은 품종화를 위해서 도입된 전이유전자(transgene)와 표현 형질의 발현 이 세대를 거쳐 안정적으로 유전되어야 하며 이를 위해 도입유전자의 삽입 위치, 구조의 변화 유무 및 전이유전자의 안정적인 발현을 반드시 확인해야 한다(Kumpatla et al.,1998; Matzke et al., 1995; Qin et al., 2014; Vain et al., 1999).
본 연구에서는 암 예방 효과가 있는 PEITC 물질이 증가한 배추 형질전환체 IGA 계통에 도입된 전이유전자와 표현형질인 PEITC 물질 증가의 후대 안정성을 확인하기 위하여 IGA 계통의 T1 및 T2 세대를 분석하였다. 먼저 도입된 전이유전자의 후대 안정성을 분석하기 위해 T-DNA의 삽입위치를 확인한 후 게놈 내로 도입된 전이유전자의 구조 변화 유무를 확인하기 위하여 T1 및 T2 세대에서 T-DNA의 내부 구조를 분석하였다. 또한 IGA 계통에서 GST 유전자의 발현조절로 인해 증가된 PEITC 함 량의 안정적인 발현 양상을 분석하고 최종적으로 PEITC의 암 예방 관련 활성을 확인하기 위해 IGA T1 및 T2 계통에서 쥐의 간 암세포를 이용하여 Quinone Reductase(QR) 활성을 측정하였다.
재료 및 방법
형질전환체 IGA 1번 계통의 T1 및 T2 세대 확보
Park et al.(2011)이 육성한, GST 유전자가 JJGST RNAi 벡터(Fig. 3A)로 발현억제 되어 PEITC 함량이 증가된 IGA 계통 중 T-DNA가 1 copy로 삽입된 IGA 1번 계통을 뇌수분 방법으로 T1 및 T2 세대로 진전시켜 본 연구에 이용하였다. T1 및 T2 계통 의 분석을 위해 세대 진전된 T1 및 T2 세대의 종자를 각각 14립씩 파종하여 선발 마커인 hygromycin 저항성 유전자(hpt)를 대 상으로 Park et al.(2011)에서 제시한 방법으로 PCR 분석을 수행하였다.
도입된 전이유전자의 삽입위치 확인
IGA 1 T1 계통(IGA 1-3)에서 T-DNA가 삽입된 위치를 확인하였다. 전이유전자의 삽입 위치 분석은 Lee et al.(2015)에서 제시한 방법에 따라 VA-TAIL(Variable Argument-Thermal Asymmetric Interlaced) PCR 방법으로 실시하였다. VA-TAIL PCR은 Lui and Whittier(1995)와 Lui and Chen(2007)이 제시한 8개의 AD primer와 pJJGST(Park et al., 2011; Fig. 2) 벡터를 기반으로 left border 방향에서 작성한 LSP1, LSP2, LSP3 및 LSP4, 그리고 right border 방향에서 작성한 RSP1, RSP2, RSP3 및 RSP4등 8개의 specific primer(SP)를 이용하여 수행하였다(Table 1). PCR 반응은 총 3차에 걸쳐 진행하였으며 1차 PCR은 추출된 T1 세대의 IGA 1 번 계통의 DNA, AD primer, LSP1 또는 RSP1 primer를 넣고 진행하고 1/10로 희석한 1차 PCR 반응 산물과 AD primer, LSP2 또는 RSP2 primer를 넣어 2차 PCR을 진행하였다. 마지막으로 3차 PCR의 경우 SP3와 SP4 primer 를 이용하였다. VA-TAIL PCR을 통해 생성된 PCR 산물은 pGemT-easy vector(Promega, USA)에 삽입한 후 염기서열을 분 석(Macrogen Co., Korea)하였다. 확인된 flanking DNA 염기서열은 “Flanking Sequence Tag Validator(FSTVAL)” 프로그램(GreenGene Bio Tech Inc., Korea)을 이용하여 배추 게놈 내 삽입 위치를 분석하였다K(im et al., 2012).
T1 세대에서의 T-DNA 내부 구조 분석
IGA 1번 계통의 T1 세대(IGA 1-3)로 도입된 T-DNA가 GST 유전자를 포함하는 JJGST RNAi 벡터와 다름없이 안정적인 지를 확인하기 위해 내부 구조를 PCR로 확인하였다. PCR을 실시하기 위해 IGA 1-3번 계통에서 확인된 flanking DNA sequence(FDS)를 바탕으로 left border쪽 FDS부터 JJGST 벡터의 hpt 영역까지, T-DNA지역을 mapping 할 수 있는 9 조합의 지역, OCS terminator부터 right border쪽 FDS영역까지 등 총 11 지역을 확인 할 수 있는 11 조합의 primer를 작성하였다(Table 2 and Fig. 3A). 각 primer는 700 bp-1 KB 정도의 PCR 산물을 획득하도록 하였으며 Tm 값은 57-62°C가 되도록 하였다. PCR 은 PCR Premix(MaximeTM PCR Premix, iNtRON biotechnology, Korea)를 이용하였으며 PCR 조건은 초기 denaturation 95°C 5분, denaturation 97°C 50초, annealing 57-62°C 30초, extension 72°C 1.5분으로 수행하였고 얻어진 PCR 산물은 아가 로즈 젤에 전기영동하여 목적 밴드를 확인 후 추출하여T -DNA 내부 염기서열 분석(Macrogen Co., Korea)을 하였다.
T2 세대에서의 T-DNA 삽입 위치 확인 및 내부 구조 분석
IGA 1-3 계통에 도입된 T-DNA가 T1 세대에서 T2 세대로 진전된 후 동일 위치상에 존재하는지 여부와 내부 구조를 확인하 기 위해 IGA 1-3-5번 계통에서 T1 세대의 분석과 동일한 11개의 primer 조합(Table 2)을 이용하여 PCR 분석을 하였다. 먼저 삽입 위치의 안정성을 확인하기 위하여 T1 세대에서 확인된 flanking DNA sequence(FDS)를 바탕으로 left border쪽 FDS부터 hpt 영역까지의 primer(F: 5′-TTGTGACACATTCGAA AATGCAG-3′, R: 5′-GTATATGCTCCGCATTGGT CTTG-3′) 와 OCS terminator부터 right border쪽 FDS영역까지의 primer(F: 5'-GCTCACTGAAGGGAAC TCCGGT-3', R: 5′-CGCAAA CTAACCAAAGTCCCACC-3′)를 작성하였다(Table 2). 또한 T2 세대로 도입된 T-DNA 구조의 변화 유무를 확인하기 위해서는 T1 세대에서 적용한 9 세트의 primer를 이용하였다. PCR 조건, 확인 및 염기서열 분석은 T1 세대 분석 시 이 용한 방법과 동일하였다.
IGA 1 계통의 세대별 PEITC 함량 분석
IGA 1번 계통의 T1 세대(1-3, 1-4, 1-5) 및 T2 세대(1-3-1, 1-3-5, 1-3-7)와 대조구인 CT001의 PEITC 함량을 HPLC 방 법으로 측정하였다. 함량분석을 위해 IGA 1번 계통의 T1 및 T2 세대의 잎을 동결건조 시킨 후 75mg의 powder를 1.5mL 증류수와 혼합하고 상온 조건에서 암상태로 18시간 동안 반응시킨 후 10분 동안 17000rpm으로 원심분리하여 상등액을 분리하였 다. 분리된 상등액 1.2mL에 20μL benzyl isothiocyanate(BITC)와 500μL methylene chloride(MC)를 첨가하여 다시 17000rpm 에서 5분 동안 원심분리하고 200μL의 하층(MC층)을 추출하였다. 추출한 MC층을 100μL의 derivatization reagent와 혼합하 여 30°C에서 한 시간 동안 유도체화를 진행한 후 질소 하에서 농축 하여 200μL의 acetonitrile/water(1:1)에 용해하고 syringe filtering 후 HPLC로 측정하였다.
HPLC 측정에 사용된 LC column은 Atlantis T3(250×4.6mm i.d., 5μm, Millford, MA)이며 flow rate는 0.8mL·min-1로 252nm의 파장에서 BEITC와 PEITC를 검출하였다. HPLC 반응 후 BITC와 PEITC의 standard curve를 작성하고 그에 따른 PEITC 함량을 계산했다.
Quinone reductase(QR) 활성 측정
IGA T1 및 T2 세대 형질전환체에서 Quinone reductase(QR) 활성을 측정하기 위해 쥐의 간암세포인 hepa1c1c7를 이용하여 Benson(1980)의 방법을 따라, 2-dichlorophenolindophenol(DCPIP)를 환원시키는 정도를 측정하였다. QR 활성은 1분간 감 소되는 흡광도와 DCPIP의 molar extinction coefficient로부터 환원된 DCIPIP 양을 계산하고 세포 균질액의 단백질 함량을 측 정하여 계산하였다.
결과 및 고찰
형질전환체 IGA 1번 계통의 T1 및 T2 세대 확보
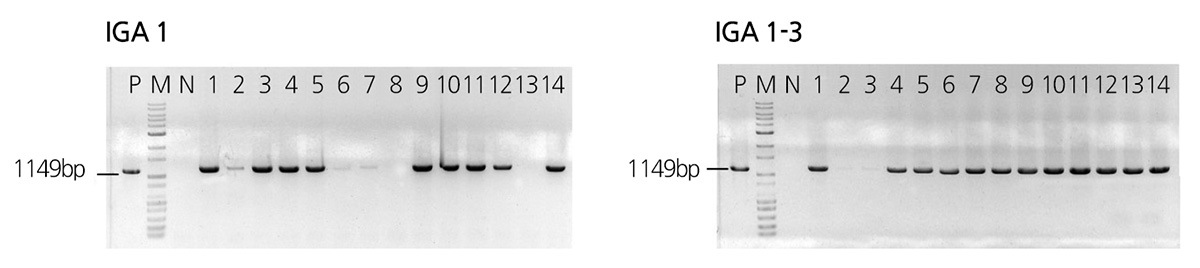
GST 유전자를 RNAi 방법으로 발현 억제시켜 PEITC 함량이 증가된 IGA 계통 중 T-DNA가 1 copy로 삽입되었으며 PEITC 물질함량이 높은 IGA 1번 계통을(Park et al., 2011) 뇌수분 방법으로 자가 수분하여 T1 및 T2 세대로 진전시켰다. 세대 진전 후 T-DNA가 유전된 T1 세대의 선발은 IGA 1번 종자를 14립 파종 후 본엽이 5-6잎 생성 시 DNA를 추출한 후 PCR 방 법으로 수행하였다. PCR 분석은 T1 세대 내로 도입된 pJJGST RNAi 벡터의 선발마커인 hpt 내의 1149bp의 지역을 대상으로 하는 primer를 이용하였으며 T1 세대에서는 14개의 개체 중 9개 개체에서 후 T-DNA가 유전된 것으로 확인되었으며(Fig. 1) 이 개체들 중 한 개체(IGA 1-3)를 선발하여 T2 세대로 진전시켰다. T2 세대에서도 T1 세대와 같은 방법으로 확인 결과 14개체 중 12개의 개체에서 T-DNA 삽입을 확인하였으며(Fig. 1) 확인된 개체들로 후대 유전 안정성 및 물질 검정에 이용하였다. 일 반적으로 Agrobacterium에 의한 형질전환 시 heterozygosus 하게 도입된 유전자는 T1 및 T2 세대로 진전되면 분리가 되어 비 형질전환체를 제외하는 선발과정이 필요하며 본 연구에서도 각 세대별 분리가 발생되어 선발 과정을 수행하였다
도입된 T-DNA 삽입위치 분석
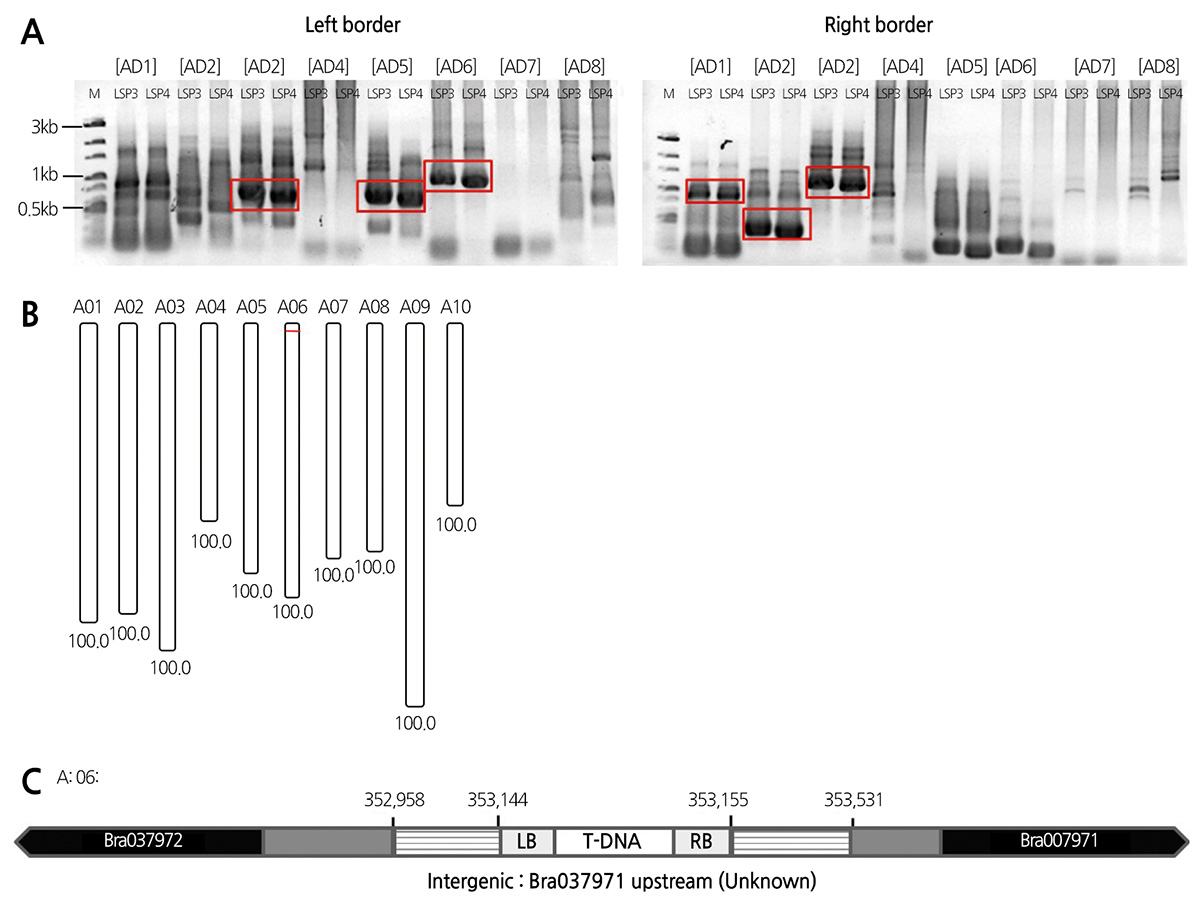
IGA 1-3번 계통의 게놈 내부로 도입된 T-DNA의 삽입위치를 확인하기 위해 VA-TAIL PCR을 실시 한 후 SP3 primer 및 SP4 primer가 사용된 3차 PCR 반응산물을 인접하여 로딩하고 특이적 밴드를 선발하였다(Fig. 2A). 특이적 밴드로는 PCR 산 물의 크기가 500 bp 이상이며 SP3의 반응산물보다 아래쪽에 위치한 SP4의 반응산물을 선발하였다. 이는 양쪽 border로부터 SP primer 작성시 SP4 primer 부터 border까지 대략 400 bp 정도로 하였기 때문에 배추 게놈 내 AD primer 인지 지역과 border 의 안쪽 SP4 primer 인지지역이 적어도 500 bp 이상일 것으로 예상되기 때문이었다. 따라서 IGA 1-3번 계통의 VA-TAIL PCR 결과 left border 쪽은 AD primer 3번, 5번, 6번에서 특이적인 밴드를 선발하였으며 right border 쪽은 AD primer 1번, 2번, 3번에서 특이적인 밴드를 선발하였다(Fig. 2A). 선별된 특이적 PCR 밴드는 추출하여 염기서열 분석을 통해 T-DNA가 삽입 된 근처의 flanking DNA sequence(FDS)를 확인하였다. 확인된 FDS를 FSTVAL을 통해 분석한 결과 IGA 1-3번 계통에 도입 된 pJJGST의 T-DNA는 배추의 6번 염색체의 353,144-353155지역에 위치함을 알 수 있었으며(Fig. 2B) 이는 Bra037972유 전자(unknown)와 Bra007971유전자(unknown) 사이의 intergenic region(Fig. 2C)으로 확인할 수 있었다.
GM 작물의 상업화를 위한 안정성 확인은 도입유전자의 삽입위치의 확인이 필수적으로 요구된다. 도입유전자의 삽입위치 는 1-copy로 작물의 게놈 내로 전이되었을 때 확인이 용이하며 또한 T-DNA의 삽입이 low copy일수록 GM 작물의 안정성을 확보할 수 있다(Pla et al., 2012). Agrobacterium을 매개로 한 식물형질전환은 자연상태에서 발생하는 현상을 응용한 것으로 원 하는 유전자가 포함된 T-DNA가 plasmid로부터 대상식물의 게놈 내부로 도입되도록 하는 방식이며 유전자 총을 이용한 형질 전환보다 적은 copy수로 T-DNA가 도입되는 장점이 있다(Brenda et al., 2009; Dai et al., 2001; Shou et al.,2004). T-DNA의 low copy수 도입은 multi-copy수의 도입보다 도입유전자의 silencing 현상으로 인한 발현억제의 확률이 낮게 존재하므로(Iyeret al., 2000; Vaucheret et al., 1998) GM 작물의 안정성의 필수 조건이라 할 수 있다. 또한 외래 유전자의 도입으로 인하여 내부 유전자의 변형이 유기될 수 있어 T-DNA 삽입이 유전자 부위가 아닌 intergenic 부위에 삽입될 때 작물의 안정성을 확보할 수 있으며 이를 위해 게놈 내로 도입된T -DNA의 위치를 확인하는 것은 필수적이라 할 수 있다.
따라서 IGA 1-3번 계통은 T-DNA pJJGST가 배추 게놈 내로 1 copy로 도입되었으며 도입 위치 또한 6번 염색체에서 유전 자와 유전자 사이인 intergenic 부위에 삽입된 것으로 분석되어 T-DNA의 삽입이 안정적으로 이루어졌다고 판단된다.
도입된 T-DNA의 안정적 유전의 확인
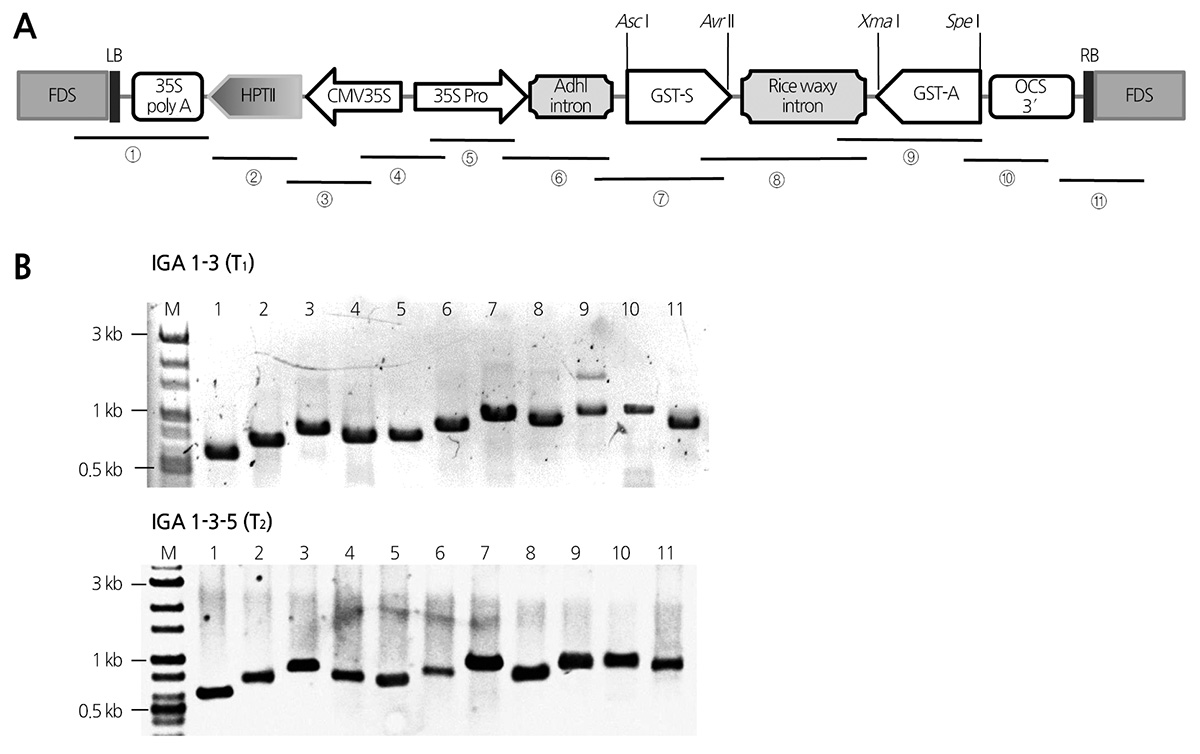
IGA 1-3번 계통의 세대진전에 따른 T-DNA 삽입위치의 동일성을 확인하고 T-DNA의 내부 구조를 확인하기 위해 IGA 1-3 계통과 IGA 1-3-5 계통에서 PCR을 실시하였다. 먼저 세대 진전에 따른 T-DNA의 유전이 변이 없이 이루어짐을 확인하 기 위해 IGA 1-3계통에서 확인된 flanking DNA sequence(FDS)를 바탕으로 FDS부터 left border쪽 지역(Fig. 3A①)과 right border쪽에서 FDS영역까지(Fig. 3A⑪)의 primer를 작성하였다. 한편 도입된 T-DNA의 내부의 변이 여부를 확인하기 위해 T-DNA 내부를 mapping할 수 있는 9 조합의 primer를 추가적으로 작성하였으며 총 11개의 PCR primer sets를 통해 도입된T-DNA의 안정성을 분석하였다. PCR 결과(Fig. 3B) IGA 1-3 계통과 IGA 1-3-5 계통의 PCR 반응산물 중 1번과 11번 lane 의 위치가 각 626 bp, 988 bp에서 확인된 것으로 보아 IGA 1-3 계통으로 도입된 T-DNA가 세대진전을 통해 안정적으로 IGA 1-3-5 계통으로 유전되었음을 확인하였다. 또한 2-10번 lane의 PCR 반응산물 역시 Table 2에 제시한 목적 크기와 같은 위치 에서 확인되는 것으로 보아 배추 유전체 내로 T-DNA의 내부 구조 변화 없이 안정적으로 삽입이 이루어졌음을 확인하였다. 마지막으로 각각의 PCR 밴드를 추출하여 확보된 염기서열을 연결하여 pJJGST 벡터와의 상동성을 확인하기 위해 BLAST Align을 실시한 결과 T-DNA의 후대 유전이 매우 안정적임을 확인할 수 있었다 .
PEITC 함량 조사와 암 예방 효과 확인
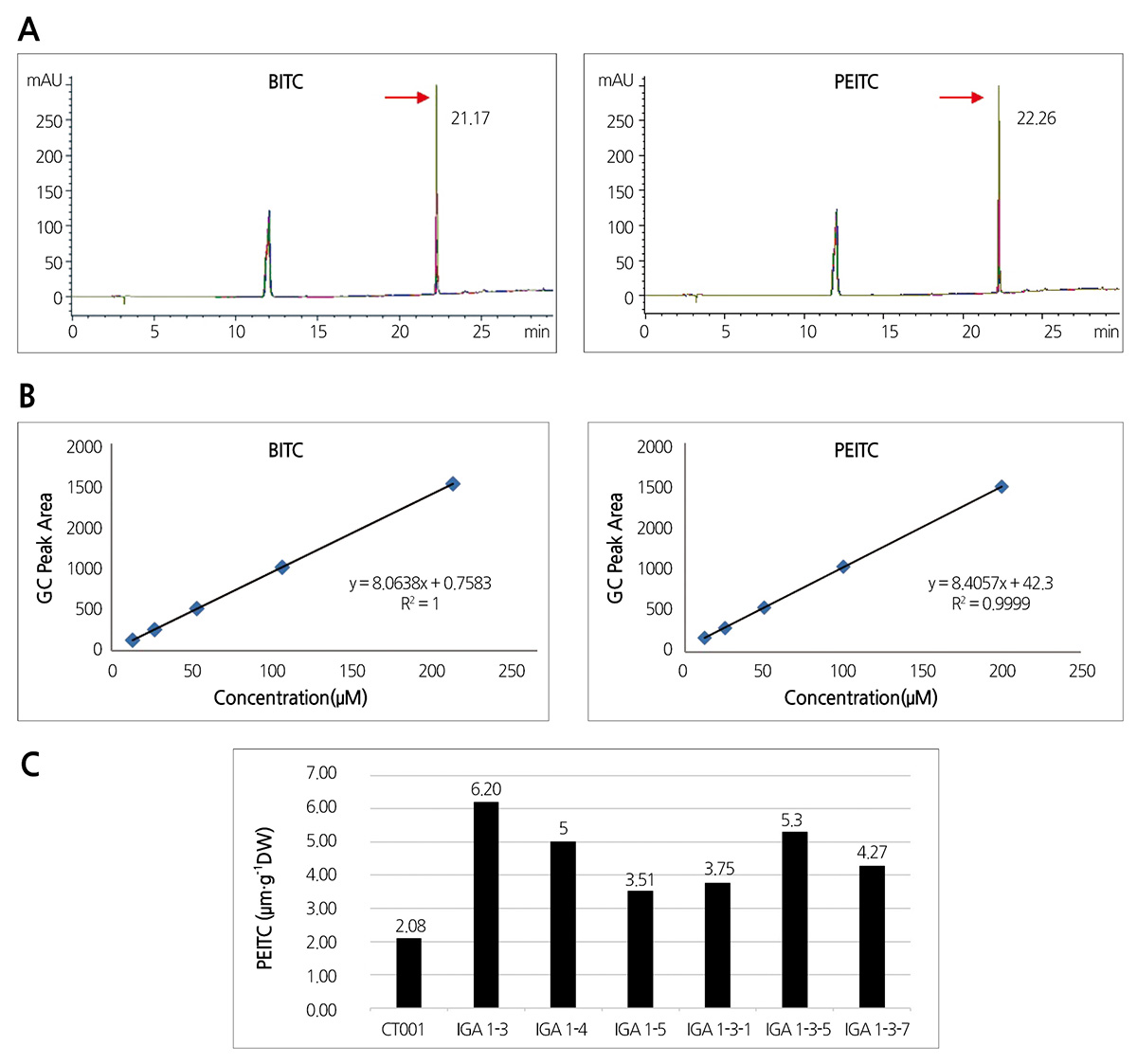
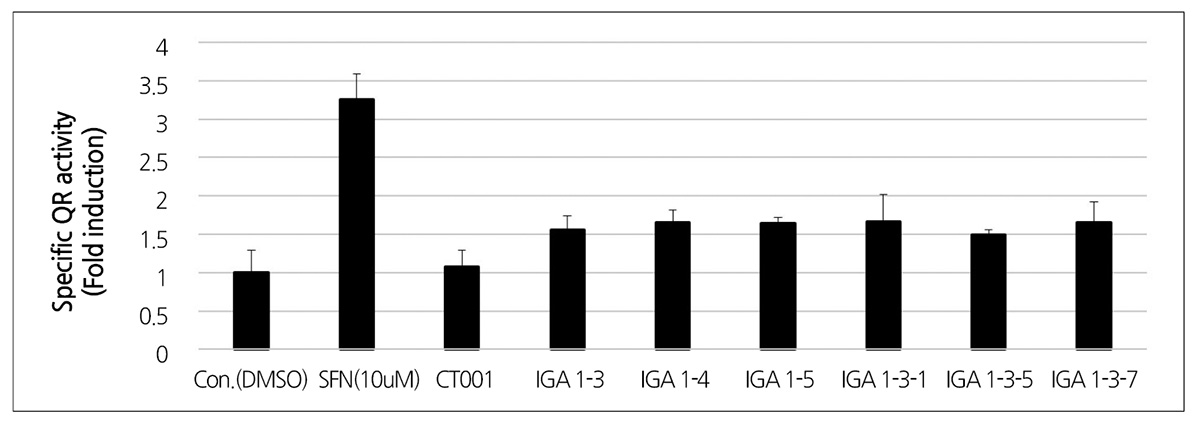
IGA 1번 계통의 T1 세대 및 T2 세대와 대조구인 CT001의 PEITC 함량을 측정하기 위해 HPLC 분석을 실시하였다. 배추시 료에서 PEITC 함량을 정확하게 측정하기 위해 benzyl isothiocyanate(BITC)를 첨가하여 내부 보정 물질로 사용하였으며 BITC는 21.17분, PEITC는 22.26분에 peak가 검출되었다(Fig. 4A). HPLC로 BITC와 PEITC의 peak area를 계산하기 위해 농 도 별로 각각의 standard curve를 작성 하였으며 T1 세대 및 T2 세대의 PEITC 함량 분석은 각 세대별로 3개의 개체들을 선발하 여 IGA 1번 계통의 T1 세대(IGA 1-3, 1-4, 1-5) 및 T2 세대(IGA 1-3-1, 1-3-5, 1-3-7)와 대조구인 CT001의 PEITC 함량을 계산하여 그래프로 나타냈다(Fig. 4B). HPLC로 PEITC 함량의 분석결과 대조구인 비형질전환체 CT001은 PEITC 함량이 건 조질량 당 2.08μM·g-1 이 검출되었으며 IGA T1 및 T2 세대 형질전환체에서는 건조 질량 당 3.51-6.20μM·g-1 의 PEITC가 측 정되었다. 따라서 IGA 1번의 T1 및 T2 계통에서 PEITC 함량이 CT001 보다 2-3배 증가한 것을 확인 하였으며, 이 계통들의 암예방 효과를 확인하기 위하여 Quinone Reductase(QR) 활성을 확인하였다. QR 활성은 활성산소 등에 의해 발생되는 발암원 들을 제거하는데 효과적으로 알려져 있는 Phase II detoxification 증진 기능으로 알려져 있어, 암 예방 효과를 확인하기 위한 기 내 실험에 많이 활용되고 있다(Ku et al., 2014). PEITC 농도와 유사하게, QR 활성도 비형질전환체 CT001에 비해 IGA T1 및 T2 세대 형질전환체에서 비교적 높은 QR 활성 경향을 보인 바, 형질전환체에서 증가된 PEITC 농도가 QR 활성의 증가를 나타 낸 것으로 판단된다. QR 활성 실험에 있어 SFN은 브로콜리 등에서 잘 알려져 있는 QR 유도 isothiocyanate 성분으로 본 실험 에서는 PEITC에 의한 QR 유도능 분석에 대한 positive control로서 사용되었다(Fig. 5).
| |
Fig. 5. Induction of quinone reductase in Hepalclc7 cell by extracts of IGA 1 T1 and T2 generation transgenic plants. DMSO, Nontreated control; SFN, Positive control; CT001, Plant control. | |
GM 작물의 안정성은 형질전환 대상 작물로 도입된 T-DNA에 대한 정보를 분자수준에서의 확인 뿐만 아니라 비형질전환 체와 비교하여 조절된 도입유전자에 의해 변화된 표현형 특징들이 세대가 진전됨에도 안정적으로 발현됨과 동시에 기존의 형 질들은 유지되어야 한다(Chen et al., 2012; Pla et al.,2012; Qin et al., 2014). 기 보고된 IGA 1번 계통은 Park et al.(2011)의 연구에서 비형질전환 개체인 CT001(Inbred line)와 비교하여 표현형으로 나타나는 원예적 형질의 차이가 없음을 확인하였고 GST 유전자가 RANi 벡터에 의해 발현 억제됨을 real-time RT PCR로 확인하였으며 GST의 발현량 감소에 따른 PEITC 함량 의 증가됨을 확인 하였다. 본 연구에서는 세대 진전으로 확보된 T1 세대의 형질전환체인 IGA 1-3, 1-4, 1-5번 계통과 T2 세대 의 1-3-1, 1-3-5, 1-3-7번 계통에서 도입유전자로 인한 GST의 발현 억제에 따른 PEITC 함량을 분석한 결과 비 형질전환체 인 CT001보다 2-3배 가량 증가함은 물론 세대진전이 되어도 안정적으로 유지되는 것을 확인하였다. 또한 QR 활성 분석으로 확인된 암 예방 효과도 우수하며 안정적으로 유지됨을 볼 수 있었다.