서 언
재료 및 방법
공시품종 및 DNA 추출
Microsatellite 분석
유전적 유연관계 분석을 통한 품종식별력 검정
결 과
Microsatellite 분석
gMS 마커를 이용한 품종식별력 검정
eMS 마커를 이용한 품종식별력 검정
gMS와 eMS 마커의 병합시 품종식별력 검정 및 마커 간 상관분석
고 찰
서 언
박과식물(Cucurbitaceae)중 수박속(Citrullus) 식물은 남아프리카가 원산인 Citrullus lanatus, 북아프리카와 중동 원산인 Citrullus colocynthis, 서남 아프리카 원산인 Citrullus ecirrhosus와 Citrullus naudinianus, 인도 원산인 Citrullus fistulosus으로 분류되고, Citrullus lanatus는 var. lanatus와 var. citroides 2종의 변종군으로 나누어지며, 우리가 식용으로 이용하는 수박은 C. lanatus var. lanatus에 속한다(Bates and Robinson, 1995). 우리나라의 수박 재배 면적은 2013년 기준 14,885ha(노지:2,586, 시설:12,299ha)이며, 생산량의 경우 672,914톤에 이를 정도로 박과작물 중에서 경제적 가치 면에서 중요도가 가장 크다(http://www.mafra.go.kr). 우리나라에서 육성된 수박 품종은 2014년 기준 수입생산판매 신고된 658 품종과 품종보호 출원된 130 품종 및 품종보호등록 설정된 69 품종이 유통되고 있다(http://www.seed.go.kr).
우리나라의 수박 품종 육성 방법은 잡종강세를 이용한 F1 품종 개발이 주류를 이루고 있다. 주요 품종 육성 목표는 당도, 내병성, 과형, 저온 적응성의 개선에 주력하고 있으며, 최근에는 소비자의 기호도가 다양해짐에 따라 씨 없는 3배체 수박, 과피와 과육의 색깔이 노란 수박, 과피가 흑색이거나 진한 녹색인 품종이 육성되어 농가에 재배되고 있다. 그러나 ‘Sambokggul’과 같이 높은 당도를 가진 단타원형 수박에 대한 소비자의 선호도가 높아지면서 품종 육종 목표도 이와 같은 방향으로 이루어져 왔기 때문에 종자회사에서 육성 및 판매되고 있는 수박 품종은 유전적으로 아주 가까운 것으로 추정되어 형태적 특성 및 유전자 분석에 의한 유전자원의 특성평가 및 품종 지문화 작업은 단순하지 않은 것으로 알려지고 있다(Che et al., 2003; Jarret et al., 1996; Lee et al., 1996).
식물의 genome 내에 존재하는 단순반복 염기서열의 차이를 이용하는 microsatellite 마커가 2000년대 초반부터 수박에서도 개발되기 시작하여 이를 유전자원 특성평가에 활용하는 연구결과가 보고되기 시작하였다(Guerra-sanz, 2002; Joobeur et al., 2006; Mujaju., et al., 2010). 최근, 차세대 자동 염기서열 분석기를 활용한 작물별 유전체 해독에 대한 연구가 활발해지면서 수박의 경우도 698개의 simple sequence repeats (SSR) 마커를 개발하여 정밀도 높은 유전자 지도 작성 및 수박 유전자원의 특성평가에 활용한 연구 결과도 보고되고 있다(Ren et al., 2012; Zhang et., 2012). 그리고 스페인에서 국제 박과 작물 유전체 연구가 수행되면서 expressed sequence tag (EST)에서 유래된 SSR 마커를 개발하여 그 정보를 공개하고 있다(http://www.icugi.org).
우리나라의 경우 국립종자원에서 멜론, 오이에서 유래된 SSR 마커와 기 보고된 수박 SSR 마커를 활용하여 수박 시판 품종 식별 체계를 구축하여(Kwon et al., 2007; Kwon et al., 2010), 이를 품종보호 출원품종에 대한 비교품종 선정 및 품종진위성과 관련된 종자분쟁의 해결 수단으로 활용하여 왔다. 그러나 마커의 다형성 정도가 높지 않아 많은 수의 마커를 활용하기 때문에 분석 기간과 노력 및 비용이 많이 소요될 뿐만 아니라 형태적 특성 차이가 있는 몇몇 품종들은 식별이 되지 않은 문제점이 제기 되었다. 따라서 최근에 개발된 수박 EST 및 genomic microsatellite 마커를 이용하여 수박 품종식별용 신규 마커를 개발하고 이를 활용한 수박 시판 품종에 대한 정밀도 높은 데이터베이스 구축은 품종보호 재배 심사의 정밀도 제고, 품종 진위성과 관계된 종자 분쟁, F1 종자의 순도검정 등 여러 가지 분야에 매우 유용하게 활용될 수 있을 것이다.
본 연구에서는 우리나라에서 최근에 육성되어 판매되고 있는 수박 99개 F1 품종과 농촌진흥청 원예특작과학원에서 육성된 자식 계통 3개 품종에 대한 정밀도 높은 DNA 프로파일 데이터베이스를 구축하고자, 최근에 개발된 genome과 EST에서 유래된 microsatellite를 활용하여 두 마커의 형태 간 다형성 정도의 비교 분석과 품종간 유연관계를 활용한 품종식별력 검정에 대한 일련의 연구를 수행하여 얻어진 결과를 보고하고자 한다.
재료 및 방법
공시품종 및 DNA 추출
본 연구에서는 국내에서 유통되고 있는 있는 수박 99개 F1 품종과 농촌진흥청 원예특작과학원에서 육성된 자식 계통 3개 품종을 공시하여 품종별 microsatellite 마커를 이용한 데이터베이스 구축에 활용하였다(Table 1). 공시 품종의 종자 10립을 무작위로 추출하여 마쇄한 다음 NucleoSpin®Plant II(Macherey-Nagel Cat. 740 770.250, Germany) 키트를 이용하여 게놈 DNA를 분리 하였다. 분리된 DNA는 2.5% 아가로스 젤에서 전기 영동하여 DNA 농도를 확인한 후 μL당 20ng의 농도로 희석하여 microsatellite 분석에 이용하였다.
Microsatellite 분석
수박 품종식별에 효과적인 microsatellite 마커를 선발하기 위하여, ‘Hwalgichanggul’, ‘Miinggul’, ‘Megaspeedggul’, ‘Gyeoulae’, ‘Jijonggul’, ‘Saecheonnyeonggul’, ‘Ssizero’, ‘Haechanggul’, ‘Sambokggul’, ‘Speedggul’, ‘Heukmi’ 품종을 대상으로 하여 중국과 미국에서 공동으로 개발하여 유전자 지도에 위치시킨 microsatellite primer 220개(Ren et al., 2012)와 국제 박과작물 게놈프로젝트(http://www.icugi.org)에서 개발된 EST 유래의 microsatellite primer 80개를 대상으로 염색체상의 위치, 반복염기서열 정도 등을 고려하여 수박 11품종에 대한 microsatellite primer별 다형성 정도를 조사하였다.
Polymerase chain reaction(PCR)을 통한 유전자 증폭 산물은 Genetic Analyzer(HDA-GT12TM System, eGEnE, USA)를 이용하여 전기 영동하고 컴퓨터 프로그램(Biocalculator 2.0)을 활용하여 각 품종별 대립 유전자의 차이를 분석하였다. 반복 재현성이 높고 밴드의 패턴이 깨끗한 나타난 프라이머의 정방향에 FAM, VIC, NED, PET의 화학 물질(Cat. 450056, Life Technology, USA)중 한가지로 형광 표지한 다음 수박 102품종(Table 1)에 대한 DNA 프로파일 데이터베이스 구축에 이용하였다.
PCR 반응은 게놈 DNA 60ng, 0.1μM의 SSR primer, 2.0μL dNTP mixture(2.5mM), HS prime taq polymerase(Cat. G-7002, Genet Bio, Korea) 1.0U, 2.5μL의 10×PCR buffer(50mM KCl, 20mM Tris-HCl, pH 8.0, .0mM MgCl2)에 증류수를 첨가하여 전체 부피를 25μL로 조절하였다. PCR(Cat. C1000, BioRad, USA) 증폭은 94°C에서 30초간 denature 한 후, 55°C에서 30초 annealing, 72°C에서 45초간 extension을 40 cycle 수행하였다. PCR이 완료된 후 3.0μL의 증폭산물을 2.5% 아가로스 젤에서 전기 영동하여 증폭 여부를 확인한 다음, 초순수 150μL에 PCR 산물 1.5μL를 희석하였다. 희석된 PCR 증폭 산물 1.5μL는 Hi-Di formamide(Cat. 4311320, Life technology, USA) 10μL, GeneScan LIZ500 size standard (Cat.4322682, Life technology, USA) 0.25μL를 혼합한 다음 94°C에서 2분간 변성시켰다. 변성시킨 PCR 증폭 산물은 자동염기서열분석기(Genetic Analyzer 3130XL, Applied Biosystem, USA)를 활용하여 전기 영동한 다음 GeneMapper(version 3.7) 컴퓨터 프로그램(Applied Biosystem, USA)을 이용하여 분자 마커별 대립 유전자의 크기를 결정하였다.
EST 및 genome 서열에서 유래된 microsatellite 마커의 다형성 정도를 비교하기 위하여 아래의 공식을 이용하여 Polymorphism information content(PIC) 값을 산출하였다. 아래 식에서 n은 마커당 분석되어지는 대립유전자의 수, Pij는 마커 i의 밴드들 중에서 j번째 공통 밴드 패턴의 빈도수이다(Anderson et al., 1993).
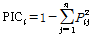
유전적 유연관계 분석을 통한 품종식별력 검정
Microsatellite 분석을 통하여 재현성이 높고 다형성을 보이는 대립유전자를 마커로 선발하여 대립유전자의 유무(dominant marker scoring; present = 1. absent = 0)에 따라 NTSYSpc(version 2.10b)(Rohlf, 2000) 컴퓨터 프로그램에 입력하고 Jaccard 방법(Jaccard, 1908)에 준하여 유전적 유사도 값을 계산한 다음 unweighted pair-group method with arithmetical average(UPGMA)(Sneath and Sokal, 1973) 방법으로 집괴 분석하고 계통도를 작성하여 microsatellite 마커의 품종 식별력을 비교 분석하였다. 그리고 Mantel matrix 분석 방법(Mantel, 1967)에 의하여 EST와 genomic에서 유래된 microsatellite를 근거로 작성된 계통도 및 2종류의 마커를 병합하여 작성된 계통도와 상관 정도를 분석하였다.
결 과
Microsatellite 분석
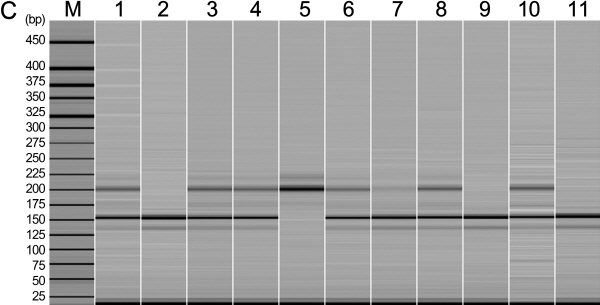
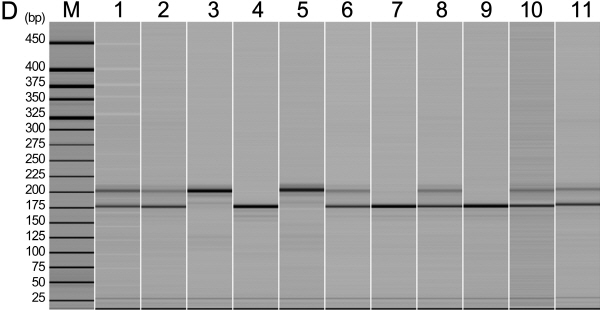
수박의 품종별 microsatellite 데이터베이스 구축에 효과적인 분자 마커를 선정하기 위하여, ‘Hwalgichanggul’ 외 10개 품종을 활용하여 genomic에서 유래된 microsatellite(gMS) 프라이머 220개와 EST에서 유래된 80개의 microsatellite(eMS) 프라이머에 대하여 다형성 정도를 조사한 바(Fig. 1), gMS 프라이머 220개 중에서 204개는 다형성을 보이지 않거나 3배체 수박인 ‘Ssizero’나 수박의 과피색이 흑색인 ‘Heukmi’ 품종과 같이 형태적 특성이 다른 1-2개 품종에서만 다형성을 나타내는 프라이머는 수박 품종별 데이터베이스 구축에 제외시켰다. 나머지 16개는 공시된 품종 내에서 높은 다형성을 나타낼 뿐만 아니라 우리나라 수박 대표 품종인 동부팜한농의 ‘Sambokggul’과 농우바이오의 ‘Speedggul’ 품종에 대하여 뚜렷한 대립 유전자의 차이를 나타내었다. 한편, 국제 박과작물 게놈 프로젝트에서 개발된 eMS 프라이머 80개를 11품종에 대하여 검정하였을 때 79개의 프라이머가 다형성을 나타내지 않았고 1개의 프라이머(WMU3039)만이 다형성을 보였다. 따라서 수박의 유전적 유연 관계를 통한 품종 식별력 검정에 gMS 마커와 eMS 마커 간에 비교 분석이 어려웠기 때문에 Kwon(2013)이 300개 eMS 마커를 분석하였을 때 국내 수박 F1 품종에 다형성이 높다고 보고한 9개와 본 연구에서 선발된 1개 프라이머를 활용하였다. 따라서 총 26개의 microsatellite 정방향 프라이머의 5’-말단에 형광물질인 FAM, VIC, NED, PET를 각각 표지하여 수박 102품종의 genomic DNA와 PCR하고 증폭 산물은 자동염기서열분석기를 이용하여 전기 영동한 다음 다형성 정도를 조사한 바(Table 2), gMS 마커는 대립유전자의 수가 2-9개로 다양하게 나타났으며 총 58개의 대립유전자가 검출되었고, 마커 당 평균 대립유전자의 수는 3.63개로 나타났다. 한편 각 마커 별 공시 품종의 유전적 다형성 정도를 나타내는 지수인 PIC 값은 0.257-0.640의 넓은 범위에서 분포하였으며, 평균값은 0.479로 나타났다. 그리고 16개의 microsatellite 프라이머 가운데 9개 프라이머(BVWS00155, BVWS00297, BVWS01734, BVWS00441, BVWS00233, BVWS01897, BVWS00433, BVWS00209, BVWS00288)는 0.5 이상의 높은 PIC 값을 나타내었다. 그러나 eMS 마커의 경우 대립유전자의 수는 2-6개의 범위에 분포하는 것으로 분석되었지만 8개의 마커에서 2개의 대립유전자만이 검출되어 평균 대립유전자의 수가 2.5개에 불과하였다. 평균 PIC 값은 0.425로 나타났고, 0.5이상의 PIC 값을 가지는 microsatellite 마커는 1개(WMU0056)에 불과하였다. 따라서 gMS 마커가 eMS 마커보다 대립유전자의 수와 PIC 값에서 높은 경향을 나타내었다.
gMS 마커를 이용한 품종식별력 검정
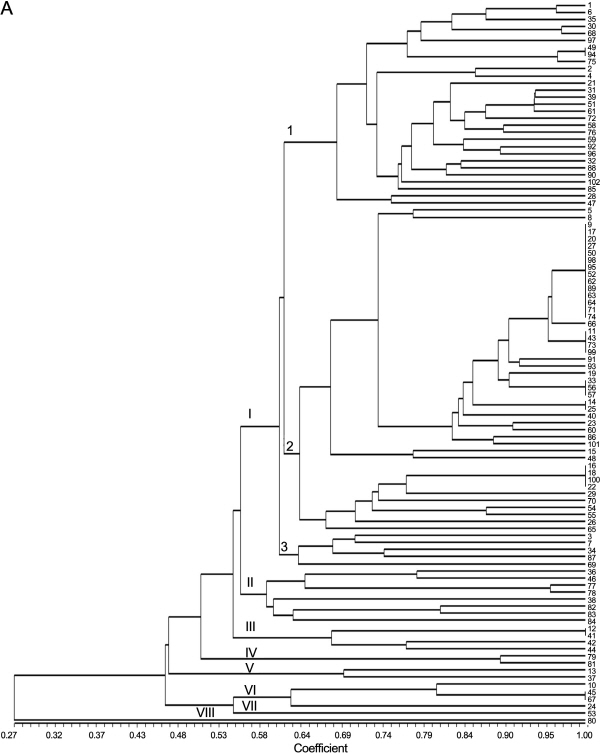
수박 11품종을 활용하여 선발된 다형성 정도가 높은 16개gMS 마커를 이용하여 수박 102개 품종에 대한 유전적 유사도 및 품종식별력을 조사한 바(Fig. 2A), 공시 품종의 전체 유사도 지수는0.27-1.00의 범위에 속하였고, 유전적 유사도 지수 0.57에서 8개의 대그룹으로 구분되었다.
I 그룹은 ‘Speedggul’ 등 80품종이 속하였고 유전적 유사도 지수 0.61에서 3개의 소그룹으로 구분되었으며 I-1 소그룹에는 ‘Speedggul’ 등 29품종이 속하였으며 농우바이오에서 육성된 ‘Speedggul’과 ‘Hwansanggul’, 농협종묘에서 육성된 ‘Haedongggul’과 삼성종묘의 ‘SSggul-plus’, 아시아종묘의 ‘Smartggul’과 고농종묘의 ‘Gononggyeoul’ 및 제농종묘의 ‘Firstggul’은 95% 이상의 높은 유전적 유사도를 나타내었으며, 특히 ‘Smartggul’과 ‘Firstggul’은 본 연구에서 활용된 분자마커에 의해 식별이 되지 않았다. I-2 소그룹은 ‘Sambokggul’ 등 46품종이 그룹화되었는데 이 품종들 중에서 24개 품종의 식별이 가능한 것으로 분석되었다. 유전적 유사도가 100%를 나타낸 ‘Sambokggul’ 등 14품종군, ‘Gohyanggul’ 등 4품종군 ‘Superggul’ 등 3품종군, ‘KP-4’와 ‘Hwanheuiggul’, ‘Joeunggul’ 등 4품종군들의 경우 특정 품종을 계통 분리하여 품종 육성 재료로 이용했기 때문이라고 추정되며 이들 품종에 대해서는 형태적 특성 조사 등을 활용한다면 품종의 구별성 여부를 명확하게 판단할 수 있을 것으로 사료된다. 한편, 2010년 품종보호 출원된 ‘Hwanheuiggul’의 경우 본 연구에 활용된 분자 마커로 검정하였을 때 ‘KP-4’와 구분이 되지 않았는데 이 두 품종의 경우 형태적 특성조사에서도 뚜렷한 구별성을 나타내지 않아 품종보호 출원된 ‘Hwanheuiggul’의 품종보호 등록이 거절된 바 있다. I-3 소그룹은 ‘Bravoggul’ 등 5품종이 속하였고 분자 마커의 유전자형에 의해 모든 품종이 뚜렷하게 구분이 되었다.
II 그룹은 과실의 형태가 원형이면서 과실 표면의 색깔이 진한 녹색이거나 검은색인 ‘Heukbo’, ‘Heukho’, ‘Blackball’, ‘Blackhall’, ‘Kinglyco’, ‘Lycosweet1’, ‘Lycosweet2’, ‘Lycofresh1’ 8품종이 그룹화 되었으며 모든 품종이 뚜렷하게 식별되었으나 ‘Blackball’과 ‘Blackhall’은 95% 이상의 유전적 유사도를 나타내어 이 두 품종의 경우 형태적 특성 조사를 통한 품종의 유사성 여부가 검토되어져야 될 것으로 사료된다.
III 그룹은 동부팜한농의 ‘Well-being’, ‘Dalgona’, ‘Manidara’, ‘Myungaggul’ 품종이 그룹화 되었고, 품종보호 등록된 ‘Well- being’과 ‘Dalgona’의 경우 100%의 유전적 유사도를 나타내어 DNA 검정의 추가적 실시와 형태적 특성 조사를 통해 품종의 구별성 여부를 재검토 해야 될 것으로 사료된다.
IV 그룹은 농촌진흥청에서 육성된 품종으로서 과형이 원형에 가까우면서, 과피색은 녹색이고 과육색이 적색인 ‘Codiwon’과 ‘Seediwon’이 속하였으며, V 그룹은 ‘Goldmat’과 ‘Jijonggul’ 두 품종이 포함되었다. VI그룹은 미니형 수박인 ‘Kkoma’, ‘Bok’, ‘Chamjoabok’ 3개의 품종이 분포하였고, VII 그룹은 과실 바탕색의 녹색이 짙고 줄무늬가 매우 넓은 긴 장타원형의 중대과종이면서 과육색은 노랑색인 ‘Super-gold’가 속하였다. VIII 그룹은 농촌진흥청에서 육성된 수박으로 과형이 단타원형으로 과피는 회록색에 줄무늬가 없으며 황적색 과육을 가지는 ‘Sosowon’ 1개의 품종이 위치하였다.
eMS 마커를 이용한 품종식별력 검정
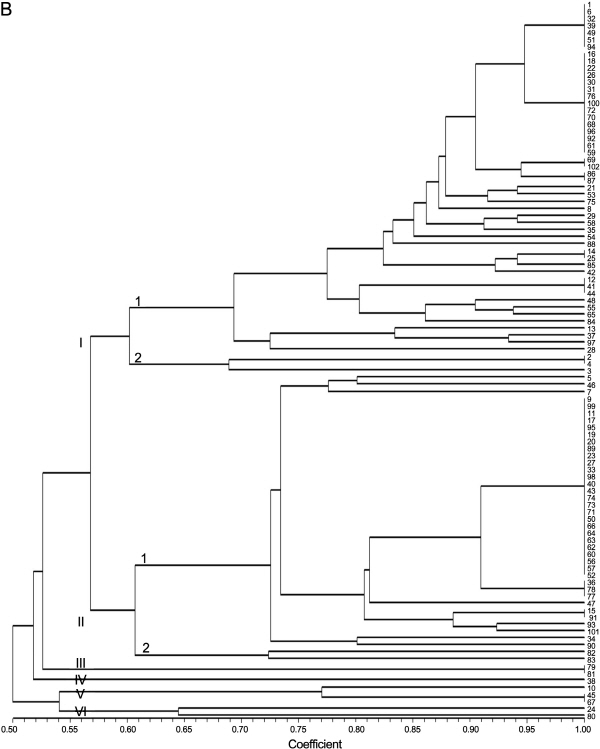
10개의 eMS 마커를 이용하여 검출된 대립유전자의 크기를 근거로 수박 102개 품종에 대한 품종식별력을 조사한 바(Fig. 2B), 공시 품종의 전체 유사도 지수는0.50-1.00의 범위에 속하였고, 유전적 유사도 지수 0.57에서 6개의 대그룹으로 크게 구분됨을 확인할 수 있었다.
I 그룹은 ‘Speedggul’ 등 53품종이 포함되었고 유전적 유사도 지수 0.61에서 2개의 소그룹으로 구분되었으며 I-1 소그룹에는 ‘Speedggul’ 등 50품종이 속하였고 I-2 소그룹은 농우바이오에서 육성된 ‘Wonderfulggul’, ‘Megaspeedggul’, ‘Bravoggul’ 3품종이 포함되었다. 총 53품종중 27품종만이 microsatellite의 유전자형에 의해 식별이 가능한 것으로 나타났다.
II 그룹은 ‘Sambokggul’ 등 41품종이 속하였고 유사도 지수 0.62에서 2개의 소그룹으로 그룹화되었으며 41품종중에서 품종 특이적인 유전자형은 13개에 불과할 정도로 품종식별력이 낮은 경향을 나타내었다. III 그룹은 농촌진흥청에서 육성된 ‘Codiwon’과 ‘Sosowon’이 100%의 유전적 유사도를 가지면서 그룹화 되었고, IV 그룹은 농협종묘에서 육성된 ‘Kinglyco’ 품종이 속하였다. V 그룹은 미니수박인 ‘Bok’과 ‘Chamjoabok’ 및 ‘Kkoma’ 품종이 그룹화 되었으며, VI 그룹은 과육의 색깔이 황색 계열인 ‘Mini-yellow-queen’과 ‘Sosowon’이 속하였다. EST 유래된 microsatellite 마커를 활용하여 작성된 계통도를 볼 때 과피색이 흑색인 ‘Heukmi’ 품종이 일반형 수박과 구분이 되지 않을 정도로 품종식별력이 낮은 것으로 분석되었다.
gMS와 eMS 마커의 병합시 품종식별력 검정 및 마커 간 상관분석
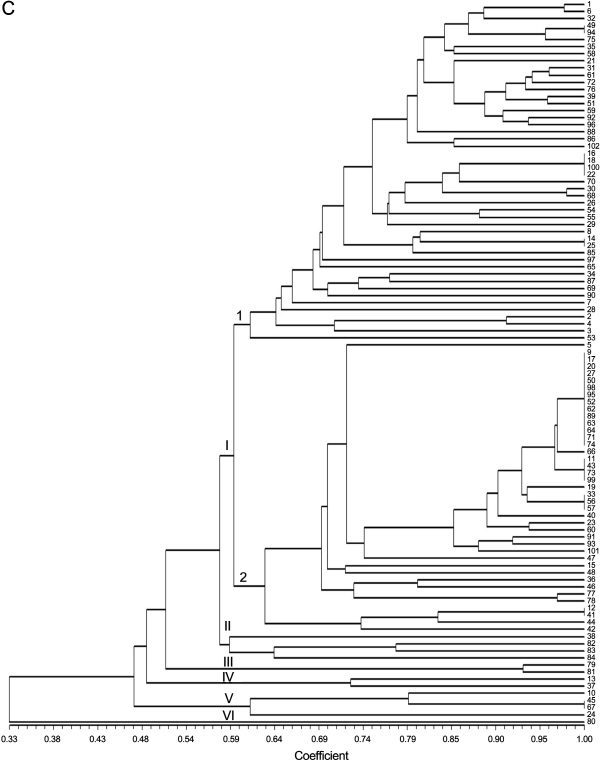
시판중인 수박 품종에 대하여 높은 다형성을 보인 gMS 마커 16개와 eMS 마커 10개를 이용하여 통합화된 계통도를 작성하였을 때(Fig. 2C), 유전적 유사도는 0.33-1.00의 범위에 속하였다. 품종식별력의 경우 gMS 마커 분석에서 100% 유전적 유사도를 나타낸 품종군들은 gMS와 eMS 유래의 마커를 병합하였을 경우에도 품종의 식별이 가능하지 않은 것으로 분석되었다. 따라서 본 연구에서 활용된 gMS에서 유래된 16개의 마커만 활용하여도 우리나라에서 시판되는 대부분의 수박 품종 식별이 가능할 것으로 분석되었으나, 품종간 유전적 유연 관계의 정밀도를 높이기 위해서는 품종식별력이 높은 eMS 마커 10개를 추가적으로 활용해야 될 것으로 판단된다.
한편, gMS와 eMS 마커를 이용하여 추정된 수박 102개 품종의 유전적 유사도를 이용하여 작성된 계통도의 상관 정도를 Mantel test(Mantel, 1967)에 의해 분석하였을 때, r = 0.713으로 나타났으며, EST와 genomic microsatellite를 병합하여 작성된 계통도를 EST(r = 0.846) 및 genomic 유래의 유사도(r = 0.928)와 각각 비교하였을 때 상관계수는 0.80이상 높게 나타났다. 위의 3가지 계통도(gMS, eMS, gMS + eMS)를 비교해 볼 때, 계통도 상에 위치하는 품종의 순서 및 유전적 유사도는 다르게 나타났지만 전체적인 계통도의 형태는 유사한 것으로 분석되었다.
이상의 결과를 종합해 볼 때 우리나라에서 유통중인 수박 102품종에 대하여 26개의 microsatellite 마커를 이용하여 분석할 경우 대부분의 수박 품종 식별이 가능하였을 뿐만 아니라 수박의 과형, 과육색, 과피색 등과 같은 형태적 특성에 따라 품종들이 그룹화되는 경향을 보였다. 특히, ‘Sambokggul’ 등 14개 품종은 26개의 microsatellite 마커에 의해 식별이 되지 않았는데 이는 수박의 품종 육성에 다양한 유전자원을 활용하지 않고 특정 품종을 순계 분리하여 양친으로 활용하였기 때문에 나타난 결과라고 추정된다.
고 찰
Genomic 및 EST에서 유래된 microsatellite 마커의 다형성 정도를 나타내는 대립유전자의 수 및 PIC 값이 다르다는 것이 오이(Hu et al., 2011), 밀(Gadaleta et al., 2011), 목화(Tabbasam et al., 2014) 등의 작물에서 보고되고 있다. 대부분 연구자의 일치된 견해가 gMS 마커가 eMS 마커보다 다형성 정도를 나타내는 요소인 대립유전자의 수도 많고 PIC 값도 높다는 것이다(Kalia et al., 2011; Varshney et al., 2005). 수박의 경우도 gMS 마커가 eMS 마커보다 높은 다형성 정도를 나타내어 오이(Hu et al., 2011), 밀(Gadaleta et al., 2011), 목화(Tabbasam et al., 2014) 등과 유사한 연구 결과를 나타내었다. 한편, 본 연구에서 다형성을 보인 26개의 microsatellite 마커를 이용하여 102품종을 분석하였을 때 평균 대립유전자의 수가 3.19개, PIC 값이 0.458로 나타나 Kwon et al.(2010)이 멜론과 수박에서 유래된 SSR 마커 30개를 활용하여 미국에서 수집된 유전자원 9점과 시판중인 40품종을 분석하였을 때 보다 다형성 정도(평균 대립유전자의 수가 4.03개, 평균 PIC 값; 0.502)가 다소 낮게 나타났는데 이는 대립유전자의 검출 방법과 공시품종의 유전적 조성이 다르기 때문에 비롯된 결과라고 사료된다. 본 연구에 최종 선정된 수박 microsatellite 마커 26개는 반복 재현성이 높을 뿐만 아니라 대립유전자의 패턴이 복잡하지 않기 때문에 향후 품종의 진위 확인 및 F1 종자의 순도 확인 등과 같은 실용적인 분야에 매우 유용하게 활용될 수 있을 것으로 판단되었다.
우리나라에서 시판되고 있는 수박은 F1 품종이 대부분이며 품종 개발에 활용되는 양친의 유전적 거리가 아주 가깝기 때문에 분자 마커에 의한 품종 지문화는 단순하지 않다. Kwon et al.(2010)은 수박 과형, 과피색, 과육색이 상이한 F1 40품종과 미국에서 수집한 유전자원 9점을 대상으로 멜론에서 유래된 SSR 마커 2개와 28개의 수박 유래의 SSR 마커를 활용하여 품종식별 체계를 구축하였으나 ‘Speedggul’과 ‘Haedonggul’, ‘Sambokggul’과 ‘Chilbokggul’ 등은 95% 이상의 높은 유전적 유사도를 나타내었다. 그러나 본 연구에서 선정된 수박 품종식별용 마커의 경우 ‘Speedggul’과 ‘Haedonggul’은 26개의 마커 중에서 5개의 마커(BVWS00155, BVWS00048, BVWS00233, BVWS01897, WMU058)에서, ‘Sambokggul’과 ‘Chilbokggul’도 2개의 마커(BVWS00208, BVWS00209)에서 뚜렷한 대립유전자의 차이를 나타내었다. 따라서 본 연구에서 선정된 분자 마커가 기존의 연구 결과보다 품종식별력이 높을 뿐만 아니라 자동염기서열분석기를 활용하여 대립유전자를 검출하였기 때문에 정밀도 또한 아주 높을 것으로 판단된다. 그리고 본 연구에 활용된 수박 102품종은 우리나라에서 현재 시판되는 대부분의 품종이기 때문에 이들 품종에 대한 DNA profile 정보를 종자업체에 이전한다면 F1 종자의 순도검정에도 매우 유용하게 활용되리라 사료된다.
국제 식물 신품종 보호 동맹(UPOV: International Union for the Protection of New Varieties of Plants) 에서는 식물 신품종 보호 제도와 품종식별에 분자 마커를 활용하기 위해서는 논문 등을 통하여 모든 연구자에게 알려져 있고 염색체상에 고르게 분포되어 있으며 공우성을 나타내는 SSR이나 single nucleotide polymorphism(SNP) 마커의 활용을 제안하고 있다(UPOV, 2010). 지금까지 우리나라 수박 품종식별에 활용된 microsatellite 마커는 염색체상 위치가 불분명하기 때문에 유전적 유사도 분석 시 다소간의 문제점을 내포하고 있다. 그러나 본 연구에 활용된 microsatellite 마커 26개 중에서 염색체상 위치가 확인된 16개 마커는 수박 12개의 염색체중에서 10번 염색체를 제외한 11개 염색체상에 고르게 분포된 다형성 높은 마커를 활용하였기 때문에 국내 수박 품종에 대한 유전적 유사도의 추정 및 품종 지문화에 있어서 가장 적합한 분자 마커라고 사료된다.
분자 마커를 이용한 작물에 따른 품종별 데이터베이스 구축은 네덜란드에서 토마토 500품종 이상에 대한 연구가 최초로 보고된 이래(Bredemeijer et al., 2002), 영국에서 감자(Reid et al., 2011), 중국에서 옥수수(Wang et al., 2011) 등의 작물에서 여러 가지 연구성과가 발표되고 있다. 우리나라에서도 국립종자원에서 오이(Kwon and Choi, 2013), 멜론(Kwon and Hong, 2014), 상추(Hong et al., 2015), 무(Bae et al., 2015), 딸기(Hong et al., 2014) 등의 작물에서 주요 시판품종에 대한 데이터베이스를 구축하여 이를 품종보호 출원 품종과 DNA특성이 가장 가까운 품종을 대조품종으로 선정하고 형태적 특성 검정에 의한 결과와 비교 분석하는 기법을 활용하여 품종보호 출원품종에 대한 구별성 심사의 보조 자료로 활용하고 있다. 그리고 품종보호 출원품종의 균일성과 안정성이 의심될 경우 본 연구에서 선정된 분자 마커로 DNA 검정을 수행하고 검정 시료간 동일성 여부를 확인한다면 심사 자료로 유용하게 이용될 수도 있을 것이다. 또한 본 연구에서 선정된 수박 품종식별용 microsatellite 마커 세트를 활용하여 실험실과 분석기기간 교차 분석 및 블라인드 테스트를 통한 검정 기술의 표준화는 신품종 육성 시 유전거리의 사전 예측이 가능하여 품종 육성 효율을 향상시킬 수 있을 것이다.
최근 경제적으로 중요도가 높은 작물에서 차세대염기서열분석기를 활용하여 대량의 염기서열 정보가 생산되고 있으며 이를 통해 SNP, insertion/deletion(INDEL), genome-wide염기서열 변이의 탐색이 용이해졌다. SNP 마커는 자동화를 통한 high-throughput 분석이 가능하여 분자유전학 연구에서 최근에 가장 많이 활용되고 있으며, quantitative PCR 보다 multiplexing이 향상된 digital PCR의 개발과 함께 품종식별용 마커로 관심이 증폭되고 있다. 또한 농촌진흥청을 중심으로 구성된 국내 연구진은 벼와 콩에서 resequencing을 통한 genome-wide variation block에 대한 분석 방법을 개발하여(Kim et al., 2014), 염색체별 variation block들을 대표할 수 있는 INDEL 마커들을 선발한 다음 이를 품종 식별을 위한 barcode system구축과 관련된 기술을 개발 중에 있다. 향후, 이러한 분석 방법들을 품종보호권이 설정된 수박 품종의 복제를 방지하기 위한 수단으로 활용한다면 검정에 소요되는 시간, 비용, 노력 절감에 크게 기여할 뿐만 아니라 신뢰도 또한 크게 높일 수 있을 보인다.