서 언
재료 및 방법
시험재료
NO 처리 및 저장 조건
가스분석
품질평가
Botrytis cinerea 배양 및 Colony 관찰
통계분석
결과 및 고찰
1개월 저장된 키위과실에 NO 처리 효과
3개월 저장된 키위과실에 NO 처리 효과
서 언
과실은 수확과 동시에 모체로부터 양분이나 수분공급의 중단과 함께 과실 내 호흡량 증가로 각종 유기물이 소비되어 품질이 급속히 저하된다(Adel, 2002). 일반적으로 과실류는 저장 후 유통과정을 거쳐 소비되며 이러한 과정에서 품질은 수확 당시 과실의 성숙도, 수확 후 저장조건과 유통 과정 중 품질관리에 크게 영향을 받는데 현재까지 유통 과정에서 보관은 상온 또는 냉장고를 이용한 저온저장에 의존해 오고 있다. 특히 상온에서와 같이 높은 온도에서의 보관은 과실로부터 많은 호흡량과 에틸렌을 발생시켜 과실의 품질을 현저히 떨어뜨린다(Kays and Paull, 2004).
키위과실은 과실류 중 저장력이 우수한 과실이나 저장 중 연화과나 부패과가 발생하면 저장력이 현저히 감소된다. 저장 중 발생하는 부패과는 수확 전이나 수확 시 상처 부위를 통해 병원균이 감염되기 때문이며(Bautista-Banos et al., 1997), 이렇게 발생된 부패에 의해서 에틸렌이 발생되는 연쇄반응이 일어나게 된다. 키위과실은 저농도의 산소 조건(2-3%)과 이산화탄소 조건(3-5%)에서 연화를 지연시킬 수 있고 저장기간도 연장되는데 저장 중 에틸렌의 제거는 중요한 요인이다(Arpaia et al., 1987; Saltveit, 1999; Stow et al., 2000). 대부분의 호흡급등형 과실은 저온에서 저장되는 동안에도 에틸렌 발생량의 증가를 보이는 반면 키위과실은 다른 과실들과는 달리 0°C 저온에서 저장될 경우 4-6개월까지 저장이 가능하며 에틸렌은 거의 발생되지 않는다(Antunes and Sfakiotakis, 2002; Antunes et al., 2000). 그러나 상온으로 옮겨지면 에틸렌은 급격히 증가하여 과실 연화를 유도함으로써 품질을 급격히 저하시키는 주요 요인이 된다(Arpaia et al., 1987; Mitchell, 1990).
일산화질소(nitric oxide, NO)는 질소원자와 산소원자만으로 결합된 분자로서 지구상의 거의 모든 생명체내에서 생성된다. NO는 지질과의 친화력이 높아 세포막을 쉽게 통과하여 다양한 형태의 산화-환원형으로 변화할 수 있고, 세포 내 존재하는 다양한 물질들과 결합하여 안정을 찾으려는 불안정한 free radical 가스이다(Wink and Mitchell, 1998).
식물분야 중 원예작물의 수확후 생리대사에 관련된 NO에 관한 연구는 내생 에틸렌 및 스트레스와의 관련성(Leshem and Pinchasov, 2000; Leshem et al., 1998), 증산작용 억제(Ku et al., 2000), 엽록소 유지(Eum et al., 2009a), 식물 면역학(Hausladen and Stamler, 1998), 병 저항성(Delledonne et al., 1998; Małolepsza and Różalska, 2005) 등 광범위하게 연구가 진행되고 있다. Leshem et al.(1998)의 연구에 따르면 내생 NO의 생성은 식물체의 성숙 및 노화가 진행되면서 줄어드는데 이러한 현상은 에틸렌 발생이 증가되는 것과 부의 상관관계를 보인다. 외생 NO 처리에 의해서도 에틸렌 발생을 감소시키는 효과를 보이는데, 토마토를 이용한 이전의 실험에서 NO를 각 숙성 단계(mature green, break, pink, red)별로 처리할 경우 에틸렌 발생 시기를 지연시키고, 발생량이 감소되는 효과가 나타났는데, 특히 미성숙 단계의 과실에서 에틸렌 발생 지연효과는 더욱 크게 나타났다(Eum et al., 2009c). 토마토에서는 NO 처리에 의한 에틸렌 발생의 감소는 에틸렌 전구물질인 aminocyclopropane-1-carboxylic acid oxidase의 활성을 저지시키면서 나타났다. 그러나 복숭아 ‘미백도’ 품종에서는 외생 NO를 처리할 경우 호흡량이 감소되고 과피의 색발현이 지연되면서 저장기간 동안 품질을 유지시킨 반면 에틸렌 발생을 지연시키지는 못했다. 또한 외생 NO 처리의 시기는 저온 저장한 다음 유통을 실시하기 전에 처리하는 것이 복숭아의 품질을 유지시키는데 효과적이라는 것을 제시하면서 처리시점의 중요성을 시사하였다(Eum et al., 2009b).
과실은 저장 기간에 따라 에틸렌에 반응하는 양상이 다르게 나타난다. 이에 본 연구에서는 1개월, 3개월 저장된 키위과실을 이용하여 저온 저장된 키위과실의 상온 유통 중 에틸렌 발생 및 품질에 미치는 영향을 확인함으로써 유통기간 연장을 위한 NO의 가능성을 제시하고자 한다.
재료 및 방법
시험재료
본 연구에 이용된 ‘Hayward’ 키위품종은 전라남도 해남지역 농장에서 수확된 과실을 공급받았다. 키위과실의 평균 과중은 95 ± 10g이며, 과피에 물리적・병리적 장해가 없는 과실을 실험에 이용하였다. NO와 N2 가스는 가스회사(대성산업가스, 서울, 한국)로부터 공급받았다.
NO 처리 및 저장 조건
1개월 또는 3개월 동안 0°C에서 저장된 키위과실을 약 3.5kg씩 각각 15L 챔버에 넣고 NO를 처리하였다. 먼저 챔버 내부의 산소를 제거하기 위해서 continuous flow system으로 유속 3L・min-1 N2를 처리하여 챔버 내부의 공기를 치환한 다음 챔버에 설치된 inlet 장치를 통해 200μL・L-1 NO를 공급하였다. NO를 처리한 후 챔버의 밸브를 막고 밀폐시켜 5시간 방치한 다음 챔버를 열어 공기를 환기시킨 후 20°C에 2주간 저장하면서 품질 변화를 관찰하였다.
가스분석
저장기간 동안 호흡률과 에틸렌 생성량은 과실을 1L 밀폐용기에 넣어 3시간 밀폐시킨 후 내부에 축적된 가스를 packed stainless steel 칼럼이 장착된 가스 크로마토그래프(Model M600D, Young Lin Instrument Co., Anyang, Korea)를 이용하여 측정하였다. 이산화탄소와 에틸렌은 각각 thermal conductivity detector(column, 100°C; detector, 120°C; carrier gas, He 30mL・min-1)와 flame ionization detector(column, 150°C; detector, 180°C; carrier gas, He 30mL・min-1)를 이용하여 검출하였다.
품질평가
저장기간 동안 품질변화와 관련하여 무게변화율과 경도변화를 관찰하였다(n = 5). 무게변화는 저장기간 동안 초기 무게에 대한 감량분을 백분율로 나타내었으며, 과실경도는 과피를 벗겨낸 후 적도부위를 경도계(TA.XT2, Stable Micro Systems Texture Technologist)를 이용하여 측정하였다.
Botrytis cinerea 배양 및 Colony 관찰
Botrytis cinerea는 키위과실로부터 직접 배양된 것을 이용하였다. 키위과실을 상온에서 3주 이상 방치한 후, 곰팡이가 배양된 생체 시료로부터 2mm 정도 크기의 디스크를 분리한 후 잡균을 제거하기 위해서 소독을 실시하였다. 1% NaClO와 70% 에탄올에서 각각 30초간 방치한 다음 멸균수를 이용하여 3차례에 걸쳐 소독하였다. 소독된 디스크를 1.5% water agar 배지에 배양하여 곰팡이를 번식시킨 후 번식한 균사를 다시 PDA 배지에 치상하였다. PDA 배지에서 번식된 균사를 또 다른 PDA 배지로 옮긴 후 NO와 대조구로서 초고순도 N2를 처리하였다. NO 농도는 200μL・L-1 NO와 500μL・L-1 NO를 처리하였다. 처리방법은 과실에 NO 처리할 때와 동일한 방법을 이용하였다. NO 처리 후 24시간 마다 72시간에 걸쳐 성장한 colony의 직경을 측정하였다.
통계분석
실험결과의 통계처리는 SAS system(SAS Institute Inc. Cary NC 27513, USA)을 이용하여 분산분석(ANOVA)을 하였으며 LSD test를 이용하여 p = 0.05 수준에서 각 처리간의 유의성을 검증하였다.
결과 및 고찰
1개월 저장된 키위과실에 NO 처리 효과
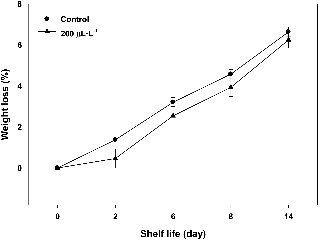
실험에 이용된 NO의 농도는 200μL・L-1 NO이며 대조구와 함께 상온(20°C)에 저장하면서 품질을 비교하였다. 20°C에서 저장하는 동안 키위과실의 무게손실은 대조구에서 저장 2일 만에 1.3% 정도 감소된 반면 처리구에서는 무게 손실률의 거의 발생되지 않았다(Fig. 1). 저장 14일이 경과되는 동안 대조구에서 6%의 무게가 감소된 것을 확인하였다. 처리구에서는 실험전반에 걸쳐 대조구에 비해 무게의 평균값은 적었으나, 대조구와 처리구간에 유의적 차이는 없었다.
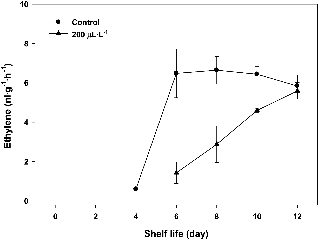
키위과실은 에틸렌에 의해서 과실의 연화가 급속히 진행되므로 NO 처리가 에틸렌 발생에 미치는 영향을 조사하였다. 대조구에서는 4일 경과 후부터 에틸렌이 발생되기 시작하여 6일에 최대치를 보였다(Fig. 2). 그 후는 일정하게 유지되는 것을 확인할 수 있다. 반면, 처리구에서는 6일부터 에틸렌의 발생이 증가되기 시작하여 서서히 증가를 보이고 있다. 저장 12일 경과 후에는 대조구와 비슷한 에틸렌 발생을 보였다. 이것으로 NO가 에틸렌의 발생을 저해함을 확인할 수 있고, 키위과실의 저온 저장 후 상온 유통 시 적용 가능성을 제안하고 있다. NO는 식물체에서 자연적으로 생성되는 식물생장 물질로써 식물체로부터 에틸렌의 방출을 줄이면서 노화를 지연시킨다(Leshem and Pinchasov, 2000; Leshem et al., 1998). 식물체로부터 NO의 방출은 에틸렌이 생성되는 것과 거의 동시에 이루어진다고 보고된다. 에틸렌과 NO의 관계는 화학량론적(stoichiometric)인 관계로 나타나는데, 식물체가 미성숙한 단계에서는 NO의 발생량이 높다가 성숙되고 노화가 진행되면서 에틸렌의 발생량이 많아지면 비례적으로 NO의 발생량은 줄어들다가 노화단계에 이르러서는 에틸렌 발생이 대부분을 차지하고 NO의 발생은 없다. 또한 외생 NO 처리는 꽃, 과일, 그리고 채소와 같은 원예작물에서 유통기한을 연장시키는데, 이는 에틸렌의 발생을 최소화함으로써 이루어진다고 보고된다(Eum et al., 2009b; Ku et al., 2000).
호흡률은 200μL・L-1 NO 처리구에서 대조구에 비해 2배 이상 낮았다(Table 1). NO 처리구는 저장 12일까지 저장 초기의 호흡률을 유지하는데 효과가 있었다. NO는 분자량이 작으며 확산속도가 빠른 기체물질이다. 이러한 성질 때문에 빠른 시간 내에 세포 내로 쉽게 확산되어가는 특징을 가지고 있다. 또한 세포 속에서 마이토콘드리아와 같은 세포 내 소기관들에 영향을 끼치는데, cytochrome oxidase와 ubiquinone- cytochrome b 위치에서 전자 전달을 저해함으로써 호흡을 억제시키는 것으로 알려져 있다(Borutaité and Brown, 1996; Laxalt et al., 1997).
3개월 저장된 키위과실에 NO 처리 효과
1개월 저장된 키위과실을 이용한 실험에서 NO의 키위과실 유통 시 적용가능성을 확인하고, 장기 저장된 키위과실에 미치는 영향을 확인하기 위하여 3개월 저장된 키위과실을 이용하여 실시하였다. 본 실험에 이용된 농도는 100, 200, 그리고 500μL・L-1 NO이다. 대조구는 NO를 처리하지 않은 구와 N2 처리구를 두었다. N2는 NO 처리 시 챔버 내부의 산소를 제거하기 위해서 적용되었으며, NO의 농도를 달리할 경우 기본 기체로 이용되었다. 따라서 과실의 유통기간 연장이 NO의 작용인지 아니면 N2의 작용인지를 확인하기 위해서 대조구로 적용하였다.
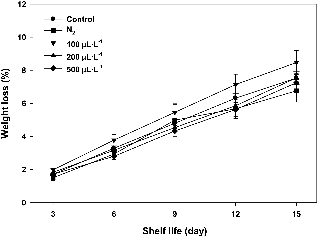
저장 기간에 걸쳐 무게 변화를 살펴보면 100μL・L-1 NO 처리구에서 무게 손실이 가장 많았으며, 대조구와 다른 농도의 NO 처리구에서는 감소율이 비슷하였다. 이러한 감소율은 1개월 저장된 시료와는 다소 차이가 있으나, 저장 기간이 길수록 과실에서 수분 증발이 심하게 일어난다는 것을 보여주고 있다(Fig. 3). 기존 연구에서 원예작물에 NO 처리 시 수분손실을 줄인다는 보고가 있는데, 이는 외생 NO에 의해서 과실, 채소, 화훼류 등의 모든 원예작물에서 증산작용을 저해시켰기 때문이다(Ku et al., 2000). 수분손실은 작물에게 직접적으로 양적인 손실을 초래할 뿐만 아니라 외관과 영양학적인 손실을 야기시키므로 품질저하를 나타내는 지표로 이용된다(Adel, 2002). 원예작물은 저장기간이 경과되면서 증발과 증산작용에 의해서 수분손실이 발생되는데, 일반적으로 키위과실은 수확 시 무게의 4-5%의 무게손실이 일어나면 시들음이 발생했다고 간주된다(Burdon et al., 2014). 비록 키위과실의 최적 저장온도인 0°C에서 수분손실을 막기 위해 PE 필름으로 포장하여 저장하여도 수분손실은 계속 일어나며 시들음이 발생된다. Burdon et al.(2014)의 연구에 따르면 14주 동안 0°C에서 저장된 키위과실을 20°C에서 4일간 방치할 경우 ‘Gold 9’과 ‘Zesy 002’ 품종은 3.1-3.5%까지 무게손실이 발생했다.
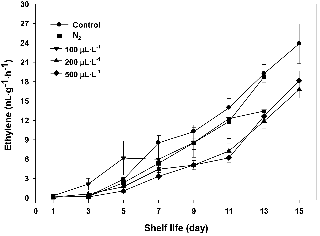
에틸렌 생성률을 비교해 보면 대조구와 100μL・L-1 NO에서 높은 반면 200μL・L-1 NO와 500μL・L-1 NO에서는 상대적으로 낮았다(Fig. 4). 저장 시기 3일과 9일의 에틸렌 발생률을 비교해 보면 3일에는 모든 처리구에서 미비하지만, 9일 경과 후에는 뚜렷한 차이를 보이고 있다. 특히 200μL・L-1 NO의 농도를 중심으로 500μL・L-1 NO의 고농도에서는 에틸렌 발생률이 낮은 반면, 저농도인 100μL・L-1 NO에서는 에틸렌 생성을 지연시키는데 효과가 적었다. 딸기를 이용한 이전 연구에서는 적정 NO 처리농도는 200μL・L-1 NO으로 500μL・L-1 NO 고농도에서는 오히려 에틸렌 생성을 촉진시키고, 꽃받침의 갈변을 유도하며 곰팡이 발생을 촉진시켰다(Eum and Lee, 2007). 이러한 결과로 미루어 보아 NO 처리의 적정 농도는 품목마다 틀리며, 딸기와 같은 연약한 과피를 가지고 있는 작물의 경우는 고농도의 NO 처리에 의해서 갈변과 같은 장해가 나타나는 반면, 키위와 같은 단단한 과피를 갖는 작물에서는 고농도인 500μL・L-1 NO의 농도에서도 장해 없이, 에틸렌 발생을 지연시키는데 효과적인 것으로 판단된다.
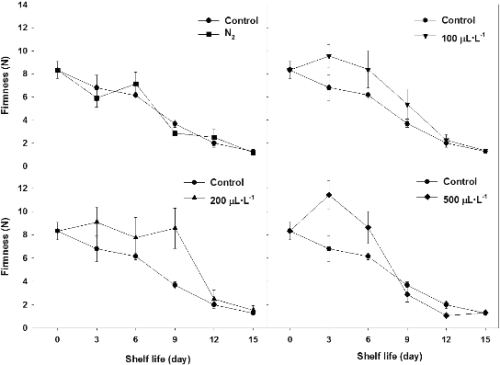
경도를 비교해 보면 무처리구와 N2 처리구는 모두 저장 일수가 경과 되면서 급격히 연화되었다(Fig. 5). NO 처리구에서는 6일까지 경도가 높게 유지된 다음, 100μL・L-1 NO와 500μL・L-1 NO 처리구는 급격한 감소를 보여 9일 경과 후에는 대조구와 비슷한 양상을 보였다. 반면 200μL・L-1 NO 처리구는 9일까지 8N 이상을 유지시켰다.
키위과실을 저장하는 동안 주로 발생되는 병리장해는 잿빛곰팡이병으로 Botrytis cinerea에 의해서 야기된다(Batta, 2007; Bautista-Banos et al., 1997). 키위과실로부터 채취하여 배양된 Botrytis cinerea에 직접 NO를 처리한 결과 처리 후 2일 경과될 때까지 무처리구와 N2 처리구에 비해서 NO 처리구는 곰팡이 번식이 적었다(Table 2). 무처리구는 1일 경과 후에는 2cm까지 colony가 커진 반면, 200μL・L-1 NO와 500μL・L-1 NO에서는 각각 1.2, 1.1cm까지 성장하였다. 3일 경과 후에는 대조구에서 colony의 크기는 가장 컸지만, 다른 처리구와 유의적 차이는 보이지 않았다. 본 실험의 결과는 NO 처리에 의해서 곰팡이의 번식을 줄일 수 있다는 것을 입증하는 것이며, 따라서 곰팡이가 발생되기 전인 유통 직전에 NO를 처리하면 효과를 증가시킬 수 있다고 판단된다.
Reactive oxygen species(ROS)와 관련된 식물체의 방어기작은 동물체에서 일어나는 감염에 대한 염증반응과 유사한데, 이때 NO가 주요한 signaling molecule로 작용한다(Beligni et al., 2002). 일반적인 ROS와 마찬가지로 NO는 감염부위에 salicylic acid(SA)의 축적을 유도하고 SA는 ROS, H2O2, 그리고, NO의 생성을 야기시킨다. 이러한 작용은 곰팡이 등과 같은 병원균의 공격에 대한 식물체의 방어 기작으로서 중요한 역할을 수행한다. NO, SA, 그리고 ROS의 또 다른 역할은 hypersensitivity reaction과 병원균을 직접적으로 죽이는 작용이다. 특히 ROS와 SA는 NO에 의해서 시너지 효과가 야기되는데, Pseudomonas syringae로 감염된 soybean suspension 세포에서 hypersensitive cell death가 강화된다는 연구결과가 보고된다(Delledonne et al., 1998; Klessig et al., 2000).
이상의 결과를 종합해 보면 키위과실의 유통기간 중 품질을 유지하기 위해서 NO를 처리할 경우 3개월 저온 저장보다는 1개월 저장된 시료를 이용하는 것이 에틸렌의 발생을 억제하는 것이 효과적이다. 하지만 장기 저온 저장된 시료일지라도 시장으로 출하하기 전에 처리하면 에틸렌 발생 및 호흡을 저지시키고, 결과적으로 연화까지 막을 수 있기 때문에 NO의 효율성은 입증된다. NO 처리 시에는 적정 농도를 찾는 것이 중요한데 본 실험결과 NO의 적정 농도는 200μL・L-1 NO을 기준으로 너무 낮거나 높으면 NO의 효과가 줄어들어 유통 중 품질을 저하시킨다.