서 언
재료 및 방법
식물 재료 및 DNA 정제
성발현 표현형 검사
중합효소연쇄반응(PCR), agarose gel 전기영동, 염기서열 분석
Marker Assisted Selection (MAS) for Monoecy
결과 및 고찰
서 언
다양한 과피색과 향 그리고 여러 가지 과형을 가지고 오리엔탈 멜론으로 불리는 참외는(Cucumis melo L.) 중앙아시아를 비롯한 일본, 중국, 한국에서 오랫동안 재배되어온 중요한 과채류이다(Pitrat et al., 2000). 연간 국내 참외 생산량은 약 5,600억원으로 박과 채소 작물 중 수박에 이어 두 번째로 큰 규모이며, 매년 생산량이 증가 추세에 있다(Korean seed association, 2014).
박과 채소작물에서 성발현은 암꽃과 숫꽃이 각각 발생하는 자웅동주(monoecy, MO), 숫꽃과 양성화가 발생하는 웅성화양성화동주(andromonoecy, AM), 암꽃만 분화하는 자성주(gynoecy, GY), 동일한 화기 에서 암술과 수술이 동시에 발생하는 양성화주(hermaphrodite, HE)로 나눌 수 있는데 참외와 멜론의 경 우는 자웅동주(MO)와 웅성화양성화동주(AM)가 주요 성발현 형태이다(Kenigsbuch and Cohen, 1990;Roy and Sarain, 1990). 일반적으로 locus A, G 그리고 M이 멜론 에서 성발현을 제어한다고 알려졌는데 locus A는 자웅동주 (MO) 식물체에서 암꽃 분화를 조절하고, locus G는 자웅동주와 웅성화양성화동주(AM)식물에서 숫꽃 분화를 조절한다고 알 려져 있다(Perl-Treves, 1999; Yamasaki et al., 2001). 박과채소작물에서 성발현 관련 유전자 연구는 멜론의 A, G locus 유전자 와 함께 오이의 locus F와 locus M의 염기서열 비교연구가 대표적이다(Boualem et al., 2008; Trebitsh et al., 1997). A, F와 M locus는 1-aminocyclopropane-1carboxylic acid synthase(ACS)를 암호화하고, ACS 유전자는 에틸렌 생합성을 통해 성 발현 을 조절하는데 중심 역할을 한다고 알려져 있다(Roy and Sarain, 1990; Rudich et al., 1972). ACS 유전자의 기능을 잃은 돌연 변이체의 경우 에틸렌 생합성이 감소하고(Li et al., 2009; Martin et al., 2009) 반대로 화아분화 시기에 에틸렌의 농도가 증가할 경우 수술의 형성을 차단하거나 억제시키고 심피의 발달을 촉진한다고 보고되었다(Boualem et al., 2008; Little et al., 2007; Trebitsh et al,. 1997).
참외의 경우 일대잡종 품종 생산에서 양성화를 이용할 경우 제웅작업이 필요하여 많은 노력과 비용이 소요되고 특히 충분한 제웅작업이 이루어지지 못할 경우 자식주 생산비율이 높아져 고순도 일대잡종 생산이 어렵다. 따라서 참외 육종에서 단성화 계 통 선발은 매우 중요한 의미를 가진다. 또한, 참외 재배에서 양성화가 발생할 경우 과실 화흔부가 이상 비대하여 기형과 발생을 유발하고 상품성을 감소시킴으로 단성화 형질이 안정적인 품종을 선택하는 것이 중요하다.
목표형질을 보유한 신품종을 육성하기 위해서는 유전자원이나 육종계통들의 유전적 차이를 정확히 분석하는 것이 선결요 건이다. 이를 위해 효율적으로 고안된 방법으로 DNA 마커를 활용한 분자 마커 선발법(marker assisted selection; MAS)이 있 다. DNA 마커는 insertion and deletion variation(Indel), simple sequence repeats(SSRs), single nucleotide polymorphism(SNP) 등이 있다. 특히 Indel과 SSR의 경우에는 PCR를 기반으로 다형성을 확인하는데 있어서 비용과 시간적인 측면에서 장점을 가 지고 있어 EST-SSR 마커 형태로 이용되고 있다. 멜론에서도 EST-SSR 마커는 중국 재래종의 유전자 변이를 조사한 연구를 포함하여 많이 이용되는 추세이다(Kong et al., 2011; Rauwolf et al., 2008; Slate et al., 2009).
또한 MAS는 마커의 유전형 분석을 통해 목표 형질이나 유전자를 가지고 있는 개체를 선발할 수 있는 방법이다(Francia et al., 2005). 실용적인 MAS 기술 개발은 전통적인 식물육종에서 소요되는 노력과 비용을 절감할 수 있고 육종연한을 크게 단축 시킬 수 있다. 또한 환경의 영향을 배제하고 식물의 모든 성장 단계에서 조사하고 선발할 수 있는 장점이 있다(Semagn et al., 2006). 특히 MAS는 선발하고자 하는 형질이 발육단계 특이적으로 발현하거나 적절한 선발압력을 부여하기 어려울 경우 그리 고 낮은 유전력으로 인해 정확한 표현형 선발이 어려울 경우 매우 효과적이고 경제적이다(Truong et al., 2011; Winter and Kahl, 1995).
본 연구는 멜론에서 개발된 단성화 관련 Indel 마커인 T1ex를 참외에 적용하기 위해 수행되었다. T1ex는 멜론에서는 실제 육종에 적용하는데 어려움이 있는 것으로 알려져 있는데 본 연구에서는 T1ex 정보를 기반으로 참외에 적용 가능한 단성화 연 관 분자마커를 개발하고 실제 육종과정에 적용할 수 있는 분자마커를 개발하고자 하였다.
재료 및 방법
식물 재료 및 DNA 정제
장춘종묘(Chilgok, Korea)로부터 제공받은 한국 품종인 ‘DANPR’(DP)과 ‘DEUN’(DE), 중국 품종인 ‘HYANG 1’(HS)의 참 외 종자를 포함하여 시판되고 있는 일반종 및 일대잡종을 단성화(monoecious: MO) 마커 분석에 사용하였다(Table 1). 그 중 ‘DANPR’은 단성화(MO), ‘DEUN’과 ‘HYANG 1’은 웅성화양성화동주(andromonoecious: AM)를 나타내는 것으로 알려져 있 다. DNA 추출은 참외 종자를 발아시켜 키운 후 어린잎을 수확하여 ?70°C 냉동고에 보관한 후 CTAB method(Doyle and Doyle, 1987)를 이용해 DNA를 추출하였다. 곱게 분쇄된 시료에 CTAB buffer를 750μL을 가하고 30초 vortexing 하여 추가로 60°C에서 1시간 배양하였다. 750μL을 phenol:chloroform:isomyl alcohol(25:24:1)을 넣고 15초 vortexing, 5분 원심분리 하였다. 원심분리 후 얻은 상층액을 2mL tube로 옮긴 후 두 번에 걸쳐 chloroform:isomyl alcohol(24:1) 용액으로 세척한 후 ethyl alcohol 600μL 넣고 ?70°C에서 1시간 보관 후에 4°C에서 10분 간 원심분리하였다. 원심분리된 DNA pellet을 확인한 후 상 층액을 버리고 자연 건조시켰다. 추출된 DNA는 증류수 60μL로 현탁시켰다.
Table 1. Expected PCR amplicon size using T1ex marker for comparison o fsex expression types in chamoe and melon. Chamoe Melon
| |
성발현 표현형 검사
DNA 마커와 형질간의 연관성을 확인하기 위한 표현형 평가는 ‘DANPR’(DP)계통, ‘DEUN’(DE), ‘HYANG 1’(HS) 및 한국 시장 참외 종자 및 일대 잡종 식물을 대상으로2 015년 3월부터 6월까지 장춘종묘 비닐하우스에서 수행하였다.
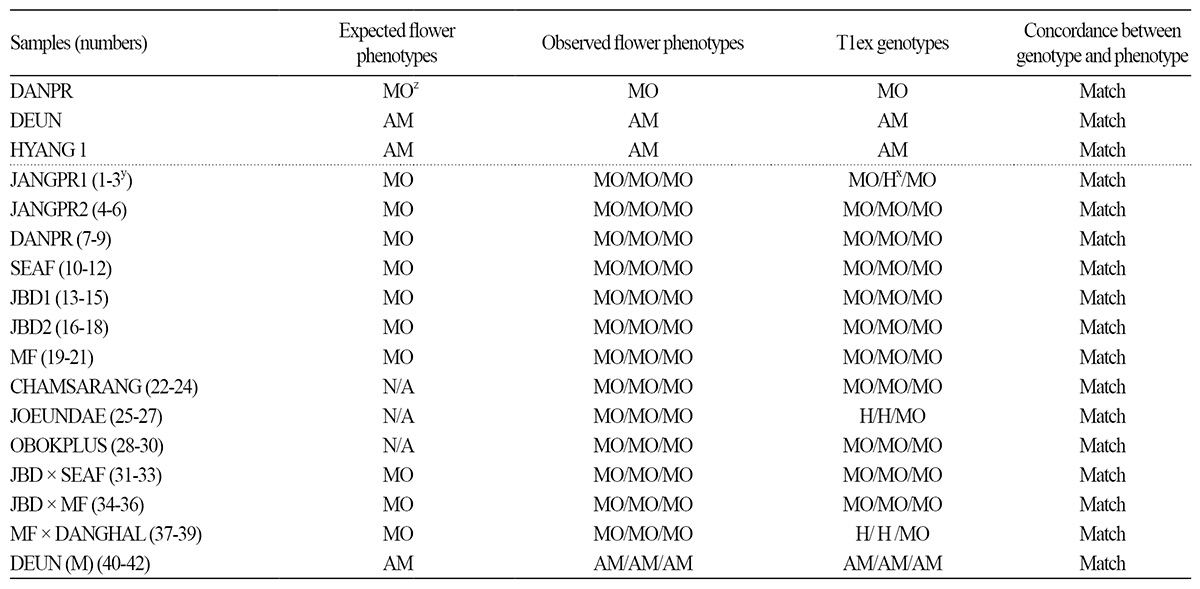
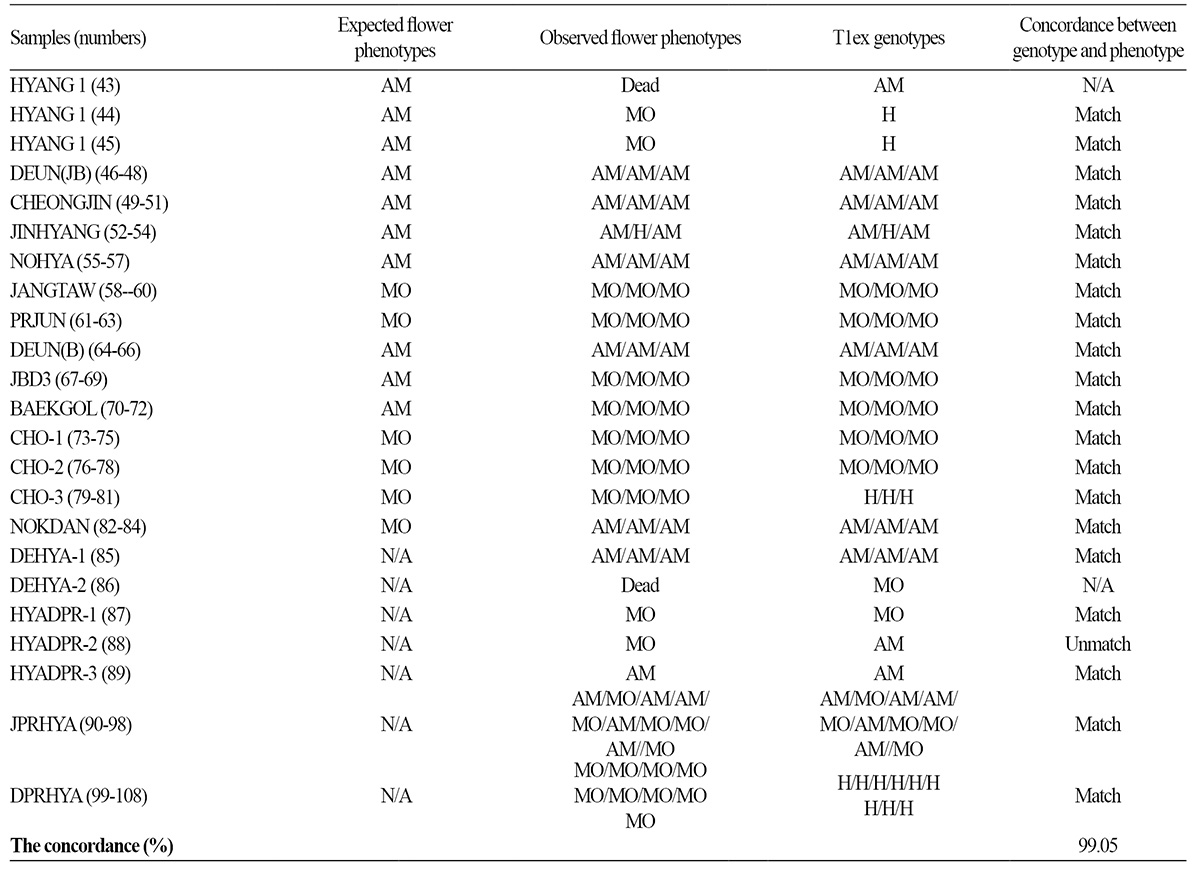
육묘하우스에서 32공 트레이를 이용하여 육묘한 후 식물체가 본엽 4매 일 때 120×40cm 간격으로 정식하였다. 인공조명 없 이 자연광 조건에서 재배하였으며, 낮과 밤의 온도범위는 각각 25-30°C와 14-16°C, 상대습도는 60-80%이었다. 각 식물체들 의 성발현은 자웅동주성(monoecious, MO)을 나타내는 단성화, 웅성화양성화성(andromonoecious, AM)을 나타내는 양성화 로 분류하였다. 어미 줄기(main branch) 6-9 마디와 이들로부터 발생하는 아들 줄기(lateral branch)의 화기 구조를 바탕으로 성발현을 분류하였다. 화기구조(암술, 수술, 갖춘꽃) 조사는 각 식물체 당 어미줄기 4개 마디와 각 마디에서 분화된 아들줄기의 첫 번째 마디에서 발생한 꽃을 대상으로 수행되었다. 어미줄기에는 수꽃만, 아들 줄기에는 갖춘꽃을 갖는 양성화 식물들은 웅 성화양성화성(AM)으로 분류되었다. 그와는 다르게 본줄기에서는 수꽃만, 아들줄기에는 암꽃만을 갖는 단성화 식물들은 자웅 동주성(MO)으로 분류되었다(Table 2).
| |
zMO: monoecious, AM: andromonoecious, H: heterozygous, N/A: Not available. ySample numbers used in Fig. 3. xAll of the heterozygous (H) genotype showed the monoecious phenotype. | |
중합효소연쇄반응(PCR), agarose gel 전기영동, 염기서열 분석
PCR 반응 용액은 솔젠트(Daejeon, Korea) 회사의 e-taq kit를 사용하여 수행 되었다. PCR 의 총 부피는 15μL, 5μL template DNA(4ng/μL), 0.08uL Taq polymerase(5U/μL), 2μL 10X PCR buffer, 0.3μL dNTPs(2.5mM each), 2μL forward, reverse primer(10pmol), 그리고 6.12μL 증류수로 구성되며, PCR 반응은 Supercycler SC-200(Kyratec, Queensland, Australia)를 이 용하여 94°C에서 5분 동안 일차 변성하고, 94°C에서 30초, 55°C에서 30초, 72°C에서 1분의 변성, 결합, 신장 3단계를 35번 반 복 후. 최종 신장 단계로 72°C에서 5분간 반응 하였다. PCR 산물은 2.0% agarose gel에서 2시간동안 300volt로 분리시켰고, ethidium bromide를 이용하여 WiseDoc(Deahan, Seoul, Korea)의 디지털 카메라를 이용하여 UV 조건에서 PCR 결과물을 확 인하였다.
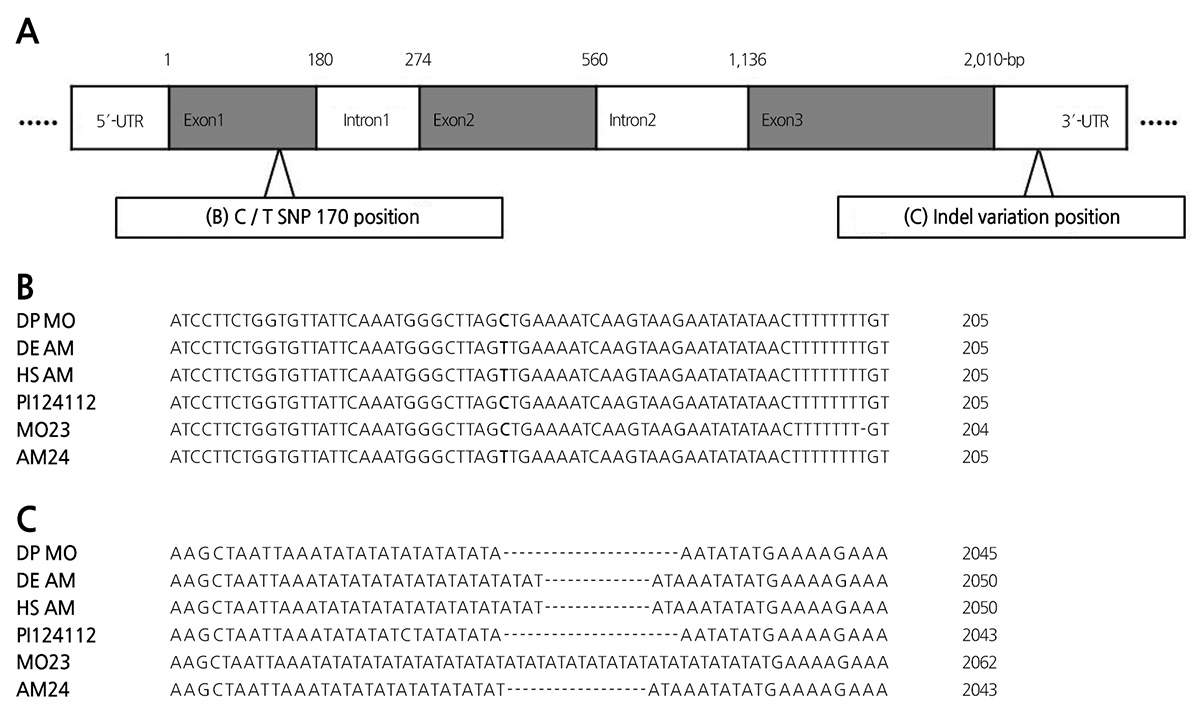
멜론의 CmACS-7 유전자의 ORF-1 과 ORF-2 프라이머(Kim et al., 2015)를 이용하여 참외의 CmACS-7 유전자 염기서열 을 솔젠트(Daejeon, Korea)에 분석 의뢰하였다. 얻어진 염기서열분석 결과는 Bioedit(http://www.mbio.ncsu.edu/BioEdit/ bioedit.html) 프로그램을 이용하여 참외와 멜론간의 CmACS-7 유전자 염기서열을 비교하였다(Fig. 1).
Marker Assisted Selection (MAS) for Monoecy
참외 육성 계통 총 장춘종묘에서 육성중인 참외 7개 계통의 240개 아계 계통을 대상으로 MAS를 진행하였다. ‘HYANG 1’(HY11중9-2) 계통 24 개체, ‘HYANG 1’(HY11중9-11) 계통 24개체, ‘HYANG 1’(HY11중9-12) 계통 24 개체, ‘JINHYANG’ (JINHY3-138-10-4-8) 계통 24개체, ‘HYASAE’(HYASAE-0-2) 계통 40개체, ‘HYASAE’(HYASAE-0-8) 계통 40개체, ‘CHO-3’(RAPA-1-5-2) 계통 40개체를 정식 전에 각각의 본엽을 채취하여, DNA 분석을 진행하였으며, 단성화와 양성화 그 리고 이형 유전자형을 분리하였다. 유전자형 분석에 따라 98개체의 단성화 및 양성화를 선택하여 정식하였다. 정식 후 관찰된 표현형과 마커에 따른 유전자형을 비교 분석하였다.
결과 및 고찰
본 연구에서는 표현형 검사를 통해서 성발현이 확인된 세 종류의 참외, 단성화 계통의 ‘DANPR’(DP MO), 양성화 계통의 ‘DEUN’(DE AM), HYANG 1(HS AM)을 ORF-1,2 F/R 프라이머를 바탕으로 CmACS-7 유전자의 전체 염기서열 분석을 진 행하였다(Fig. 1).
멜론에서 BLAST 검색 및 염기 서열 분석으로 CmACS-7의 구조(Fig. 1A) 및 엑손1 지역에 SNP가 에틸렌 합성에 영향을 일 으켜 andromonoecy를 발생시키는 것이 보고되었다(Boualem et al., 2008). PCR을 기초로 하여 쉽고 빠르게 확인 가능한 마커 개발을 위해, CmACS-7 유전자의 3’-untranslation region(UTR) 지역의 Indel 부분에 AT 서열 반복수가 다른 것에 착안하여 공동우성 T1 마커에 대한 연구가 보고되었다(Feng et al., 2009). 그러나 T1 마커를 이용한 PCR 분석에서 그 재현성이 낮았기 때문에, T1 마커에 염기를 추가하여 만들어진 sequence characterized amplified reg ion(SCAR) T1ex 마커가 멜론에서 새롭게 제시 되었다(Kim et al., 2015). 이 마커를 이용하여 멜론의 단성화 라인 MO23과 양성화 라인 AM24 및 야생형 단성화 멜론, PI113112(Genbank accession no. EU791279.1)의 3-UTR 부분의 염기서열의 차이를 확인하였다(Kim et al., 2015). 하지만 T1ex 마커는 멜론에서 단성화의 경우 다양한 크기 변이를 보이는 이유로 T1ex 마커의 이용가능성은 매우 낮은 것으로 보고 되 었다.
멜론과 참외의 염기서열을 바탕으로 exon 1의 SNP 부분과 Indel 부분을 포함하고 있는 3-UTR 부분을 재배열 하였는데 멜 론에서는 단성화 계통 ‘MO23’과 ‘PI124112’에서는 사이토신(C)을 양성화 계통 ‘AM24’에서는 티민(T)을 나타내었고, 마찬가 지로 참외에서도 DP MO(단성화)에서는 사이토신을, DE AM(양성화)과 HS AM(양성화)에서는 티민을 나타내어 멜론과 참 외에서는 다른 차이는 존재하지 않았다(Fig. 1). 그러나 Fig. 1C에서 보듯이 3-UTR 부분의 염기 변이가 참외와 멜론에서는 다 른 패턴을 보였는데 멜론의 경우 먼저 단성화 사이에서도 211bp와 187bp라는 다양한 양상을 보이며(Fig. 1 and Table 1), 대표 적인 단성화 계통인 ‘MO23’이 양성화 계통 ‘AM24’ 보다 더 많은 염기서열을 가지고 있었지만, 참외에서는 양성화와 단성화에 각각 단일 종류의 크기 변이를 보였다. 따라서 멜론과 참외의 CmACS-7 유전자 두 지역의 서열비교를 통해서 상대적으로 이 용이 쉽고 비용이 저렴한 Indel 기반의 마커인 T1ex 마커가 참외에 적용 여부를 확인 하기 위해 다양한 참외계통에 적용해 보 았다.
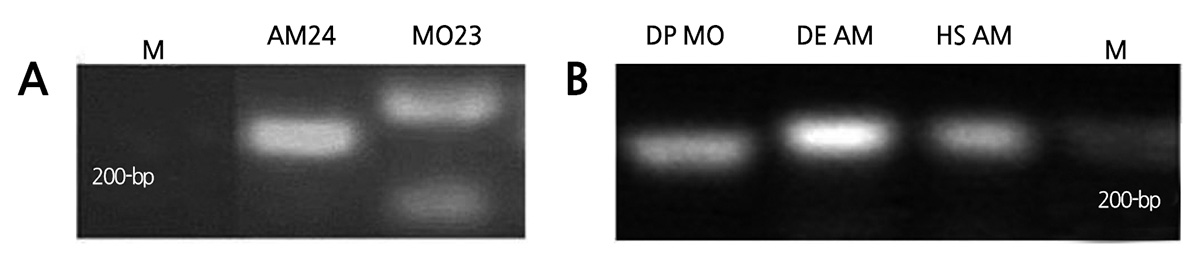
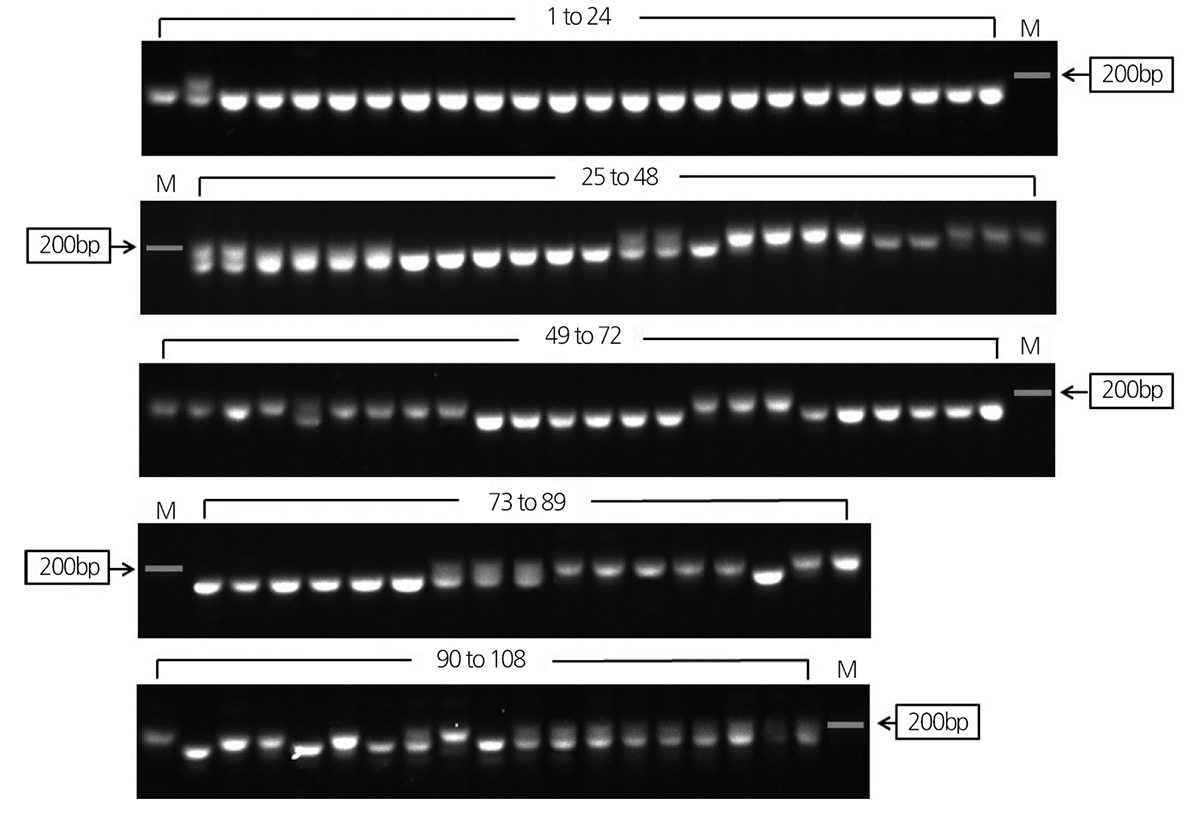
세 종류의 참외 ‘DANPR’, ‘DEUN’, ‘HYANG 1’을 PCR을 이용하여 DNA를 증폭시킨 결과 ‘DANPR’은 약 190bp, ‘DEUN’ 과 ‘HYANG 1’은 약 200bp 크기를 확인하고, T1ex를 통해 서로 다른 성표현을 가지는 참외의 염기 서열 간에 약 10bp의 차이 가 있음을 확인하였다(Fig. 2). 멜론에서는 T1ex 마커의 경우 단성화 라인이 약 211bp, 양성화 라인이 약 192bp 크기로 보고되 었다(Fig. 2). 하지만 Kim et al.(2015)에 따르면 야생형 멜론의 경우 단성화를 나타내는 약 190bp의 유전자형도 존재하는 것으 로 알려져(Table 1) T1ex 마커의 이용이 MAS 과정에서 실용화가 어렵다고 보고되었다. 이러한 문제점이 참외에서도 존재하 는지 확인하기 위해 본 연구에서는 장춘종묘에서 제공 받은 총 108개의 참외의 유전자형 분석을 진행하였고, 108 개체의 참외 중 106 개체의 표현형 검사를 통해 T1ex 마커 유전자형과 성발현 표현형과의 연관성을 조사하였다(Table 2). T1ex 마커를 이 용하여 나머지 참외 DNA의 PCR 증폭 결과, ‘DANPR’, ‘DEUN’, ‘HYANG 1’ 참외를 증폭한 결과에서는 두 종류의 DNA 크기 패턴이 나타났지만 106개 참외 유전자형 분석을 통해 총 세 가지 유형으로 PCR 밴드 패턴을 분류하였다. 단성화를 나타냈던 약 190bp 크기와, 양성화를 나타냈던 약 200bp, 그리고 약 190bp와 약 200bp을 모두 가진 이형 유형을 새롭게 확인할 수 있었 다. 총 106개의 참외에서 이형 유형을 보이는 참외는 21개였고, 21개 모두 단성화의 표현형을 나타냈다(Fig. 3 and Table 2). 세 가지 유전자형 중에서 약 190bp 와 약 200bp를 모두 나타내는 이형에서는 단성화 표현형과 일치했고 양성화의 경우 오직 200bp 크기의 결과만이 나타났다. 종합적으로 샘플번호 88번의 해당하는 ‘HYADPR-2’ 참외 개체를 제외하고 성발현 표현형 형질에 대한 유전자형과의 일치도가 약 99%인 것을 확인할 수 있었다(Table 2). 샘플 번호 88이 포함된 ‘HYADPR’의 경우 세 개체 중 한 개의 개체에서 불일치가 발견되었으므로 본 연구에서 사용된 참외 계통에서의 성발현 표현형과 T1ex 마커 유전자 형의 일치도는 100%를 보인다고 판단된다(Table 2).
높은 일치도를 바탕으로 참외에서 T1ex 마커의 MAS 적용 가능성을 평가하기 위하여 T1ex marker를 이용하여 MAS를 진행하였다. 총 참외 육성 계통의 240개체를 대상으로 정식 전 유전자형 분석을 진행하였고 그 중 T1ex 마커 유전자형에 따라 총 98개체를 선택하여 정식하였다. 선발된 98개체에서 추후 표현형과 T1ex 마커 유전자형과는 모두 100%의 일치를 나타내었다 (Table 3). 이러한 결과를 통해서 멜론에서는 T1ex 마커를 이용하여 단성화의 구분이 어렵다고 판단되었지만 참외에서는 T1ex 마커를 이용한 MAS 성공율이 매우 높다고 판단된다.
본 연구에서는 참외 육종에서 MAS를 이용하여 유묘기에서 성표현형을 선발할 수 있어 식물체가 개화할 때까지 기다릴 필 요가 없음을 확인하였다. 특히 표현형으로는 구분하기 힘든 동형과 이형의 개체를 마커 분석을 통하여 이형유전자형을 효과적 으로 제거할 수 있었다. 이는 이형유전자형의 경우 유전자형이 다음 세대에서 분리하게 되어 추가적인 선발작업이 필요하게 되 는데 MAS를 통해서 이형 개체를 미리 제거 함으로써 형질 고정에 유용하게 사용 될 수 있다. 따라서 본 연구를 통해 확인된 높 은 효율의 T1ex 마커를 이용한 MAS는 단성화 참외 품종 육종에 실질적으로 활용될 수 있으며 이을 통해 육종 비용 절감과 육 종연한 단축에 기여할 수 있음을 확인하였다.