서 언
재료 및 방법
실험 재료
일장 처리
조사 항목
결과 및 고찰
서 언
살비아는 꽃의 수가 많고 색이 선명하여 화단용으로 많이 사용되고 있는 일년생 초화류이다. 실외 조경용으로 사용 시 여름에서 가을 사이에 그 수요가 집중되므로 이 때에 개화 시기를 맞추지 못하면 가격이 폭락할 수 있어, 원하는 시기에 개화시키면서 상품의 질을 향상하고 공급을 원활하게 하기 위해서는 영양생장 및 개화 생리에 관한 연구가 필수적이다.
일장은 식물의 생육 및 개화에 큰 영향을 끼치는 환경 조건 중 하나로 많은 식물이 일장의 영향을 받아 그 개화 양상을 달리하고 있다(Mattson and Erwin, 2005). 본 실험에서 사용된 살비아는 장일 조건에서 개화가 촉진된다(Crawford, 1961). 이와 같은 식물의 일장 반응은 근본적으로 연속된 암기의 길이에 의해서 조절되므로(Runkle et al., 2012) 암기 중간에 빛을 공급하여 연속된 암기를 끊는 야파 처리(night interruption, NI)는 장일 조건을 조성하여 크로코스미아, 시클라멘, 캄파눌라, 코레옵시스, 페튜니아, 루드베키아 등 장일식물의 개화 촉진에 효과적인 것으로 보고되었다(Blanchard and Runkle, 2010; Kang et al., 2008; Park et al., 2006).
야파 처리는 영양생장을 촉진하기도 하는데, 예를 들어 심비디움은 야간에 저광도(3-7µmol・m-2・s-1)로 4시간(22시-02시) 동안 야파 처리를 하였을 때 광합성량이 증가하였고(Kim et al., 2013b), 이로 인해 영양생장이 증가하는 것 뿐만 아니라 개화가 촉진되었다(Kim et al., 2011a, 2011b, 2013a).
현재 온실 재배에서 이루어지고 있는 야파 처리는 22시부터 02시까지가 일반적이다(Blanchard and Runkle, 2010; Mattson and Erwin, 2005). 하지만 나팔꽃과 도꼬마리를 대상으로 한 야파 처리 실험에서 암기 시작 후 9-9.5시간, 8.5시간 후에 야파 처리하였을 때 가장 민감하게 반응하여 개화가 촉진된 것으로 보고되었으며(Thomas and Vince-Prue, 1997), 장일식물인 석죽에서는 02시에서 06시까지 야파 처리를 하였을 때 개화가 촉진되었다(Park et al., 2013). 살비아의 경우 야파를 통한 영양생장 및 개화 조절에 관한 연구 결과는 보고되지 않았다. 따라서 본 연구는 살비아를 대상으로 첫째, 야파 시 광합성량이 증가하였는지와 이로 인해 영양생장이 촉진되었는지, 둘째, 야파가 개화 시기에 어떤 영향을 미치는지와 살비아의 개화를 촉진하기에 가장 적합한 야파 시간대는 언제인지를 조사하고자 수행되었다.
재료 및 방법
실험 재료
본 실험은 국내에서 재배, 생산되고 있는 살비아의 품종 중 Salvia splendens ‘Salsa’를 대상으로 수행되었다. 실험에 사용한 개체들은 어린 잎이 2개 달린 플러그묘를 신농화훼종묘(안성, 대한민국)에서 구입해 온도 변화에 의한 차이를 배제하고 일장의 영향만을 알아보기 위해 주/야간 온도는 23°C, 광도는 130µmol・m-2・s-1 photosynthetic photon flux(PPF) (Apologee Instruments, Inc., Logan, UT, USA)로 고정된 식물 생육상에서 2주간 순화시킨 후 사용하였다. 순화 종료 후 잎이 6개 발생한 2012년 7월 19일에 10cm 포트에 정식하여 실험을 시행하였고, 정식 시 상토는 Sunshine Mix#1 (Sun-Gro Horticulture, Bellevue, WA, USA)를 사용하였다. 실험은 서울대학교 농업생명과학대학 공동기기실에 비치된 식물 생육상에서 이루어졌으며, 식물 생육상 내의 환경은 순화 시기와 동일하게 유지하였다. 실험 기간 중 수분 관리는 주당 2회 EC 1.0dS・m-1의 양액(Technigro 20N-9P-20K Plus fertilizer, Sun-Gro Horticulture, WA, USA)을 이용하여 저면관수법으로 시행하였다.
일장 처리
일장 처리는 단일 처리(주/야, 9/15h), 단일 + 야파 처리를 하였고, 야파 처리는 18시-22시(NI18), 22시-02시(NI22), 02시-06시(NI02)로 나누어 처리하였으며, 처리당 12개체씩 12구 포트 트레이(가로 423mm × 세로 321mm)에 배치하여 처리구별 식물 생육상에서 실험을 시행하였다. 일장 처리는 메탈할라이드등(MH 250W, Hanyoung Electric Co., Gwangju, Korea)과 백색형광등(FLR40EX-W/A, Osram Korea, Ansan, Korea)을 사용하여 9시간(08시-17시) 동안 단일 조건으로 처리하였으며, 이때 광도는 130µmol・m-2・s-1 PPF(Apologee Instruments, Inc., Logan, UT, USA)를 유지하였다. 야파 처리 시 백색형광등(AL-2220D, A-lim Industrial Co., Ltd., Incheon, Korea)을 사용하였으며, 광도는 3-5µmol・m-2・s-1 PPF로 NI18, NI22, NI02 처리군 모두 같게 처리하였다.
조사 항목
실험은 2012년 7월 19일부터 2012년 11월 15일까지 시행되었으며 실험 기간 동안 주 1회 엽수, 측지 엽수, 엽장, 엽폭을 측정하였고 화아분화 이후에는 화아의 수와 꽃의 수를 측정하였다. 휴대용 광합성 측정 장치(Li-6400, Li-Cor Co., Inc., Lincoln, NE, USA)를 사용하여 24시간 동안 광합성량의 변화를 조사하였으며, 야파 처리 5주 후부터 9주 후까지 처리별 3개체씩 반복 측정하였다. 광합성 측정 시 6cm2 챔버(clear open chamber)에 위에서 4-5번째의 성숙한 잎을 물려 측정하였고, 주간 및 야파 처리 시 광도는 식물 생육상의 환경과 동일하였다. 식물 생육상 내 온도는 23°C, 습도는 40-50%를 유지하였고, 식물 생육상에 공급되는 CO2의 농도는 400µmol・mol-1로 설정하였다. 실험 종료 후 부위별 생체중을 측정하였고, 부위별로 건조기(HB-502M, Hanbaek Scientific Technology, Suwon, Korea)에 5일간 건조 후 건중량을 조사하였다. 측정된 데이터의 통계분석은 SAS 9.3 프로그램을 이용하였고 시간대별 처리 간 효과는 Duncan’s multiple range test를 통하여 유의성을 검정하였다.
결과 및 고찰
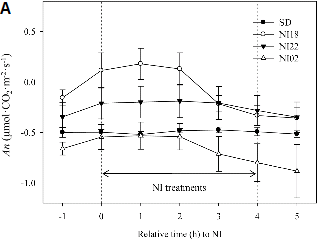
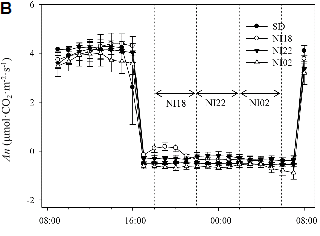
야파 처리를 8주간 실시한 결과, NI02 처리 조건에서 엽수가 가장 적었지만, 측지 엽수는 3.9개로 가장 많았다(Table 1). NI18, NI22 조건에서는 SD 처리와 비교하여 유의적인 차이가 나타나지 않았다. 24시간 동안 광합성량을 측정하였을 때 NI18, NI22, NI02 처리구에서 야파 처리 시간 동안 광합성량이 각각 0.33, 0.16, 0.13µmol・CO2・m-2・s-1 증가하였고, NI18 처리구에서는 야파 기간 동안 순광합성량이 0.18µmol・CO2・m-2・s-1 증가하였다(Fig. 1A). 국화, 캄파눌라, 시클라멘의 연구에서 일적산광량(day light integral, DLI)이 증가할수록 광합성에 의한 영양생장이 증가한다고 보고된 바 있으나(Kjaer and Ottosen, 2011; Niu et al., 2001; Oh et al., 2009), 2µmol・m-2・s-1의 저광도로 Tecoma stans에 일장 연장 처리(day extension)를 하였을 때에는 일적산광량이 거의 증가하지 않아 영양생장이 증가하지 않았다(Torres and Lopez, 2011). 살비아의 경우 저광도 야파 처리 시 광합성량이 다소 증가하였지만 일적산광량이 거의 증가하지 않아 엽장, 엽폭 등의 영양생장이 증가하지는 않았음을 알 수 있었다.
Table 1. Influences of application timings of night interruption (NI) on the number of leaves, number of lateral leaves, leaf length, and leaf width in Salvia splendens ‘Salsa’ at 8 weeks after treatment. |
Treatmentz | Number of leaves | Number of lateral leaves | Leaf length (cm) | Leaf width (cm) |
SD | 22.8 ay | 2.8 b | 11.4 a | 10.6 a |
NI18 | 22.3 a | 3.0 ab | 11.1 a | 9.8 b |
NI22 | 22.3 a | 2.6 b | 11.0 a | 10.3 ab |
NI02 | 19.1 b | 3.9 a | 11.4 a | 10.5 ab |
zThe plants were grown in a growth chamber under 9 h photoperiod [short-day (SD) condition] or 9 h photoperiod with 4 h NI at 3-5 µmol・m-2・s-1. NI timings were 18:00-22:00 HR (NI18), 22:00-02:00 HR (NI22), and 02:00-06:00 HR (NI02). yMean separation within columns by Duncan’s multiple range test at 5% level. |
|
Fig. 1. Changes in net photosynthetic rate (An) of Salvia splendens ‘Salsa’ during the dark period (A) and during 24 hours (B). The plants were grown in a growth chamber under 9 h photoperiod [short-day (SD) condition] or 9 h photoperiod with 4 h NI at 3-5 µmol・m-2・s-1. The NI timings were 18:00-22:00 HR (NI18), 22:00-02:00 HR (NI22), and 02:00-06:00 HR (NI02). Vertical bars are SE of the means (n = 3). |
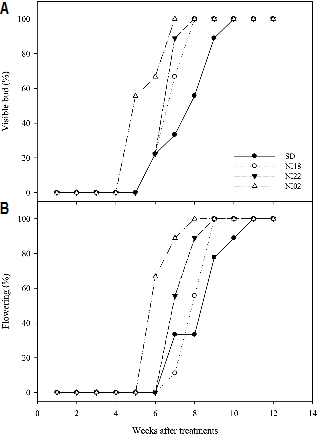
화아 분화 및 개화까지 소요되는 일수는 단일조건에서보다 야파 처리구에서 단축되었다. 야파 적용 시간대에 따른 살비아의 개화는 NI02 처리 시 첫 개화까지 43.4일이 소요되어 개화까지 가장 오랜 시간이 걸렸던 NI18 처리구보다 개화가 10.6일 촉진되었고, SD와 NI22 처리구보다는 9.8일, 5.6일 단축되었다(Table 2 and Fig. 2). 야파 처리 시작일부터 발생한 화아의 수를 1주 간격으로 조사한 결과, 야파 처리 5주 후에 NI02에서 가장 먼저 화아가 나타났고, 야파 처리 7주 후에도 NI02에서 화아가 발생한 개체들의 수가 가장 많았다(Table 2 and Fig. 3A). 야파 처리 6주 이후부터는 NI02에서 개화한 개체들의 수가 가장 많았고, 야파 처리 17주 후에는 NI02에서 꽃의 수가 138.7개로 가장 많았다(Table 2 and Fig. 3B). 따라서 본 연구에 사용된 살비아 ‘Salsa’는 야파 처리 시 개화가 촉진되었고, 그 중 NI02 처리가 가장 효과적임을 알 수 있었다. 일반적으로는 암기 시작 후 5-6시간 뒤인 22시부터 02시까지 야파 처리를 하고 있으나(Blanchard and Runkle, 2010; Mattson and Erwin, 2005), 장일식물인 석죽, Lolium, 후크시아는 암기 시작 후 각각 9, 9, 8시간 후 야파 적용 시 개화가 가장 촉진되었다(Park et al., 2013; Thomas and Vince-Prue, 1997). 이는 광주기에 의한 개화 반응을 결정하는 요소 중 하나로 일주기성 리듬(circadian rhythm)이 있는데, 이로 인해 하루 24시간 중 광에 민감하게 반응하는 시기가 존재하고, 이는 식물의 종류에 따라 서로 다른 특성을 나타낸다(Taiz and Zeiger, 2006). 식물의 개화를 유도하는 유전자 중 GIGANTEA는 LHY, CCA1 유전자에 의해 억제되는데(Mizoguchi et al., 2005), 이 세 유전자는 하루 24시간 중 그 발현 정도에 있어 일정한 양상을 보이며 이는 일주기성 리듬을 따르고 있다(Park et al., 1999). 암기가 진행될수록 개화를 억제하는 LHY, CCA1 유전자의 발현 정도가 증가하였고, 이후 24시간 동안 계속 빛을 공급하였을 때 그 발현 정도가 감소하는 것으로 보아 모든 처리구 중 가장 늦은 시간대인 NI02 처리구에서 암기를 중단하였을 때 이 두 유전자의 활성도가 가장 큰 폭으로 감소할 것이라 판단할 수 있다. 본 실험의 결과와 일주기성 리듬을 고려해 볼 때, 시간대별로 광에 반응하는 민감도에 차이가 있으므로 야파 처리한 시간대에 따라 개화의 양상이 달라진 것을 알 수 있었고, 살비아의 경우 NI02에서 가장 민감하게 나타났다.
Table 2. Influences of application timings of night interruption (NI) on days to visible bud (VB), days to flower, number of flowers, VB (%), and flowering (%) in Salvia splendens ‘Salsa’. |
Treatmentz | Days to VB | Days to flower | Number of flowersy | VB (%)x | Flowering (%) |
Stemw | Branchv |
SD | 49.0 au | 53.2 a | 36.4 b | 33.3 | 0 | 44.4 |
NI18 | 47.8 a | 54.0 a | 70.4 b | 66.7 | 33.3 | 77.8 |
NI22 | 44.6 ab | 49.0 ab | 69.0 b | 88.9 | 33.3 | 88.9 |
NI02 | 38.4 b | 43.4 b | 138.7 a | 100.0 | 88.9 | 100.0 |
zThe plants were grown in a growth chamber under 9 h photoperiod [short-day (SD) condition] or 9 h photoperiod with 4 h NI at 3-5 µmol・m-2・s-1. NI timings were 18:00-22:00 HR (NI18), 22:00-02:00 HR (NI22), and 02:00-06:00 HR (NI02). yNumber of flowers at 17 weeks after treatment. xPercentage of plants with visible bud at 7 weeks after treatment. wPercentage of plants with flower on stem at 8 weeks after treatment. vPercentage of plants with branch with flower at 12 weeks after treatment. uMean separation within columns by Duncan’s multiple range test at 5% level. |
|

|
Fig. 2. Influences of application timings of night interruption (NI) on flowering of Salvia splendens ‘Salsa’. The plants were grown in a growth chamber under 9 h photoperiod [short-day (SD) condition] or 9 h photoperiod with 4 h NI at 3-5 µmol・m-2・s-1. The NI timings were 18:00-22:00 HR (NI18), 22:00-02:00 HR (NI22), and 02:00-06:00 HR (NI02). Photographs were taken at 8 weeks after treatment. |
결론적으로 살비아에 야파 처리 시 광합성이 증가되었으나 DLI 증가를 가져올만큼 충분한 증가는 아니었기 때문에 영양생장을 증가시키지는 못하였다. 그러나 야파 처리로 개화 시기를 단축하였고, 야파 처리 시기는 새벽 2시에 실시한 NI02 처리가 가장 효과적이었다. 또한 이를 통해 재배 기간 중 야파에 가장 민감하게 반응하는 시기와 시간대를 구명하여 특정 시기에 야파를 처리해 개화를 촉진시킬 수 있는 효율적인 처리 방법을 개발할 수 있을 것이며, 이러한 연구는 초화류 재배 시 개화 조절을 위한 중요한 기초자료가 될 것이다.
|
Fig. 3. Change in percentage of plants with visible bud (A) and flower (B) of Salvia splendens ‘Salsa’. The plants were grown in a growth chamber under 9 h photoperiod [short-day (SD) condition] or 9 h photoperiod with 4 h NI at 3-5 µmol・m-2・s-1. The NI timings were 18:00-22:00 HR (NI18), 22:00-02:00 HR (NI22), and 02:00-06:00 HR (NI02). |
Acknowledgements
본 연구는 한국연구재단(2010-0009120)의 지원에 의해 수행되었음.
References
Blanchard, M.G. and E.S. Runkle. 2010. Intermittent light from a rotating high-pressure sodium lamp promotes flowering of long-day plants. HortScience 45:236-241.
Crawford, R.M.M. 1961. The photoperiodic reaction in relation to development in Salvia splendens. Ann. Bot. 25:78-84.
Kang, K.J., W. Oh, J.H. Shin, and K.S. Kim. 2008. Night interruption and cyclic lighting promote flowering of Cyclamen persicum under low temperature regime. Hort. Environ. Biotechnol. 49:72-77.
Kjaer, K.H. and C.O. Ottosen. 2011. Growth of chrysanthemum in response to supplemental light provided by irregular light breaks during the night. J. Amer. Soc. Hort. Sci. 136:3-9.
Kim, H.J., H.H. Jung, and K.S. Kim. 2011a. Influence of photoperiod on growth and flowering of dwarf purple loosestrife. Hort. Environ. Biotechnol. 52:1-5.
Kim, Y.J., H.J. Lee, and K.S. Kim. 2011b. Night interruption promotes vegetative growth and flowering of Cymbidium. Sci. Hortic. 130:887-893.
Kim, Y.J., H.J. Lee, and K.S. Kim. 2013a. Carbohydrate changes in Cymbidium ‘Red Fire’ in response to night interruption. Sci. Hortic. 162:82-89.
Kim, Y.J., S.Y. Lee, and K.S. Kim. 2013b. Photosynthetic characteristics of Cymbidium ‘Red Fire’ and ‘Yokihi’ at different developmental stages. Hort. Environ. Biotechnol. 54:9-13.
Mattson, N.S. and J.E. Erwin. 2005. The impact of photoperiod and irradiance on flowering of several herbaceous ornamentals. Sci. Hortic. 104:275-292.
Mizoguchi, T., L. Wright, S. Fujiwara, F. Cremer, K. Lee, H. Onouchi, A. Mouradov, S. Fowler, H. Kamada, J. Putterill, and G. Coupland. 2005. Distinct roles of GIGANTEA in promoting flowering and regulating circadian rhythms in Arabidopsis. Plant Cell 17: 2255-2270.
Niu, G., R.D. Heins, A.C. Cameron, and W.H. Carlson. 2001. Day and night temperatures, daily light integral, and CO2 enrichment affect growth and flower development of Campanula carpatica ‘Blue Clips’. Sci. Hortic. 87:93-105.
Oh, W., I.H. Cheon, K.S. Kim, and E.S. Runkle. 2009. Photosynthetic daily light integral influences flowering time and crop cha-racteristics of Cyclamen persicum. HortScience 44:341-344.
Park, D.H., D.E. Somers, Y.S. Kim, Y.H. Choy, H.K. Lim, M.S. Soh, H.J. Kim, S.A. Kay, and H.G. Nam. 1999. Control of circadian rhythms and photoperiodic flowering by the Arabidopsis GIGANTEA gene. Science 285:1579-1582.
Park, H.G., H.G. Ahn, S.T. Kim, and S.T. Choi. 2006. Effect of photoperiodic treatments on growth and flowering of Crocosmia crocosmiiflora. Flower Res. J. 14:252-257.
Park, Y.J., Y.J. Kim, and K.S. Kim. 2013. Vegetative growth and flowering of Dianthus, Zinnia, and Pelargonium as affected by night interruption at different timings. Hort. Environ. Biotechnol. 54:236-242.
Runkle, E.S., S.R. Padhye, W. Oh, and K. Getter. 2012. Replacing incandescent lamps with compact fluorescent lamps may delay flowering. Sci. Hortic. 143:56-61.
Taiz, L. and E. Zeiger. 2006. Plant physiology. 4th ed. Sinauer Associates, Sunderland, MA, USA.
Thomas, B. and D. Vince-Prue. 1997. Photoperiodism in plants. 2nd ed. Academic Press, London, UK.
Torres, A.T. and R.G. Lopez. 2011. Photoperiod and temperature influence flowering responses and morphology of Tecoma stans. HortScience 46:416-419.






