서 언
재료 및 방법
기내배양을 통한 식물 재료의 획득
인편삽(scaling) 및 소인편삽(in vitro scale culture, microscaling)
기내배양에 의한 LSV 제거율 및 노지 재배조건에 따른 재감염률 조사
바이러스 검정
엽록소 및 단백질 정량 분석
통계 분석
결과 및 고찰
기내배양 횟수에 따른 LSV 제거
포장 구근비대 과정에서의 LSV 감염률 변화
서 언
자생나리의 활용 빈도나 가치가 크게 높아지고 수요도 급속히 증가하고 있지만 구근 값이 비싸고 바이러스의 감염 정도가 심하여 저렴한 우량 종구의 보급을 통한 산업 확장이 어려운 실정이다. 또한 영양번식에 의한 병 감염, 토양 감염, 다른 작물로의 전염, 소비자로부터의 외면 등으로 인해 자생나리 원종이 멸종 위기에 있다. 또한 일반 농가에서는 자생나리 자구가 연작에 의해 생산되기 때문에 바이러스 복합감염이 심각하다.
나리에 발생하는 주요 바이러스는 lily symptomless virus (LSV), cucumber mosaic virus(CMV), tulip breaking virus (TBV), tomato ringspot virus(ToRSV) 등 약 20여 종이 보고되고 있다(Kim and de Hertogh, 1997). 이 중 LSV의 감염이 가장 일반적인데, 단독으로는 뚜렷한 병징을 보이지 않거나 엷은 황색 줄무늬 병징을 보이기도 하지만, CMV 등과 복합 감염되면 모자이크와 괴저 반점이 생기며, 심하면 낙엽 등 치명적 피해를 준다(Lim et al., 2009). 이와 같이 LSV가 다른 바이러스와 복합 감염되면 그 병징이 심화되고 식물체의 생장이 저조해지는(Niimi et al., 1999) 등 피해 정도가 심화된다. LSV와의 복합 감염에 의해 잎 투명화, 줄무늬, 조기 노화, 생장 감소, 꽃의 왜소화, 절화수명 단축, 구근 수량 감소 등으로 품질과 수량에 많은 영향을 미친다(Woo et al., 2004). 이와 같이 나리는 바이러스의 복합감염 등에 의해 구근의 품질과 화훼작물로서의 상품적 가치가 현저히 감소하지만, 조직배양을 통해서 병원균 제거와 무병주 생산이 가능하게 되어 이를 극복하고 있다(Kim and de Hertogh, 1997). 즉 나리의 바이러스 무병주는 기내 인편삽(Cohen et al., 1985), 경정배양(Kim et al., 1996), 캘러스 배양(Mori and Hosokawa, 1977) 등의 조직배양과 열처리 및 화학처리를 병행함으로써 얻을 수 있다.
바이러스 무병주는 일반적으로 초장이 길고 생장이 왕성하며, 절화수명이 길고, 구근 비대가 빠르며 꽃 자체의 품질이 양호한 편이다(Woo et al., 2005). 나리의 개화구 생산을 위해서는 포장에서 2-3년 구근을 비대시켜야 한다. 따라서 건전한 식물체의 유지와 바이러스의 감염 방지를 위해서는 재배상의 관리, 즉 이병 매개체 방제, 이병주 제거, 무병주 사용 등이 중요하며, 이를 위해서는 바이러스 검정은 필수적인 과정이다.
나리의 바이러스에 대한 국내 연구는 LSV에 대한 검정기술의 정립(Kim et al., 1995a, b), 바이러스의 동정(Chang and Kim, 1996), 바이러스 제거를 위한 화학적 처리법과 열처리법 등이 시도되었으며(Seo et al., 1999), 바이러스 무병주 생산은 생장점 배양, 캘러스 배양과 Virazole 처리 등으로 가능하게 되었다(Kim et al., 1996; Park and Kim, 2003; Woo et al., 2004). 바이러스 감염 정도는 항체를 이용한 direct tissue blotting immunobinding assay(DTBIA)와 enzyme-linked immuno-sorbent assay(ELISA)에 의해 진단할 수 있으며(Park et al., 2003), 조기 발견과 정확한 진단에는 reverse transcription polymerase chain reaction(RT-PCR) 분석을 이용할 수 있다(Joung et al., 1996; Kim et al., 2001). 그러나 대부분의 연구가 국내 재배면적이 월등한 수입 품종에 집중되어 있고(Chinestra et al., 2010; Park and Kim, 2003; Park et al., 2003; Seo et al., 1999; Woo et al., 2005), 자생나리와 관련해서는 미흡한 실정이다.
따라서 이 연구에서는 개발 가치가 높은 자생나리 4종을 대상으로 LSV 무병주 생산을 위한 적정 계대배양 횟수 및 무병 구근 정식 후 구근비대 조건에 따른 LSV 재감염률을 분석하여 자생나리 구근생산 체계 확립에 대한 기초자료를 제공하고자 하였다.
재료 및 방법
기내배양을 통한 식물 재료의 획득
이 연구에서는 날개하늘나리(Lilium dauricum), 말나리(L. distichum), 참나리(L. lancifolium), 중나리(L. maximowitzii) 등 4종의 기내배양 소인경을 사용하였다. 자생나리의 초대배양을 위한 재료(exlpant)는 인편삽으로 얻은 소인경의 인편을 사용하였다. 구체적으로는 포장에서 수확한 인경에서 인편을 분리하여 소독한 다음, 기외에서 인편삽(in vivo scaling)하고, 여기에서 얻은 소인경의 인편을 소독하여 기내에서 인편삽(in vitro microscaling)하여 무균상태에서 자생나리 소인경을 유도하였다. 이들 자생나리 소인경의 기내 유지와 증식, 즉 계대배양은 소인경의 인편을 기내에서 인편삽하여 소인경을 유도하고 비대시킨 다음, 비대된 소인경의 인편을 다시 기내에서 인편삽하는 방법을 반복하였다. 소인경의 유도와 비대를 위한 배양기간은 각각 8주과 12주였다.
기본배지는 MS(Murashige and Skoog, 1962) 배지를 사용하였으며, 소인편으로부터 소인경 유도는 sucrose 30g・L-1, 소인경 비대는 sucrose 90g・L-1를 각각 기본배지에 첨가한 다음 pH 5.7로 조정한 후 한천 7g・L-1를 첨가하였다. 배지는 120°C, 1.2기압에서 10분간 고압 멸균소독하였다. 배양실은 온도 22 ± 2°C, 광도는 형광등을 이용하여 하루 16시간동안 배양병 상단에서 PPFD 24μmol・m-2・s-1(1,700Lux)로 유지시켰다.
인편삽(scaling) 및 소인편삽(in vitro scale culture, microscaling)
초대배양을 위한 재료를 얻기 위해 자생나리 구근의 가장 바깥쪽 인편을 제거하고 깨끗한 인편들을 분리해서 상대습도 70-80%, 온도 25-30°C, 암조건의 생장상에서 3-4일간 큐어링한 다음 실온에서 베노밀수화제(a.i. 50%) 수용액(2g・L-1)에 인편을 넣어 1시간 동안 침지처리한 후 수돗물로 깨끗이 세척하였다. 플라워박스 바닥에 하이드로볼을 깔고 코코피트, 펄라이트, 훈탄, 버미큘라이트 등이 혼합된 플러그용 상토(토실, 신안그로, 진주, 한국)로 채운 다음 표면에서 깊이 2cm 아래에 인편삽한 후 20 ± 3°C의 온실에서 관리하였다
기내에서 유도된 소인경을 기외에서 인편삽할 경우에는 인편들을 분리하여 수세하고 위와 같은 요령으로 큐어링한 후 35°C의 GA3 100mg・L-1 용액에 1-2시간 동안 구근을 침지하여 온탕처리하였다. 이후 인편들을 수세하여 온도를 떨어뜨린 후 육묘용 트레이(5.5 × 5.5cm, 32공)에 인편삽과 동일한 원예용 상토를 채운 다음 각 셀당 5개의 소인편을 표면에서 2cm 깊이로 심었다. 소인편 삽상의 상대습도는 70-80%, 온도는 20°C, 광조건은 암상태로 하였으며, 소인편삽의 기간은 8주로 하였다.
기내배양에 의한 LSV 제거율 및 노지 재배조건에 따른 재감염률 조사
기내배양 횟수에 따른 LSV 감염률 변화를 구명하기 위해 노지에서 수확한 인경, 이 인경의 기외 인편삽을 통해 얻은 인경, 그리고 이것으로부터 획득한 인편의 기내 초대배양과 5차에 걸친 계대배양에서 얻은 소인경의 LSV 감염 여부를 조사하였다. 실험은 3반복으로 수행하였고, 반복당 15개의 인편을 사용하였다.
기내배양(소인편삽)을 통해 획득한 무병구를 나이에 따라 노지에서 계절별 식재와 수확을 반복하면서 LSV 감염률을 조사하였다. 최초 기내 인편삽 유래의 소인경과 이 소인경을 경북 경산시 영남대학교 부속농장의 온실에서 1-3년간 비대시켜 얻은 인경을 재료로 인편삽하여 얻은 구근들을 각각 가을(10월 20일)과 봄(이듬해 3월 31일)에 포장에 정식한 후 가을에 수확하여 바이러스 감염 여부를 조사하였다. 실험은 3반복으로 수행하였고, 반복당 30개의 인경을 10 × 10cm 간격으로 정식하였다.
한편, 재배조건에 따른 LSV 감염률을 분석하기 위해 기내 인편삽 유래 소인경을 구근비대시키면서 획득한 구근의 나이(1, 2, 3년), 정식거리(5 × 10, 10 × 10, 10 × 15, 15 × 15cm), 그리고 재배지역(포항, 경산)을 달리하여 노지 포장에 10월 20일에 정식하였으며, 가을에 수확하여 바이러스 감염 여부를 조사하였다. 구근의 나이별로 균일한 구근 480개씩을 선별하여 2개 지역으로 나누고 다시 4가지 정식거리로 나누어 최종 처리별 3반복, 반복당 20구씩을 정식하였다.
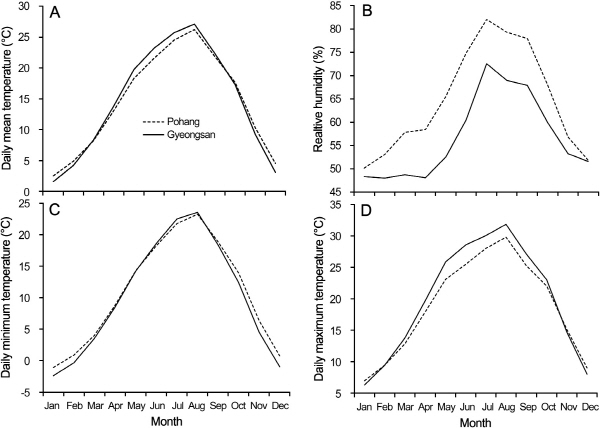
경상북도의 포항과 경산은 비슷한 위도에 위치한 해안 및 내륙지역이며, 이들 지역의 실험기간(2006-2010) 중 일평균기온(daily mean temperature, DMT), 일최저기온(daily minimum temperature), 일최고기온(daily maximum temperature) 및 상대습도(relative humidity, RH)의 월 평균값은 Fig. 1과 같다. LSV 감염률은 DTBIA로 확인하였고, LSV 감염주와 무병주의 엽록소 함량과 단백질 함량을 비교하였는데 그 방법들은 다음과 같다.
바이러스 검정
LSV의 감염 유무는 계대배양 중인 소인경의 소인편과 포장에서 생육 중인 식물체의 잎을 재료로 Park et al.(2003)이 수행한 방법에 따라 DTBIA법으로 검정하였다. 처리구의 반복당 검정 수는 맹아 및 생육이 어느 정도 진행된 10- 20개로 하였다. 잎과 인편을 면도칼로 자른 다음, 직경 0.45μm pore의 nitrocellulose membrane(NC막; LC2001, Thermo Fisher Scientific, MA, USA)에 즙액인 항원을 묻히고 불순물을 제거하기 위해 1-2% bovine serum albumin(BSA; Sigma-Aldrich Co., St. Louis, MO, USA)이 포함된 phosphate buffered saline(PBS, NaCl 8.09, KH2PO4 0.29, Na2HPO4・12H2O 2.99, KCl 0.29g・L-1, pH 7.4) 용액에 1시간 동안 침지시켰다. 침지 후 NC막을 PBST buffer(NaCl 8.09, KH2PO4 0.29, Na2HPO4・12H2O 2.99, KCl 0.29g・L-1, Tween 20 0.5 mL・L-1, pH 7.4)로 3회 세척한 후, PBS 용액에 항혈청(1차 항체, capture antibody; rabbit polycolonal antisera; Antibodies Inc., Davis, CA, USA)을 넣고 실온에서 2시간 동안 NC막에 항체가 부착되도록 반응시킨 다음 PBST 용액으로 3회 세척하였다. 그리고 효소가 부착된 두 번째 항체(2차 항체, conjugated 2nd antibody; alkaline phosphatase enzyme conjugate- labelled rabbit immunoglobulins; Promega Co., Madison, WI, USA)를 PBS 용액에 넣은 다음 2시간 동안 NC막을 반응시켰다. 다시 동일한 과정으로 세척한 다음 기질용액 A [(2mL 2.5M Tris-HCl(pH 9.5) + 2mL 2M NaCl + 0.2mL 1M MgCl2 + 35.5mL DW)], B(14mg NBT/0.3mL MeOH)와 C(7mg BCIP/0.05mL DMSO)에 넣어 발색시켰다. 발색된 NC막을 증류수로 세척하고 stop buffer(0.01M Tris-HCl, 0.001M EDTA, pH 7.5)에서 10분간 2회 침지시켜 반응을 정지시킨 후, 상온에서 건조시켜 감염 여부를 육안으로 관찰하였다.
엽록소 및 단백질 정량 분석
엽록소 함량 분석을 위해 모구 및 기내 인편삽 후 기외 인편삽 유래 식물체 각 10개체로부터 채취한 잎 1g당 80% 아세톤 용액 50mL로 마쇄한 후 여과지(Whatman No. 2)로 여과하여 분석하였다. 추출액은 UV-visible spectrophotometer (S-3130, Sinco, Korea)를 이용하여 652nm에서 흡광도를 측정한 다음, Yoshita et al.(1971)의 방법에 따라 총 엽록소(total chlorophyll) 함량을 계산하였으며 mg・g-1 FW로 표시하였다.
단백질 분석을 위한 단백질 추출은 Kim et al.(1999)의 방법에 따라 모구 및 기내 인편삽 후 기외 인편삽 유래 식물체 각 10개체로부터 채취한 잎 2g을 액체질소를 사용하여 마쇄하여 분말로 만들었다. 마쇄액[0.4M sucrose, 25mM Tris-HCL (pH 7.6), 1mM DTT, 0.1% BSA, 10mM KCl, 1mM EDTA, 0.1mM MgCl2] 8mL를 첨가해 균질화한 다음 500×g에서 15분간 원심분리하여 얻은 상징액(supernatant)을 10,000×g에서 15분간 다시 원심분리하여 상징액을 회수하여 단백질 측정용 시료로 사용하였다. 모든 실험상의 조작은 0-4°C에서 수행하였다. 단백질의 농도 측정은 Bradford(1976)의 방법에 따라 BSA를 표준 단백질로 하여 정량하였다. 즉 BSA 0, 0.1, 0.2, 0.4, 0.8, 1, 2, 4μL씩, 추출한 시료 단백질 1, 2μL, Bradford reagent 80μL, 그리고 멸균한 물로 각각 최종 볼륨이 200μL가 되도록 맞춰 96-well plate(SPL, 한국)에 넣은 후 microplate reader(UVM340, Biochrom Ltd., UK) 이용하여 595nm에서 흡광도를 측정하였다. 정량 후 시료의 단백질의 양은 Microsoft Excel을 이용하여 그래프와 R2의 값이 0.9 이상인 방정식을 구하여 계산하였다. 단백질 함량은 mg・g-1 FW로 나타내었다.
통계 분석
SAS(Statistical Analysis System, V.6.12, USA) 프로그램을 이용하여 Duncan’s multiple range test와 least significant difference test에 의해 처리 평균값 간의 차이를 유의수준 p < 0.05에서 검정하였다.
결과 및 고찰
기내배양 횟수에 따른 LSV 제거
LSV에 감염된 자생나리를 포장에서 수확한 후 기내배양의 재료로 사용하여 각 인편배양 횟수별로 LSV 감염률을 조사하였다(Table 1). 먼저 모구(mother plant) 및 기외에서 모구 인편삽(in vivo scaling)으로 얻은 식물체의 LSV 감염률은 4종 모두 100%였다. 여기에서 획득한 소인경을 소독하여 초대배양(기내 인편삽, primary culture)한 후에는 날개하늘나리(L. dauricum)와 말나리(L. distichum)의 경우 LSV가 100% 제거되었다. 반면 참나리(L. lancifolium)와 중나리(L. maximowitzii)는 감염률이 80%와 90%로 여전히 높았다. 그러나 계대배양(subculture) 횟수가 늘어날수록 LSV의 감염도가 줄었으며 모두 5회 인편배양(5th subculture) 시에 완전히 제거되었다(Table 1).
일반적으로 아시아틱 나리는 경정배양이 인편배양보다 바이러스 제거율이 높은 것으로 보고되었지만(Park and Kim, 2003), 날개하늘나리와 말나리의 경우에는 기내 인편배양만으로도 LSV 제거효과가 높았다(Table 1). 이에 대한 원인을 본 연구에서 직접 밝히지는 않았으나, 그 원인은 인편의 기부에서도 경정분열조직처럼 바이러스의 이동에 비해 세포분열이 빨라 바이러스의 이동이 어렵고, 이 조직의 세포 대사활성이 커 바이러스의 복제가 불가능하게 되며, 바이러스 불활성화계가 활발하여 감염되지 않았거나 내생 옥신의 함량이 높아 바이러스의 증식이 억제되었기 때문으로 추정된다(Allen and Anderson, 1980; Blom-Barnhoorn et al., 1986; Chang and Kim, 1996; Horst, 1988; Kassanis, 1957; Lawson, 1990).
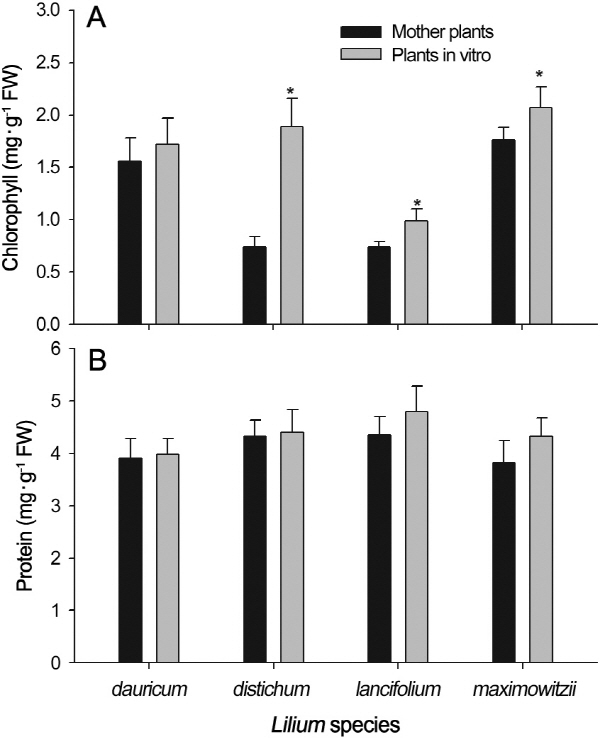
본 연구에서 LSV에 감염된 식물체에서 엽색이 옅어지는 현상이 나타났는데, 자생나리 4종의 LSV 감염 모체와 기내 인편삽을 통해 획득한 LSV 무병주의 엽록소 함량을 비교한 결과, 날개하늘나리를 제외한 3종에서 기내배양으로 획득한 LSV 무병주의 엽내 엽록소 함량이 LSV 감염 모체보다 다소 높았다(Fig. 2A). 바이러스 감염주의 병징 중 잎에 줄무늬가 생기거나 투명화가 되는 것은 엽록소 함량의 감소에 기인한다(Plattt et al., 1979; Woo et al., 2004). 이들 4종의 LSV 감염 모체와 기내배양으로 획득한 LSV 무병주의 단백질 함량을 측정한 결과, 모두 기내배양으로 획득한 LSV 무병주에서 단백질 함량이 높은 경향을 보였지만, 통계적 유의차는 없었다(Fig. 2B). 따라서 감염주를 손쉽게 판별하는 방법으로 엽록소 함량의 감소 정도를 활용할 수 있을 것으로 판단되었다. 다만 좀더 쉽게 판별하기 위해 엽록소 정량 분석값과 간이 엽록소측정기(chlorophyll meter SPAD-502 Plus, Minolta, Japan)의 측정값과의 상관관계를 밝히는 연구가 필요하다고 생각된다.
포장 구근비대 과정에서의 LSV 감염률 변화
포장에서의 구근비대 과정에서 LSV 감염률 변화를 알아보기 위해 기내 소인경과 기외 인편번식 인경의 정식시기를 달리하여 LSV의 감염률을 조사하였다(Table 2). LSV의 감염 정도는 기내배양 소인경이나 포장재배 기간이 짧아 기외 노출기간이 짧은 1년생 구근(1-year-old bulb through scaling)에서는 시기별 뚜렷한 차이를 보이지 않았지만, 포장 노출기간이 길었던 2-3년생 구근의 경우 봄 정식보다는 가을 정식에서 더 높은 바이러스 감염률을 나타냈다. Goo et al.(2013)에 의해 경기도 수원에서 조사된 진딧물의 연간 발생빈도를 보면, 3월부터 발생하여 5월에 최성기를 이루고 이후 감소하다가 10월경에 거의 비래(flying)가 끝나는 것을 알 수 있었다. 수원보다 봄과 가을 온도가 높은 경산지역은 좀더 일찍 발생하고 좀더 늦게까지 비래한다고 예측할 수 있다. 따라서, 가을에 정식할 경우 이른 봄부터 생장을 시작하기 때문에 그만큼 LSV 매개곤충인 진딧물에 노출되는 기간이 상대적으로 길어 LSV 감염률도 높을 것으로 생각되었다. 기내배양 소인경(bulblet through in vitro culture)의 경우 참나리는 LSV에 감염되지 않았고, 날개하늘나리와 중나리에서는 LSV에 1.7-7.2% 감염되었다(Table 2). 반면, 인편삽 1년생 구근에서는 3종 모두 6.1-25.4%로 LSV 감염도가 높았는데, 이것은 인편삽 모구가 이미 LSV에 감염되어 있었기 때문으로 생각된다.
종구의 재배기간이 길어질수록 LSV의 감염률이 높아져 3년된 종구에서는 가을 정식구 모두 50% 이상의 감염률을 나타내었고, 특히 중나리의 경우 96.2%의 감염률을 나타냈다(Table 2). 신나팔나리의 경우, 포장에서 6년 이상 재배 시 LSV, CMV 등 두 종류 이상의 바이러스에 의한 복합감염률이 80% 이상이라는 보고(Chung et al., 2003)도 있다. 이러한 LSV의 감염은 주 발생시기인 5월 중순 이후에 심해졌고, 특히 인편삽 3년생묘에서 그 정도가 심했다. 이는 LSV의 주된 매개체인 진딧물에 의한 감염이 원인(Asjes, 2000)으로 생각된다. 따라서 LSV의 감염을 예방하거나 감소시키기 위해서는 이 시기에 방충망 등으로 진딧물과의 접촉을 차단하고 살충제를 주기적으로 살포할 필요가 있을 것으로 판단되었다.
이상의 결과는 기내배양으로 생산된 소인경의 경우 바이러스 감염률이 매우 낮으나 구근의 재배기간이 길어질수록, 즉 구근의 노지 노출기간이 길어질수록 LSV의 감염률이 높아졌다는 것을 나타낸다. LSV는 진딧물에 의해 비영속적으로 전염되며, 자연기주는 튤립이나 알스트로메리아 등이며 종자 전염은 되지 않으나 종구 전염이 되는 것으로 알려져 있다(Asjes, 2000; Asjes et al., 2002; Chinestra et al., 2010; Hsu et al., 1995). 즉 종구의 감염률이 높거나 진딧물 피해가 많을 경우 LSV에 감염될 확률이 높아지게 된다. 따라서 LSV 무병 구근의 생산을 위해서는 바이러스 무병 종구의 선별 재배, 맹아 시 병징 발병주의 즉시 제거, 그리고 진딧물 방제가 중요하며(Asjes, 2000; Chinestra et al., 2010; Goo et al., 2013), 노지 재배기간이 길어질수록 감염 확률은 높아질 것으로 판단된다.
자생나리의 LSV 감염률에 미치는 재배지, 구근 크기 및 정식거리의 영향을 살펴본 결과(Table 3), 날개하늘나리는 LSV 감염률이 재배기간이 길수록, 또 밀식한 구에서 높아지는 경향이었다. 날개하늘나리와 중나리는 2년 이후 내륙인 경산보다는 해안가인 포항에서 LSV 감염률이 낮은 경향을 보였다. 참나리는 재배지 간에 큰 차이가 없었다(Table 3). 중나리는 LSV의 감염률이 다른 종에 비해 월등히 높게 나타났고, 포항보다 경산이 높았다(Table 3). 오리엔탈나리 ‘Casa Blanca’, ‘Acapulco’, ‘Marco Polo’의 경우 구근 생산성은 해안지가 평야지보다 높았다는 보고(Kim et al., 1998)가 있었다. Goo et al.(2013)도 국내에서 우량종구를 생산하기 위해서는 해풍이 잘 불고 물빠짐이 좋은 해변지나 여름이 시원한 고랭지 등을 구근생산지로 선택해야 한다고 하였다. 이는 LSV의 재감염 정도가 종간에 다르게 나타나며, 유전적 원인 외에도 재식거리나 재배환경, 매개곤충 밀도의 영향도 받는다는 것을 의미한다.
경산과 포항의 2006-2010년의 기상 특성을 비교 분석해 보면, 연평균기온은 각각 14.7°C와 14.5°C로 유사하지만, 10-2월까지의 일평균기온(daily mean temperature, DMT)은 해안지역인 포항이 높았고, 4-9월에는 내륙지역인 경산이 높았다(Fig. 1A). 일최저기온(daily minimum temperature)의 연평균은 경산이 10.2°C로 포항의 10.9°C보다 약간 낮았는데, 월별 차이를 보면 10-4월엔 포항이 높았고, 6-8월엔 경산이 조금 높았다(Fig. 1C). 반면 일최고기온(daily maximum temperature)의 연평균은 경산이 19.9°C로 포항의 18.8°C보다 1.1°C 높았는데, 특히 5-8월에 2°C 이상 높았다(Fig. 1D). 반면 상대습도는 경산의 연평균이 56.7%로 포항의 64.5%보다 7.8%p 낮았다(Fig. 1B). 특히 4-9월에는 그 차이가 10%p를 넘었으며, 10-2월에는 차이가 5%p 이하로 줄었다. 이를 종합하면 경산은 포항에 비해 겨울이 더 춥고 여름이 더 덥고 건조한 것으로 나타났다. Lee et al.(1997)은 6-8월 진딧물 발생이 상대습도와 부의 상관관계가 있다고 보고하였는데, 이것이 상대습도가 낮은 경산의 LSV 감염률이 포항보다 높은 이유라 생각되었다.
이상의 결과에서, 자생나리 구근의 기내 인편삽으로 최대 5회의 계대배양을 통해 LSV 무병주 생산이 가능하였다. 또한 저온저장을 거쳐 봄 정식, 구근 크기에 따른 정식거리 조절 및 해안지 재배를 병행할 경우 종에 따라서는 LSV 감염을 어느 정도 지연시킬 수 있을 것으로 판단된다.