서 언
재료 및 방법
잔디 유전자원
잔디 DNA 추출 및 ITS 구간 증폭
잔디 ITS 염기서열 확보 및 염기서열 유사도와 유연관계 분석
ITS 염기서열의 CAPS marker 전환 및 분석
결과 및 고찰
잔디의 ITS 증폭 및 염기서열 분석
잔디 ITS 염기서열 기반 CAPS marker 전환 및 적용
미동정 수집 자생 Zoysia 속 잔디의 외부형태적 및 ITS 기반 CAPS marker 분석을 통한 잔디 분류
동정된 들잔디와 갯잔디의 ITS 염기서열 유사성 분석 및 유연관계 분석
Measurement of Silicon Content
서 언
잔디는 학교운동장 및 공원, 도로변, 골프장, 스포츠 경기장 등에 다양한 장소에 식재되고 있는 주요 원예 작물이다. 최근 그 범위가 확대되고 있어 실용적 및 잠재적 가치가 점차 증가하고 있는 추세이다(Sun et al., 2010; Hyun et al., 2012). 잔디는 생육 적온에 따라 고온에 강한 난지형 잔디와 저온에 강한 한지형 잔디로 구분되며, 난지형 잔디에는 대표적으로 들잔디(Zoysia japonica)와 갯잔디(Zoysia sinica), 금잔디(Zoysia matrella), 왕잔디(Zoysia macrostachya), 버뮤다그라스(Cynodon dactylon) 등이 속하며, 한지형 잔디는 크리핑 벤트그라스(Agrostis stolonifera), 켄터키 블루그라스(Poa pratensis), 톨훼스큐(Festuca arundinacea), 라이그라스(Lolium perenne) 등이 있다(Kim and Lee, 2010). 우리나라에서 주로 자생하는 난지형 잔디 Zoysia 속(Zoysia species) 중 잔디로 이용되는 것은 들잔디(Z. japonica)와 금잔디(Z. matrella)가 있으며, 특히 들잔디는 여름철의 극 심한 고온 및 건조, 해안가 모래의 염분 같은 환경에서도 잘 적응하는 특성이 있다(Sun et al., 2010; Hyun et al., 2012). 그 외에 해안지대에서 자생하는 갯잔디(Z. sinica)와 왕잔디(Z. macrostachya)가 있으며, 그 중 갯잔디는 수분과 양분의 요구도가 비교 적 적다는 점에서 들잔디와 유사하지만, 내염성과 내건성이 들잔디 보다 매우 강한 특성이 있어 종 및 속간 교잡을 이용하여 신 품종 개발에 활용될 수 있는 유전자원이다(Yu et al., 1974; Li et al., 2006; Hyun et al., 2012; Chung et al., 2013). 그러나 바닷 가 및 갯벌과 같은 장소에서 자생하는 내염성 들잔디 및 갯잔디의 경우에는 다른 난지형 잔디에 비해 외부 형태적 특성이 매우 유사하여 비전문가가 구별하는 것이 쉽지 않다. 따라서 기존의 외부형태학적 동정법에만 의존하기 보다는 분자생물학적 기법 을 이용한 분류 또한 필요한 실정이다.
이러한 문제점을 해결하기 위해서 restriction fragment length polymorphism(RFLP), random amplified polymorphic DNA(RAPD), amplified fragment length polymorphism(AFLP), simple sequence repeat(SSR), sequence related amplified polymorphism(SRAP) 등 많은 종류의 식물 분류를 위한 molecular marker가 개발되어 왔다. 잔디의 경우 라이그라스(Kubik et al., 2001), 버팔로그라스(Wu et al., 1994; Budak et al., 2004), 텍사스 블루그라스(Renganayaki et al., 2001)에서 marker가 보고되어 있다. 그러나 이러한 marker들은 비교적 비용과 시간이 많이 들고 다소 복잡하다.
최근 표준화 가능한 분류 및 동정법으로 모든 생물에 존재하는 DNA 염기서열 정보를 동정에 응용하는 DNA 바코드(DNA barcode) 분석법이 개발되었다(Hebert et al., 2003). DNA 바코드는 다양한 생물종에 공통적으로 보존 및 변이되어 존재하는 특정한 유전자 및 염기서열 구간이며, 생물의 아주 작은 조각에서도 DNA 분석이 가능하고 간단한 PCR 증폭과 염기서열 분석 을 통하여 미동정 생물체 동정에 활용되고 있다(Hebert et al., 2003; Kress et al., 2005; Koch, 2010; Kim et al., 2015). 이러한 DNA 바코드 분석법은 생물다양성협약(Convention on Biological Diversity, CBD)의 국제적 생물종 분류기준(Consortium for the Barcode of Life, CBOL, http://barcoding.si.edu)으로 채택되어 나라별 고유종 및 신종 등록과 수집한 생물의 표본관리, 의약품 등 신물질 재료 판별 검증 등에 응용이 가능하여 식약처 및 환경부, 농림부 등 다양한 기관에서 생물 분류시 연구 및 활 용되고 있다(Baigalmaa et al., 2009; Ahn et al., 2010; Hong et al., 2012; Moon et al., 2013). 생물 분류를 위한 DNA 바코드 분 석은 핵 내 ribosomal DNA(nrDNA)의 internal transcribed spacer (ITS) 염기서열 구간 등을 이용하여 연구되어 왔다(Kress et al., 2005; Baigalmaa et al., 2009; Ahn et al., 2010; China Plant BOL Group et al., 2011; Hong et al., 2012; Kress and Erickson, 2008; Moon et al., 2013). ITS 염기서열 구간은 18S와 26S ribosomal DNA 사이에 존재하는 ITS1과 ITS2 염기서열로(Fig. 2), 양친 유전성을 가지며, 생물 종에 따라 보존 지역과 변이 지역이 뚜렷하여 polymerase chain reaction(PCR)을 통한 분리 및 염 기서열 분석에 유리하다(Kress et al., 2005; CBOL Plant Working Group, 2009; Ahn et al., 2010; Hong et al., 2012). 또한, ITS 는 종간 및 속간 유연관계, 진화양상, 시중에 유통되는 한약제 위품들의 판별 등을 분석하는데 중요한 자료로도 이용되고 있다 (Baigalmaa et al., 2009; Gao et al., 2010; Yao et al. 2010).
그러나 ITS 분석을 바탕으로 Zoysia 속 들잔디와 갯잔디 간의 유연관계 및 종 구별을 위한 분자생물학적 연구는 미흡한 실 정이다. 따라서 본 연구에서는 제주도 및 전라남도, 전라북도, 경상남도, 경상북도의 산, 해안지역, 섬에서 자생하는 Zoysia 속 잔디를 수집하고, ITS 염기서열 구간을 이용하여 자생 Zoysia 속 잔디로부터 들잔디 및 갯잔디를 구별하고자 하였다. 또한, 각 잔디별 ITS 염기서열 차이를 기반으로 cleaved amplified polymorphic sequence (CAPS) marker (Konieczny and Ausubel 1993; Kunihisa et al., 2003; Kim et al., 2012)를 개발하고자 하였다
재료 및 방법
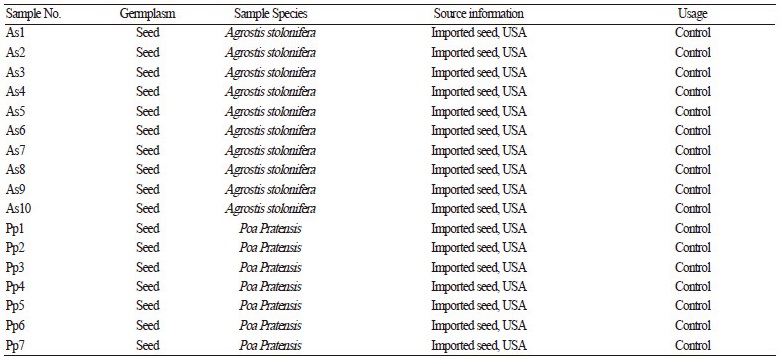
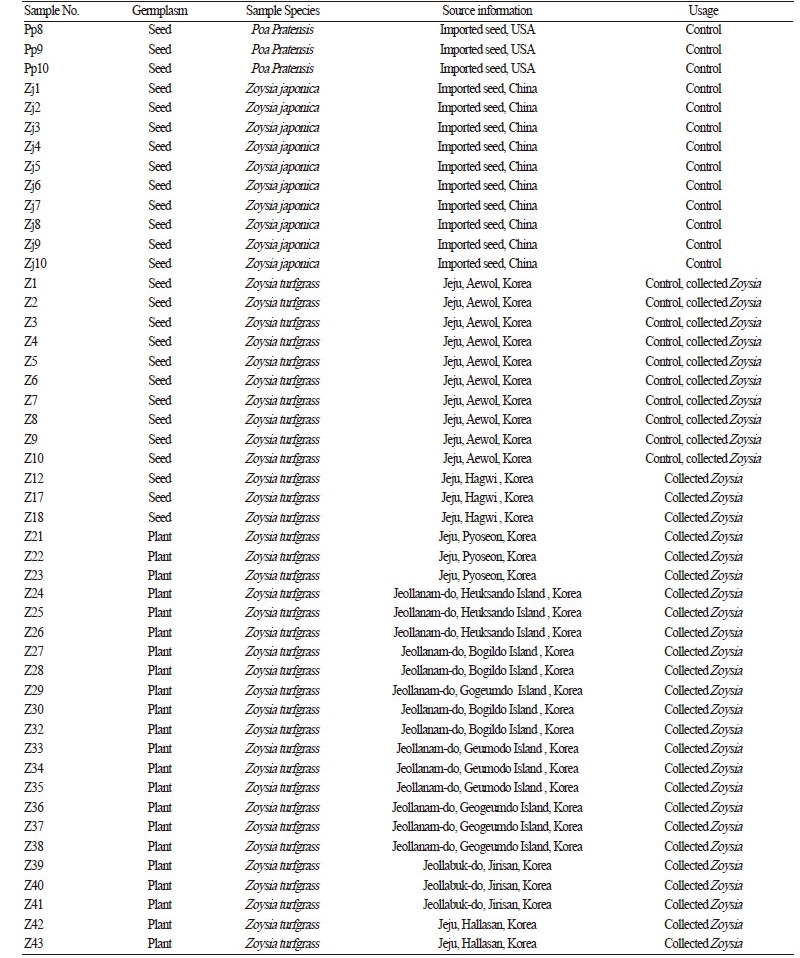
잔디 유전자원
본 연구에서 사용된 들잔디(Z. japonica, China)와 크리핑 벤트그라스(A. stolonifera, USA), 켄터키 블루그라스(P. pratensis, USA)의 판매 종자 및 수집된 갯잔디(Z. sinica, Jeju, Korea ) 종자는 ITS DNA 바코드 분석에 의한 분자 생물학적 분류를 위해 서 대조구로 사용하였으며, 2010년부터 2014년까지 수집된 자생 Zoysia 속 종자와 영양체는 대조구와 비교 분석을 위해 사용 하였다(Table 1). 종자는 소독 및 파종 후 MS(Murashige and Skoog, 1962) 기본배지에 배양하였으며, 각 잔디잎은 ITS의 DNA 바코드 분석을 위한 DNA 추출 재료로 사용되었다. 수집된 자생 Zoysia 속 잔디 영양체는 제주대학교 아열대원예산업연구소 포장 및 온실에 이식되었다. 수집된 잔디는 외부형태적 분류의 주요 방법인 잎표면의 털유무(Yang et al., 1995)에 의해 들잔디 (유)와 갯잔디(무)로 1차 분류하였으며, 수집된 잔디 잎표면의 털유무 확인은 실체현미경(NikonSMZ18, Japan)를 이용하여 3 반복으로 관찰하였으며, 각 잔디잎은 DNA 추출 재료로 사용되었다.
잔디 DNA 추출 및 ITS 구간 증폭
DNA 추출은 GeneAll 회사의 ExgeneTM Plant SV Mini Kit(GeneAll, Korea)를 이용하여 추출하였으며, 추출한 DNA는 0.8% 겔을 이용하여 전기영동 상에서 확인한 후 정량하여P CR에 사용하였다. ITS 증폭을 위한 primer는 Gehrig et al. (2001) 이 보고한 ITS1-forward primer(5’ ̵ TCCGTAGGTGAACCTGCGG ̵ 3’)와 ITS4 ̵ reverse primer(5’ ̵ TCCTCCGCTTATT ATATGC ̵ 3’)가 사용되었다(Fig. 1). PCR은 AccuPower® PCR PreMix(Bioneer, Korea)의 Protocol을 따랐으며, DNA 증폭 은 PCR Thermal Cycler Dice(TaKaRa, Japan)를 사용하여 수행되었다. PCR 조건은 95°C에서 5분간 전처리 후, 95°C에서 30초, 57°C에서 30초, 72°C에서 40초를 30회 cycle로 반복한 후 72°C에서 10분간 후처리 하였다. 증폭된 PCR 산물은 마크 로젠㈜에서 염기서열을 분석하였다.
잔디 ITS 염기서열 확보 및 염기서열 유사도와 유연관계 분석
구입 및 수집한 Zoysia 잔디류는 기존에 보고된 들잔디와 갯잔디, 크리핑 벤트그라스, 켄터키 블루그라스의 ITS 염기서열 구 간과의 유사성을 비교 및 분석하기 위해서 NCBI Database (http://www.ncbi.nlm.nih.gov)와 BLAST 프로그램을 이용하였다. 또한 NCBI를 이용하여 ITS1와 ITS2 구간을 분석하고, DNA Baser Sequence Assembler Ver. 4 (Heracle BioSoft, Romania) 프로그램과 BioEdit Sequence Alignment Editor 프로그램의 ClustalW Multiple Alignment (Thompson, 1994)을 이용하여 염 기서열 차이를 확인하였다. 확보된 ITS 구간은 MEGA 6.06 (Tamura et al., 2013)을 사용하여 정렬 후 잔디의 유사도 분석을 수행하였으며, 분석방법으로는 Unweighted Pair Group Method with Arithmetic Mean(UPGMA)와 kimura 2 ̵ parameter (K2P) model을 이용하였으며, 각 분계도의 지지 정도를 나타내기 위해bo otstrap(Felsenstain, 1985)으로 1000회 반복 분석하였다.
Fig. 1.
Schematic diagram of internal transcribed spacer (ITS) regions: Black arrows indicate positions and directions of two universal ITS sequence region primers.
ITS 염기서열의 CAPS marker 전환 및 분석
본 연구에서 확보한 ITS 염기서열을 바탕으로 CAPS marker 전환을 위해 NEB (NEW ENGLAND BioLabs) 회사의 Enzyme Finder 프로그램을 사용하여 ITS 염기서열에 존재하는 모든 제한효소의 위치를 탐색하였다. CAPS marker 검증을 위 한 PCR은 ITS 염기서열 분석에서와 동일한 DNA와 PCR primer인 ITS1 ̵ forward primer(5’ ̵ TCCGTAGGTGAACCTGC GG ̵ 3’)와 ITS4 ̵ reverse primer(5’ ̵ TCCTCCGCTTATTGATATGC ̵ 3’) 및 protocol을 사용하였으며, 증폭된 PCR 산물은 ExpinTM PCR SV Kit(GeneAll, Korea)를 이용하여 정제하였다. 정제된 PCR 산물과 5 unit의 BglI, StyI, FauI 제한효소(NEB, England), 10X 3.1 buffer (BglI과 StyI) 또는 10X CutSmart buffer (FauI)가 포함된 14μL 반응액은 최적 반응 온도에서 충분한 시간 동안 반응시켰다. 최종 반응물은 2% agarose gel에서 전기영동 하여 CAPS marker를 분석하였다..
결과 및 고찰
잔디의 ITS 증폭 및 염기서열 분석
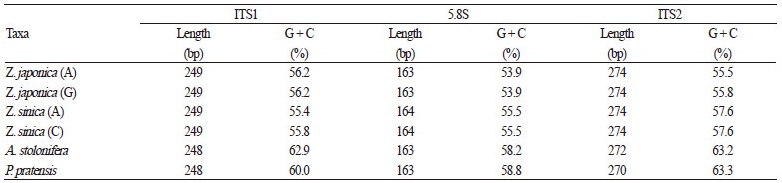
ITS 염기서열 구간을 이용한 분자생물학적 잔디의 분류는 기존 NCBI에 보고된 들잔디 및 갯잔디, 크리핑 벤트그라스, 켄터 키 블루그라스의 ITS 염기서열 구간을 기준라인으로 설정하고 대조구로 사용할 판매종자인 들잔디, 크리핑 벤트그라스, 켄터 키 블루그라스 및 수집된 갯잔디 종자의 ITS와 비교 분석하였다(Table 1). 각 잔디 잎에서 ITS PCR 증폭 및 염기서열 분석 후 기존 NCBI에 등록된 서열들과 비교 분석을 수행한 결과, 들잔디 판매종자의 경우 10개체 모두 Peterson et al.(2010)이 얻어낸 들잔디 ITS 서열(Accession No. GU359196)과 99%의 상동성 보였으며, 들잔디 10개체내에서 1bp(A 및 G) 차이 2 그룹으로 Z. japonica(A) 그룹 5개체와 Z. japonica(G) 그룹 5개체로 분류됨을 Table 2 및 Fig. 2에서 확인하였다. 또한, Fig. 1에서 ITS 염 기서열 구간은 18S와 26S ribosomal DNA 사이 특이적 변이를 보이는 ITS1과 ITS2 구간이 존재하므로, ITS 내부에 존재하는 ITS1과 5.8S rDNA, ITS2 염기서열 구간을 분석하였다. 들잔디 ITS 염기서열은 총 686bp이며, ITS1의 크기가 249bp, 5.8S rDNA는 163bp, ITS2는 274bp임을 알 수 있었다(Table 2). DNA의 구조 및 물리적 특성을 결정하는 G + C 함량은 들잔디 ITS 전체 염기서열 구간에서 55%로 확인되었다(Table 2). 갯잔디의 경우, 판매종자가 없어서 외부형태학적 주요 분류기준인 잎 표 면의 털 유무(Yang et al., 1995)로 수집 당시 갯잔디로 분류된 갯잔디의 종자 10개체도 ITS 염기서열을 분석하였다. 수집 갯잔 디 종자 10개체는 1bp(A 및 C) 차이로 2 그룹으로 Z. sinica (A) 그룹 6개체와 Z. sinica (C) 그룹 4개체로 분류되었다. 4개체는 기존에 보고된 갯잔디로 등록된 서열(Accession No. KP057082)과 100%의 상동성을 보였으며, 6개체는 99%의 상동성을 Table 2 및 Fig. 2에서 확인하였다. 갯잔디(Z. sinica) ITS 염기서열은 총 687bp이며, 249bp의 ITS1과 164bp의 5.8S rDNA, 274bp의 ITS2를 확보하였으며 ITS 전 구간의 G + C 함량은 56%를 보였다. 한지형 잔디인 크리핑 벤트그라스 및 켄터키 블루 그라스의 판매 종자의 경우는 모두 기존에 NCBI에 보고된 서열들과 비교하여 크리핑벤트그라스 Accession No. KM999958 및 켄터키 블루그라스 No. KF800192와 100% 일치함을 Table 2 및 Fig. 2에서 확인하였다. 크리핑 벤트그라스와 켄터키 블루 그라스는 총 683bp와 681bp의 ITS 구간 염기서열을 각각 확보하였으며, 기존에 등록된 서열(Accession No. KM999958과 No. KF800192)들과 비교하였을 때 크리핑 벤트그라스는 ITS1 248bp와 5.8S rDNA 163bp, ITS2 272bp, 켄터키 블루그라스 는 248bp의 ITS1과 163bp의 5.8S rDNA, 270bp의 ITS2를 포함함을 알 수 있었다. 전체 ITS 구간의 G + C 함량은 각각 62% 와 61%로 대체적으로 난지형 잔디가 한지형 잔디보다 낮은G +C 함량을 가짐을 알 수 있었다(Table 2).
Fig. 2.
Comparison of internal transcribed spacer (ITS) sequences in control lines of Zoysia japonica (Z. japonica-A and Z. japonica-G groups), Z. sinica (Z. sinica-A and Z. sinica-G groups), Agrostis stolonifera, and Poa pratensis: Sizes of ITS sequences in each species are 686 bp, and 687 bp, 683 bp, and 681 bp, repsectively.
본 연구에서 대조구로 사용된 판매 및 수집종자인 들잔디, 갯잔디, 크리핑 벤트그라스, 켄터키 블루그라스의 각 잔디들 간 ITS 염기서열 유사성 비교 분석을 multiple sequence alignment를 수행하였다. 들잔디 및 갯잔디, 크리핑 벤트그라스, 켄터키 블루 그라스의 ITS 염기서열 전체 구간은 각 686bp와 687bp, 683bp, 681bp 크기이며, 잔디 4종은 각 1 ̵ 5bp차이로 총 206bp의 염기 서열 차이를 보였다. 그 중 31bp는 INDEL에 의한 차이임을 확인하였다(Fig. 2). 차이가 나는 전체 206bp의 염기서열 차이 중 에서 160bp는 두 개의 Zoysia 종을 다른 속들로부터 구분되도록 하며, 다른 13bp의 염기서열 차이들은 세 가지 속들이 모두 다 른 염기를 가짐으로써 각각의 속들(Zoysia 속, Agrostis 속, Poa속)의 구분을 가능하게 하였다. 종을 구별하게 하는 종 특이적 염 기는 크리핑 벤트그라스에서 32개, 켄터키 블루그라스에서 26개, 갯잔디에서 10개, 들잔디에서 5개가 존재함을 확인하였다.
이는 크리핑 벤트그라스와 켄터키 블루그라스가 다른 속(Agrostis 속, Poa 속)에 속하는 종인 반면, 들잔디와 갯잔디는 같은 속 (Zoysia 속)에 속하는 종이므로 유전적 유연관계와 관계되는 ITS 염기서열 구간의 차이가 상대적으로 적게 나타나는 것으로 추정된다. 이러한 결과는 ITS 염기서열의 종간 차이가 종내 보다 크다고 보고한 결과와 유사하다(Han et al., 2006; Yao et al., 2010). 또한 들잔디와 갯잔디 두 종간의 전체 ITS 구간 염기서열들을 비교 분석한 결과, 치환된 염기의 수는 18개이며, 오직 1bp 의 염기만이 INDEL에 의한 차이임을 확인하였다(Fig. 2). 치환된 18bp의 염기들 중 16bp와 INDEL에 의한 1bp의 차이는 서 로 다른 종의 들잔디와 갯잔디를 명확하게 구분하는 기준이 되었으며, 이를 제외한 나머지 2bp의 염기 차이 중 한 염기는 같은 갯잔디 종의 라인(line)들을 서로 다른 두 그룹으로, 또 다른 1bp의 염기 치환은 동일한 들잔디 종내 라인들을 두 개의 그룹으로 나누는 것을 확인하였다. 따라서, ITS 전 구간 내의 염기치환 및 INDEL에 의한 염기 차이를 이용하여 들잔디와 갯잔디, 크리 핑 벤트그라스, 켄터키 블루그라스의 속간 및 종간의 구별뿐만 아니라 들잔디와 갯잔디의 종내 구별 또한 가능함을 확인하 였다.
따라서, ITS 염기서열 차이를 바탕으로 들잔디 및 갯잔디, 크리핑 벤트그라스, 켄터키 블루그라스의 분류가 가능함을 확인하 였으며, 들잔디, 크리핑 벤트그라스, 켄터키 블루그라스의 판매종자와 갯잔디 수집종자를 대조구로 설정하여 우리나라에서 수 집된 자생 Zoysia 속 잔디를 분류하고, 비교 분석하는데 대조구로 적절함을 확인하였다. 이상의 결과는 ITS 염기서열 구간이 생물 종에 따른 보존 및 변이가 뚜렷하여 다양한 생물종을 분류하는데 활용되고 있다는 기존의 보고와 일치하는 결과이다 (Hebert et al., 2003; Kress et al., 2005; CBOL Plant Working Group, 2009; Ahn et al., 2010; Koch et al., 2010; Hong et al., 2012).
잔디 ITS 염기서열 기반 CAPS marker 전환 및 적용
들잔디와 갯잔디의 ITS 염기서열 차이를 바탕으로 CAPS marker를 개발하기 위해, 대조구 잔디 4종의 ITS 염기서열 내부 에 제한효소 인식부위를 탐색한 결과, 각 잔디간에 구별 가능한 BglI, StyI, FauI 등의 주요 제한효소 인식부위를 확인할 수 있 었다(Fig. 3). 이러한 선별된 3 가지 제한효소가 들잔디와 갯잔디를 식별 가능한 CAPS marker로 적합한 지를 검토하기 위해, 대조구인 들잔디와 갯잔디, 크리핑 벤트그라스, 켄터키 블루그라스로부터 ITS1과 ITS4 primer를 사용하여 ITS 염기서열 구간 PCR 증폭을 수행한 후 BglI, StyI, FauI 제한효소를 각각 처리하였다. 그 결과, 갯잔디(Z)는 인식 부위가 효소에 의해 절단되어 375bp와 312bp 두 개의 조각으로 나뉘는 반면 한지형 잔디(As, Pp) 및 들잔디(Zj)는 ITS 염기서열 내에 BglI 제한효소 인식 부 위가 없어서 기존에 증폭된 약 700bp 한 개의 밴드만이 관찰되었다(Fig. 4A). StyI 제한효소의 경우 제한효소가 켄터키 블루그 라스(Pp) ITS 구간의 인식 부위에 작용하여 555bp와 126bp의 두 개의 조각으로 분리되었다(Fig. 4B). 갯잔디(Z)에서는 StyI이 BglI 제한효소의 작용 부위와 인접한 위치의 인식부위에 작용하여 385bp와 302bp의 두 개의 조각으로 나뉘어 앞선 BglI의 결 과와 유사하였다. FauI 제한효소의 경우 크리핑 벤트그라스(As)와 켄터키 블루그라스(Pp) ITS 구간 내 인식 부위에 제한효소 가 작용하여 각각 333bp, 200bp, 108bp와 306bp, 200bp, 133bp의 세 개의 밴드를, 갯잔디(Z)는 480bp와 91bp 두 개의 밴드 양 상을 확인하였다(Fig. 4C). 들잔디(Zj)의 경우 ITS 염기서열 내에 FauI 제한효소 인식 부위가 653bp 부근에 있어서 653bp와 33bp 중 2% agarose gel 상에서 653bp 크기의 밴드 한 개만이 확인되었다(Fig. 4C). 세 가지 종류의 효소(BglI과 StyI, FauI)를 이용함으로써 들잔디 ITS 염기서열에서는 제한효소에 의해 절단되지 않고 갯잔디에서만 절단되어 들잔디와 갯잔디간의 구별 이 쉽게 가능하게 하였으며, 특히 FauI 효소는 들잔디와 갯잔디 뿐만 아니라 크리핑 벤트그라스와 켄터키 블루그라스 같은 한 지형 잔디도 함께 구분하였다(Fig. 4C). 따라서 들잔디와 갯잔디를 식별하는 CAPS marker에 BglI과 StyI, FauI이 적합함을 확 인할 수 있었다.
Fig. 3.
Recognition sites of three restriction enzymes (Bgl I, Sty I, Fau I) in each turfgrass species: Numbers underneath the lines indicate the sizes of each internal transcribed spacer (ITS) sequence in Agrostis stolonifera (A), Poa pratensis (B), Zoysia japonica (C), and Z. sinica (D).
또한, 바닷가 근처에서 수집한 잔디 종자의 분자생물학적 분류를 하기 위해서, 본 연구에서 개발한 ITS 염기서열 기반 CAPS marker를 이용하여 구분하였다. 수집 종자를 파종 후 ITS CAPS marker 분석을 수행한 결과, 12번 잔디(Z12)는 BglI 제한효소 에 의해 절단되어 375bp와 312bp 두 개의 조각으로, StyI 제한효소에 의해 385bp와 302bp, FauI 제한효소에 의해 480bp와 91bp으로 나누어 지는 것을 확인할 수 있어, 12번 잔디(Z12)는 갯잔디임을 확인하였다(Fig. 5). 18번 잔디(Z18)는 BglI와 StyI, FauI 제한효소에 의해 약 700bp 밴드 한 개만 확인할 수 있어, 18번 잔디(Z18)는 들잔디임을 확인하였다(Fig. 5). 예상했던 것 과는 달리 17번 잔디(Z17)의 경우는 각 BglI 제한효소에 의해 갯잔디 패턴을 나타내는 밴드 두 개와 들잔디 패턴을 나타내는 밴드 한 개를 확인하였으며, StyI 경우도 BglI 제한효소와 같은 패턴으로 나타나 갯잔디와 들잔디 패턴이 동시에 존재하였으 며, FauI 경우도 갯잔디 패턴을 나타내는 밴드 한 개와 들잔디 패턴을 나타내는 밴드 한 개를 확인할 수 있어, 17번 잔디(Z17)는 들잔디와 갯잔디의 자연교배된 개체임을 확인하였다(Fig. 5). 이는 Zoysia 속이 자가수정 및 타가수정에 의하여 모두 수정이 가 능하므로 종내 및 종간 교잡이 가능하다는 기존의 보고를 근거로 들잔디와 갯잔디가 자연 교배된 것으로 보여진다(Yu et al., 1974; Choi et al., 2008; Chung et al., 2013). 이러한 결과는 본 연구에서 개발한 ITS 염기서열 기반 CAPS marker 분석을 통하 여 들잔디와 갯잔디 뿐만 아니라 이들의 자연교배종(hybrid between Z. japonica and Z. sinica)도 신속하게 식별 가능함을 보 여 준다.
Fig. 4.
Molecular classification of control lines of Zoysia japonica (Zj), Z. sinica (Z), Agrostis stolonifera (As), and Poa pratensis (Pp) turfgrasses using cleaved amplified polymorphic sequence (CAPS) markers: ITS products purified by the polymerase chain reaction (PCR) were digested by Bgl I (A), Sty I (B), and FauI (C), respectively; Black arrows indicate original PCR product sizes (about 700 bp), and red arrows indicate digested sizes; M indicates size marker. Sample numbers are shown in Table 1.
미동정 수집 자생 Zoysia 속 잔디의 외부형태적 및 ITS 기반 CAPS marker 분석을 통한 잔디 분류
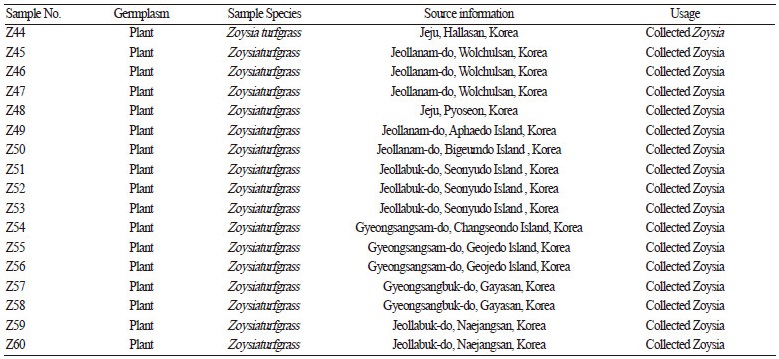
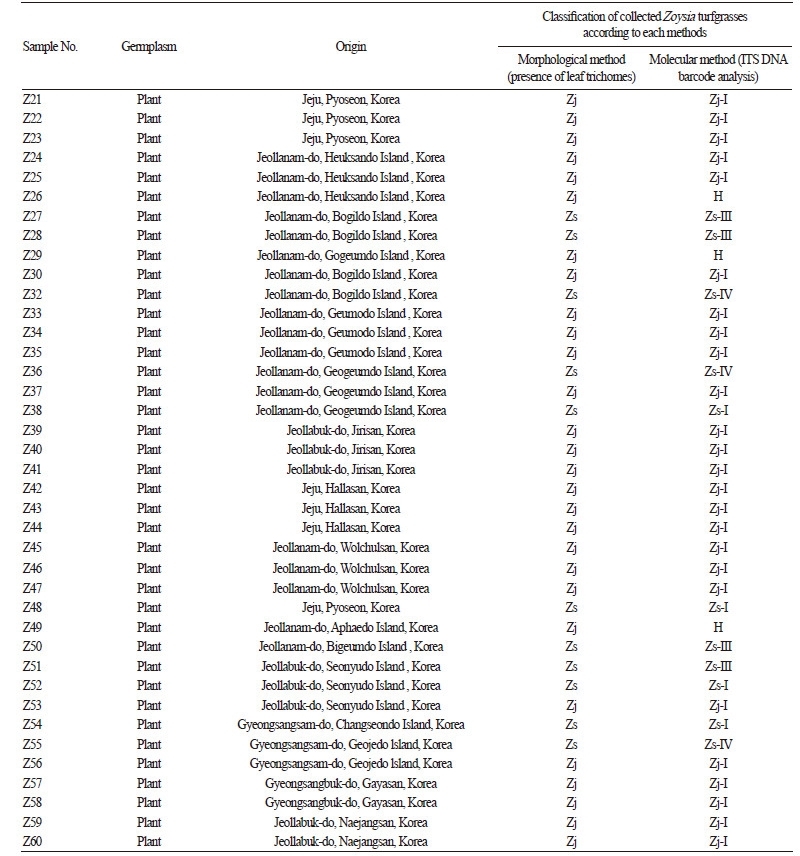
자생 Zoysia 속 들잔디와 갯잔디의 외부형태적 분류는 주로 잎 표면의 털 유무 등이 주요 분류학적 형질로 활용되고 있다 (Yang et al., 1995). 들잔디의 경우 잎 앞면 및 뒷면에 털이 존재하며, 갯잔디는 앞 뒤면 모두 털이 존재하지 않기 때문에(Yang et al., 1995), 수집된 자생 Zoysia 속 잔디는 실체현미경(Nikon SMZ18, Japan)를 이용하여 잎 표면의 털 유무를 관찰한 후 들 잔디 및 갯잔디로 1차 분류하였다. Fig. 6에서 수집 잔디 영양체 Z27, Z28, Z32, Z36, Z38, Z48, Z50, Z51, Z52, Z54, Z55번은 잎 표면에 털이 존재하지 않아서 갯잔디로 분류되었고, 그 외 잔디는 잎 한쪽 표면에만 털이 존재하거나, 양쪽면 모두 털이 존 재하여 모두 들잔디로 1차 분류되었다(Table 3).
외부형태적으로 들잔디 및 갯잔디로 1차 분류된 수집된 Zoysia 속 잔디 영양체는 들잔디 및 갯잔디의 대조구 종자로부터 개 발된 ITS CAPS marker를 이용하여 수집 잔디에 적용하여 들잔디 및 갯잔디 뿐만 아니라 들잔디와 갯잔디 교배종으로 2차 분 류를 수행하였다. 대조구 잔디에서 BglI과 StyI은 제한효소 인식 부위가 ITS 염기서열 내부에서 인접해 있기 때문에 BglI만 잔 디에 이용하였다(Fig. 3). 수집된 잔디 영양체는 BglI 및 FauI에서 각각 들잔디, 갯잔디, 들잔디와 갯잔디 교배종 패턴으로 밴드 가 확인되었으며, ITS CAPS marker가 대조구인 들잔디와 갯잔디의 종자 뿐 만 아니라 수집된 자생 Zoysia 속 잔디 영양체에 서도 적용이 됨을 확인하였다(Fig. 7). 또한 Z26, Z29, Z49번의 수집된 잔디 영양체를 제외한 모든 잔디에서 외부형태학적 1차 분류와 ITS CAPS marker 분석에 의한 2차 분류 결과가 일치 함을 확인 할 수 있었다(Table 3). Z26, Z29, Z49번의 경우, Fig. 6 에서 외부형태학적으로 잎 표면에 털이 관찰되어 들잔디로 분류된 Z26, Z29, Z49은 Fig. 7에서 ITS CAPS marker 2차 분석을 통해 들잔디와 갯잔디의 자연교배종(H)으로 최종 분류되었다(Table 3). 따라서, 털 유무의 기준으로 들잔디와 갯잔디는 구분할 수 있으나, 교배종을 구별하는 것은 불가능 하다고 판단되며, 이를 바탕으로 들잔디, 갯잔디, 교배종을 정확히 식별하기 위해서 는 외부형태학적 구별법 뿐만 아니라 분자생물학적 종 구별법도 반드시 필요하다는 것을 확인할 수 있었 다.
Fig. 5.
Molecular classification of control lines of Zoysia japonica (Zj), Z. sinica (Z), Agrostis stolonifera (As), and Poa pratensis (Pp) turfgrasses using cleaved amplified polymorphic sequence (CAPS) markers: ITS products purified by the polymerase chain reaction (PCR) were digested by Bgl I (A), Sty I (B), and FauI (C), respectively; Black arrows indicate original PCR product sizes (about 700 bp), and red arrows indicate digested sizes; M indicates size marker. Sample numbers are shown in Table 1.
Fig. 6.
Morphological classification of collected Zoysia turfgrasses by presence of leaf trichomes indicated Z. japonica (Zj) and Z. sinica (Zs): Left and right sides of each panel show adaxial and abaxial leaf surfaces, respectively; Trichomes were present on the surfaces of Z. japonica leaves, a few trichomes were present the leaves of Z. japonica/Z. sinica hybrid (Z26, Z29, Z49), and no trichomes were present on Z. sinica leaves; Sample numbers are shown in Table 1. Scale bars = 1 mm.
동정된 들잔디와 갯잔디의 ITS 염기서열 유사성 분석 및 유연관계 분석
Fig. 7.
Molecular classification of collected Zoysia turfgrasses using internal transcribed space (ITS)-based cleaved amplified polymorphic sequence (CAPS) markers: ITS products purified by the polymerase chain reaction (PCR) were digested by BglI and FauI, respectively; Analysis of ITS CAPS markers allowed classification of Zoysia turfgrasses into Z. japonica (J), Z. sinica (S), and Z. japonica/Z. sinica hybrid (H); M indicates size marker; Sample numbers are shownin Table 1.
ITS 염기서열 및 ITS 기반 CAPS 마커에 의해 들잔디와 갯잔디로 분류된 대조구로 사용된 들잔디 및 갯잔디 종자와 제주도 및 전라도, 경상도의 산 및 해안, 섬에서 수집된 들잔디 및 갯잔디 영양체 간에 ITS 염기서열 유사성 분석 및 유전적 유연관계를 분석하기 위해 각 잔디 ITS 염기서열 구간의 multiple sequence alignment(Fig. 8) 및 MEGA 6.0 프로그램에 의한 계통학적 분 석(Fig. 9)을 수행하였다. 총 62개의 잔디 중에서 들잔디와 갯잔디 교배종의 잔디 종자 1개체와 영양체 3개체는 들잔디 및 갯잔디의 ITS 염기서열 피크가 2개로 중첩되어 염기서열 확보되지 않기 때문에 유사성 및 유연관계 분석에서 제외되었다. 총 58개 체의 들잔디 및 갯잔디는 Fig. 8의 ITS 염기서열 차이에 의해 Fig. 9 및 Table 4에서 들잔디 2 그룹(Zj ̵ I, Zj ̵ II), 갯잔디 4 그룹(Zs ̵ I ̵ Zs ̵ IV)으로 총 6개의 그룹으로 유집되었다. 들잔디의 경우에는 Zj3, Zj6, Zj8, Zj9, Zj10의 대조구 들잔디 5개체 종자라인 들을 포함하는 Z. japonica(A) 그룹과 제주도 및 전라남도, 전라북도, 경상남도, 경상북도에서 수집된 들잔디 영양체 25개체가 Zj ̵ I로 분류 되었으며, Fig. 8에서 1bp의 염기치환으로 구분되는 Zj1, Zj2, Zj4, Zj5, Zj7의 5개체 종자라인들을 포함하는 Z. japonica(G) 그룹과 제주 하귀에서 수집된 들잔디 종자 1개체 Z18이 Zj ̵ II 그룹으로 유집 되었으며(Table 4), 각 2 그룹별로 그 룹내의 모든 개체들은 염기서열이 100% 일치하여 Fig. 8에서 Zj ̵ I 및 Zj ̵ II으로 나타내었다. 갯잔디의 경우에는 Z1, Z5, Z6, Z8 의 대조구 갯잔디 종자 4개체 Z. sinica(C) 그룹이 Zs ̵ II 그룹으로 유집되었으며(Table 4), Zs ̵ II 그룹의 ITS 염기서열 1bp의 염 기치환으로 분리된 Zs ̵ I 그룹은 Z2, Z3, Z4, Z7, Z9, Z10의 대조구 갯잔디 종자 6개체 Z. sinica(A) 그룹과 제주 하귀에서 수집 된 갯잔디 종자 Z12 및 수집된 갯잔디 영양체인 제주 표선Z 48, 전라남도 거금도 Z38, 전라북도 선유도 Z52, 경상남도 창선도 Z54의 영양체 5개체로 총 11개체가 한 그룹으로 유집되었다(Table 4). 갯잔디의 Zs ̵ III 그룹은 Zs ̵ I 그룹과 1bp 및 Zs ̵ II 그룹 과 2bp의 염기치환으로 확인되어(Fig. 8), Table 4 및 Fig. 9에서 수집 갯잔디 영양체인 전라남도 보길도에서 Z27과 Z28, 비금 도 Z50, 전라북도 선유도 Z51의 영양체 4개체가 한 그룹으로 유집되었다. Zs ̵ IV는 Fig. 8에서 Zs ̵ I과 insert / deletion(INDEL) 에 의한 염기서열 차이는 각 1bp의 삽입과 2bp의 염기치환이 확인되었으며, Zs ̵ II와 INDEL 의한 1bp 삽입과 3bp의 염기치환, Zs ̵ III와 INDEL 의한 염기서열 1bp 삽입과 염기치환 3bp로 Fig. 8에서 확인되었으며, Zs ̵ IV 그룹은 Table 4 및 Fig. 9에서 수 집 갯잔디 영양체인 전라남도 보길도 Z32, 전라남도 거금도 Z36, 경상남도 거제도 Z55의 총 3개체가 한 그룹으로 유집되었다.
Fig. 8.
Internal transcribed spacer (ITS) alignment of control and collected Zoysia japonica (Zj-I and Zj-II) and Z. sinica (Zs-I–IV): According to differences in their ITS sequences, control and collected samples of Z. japonica and Z. sinica were classified into two Z. japonica groups (Zj-I and Zj-II), and four Z. sinica groups (Zs-I–Zs-IV); The number of Zj-I, Zj-II and Zs-I–IV groups are shown in Table 4.
Table 4 및 Fig. 8와 9에서 갯잔디 수집종의 경우, 제주도에서 수집한 갯잔디는Z s ̵ I과 Zs ̵ II그룹에 속해 있으며, 경상남도Z s̵ I과 Zs ̵ IV그룹, 전라남도 Zs ̵ III과 Zs ̵ IV, 전라북도 Zs ̵ I과 Zs ̵ III으로 갯잔디의 수집 지역별 차이가 나타나는 것을 확인 할 수 있었다. 반면에 들잔디 그룹은 수집 지역별 차이는 미흡하였으나, 들잔디와 갯잔디 그룹간에 들잔디 Zj ̵ II 그룹과 갯잔디 Zs ̵ II 가 먼 유연관계를 나타냈으며, 특히 갯잔디 그룹의 제주 수집종의 일부인 Zs ̵ II와 전라남도 및 경상남도 수집종 Zs ̵ IV는 갯잔 디 그룹별 유연관계가 가장 차이가 많음을 알 수 있었다(Fig. 9). 이상의 결과에서 Zoysia 속 대조구 잔디 종자 및 수집 잔디 영 양체는 외부형태학적 분류법에 비해 DNA 바코드 분석의 ITS 염기서열 차이에 의해 신속하게 들잔디 2그룹과 갯잔디 4그룹 으로 종간 및 종내 구별에 성공하였으며, 유전적 유연관계 또한 확인 할 수 있었다. 이러한 결과는 ITS 염기서열 구간은 진화속 도가 비교적 빠르기 때문에 종 속간 분류 연구에 적합하다는 기존의 보고와 유사하다(Kress et al., 2005; Han et al., 2006; Kress and Erickson, 2008; Baigalmaa et al., 2009; Ahn et al., 2010; Gao et al., 2010; Yao et al. 2010; Hong et al., 2012; Moon et al., 2013).
본 연구는 잔디류의 분류 및 식별을 위해서 ITS 염기서열을 비교 분석하였고, ITS 염기서열 차이를 기반으로 CAPS marker 를 개발하였다. 본 연구에서 개발된 CAPS marker를 이용하면 우리나라에서 자생하는 들잔디 및 갯잔디, 들잔디와 갯잔디의 자연 교배종을 분자생물학적 수준에서 구별할 뿐만 아니라 교잡종 개발 및 교잡 가능성 분석, 신품종 계통 분석에 응용될 수 있 을 것으로 사료된다.