서 언
재료 및 방법
식물재료 수송 및 전처리
잎 엽록소 및 형광, 색 측정
통계처리
결과 및 고찰
서 언
우리나라의 나리 절화 수출액은 2012년 30,090천$로 절화 수출 품목 중 1위이다(MAFRA, 2013). 주 수출국은 일본으로 오리엔탈 계통의 ‘Casa Blanca’, ‘Le Reve’, ‘Sorbonne’ 및 ‘Siberia’ 등이 주요 수출 품종이다(Hwang et al., 2007). 하지만 나리 절화는 수출 시 잎 황화로 인해 상품성이 저하되어 한국산 나리 절화가 저품질로 인식될 수 있다. 따라서 수출용 나리 절화의 잎 황화를 경감하여 품질을 향상시킬 수 있는 연구가 필요하다. 절화는 화판이 위조되기 전에 잎이 황화되어 품질이 저하될 수 있다. 수확 후 적절하지 못한 저장 조건과 cytokinin의 결핍, ethylene 발생, 암조건, abscisic acid의 축적, 잎의 노화 또는 기계적 손상 등과 같은 요인들은 잎의 황화를 촉진시킨다(Ferrante et al., 2009). 절화는 종과 품종에 따라 잎 황화에 대한 감수성이 크거나 작을 수 있다(Ferrante et al., 2002). 백합과 알스트로메리아는 잎이 먼저 노화되어 잎 황화가 절화의 수명을 결정지을 수 있다(Dai and Paull, 1991; Han, 1995; Hicklenton, 1991). 식물체 잎의 노화는 세포 내 막단백질이 변화되고 엽록소가 붕괴하면서 죽음에 이르게 되는 식물 대사의 한 과정으로써 내생 호르몬의 감소와 상관 관계가 있다. 그 과정은 내생 물질의 변화뿐만 아니라 광, 온도, 공중습도와 같은 외부의 환경 요인과 상호작용에 의해 조절된다. 온도가 증가함에 따라 호흡량의 증가로 체내 물질의 소비가 증가되어 노화가 촉진된다(Sebanek, 1992). 나리의 잎 황화는 암조건 저장과 낮은 온도에 대한 스트레스로 인해 일반적으로 발생한다(Ranwala and Miller, 1998). Anil and William(2000)은 gibberellic acid (GA4+7) 처리 시 엽록소 및 단백질 가수 분해와 catalase 활성의 감소를 방지하여 나리 절화의 품질을 향상시키며, 나팔 나리와 오리엔탈 나리는 GA4+7 처리 시 기저부의 잎 황화가 감소되거나 예방되었다(Han, 1997; Ranwala and Meller, 2000; Ranwala et al., 2000, 2003). Ranwala and Meller(1998)는 오리엔탈 나리 ‘Stargazer’의 GA4+7 분무 처리 시 저온 저장에 의한 잎 황화를 효과적으로 예방한다고 하였다. 하지만 국화 절화는 GA3 처리구에 비해 benzylaminopurine (BAP)처리구가 엽록소 유지효과에서 월등하였고, 잎 황화 방지에는 BAP가 주동적인 역할을 한다(Suh and Kwack, 1994). 그리고 Ferrante et al.(2003)은 thidiazuron(TDZ) 처리 시 국화 절화 ‘Regan Bianco’와 ‘Regan Giallo’는 잎 황화가 나타나지 않았고, 튤립 절화 ‘Attila’와 ‘White Dream’의 잎 황화를 상당히 억제할 수 있다고 보고하였다. 또한 스톡 절화는 광 조건에서 5μM TDZ의 침지 처리 시 잎 황화를 지연시켰지만 어두운 곳에서 저장 시에는 그 효과는 줄어들고, TDZ와 GA3의 혼합처리는 어떠한 상승 효과가 없어 바람직하지 않았다(Ferrante et al., 2009). 튤립 수확 후 잎 황화 현상은 benzyladenine(BA)과 GA4+7 처리 시 감소되었으며(Kim and Miller, 2009), 팬지와 비올라는 BA와 GA4+7를 각각 처리하거나 에틸렌 작용 억제제인 1-MCP를 처리 시에는 잎 황화가 발생하였지만 5 또는 10mg・L-1 BA와 GA4+7의 혼합처리가 잎 황화를 예방하였다(Waterland et al., 2010). 나팔 나리의 경우, 잎 황화는 에틸렌 생성과 관련이 없고, BA 또는 GA4+7, 그리고 BA와 GA4+7 혼합처리가 잎 황화를 예방하였고, 나팔 나리 절화 ‘Georgia’는 GA3와 BA를 25mg・L-1 농도로 혼용 처리한 경우 대조구에 비해 잎의 엽록소 함량이 장기간 유지되어 잎 황화 억제에 매우 효과적이었다(Byun et al., 2004; Franco and Han, 1997). 아시아틱 나리 절화 ‘Elite’는 화학적 전처리를 하지 않고 짧은 시간 동안 뜨거운 물에 침지 전처리 하는 것만으로도 잎 황화 예방에 빠르고 효과적이었다(Woolf et al., 2012). 오리엔탈 나리 절화 ‘Siberia’는 수송 시 온도가 높아지면 잎의 황화가 심하게 발생하여 꽃의 수명이 길더라도 절화의 품질을 크게 낮출 수 있는 요인이 된다. 따라서 잎 황화를 예방할 수 있는 수송온도를 구명하고, 상온 수송 시 잎 황화를 경감시킬 수 있는 전처리를 구명하고자 본 연구를 수행하였다.
재료 및 방법
식물재료 수송 및 전처리
2012년 8월, 강원도 강릉시 왕산면에서 생산된 오리엔탈 나리 ‘Siberia’(구근 크기: 14-16cm 정식)를 1번화의 봉오리 길이가 약 10cm 이상, 봉오리 색이 백색으로 약 30% 정도 물드는 시기에 수확하여 무처리, 100mg・L-1 gibberellic acid3 (GA3), 1mL・L-1 Promalin(BA + GA4+7), 500mg・L-1 Chrysal SVB에 3시간 동안 침지 전처리하거나 같은 전처리 용액을 분무기를 이용해 나리 절화의 잎과 줄기에 처리별로 30mL씩 분무 처리한 후 수돗물에 침지 시켜 국립원예특작과학원으로 습식수송하였다. 무처리와 전처리한 나리 절화는 수출용 포장상자에 넣어 5, 10, 15, 25°C로 설정된 chamber에 가로로 넣은 후 일본으로 선박 수출 시 소요되는 유통기간인 5일 동안 암조건에서 건식으로 모의 수송하였다. 그 후 나리 절화를 70cm로 재절단하여 수돗물이 담긴 유리병에 꽂아 항온실(25 ± 1°C)에 두면서 절화의 품질을 처리당 5반복으로 매일 절화 수명 및 품질 등을 조사하였다.
잎 엽록소 및 형광, 색 측정
모의 수송 후 0, 3, 6, 9일째에는 처리별로 줄기 기부에서 1, 2, 3번째 잎을 엽록소 측정기(SPAD-502, Minolta Co., Ltd., Japan)를 이용하여 엽록소 함량을 측정하였고, 엽록소 형광반응은 엽록소 형광 반응 측정기(OS5p, ADC BioScientific Ltd., England)로 암적응 클립을 이용하여 암적응을 시킨 후 측정해 최소 형광값(Fo)과 최대 형광값(Fm), 그리고 최대광량자수율값(Fv/Fm)을 구하였다. Fv/Fm 값은 Fv/Fm = (Fm-Fo)/Fm으로 계산하였다(Genty et al., 1989). 잎의 색은 분광 측색계(CM-700d, Minolta Co., Ltd., Japan)를 이용하여 Hunter L(Lightness; Black = 0, White = 100), a(Red-Green: Red = +60, Green = -60), b(Yellow-Blue:Yellow = +60, Blue = -60) 및 수송 전 잎의 색을 기준으로 ΔE값을 측정하여 비교하였다. ΔE값은 기준 샘플의 L, a, b값을 Lt, at, bt로 시료 샘플의 L, a, b값을 L, a, b로 하였을 때 ΔL = Lt-L, Δa = at-a, Δb = bt-b, ΔE = [(ΔL)2 + (Δa)2 + (Δb)2]1/2로 구하였다.
통계처리
통계처리는 SPSS 18.0 software를 이용하여 각 처리 효과의 유의성 검정을 위해 분산분석과 p < 0.05 수준에서 Duncan’s multiple range test를 실시하였다.
결과 및 고찰
오리엔탈 나리 절화 ‘Siberia’는 25°C로 수송 후 3일째에 아래의 잎이 심하게 황화되면서 말리는 현상을 보였다. 하지만 수송온도 5°C에서 15°C는 잎의 황화현상이 거의 나타나지 않았다(Fig. 1). Lee et al.(2009)은 ‘Siberia’ 나리 절화를 5°C에서 3일 동안 건식 저장하였을 경우 품질에 이상이 없이 상품성을 유지한 반면, 6일 이상 저장할 경우 이상 개화가 발생하였으며, 12일 저장 이후에는 이상 개화 및 잎 황화 등으로 품질이 급격히 저하되어 ‘Siberia’ 나리 절화를 5°C에 건식 저장 시 3일 정도로 하며 6일 이상을 넘기지 않도록 유의해야 한다고 보고하였다. 수송 후 3일째에 잎의 엽록소 함량은 5°C로 수송 시 SPAD 값이 46.7로 가장 높게 유지되었고, 25°C로 수송 시에는 12.9로 가장 낮았다. 특히 수송온도 5°C에서 15°C는 25°C와 비교해 SPAD 값이 약 3배 이상 높았다(Table 1). Hunter value에서 L값은 명도, +a 값은 적색, -a값은 녹색, +b값은 황색, -b값은 청색을 나타낸다. ‘Siberia’는 5°C 수송 시 황색을 나타내는 b값이 18.1로 가장 낮았으며, 25°C와 비교했을 때 약 1/2 수준이었다. 5°C에서 15°C로 수송 시 녹색을 나타내는 -a의 값이 약 -9.2였으며, 25°C로 수송 시에는 +8.6으로 적색값을 나타냈다.

|
Fig. 1. Effect of shipping temperature on leaf chlorosis of cut Lilium Oriental hybrid ‘Siberia’ flowers. Photographed on 3 days after dry shipping. Cut flowers were treated, shipped for 5 days then assessed at 25 ± 1°C. |
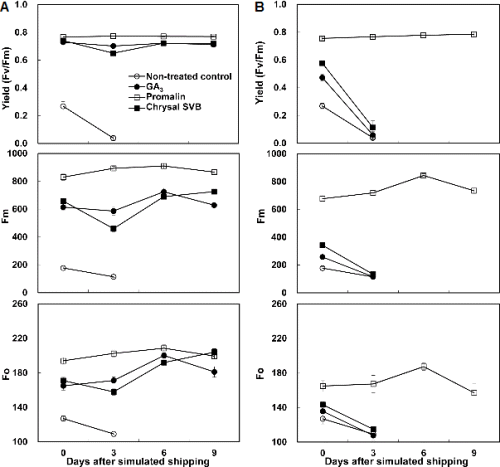
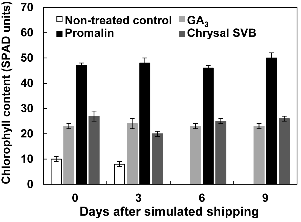
건식으로 5일 동안 25°C로 수송하였을 때, 오리엔탈 나리 절화 ‘Siberia’는 무처리 시 수송 후 3일째에 아래의 잎이 심하게 황화되면서 탈리되었지만 Promalin 침지 전처리 시 절화 수명이 끝날 때까지 잎의 황화현상은 나타나지 않았다(Fig. 2). GA3와 Chrysal SVB 침지 전처리도 잎 황화 경감에 대한 효과를 나타냈지만 Promalin 처리와 비교해 상대적으로 그 효과는 약하게 나타났다. 분무처리에서는 Promalin 처리에서만 잎 황화현상이 거의 일어나지 않았고, 다른 처리들에서는 잎의 황화현상이 심하게 나타났다. 나팔 나리 ‘Nellie White’는 수확 후 1000mg・L-1 GA3는 효과적이지 않았지만 100mg・L-1 Promalin 분무처리 시 잎 황화를 완벽히 예방하였고(Ranwala et al., 2000), 또한 Promalin은 줄기로부터의 물질대사 이동을 촉진시켜 개화를 유도한다(Son et al., 1993). Suh and Kim(2004)은 ‘Casablanca’는 Promalin 전처리 하였을 경우, 다른 식물생장 조절물질의 전처리보다 수분흡수가 활발히 나타났으며, 이는 Promalin 처리가 수분 흡수를 촉진시켜 체내 수분함량을 높이기 때문이라고 하였다. 또한 상부의 소화까지 적절한 수분이 공급됨으로써 수분 스트레스를 감소시켜 Promalin 전처리 시 소화의 노화가 천천히 나타나 절화 수명을 연장시킨다고 보고하였다. 나아가 Suh and Kim(2006)은 나리 절화 ‘Siberia’를 20분 동안 promalin 침지 전처리 시, 그리고 나리 절화 ‘Dream Land’는 Promalin 분무 처리 시 1번화의 수명을 연장시킨다고 하였다. 본 실험에서도 ‘Siberia’는 Promalin 침지 전처리 시 무처리보다 1번화의 수명은 2.4일, 전체 절화 수명은 3.2일 길어졌다. 또한 각 소화의 수명도 Promalin 침지 전처리 시 가장 길었다(Table 2). 따라서 ‘Siberia’는 Promalin 분무 전처리보다는 침지 전처리 하였을 때 절화 수명 연장 효과가 더 큰 것을 알 수 있었다. 수송 후 3일째에 잎의 색 변화를 살펴 보았을 때, 다른 처리들과 비교해 Promalin 침지 전처리 시 a 값이 -8.4로 가장 낮아 녹색을 나타냈고, 황색을 나타내는 b값이 16으로 다른 침지 처리들의 약 1/2 수준이었다. Promalin 분무 처리 시에는 b값이 25.6으로 침지 처리보다 높았다. 또한 Promalin 침지 전처리 시 ΔE값이 0.8이었다. 따라서 ‘Siberia’는 Promalin 전처리 시 분무처리보다 침지처리에서 절화 수명이 연장되고, 잎 황화 현상이 크게 경감되었다. 전체적인 절화의 수명은 전처리 방법과 용액의 상호효과가 유의적인 것으로 나타났다. 또한 1번화의 수명은 전처리 방법 또는 용액에 따라 유의적인 차이를 보였다. 하지만 상호효과에서는 유의적이지 않았다. Hunter a와 b 값은 전처리 방법과 용액의 상호효과가 매우 유의적인 것으로 나타났다. Lee et al. (1996)은 강광 하에서 잎의 엽맥을 따라 생기는 황화현상은 carotenoid계 색소가 엽색소인 chlorophyll의 광산화에 대한 보호기능으로 잎의 표면에 출현하는 현상으로 추정하였으며, 강광 하에서는 생성되는 엽록소량보다 파괴되는 엽록소량이 많아져 엽록소축적이 적어지고 심지어 엽록소세포가 파괴됨으로써 황화현상 및 일소현상이 일어난다고 하였다. 암적응된 잎의 Fv/Fm값은 식물 잎이 광합성을 수행할 수 있는 최대값 즉, 잠재력을 의미하며 대부분의 식물에서 건강한 잎의 경우 보통 0.83 정도의 값을 가진다(Johnson et al., 1993). 전처리에 따른 나리 절화 ‘Siberia’ 잎의 엽록소 형광반응을 측정한 결과(Fig. 3), 침지 전처리에서 무처리는 수송후 0일째에 가장 낮은 Fv/Fm값을 보였고, 3일 이후에는 하엽이 탈리되어 측정을 할 수 없었다. Promalin 처리는 Fv/Fm과 Fm값이 다른 처리들보다 항상 높게 유지되었다. 분무 전처리에서는 Promalin 처리를 제외한 다른 처리들은 수송 후 0일부터 3일까지 Fv/Fm값이 급격히 떨어졌지만 Promalin 처리는 9일까지 Fv/Fm과 Fm, 그리고 Fo 값이 모두 높게 유지되었다. Promalin 처리 시 Fv/Fm 값은 약 0.77정도로 침지, 분무 처리 모두 0일부터 9일까지 일정한 수준으로 높게 유지되었다. ‘Siberia’는 침지 전처리에서 Promalin 처리 시 9일 동안 잎의 엽록소 함량이 50 가까이 유지되어 가장 높았지만 GA3와 Chrysal SVB 처리는 20에서 30정도에 머물러 Promalin 처리와 큰 차이를 나타냈다(Fig. 4). 따라서 오리엔탈 나리 절화 ‘Siberia’는 Promalin 침지 전처리 시 엽록소 함량이 높게 유지되어 잎 황화 현상이 크게 경감되었다.

|
Fig. 2. Effect of pretreatment (A, dipping; B, spray) solution on leaf chlorosis of cut Lilium Oriental hybrid ‘Siberia’ flowers. Photographed on 3 days after dry shipping at 25°C. GA3, 100 mg・L-1 gibberellic acid3; Promalin, 1 mL・L-1 Promalin (benzyladenine + GA4+7); Chrysal SVB, 500 mg・L-1 Chrysal SVB. Cut flowers were treated, shipped for 5 days then assessed at 25 ± 1°C. |
|
Table 1. Effect of shipping temperature on chlorophyll content and leaf color of cut Lilium Oriental hybrid ‘Siberia’ flowers. |
Shipping temperature (°C) | Hunter valuez | | Chlorophyll content |
Ly | a | b | (SPAD value) |
5 | 36.0x aw | -9.2 a | 18.1 a | | 46.7 a |
10 | 43.2 b | -8.9 a | 26.1 b | | 41.2 ab |
15 | 39.8 ab | -10.3 a | 23.8 ab | | 35.8 b |
25 | 54.0 c | 8.6 b | 32.6 c | | 12.9 c |
zCut flowers were treated, dry shipped for 5 days then assessed at 25 ± 1°C. yL, Lightness (100 = White, 0 = Black); a, Redness (- = Green, + = Red); b, Yellowness (- = Blue, + = Yellow). xBasal leaves of cut flowers were assessed at 3 days after shipping. wMean separation within columns by Duncan’s multiple range test at p = 0.05 (n = 9). |
Table 2. Effect of pretreatment solution on vase life and leaf color of cut Lilium Oriental hybrid ‘Siberia’ flowers. |
Method | Pretreatmentz | Vase life (days)y | | Hunter value |
1st floret | 2nd floret | 3rd floret | 4th floret | Total flower | Lx | a | b | ΔE |
Non-treated control | 6.8 cw | 6.3 c | 5.5 c | 5.3 b | 14.8 b | | 54.6 dv | 7.0 e | 34.1 d | 30.1 d |
Dippingu | GA3 | 8.5 ab | 8.3 ab | 7.3 ab | 6.0 ab | 14.8 b | | 49.7 c | -7.3 b | 32.1 cd | 20.8 c |
| Promalin | 9.2 a | 9.0 a | 8.0 a | 6.4 a | 18.0 a | | 35.4 a | -8.4 a | 16.0 a | 0.8 a |
| Chrysal SVB | 8.6 ab | 7.4 b | 6.4 bc | 5.6 ab | 15.0 b | | 53.3 cd | -5.0 c | 37.3 e | 27.4 d |
Sprayt | GA3 | 7.2 c | 7.4 b | 6.0 c | 5.6 ab | 14.6 b | | 54.7 d | 8.0 f | 31.0 c | 29.1 d |
| Promalin | 7.8 bc | 8.2 ab | 7.2 ab | 5.4 ab | 15.2 b | | 40.7 b | -7.2 b | 25.6 b | 10.4 b |
| Chrysal SVB | 7.3 c | 7.8 b | 6.3 bc | 5.0 b | 14.8 b | | 57.6 d | 4.0 d | 34.0 d | 30.6 d |
Source of variation | | | | | | | | | | |
Method (A) | ** | NS | NS | NS | NS | | ** | NS | NS | NS |
Pretreatment (B) | *** | NS | NS | NS | NS | | ** | NS | NS | * |
A × B | NS | NS | NS | NS | ** | | NS | *** | *** | NS |
zGA3, 100 mg・L-1 gibberellic acid3; Promalin, 1 mL・L-1 Promalin (benzyladenine + GA4+7); Chrysal SVB, 500 mg・L-1 Chrysal SVB. yCut flowers were treated, dry shipped for 5 days at 25°C then assessed at 25 ± 1°C. xL, Lightness (100 = White, 0 = Black); a, Redness (- = Green, + = Red); b, Yellowness (- = Blue, + = Yellow). wMean separation within columns by Duncan’s multiple range test at p = 0.05 (n = 5). vBasal leaves of cut flowers were assessed at 3 days after shipping. uCut flower were dipped for 3 hours after harvest. tStem and leaves of cut flower were sprayed (30 mL) after harvest. NS,*,**,***Indicate non-significant and significant at p≤0.05 or 0.01, 0.001, respectively. |
|
Fig. 3. Effect of pretreatment (A, dipping; B, spray) solution on chlorophyll fluorescence (Fv/Fm, Fm and Fo) of cut Lilium Oriental hybrid ‘Siberia’ flowers. Bars represent ± SE (n = 9). GA3, 100 mg・L-1 gibberellic acid; Promalin, 1 mL・L-1 Promalin (benzyladenine + GA4+7); Chrysal SVB, 500 mg・L-1 Chrysal SVB. Cut flowers were treated, dry shipped for 5 days at 25°C then assessed at 25 ± 1°C. Leaves were assessed from basal sections of the stem in evaluation room. |
|
Fig. 4. Effect of dip pretreatment solution on chlorophyll content of cut Lilium Oriental hybrid ‘Siberia’ flowers. Different letters represent a significant difference by Duncan’s multiple range test at p = 0.05 (n = 9). Bars represent ± SE (n = 9). GA3, 100 mg・L-1 gibberellic acid3; Promalin, 1 mL・L-1 Promalin (benzyladenine + GA4+7); Chrysal SVB, 500 mg・L-1 Chrysal SVB. Cut flowers were treated, dry shipped for 5 days at 25°C then assessed at 25 ± 1°C. Leaves were assessed from basal sections of the stem in evaluation room. |
Acknowledgements
본 연구는 2012년도 농촌진흥청 국립원예특작과학원 박사후연수과정지원사업에 의해 이루어진 것임.
References
Anil, P.R. and B.M. William. 2000. Preventive mechanisms of gibberellin4+7 and light on low-temperature-induced leaf senescence in Lilium cv. Stargazer. Postharvest Biol. Technol. 19:85-92.
Byun, M.S., I.J. Han, and K.W. Kim. 2004. Prolongation vase life in cut Lilium longiflorum ‘Georgia’ by ethylene inhibitors and plant growth regulators. Kor. J. Hort. Sci. Technol. 22:236-241.
Dai, J.W. and R.E. Paull. 1991. Postharvest handling of alstroemeria. HortScience 26:314.
Ferrante, A., A. Mensuali-Sodi, and G. Serra. 2009. Effect of thidiazuron and gibberellic acid on leaf yellowing of cut stock flowers. Cent. Eur. J. Biol. 4:461-468.
Ferrante, A., D.A. Hunter, P.H. Wesley, and M.S. Reid. 2002. Thidiazuron - A potent inhibitor of leaf senescence in alstroemeria. Postharvest Biol. Technol. 25:333-338.
Ferrante, A., F. Tognoni, A. Mensuali-Sodi, and G. Serra. 2003. Treatment with thidiazuron for preventing leaf yellowing in cut tulips and chrysanthemum. Acta Hortic. 624:357-363.
Franco, R.E. and S.S. Han. 1997. Respiratory changes associated with growth-regulator-delayed leaf yellowing in Easter lily. J. Amer. Soc. Hort. Sci. 122:117-121.
Genty, B., J.M. Briantais, and N.R. Baker. 1989. The relationship between the quantum yield of photosynthetic electron transport and quenching of chlorophyll fluorescence. Biochim. Biophys. Acta 990:87-92.
Han, S.S. 1995. Growth regulators delay foliar chlorosis of easter lily leaves. J. Amer. Soc. Hort. Sci. 120:254-258.
Han, S.S. 1997. Preventing postproduction leaf yellowing in Easter lily. J. Amer. Soc. Hort. Sci. 22:869-872.
Hicklenton, P.R. 1991. GA3 and benzylaminopurine delay leaf yellowing in cut Alstroemeria stem. HortScience 26:1198-1199.
Hwang, S.A., J.S. Lee, P.O. Lee, Y.A. Kim, and J.K. Suh. 2007. Effect of pretreatments on vase life and flower quality of cut Lilium Oriental hybrid ‘Casa Blanca’. Flower Res. J. 15:245-249.
Johnson, G.N., A.J. Young, J.D. Scholes, and P. Horton. 1993. The dissipation of excess excitation energy in British plant species. Plant Cell Environ. 16:673-679.
Kim, H.J. and W.B. Miller. 2009. GA4+7 plus BA enhances postproduction quality in pot tulips. Postharvest Biol. Technol. 51:272-277.
Lee, J.L., S.W. Kwon, and J.C. Kim. 1996. Effects of field and shade culture on plastid, proline, protein, and polyamine content in Aloes. J. Kor. Soc. Hort. Sci. 37:309-312.
Lee, J.S., H.K. Rhee, H.E. Lee, J.W. Lee, S.Y. Choi, J.H. Lim, S.K. Park, M.S. Shim, and Y.S. Lee. 2009. Effect of dry storage period in low temperature on the vase-life and quality of cut lily flower. Kor. J. Hort. Sci. Technol. 27:145. (Abstr.)
Ministry of Agriculture, Food and Rural Affairs (MAFRA). 2013. Statistics for floricultural industry in 2012. MAFRA, Gwacheon, Korea p. 398.
Ranwala, A.P., G. Legnani, and W.B. Miller. 2003. Minimizing stem elongation during spray applications of gibberellins4+7 and benzyladenine to prevent leaf chlorosis in Easter lilies. HortScience 38:1210-1213.
Ranwala, A.P. and W.B. Miller. 1998. Gibberellin 4+7, benzyladenine, and supplemental light improve postharvest leaf and flower quality of cold-stored ‘Stargazer’ hybrid lilies. J. Amer. Soc. Hort. Sci. 123:563-568.
Ranwala, A.P. and W.B. Miller. 2000. Preventive mechanisms of gibberellins4+7 and light on low-temperature- induced leaf senescence in Lilium cv. Stargazer. Postharvest Biol. Technol. 19:85-92.
Ranwala, A.P., W.B. Miller, T.I. Kirk, and P.A. Hammer 2000. Ancymidol drenches, reversed greenhouse temperatures, post-greenhouse cold storage, and hormone sprays affect postharvest leaf chlorosis in easter lily. J. Amer. Soc. Hort. Sci. 125:248-253.
Sebanek, J. 1992. Plant physiology. Elsevier Publishing Co., Amsterdam p. 255-257.
Son, K.C. and M.S. Han, and J.J. Choi. 1993. Effect of GA, BA, and pre-STS treatment on the longevity of cut Lilium oriental hybrid ‘Casa Blanca’. J. Kor. Flower. Res. Soc. 2:33-40.
Suh, J.N. and B.H. Kwack. 1994. Effects of GA3 and benzy-laminopurine on leaf-yellowing of cut chrysanthemum during storage. J. Kor. Soc. Hort. Sci. 35:251-257.
Suh, J.K. and J.H. Kim. 2004. Effects of pre-treatment and storage temperature on flowering and quality of cut Lilium oriental hybrid ‘Casa Blanca’. Kor. J. Intl. Agri. 16:99-105.
Suh, J.K. and J.H. Kim. 2006. Effect of plant growth substances on vase life and physiological change in cut Lilium spp. J. Korean Soc. People Plants Environ. 9:69-77.
Waterland, N.L., J.J. Finer, and M.L. Jones. 2010. Benzyladenine and gibberellic acid application prevents abscisic acid-induced leaf chlorosis in pansy and viola. HortScience 45:925-933.
Woolf, A.B., S. Combes, M. Petley, S.R. Olsson, and M. Wohlers. 2012. Hot water treatments reduce leaf yellowing and extend vase life of Asiatic hybrid lilies. Postharvest Biol. Technol. 64:9-18.






