서 언
재료 및 방법
형질전환체 확보
T-DNA 도입 위치 분석
BrDSR 발현 수준 및 표현형 분석
B. rapa 135K microarray 분석
결과 및 고찰
형질전환체 선발
게놈 내 도입된 T-DNA 분석
건조 스트레스 저항성 분석
건조 스트레스 반응 유전자 분석
유전자 상호 네트워크 분석
서 언
배추는 한국과 중국을 포함한 아시아 지역에서 널리 재배되는 농업적ㆍ경제적 중요 작물이다. 다른 재 배작물처럼 배추도 재배 시 비생물적 환경 스트레스에 영향을 많이 받으며, 그 중 특히 건조 스트레스는 배추생장 및 생존, 수확량에 결정하는 매우 중요한 요인으로 작용한다(Agarwal et al., 2006; Chen et al., 2002; Rabbani et al., 2003). 이러한 비생물적 스트레스로부터 작물피해를 감소시키기 위해 스트레스 저 항성 향상 관련 연구들이 많이 진행되고 있다. 이 연구들은 크게 두 유형으로 진행되는데 첫 번째는 dehydration-responsive element binding 1A(DREB1A)와 C-box binding factor 1(CBF1)처럼 유전자와 관련된 전사조절인자(transcription factor)들의 조절을 통해 하위 유전자들의 발현 수준을 변화시켜 저항성을 향상시키는 것으로 애기장대(Arabidopsis thaliana)에서 시작되어 지금까지 다양한 작물에서 연구되고 있다(Jaglo-Ottosen et al., 1998; Kasuga et al., 1999). 두 번째 유형은 직접적으로 내생 저항성 유전자를 과발현 시키는 것으로, 대표적으로 벼(Oryza sativa)에 서 calcium-dependent protein kinase(CDPK)의 과발현을 통해 건조 저항성이 향상되었다는 보고가 있다(Kreps et al., 2002; Saijo et al., 2000). 환경 스트레스에 대한 식물체의 반응 기작을 알기 위해서는 스트레스에 따른 내부 유전자들의 발현 변화를 총괄적으로 분석할 수 있어야 한다. 이를 위해 다양한 분석 방법들이 수행되고 있으며, 이들 중 대표적으로 식물의 발달 단계별 또는 스트레스 처리 별 microarray 분석 데이터를 바탕으로 한 “Gene expression profiling” 연구가 2000년대에 들어 시작되었 다(Maleck et al., 2000; Seki et al.,2001; Zhu et al., 2001). 또한 한국의 주도하에 미국, 중국, 영국, 호주, 캐나다 등 8개국이 참 가하여 수행된 Brassica rapa Genome Sequencing Project Consortium(BrGSPC)를 통해 배추 유전체 해독을 완료하여, 지금 의 배추는 41,000여 개의 유전자를 가지고 있으며 16,917개의 유전자군 중 1,003개의 유전자군이 배추 고유의 유전자임을 보 고하였다(Wang et al., 2011). 이러한 배추 유전체 해독 정보는 앞서 언급한 두 가지 유형의 스트레스 저항성 연구에도 적극적 으로 활용될 수 있을 것이다.
본 연구팀은 건조 처리된 B. rapa ssp. pekinensis ‘Chiifu’를 대상으로 한 KBGP-24K oligo chip 데이터를 분석하여, 기능이 보고되어 있지 않고 건조 저항성 관련 내생 유전자들보다 발현량이 크게 증가한 BrDSR(Drought Stress Resistance in B. rapa) 유전자를 내혼계 배추 ‘CT001’(시원씨드, 경기도 평택)에서 동정하였다. 그 후 선행연구로 담배(Nicotiana tabacum ‘SR1’)에 서 과발현을 유도하여 BrDSR의 과발현이 건조 저항성 획득에 영향을 주는 것을 확인하였다(Yu and Park, 2015). 따라서 본 연 구는 건조 저항성 유전자로 추정되는 BrDSR을 과발현시킨 형질전환 배추를 이용하여 건조 저항성 기능 검정을 수행하였다. 그리고 microarray 분석을 통해 배추의 건조 저항성 관련 유전자들의 발현 네트워크를 비교ㆍ분석하였다.
재료 및 방법
형질전환체 확보
본 연구에 이용된 BrDSR 유전자는 건조 스트레스가 처리된 내혼계 배추(B. rapa ssp. pekinensis inbred line ‘Chiifu’)를 대상 으로 한 KBGP-24K oligo chip 분석(BRAS0001S00002943, AT1G16850)을 통하여 건조 저항성 유전자로 예측되어 동정하 였으며, 모델 작물인 담배(N. tabacum ‘SR1’)를 이용하여 건조 저항성을 확인하였다(Yu and Park, 2015). 배추 형질전환은 모 델 식물인 담배에서 건조 저항성 향상 기능이 확인된 BrDSR이 실제 배추에서도 저항성 획득에 관여할 지를 검정하고, microarray 분석을 통해 BrDSR과 네트워크적으로 관련된 유전자들을 분석하기 위해 수행되었으며, 그 방법은 Yu et al.(2010) 에 보고된 방법과 동일하게 진행하였다. 생산된 형질전환체들은 PCR 분석을 통해 형질전환 유무를 검정하였고 선발된 형질 전환체들은 뇌수분 방법으로 세대진전시켰다. Genomic DNA 추출과 형질전환체들을 선발하기 위한 PCR 분석 및 도입된 T-DNA 개수 확인을 위한 DNA blot 분석은 T-DNA 내 hygromycin 저항성 유전자(hpt)를 대상으로 수행하였다(Yu et al., 2010). 이를 위해 사용된 primer set은 hpt-F: 5′-TTT CCA CT GCG AGT AC-3′와 hpt-R: 5′-TGT CGA GAA GTT TCT GAT CGA-3′이었다.
T-DNA 도입 위치 분석
Inverse PCR 분석을 통해 형질전환으로 도입된 T-DNA의 배추 게놈 내 위치를 분석하였다. 10μg의 gDNA를 제한효소 SacI(cat#R6061, Promega, Madison, WI, USA)으로 15시간 절단한 후, phenol:chloroform:isoamyl alcohol 25:24:1 용액 (cat#P3803, Sigma-Aldrich, Saint Louis, MO, USA)을 이용하여 정제하였다. 그 후, 4°C에서 18시간 동안 self-ligation된 DNA를 대상으로 thermocycler(cat#050-801, Biometra, Goettingen, Germany)를 이용하여 inverse PCR 반응을 수행하였다.
증폭된 PCR 산물은 pGEM-T easy vector(cat#A1360, Promega, Madison, WI, USA)에 삽입 후 염기서열을 분석(Macrogen Co., Seoul, Korea)하였다. 분석된 flanking DNA 염기서열은 Flanking Sequence Tag Validator(FSTVAL) 프로그램(http:// bioinfo.mju.ac.kr/fstval/)을 이용하여 배추 게놈 내 도입 위치를 확인하였다(Kim et al., 2012).
BrDSR 발현 수준 및 표현형 분석
건조 스트레스 조건에서 BrDSR의 체내 발현 수준 및 표현형 변화를 분석하기위해, 형질전환체와 비형질전환체를 광도 250μmolㆍm-2ㆍsec-1, 광주기 16시간 명처리/8시간 암처리, 온도 24 ± 2°C, 습도 40-60%의 조건에서 재배하였다. 물을 충분 히 준 후, 건조 처리 5일 째 유전자 발현 수준 분석용으로 total RNA를 추출하고 quantitative real-time RT PCR을 수행하여 체내 BrDSR의 발현 수준을 비교ㆍ분석하였다. 각각의 total RNA는 200mg의 잎을 채취하여 RNeasy® Plant Mini Kit(cat#74903; QIAGEN, Valencia, CA, USA)를 이용하여 추출하였다. Quantitative real-time RT PCR 분석은 DSRreal-F: 5′-ATG ACT TTG CAA GTT TTC CA-3′과 DSRreal-R: 5′-TCC TTC TAT GTT TGG AGG A-3′ primer set을 이용하 여 Yu et al. (2014)에 보고된 방법과 동일하게 수행하였다. 실험은 3반복으로 수행하였으며, 항시 일정수준으로 발현되는 대 조 유전자로는 actin 유전자를 이용하였다(actin-F: 5′-GGT ATT GTA AGC AAC TGG GAT-3′과 actin-R: 5′-TCA CCA GAG TCA AGC ACA ATA-3′). 한편, 표현형 분석은1 5일 동안 건조 처리 후 생육상태의 변화를 관찰하였다 .
B. rapa 135K microarray 분석
배추 내 유전자들의 발현 패턴은 “B. rapa genome 135K cDNA chip”을 이용하여 분석하였다(NimbleGen, Madison, WI, USA; GreenGene Bio Tech Inc., Yongin, Korea). 추출된 RNA를 이용한 혼성화 단계는 Yu et al.(2014)에 제시된 방법과 동일 하게 수행하였다. 최종 시그널은 GenePix scanner 4000B(Axon Instruments, Union, CA, USA)로 읽었고, 그 세기는 Nimblescan(Nimblegen Systems, Madison, WI, USA)을 이용하여 수치화하였다. 수집된 데이터는 MultiExperiment Viewer(MeV) 프로그램(www.tm4.org)을 이용하여 발현 패턴에 따라 1차 분류하고, 유의성이 높은 false discovery rate(FDR) < 0.05(Benjamini and Hochberg, 1995)의 유전자들은 애기장대 데이터베이스를 이용하여 gene ontology(GO) annotation 분 석(http://www.arabidopsis.org)과 MapMan(http://mapman.gabipd.org), cytoscape(http://www.cytoscape.org) 분석 프로그 램들을 이용하여 BrDSR과 건조 저항성 관련 유전자들의 발현 패턴을 비교ㆍ분석하였다.
결과 및 고찰
형질전환체 선발
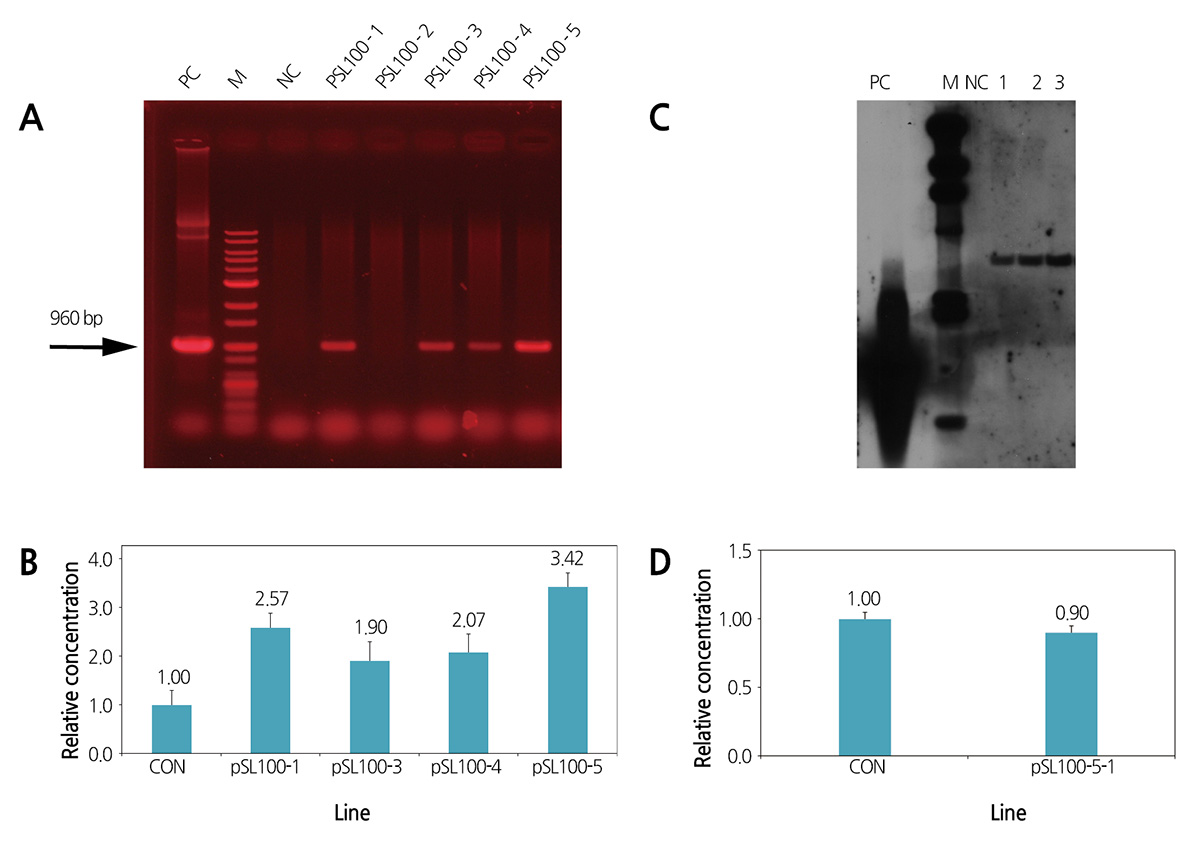
BrDSR 유전자가 과발현된 배추 형질전환체를 확보하기 위해, 제작된 pSL100 vector와 내혼계 배추(‘CT001’)를 이용하여 Yu et al. (2010)에 제시된 방법으로 형질전환을 수행하였다. 생산된 형질전환체들은 도입된 T-DNA내 hpt 유전자를 대상으로 한 PCR 분석으로 형질전환 유무를 검정하여 4개의 배추 형질전환체를 선발하였다(Fig. 1A). PCR 분석으로 선발된 4개체와 비형질전환체를 대상으로 5일 동안 건조 처리 후 각각의 total RNA를 추출하여 quantitative real-time RT PCR 분석을 수행하 였다. 그 결과, 형질전환체들의 체내 BrDSR 유전자의 발현 수준이 비형질전환체에 비해 1.9-3.4배 정도 증가한 것으로 분석되 었다(Fig. 1B). 각 개체의 발현값은 내부 대조 유전자인 actin 유전자의 발현량을 이용하여 BrDSR의 발현값을 보정하였다. PCR 분석으로 T-DNA가 성공적으로 도입되었음을 확인하고, quantitative real-time RT PCR 분석으로 도입 유전자의 과발현이 확인된 4개의 형질전환체를 pSL100-1, pSL100-3, pSL100-4 및 pSL100-5로 각각 명명하였으며 모두 세대진전시켰다.
게놈 내 도입된 T-DNA 분석
PCR분석으로 형질전환체임이 확인되고 quantitative real-time RT PCR 분석으로 대조군 대비 발현량이 증가한 pSL100- 1, pSL100-3, pSL100-4 및 pSL100-5 계통 중 발현량이 가장 크게 증가한 pSL100-5 계통의 T1 세대 개체들을 이용하여 도 입된 T-DNA를 분석하였다. 우선, DNA blot 분석으로 pSL100-5 계통은 1 copy의 T-DNA가 전이된 형질전환체임을 확인 하였다(Fig. 1C). 그리고 inverse PCR 분석결과를 바탕으로 Flanking Sequence Tag Validator(FSTVAL) 프로그램(GreenGene Bio Tech Inc., Korea)과 BLASTN분석(www.ncbi.nlm.nih.gov)을 이용하여 정확한 삽입위치를 확인한 결과, 전이된 T-DNA 는 99.39%의 상동성으로 5번염색체의 “KBrB019N06” BAC clone 내 ‘ethylene-responsive transcription factor RAP- 2(RAP2.2, AT3G14230)’ 유전자 3′-UTR 앞부분에 삽입되어 있는 것으로 분석되었다. T-DNA가 게놈 내 intergenic region에 삽입된 것이 아니므로, pSL100-5 계통 개체들의 BrDSR 과발현 현상이 도입 유전자의 발현 때문인지 아니면 T-DNA 삽입으 로 인한 RAP2.2의 발현량 변화 때문인지를 명확히 확인하기 위해 T1 세대 형질전환체인 pSL100-5-1 개체와 비형질전환체 인 ‘CT001’ 배추(CON)를 이용하여 체내 RAP2.2의 발현 수준을 3반복의 quantitative real-time RT PCR로 분석하였다. 그 결 과, 발현 수준의 변화가 발생했을 것으로 의심되었던 형질전환체의 RAP2.2의 발현량은 비형질전환체의 RAP2.2와 비교하여 0.9 : 1.0 정도로 거의 동일한 발현 수준을 보였다. 이로써 pSL100-5 계통의 체내 유전자들의 발현 패턴 변화는 도입유전자의 전이 및 발현 때문인 것으로 판단하였다(Fig. 1D).
건조 스트레스 저항성 분석
체내 BrDSR 유전자의 발현량이 현저히 증가하고 T-DNA 도입 위치가 분석된 pSL100-5 계통의 T1 세대 개체들을 대상으 로 건조 스트레스 하에서 저항성 여부를 관찰하였다. 유리온실 내에서 사각형 화분에 비형질전환체(CON) 4개체와 형질전환 체(T1) 9개체를 정식한 후 충분히 수분을 공급한 후 15일간 건조 스트레스 처리하였다. 그 결과, 형질전환체들 간 비교에서는 건조 저항성 수준의 차이가 거의 없었으며, 비형질전환체와 형질전환체들간의 비교에서는 pSL100-5 계통의 건조 저항성이 비형질전환체에 비해 월등히 우수함을 확인할 수 있었다(Fig. 2). 따라서 표현형 검정 결과 모든 형질전환체가 우수한 건조 저 항성을 보여주어, 아직 정확한 기능은 보고되지는 않았지만 BrDSR 유전자의 과발현이 배추의 건조 스트레스 저항성 향상에 크게 기여하고 있는 것으로 판단되었다.
건조 스트레스 반응 유전자 분석
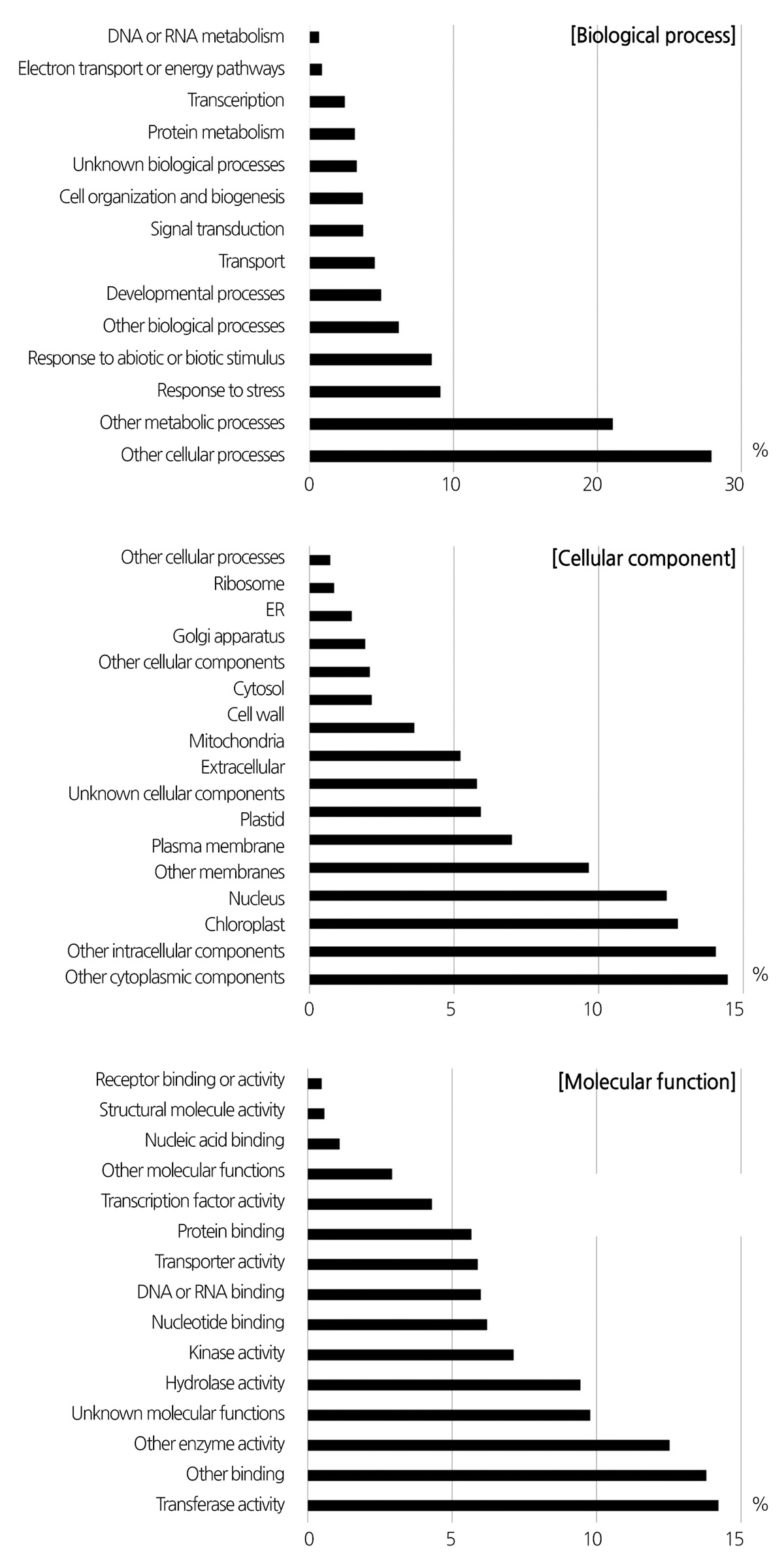
cDNA chip)을 수행하였다. BrDSR의 과발현과 연관되어 건조 스트레스에 반응하는 유전자들의 발현 양상을 분석한 결과, 총 3,838개의 유전자가 확인되었으며 이 중 1,924개는 대조군 대비 발현량이 증가하였고 1,914개는 발현량이 감소하였다. 이들 유전자를 대상으로 FDR < 0.05인 유전자들을 2차 분류하여 발현량 증가 그룹에서 195개 유전자, 발현량 감소 그룹에서 160개 유전자를 선발하였다. 발현이 변화된 유전자들을 대상으로 먼저 Gene ontology annotation 프로그램을 이용한 분석 결과, Molecular function 범주에서는 “Transferase activity” 및 “Hydrolase activity”에 속한 유전자들이 다수 속해 있었으며, Cellular component 범주에서는 스트레스와 밀접한 관련이 있는 광합성과 연관된 “Chloroplast”에 속한 유전자들의 발현이 많 이 변화되고 있음을 확인하였다. 또한 Biological process 범주에서는 예상대로 “Response to abiotic or biotic stimulus” 및“Response to stress”에 속한 유전자들이 주를 이루었다(Fig. 3). 건조 스트레스 반응 유전자들 중 특히 ‘Calcineurin B-Like 1/CBL-interacting protein kinase 6(CBL1/CIPK6, Bra011236, AT4G30960)’의 발현량이 16배 이상 증가한 것으로 분석되었 다(Table 1). CIPK6의 경우 2000년대 초반부터 그 기능이 밝혀지기 시작하여 비생물적 스트레스 중 염 및 삼투압 스트레스 또 는 앱시스산(abscisic acid, ABA) 시그널 발생 시 발현량이 크게 증가하여 K+ channel들의 활성을 높임으로써 식물체의 저항 성을 향상시켜 주는 것으로 보고되어 있다(Chen et al., 2013; Martinez-Atienza et al., 2007; Tang et al., 2010; Zhao et al.,2009). 하지만, 건조 스트레스 처리에서 발현량이 크게 변하는 것은 보고되었으나 건조 저항성 기작과의 관련성은 아직 명확히 밝혀지지 않았다(Chen et al., 2013). 또한 ‘3-ketoacyl-CoA synthase 2(KCS2, Bra015296, AT1G04220)’의 발현량도 크게 증 가하였는데, KCS2는 식물의 표피왁스(cuticular wax) 형성 관련 유전자로서 건조 스트레스 발생 시 발현량의 증가를 통해 식 물체의 기계적(물리적) 보호 역할을 하며(Lee et al., 2009), 최근에는 갓류(Eutrema salsugineum)에서 분리한 EsWAX1의 과발 현이 KCS2의 발현을 증가시킴으로써 애기장대의 건조 스트레스 저항성을 향상시킴이 보고되었다(Zhu et al., 2014).
두 번째로 MapMan 프로그램을 이용하여 체내 대사과정에서의 주요 유전자들의 발현 패턴을 분석하였다. 다양한 대사과정 에서 주요 유전자들의 발현 변화가 확인되었는데, 특히 비생물적 스트레스 관련 대사과정(abiotic stress pathway)에서는 ‘Calcium-dependent lipid-binding protein(CLB, Bra003434, AT3G61050)’의 발현이 감소하였는데 이는 CLB의 발현이 비 생물적 스트레스에 대한 반응을 억제한다는 보고와 유사한 결과이다(de Silva et al., 2011). 또한, 식물 5대 호르몬 중 앱시스산 합성 관련 대사과정(ABA synthesis pathway)에서 ‘9-cis-epoxycarotenoid dioxygenase 3(NCED3, Bra001552, AT3G14440)’, ‘9-cis-epoxycarotenoid dioxygenase 4 (NCED4, Bra020970, AT4G19170)’ 유전자들을 비교한 결과, NCED4 유전자는 발현이 증가하는 것으로 나타나는데 반해, NCED3 유전자는 오히려 발현이 크게 감소한 것으로 분석되었다. 이는 스 트레스 반응 물질인 앱시스산의 합성에 있어 건조 스트레스 발생 시에는 NCED3 보다는 NCED4 유전자가 주로 작동하는 것 으로 추정된다(Frey et al., 2012; Thiel et al., 2011). 또한 앱시스산을 분해하는(ABA catabolic pathway) 유전자인 ‘ABA 8'-hydroxylase(Bra040762, AT2G29090)’와 ‘ABA glucosyltransferase(Bra012784, AT4G15480)’의 발현이 크게 감소한 것 으로 나타나 건조 스트레스 발생 시 앱시스산이 중요하게 작용하고 있음을 확인할 수 있었다. 아울러, 이런 앱시스산의 고농도 유지는 잎의 공변세포에서 K+이온의 흡수를 억제하고 방출을 활성화하여, 공변세포 내 수분이 유출됨으로써 기공이 닫히는 현상을 발생시키게 된다(Leckie et al., 1998; Pantin et al., 2013).
유전자 상호 네트워크 분석
건조 스트레스 저항성인 BrDSR과 관련된 체내 유전자들을 분석하기 위해 먼저 24,000개의 unigene으로 분석된 ‘KBGP- 24K oligo chip’ 데이터(Lee et al., 2008)와 ‘PlantArrayNet’ 프로그램(http://arraynet.mju.ac.kr/arraynet/)의 ‘Brassica 300K microarray’ 데이터를 활용하여 배추의 건조 저항성 관련 유전자들의 네트워크를 구축하였다. 구축된 네트워크는 총 23,937개 의 분석 probe 중 1,560개의 probe가 건조 스트레스 조건에서 유의적으로 반응함을 보여 주었다. 특히, proline 생합성에 관련 된 유전자들이 다수 발현량 증가를 보여 건조 스트레스 반응 기작에 proline이 긴밀한 관련이 있는 것으로 분석되었다(Table 2). 약 2.8배 증가한 ‘salt tolerance zinc finger(STZ, Bra010922, AT1G27730)’ 유전자의 경우 proline과 밀접한 관계를 가지고 있 으며 reactive oxygen species(ROS) 제거 등 염을 포함한 환경 스트레스 저항성과 관련이 있는 것으로 보고 되어있다(Mehterov et al., 2012). 또한, 앱시스산과 촉매반응으로 H2O2를 생성하여 ‘delta1-pyrroline-5-carboxylate synthase(P5CS1)’의 활성을 증가시킴으로써 proline의 합성량을 증가 시키는 것으로 보고된 ‘ABA insensitive 1(ABI1, Bra001994, AT4G26080) 유전자 의 발현도 5배 정도 크게 증가하였다.
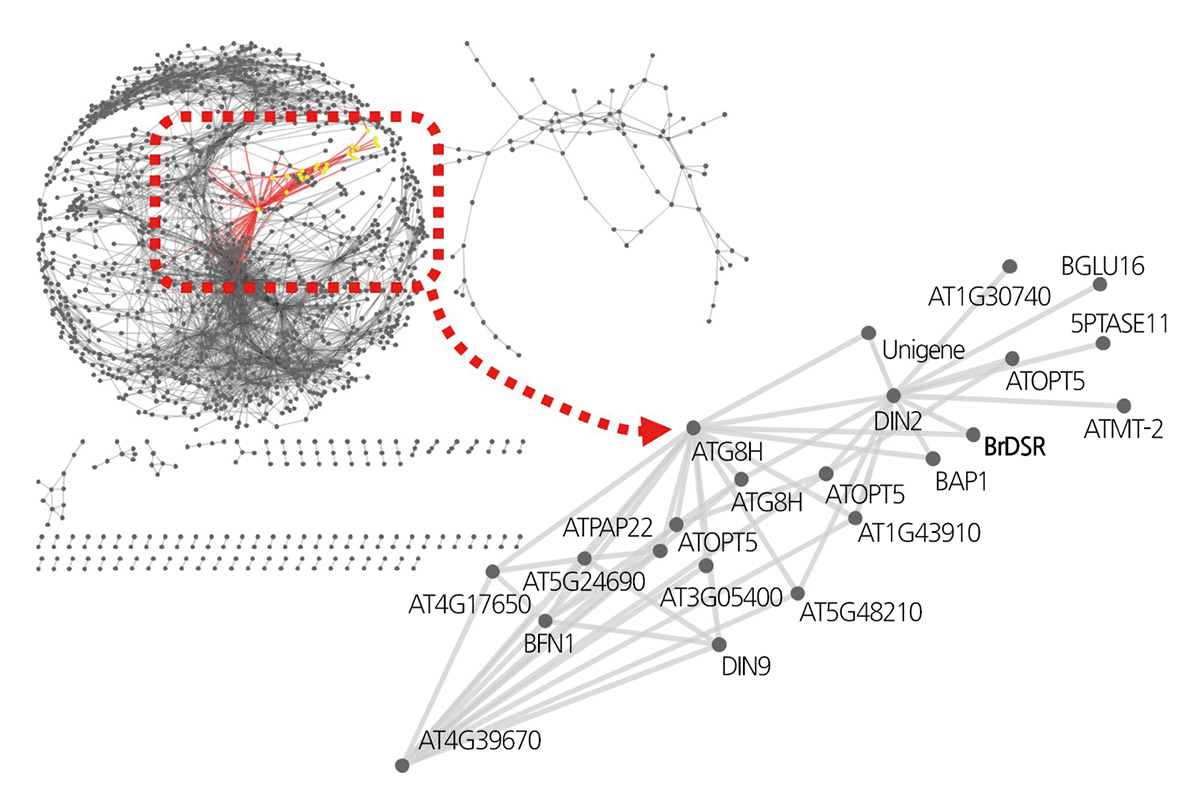
구축된 건조 스트레스 반응 유전자들의 네트워크 상에서 도입유전자인 BrDSR의 위치를 확인하고 이와 연관된 유전자들을 분류하였다(Fig. 4). BrDSR 유전자와 직접적으로 연결된 주요 유전자는 ‘DARK INDUCIBLE 2(DIN2, Bra014510, AT3G60140)’와 ‘AUTOPHAGY 8H(ATG8H, Bra020749, AT3G06420)’로 확인되었다. DIN2의 경우 환경 스트레스와의 연관성은 명확히 보고되어 있지는 않지만, 잎의 노화에 관여하는 것으로 보고되어 있다(Baena-González et al., 2007). ATG8H는 자가 소화(autophagy) 를 통한 단백질분해(protein degradation)를 촉진시키며, 이에 따라 식물체 잎의 노화가 유발 된다(Devarenne, 2011). 한편, ATG8H와 연결된 ‘bifunctional nuclease 1(BFN1, Bra031758, AT1G11190)’는 노화된 조직의 DNA로부터 phosphate를 회수 하는 역할을 하며(Sakamoto and Takami, 2014), 정확한 기능은 밝혀져 있지는 않으나 식물체 방어기작과 관련된 ‘Glycolipid transfer protein family protein(GLTP, Bra004321, AT4G39670)’과 직접적인 연관관계를 보였다.
지금까지의 도입유전자의 건조 스트레스 발생 시 발현량 및 표현형 분석, 발현 네트워크 결과를 종합해 보면, BrDSR 유전자 는 건조 스트레스 저항성 관련 유전자로 보고된 다수의 유전자들과 네트워크적으로 연결되어 있었고, 스트레스 발생 시 발현 량 증가를 통해 배추의 건조 저항성을 크게 향상시켜 주었다. 그러므로 BrDSR 유전자는 작물의 건조 저항성 확보에 매우 중요 한 역할을 하는 것으로 판단된다.
Table 2. Significantly changed genes related to proline metabolism from the B. rapa genome 135K cDNA chip data. ATRZF1 plays a negative regulator of proline biosynthetic process.
| |
zLog2 scale. | |