서 언
재료 및 방법
Microarray 정보 수집 및 네트워크 모델 구축
저온 처리간 배추 내부 유전자 발현 변화 분석
결과 및 고찰
저온 스트레스 처리 시 유전자 발현 네트워크 모델 구축
저온 스트레스 관련 네트워크 모델을 이용한 처리시간별 반응 기작 분석
서 언
식물은 저온, 건조, 염 스트레스와 같은 비생물적 스트레스 환경과 병해충 및 섭식 동물에 의한 피해와 같은 생물적 스트레스 환경에 적응하기 위해 다양한 방향으로 진화했다(Alonso-Blanco et al., 2009). 특히, 염 스트레스는 식물체의 고사(枯死)에 간접적인 원인을 제공하지만, 저온 스트레스는 직접적으로 발아율 저하, 잎의 시듦 및 팽압 감소, 식물 조직의 괴사(necrosis) 및 백화 현상(chlorosis) 유발 등을 초래한다(Sanghera et al., 2011). 이러한 저온 자극은 식물 세포막의 수용인자에 전달되어 저온 저항성을 획득하기 위한 다양한 대사과정 및 이에 속한 유전자들의 발현을 복합적으로 조절하게 할 뿐만 아니라, 배추 및 양배추와 같은 저온 감응이 필요한 작물에서는 flowering locus C(FLC) 등의 개화관련 유전자의 발현을 조절하여 작물의 영양 생장 단계를 생식 생장 단계로 전환 시키는 주요한 요소로써 작용하기도 한다(He and Amasino, 2005; Penfield, 2008). 최근 애기장대(Barah et al., 2013; Chawade et al., 2007; Naika et al., 2013), 벼(Cho et al., 2012), 미국가문비나무(Picea sitchensis; Grene et al., 2012), 꽃다지종(Draba species; Zhou et al., 2009), Chorispora bungeana(Zhao et al., 2012) 및 녹조류(Valledor et al., 2013)에서 저온 스트레스에 관련된 전사 인자 연구, 유전자 발현 네트워크 구축을 통한 저항성 기작의 심층적 분석, 저항성 획득 관련 유전자 발굴 등이 활발히 진행되고 있다. 이러한 연구들은 식물이 저온에 노출되었을 때 COR(cold- regulated) 또는 CBF(C-repeat binding factor transcriptional activator) 전사조절인자의 발현 조절로 약 100개 이상의 하위 유전자의 발현이 복합적으로 조절되며, 이는 플라보노이드(flavonoid) 관련 대사과정 조절, 세포막 구조 변화, 및 당(sucrose), 라피노즈(raffinose), 프롤린(proline)과 같은 용질 축적 변화 등과 같은 생리적 및 생화학적 변화를 통해 저온 저항성이 획득되었음을 보고하였다(Barah et al., 2013; Kamata and Uemura, 2004; Korn et al., 2008; Zhao et al., 2012).
배추속(Brassica genus)식물은 대한민국뿐만 아니라 전 세계적으로 식용 및 조미료, 사료 등으로 사용되고, 바이오디젤과 같은 대체 에너지로도 활용되는 등 작물로서의 가치가 높으며, 모델 식물로 많은 연구가 이루어진 애기장대(Arabidopsis thaliana)와 같은 배추과(Brassicaceae)이므로 중요한 학문적 가치를 가진다(Yu et al., 2010; Zhao et al., 2005). 배추는 일반적으로 -4°C, 유채는 -20°C에서도 짧은 기간 동안은 생존이 가능하지만, 저온 감응이 이루어진 추대 후에는 생장점이 외부로 노출되어 한파 등의 저온 스트레스 환경에 더욱 피해가 크다(Ananga et al., 2012). 한편, 2011년 “Brassica Genome Sequencing Project Consortium”의 유전체 연구 결과는 배추에서 다양한 분자 마커 개발 및 저온 스트레스를 포함한 비생물적 스트레스 반응하는 유전자들에 대한 심층적 분석을 가능케 하였다.
본 연구는 배추 EST 및 Microarray 데이터베이스(RDA, 2008)를 이용하여 저온 스트레스에 대한 microarray 정보를 획득하고, 이것을 통계적 분석 및 관련 유전자들의 가시화를 통하여 배추에서의 시간경과에 따른 저온 스트레스 반응 유전자들의 발현 네트워크모델을 구축하였다
재료 및 방법
Microarray 정보 수집 및 네트워크 모델 구축
본 연구에 이용된 배추의 저온 스트레스 처리에 따른 microarray 분석 자료는 BrEMD(Brassica rapa EST and Microarray Database, http://www.brassica-rapa.org/BrEMD; 현재 농업생명공학정보센터, http://nabic.rda.go.kr/)에서 획득하였다. 해당 분석 결과는 생육환경이 일정한 식물생장상(온도 4°C, 광주기 16시간 명처리/8시간 암처리, 광도 290 uE・m-2・s-1, 습도 40-70%)에서 3주간 생육된 근교계통 배추인 ‘Chiifu’를 대상으로 저온 처리 후 0.5, 3, 12, 24, 48시간 간격으로 total RNA를 분리하고, 발현하는 배추 유전자를 NimbleGen System을 이용한 KBGP-24K microarray chip으로 분석한 결과로서 2반복으로 진행된 연구 결과이다(Lee et al., 2008).
저온 스트레스에 의한 배추 내 발현 유전자의 상호 관계 분석은 Brassica 300K microarray data를 기반으로 각 유전자 간 발현 연관성을 분석 및 제공하는 PlantArrayNet(GreenGene BioTech Inc.; http://bioinfo.mju.ac.kr/arraynet/)을 이용하였다. 저온 스트레스 처리 시간별 KBGP-24K microarray chip 분석 결과에서 처리 대조군(0시간)을 기준으로 2배 이상 발현이 변화하는 유전자 중 PlantArrayNet 분석에서 correlations value > 0.85로 나타나는 유전자군을 선발하였다. 분석된 저온 스트레스 관련 유전자 발현 네트워크 모델은 Cytoscape program(version 2.8.3, Cytoscape Consortium; Smoot et al., 2011)을 이용하여 구축하였으며, 네트워크의 구조는 spring embedded layout을 이용하여 가시적으로 형상화 하였다(Barnes and Hut, 1986).
저온 처리간 배추 내부 유전자 발현 변화 분석
구축한 네트워크를 이용하여 저온 스트레스 처리 시간별 유전자 발현 및 주요 기능 변화를 분석하였다. 발현 네트워크 상 유전자군의 대사과정의 변화는 KEGG(Kyoto Encyclopedia of Genes and Genomes, http://www.genome.jp/kegg/)와 TAIR(The Arabidopsis Information Resource, http://www.arabidopsis.org/)를 이용하여 획득하였으며, 발현 유전자들의 기능 분석을 통한 배추의 저온 저항성 기능 유추는 DAVID(The Database for Annotation, Visualization and Integrated Discovery, http:// david.abcc.ncifcrf.gov/)를 사용하여 수행하였다(Huang et al., 2009; Kanehisa et al., 2012). 이후 획득한 정보를 바탕으로 gene ontology 분석은 Cytoscape plug-in program인 ClueGO를 이용하여 분석 및 가시화하였다(Bindea et al., 2009).
결과 및 고찰
저온 스트레스 처리 시 유전자 발현 네트워크 모델 구축
PlantArrayNet가 제공하는 Brassica 300K microarray 분석 결과와 본 연구팀 및 (구)농업생명공학연구원 배추제놈팀과의 공동연구 결과인 KBGP-24K microarray chip 분석 데이터를 이용하여 배추에서 저온 스트레스 반응 유전자들의 발현 네트워크 모델을 구축하였다. 저온 스트레스에 따른 배추 내 유전자 발현 연관 관계를 correlations value > 0.85로 선발한 결과 총 23,937개의 probe 중에서 저온 스트레스 조건에서 유의적으로 발현하는 2,030개의 probe를 선발하였다. 구축된 네트워크 상에서 선발된 유전자군의 기능을 분석하기 위하여 DAVID bioinformatics resources를 이용하여 functional annotation clustering을 실시하였다. 분석된 198개의 functional cluster 중 enrichment score가 높은 순서로 5개의 cluster를 선발하였다(Table 1). 그 결과 functional cluster 중 가장 높은 enrichment score를 가진 [cluster 1]의 경우 저온 스트레스 조건 하에 반응하는 유전자군인 [response to abiotic stimulus], [response to temperature stimulus], [response to cold]가 확인되었으며, 다른 cluster에서는 [nuclear lumen], [response to hormone stimulus], [response to cadmium ion] 및 [cell wall]과 관련된 유전자가 다수 발현되었다. 식물체가 저온 스트레스를 받게 되면 세포 경화 현상 및 Ca2+ 신호에 의한 저온 저항성 관련 protein kinase가 활성화되고, ICE1(inducer of CBF expression 1) 및 ZAT 등에 의해 COR 유전자군의 발현을 조절하여 저온 저항성 획득하게 되는데(Chinnusamy et al., 2007), 이러한 기작들이 상기 도출된 functional cluster들과 일치하였다. 즉, 네트워크를 구축하기 위해 선발된 probe 집단이 저온 스트레스 저항성과 유의적인 관련이 있는 것으로 분석되었다. 이에 따라 분석된 결과를 spring embedded layout을 이용하여 가시화하였다(Fig. 1). 구축된 유전자 발현 네트워크는 각각의 유전자를 나타내는 node와 각 유전자간의 유의적 발현 상호관계를 edge로 표현하였으며, 네트워크 모델 구축 후 multi-edge node pair와 self-loop node는 분석 후 제거하여 총 2,030개 node와 20,235개 edge 및 34개 connected component로 구축하였다. 특히 하위 connected component 중 가장 크게 차지하고 있는 독립 네트워크 그룹이 전체 node 중 91.97%(1,867개)를 차지하고, 전체 edge 중에서도 98.96%(20,026개)를 포함하고 있어 구축된 네트워크 모델이 높은 연관 관계로 구축된 것을 검증할 수 있었다.
저온 스트레스 관련 네트워크 모델을 이용한 처리시간별 반응 기작 분석
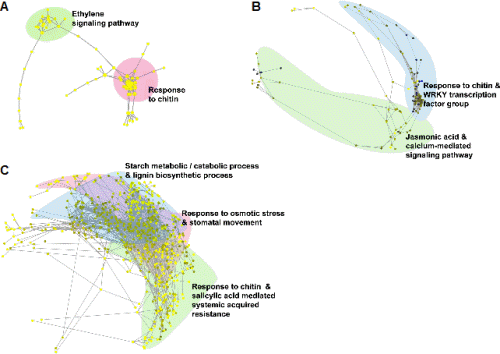
구축한 네트워크를 바탕으로 배추에서 저온 스트레스(4°C) 발생 시 시간경과에 따른 내부 유전자군들의 유의적 발현 패턴을 분석한 결과 총 2,030개의 유전자 중에서 30분(0.5h) 경과 후에는 101개(4.98%), 3시간 경과 시 142개(7.00%), 12시간 경과 시 692개(34.09%), 24시간 경과 시 240개(11.82%), 48시간 경과 시에는 855개(42.12%) 유전자가 유의적인 상호 관계를 가지는 것으로 분석되었다(Fig. 1).
저온 처리 30분(0.5h) 후 반응하는 유전자군은 주로 [ethylene signaling pathway]와 [response chitin]에 속하는 것으로 분석되었다(Fig. 2A). 우선 [ethylene signaling pathway] 유전자군의 경우 저온 스트레스에 의한 ethylene-responsive transcription factor(ERF) 유전자들이 주로 발현되는 것으로 분석되었다. 저온, 건조, 염 및 상처와 같은 비생물적 스트레스에 의해 발생되는 에틸렌(ethylene)은 저온 저항성을 획득하기 위한 필수적인 요소 중 하나로 ‘ETHYLENE-INSENSITIVE2-dependent or -independent pathways’에 속한 ERF 유전자군을 조절하여 병 저항성 단백질(pathogenesis-related protein, PR)의 생성에 관여하는 유전자들의 발현을 유도한다(Fujimoto et al., 2000; Hon et al., 1994; Yu et al., 2001). 특히, glucanases, chitinases, thaumatin-like proteins 등과 같은 병 저항성 단백질은 부동단백질(antifreeze protein, AFP)의 역할을 하는 것으로 알려져 있는데 이들 단백질들은 축적된 저온 자극을 극복하기 위해 생성된 얼음 조각의 표면에 결합해서 수소 결합 및 반데르발스 힘(van der Waals force)에 의해 얼음 조각이 확대되는 것을 억제한다(Griffith et al., 1992; Pihakaski- Maunsbach et al., 2001; Yeh et al., 2000). 이들 중 chitinases- AFP의 경우는 저온 자극 시 뿌리를 제외한 대사활성이 있는 모든 세포에서 발현되어 식물체의 저온 저항성 획득에 있어 주요 요소이다(Pihakaski-Maunsbach et al., 2001). 이러한 연구보고들과 동일하게 배추를 대상으로 한 본 연구에서도 저온 스트레스 초기 30분 동안 에틸렌에 의한 신호가 발생하고 이를 통한 chitinases-AFP가 활성화되어 저온 저항성을 획득하기 위한 신호가 전달되는 것을 확인하였다.
저온 처리 3시간(3h) 후 반응하는 유전자군은 크게 [response to chitin] 및 [WRKY transcription factor group] 유전자군과 [Jasmonic acid mediated signaling pathway] 유전자군으로 분석되었다(Fig. 2B). 특히 chitinase 유전자군은 저온 처리 30분에 이어 지속적으로 chitinases-AFP를 활성화하였으며, 이렇게 활성화된 저온 저항성 신호는 구축한 네트워크 상에서 WRKY 전사인자(transcription factor) 유전자군과 유의적으로 연결되었다. WRKY 전사인자는 식물의 생장 및 호르몬 신호 전달에 영향을 주기도 하지만, 생물적 및 비생물적 스트레스 관련 저항성 향상에도 관여하는 주요 인자이다(Eulgem et al., 2000). 특히 저온 처리된 애기장대를 이용한 microarray 분석에서 발현된 전사인자 중 7종의 WRKY 전사인자(WRKY7, WRKY22, WRKY33, WRKY40, WRKY46, WRKY53, WRKY70)가 유의적인 관련이 있는 것으로 보고되었다(Chawade et al., 2007). 배추를 이용한 본 연구 결과에서도 처리 3시간 후 대조군 대비 WRKY33은 5.38배, WRKY40은 14.88배, WRKY53은 8.83배 과발현하여, 배추의 저온 저항성 관련 신호 전달이 WRKY 전사인자의 발현과 밀접한 관련이 있음을 확인할 수 있었다. 이후 활성화된 WRKY 전사인자에 의해 자스모닉산(jasmonic acid)과 칼슘에 의한 신호전달 기작이 유기적으로 연결되어 발현되는 것으로 분석되었다.
다음으로 저온 처리 12시간(12h) 후 반응하는 유전자군은 [response to chitin and salicylic acid mediated systemic acquired resistance], [response to osmotic stress & stomatal movement], [starch metabolic/catabolic process], [lignin bio-synthetic process]로 분석되었다(Fig. 2B). 저온 처리 12시간도 앞선 3시간째의 chitinases-AFP 및 WRKY 전사인자들의 영향을 받아 전체 네트워크 중 34%(692개)의 유전자가 발현한 것으로 확인되었으며, 이는 앞선 3시간째의 발현 유전자 수보다 4.87배나 증가한 수치이다. 이렇게 증가한 유전자군은 살리실산(salicylic acid, SA)에 의해 장기적 저항성 기작인 전신적 획득저항성(systemic acquired resistance, SAR) 기능을 하는 유전자군으로 네트워크가 연결되었다. 살리실산의 경우 식물체에서 병원성 관련(pathogenesis-related, PR) 유전자 발현 및 과민성 반응과 같은 병 저항성 기작에 중요한 요소이다. 또한 비생물적 스트레스에도 밀접한 관련이 있어, 살리실산 처리 시 벼, 밀, 옥수수, 토마토, 호박, 수박과 같은 작물의 저온 저항성이 증진되었다는 보고들이 있다(Ding et al., 2002; Hua et al., 2008; Kang and Saltveit, 2002; Kunkel and Brooks, 2002; Scott et al., 2004; Tasgin et al., 2003). 즉, 배추가 저온 스트레스 조건에서 저항성을 획득하기 위해 살리실산을 매개로 전신적 획득저항성 관련 기작을 작동하는 것으로 분석되었다. 한편, 전신적 획득저항성은 삼투 스트레스 및 기공의 변화를 초래한다. 저온, 건조, 염과 같은 비생물적 스트레스 조건에서 식물체는 수분의 손실을 막기 위해 기공을 폐쇄하며, 이러한 기작은 ABA에 의해 천천히 기공 개폐가 조절되는 대사과정과 ABA와는 독립적으로 환경의 변화에 의해 신속히 조절되는 대사과정으로 나누어 진다(Kim et al., 2008; Luan, 2002). 본 연구 결과에서는 기공 개폐와 관련된 유전자들인 glycine-rich RNA-binding proteins 7(GRP7)의 경우 대조군 대비 12배, ABA insensitive 1(ABI1)은 2.44배, responsive to dessication 20(RD20)은 1.91배 과발현되었다. 이들 중 GRP7은 ABA에 독립적인 대사과정에 속하는 유전자로 건조 및 염 스트레스 조건에서는 기공을 열어 식물체에 부정적인 영향을 주지만, 저온 스트레스 조건에서는 기공을 닫아 저항성을 부여하는 기능을 가지고 있어(Kim et al., 2008), 배추에서도 저온 저항성을 획득하기 위해 수분 스트레스 관련 유전자 및 기공 개폐 유전자의 발현을 조절하여 기공을 닫는 것으로 분석되었다. 한편, 광합성과 관련된 탄수화물 분해 대사 과정 및 리그닌 생합성 관련 유전자들의 발현이 촉진되었는데, 이러한 결과는 애기장대, 밀, 벼 등에서 저온 스트레스 처리 시 발현되는 전사체 및 단백질의 유전 정보학적 분석과 동일한 결과였다(Hirose et al., 2013; Janská et al., 2010; Renaut et al., 2006). 이러한 탄수화물의 분해를 통한 당의 축적은 식물체가 저온 저항성을 획득하기 위한 필수적인 과정 중 하나이며, 특히 starch excess 1(SEX1)이 핵심적인 유전자 중 하나이다(Maruyama et al., 2009; Yano et al., 2005). 배추의 경우에서도 SEX1 유전자가 대조군 대비 최대 12.13배 과발현하여 저온 저항성을 획득하는 주요 과정 중 하나로 판단된다.
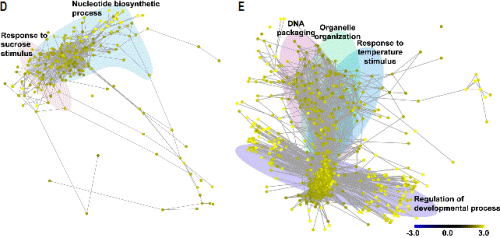
다음으로 저온 처리 24시간(24h) 후 반응하는 유전자군은 크게 [response to sucrose stimulus]와 [nucleotide biosynthetic process]의 그룹으로 분석되었다(Fig. 2D). 이는 12시간대의 탄수화물의 분해를 통한 당 축적으로 인해 24시간 후에는 당에 의한 자극 반응이 활성화되는 것으로 판단된다. 이들 중 엽록소에 결합하여 광합성 과정에 관여하며 저온 자극과 관련이 있으나 아직 정확한 상호관계가 밝혀지지 않은 ELIP1과 ELIP2가 각각 17.62배, 19.46배 과발현되었으며(Kreps et al., 2002; Rossini et al., 2006), 기공 개폐를 조절하는 유전자 중 하나인 iPGAM의 발현도 2.58배 증가하였다(Zhao and Assmann, 2011). 또한 당 축적으로 인한 자극 중 일부는 저온 저항성과 관련된 안토시아닌(anthocyanin)의 생합성에 관여하는 유전자들인 CHIL(2.54배), FLS1(2.68배), CHS(2.21배)의 과발현을 유도하였다(Hara et al., 2004; Leyva et al., 1995). 다음으로 [nucleotide biosynthetic process]에 속하는 유전자군은 전체 240개 유전자 중 기능이 알려진 유전자가 54개(22.5%)였으나, 네트워크 상에서 이들 유전자와 직접적으로 연결된 유전자는 155개(64.58%)로 12시간대 발현한 유전자들이 대부분을 차지하였다. 이것은 앞선 반응으로 기인한 저온 저항성 기작들이 본격적으로 작동하는 것으로 판단된다.
|
Fig. 3. A simplified hypothetical model depicting gene expression related to cold stress during 0.5 h, 3 h, 12 h, 24 h, and 48 h after 4°C treatment in Chinese cabbage. |
마지막으로 저온 처리 48시간(48h) 후 반응하는 유전자군은 [response to temperature stimulus], [regulation of developmental process], [DNA packaging], [organelle organization], [succinate metabolic process]으로 분석되었다. 이 단계에서는 전체 네트워크 중 42.12%(855개)의 유전자가 발현하여 전체 단계별 가장 많은 유전자가 유의적으로 발현하였으며, 24시간대의 [nucleotide biosynthetic process]에 속하는 유전자군의 영향으로 유전자 수가 3.56배로 급격히 증가한 것으로 판단된다(Fig. 2E). 우선 [response to temperature stimulus] 유전자군의 경우 저온 자극에 따른 반응과 관련된 대표적 유전자로 저온 저항성과 관련된 frostbite1(FRO1)이 2.84배, thiamine4 (THI1)이 2.57배 과발현되었다(Lee et al., 2002; Rapala-Kozik et al., 2012). 특히 미토콘드리아에서 발현되는 유전자인 FRO1의 발현 증가는 앞선 24시간대의 핵 내부로부터 증폭된 저온 감응 신호가 식물체 전체로 유기적인 전파가 이루어지고 있음을 보여준다(Lee et al., 2002). 또한 외부로부터 저온 스트레스 신호가 들어올 시에는 저온 저항성을 부여하기 위해 [regulation of developmental process]에 속하는 ‘positive regulation of developmental process’ 유전자 그룹을 매개로 [steroid biosynthetic process]로 넘어가서 저항성 기작을 작동하는 것으로 분석되었다. 이 그룹에는 식물체의 생육 및 세포 분열을 촉진 하는 것으로 알려져 있는 브라시노스테로이드(brassinosteroid)와 피토스테로이드(phytosteroid)에 속한 유전자군이 유의적으로 발현되었다. 세부 유전자들을 살펴보면 브라시노스테로이드 관련 유전자로는 대표적으로 ARGOS-LIKE(ARL)가 2.83배, BR-signaling kinase 1(BSK1)이 2.86배, general regulatory factor 2(GRF2)가 2.54배 과발현되었으며, 피토스테로이드 관련 유전자로는 fasciclin-like arabinogalactan-protein 2(FLA2)가 2.99배, constitutive photo-morphogenic dwarf(CPD)는 2.25배 과발현되었다. 다음으로 [DNA packaging]에 속하는 유전자군은 식물체의 영양 생장 단계를 생식 생장 단계로 전환시키는 역할을 하는 ‘vegetative to reproductive phase transition of meristem’과 ‘regulation of reproductive process’의 기작을 작동시키는 것으로 분석되었다. 이러한 신호 네트워크는 ‘anatomical structure formation’ 유전자군에 의해 생식 생장으로 전환하게 되며, 이후 이 신호는 [organelle organization]과 네트워크로 연결되어 기관 형성 관련 기작의 발현에 이용되는 것으로 분석되었다.
결론적으로 저온 스트레스 발생 시 배추에서 일어나는 주요 기작을 경과 시간 순서에 따라 정리하면, 먼저 저온 처리 초기인 30분 경과 후에는 저온 스트레스에 의해서 ethylene- responsive transcription factor(ERF) 유전자군과 chitinases- AFP에 의한 저온 저항성 획득 기작이 활성화되고, 3시간 경과 후에는 WRKY 전사인자와 자스몬산 및 칼슘에 의한 신호가 증폭되어 전달되게 된다. 다음으로 12시간 경과 후에는 앞서 활성화된 신호가 식물체에 전신적 획득저항성을 작동시키고, 기공을 닫고 당을 축적함으로써 저온 저항성을 획득한다. 24시간 경과 후에는 증가된 당에 의해 광합성 효율 및 안토시아닌 합성이 증가하고 저온 저항성 유전자가 작동하기 시작한다. 끝으로 48시간 경과 후에는 다양한 저온 저항성 관련 유전자가 발현될 뿐만 아니라, 식물체가 영양 생장에서 생식 생장으로 전환하는 것으로 분석되었다(Fig. 3).
본 연구로 제시된 네트워크는 배추의 저온 스트레스에 따른 유전자 발현 변화를 확인함으로써 배추에 대한 저온 저항성 및 저온 감응 현상 대한 이해를 증진시킬 수 있을 것이며, 저온 스트레스 저항성 유전자를 대량 발굴하여 유용 GM 작물 개발에 이용될 수 있을 것이다.