서 언
재료 및 방법
실험 재료 및 시료 채취
수확 기준 설정
과실 품질 분석
형태학적 특성 관찰
통계분석
결과 및 고찰
과실 발달 및 수확 시기
생육 단계에 따른 과실의 세포 비대 양상
생육 단계에 따른 과경 유관속 조직의 발달
생육기별 과실 품질
서 언
포도의 과실 발달은 2중 S자형 생장 곡선 형태를 나타내며, 각 생육기별 세포 수, 크기, 형태 및 기간은 성숙에 차이를 나타내어 이는 곧 과실 품질을 결정하는 중요한 요인이 되기도 한다C(oombe and McCarthy, 2000; Dokoozlian, 2000).
과실의 크기는 세포 수와 세포 비대에 의하여 결정되며(Bain and Robertson 1950; Johnson et al., 2011), 복숭아와 올리브의 과실 크기는 세포분열율에 크게 영향을 받는다(Scorza, 1991; Hammami et al., 2011). 또한 Bain and Robertson(1951)은 과실의 크기가 비슷한 품종에서 조생종의 경우 세포수가 많고 만생종의 경우 세포의 용적이 큰 경향을 나타내었으며 사과의 생육 중 호흡율을 비교하였을 때 호흡율이 더 높은 사과에서 용적이 크고 품질이 떨어진다고 보고하였다. 이와 같은 세포의 특징적 차이로 인해 세포의 형태 및 구조가 달라지며 이는 과실의 성숙과 연화에 직접적으로 영향을 미친다(Ortega-Regules et al., 2008; McAtee et al., 2009; Jovyn et al., 2013).
과실의 세포 수와 크기는 온도, 적과, 저장 양분의 이동 등에 영향을 받으며(Bertin et al., 2001; Rosati et al., 2011), 과경의 유관속 조직 역시 크게 영향을 미치는 것으로 보고되었다C(heng and Breen, 1992; Keller et al., 2006).
‘흑보석’ 포도는 착색이 우수하고 열과가 적어 ‘거봉’의 단점을 보완 할 수 있는 품종으로 재배 지역이 확대되고 있으나 수확기에 과립이 쉽게 물러져 상품성 저하의 원인이 된다. 따라서 본 실험에서는 같은 4배체 품종으로 성숙기에도 과실이 물러지지않는 ‘자옥’과 ‘흑보석’ 포도의 생육 특성 및 과실과 과경의 해부학적 연구를 통하여 두 품종의 생리적 특성을 구명하고자 한다.
재료 및 방법
실험 재료 및 시료 채취
경기도 천안시 입장면 소재의 포도원에서 5년생 ‘흑보석’ 포도와 4년생 ‘자옥’ 포도를 대상으로 실험을 실시하였다. 목표 수량 설정은 990m2당 1800kg으로 착과량을 설정하고 한 과립당 10.5g을 기준으로 450g 이내로 과방중을 조절하였다. 생육기별 해부학적 관찰을 위한 시료 채취는 만개기부터 수확기까지, 과실 품질을 위한 시료 채취는 만개 후 30일부터 수확기까지 10일 간격으로 1나무당 3송이씩 무작위로 채취하여 실험실로 즉시 가져와 분석하였다. 각 처리구는 1주를 1반복으로 하여 3반복으로 실시하였으며 총 6주의 포도나무를 사용하였다.
수확 기준 설정
수확은 관행수확기를 기준으로 조기 수확, 관행 수확, 지연 수확으로 구분하여 3차에 걸쳐 수확하였으며 조기 수확(1차)과 관행 수확(2차)의 숙기 판정은 국립특작과학원에서 개발한 ‘거봉’ 포도 숙기 판정용 칼라차트(농촌진흥청)을 기준으로 과피색이 9등급 이상의 과실을 수확하고 지연수확(3차)은 전량 수확하였다.
과실 품질 분석
생육기별 과실의 외적 특성을 조사하기 위해 생육 단계, 과방중, 과경의 직경 등을 측정하였다. 경도는 과립의 적도 부위의 과피를 얇게 벗겨낸 후 texture analyzer를 이용하여 직경이 2mm인 탐침으로 2mm·s-1의 속도로 5mm의 깊이까지 압축강도(N)를 측정하였다. 가용성고형물(SSC)은 디지털 굴절 당도계(Atago Corp., PR-32 Japan)를 사용하여 측정하였고 산 함량은 과즙과 증류수의 비율을 1:4(v:v)로 희석하여 pH가 8.1이 될 때까지 NaOH(0.1N)로 적정한 후 tartaric acid의 상당량으로 환산하였다. 안토시아닌 함량은 무작위로 과립을 선발해 1.1cm 크기의 과피 disk 10개를 cork borer를 사용하여 만들었다. 이 disk는 HCl(0.1N)과 MeOH(100%)를 15:85(v:v)의 비율로 혼합한 용매에 12시간동안 암처리하여 침출한 후 spectrophotometer(UV-1240, Shimadzu, Japan)를 사용하여 흡광도(530nm)를 측정하였다. 측정된 값은 Siegelman and Hendricks(1958)의 방법으로 환산하였다.
형태학적 특성 관찰
해부학적 특성 조사는 포도원에서 즉시 실험실로 가져와 과립과 과경을 2mm 크기로 채취한 후 2중고정법을 이용하여 고정하였다. 1차 고정은 2.5% glutaraldehyde, 2차 고정은 1% osmic acid를 이용하여 세포조직을 안정적으로 고정시킨 후 40-100%의 에탄올을 사용하여 순차적으로 탈수하였다. 완전히 탈수된 시료는 propylene oxide(100%)와 epon 용액에 각각 2:1, 1:1 비율에 약 60분 이상 침지 하여 점진적으로 포매제와 잘 섞일 수 있게 치환하였다. 치환된 시료는 epon 용액 내에서 overnight 하여 세포 사이사이에 포매제가 완전히 채워질 수 있도록 하였다. 다음날 DMP-30(경화촉진제)이 첨가된 epon 용액에 시료를 넣은 후 60°C에서 4일간 silicon mold에서 block을 제작하였다. 이 block은 ultramicrotome(PT-X, RMC, USA)으로 1000nm로 자른 후 슬라이드 글라스 위에 올린 뒤 PAS(periodic acid-Schiff) 염색법을 이용하여 염색하였다. 염색된 시료는 광학현미경(BX51, Olympus, Japan)으로 촬영한 후 과립과 과경 유관속 조직의 시기별 세포 발달을 관찰하였다 .
통계분석
수집된 데이터는 PASW statistics 18(SPSS Inc., USA) 프로그램으로 t-test (p ≤ 0.05, 0.01)로 유의성을 검정하였다.
결과 및 고찰
과실 발달 및 수확 시기
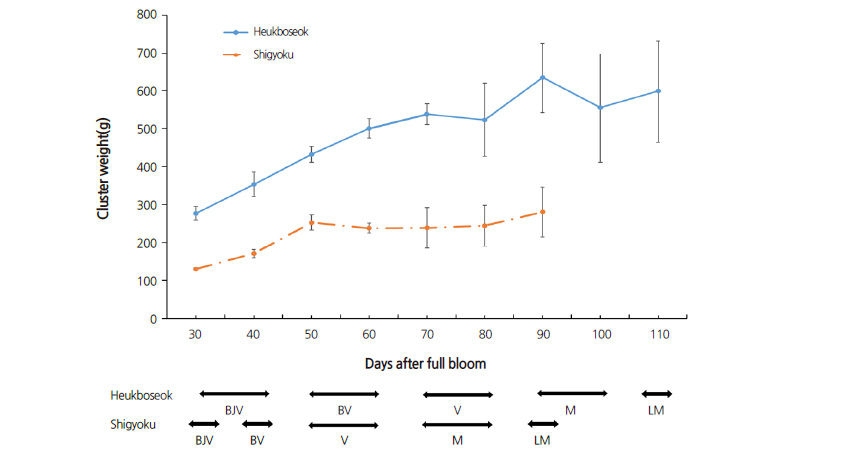
‘흑보석’ 포도의 변색기는 만개 후 70-80일 사이이며 ‘자옥’의 변색기는 만개 후 50-60일 사이로 조생종인 ‘자옥’ 포도의 변색기가 ‘흑보석’ 포도에 비하여 약 20일 가량 빠른 것으로 조사되었다. 수확기 또한 ‘자옥’ 포도는 만개 후 70일부터 1차 수확이 가능하였으며 ‘흑보석’ 포도는 만개 후 90일부터 수확이 가능하였다. 과실 비대는 ‘흑보석’ 포도는 변색기 전후 모두 급격한 비대 양상을 보여 전형적인 2중 S자 곡선 형태를 나타내었으나 ‘자옥’ 포도는 변색기 이전에 급격한 증가를 보인 후 수확기까지는 변화가 미미하여 2차 과실 비대가 크지 않은 특징을 나타내었다(Fig 1). ‘자옥’과 ‘흑보석’ 포도 수확기의 평균 안토시아닌 함량은 각각 0.0701μg·cm-2, 0.0713μg·cm-2로 육안으로 두 품종간 색의 차이가 확연 함에도 불구하고 통계적 유의성이 나타나지 않은 이유는 두 품종의 안토시아니딘의 조성에 의한 차이일 것으로 생각되나(Kwon and Park, 2015) 이에 대한 분석이 더 필요할 것으로 생각되었다. 따라서 ‘자옥’과 ‘흑보석’ 포도는 생장 기간에 있어서 시기적 차이가 관찰되며 품종에 따른 성숙 일수의 차이를 뚜렷이 나타내었다. 또한 유핵재배시 ‘흑보석’ 포도에 비해 ‘자옥’ 포도의 소립과 생산이 두드러져 시기별 수확율에 영향을 미쳤으나 수확된 과실의 안토시아닌 함량은 비슷하여 착색 불량은 나타나지 않은 것으로 판단되었다 .
| |
Fig. 1. Seasonal changes in cluster weight of ‘Shigyoku’ and ‘Heukboseok’ grapes. JBV: just before veraison; EV: early veraison; V: veraison; M:m aturity; LM: late maturity | |
| |
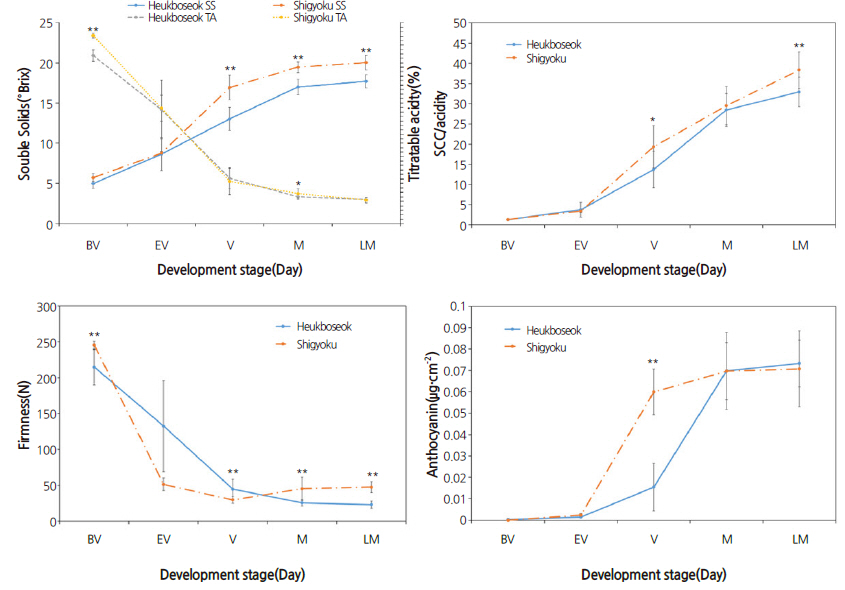
Fig. 2. Seasonal changes in fruit quality and anthocyanin content of ‘Shigyoku’ and ‘Heukboseok’ grapes. *, **(significant difference between varieties p ≤ 0.05, 0.01. respectively). | |
생육 단계에 따른 과실의 세포 비대 양상
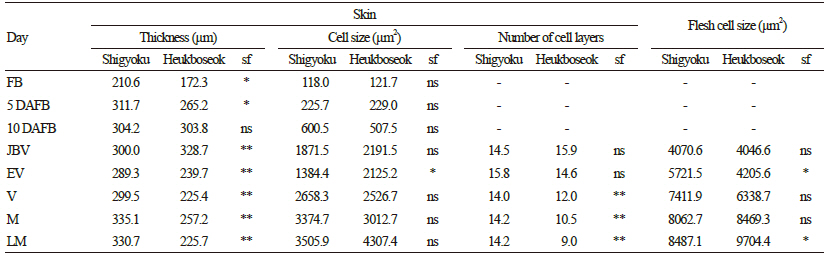
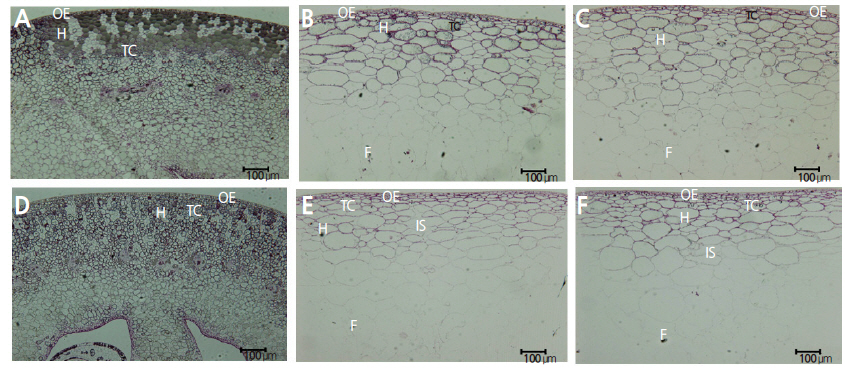
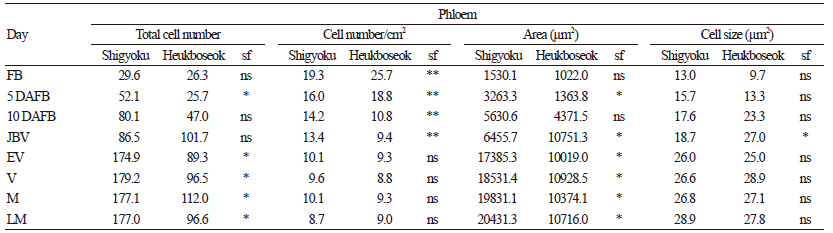
과실의 생장은 세포 분열과 세포 비대에 의해서 형성되는데 포도의 세포분열기는 착과 후 약 2주간 진행된다는 보고에서처럼(Fougere-Rifot et al., 1997) 만개기부터 만개 후 10일까지는 세포 분열과 비대가 함께 일어나며 세포 분열이 더 지배적인 것으로 관찰되었다. 이 시기의 세포 크기는 ‘자옥’과 ‘흑보석’ 포도 각각 118.0~600.5μm, 121.7~507.5μm로 두 품종간 통계적 유의성은 없었다(Table 1). 또한 만개 후 10일까지는 아표피층과 과육의 구분이 되지 않아 과육 조직의 분화가 이루어지지 않은 것으로 나타났으며(Fig. 3A, 3D), 이는 Park et al.,(2013)이 ‘만풍배’의 과실 구조에서 세포분열기에 세포의 분화가 완전하지 않아 아표피와 과육 조직을 형태적으로 구분하는 것이 불가능하다고 보고한 연구와 유사한 결과를 나타내었다. 만개기와 만개 후 5일의 표피층부터 유관속까지의 두께는 ‘자옥’ 포도가 각각 210.6, 311.7μm, ‘흑보석’ 포도가 172.3, 265.2μm로 ‘자옥’ 포도가 약간 두꺼웠으나 만개 후 10일에는 각각 304.2, 303.8μm로 비슷하였다. 아표피층과 과육이 구분되는 만개 후 30일부터 성숙기까지 ‘자옥’ 포도의 과피를 구성하는 외표피와 아표피 세포층의 수는 크게 변화가 없었으나 ‘흑보석’ 포도의 과피의 세포 층수는 15.9층에서 9.0층으로 크게 적어지는 것으로 나타났다(Table 1, Fig. 3C, 3F). 또한 ‘흑보석’ 포도의 세포 크기는 적정 수확기 이후에도 계속 증가되어 수확이 지연될 수록 ‘흑보석’ 포도는 큰 세포와 적은 세포 수로 과피가 형성됨을 알 수 있었다. 반면에 ‘자옥’포도는 과피를 구성하는 세포수가 만개 30일 이후 거의 변화가 없고 적정 수확기 이후에도 세포의 비대가 크지 않아 수확기간 내내 과피가 두껍게 유지되는 것으로 조사되었다(Table 1). Fougere-Rifot et al.,(1997)은 변색기 이후 일부 아표피 세포가 세포벽이 얇아지면서 아표피 세포의 특성을 잃고 과육 세포로 전환되어 포도의 아표피 세포 층수는 계속 감소하며 이는 품종에 따라 정도의 차이가 있다고 하였다. 본 실험에서도 ‘흑보석’ 포도는 아표피 세포가 생육이 진전되는 동안 계속 과육 세포로 변하는 것으로 나타났으나 ‘자옥’ 포도는 아표피 세포들이 계속 유지되는 것으로 조사되어 품종간에 차이를 보였다. 과육 세포의 크기는 ‘자옥’ 포도에서 만개 후 30일부터 변색기인 만개 후 60일까지 4070.6μm2에서 7411.9μm2로 증가하였으나 그 이후에는 세포 크기의 증가는 나타나지 않았다. 반면 ‘흑보석’ 포도는 만개 후 30일부터 변색기인 80일까지 과육 세포의 크기가 4046.6μm2에서 6338.7μm2로 점진적으로 증가하였고 변색기 이후에도 세포 비대가 계속되어 만개 후 100일과 110일에는 8469.4, 9704.4μm2로 ‘자옥’ 포도에 비해 세포의 크기가 큰 것으로 확인되었다(Table 1). 이는 Bain and Robertson(1950)이 조생종 사과에 비해 만생종 사과에서 용적이 큰 세포를 가진다는 보고와 일치하였으며, 용적이 큰 세포는 생육기간 중 높은 호흡율을 가져 과실 연화를 촉진한다고 하였다.
생육 단계에 따른 과경 유관속 조직의 발달
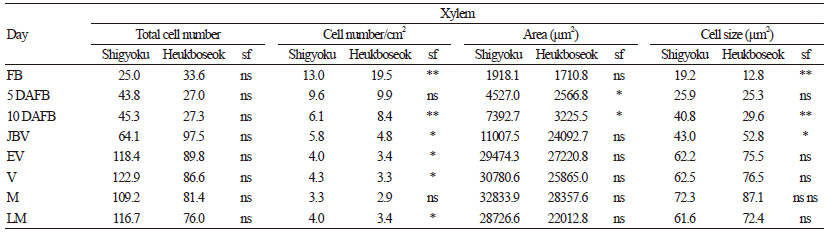
‘자옥’과 ‘흑보석’ 포도의 과경 유관속조직은 유관속형성층을 중심으로 바깥쪽에는 체관부, 안쪽에는 물관부가 형성되며 둥근 통 모양으로 세포들이 분열하여 유관속조직을 구성하였다(Fig. 4). ‘자옥’과 ‘흑보석’ 포도의 체관부의 세포 크기는 각각 13.0~28.9μm2, 9.7~28.9μm2로 비슷한 범위 안에 있었으며 물관부의 세포 크기는 각각19 .2~72.3μm2, 128~87.1μm2로 변색기 이후 ‘흑보석’ 포도가 수치적으로 약간 크지만 통계적 유의성은 없었다. 반면에 변색기 이후 체관부의 세포 수는 ‘자옥’ 포도의 체관부 세포수가 평균 177.1개로 ‘흑보석’ 포도의 평균 98.6개에 비해 약 1.8배 정도 많으며 특히, 두 품종 모두 초기 변색기 이후 체관부 세포수의 격차가 뚜렷해 지는 것으로 관찰되었다. 이에 따라 ‘자옥’과 ‘흑보석’ 포도의 변색기 이후 과경의 체관부 면적도 각각 평균 19044.8μm2, 10509.4μm2로 조사되었으나, 1cm2당 세포 수에서 변색기 이후 유의성이 나타나지 않아 체관부의 면적은 세포 크기 보다는 세포 수에 의한 영향임을 확인할 수 있었다. 물관부를 구성하는 단위면적당 세포 수는 ‘자옥’ 포도에서 약간 많은 것으로 나타났으나 전체 세포 수와 세포 크기에서 통계적 유의성이 인정되지 않아 ‘흑보석’ 포도와 ‘자옥’ 포도의 물관부 세포 크기는 큰 차이가 없는 것으로 조사되었다. 또한 과경의 체관부와 물관부를 구성하는 세포 수와 면적은 ‘자옥’과 ‘흑보석’ 모두 초기 변색기까지 점점 증가하다가 변색기 이후부터는 일정한 경향이 나타나지 않았다(Table 2, 3 and Fig. 4). 포도에서 성숙이 시작될 때 체관부로부터 용질의 유입은 증가하고 물관부의 수분 유입은 감소하여 물관부를 통해 모체로 backflow 한다. 이때 과실 세포는 부피를 유지하기 위하여 체관부의 용질을 더 유입하게 하여 과실 세포에 더 농축된 당을 축적하게 된다. 그러나 가뭄 등에 의한 물관부의 backflow가 원활하지 않을 경우 잎의 광합성 활동이 약해지며 당의 축적에 의한 과립의 발달이 억제되어 과립이 쪼그라드는 현상을 나타내며(Bondada et al., 2005; Chatelet et al., 2008; Keller et al., 2015), 이와 같은 연구결과는 키위를 통해서도 확인되었다(Morandi et al., 2010; Clearwater et al., 2012,). 따라서 체관부와 물관부 각각의 역할에 따라 당의 축적이 향상되며 ‘자옥’ 포도가 체관부 면적이 ‘흑보석’ 포도에 비해 커 sink 기관의 능력이 활발할 것으로 생각되어 당의 축적은 더 효과적일 것으로 생각되었다 .
생육기별 과실 품질
‘자옥’과 ‘흑보석’ 포도의 가용성 고형물은 변색기부터 축적되는 것으로 조사되었다(Fig. 2). 성숙이 진행됨에 따라 착색에 근거한 수확 시기와 관계없이 가용성 고형물 함량은 ‘자옥’에서 18.4, 19.8, 20.4°Brix, ‘흑보석’은 16.3, 17.2, 17.7°Brix로 계속 증가하였다. 이는 Jung et al.,(2014)이 ‘흑보석’ 포도에서 착색과 무관하게 성숙이 진행될수록 당 함량이 증가한다는 보고와 일치하였으며 착색이 좋은 ‘흑보석’ 포도의 조기 수확시 과피색 만을 보고 수확할 경우 당의 함량이 낮은 과실을 수확할 수 있다는 기존 보고를 확인하였다. 한편 ‘자옥’ 포도의 경우 변색기 이후 ‘흑보석’ 포도에 비해 가용성 고형물의 증가 양상이 높아 품종간 유의성이 인정되었다(Fig. 2). Cheng and Breen(1992)은 딸기에서 과경의 세포 수에 따라 각 품종의 과실의 크기가 달라짐을 보고하였으며, Keller et al.,(2006)은 포도에서 과경 유관속 조직의 세포 활동이 원활하지 않을 경우 과실이 쉽게 물러지거나 쪼그라지는 현상을 보고하였다(Keller et al., 2006). 본 실험에서도 ‘흑보석’ 포도에 비해 ‘자옥’ 포도의 가용성 고형물 함량이 높은 것은 체관부의 면적 차이에 따른 당의 이동이 영향을 미쳤을 것으로 생각되었으나 이에 대한 연구는 다양한 품종을 대상으로보다 깊은 연구가 필요할 것으로 생각되었다. 산도는 당도의 증가와 반비례의 양상을 나타내며 수확기의 두 품종간의 차이는 없는 것으로 조사되었다(Fig. 2). 당산비는 두 품종 모두 산도가 낮아짐에 따라 증가하였지만 성숙이 진행될수록 ‘자옥’ 포도의 당도가 더 높아 당산비가 크게 증가하여 적정수확기부터는 품종간 유의성이 인정되었다 .
경도는 ‘자옥’ 포도의 경우 변색 초기, ‘흑보석’ 포도의 경우 변색기까지 급격한 감소를 나타내다가 성숙단계부터는 감소 양상이 완만해 지지만 ‘자옥’과 ‘흑보석’의 감소 차이는 고도의 유의성이 인정되는 것으로 조사되었다. 수확시기별 경도에서 ‘자옥’ 포도는 평균 45.9N으로 ‘흑보석’ 25.0N 비해 1.8배 높게 조사되었으며 성숙이 진행될수록 ‘흑보석’ 포도의 경도가 점차적으로 감소하여 지연수확기에는 22.9N으로 낮아졌으나 ‘자옥’ 포도는 변색기 이후 비슷한 경도를 유지하는 것으로 조사되었다(Fig. 2). 이는 ‘자옥’ 포도의 아표피층의 두께가 두껍고 성숙이 진행되어도 감소하지 않는 것이 원인으로 생각되며, Jung et al.,(2015)은 ‘흑보석’ 포도에 생장조절제를 처리 할 때 아표피층 세포의 비대로 늦은 성숙기까지 경도를 유지할 수 있다고 보고하여 유사한 결과를 나타내었다. 경도의 감소는 세포벽의 middle lamella층이 분해되면서 과육의 연화가 일어나는 현상으로 ‘자옥’ 포도에서 가용성 고형물 함량과 경도가 높은 것은 체관부의 면적이 ‘흑보석’ 포도에 비해 커 당의 축적에 더 유리했기 때문일 것으로 생각된다.
따라서 ‘흑보석’ 포도는 ‘자옥’ 포도에 비해 유관속 조직의 발달이 미흡하여 체관부를 통한 가용성 고형물의 이동이 ‘자옥’ 포도에 비해 제한적인 것으로 생각되며, 이는 ‘흑보석’ 포도의 과실이 성숙이 진행될수록 세포벽의 분해로 인한 과실 연화를 촉진하여 과실이 물러지는 것으로 판단되었다.