서 언
발광다이오드(light-emitting diodes, LED)는 소형으로서, 높은 신뢰성과 응답성을 지니고 있으며, 전력소모가 낮고, 수명이 길며, 광합성속도에 영향을 미치는 펄스 조사가 가능한 점 등의 장점을 지니고 있다(Barta et al., 1992; Kim, 1999; Tennessen et al., 1995). 때문에 LED를 식물조직배양(Eun et al., 2000), 과채류의 보광재배(An et al., 2011; Brown et al., 1995; Lee et al., 2012), 접목묘의 활착(Kim and Park, 2003), 식물공장 또는 폐쇄형 식물 생산시스템의 인공광원(Johkan et al., 2010)으로 활용하기 위한 연구가 활발하게 이루어지고 있다.
작물 생장에 적합한 파장을 선택적으로 조사할 수 있으며, 근접 조명이 가능할 것으로 기대되는 LED는 피크파장이 630-670nm에 포함되는 적색광 영역과 430-470nm에 속하는 청색광 영역 가운데 특정 파장의 LED가 주로 사용되고 있다(An et al., 2011; Johkan et al., 2010; Lee et al., 2010; Xu et al., 2012). 이것은 적색광 또는 청색광 영역의 LED 가운데 작물별로 생장 촉진에 적합한 파장을 실험 결과에 기초하여 결정하기보다는, 적색광 또는 청색광 LED를 작물 재배에 이용하려는 수요자로부터 요청을 받은 LED 조명기구 제조업자들이 디스플레이 용도의 LED 모듈(module) 중에서 비교적 저렴한 가격으로 손쉽게 구할 수 있는 파장의 모듈을 이용한 결과로 판단된다. 이로 말미암아 작물의 생장, 형태형성 또는 기능성성분에 미치는 LED의 광질 효과를 분석하기 위한 다른 시도에서도 적색광 또는 청색광 영역에서 연구 목적에 적합합 파장의 LED가 선택되지 않고 있다. 또한 공시작물이 다를지라도 여전히 기존 연구에서 많이 사용되고 있는, 즉 피크파장이 660nm인 적색광 또는 450nm인 청색광 LED가 인공광원으로 사용되면서 적용된 LED와 작물 생장의 단순 인과관계 해석에만 치중된 연구가 수행되고 있다. 때문에 작물의 종류에 따른 생장 촉진 또는 기능성성분의 증대에 적합한 LED의 피크파장이 제시되지 않은 가운데, 실험에 사용된 LED의 처리 효과만 제한적으로 보고되고 있다. 이러한 시도는 작물의 생장 촉진과 기능성성분의 증대에 효과적인 LED를 개발하는 데 있어서 적합하지 않을 뿐만 아니라 오히려 발열 저감, 수명 연장 등 LED의 안정성을 향상시키는데 부정적인 요인으로 나타나고 있다. 작물의 생장 촉진에 적합하지 않은 파장의 모듈로 제조되거나, 광량이 부족하게 설계된 LED에 공급전류를 과도하게 공급하는 방식으로 광량을 무리하게 증가시킬 경우 LED의 수명이 빠르게 저하될 수 있다(Lee and Kim, 2012). 그러므로 칩 수준에서 50,000h 정도의 수명을 갖는 것으로 알려진 LED의 수명을 제대로 유지하려면 적극적인 방열 설계와 LED 조명기구에 대한 냉각이 요구된다(Park et al., 2011).
식물체의 잎에는 엽록소, 카로티노이드, 안토시아닌 등의 다양한 색소가 분포되어 있다. 그런데 생육 단계에 따라 주도적으로 발현되는 색소의 종류가 달라 엽색 또한 다르게 나타난다. 식물체의 광합성 반응에 절대적으로 필요한 색소인 엽록소는 생장이 활발하게 이루어지는 시기에 잎의 세포에 다량으로 존재하므로 식물체가 녹색을 띄게 된다. 이때 카로티노이드 또는 안토시아닌 등과 같은 색소는 엽록소에 의해서 가리워져 주황색, 적색 또는 자주색 등과 같은 고유의 색을 나타내지 못한다. 안토시아닌은 식물의 천연색소를 구성하는 파이토케미컬(phytochemicals)의 한 종류로서, 과일, 채소, 꽃 등에 많이 포함되어 있는 플라보노이드(flavonoids)계의 수용성 물질이다. 수소이온농도에 따라 적색 또는 자색을 나타내는 안토시아닌의 발현 기작은 매우 복잡하여, 유전적 요소뿐만 아니라 여러가지 환경 조건에 의해서도 크게 좌우된다(Oren-Shamir, 2009). 엽록소와 카로티노이드는 식물체의 전체 생육 과정에 존재하나, 안토시아닌은 환경 변화에 의해서 발현된다. 이 가운데 광환경은 안토시아닌을 비롯한 파이토케미컬의 생성과 발현을 촉진하는 데 있어서 효과적인 환경 요인으로 알려져 있다(Li and Kubota, 2009; Ninu et al., 1999). 세포가 노화되는 과정에서 발생하는 활성산소를 제거하는 능력이 뛰어난 안토시아닌의 항산화 작용(Kong et al., 2003)이 알려지면서 안토시아닌이 기능성물질로 주목받고 있다. 때문에 상추류의 기능성 물질에 미치는 인공광원의 조명 효과가 부분적으로 보고되고 있으나(Lee et al., 2010; Park et al., 2012; Son et al., 2012), 안토시아닌의 함량을 증진시키는데 효과적인 광질 선발에 관한 연구는 미흡한 실정이다. 특히 작물의 생장을 촉진하거나 기능성성분을 증진시키는 데 적합한 적색광과 청색광의 피크파장이 다를 것으로 예상되나, 적색광 또는 청색광 영역을 세분화한 파장이 작물의 생장 또는 안토시아닌 함량에 미치는 효과에 대한 정량적인 실험 결과가 아직까지 보고되지 않고 있다.
본 연구의 목적은 엽채류의 생장 촉진과 파이토케미컬의 증진에 적합한 조명시스템 개발에 필요한 기초 자료를 제공하고자 630-670nm의 적색광 영역과 430-470nm의 청색광 영역을 5nm 간격으로 세분화한 LED를 인공광원으로 사용한 가운데 상추의 생장 및 안토시아닌 축적에 효과적인 적색광과 청색광 영역의 피크파장을 제시하는 데 있다.
재료 및 방법
실험재료
630-670nm의 적색광 영역과 430-470nm의 청색광 영역을 5nm 간격으로 세분화한 LED 모듈(Luxpia Co., Ltd., Korea)로 만들어진 LED 조명 하에서 생장된 상추의 생장 특성과 안토시아닌 함량을 분석하고자 적치마상추(Lactuca sativa L. ‘중생종’, 흥농씨앗)를 공시재료로 사용하였다.
200셀의 플러그트레이(Bumnong Co., Ltd., Korea)에 피트모쓰, 펄라이트 및 버미큘라이트가 70:5:25(v/v)의 비율로 혼합된 상토(BM2, BergerPeat Moss Co., Ltd., Canada)를 채운 후 상추 종자를 1립씩 파종하여 폐쇄형시스템에서 14일간 육묘하였다. 육묘 조건은 기온 22°C, 습도 70%, 광주기 16/8h(명기/암기), 광합성유효광양자속(photosynthetic photon flux, PPF) 200μmol・m-2・s-1이었다. 본엽이 3매일 때 직경 100mm의 포트에 육묘 과정에 사용된 동일한 상토를 충전한 후 1주씩 정식하였고, 각 처리구당 15 × 15cm 간격으로 21개의 포트를 배치하였다. 정식 직후부터 각 포트에 설치된 드리퍼를 통해서 엽채류 배양액(N-P-K-Ca-Mg = 0.8-2.0- 6.0-3.0-2.0mg・L-1, pH 6.0, EC 1.5dS・m-1)을 매일 200mL (40mL × 5회)씩 공급하였다. 폐쇄형시스템 내의 환경조건은 광주기 16/8h, 기온 22/18°C, 습도 70%, CO2 농도 400 μmol・mol-1로 설정하였고, 베드 면에서의 PPF가 201 ± 2 μmol・m-2・s-1를 유지하도록 각 처리구의 LED 조명기구에 연결된 SMPS(SP-320-48, Mean Well, Taiwan)를 이용하여 광양을 조절하였다.
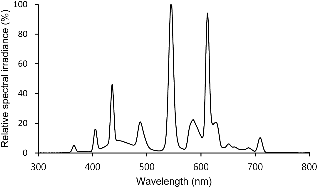
폐쇄형 식물 생산시스템(이하 ‘폐쇄형시스템’) 내에 설치된 처리구 B1-B8은 430-470nm의 청색광 영역을 피크파장에 따라 5nm 간격으로 구분한 것이고, 처리구 R1-R8은 630-670nm의 적색광 영역을 5nm 간격으로 구분한 것이다(Table 1). 한편 색온도가 4,000K인 냉백색형광등(DULUX L55W/840, Osram, Germany)이 대조구로 사용되었다(Fig. 1).
생장조사
MATLAB(R2011b, MathWorks Inc., USA)의 랜덤함수를 이용하여 처리구당 5주씩 임의로 선택된 상추를 대상으로 정식 후 11일째와 21일째에 생장조사를 수행하였다. 처리구별 상추의 생장특성으로 엽수, 엽장, 엽폭, 엽록소 함량, 엽면적, 엽색, 지상부 및 지하부의 생체중 및 건물중, 광합성속도를 조사하였다. 3번째 본엽에 대한 엽록소 함량은 엽록소 측정기(SPAD-502, Minolta Co., Japan)를 사용하여 측정하였고, 엽면적은 CCD 카메라(VK-C370, Hitachi, Japan)로 측정된 상추 잎의 영상에 기지의 물체 면적과 화소수 사이의 회귀관계를 적용하여 계산하였다. 엽색의 측정에 색채색차계(CR-200, Minolta Co., Japan)가 사용되었다. 이제까지 식물체의 엽색을 표시할 때 Lab 좌표계로 측정된 a 또는 b 값이 주로 사용되었다. 그런데 a, b 값은 각각 적색과 녹색 사이의 정도, 황색과 청색 사이의 정도를 표시하므로 측정하고자하는 물체 본래의 색상을 표시하는 값으로는 적합하지 않다. 한편 식 (1)과 식 (2)에 의해서 정의되는 색상(hue)과 채도(saturation)가 본래의 엽색과 순도를 의미하므로 엽색을 비교할 때 a, b 값 대신에 hue, saturation 값의 사용이 바람직하다. 이때 색상은 색좌표계 기준 축으로부터의 각도를 표시하고, 채도는 좌표계 원점으로부터의 거리에 해당된다. 지상부와 지하부를 구분된 상추의 생체중과 건물중의 측정에 전자저울(SBA51, Scaltec Instruments, Germany)을 이용하였다. 건물중의 측정에 사용된 시료는 기온이 70°C로 유지되는 오븐(ON-21, Jeio Tech, Korea)에서 3일간 건조되었다. 상추의 광합성속도는 정식 후 21일째에 기온, 상대습도, PPF 및 CO2 농도가 각각 22°C, 70%, 201μmol・m-2・s-1, 400μmol・mol-1로 조절되는 폐쇄형시스템 내에서 상추의 3번째 본엽을 대상으로 휴대용광합성측정기(LCi, ADC Bioscientific Co., UK)를 사용하여 측정하였다.
Hue=tan-1(b/a) (1)
Saturation=(a2+b2)1/2 (2)
안토시아닌 함량 분석
상추 잎의 안토시아닌 추출을 위하여 정식 후 21일째에 각 처리구 당 생체중 5g을 3반복으로 채취하였다. 채취된 상추를 막자사발을 이용하여 마쇄한 후 시료 500mg을 채취하여 95% ethanol과 1.5N HCL을 85:15(v/v)로 혼합하였다. 혼합한 추출액을 4°C 암조건 하에서 16시간 shaking한 후 13,000rpm에서 20분간 원심분리하였다. 원심분리로 얻은 상징액을 흡광도계(SpectraMax M2 Microplate Reader, USA)를 사용하여 530nm와 680nm에서 흡광도를 산출하였으며, 이것에 기초하여 안토시아닌 함량을 산출하였다(Fuleki and Francis, 1968).
통계처리
상추의 생장 특성 및 안토시아닌 함량을 분석하고자 SAS 프로그램(V9.3, SAS Institute Inc., USA)을 이용하여 분산분석을 하였으며 최소유의차 검정으로 5% 수준에서 각 처리간의 유의성을 검증하였다.
결과 및 고찰
상추의 엽수, 엽장, 엽폭, 엽면적 등 지상부 생장 특성은 본 실험에서 적용된 청색광 또는 적색광 영역의 LED에 따라 유의차가 인정되었다. 정식 후 21일째에 적색광 처리구에서의 엽수는 대조구와 비교할 때 유의차가 인정되지 않았으나, 청색광 영역의 처리구에서는 모두 작게 나타난 가운데 유의차가 인정되었다. 적색광 또는 청색광 영역의 피크파장 조사가 상추의 엽장에 미치는 영향은 크지 않았다. R8 처리구(피크파장 668nm), B2 처리구(피크파장 436nm) 및 B4 처리구(피크파장 446nm)를 제외한 나머지 처리구에서의 엽장은 대조구에 비해서 크게 나타났다. 엽폭은 적색광 영역의 처리구에서 전체적으로 크게 나타난 가운데 R1 처리구(피크파장 634nm), R2 처리구(피크파장 638nm), R3 처리구(피크파장 644nm) 및 R6 처리구(피크파장 659nm)에서는 대조구보다 크게 나타났다. 한편 대조구와 비교할 때 청색광 처리구의 엽폭은 유의차가 인정되지 않았다. 그러므로 엽폭에 대한 엽장의 상대적인 크기로 정의된 엽형지수가 청색광 영역에서는 1.53, 적색광 영역에서는 1.40으로서 청색광 영역의 처리구에서 크게 나타났다. 이러한 결과는 적색광이 상추의 엽장과 엽폭의 신장을 모두 촉진하였으나, 청색광하에서는 엽폭의 신장이 상대적으로 억제되었음을 의미하는 것이다. 적색광을 많이 포함하고 있는 고압나트륨램프 하에서 생장된 상추의 엽장과 엽폭은 모두 신장되었으나, 청색광을 많이 지니고 있는 메탈할라이드램프 하에서는 엽폭의 신장이 억제되었다(Park et al., 2012). 결과적으로 상추의 엽장과 엽폭의 신장에 적색광의 처리가 모두 효과적이나, 청색광의 처리는 엽장의 신장에만 효과적인 것으로 판단된다.
R1 처리구(피크파장 634nm)에서 상추의 엽면적은 2,559.1 cm2로서 대조구에 비해서 높게 나타났으나, B4 처리구(피크파장 446nm), B2 처리구(피크파장 436nm) 및 B8 처리구(피크파장 466nm)에서는 대조구보다 작게 나타났다. LED의 피크파장이 상추의 엽면적에 미치는 효과는 적색광 처리구에서 전체적으로 높게 나타났고, 청색광 처리구에서는 작게 나타났다. 그러므로 적색광의 처리가 엽면적의 증가에 기여함을 알 수 있다. 본 연구에서 얻어진 상추의 엽면적에 미치는 적색광 또는 청색광 LED의 광질 효과는 이전에 보고된 연구결과(Johkan et al., 2010; Son et al., 2012)와 유사하였다.
지상부 생체중은 대조구에 비해서 작게 나타난 B5 처리구(피크파장 450nm)와 B8 처리구(피크파장 466nm)를 제외하면 유의차가 인정되지 않았다. 지상부 생체중에 미치는 청색광 또는 적색광 영역의 광질 조사 효과는 엽면적의 경우와 유사하게 청색광 영역에서 생체중의 감소 효과가 분명하게 나타났다. 한편 지상부 건물중에 미치는 청색광 또는 적색광 영역의 광질 처리 효과가 지상부 생체중에 비해서 크지 않았으며, 대조구와 비교할 때 유의차가 인정되지 않았다. 이전 연구결과(Yorio et al., 2001)에서 적색광 LED 하에서 생장된 상추의 지상부 건물중은 냉백색형광등에 비해서 작게 나타났다. 적색광과 청색광 처리구에서의 평균 건물율은 각각 3.1%, 3.8%로서 대조구의 3.3%와 비교된다. 적색광 처리구에서의 지상부 생체중이 높게 나타났음에도 불구하고 건물중이 작게 나타난 것은 적색광 영역에서 생장된 상추의 경우 세포의 크기가 증가함에 따라 엽장과 엽폭의 신장이 촉진되면서 세포 내에 수분이 상대적으로 많이 함유되었던 결과로 판단된다. 실제로 적색광 처리구에서의 평균 건물율은 대조구에 비해서 6.0% 작게 나타났다. 한편 청색광 처리구에서의 평균 건물율은 대조구에 비해서 15.2% 높게 나타났다. 이러한 결과는 적색광 처리구에서 생장된 상추에 수분이 상대적으로 많이 함유되어 있음을 의미하는 것이다.
상추 잎의 건물중에 대한 엽면적의 비, 즉 비면적(specific leaf area, SLA)은 적색광 처리구에서 전체적으로 크게 나타났다. 대조구와 비교할 때 R5 처리구(피크파장 654nm)를 비롯하여 R3 처리구(피크파장 644nm)와 R1 처리구(피크파장 634nm)에서 크게 나타났으며, B2 처리구(피크파장 436nm)와 B4 처리구(피크파장 446nm)에서 작게 나타났다. 잎의 비면적이 크다는 것은 잎의 단위무게에 해당하는 엽면적이 높음을 의미하는 것으로서, 비면적이 클수록 잎의 두께가 작음을 의미한다(Johkan et al., 2010). 그러므로 적색광 처리구에서 생장된 상추 잎의 두께가 청색광 처리구에 비해서 얇은 것으로 판단된다.
상추 잎의 광합성속도에 미치는 적색광 영역 처리구의 조사 효과는 대조구와 유사하게 나타난 가운데 R6 처리구(피크파장 659nm)에서 6.21μmol・m-2・s-1로 높게 나타났다. 한편 청색광 영역의 처리구에서는 B5 처리구(피크파장 450nm)와 B8 처리구(피크파장 466nm)에서 작게 나타났다. 상추 잎의 광합성속도는 생장 특성에 커다란 영향을 주는 요소이다. 실제로 상추 잎의 지상부 생체중(FW, g) 또는 지상부 건물중(DW, g)은 광합성속도(Pn, μmol・m-2・s-1)가 증가함에 따라 식 (3)과 식 (4)의 회귀 관계로서 증가하였다.
FW = 21.23 Pn - 15.26
(R2=0.6035) (3)
DW = 0.44Pn + 0.88
(R2=0.6919) (4)
물체의 색상을 나타내는 hue 값은 0-360의 값을 갖는다. 그런데 hue 값이 0(또는 360), 120, 240일 경우 해당 물체의 색상은 각각 적색, 녹색, 청색에 해당한다. 식 (1)에 의해서 계산된 상추 잎의 색상, 즉 hue 값은 R5 처리구(피크파장 654nm)에서 116.4로 대조구에 비해서 높게 나타난 가운데 유의차가 인정되었다. 한편 청색광 처리구에서의 엽색은 모두 대조구에 비해서 작게 나타났다(Table 3). 그러므로 적색광 영역에서 생장된 상추 잎에서의 녹색 발현이 청색광 처리구에 비해서 상대적으로 많이 이루어졌음을 알 수 있다. 채도를 의미하는 saturation는 회색 정도을 나타내는 0에서부터 순수한 색상을 나타내는 100 사이의 값을 갖는다. 따라서 saturation 값이 크다는 것은 물체의 색상이 밝고 순수한 색에 근접함을 의미한다. 적색광 영역에서 생장된 상추 잎의 채도는 45.6-47.4로서 대조구의 42.6보다 높게 나타났으나, 청색광 영역의 처리구에서는 28.1-36.4로서 작게 나타났다. 이러한 결과는 청색광 또는 적색광의 조사에 따라 상추 잎 표면에서 이루어진 색소의 발현과 관련가 있는 것으로 판단된다. 본 연구에서 사용된 공시재료가 적치마상추이기 때문에 생장 과정을 거치면서 잎 표면에 적색의 발현이 자연스럽게 이루어져야 하나, 630-670nm 영역의 적색광 처리구에서는 적색 발현이 거의 이루어지지 않았고 오히려 연한 녹색이 잎 표면 전체에 나타났다. 한편 청색광 처리구에서 생장된 상추 잎에서는 적색 발현이 제대로 이루어졌다(Fig. 2). 이전 연구 결과(Xu et al., 2012)에서 청색광의 조사는 엽색 뿐만 아니라 토마토 과피색의 발현에도 영향을 미친 것으로 나타났다.
적색광과 청색광 영역에서 생장된 상추 잎의 엽록소함량을 비교하고자 휴대형 엽록소계로서 측정된 SPAD 값을 분석하였다. 청색광 영역에서 SPAD 값은 13.4-15.5의 범위로서, B8 처리구(피크파장 466nm)를 제외하면 대조구와 비슷하게 나타났다. 이러한 결과는 상추 잎의 엽록소함량 증가에 466nm보다 짧은 청색광의 조사가 효과적임을 의미한다. 적색광 영역에서의 SPAD 값은 11.3-14.1로서 R4 처리구(피크파장 649nm)를 제외하면 대조구에 비해서 작게 나타났다. 한편 청색광 영역의 처리구와 다르게 적색광 영역의 피크파장이 클수록 SPAD 값이 증가하였다.
상추 잎에 축적된 안토시아닌 함량은 적색광 영역에 비해서 청색광 영역의 처리구에서 매우 높게 나타났다. 청색광 영역에서의 안토시아닌 함량은 41.86-65.35mg・100g-1으로서, 대조구에 비해서 2.4-3.7배 높게 나타났다. 청색광 영역의 피크파장에 따른 안토시아닌 함량은 유의차가 인정된 가운데 B5 처리구(피크파장 450nm)에서 가장 크게 나타났다. 적색광 영역에서의 안토시아닌 함량은 3.38-8.96mg・100g-1으로서, 대조구의 19.2-50.8%로 나타났다. 한편 적색광 LED의 피크파장이 길어질수록 안토시아닌 함량이 증가하는 것으로 나타났다. 적색광 영역에서의 피크파장이 길어짐에 따라 엽록소함량이 증가하였고, 안토시아닌 함량도 증가하는 결과가 나타났는데, 이에 대한 인과관계는 추후 구명되어야 할 것으로 판단한다. 결과적으로 450nm를 포함한 청색광의 조사가 상추 잎의 안토시아닌 생성에 크게 기여한 것으로 판단된다. 페놀계 화합물로서 안토시아닌의 생합성과 관계된 경로에서 청색광 및 자외선(ultraviolet, UV)의 조사가 안토시아닌의 축적에 효과적이라는 보고(Wang et al., 2012; Sponga et al., 1986)가 이어지고 있다. 양배추와 토마토 묘에 인공광을 조사한 실험에서 청색광 수용체인 크립토크롬과 적색광/원적색광 수용체인 피토크롬의 상호작용에 의해서 안토시아닌의 생성이 결정된다고 보고되었다(Mancinelli et al., 1991). 최근에는 제어된 환경하에서 안토시아닌을 합성하고자 식물기내배양 또는 생물배양기를 이용한 최적화가 시도되고 있다(Cormier et al., 1990; Meyer et al., 2002). 이 가운데 UV-A의 연속적인 조사, 페닐프로파노이드(phenylpropanoid)와 플라보노이드 경로에 작용하는 효소를 이용한 당근 또는 고구마의 세포배양에서 안토시아닌의 생성이 향상되었다(Hirner et al., 2001; Konczak-Islam et al., 2000). 그러므로 450nm의 피크파장을 포함한 430-470nm의 청색광 LED의 조사가 안토시아닌과 같은 식물유래의 페놀계 화합물을 합성시키는데 크게 기여하는 광환경 요소임을 알 수 있다.
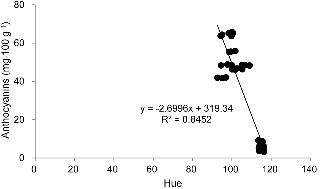
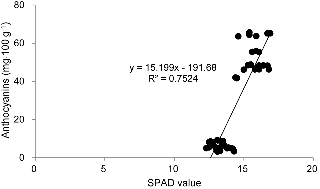
상추 잎의 색상과 SPAD 값이 안토시아닌 함량에 미치는 영향에 대한 선형 회귀관계를 분석하였다. 그 결과 상추 잎의 색상 또는 SPAD 값은 안토시아닌 함량의 변화와 밀접한 관계를 지니고 있었다. 안토시아닌 함량과 엽색의 hue 값 사이의 선형회귀에 대한 결정계수가 0.8542로 나타난 가운데 엽색의 hue 값이 작아질수록 안토시아닌 함량이 증가하였다(Fig. 3). 안토시아닌 함량과 SPAD 값의 선형회귀에 대한 결정계수는 0.7524로 나타났으며, SPAD 값이 커질수록 안토시아닌 함량이 증가하였다(Fig. 4). 그러므로 엽색의 hue 값 또는 SPAD 값을 이용하면 상추 잎의 안토시아닌 함량에 대하 예측이 가능할 것이다. 이러한 결과는 엽색에 미치는 청색광과 적색광 처리 효과에서 예상할 수 있었다. 즉 잎의 표면에서 적색 발현이 제대로 이루어진 청색광 처리구에서는 안토시아닌의 함량이 크게 나타났으나, 적색광 처리구의 경우 적색 발현이 거의 이루어지지 않은 가운데 안토시아닌 함량이 작게 나타날 수밖에 없었다.
식물은 유전자를 통한 신호전달 체계에 의해서 외부로부터의 자극을 신호로 전달하거나 환경 변화를 감지한다. 이와 같이 신호전달에 관여하는 유전자들은 관련된 생화학 반응의 조절 또는 촉매 작용을 위해서 합성된 효소에 의해서 활성화된다(Smith and Gallon, 2001; Yang et al., 1997). 청색광 수용체인 크립토크롬(cryptochrome) 또는 포토트로핀(phototropins)의 반응에는 배축의 신장 억제, 자엽의 전개, 유전자 표현형의 변화 및 엽록체의 발달 유도가 포함된다(Lin, 2002). 한편 피토크롬(phytochrome)은 적색광/원적색광 수용체로서 식물의 발아, 묘종의 발달과 개화에 이르기까지 다양한 생리학적 반응에 관여한다(Botto et al., 1996). 그러므로 식물체에 조사된 광질과 이들을 흡수하는 광수용체의 종류에 따라 작물의 생장 반응이 다르게 나타날 수 있다.
본 연구에서는 430-470nm의 청색광과 630-670nm의 적색광 LED의 피크파장에 따른 상추의 생장 반응과 안토시아닌 함량에 미치는 영향을 분석하였다. 정식 후 21일째에 적색광 또는 청색광 LED의 피크파장에 따라 상추의 생장 특성 및 안토시아닌 함량이 다르게 나타났다. 본 연구에서 처리된 LED의 피크파장 가운데 R1 처리구(피크파장 634nm)와 R6 처리구(피크파장 659nm)가 엽폭, 엽면적, 지상부 생체중 및 광합성속도의 증가에 효과적이었다. 한편 안토시아닌의 축적에 B5 처리구(피크파장 450nm)가 효과적이었다. 상추 잎의 안토시아닌 함량에 미치는 엽색 또는 SPAD 값의 영향은 직선성이 높게 나타났다. 그 결과, 엽색의 hue 값이 작아질수록 안토시아닌 함량은 직선적인 관계를 이루면서 증가하였다. 또한 SPAD 값이 커질수록 안토시아닌 함량이 증가하였다. 상추와 같은 엽채류가 식물공장에 적합한 작물로서 관심의 대상이 되고 있다. 그런데 식물공장의 상업화를 위해서는 재배작물의 생장 촉진뿐만 아니라 작물의 2차대사산물을 증진시키기 위한 적정 피크파장의 선택 및 조명기술의 개발이 병행되어야 한다. 본 연구에서 얻어진 634nm와 659nm의 적색광, 450nm의 청색광은 엽채류의 생산량 증대와 안토시아닌 함량의 증진을 목적으로 한 LED 조명시스템의 개발에 필요한 기초자료로서 활용될 수 있다.