서 언
재료 및 방법
식물재료
흰가루병 저항성 검정
RAPD-BSA 분석
SCAR 및 CAPS 마커 개발
결과 및 고찰
흰가루병 저항성의 유전양상
RAPD-BSA 분석
SCAR 및 CAPS 마커 개발
서 언
딸기(Fragaria × ananassa Duchesne)는 경제적으로 중요한 소득작물 중 하나로 2014년도 기준으로 재배면적은 6,875ha, 생산량은 209,901톤이며, 국내 생산액이 13,106억원으로 우리나라 전체 채소 생산액 84,942억원의 14.7%를 차지한다(MIFAFF, 2015).
딸기는 시설재배와 촉성재배 작형의 증가로 Podosphaera aphanis에 의한 흰가루병(powdery mildew)이 많이 발생되는 경향이다. 딸기 흰가루병 발생은 품종에 따라 차이가 나는데 아끼히메, 매향 등은 흰가루병 발생이 많으며, 다른 품종에 비해 설향 등이 내병성이 강한 품종이다(Kim et al., 2008). 흰가루병이 발생하면 광합성이 감소되고, 심하면 조직의 괴사와 적엽이 일어난다(Mass, 1998). 또한 흰가루병 발생으로 품종에 따라 수확량이 60%까지 손실될 수 있다(Nelson et al., 1995). 딸기 흰가루병은 수확기까지 과실에 발생되어 수확량의 손실을 초래함으로써 농가에 경제적인 피해를 주는 병으로, 현재는 방제하기 위해 주로 농약에 의존하고 있다. 하지만, 수확기까지 약제방제 함으로써 소비자의 구매 욕구를 저하 시킬 뿐만 아니라 안전성이 제기되고 있어 농약 사용을 줄이며 방제효과를 증진시키기 위한 방법의 개발이 필요한 실정이다.
딸기 흰가루병 방제를 위한 효율적인 방법으로는 저항성 품종을 육성하는 것이며, 저항성 계통선발의 정확성과 효율성을 높이기 위해 분자마커 개발이 시도되고 있다(Korbin, 2011; Lifshitz et al., 2008; Yamamoto et al., 2003). 이러한 분자마커를 이용한 목적 형질 보유 개체 또는 계통선발(Marker-assisted selection, MAS)은 특정 형질에 대한 유전자, 또는 유전자와 염색체상 매우 근접한 연관 마커를 개발하여 이를 선발에 직접 이용하는 방법이다. MAS를 이용한 병 저항성 계통 선발방법은 기존 생물검정법으로는 어려운 동형접합자와 이형접합자의 식별, 생육후기 형질의 발현을 탐색할 수 있으며, 농업적으로 중요한 형질의 조기선발이 가능함에 따라 육종 연한과 비용을 효율적으로 감소 시킬 수 있는 기술이다. 분자마커로는 PCR 기법을 이용한 RAPD (Ramdom Amplified Polymorpic DNA)는 가격이 저렴하고 분석이 간편하지만 재현성이 떨어지며, PCR조건에 민감하므로 MAS 적용을 위해 공우성 SCAR(Sequence Characterized Amplified Region) 마커로 전환이 필요하다(Paran et al., 1993). 일반적으로 RAPD 절편 내에 insertion/deletion(Indel)과 같은 염기서열 길이의 변이가 존재하지 않을 경우 SCAR마커에서 다형성이 나타나지 않는 반면, 제한효소 인식부위에 SNP(Single Nucleotide Polymorphism)가 존재할 경우 증폭된 SCAR 산물을 제한효소 처리함으로써 CAPS(Cleaved Amplified Polymorphic Sequences)마커로 전환이 가능하다(Zhang and Stommel, 2001). CAPS 마커는 RAPD마커에 비해 대립 유전자 특이적인 재현성이 높은 공우성 마커이며, SNP에 기반하기 때문에 대량샘플 자동화 분석이 가능한 genotyping platform으로의 변환이 용이하다(Konieczny et al., 1993).
흰가루병은 다른 작물에서도 발생되는 주요 병해로서 저항성 관련 연구가 많이 수행되었다. 흰가루병 저항성은 유전적인 요인과 함께 환경적인 요인에 의한 영향을 많이 받는데, 딸기의 경우 흰가루병 저항성의 유전력(H2)은 비교적 낮아(0.41-0.71) 동일 품종 또는 분리집단 내에서도 개체간에 병반응 차이를 보인다(Nelson et al., 1995). 또한 장미과(Rosaceae)작물을 포함한 여러 작물에서 흰가루병 저항성은 다수의 유전자에 의해 조절되는 복잡한 유전양상의 양적형질인 것으로 알려져 있다. 딸기와 동일한 장미과 작물인 장미(Rosa hybrida)의 QTL(Quantitative Trait Loci) 분석을 통해 흰가루병 저항성 유전자위 Rpp1와 연관된 SCAR 마커 개발이 이루어진 바 있고(Linde et al., 2006), 사과(Malus pumila Miller)에서도 흰가루병 저항성 유전자위 Pl-w에 연관된 마커 탐색이 보고되었으며(Evans et al., 2003) 복숭아(Prunus persica) 등에서도 관련 연구가 수행되었다(Foulongne et al., 2003).
본 연구는 딸기 흰가루병 저항성 품종 육성을 위한 흰가루병 저항성 특이적 마커 개발로 육종 초기세대에 선발함으로써 기존의 육종기술과 같이 접목을 통해 내병성 육종효율을 높이고자 하였다.
재료 및 방법
식물재료
흰가루병 저항성 계통 선발을 위한 분자마커를 개발하기 위해 흰가루병에 저항성을 가지는 ‘설향’(Fragaria × ananassa cv. Seolhyang, 2n = 8x = 56)과 감수성을 가지는 ‘아끼히메’(Fragaria × ananassa cv. Akihime, 2n = 8x = 56)를 교배하여 F1 66 개체를양성하였다. 2010년 2월에 각 F1 개체들을 자가 수분하여 총 450 개체의 F2 집단을 양성하였다. 그 중 자식약세 현상 및 발아율이 낮은 개체를 제외한 128 개체를 선발 후 흰가루병 저항성 검정시험을 수행하였다.
흰가루병 저항성 검정
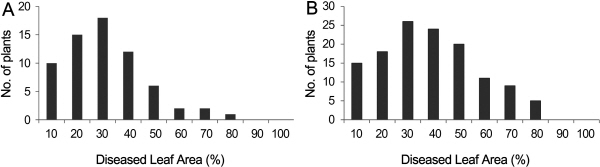
병리검정을 위한 흰가루 병원균은 경남 진주지역을 중심으로 딸기재배포장에서 자연발병한 병원균을 수집하여 사용하였으며, 2010년 5월에 파종한 F2 집단의 실생은 육묘 포트(32cm × 54cm, 24공)에 이식하여 본엽 6-10매 정도의 생육단계까지 하우스 내에서 키운 후 식물생장상 내에서 발병시켰다. 발병 조건은 식물생장상에서 병발생율을 높이기 위해서 온도는 주간(22 ± 2°C), 야간(15 ± 2°C)에 따라 변온을 주었으며, 습도는 포자의 발아율을 높이기 위해 고습(80 ± 10%)으로 1일간 유지시키고 이후는 40 ± 10%으로 유지하였으며, 광도는 50,000lux로 일정 환경조건을 유지하였다. 접종방법으로는 잎을 포개어 접착한 후 감염시키는 압착접종법과 균을 붓으로 떨어뜨리거나 묻혀 전염시키는 타락접종법으로 접종 후 5주간 1주일간격으로 발병조사를 수행하였다(Fig. 1). 발병조사는 주당 발병 엽면적률(%)을 기준으로 발병지수(DSI ; disease severity index)를 0에서 4까지 5단계로 다음과 같이 설정하여 수행하였다; 0 = 병징이 전혀 나타나지 않음, 1 = 잎 표면적의 0.1-5% 발병, 2 = 5.1-20% 발병, 3 = 20.1-40% 발병, 4 = 40.1%.
RAPD-BSA 분석
부모본과 F1개체들의 DNA 추출은 DNeasy plant mini kit(Qiagen, Valencia, CA, USA)을 이용하여 수행하였다. Bulked segregant analysis(BSA)를 위해 흰가루병 검정결과 저항성(DSI = 0) 및 감수성(DSI = 4) 각각 6 개체에 대한 DNA sample을 bulking 하여 RAPD 분석에 사용하였다. RAPD 분석을 위한 PCR은 template DNA 40ng, RAPD 10-mer OPERON primer 1.25μM, dNTP 0.2mM, MgCl2 2.5mM, Taq DNA polymerase 1 unit(Solgent, Deageon, Korea)으로 구성된 PCR mixture 총 20μL로 수행하였다(Je et al., 2009). PCR 조건은 95°C에서 5분간 반응시키고, 95°C에서 30초, 40°C에서 30초, 72°C에서 2분간 35회 반복 후 72°C에서 3분간 반응시켰다.
SCAR 및 CAPS 마커 개발
BSA를 통해 저항성과 감수성 집단에서 다형성을 보이는 RAPD 단편을 찾아내고 이를 agarose gel에서 GeneAll Expin Gel SV kit(General Biosystem, Seoul, Korea)을 사용하여 회수였다. 회수된 DNA 단편은 cloning 하기 위해 pGEM-T easy Vector(Promega, Madison, WI, USA)에 insert로 ligation하고 E. coli 균주(DH5α)로 transformation 한 후, LB 배지에 증식 후 GeneAll Exprep plasmid SV kit(General Biosystem, Seoul, Korea)으로 miniprep 하여 recombinant vector를 회수하였다. 회수된 vector의 insert DNA에 대한 염기서열을 분석은 Macrogen(Seoul, Korea)에 의뢰하였다. 이와 같이 선발된 RAPD 마커의 염기서열분석 결과를 토대로 하여 RAPD primer의 10개 염기를 포함하거나 포함하지 않는 20-mer 정도 크기의 SCAR 마커 primer를 Primer3(http://frodo.wi.mit.edu/ primer3)를 이용하여 제작하였다. SCAR 마커의 PCR은 template DNA 40ng, forward와 reverse primer 각각 1.25μM, dNTP 0.2mM, MgCl2 2.5mM, Taq DNA polymerase 1 unit(Solgent, Korea)를 총 20μL 반응액으로 하여 수행하였다. PCR 조건은 95°C에서 5분간 반응시키고, 95°C에서 30초, 55°C에서 30초, 72°C에서 1분간 35회 반복하고 72°C에서 10분간 처리하였다. Agarose gel 상에서 단편을 확인 후 염기서열을 위에서 기술한 바와 같이 분석하였다. CAPS 마커 개발은 저항성, 감수성 개체간 분석된 염기서열의 비교 및 SNP, In/Del 다형성 유무는 ClustalW(Chenna et al., 2003)을 이용하여 확인하였다. 개발된 CAPS 마커의 분석은 PCR product 5μL를 이용하여 총 10μL의 반응액에 0.5U의 제한효소를 처리한 후 1.5% Agarose gel상에서 확인하였다.
결과 및 고찰
흰가루병 저항성의 유전양상
‘설향’과 ‘아끼히메’, 그리고 이들 간 F2 128 개체를 대상으로 유묘기에 병원균을 접종 후 흰가루병 저항성 검정을 수행하였다. 그 결과, ‘설향’과 ‘아끼히메’는 흰가루병에 각각 높은 수준의 저항성(DSI = 0)과 감수성(DSI = 4)를 지님을 확인하였으며, 주당 발병 엽면적률(%) 분포가 10-80% (DSI = 0-4)로 연속변이의 정규분포양상을 보여(Fig. 1, 2), 본 연구에서는 흰가루 저항성이 다수의 유전자에 의해 조절되는 양적형질임을 확인할 수 있었다. 딸기 흰가루병에 관한 현재까지 알려진 유전양식으로 Hsu 등(1969)은 교배집단을 대상으로 양적형질 분석과 Mendelian 분석을 동시에 수행한 결과, 양적형질 분석에 있어 분산은 개체간 변이를 표현할 때 가장 중요한 것으로 흰가루병 유전의 상위분산(epistatic variance)은 총 유전분산의 중요한 부분을 차지하며, Mendelian 분석에 있어서는 저항성에 관여하는 2개의 상가유전자(additive gene), 감수성은 하나의 상위유전자(epistatic gene)에 의해 영향을 받는다고 하였다. Simpson (1987) 또한 이와 유사한 양적형질 분석결과를 보고하였다. 딸기와 동일한 장미과(Rosaceae)작물인 사과에서도 흰가루병 저항성은 다수의 유전자좌와 유전자간 상호작용에 의해 영향을 받는 복합적 유전형질로 보여진다고 보고되었다(James, 2004). 하지만, 현재까지는 딸기 흰가루병 저항성의 유전양상에 대한 연구가 충분히 진행되지 않은 상황이며, 정확한 흰가루병 저항성의 유전적 기작을 파악하고 관여 유전자를 찾아내기 위해서는 보다 다양한 교배집단에서의 표현형 분석이 필요할 것이다.
RAPD-BSA 분석
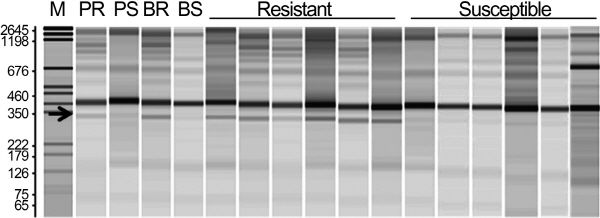
RAPD를 이용한 BSA 방법을 통해 흰가루병 저항성 계통 선발을 위한 분자마커를 탐색하였다(Michelmore, 1991). ‘아끼히메’ × ‘설향’의 F1개체를대상으로 흰가루병 저항성 검정 결과 저항성(DSI = 0)과 감수성(DSI = 4) 각각 6개체씩 선발하여 genomic DNA를 추출한 후 bulking 하였다. 저항성 및 감수성 bulked DNA 샘플에 대해 총 200종의 Operon RAPD primer를 검정한 결과 총 46개 primer들에서 샘플 간 다형성을 확인하였다. 46개의 primer들을 이용하여 저항성과 감수성 개체를 pooling하여 분석한 결과 이 중 primer OPE10에서 저항성 bulked DNA 샘플에서 특이적으로 증폭되는 약 331bp 크기의 PCR band(OPE10-331bp)를 확인하였으며 이를 대상으로 공우성 마커전환을 수행하였다(Fig. 3). 딸기의 RAPD분석 결과 부모본 및 bulked DNA sample간 다형성 밴드의 출현빈도가 낮았는데(23%), 이는 ‘아끼히메’와 ‘설향’을 비롯하여 현재 재배되고 있는 품종들 대부분이 한정된 재배종간 교배선발 되어졌기 때문에 유전적 배경이 매우 좁고 다양성이 크지 않기 때문인 것으로 추정된다.
SCAR 및 CAPS 마커 개발
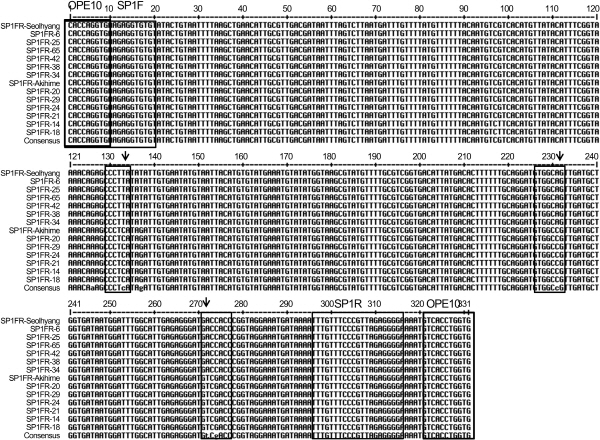
‘설향’과 저항성 F1 6개체로부터 흰가루병 저항성과 연관된 것으로 추정되는 OPE10-331bp 단편을 클로닝 후 염기서열을 분석하였다. 그 결과 모든 클론으로부터 331bp 길이의 동일 염기서열이 확인 되었다. OPE-331bp의 염기서열 정보를 NCBI BlastN에서 sequence similarity를 본 결과 2배체 딸기인 Fragaria vesca subsp. vesca의 linkage group LG7의 FAR1에 위치하는 mRNA와 52bp(51bp-102bp) 정도가 100% 일치하였다. OPE10-331bp 단편만을 특이적으로 증폭하는 SCAR 마커를 개발하기 위하여 OPE10 primer 염기서열로부터 3’ 방향으로 10bp 연장된 primer set(SP1F/R)을 제작하였다(Table 1 and Fig. 4).
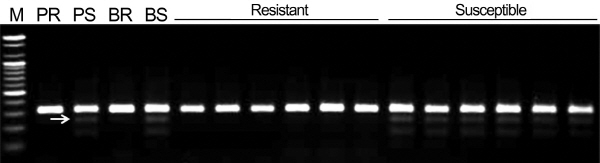
제작된 SCAR 마커(SP1F/R primer set)을 이용하여 ‘설향’과 ‘아끼히메’, 흰가루 저항성 F1 개체 및 감수성 F1 개체들을 대상으로 PCR 검정한 결과 316bp 크기의 DNA 단편을 얻었으나 단편의 크기 다형성은 확인되지 않았다. 따라서, 저항성, 감수성 개체간의 단일 염기서열 변이(single nucleotide polymorphism, SNP)를 확인하기 위하여 ‘아끼히메’와 흰가루 감수성 F1 6 개체로부터 SCAR 마커의 증폭산물을 클로닝하여 저항성 개체의 염기서열과 비교 분석한 결과, 두 집단 간에 총 6개의 SNP가 존재하였다. 그 중 133bp(T/C), 231bp(A/C), 272bp(A/T) 위치의 SNP에서 각각 제한효소 Mnl I, Eae I, Sal I의 처리로 CAPS 마커 전환이 가능함을 확인하였다(Fig. 4). 이 중 제한효소 Eae I의 인식서열(Y/GGCCR)에 위치한 SNP를 타겟으로 저항성 계통(TGGCAG)에서는 Eae I 처리시 절단되지 않은 316bp 크기의 밴드가 관찰되는 반면, 감수성 계통(T/GGCCG)에서는 절단되어 231bp와 85bp 크기의 두 밴드가 나타나도록 CAPS 마커 SP1-Eae I을 제작하였다(Fig. 5). 부모본 계통 및 BSA에 사용된 12개의 F1 개체에 SP1-Eae I 마커를 검정한 결과, 예상과는 다르게 모든 개체에서 316bp의 밴드가 확인되었으며, 감수성 개체에서는 231bp와 예상치 못한 150bp 정도 크기의 밴드가 추가적으로 관찰되었다. 85bp 절편은 매우 작은 단편으로 Agarose gel 상에서 확인이 어려웠다. 결과적으로 공우성이 아닌 우성의 CAPS가 개발되었는데, 이는 증폭된 유전자위의 유전자형이 이형접합으로 존재하기 때문인 것으로 추정된다. 딸기 재배종은 이질배수성(8배체) 영양번식 작물로서 대부분의 상동염색체의 유전자위가 동형접합이 아닌 이형접합일 가능성이 매우 크며, 한 개체 내 동일 유전자위에서의 특정 대립유전자형의 비율(gene dosage)은 다양할 수 있다는 점에서 유추가 가능하다(Cho et al., 2008). PCR 증폭산물의 염기서열 분석에서 모든 6개 클론들이 동일 염기서열을 보인 것(Fig. 4)은 PCR 시 높은 빈도로 존재하는 대립유전자의 증폭량이 그렇지 않은 대립유전자 보다 상대적으로 많을 것이고, 따라서 클로닝 단계에서 이들 산물들이 보다 높은 확률로 클로닝 될 수 있기 때문으로 추정된다. 또한 CAPS 마커 제작시 예상치 못한 150bp 절편이 관찰된 것은 한 유전자위에 최소 3가지 이상의 대립유전자가 이형접합으로 존재할 수 있음을 암시한다. 하지만, 클로닝된 유전자위 이외에 이와 염기서열 유사성을 지닌 또 다른 유전자위가 독립적으로 존재하여 PCR 및 제한효소 처리 결과에 영향을 미쳤을 가능성도 있다.
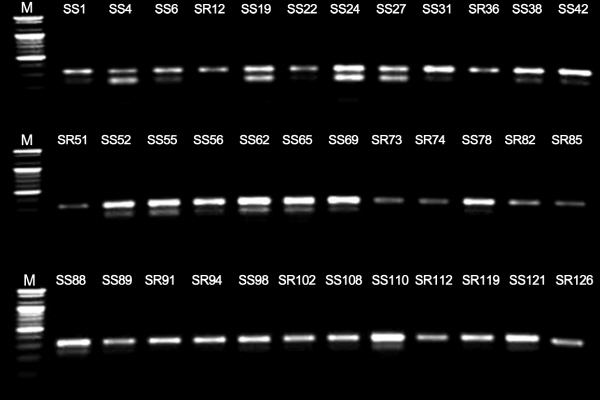
CAPS 마커 SP1-Eae I의 흰가루 저항성 연관과 MAS 적용 가능성을 검정하기 위해 F2 집단에서 임의로 선발한 36 개체를 대상으로 유전자형을 분석하였다. F1 개체의 마커검정 결과와 마찬가지로 331bp의 밴드는 저항성, 감수성 모두에서 강하게 나타났으며, 흰가루 감수성 특이적 마커인 231bp 밴드는 개체에 따라 강약의 차이가 관찰 되었다(Fig. 6). 이는 위에서 설명된 이형접합성과 gene dosage의 영향과 동일한 맥락으로 설명 가능할 것으로 사료된다. 흰가루병 저항성 표현형과 마커형을 비교한 결과 높은 저항성(DSI=0)을 보이는 F2 10 개체는 모두 마커형이 저항성(R)으로 나타났으나, 중도저항성(DSI = 1) 5 개체 중 3 개체가 저항성의 마커형이, 2 개체는 이형접합(H) 또는 감수성(S)으로 나타났다. 감수성(DSI > 1) 21 개체는 모두 이형접합(H) 또는 감수성(S)의 마커형을 보여, SP1-Eae I 마커를 통해 저항성(R) / 중도저항성(H), 감수성(S) 판별이 가능함을 확인하였다(Table 2). 따라서, 본 연구에서 개발된 CAPS 마커는 비록 우성의 마커 특성을 지니고 있지만, ‘아끼히메’ × ‘설향’ 후대집단에서 흰가루병 저항성 계통 선발을 위한 분자마커로 활용될 가능성이 기대된다, 하지만, 보다 폭넓은 육성집단의 MAS에 적용하기 위해서는 다양한 계통 및 품종에서의 본 마커의 다형성 확인이 요구되며, 향후 공우성의 마커로 전환할 수 있는 추가적인 연구가 필요하다.