서 언
재료 및 방법
신규 건조 저항성 관련 유전자 동정
과발현 vector 제작 및 담배 형질전환체 유기
형질전환 유무 분석
도입유전자 발현량 분석
형질전환체 표현형 분석
결과 및 고찰
신규 건조 저항성 관련 유전자 동정
BrDSR 유전자 기능 분석
서 언
비생물적 스트레스 중 건조 스트레스는 발아지연, 불량한 뿌리 발달, 잎의 노화 촉진 등과 같은 작물의 생리적 변화를 야기함으로써 생장을 크게 저하시키거나 작물의 고사를 발생시켜 최종적으로는 수확량의 감소를 유발하는 매우 중요한 요인이다(Agarwal et al., 2006; RDA 2007; Seki et al., 2007; Wang et al., 2003). 그러므로 건조한 생육조건에 작물이 생존 및 적응하기 위해서는 다양한 생리적・생화학적 반응들을 통한 저항성 기작들의 작동이 필수적이다(Lee et al., 2008; Rabbani et al., 2003). 이러한 스트레스 저항성 기작을 연구하기 위해서는 스트레스 자극과 관련된 기능 유전자들과 다양한 전사조절인자(transcription factor)들의 발현 패턴을 분석할 수 있는 microarray 기술이 매우 유용하다(Fei et al., 2007; Lee et al., 2008; Soeda et al., 2005; Yin et al., 2006). Microarray 분석을 통한 스트레스 반응 유전자들의 발현 분석과 실제 식물 생리연구의 결과를 동반 분석한 결과, 건조 스트레스 조건에서 삼투질(osmolyte) 및 항산화물질로 작용하는 것으로 알려진 프롤린(proline), 폴리아민류(polyamines), 당류(sugars)들의 생성이 촉진된 것으로 보고되었다(Verbruggen and Hermans, 2008; Wang et al., 2003; Yamada et al., 2005). 한편, 5대 식물호르몬 중 하나인 앱시스산(abscisic acid, ABA)의 체내 생성량이 증가하여 잎의 기공을 닫고, 저항성과 관련된 유전자들의 발현 변화를 유도하여 다양한 대사작용을 작동시킨다는 결과도 보고되었다 (Downton et al., 1988; Li et al., 2000; Seki et al., 2007). 전세계적으로 재배되고 있는 다양한 작물을 대상으로 급변하는 기후 변화에 대응하기 위한 수많은 연구들이 진행되고 있지만, 전통적 또는 분자생물학적 육종 분야에서 아직까지 비생물적 스트레스에 대한 뚜렷한 저항성 작물은 개발하지 못한 실정이다. 배추(B. rapa ssp. pekinensis)는 아시아 지역에서 매우 중요한 채소 중 하나로서, 1990년대 초반부터 진행된 많은 연구들과 2011년 완전 해독된 게놈 염기서열 데이터(Brassica rapa Genome Sequencing Project Consortium, BrGSPC)를 활용하여 다양한 유전체 연구들이 빠른 속도로 진행되고 있으며 우수한 연구결과들이 계속 보고되고 있다(Wang et al., 2011). 최근 배추(B. rapa cv. Osome)의 3,429 ESTs(Expressed Sequence Tags)분석을 통해 “Brassica defensin- like family protein(BrDLFP)” 유전자와 “Brassica Betv1 allergen family protein(BrBetv1AFP)”유전자가 건조 스트레스 발생 초반에 발현량이 급격히 증가하였다가 서서히 감소하였음을 보고하였다(Ahmed et al., 2012). 또한 유채(B. napus)를 대상으로 연구한 보고에서 B. napus lateral suppressor(BnLAS) (Yang et al., 2011) 유전자와 B. napus annexin 1(BnAnn1) (Xiao et al., 2012) 유전자 또한 건조 자극 시 발현량이 크게 증가하여 저항성 획득에 관여할 것으로 보고하였다.
본 연구는 비생물적 스트레스인 건조 스트레스 처리된 내혼계배추(B. rapa ssp. pekinensis inbred line ‘Chiifu’)를 대상으로 microarray 분석을 통하여 건조 저항성 유전자로 예측되는 유전자를 동정하고, 모델 작물인 담배(Nicotiana tabacum ‘SR1’)를 이용하여 그 기능을 분석하였다. 제작된 과발현(over-expression) vector를 이용하여 생산된 담배 형질전환체에서 건조 스트레스 처리 시 도입유전자의 발현이 증가함을 확인하였고 실제 표현형 분석에서 건조 저항성을 획득한 것으로 판단되어, 해당 도입유전자를 BrDSR(Brassica rapa Drought Stress Resistance)로 명명하였다.
재료 및 방법
신규 건조 저항성 관련 유전자 동정
내혼계배추(‘Chiifu’)를 생장상(광도 250µmol・m-2・sec-1, 광주기 명처리 16시간/암처리 8시간, 온도 25 ± 2°C, 습도 30-70%)에 파종하여 25일간 재배하고 건조(air-dry)처리를 48시간까지 처리한 후, 처리 6, 12, 24, 36, 48시간 별로 total RNA를 추출하고 KBGP-24K oligo chip(NimbleGen, Madison, WI, USA; GreenGene Bio Tech Inc., Yongin, Korea)을 이용하여 각 유전자들의 발현 변화를 비교・분석하였다(Lee et al., 2008). 이 연구 결과를 활용하여 건조 스트레스 처리 시 반응하는 유전자들 중 발현이 강하게 증가한 유전자들을 우선 선발하고 완전장(full-length sequence)을 갖추고 있으며 기능이 알려지지 않은 유전자들을 차례로 분류하여 본 연구의 대상유전자를 최종적으로 선발하였다.
유전자 동정은 건조 처리된 잎에서 추출한 total RNA를 이용하여 RT-PCR방법으로 수행하였다. 이를 위해 KBGP-24K oligo chip 내 438bp ORF(Open Reading Frame) 및 애기장대(Arabidopsis thaliana)에서 상동성을 가지는 cDNA 염기서열(AT1G16850)과 NCBI에 등록된 Brassica rapa uncharacterized LOC103842825 mRNA 염기서열(XM009119491.1)을 바탕으로 primer set(BrDSR-F: 5'-ATG ACT TTG CAA GTT TTC CAC T-3', BrDSR-R: 5'-TTA GAG CTC CTC AGT ACC ATA T-3')를 제작하였다. Total RNA를 주형으로 증폭된 PCR 산물은 pGemT-easy vector(cat#A1360; Promega, Madison, USA)를 이용하여 염기서열을 확인하였다(Macrogen Co., Seoul, Korea). 확보한 염기서열은 National Center for Biotechnology Information(NCBI) database(www.ncbi.nlm.nih.gov)를 이용하여 애기장대를 비롯한 타 작물의 유전자 염기서열과 상동성 수준을 분석하였다.
과발현 vector 제작 및 담배 형질전환체 유기
동정한 BrDSR 유전자가 과발현된 형질전환체를 생산하기 위해, 우선 동정한 438bp cDNA를 pCR™8/GW/TOPO® TA Cloning® Kit(cat#K2500-20, Life Technologies, CA, USA)로 TOPO® vector에 삽입하고, Gateway® LR ClonaseTM Enzyme Mix(cat#11791-019, Life Technologies, CA, USA)를 사용하여 LR recombination 방법(Karimi et al., 2007)으로 438bp cDNA를 binary gateway over-expression vector인 pH2GW7 (VIB-Ghent University, Belgium)에 최종 전이하여 형질전환용 vector를 제작하였으며, 이를 pSL100으로 명명하였다(Fig. 1). 담배 형질전환은 무균 상태로 기내 배양된 담배(‘SR1’)의 잎을 재료로 사용하여, Lee et al.(2004)에 보고된 형질전환 방법을 참고로 수행하였다. 생산된 T0 담배 형질전환체들은 전이된 T-DNA 상의 hygromycin 저항성 유전자(hpt)를 이용하여 형질전환 유무를 검정하였으며, 선발된 5계통의 형질전환체들은 자가수정(self-pollination) 방식으로 세대진전 시켰다. 본 연구는 T1 세대 담배 형질전환체를 이용하여 수행하였다.
형질전환 유무 분석
BrDSR의 건조 저항성 관련 기능 분석을 위해, 세대 진전된 5계통의 T1 종자를 다수 파종하여 각각의 genomic DNA를 추출하고 hpt 유전자를 대상으로 한 PCR 분석을 통해 형질전환체를 선발하였다. 생산된 담배의 잎을 500mg 채취하여 막자와 막자사발로 분쇄한 후, Yu et al.(2014)에 제시된 방법을 참고로 DNA 추출 buffer(0.5M NaCl, 0.1M Tris-HCl, 50mM EDTA, 1.25% SDS) 처리 후, phenol, chloroform, isoamyl alcohol를 사용하여 genomic DNA를 추출하였다.
PCR 분석은 gDNA 100ng과 hpt 유전자 염기서열을 바탕으로 제작된 HPT-UP: 5'- AAT CTC GTG CTT TCA GCT TCG -3'와 HPT-DOWN: 5'- CAA AGC ATC AGC TCA TCG AGA G -3' primer set, Maxime PCR PreMix Kit(cat#25167; iNtRON Biotechnology, Seongnam, Korea)를 이용하여 수행하였다. PCR조건은 95°C에서 3분간/1회 predenaturation한 후 95°C에서 30초간 denaturation, 58°C에서 30초간 annealing, 72°C에서 30초간 extension 과정을 30회 반복하고, 마지막으로 72°C에서 5분간/1회 final extension 하였다. 증폭된 PCR 산물은 1× TBE buffer를 사용하여 1.2% agarose gel 상에서 80V, 45분간 전기영동하여 ethidium bromide로 염색한 후, UV illuminator를 이용하여 반응산물을 확인하였다.
PCR 분석으로 확인된 형질전환체들 중 도입유전자의 발현량 분석을 통해 발현량이 큰 3계통을 선별하여 이들의 도입유전자 copy수를 분석하였다. DNA blot 분석은 제한효소 BamHI 사용과 도입된 pSL100 vector의 hpt 유전자를 탐침하는 [32P]-dCTP로 labeling된 454bp의 probe를 사용을 제외하고는 Yu et al.(2014)에 제시된 방법과 동일하게 실험을 수행하였다.
도입유전자 발현량 분석
PCR분석을 통해 형질전환체로 분석된 5계통을 대상으로 건조 스트레스를 처리한 후 도입유전자의 발현량을 분석하였다. 건조 스트레스는 본엽이 6-7매가 된 비형질전환체와 형질전환체를 비생물적 자극(수분, 온도, 빛 등)이나 생물적 자극(병원균 감염, 해충 피해 등)이 발생하지 않는 제한된 조건(광도 250µmol・m-2・sec-1, 광주기 16시간 명처리/8시간 암처리, 온도 25 ± 2°C)에서 72시간 처리하였다.
Total RNA는 건조 처리 후 채취한 100mg의 잎을 RNeasy® Plant Mini Kit(cat#74903; QIAGEN, Hilden, Germany)를 사용하여 추출하였으며, 도입유전자의 발현량 분석을 위한 quantitative real-time RT PCR은 Rotor-Gene Q(cat#9001560, QIAGEN, Hilden, Germany)과 SensiMixTM One-Step Kit (cat#QT205-02, Bioline, London, UK)를 이용하여 수행하였다. 사용한 primer set은 DSRreal-F: 5'-ATG ACT TTG CAA GTT TTC CA-3'과 DSRreal-R: 5'-TCC TTC TAT GTT TGG AGG A-3'이며, 방법은 42°C에서 30분간 cDNA 합성 후 95°C에서 10분간 predenaturation을 수행하고, 95°C에서 10초간 danaturation, 54°C에서 15초간 annealing, 72°C에서 20초간 extension 반응을 35회 반복하였다. 분석된 각 형질전환체의 발현량 수치는 actin 유전자의 발현값에 비례하여 상대적으로 계산하였다.
형질전환체 표현형 분석
표현형 분석은 도입유전자 발현량 분석과 동일한 방법으로 건조 스트레스를 처리한 후, 비형질전환체와 형질전환체가 표현형적으로 뚜렷한 차이(엽색 및 생육 모습, 도복 여부)를 보인 처리 10일째 수행하였다.
결과 및 고찰
신규 건조 저항성 관련 유전자 동정
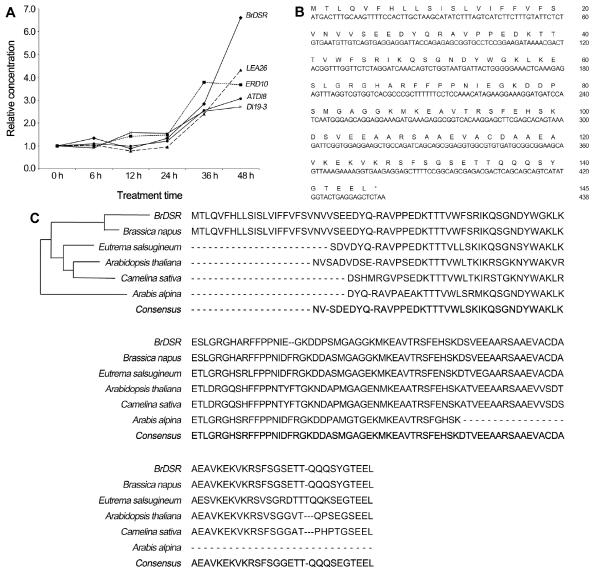
건조 스트레스가 처리된 내혼계배추(‘Chiifu’)를 대상으로 2반복 분석된 KBGP-24K oligo chip 데이터를 활용하여 대조군 대비 5배이상 발현이 크게 증가한 738개의 unigene들을 1차 선발하고, 전체 염기서열이 보고되어 있으나 그 기능은 알려지지 않은 유전자들 중 발현량이 5배 이상 크게 증가한 유전자들을 2차 선발하였다. Chip 데이터 중 수분 스트레스와 연관이 있는 것으로 보고되어 있는 ERD10(early responsive to dehydration 10, AT1G20450)(Candat et al., 2014; Luhua et al., 2013), LEA26(late embryogenesis abundant 26, AT2G44060) (Candat et al., 2014), DI19-3(drought-induced protein 19, AT3G05700)(Qin et al., 2014), ATDI8(dehydrin RAB18-like protein, AT5G66400)(Shi et al., 2013)들의 시간대별 발현 수준을 근거로 수분(건조) 스트레스에 민감하게 반응하여 처리 48시간째 대조군 대비 6.6배 발현이 증가한 유전자를 최종 선발하여 “BrDSR”로 명명하였다(Fig. 2A). 선발된 BrDSR의 KBGP-24K oligo chip seqID는 “BRAS0001S00002943”이고, 5’ end EST clone 이름은 “KBCD-040F11”이며, TAIR ID는 “AT1G16850”이다. Chip상에 공개된 791bp의 cDNA 염기서열에서 438bp의 ORF와 145개의 아미노산을 확인하였으며(Fig. 2B), 이 정보들을 근거로 내혼계배추(‘CT001’, Si One Seed, Pyeongtaek, Korea)의 잎의 RNA를 이용하여 BrDSR을 동정하였다. 동정된 BrDSR의 염기서열을 이용하여 BlastX(http://blast.ncbi.nlm.nih.gov/Blast.cgi) 분석 결과, 유채(B. napus), saltwater cress(Eutrema salsugineum), 애기장대(A. thaliana), 양구슬냉이(Camelina sativa), 고산장대(Arabis alpina) 등과 65% 이상의 아미노산 상동성을 보였으나, 해당 유전자의 기능은 아직 보고되어 있지 않았다(Fig. 2C). 한편, 정보가 공개된 2,026개의 배추 BAC clone을 이용하여 BrDSR의 위치를 확인한 결과, JWF3p genetic map에서 9번 염색체의 310개 BAC clone 중 KBrH109O07 (54.581cM, Genebank No. AC240946)에 속해져 있음을 확인하였다(National Agricultural Biotechnology Information Center, http://nabic.rda.go.kr/).
BrDSR 유전자 기능 분석
형질전환체를 이용한 유전자 기능 분석 전, 애기장대 데이터베이스를 이용하여 BrDSR의 기능을 in silico 분석을 수행하였다. 먼저 “Arabidopsis eFP Browser”(www.bar.utoronto.ca) (Winter et al., 2007)를 이용한 분석에서 식물체 발달 단계 중에서는 종자 배 발생단계가 진행될수록 발현이 점차 증가하고, 수분이 부족한 종자에서 발현되는 것으로 분석되었다. 애기장대의 비생물적 스트레스에 대한 발현 수준 데이터 중 건조 스트레스(air-dry, 24시간) 처리에서는 BrDSR의 발현량 변화가 거의 없었는데, 이는 KBGP-24K oligo chip 데이터를 이용한 시간대별 발현 패턴 분석(Fig. 2A)에서 보였듯이 24시간 이후 발현량이 급속히 증가하는 특성 때문일 것으로 판단되었다. 한편, BrDSR이 저온 스트레스(4°C, 24시간) 처리와 삼투 스트레스(300mM mannitol, 12시간) 처리에서 발현이 증가하는 것으로 분석되었다. 이는 BrDSR 유전자가 건조 스트레스만 특이적으로 반응하는 유전자가 아니라, 수분 스트레스 전반에 관여하는 중요 유전자임을 유추할 수 있었으며, 실제로 저온 스트레스 처리 배추를 이용한 microarray 데이터에서도 처리 48시간 째 발현량이 대조군 대비 4.5배까지 증가하였다(Lee et al., 2008; Oono et al., 2006; Xin et al., 2007). 식물 조직별 발현 분석에서는 조직특이성을 확인할 없었으며, 식물 호르몬 처리에 따른 발현 패턴 분석에서는 zeatin, indole-acetic acid(IAA), ABA, methyl jasmonate, gibberellic acid 3(GA3), brassinosteroids 모두에서 처리 전후의 발현량 변화를 확인할 수 없어 BrDSR은 호르몬의 작용과는 별개로 건조 스트레스 저항성에 관여할 것으로 예측하였다. 또한 BrDSR과 네트워크적으로 관련된 유전자들을 분석함으로써 BrDSR의 기능을 유추하기 위해 “GeneMANIA”(http://genemania.org/) 프로그램을 이용하여 분석하였다(Warde-Farley et al., 2010). 총 20개의 유전자들이 매우 유의적인 관계를 가지고 있는 것으로 분석되었으며, 이 중 5개의 유전자[late embryogenesis abundant protein(AT1G01470), late embryogenesis abundant 4-5(AT5G06760), late embryogenesis abundant protein family protein(AT3G02480), dehydrin family protein(AT5G66400), cold-regulated 47(AT1G20440)]가 “response to water deprivation” 기능 범주에 속하는 것으로 분석되었다. Late embryogenesis abundant(LEA) 유전자군은 저온, 건조, 염 스트레스 저항성 관련 유전자임이 많이 보고되어 있으며(Hundertmark and Hincha, 2008; Olvera-Carrillo et al., 2011; Vaseva et al., 2010), dehydrin 단백질은 LEA 단백질과 유사하게 저온과 건조 스트레스 하에서 특히 생성량이 증가하여 식물체의 저항성에 관여하는 것으로 보고되어 있다(Hara et al., 2014; Velasco-Conde et al., 2012, Yang et al., 2012).
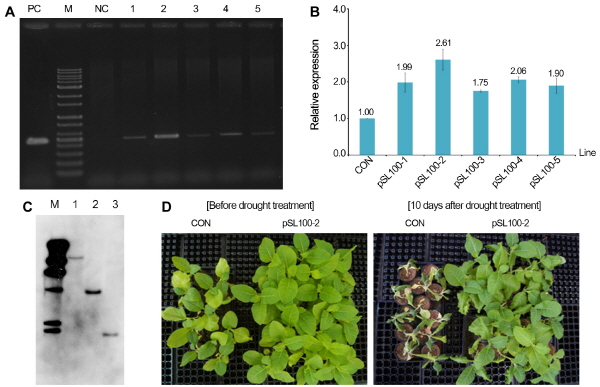
In silico 분석 결과로 배추의 건조 저항성 관련 유전자로 예측되는 BrDSR 유전자의 기능을 알아보기 위해, 모델 식물인 담배(‘SR1’)를 대상으로 형질전환을 수행하여 BrDSR 유전자가 도입된 담배 형질전환체를 생산하였다. 전이된 T-DNA 내의 hpt 유전자를 대상으로 PCR 검정 및 각 PCR산물의 염기서열 분석을 통해 5계통의 담배 형질전환체를 선발하였다(순서대로 pSL100-1, -2, -3, -4, -5로 명명함)(Fig. 3A). PCR분석으로 확인된 형질전환체들을 대상으로 도입된 BrDSR의 발현 수준은 제작된 DSRreal-F와 DSRreal-R primer set을 이용하여 quantitative real-time RT PCR로 분석하였다. 실험의 신뢰성을 높이기 위해 3반복으로 실험을 진행하고, 각 반복마다 내부 대조 유전자로서 actin 유전자의 발현 분석을 동시에 수행하였다. Quantitative real-time RT PCR 분석 결과, 모든 형질전환체들이 비형질전환체(CON) 보다 발현량이 약 1.7-2.6배 가량 증가한 것으로 분석되어 목적한 BrDSR 과발현 담배 형질전환체를 확보하였다(Fig. 3B). 제작된 DSRreal-F와 DSRreal-R primer set에 대해 대조군에서도 일정 수준의 발현이 확인되는 것은 도입한 BrDSR과 유사한 염기서열을 가진 유전자가 담배에도 존재하며 그것이 반응하여 발현된 것으로 추측된다. 또한 quantitative real-time RT PCR 분석 결과를 근거로 발현량이 큰 3계통(pSL100-1, -2, -4)을 선별하여 이들의 도입유전자 copy수를 분석하여, 모두 1개의 T-DNA가 담배 게놈 상에 삽입되었음을 확인할 수 있었다(Fig. 3C). 1개의 T-DNA가 삽입되었으며 대조군 대비 BrDSR의 발현량 증가가 가장 큰 것으로 분석된 pSL100-2 계통의 T1 종자를 다수 파종하여 건조처리 시 표현형 변화 관찰을 통해 BrDSR의 기능 분석을 수행하였다. 대조군(CON)과 pSL100-2 계통은 본엽이 6-8매인 시기에 충분히 수분을 공급한 후 뚜렷한 표현형적 차이(엽색 및 생육 모습, 도복 여부)를 보일 때까지 계속적으로 건조 처리를 수행하였으며, 처리 10일째 명확한 차이를 구별할 수가 있었다(Fig. 3D). 건조 처리 전 대조군에서 pSL100-2 계통보다 엽색이 다소 연한 개체들이 확인되었으나, 이러한 생육상태의 미비한 차이는 표현형 실험 결과에 영향을 미치지 않는 것으로 판단하였다. 처리 3일째부터 대조군의 약한 잎들은 급격히 노란 색으로 변해 가지 시작하였고, 처리 5일째는 대조군의 진한 녹색 잎들도 색이 옅어지며 아래로 늘어지고 말라가기 시작하였다. 이는 식물체는 건조 스트레스를 받게 되면 체내 수분함량이 감소하게 되어 잎과 줄기가 쳐지게 되는 동시에, 광합성 반응의 광계 II(photosystem II)에서의 광화학 반응 효율(photochemical efficiency)이 크게 낮아져 녹색을 잃게 된다는 연구 결과와 동일한 표현형적 결과이다[면화(Gossypium hirsutum)(Mssacci et al., 2008), 병아리콩(Cicer Arietinum) (Rahbarian et al., 2011), 유채(B. napus)(Kauser et al., 2006), 염소풀류(Aegilops species)(Dulai et al., 2006)]. 처리 10일 후 형질전환체들이 대조군과 비교해서는 건조 스트레스 저항성이 크게 향상되었음을 확인할 수 있었다.
건조 스트레스 발생 시, 기 보고된 저항성 관련 유전자들보다 높은 발현량을 보인 시간대별 발현량 비교 분석(KBGP-24K oligo chip 분석), 애기장대 데이터베이스를 이용한 종자 발생 단계 및 비생물적 스트레스 자극 시 발현량 변화 분석(Arabidopsis dFP Browser 분석), 네트워크적 관련 유전자 비교 분석(GeneMANIA 분석), 담배 형질전환체를 이용한 건조 자극 시 발현량 증가(quantitative real-time RT PCR 분석)와 실제 표현형 분석들을 근거로, BrDSR 유전자는 건조 스트레스 발생 시 체내 발현량을 증가시켜 식물체의 건조 스트레스 저항성 향상에 기여하는 중요 유전자로 예측된다. 이러한 BrDSR 유전자는 지적재산권 확보를 위해 특허출원(출원번호 : 10-2014-0132453)을 실시하였다.
본 연구에서 분리 검정된 BrDSR 유전자는 건조 스트레스에 대한 뚜렷한 저항성을 보이므로 추후 분자생물학적 육종을 통한 저항성 작물 개발에 있어 다양하게 이용될 수 있으리라 기대된다.