서 언
수경재배에 있어 중요한 부분 중 하나는 배양액이고 이러한 배양액을 만들 때 사용되는 적절한 무기이온들의 조성과 그 비율이 작물에 따라 다양하다. 배양액의 초기 설정으로 무기이온이 공급되면 생산 환경에 맞춰 작물이 생육하면서 이온 흡수 특성이 다양하게 나타나고 이에 따라 배양액의 EC와 pH는 변하게 된다. 이러한 변화 양상은 작물의 종류 및 재배 시스템에 맞춰 무기이온의 기준을 설정을 한 후 배양액 농도의 배율에 따른 조성을 통하여 이온 밸런스 특성을 추정할 수 있도록 배양액의 설계와 해석이 연구되어 왔다(Rush, 2005). 배양액 내 pH는 H+과 OH-의 농도에 따라 0에서 14까지의 값을 나타내는데, pH의 변화는 무기 이온의 용해도와 작물의 영양소 흡수에 큰 영향을 준다(Trejo-Téllez and Gómez-Merino, 2012). 배양액 내 pH 변화에는 NH3-/NH4+의 구배(De Rijck and Schrevens, 1999), NO3-/NO2-의 구배(De Rijck and Schrevens, 1998), HPO4-2/H2PO4-의 구배(Dyśko et al., 2008), 양이온과 SO4- 및 C1-의 구배(De Rijck and Schrevens, 1998), K+와 Ca+2간의 함량 비율(Steiner, 1961) 등이 영향을 준다. 이 중에서 배양액 pH에 따라 HPO4-2와 H2PO4-의 해리 농도가 다르게 나타나기 때문에 인산 이온 형태 변화에 주목하여 무기 이온 흡수 패턴에 대한 해석이 시도되었다(Steiner, 1984). 배양액 pH 5.0에서 H2PO4-가 거의 대부분을 차지하지만 pH가 상승함에 따라 HPO4-2가 증가하고 H2PO4-가 감소한다. 배양액 pH 7.3에서 HPO4-2와 H2PO4-가 균형을 이루다가 pH가 더욱 상승하게 되어 pH 10.0에 근접하면 HPO4-2가 100%에 이르게 된다(Trejo-Téllez and Gómez-Merino, 2012). 따라서 HPO4-2와 H2PO4-의 농도 변화가 배양액 내 다양한 pH 구배에 영향을 주며 이로 인해 pH 모형 설정이 중요하다(De Rijck and Schrevens, 1997).
이러한 배양액 내 pH 변화는 작물의 무기이온 흡수와 이온 교환을 통해 상호 영향을 주게 된다. 이온균형모형(ion balance model; IBM)은 배양액 내 이온의 함량비율과 EC의 변화 특성을 4분면으로 구획하여 양이온과 음이온의 함량 변화를 통해 EC의 변화와 구배를 해석하였다(Soh and Lee, 2012). 따라서 본 연구는 배양액 내 HPO4-2와 H2PO4-의 함량 비율 변화에 의해 이온과 EC의 변량을 추정하여 배양액 내 pH의 변화에 의한 이온 균형에 대해 구명하고자 한다.
재료 및 방법
본 실험은 청치마 상추(Jincheongmat, Kwonnong Seed Co., Korea)를 공시하여 100주씩 3반복으로 총 300주를 정식하였다. 수경재배방법은 박막수경재배 시설 하에서 서울시립대학교 순환식 잎상추 전용 배양액(NO3-N 10.6, NH4-N 1.0, P 2.0, K 6.7, Ca 4.0, Mg 2.0, S 2.0meq・L-1)을 이용하여 초기 배양액 기준을 pH 5.8과 EC 1.6dS・m-1으로 설정하였다.
배양액 내 pH는 pH 메타(HI 98140, Hanna Inst., USA)와 EC는 EC 메타(HI 99300, Hanna Inst., USA), 질소는 자동증류기(Büchi 323, Büchi, Switzeland), 인산은 460nm에서 비색계(UV 2100, Shimadzu, Japan), 무기 양이온은 원자흡광광도계(Perkin Elmer 3100, Perkin Elmer, USA), 음이온 분석은 이온크로마토그래피(DX-120, Dionex, USA)를 이용하여 매일 수집하여 분석하였다.
배양액의 pH 변화에 따른 이온 변량을 구명하기 위해 Steiner(1980)의 pH 변화에 의한 HPO4-2/H2PO4-의 변화율에 따라 pH 4.0-8.0 범위에서 0.1 수준으로 보정하였다. 배양액 내 무기 이온의 농도는 공급 배양액에 누적되는 다량 원소의 농도를 기준으로 하였다. 또한 배양액 내 각각의 이온 당량도는 Robinson and Strokes(1959)와 Tanji(1960)의 등가 이온 방법에 따라 산출하였고, Soh et al.(2012)의 이온균형모형에 따라 이온과 EC의 정점을 연결한 4분면에 분포 양상으로 양이온과 음이온의 변화 추이와 EC의 농도 변화를 분석하였다. K+과 Ca+2의 비율에 따른 pH와 EC의 변화 특성을 구명하기 위해 Steiner(1961)의 양이온에 따른 pH 변화 모형에 따라 설계한 후 Rush(2005)에 따라 pH 4.0-8.0에서 K+과 Ca+2의 함량비율을 각각 1, 10, 50, 100배로 설계하였다. 배양액 내 pH 변화에 따른 K+, Ca+2, EC의 추정은 상기의 동일한 방법으로 산출하였다. 모형 설계 과정에서 이온 변량 표본은 40점으로 정하여 3반복으로 수행하였다. 상기의 통계 분석은 SAS(Ver. 9.02, SAS Institute Inc., USA)와 Minitab(Ver 15.1, Minitab Inc., USA)을 이용하여 신뢰수준 0.05에서 가설 검정을 수행하였다.
결과 및 고찰
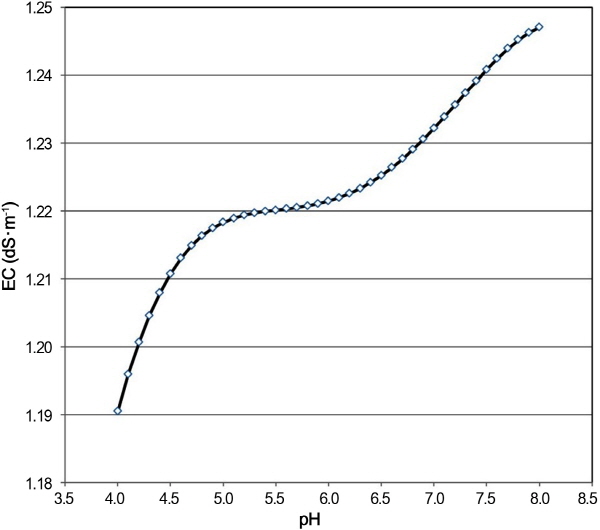
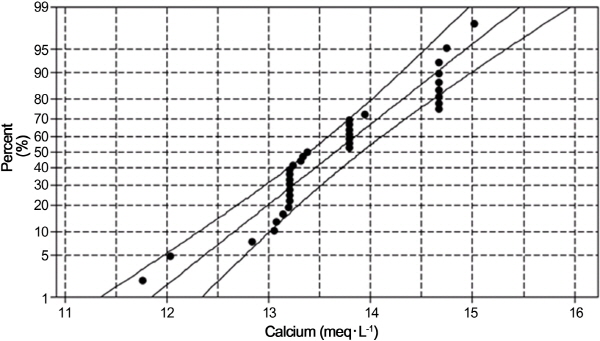
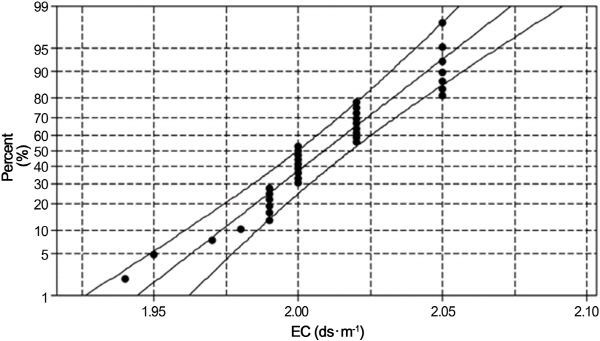
배양액 내 pH의 변화와 EC 변화의 변화 추이를 분석하였다(Fig. 1). Steiner(1980)의 pH 변량 모형에 따르면 HPO4-2와 H2PO4-의 변량에 의한 pH 변량이 pH 4.0-8.0 범위에서 크다고 알려져 있지만, pH 변화에 따른 EC의 변화는 1.19- 1.25dS・m-1로 미세하게 상승하였다. 배양액 pH 4.0-5.0 범위에서 EC 변량이 다소 상승하였는데, 이는 Steiner(1980)의 pH 변량 모형에 의하면 배양액 내 인산 이온이 H2PO4- 형태로 약 95% 이상 존재하는 범위이다(Trejo-Téllez and Gómez-Merino, 2012). 배양액 pH 5.0-7.0 범위에서 pH의 변화에 따른 EC의 변량이 완만하게 상승하였다. 특히 pH 5.0-7.0은 대부분의 수경재배에서 배양액의 적정 pH 범위에 포함되는 범위이다. 즉 배양액 pH를 적정한 범위에서 관리하면 HPO4-2와 H2PO4-의 변량에 의한 이온 불균형과 EC의 급격한 변화가 초래될 가능성은 많지 않다. 배양액 pH 7.0-8.0 범위에서 pH가 상승함에 따라 EC의 변량이 다시 상승하는데, 인산 이온의 형태가 H2PO4- 보다 HPO4-2의 함량 비율이 50%를 초과하여 존재하는 범위이다(Trejo-Téllez and Gómez-Merino, 2012). 결국 배양액의 적정 pH 범위를 벗어난 pH 5.0-7.0에서 인산의 이온 형태가 HPO4-2와 H2PO4-의 급격한 변화가 나타나 EC의 변량에 대하여 보다 크게 영향을 주어 배양액 내 무기이온 불균형을 초래하는 것으로 생각된다. 따라서 직접적으로 EC의 변화를 일으키는 이온 총량을 추정하면 인산 이온의 형태 구배가 EC 변화에 어느 정도 영향을 주는지 명확히 알 수 있다.
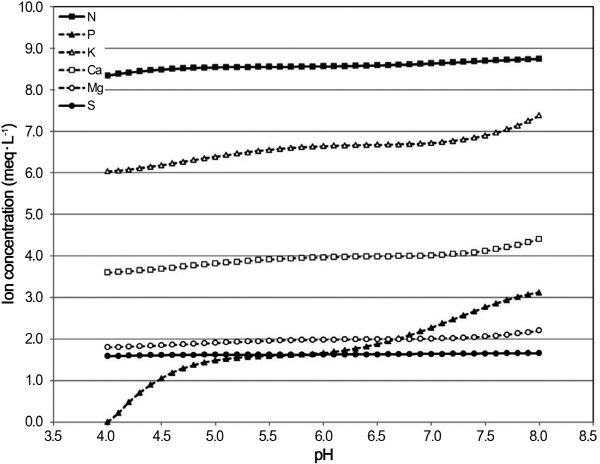
Robinson and Strokes(1959)와 Tanji(1960)의 등가 이온 방법에 배양액 내 pH 변화에 따른 이온 함량의 변화를 추정하였다(Fig. 2). 배양액 내 pH가 낮아질수록 S를 제외한 무기 이온들이 감소하였고, pH가 높아질수록 S를 제외한 무기 이온들이 증가하였다. 배양액 내 pH 변화에 따른 각 이온의 변화량을 보면 K, Ca, N, P은 상승하였다. pH가 상승함에 따라 배양액 내 K는 6.03-7.38meq・L-1로 가장 큰 변화를 보였고, Ca은 3.60-4.41meq・L-1로 나타났다. Total N는 pH가 상승함에 따라 8.34-8.74meq・L-1를 보여 비교적 완만한 상승을 나타냈다. 그러나 P은 pH가 상승함에 따라 0.00-3.11 meq・L-1로 그 변량이 크게 나타냈다. 이러한 변화는 Steiner (1980)의 mutual ratio에 의한 배양액 모형에서 K+, Ca+2, Mg+2의 다량 양이온의 변량에 대한 인산 이온의 보정에 의한 가정을 따른 것이다. 따라서 P의 변량의 결과값보다 배양액 내 pH 변화가 P의 이온 형태의 변화를 야기되었다는 사실이 다시 확인할 수 있다.
|
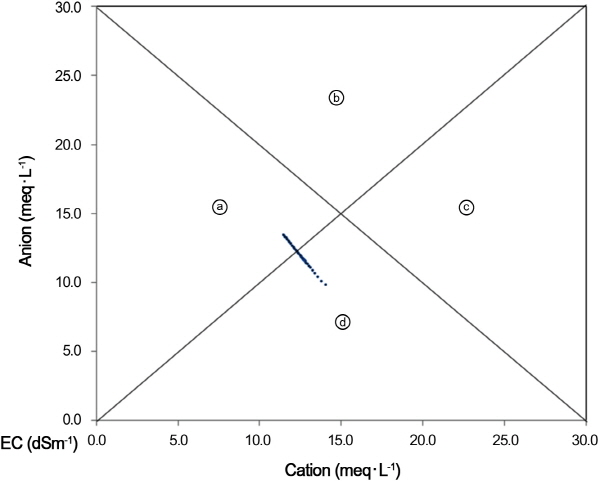
Fig. 3. Analysis of ion balance among cation, anion, and EC depending on the pH. ⓐ: low cation and EC, ⓑ: high anion and EC, ⓒ: high cation and EC, ⓓ: low cation and EC. |
이러한 pH 변화가 배양액 내 양이온 변량, 음이온 변량, EC 변량에 대하여 어떠한 영향을 주는지 구명하기 위해 Soh et al.(2012)에 의한 이온균형모형에 따라 분석하였다(Fig. 3). 이온균형모형은 양이온과 음이온을 대각선 방향으로 4개의 분면으로 구획하여 이온 밸런스를 분석할 수 있다. 또한 하단 좌측에서 상단 우측의 대각선은 EC 변화율을 나타내어 전체적인 양수분 흡수 특성을 알 수 있다. 상단 좌측에서 하단 우측의 대각선은 양이온과 음이온간의 변화를 볼 수 있기 때문에 이들 변화에 따라 작물의 이온 흡수 특성을 보여준다. 또한 구획 중 a분면은 음이온 비율이 높고 EC가 낮은 배양액, b분면은 음이온 비율이 높고 EC가 높은 배양액, c분면은 양이온 비율이 높고 EC가 높은 배양액, d분면은 양이온 비율이 높고 EC가 낮은 배양액이다. 따라서 0점과 30점의 EC 극점을 연결한 EC 중앙선에 근접할수록 양이온과 음이온의 균형이 잘 이루어진 배양액이라고 하였다(Soh et al., 2012). 이와 같이 양이온과 음이온의 구배는 배양액 내 OH-와 H2PO4-의 함량 비율 변화에 따라 작물이 K+과 Ca+2의 흡수 특성 변화에 영향을 준다(Steiner, 1961).
배양액 내 pH 변화에 의해 양이온과 음이온의 함량 비율이 a분면에서 d분면으로 이동하였지만, EC의 변량은 이온 변량과 비교하여 그 변화량이 크지 않았다. 배양액 내 pH 변화에 의해 낮은 EC 농도와 음이온이 상대적으로 많이 분포하는 특성을 보이는 a분면에서 높은 EC 농도와 양이온이 상대적으로 많이 분포하는 d분면으로 이동하였다. 따라서 배양액 내 pH 변화가 EC 변화보다 양이온과 음이온의 당량 비율을 크게 변화시켜는 것으로 나타났다. 이처럼 배양액 내 a분면과 d분면간의 대칭 이동은 배양액 내 EC 변화는 거의 나타나지 않고, 양이온과 음이온간 이온 밸런스의 변화가 심하게 나타났다는 것을 의미한다. 따라서 pH의 변화가 배양액 내 무기 이온의 균형을 크게 변화시키는 것으로 pH 변화에 따라 작물의 무기이온 흡수 특성뿐만 아니라 순환식 배양액에서 pH 변화에 의해 무기 이온 함량까지 변화시킨 것으로 나타났다. 배양액 내 pH가 5.0 이하이거나 7.0 이상에서는 EC 중앙선으로부터 점점 멀어지는 것으로 나타나 이온 불균형이 증가되는 것을 알 수 있다. Steiner(1980)의 mutual ratio 모형은 초기 설계 과정에서 이온 당량비의 합계에서 발생하는 불균형과 pH 불균형을 인산의 이온 형태에 따른 분압으로 보정하도록 가정하고 있는데, 이 과정에서 K+와 Ca+2의 함량 비율이 OH-와 H2PO4-의 변화에 크게 영향을 준다(Steiner, 1961). 따라서 HPO4-2와 H2PO4-의 변량에 대한 K+와 Ca+2의 함량비를 통해 pH와 EC의 변량에 어느 정도 영향을 주는지 구명되어야 한다.
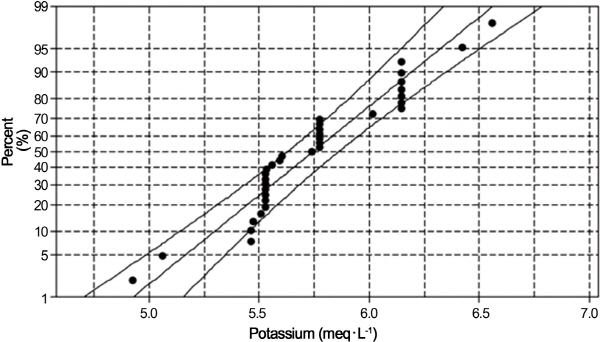
배양액 내 Soh and Lee(2012)에 따른 pH 변량에 대한 K+/Ca+2의 당량비를 통한 보정과 Rush(2005)에 따른 배양액 농도 변화에 따른 이온 밸런스 특성을 살펴보기 위해 각각 1, 10, 50, 100 배율로 설계하여 pH, K+, Ca+2, EC의 변량을 분석하였다. 이를 위해 pH 변량에 따른 K+, Ca+2, EC의 신뢰도 검정을 수행하였다(Fig. 4). 대부분의 K+, Ca+2, EC의 표본값이 신뢰 수준 p = 0.05 안에 포함되는 것으로 나타나 Steiner(1980)가 제안한 mutual ratio 배양액 모형에서 pH 보정값을 K+와 Ca+2의 당량비의 설계가 가능한 것으로 확인되었다.
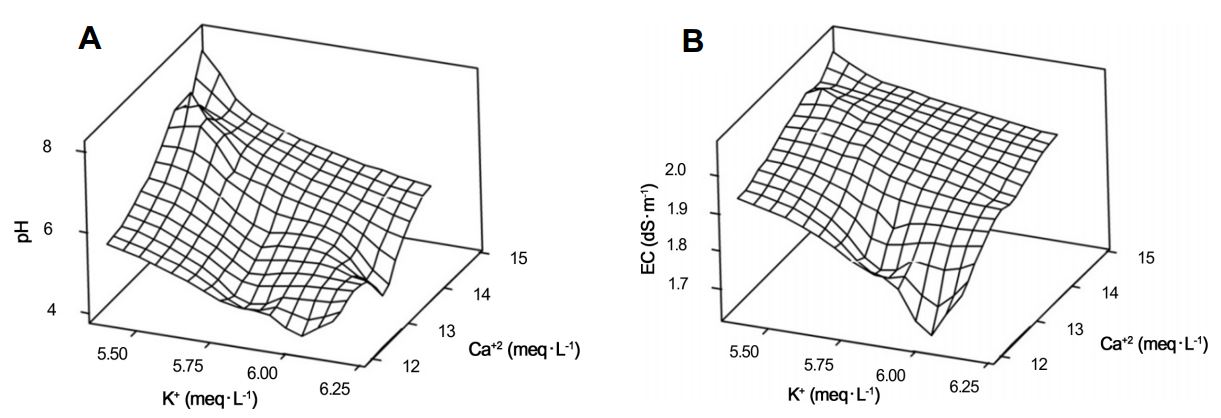
배양액 pH 보정을 K+/Ca+2의 당량비 조성하였을 때, K, Ca, pH의 변량 그리고 이로 인한 K, Ca, EC의 변량을 분석하였다(Fig. 5). K, Ca, pH 간의 관계에서 pH가 상승할수록 K은 감소하였지만 Ca은 증가하는 경향을 보였는데, K+과 Ca+2의 당량비 보정에서 Ca의 당량이 K의 당량과 비교해 2배의 이온가를 가지기 때문이다. K, Ca, EC 간의 관계는 pH, K, Ca의 관계보다 급격한 변화를 보였다. 이는 pH 보정을 K+/Ca+2의 당량비로 산출할 경우 이온 함량 변화에 직접적인 영향을 주기 때문이다. 따라서 K+/Ca+2의 당량비를 통한 보정이 pH 변화에 어느 정도 효과적인지 구명할 필요가 있다.
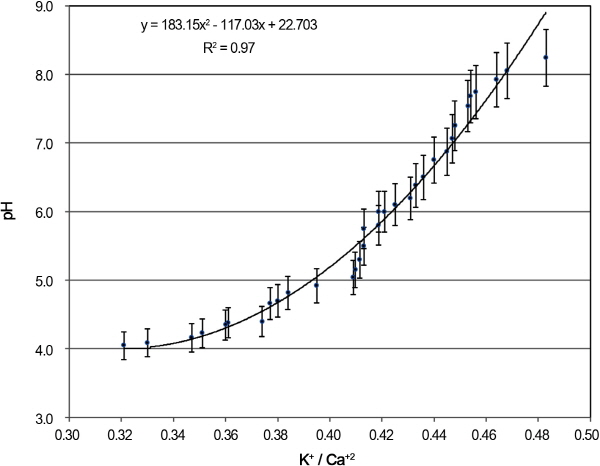
상기의 K와 Ca의 당량비 보정에 따라 pH의 변화를 분석하였다(Fig. 6). K+/Ca+2의 값이 감소하면 pH는 감소하고, K+/Ca+2의 값이 증가하면 pH는 증가하였다. 이는 Steiner(1984)의 K+/Ca+2와 OH-/H2PO4-의 함량비율에 대한 보고와 일치하는 것으로 회귀 계수 0.97의 높은 정의 관계가 구명되었다. 특히 K과 Ca의 양이온에 의한 HPO4-2와 H2PO4-가 균등한 보정이 이루어지는 과정에서 이온가 2의 Ca과 기준 농도가 높은 K이 순환식 배양액에서 Ca보다 등가 이온 총량에 대한 기여도가 높기 때문이다(Soh and Lee, 2012). 고추와 토마토의 순환식 수경재배에서도 배양액 내 K와 Ca의 함량 변화가 나타나는데(Ahn et al., 2010), 특히 생식 생장기에 들어 K의 변화가 심하게 나타나고 이로 인한 pH 변화도 함께 유발된다고 하였다(Masuda et al., 1989). 따라서 순환식 배양액에서 H+와 OH- 구배는 Ca과 K에 의한 HPO4-2와 H2PO4-의 변량에 크게 작용하는 것으로 생각된다. 본 연구를 통해 HPO4-2와 H2PO4-의 구배에 따른 pH, 이온, EC의 변량에 관한 pH 변량 모형이 구명되었다.