서 언
재료 및 방법
식물재료
UV-VIS Spectrophotometer를 이용한 Chlorophyll a, b/Carotenoids 측정
UV-VIS Spectrophotometer을 이용한 Total Flavonoids 측정
UV-VIS Sspectrophotometer을 이용한 Total Phenolics 함량 측정
FT-IR 스펙트럼 조사 및 스펙트럼 데이터 다변량 통계분석
아프리칸 얌 구근으로부터 Total Carotenoids, Flavonoids 및 Phenolics 함량 예측 PLS 모델링
결과 및 고찰
아프리칸 얌 구근으로부터 Total Carotenoids, Flavonoids 및 Phenolics 함량 조사
아프리칸 얌 시료의 FT-IR 스펙트럼 비교분석
아프리칸 얌 시료의 FT-IR 스펙트럼 데이터 다변량통계분석
아프리칸 얌의 FT-IR 스펙트럼으로부터 Total Carotenoids, Flavonoids 및 Phenolic 함량 예측 PLS Regression 모델링
서 언
아프리칸 얌은 주로 아프리카 지역에서 재배되고 있는 다년생작물로, 카사바, 감자, 고구마와 같이 전분 함량이 높아 중요한 식량자원으로 이용되고 있다. 얌의 구근은 전분질 15-20%, 단백질 1-1.5%, 지질 1% 및 기타 미네랄 및 비타민 등을 함유하고 있다(Adeleke, 2010; Kwon et al., 2010). 또한 얌의 구근에는 다양한 약리적 활성을 갖는 유용 기능성물질, saponin, tannin, sitosterol, diosgenin, carotenoid, flavonoid, polyphenol, allantoin, araginine, mucin 등을 함유하고 있어 약용작물로서 활용 가치가 매우 높은 식물이다(Kim et al., 2009; Kum et al., 2006; Kwon et al., 2010). 특히 얌의 구근에 존재하는 다양한 페놀성 화합물들은 자유 라디칼 제거, 항산화 효과 및 항염증 작용 등 다양한 약리적 기능을 가지고 있다(Yang et al., 2009; Yao et al., 2004). 따라서 얌은 자양, 강장, 폐결핵, 고혈압, 당뇨병, 스트레스와 피로 회복에 효능이 알려져 있다(Song et al., 2010; Yoon et al., 1989). 이처럼 아프리칸 얌은 식용 및 약용작물로서 가치가 높은 작물이지만 주요 성분에 대한 정확한 분석이 활발하게 이루어지지 않고 있다. Im et al.(1995)은 아프리칸 얌의 경우 사포닌, 알칼로이드, 페놀성 성분이 국내산 얌에 비해 높아서 보다 쓴맛이 강하다고 보고하였다. 따라서 식량 및 약리적 측면에서 우수한 아프리카 얌의 농업적 활용 기반 구축을 위해 다양한 아프리카산 얌의 기능성 성분 분석이 이루어져야 할 것으로 사료된다. 아울러 기능성 성분분석 데이터를 기반으로 고기능성 얌 라인의 신속한 선발시스템 확립이 이루어져야 할 것으로 사료된다.
유용 기능성 물질들의 정량 및 정성분석은 주로 gas chro-matography(GC)나 high performance liquid chromatography (HPLC) 및 질량분석기와 연계를 통해 정확한 성분의 정량 및 정성 분석이 이루어진다(Aktumsek et al., 2013; Kimura et al., 2002). 그러나 이러한 분획 컬럼을 통한 기능성 성분 정량 분석의 경우 분석 결과는 매우 정확하지만, 상대적으로 시료의 준비과정이 복잡하며, 추출 및 시료 분석 비용이 많이 소요되고, 다수의 시료를 분석할 경우 많은 시간이 요구되는 한계점을 가지고 있다(Yuan et al., 2013). 이러한 정량 및 정성분석의 복잡성 문제를 해결하기 위한 하나의 대안으로 ultraviolet-visible(UV-VIS) spectrophotometer를 이용한 기능성 성분들의 신속한 함량 조사가 가능함이 보고되고 있다(Kofalvi and Nassuth, 1995; Stadnik and Buchenauer, 2000; Zhishen et al., 1999).
최근 오믹스 연구기법의 발달에 힘입어, 대사체 수준에서 시료간의 양적, 질적 패턴 차이를 구명하는 대사체학 연구가 활발하게 이루어지고 있다. 대사체 연구는 주로 Fourier transform infrared(FT-IR) spectroscopy, proton nuclear magnetic resonance(HNMR) spectroscopy 및 mass spectrometry(MS) 등의 분석 데이터를 이용하여 진행되고 있으며 각종 시료의 식별 및 대사체 마커 개발에 활용이 되고 있다(Krishnan et al., 2005). 특히, FT-IR 분석 방법은 스펙트럼이 가지고 있는 다양한 정보를 다변량통계분석을 이용하여 신속하고 정확하게 구분할 수 있다(Gallardo-Velázquez et al., 2009). 따라서 대사체체 기은법 대사성분의 작용기작 구명 등 기초학문적 활용은 물론 농산물의 품종, 원산지, 재배연령, 진위 식별, 식품이나 의약품 산업의 표준화 및 안정성 관련 다양한 활용이 가능하다. 대사체 분석데이터로부터 보다 유용한 생물학적 정보를 추출하기 위하여 다양한 다변량통계분석 기법이 필수적으로 동반되고 있다. 이중에서 대표적인 다변량통계분석기법중 하나인 partial least squares(PLS) regression은 시료로부터 정확한 정량분석 데이터와 동일시료의 스펙트럼 데이터의 상관분석을 통해 다양한 성분들의 함량 예측 모델링 방법으로 활용이 이루어지고 있다(Bastiena et al., 2005; Höskuldsson, 1988; Mevik and Wehrens, 2007; Wold et al., 2001). 최근에는 PLS regression 기법을 이용하여 동백나무속 식물(Camellia oleifera)에서 지방산 함량 예측 모델링(Yuan et al., 2013), 사과, 오렌지 그리고 복숭아 주스에 함유되어 있는 carotenoid 성분 함량 예측 모델링(Leopold et al., 2011), 버섯에 존재하는 단당류와 다당류 함량 예측 모델링(Chen et al., 2012), 육류의 부패 및 손상에 대한 예측 모델링(Argyri et al., 2013)이 가능한 것으로 보고되고 있으며 예측정확도 또한 매우 높아 산업적 활용 측면에서 실용화 가능성이 매우 높아지고 있는 실정이다.
따라서 본 연구에서는 FT-IR 스펙트럼 데이터의 다변량통계분석 기법을 이용하여 아프리칸 얌의 신속한 구분 및 식별체계를 확립하고 더 나아가 아프리칸 얌의 구근에 존재하는 total carotenoids, flavonoids, phenolic compounds의 신속한 함량예측 모델링을 개발하여 기능성 성분이 우수한 아프리칸 얌의 신속한 선발체계를 확립하고자 하였다.
재료 및 방법
식물재료
본 연구에 사용된 아프리칸 얌(Dioscorea)은 탄자니아 넬슨만델라 아프리카과학기술원 생명공학대학으로부터 제공받은 아프리칸 얌 구근을 사용하였다. 실험에 사용된 각각의 얌 라인은 Dioscorea alata 15라인, D. bulbifera 6라인, D. cayensis 5라인, D. dumetorum 13라인, D. rotunalata 12라인, D. mangenotiana 1라인, D. prahensilis 2라인 그리고 분류학적 동정이 이루어지지 않은 케냐의 얌 시료 8라인 등 총 62라인을 사용하였다(Table 1). 건조된 아프리칸 얌 구근은 막자와 막자사발을 이용하여 미세한 분말로 분쇄하였으며 -70°C 초저온냉동고에 보관하면서 실험에 사용하였다.
UV-VIS Spectrophotometer를 이용한 Chlorophyll a, b/Carotenoids 측정
아프리칸 얌으로부터 total carotenoids 함량은 Yang et al. (1998)의 방법을 이용하여 UV-VIS spectrophotometer(DU®730, BECKMAN COULTER, Brea, CA, America)를 통해 조사하였다. 아프리칸 얌 분말 시료 20mg을 80% acetone 1mL이 들어있는 tube에 넣어주고 용매와 잘 섞이도록 흔들어 주었다. 용매와 잘 섞인 시료를 상온에서 13,000rpm으로 5분간 원심분리 하였다. 원심분리가 끝난 후 시료의 상징액을 새로운 tube에 옮겨 주었다. 새로운 tube에 옮겨진 추출물을 흡광도가 0.3-0.85이 되도록 희석하였고, 350-750nm 측정범위에서 > 2nm 간격으로 UV-VIS spectrophotometer를 이용하여 흡광도를 측정하였다. 측정된 흡광도로부터 Lichtenthaler Lichtenthaler and Buschmann(2001)의 방법을 이용하여 아프리칸 얌 시료로부터 total carotenoids 함량을 조사하였고 함량계산식은 다음과 같다.
Ca (μg・L-1) = 12.25*A663-2.79*A647
Cb (μg・L-1) = 21.50*A647-5.1*A663
C(x+c) (μg・L-1) = (1000*A470-1.82*Ca-85.02*Cb)/198
함량계산식에 사용된 Ca는 chlorophyll a, Cb는 chlorophyll b를 나타낸다. 또한, C(x+c)에서 x+c는 xanthophylls와 carotenes의 합을 total carotenoids 함량을 나타낸다. 측정된 값은 ANOVA를 이용하여 유의성을 판별하였다.
UV-VIS Spectrophotometer을 이용한 Total Flavonoids 측정
아프리칸 얌으로부터 total flavonoids 함량은 Zhishen et al.(1999)의 방법을 이용하여 UV-VIS spectrophotometer를 통해 조사하였다. 아프리칸 얌 시료 10mg을 absolute ethanol 1mL 들어가 있는 tube에 넣어주었다. 용매와 잘 섞이도록 흔들어준 후 1시간 동안 상온에서 반응 시켰다. 반응이 끝난 시료를 상온에서 13,000rpm으로 5분간 원심분리하고, 원심분리가 끝난 시료의 상징액 100μL를 새로운 tube에 옮겼다. 옮겨진 시료 100μL에 2차 증류수 400μL를 첨가하여 혼합한 다음 5% NaNO2 30μL를 첨가하여 상온에서 10분간 반응시켰다. 10분간 반응이 끝난 후 10% AlCl3 용액 30μL를 첨가하여 상온에서 다시 1분간 반응시켰다. 반응이 끝난 후 1M NaOH 200μL를 첨가하여 반응액의 최종 부피가 1mL가 되도록 2차 증류수 240μL를 첨가하였다. 준비된 시료는 UV-VIS spectrophotometer를 이용하여 510nm 파장에서 흡광도를 측정하였다. Reference compounds로는 catechin(100mg・L-1)을 사용하여 조사하여 total flavonoids 함량을 측정하였다. 측정된 값은 ANOVA를 이용하여 유의성을 판별하였다.
UV-VIS Sspectrophotometer을 이용한 Total Phenolics 함량 측정
아프리칸 얌으로부터 total phenolics compounds 함량은 Wu et al.(2007)의 방법을 이용하여 UV-VIS spectrophotometer를 통해 조사하였다. 아프리칸 얌 시료 10mg을 80% ethanol 50μL가 들어가 있는 tube에 넣어주었다. 용매와 잘 섞이도록 흔들어준 후 95°C에서 5분간 가열하여 추출하였다. 추출된 시료는 상온에서 12,000rpm으로 15분간 원심분리하고, 원심분리가 끝난 시료의 상징액 20μL를 새로운 tube에 옮겼다. 옮겨진 추출물 20μL에 2N Folin-Ciocalteu reagent 50μL와 20% Na2CO3 100μL를 첨가하고 최종 부피가 1mL가 되게 2차 증류수 830μL를 첨가하여 준비하였다. Control로 사용될 용액은 2차 증류수 850μL에 2N Folin-Ciocalteu reagent 50μL와 20% Na2CO3 100μL를 첨가하고 최종 부피가 1mL가 되게 준비하였다. 표준물질은 20μL ethanol이 포함된 chlorogenic acid에 2N Folin-Ciocalteu reagent 50μL와 20% Na2CO3 100μL를 첨가하고 최종 부피가 1mL가 되도록 2차 증류수 830μL를 첨가하여 부피를 조정하였다. 준비된 시료는 상온에서 20분간 반응 시킨 후에 UV-VIS spectrophotometer를 이용하여 725nm 파장에서 흡광도를 조사하였다. 측정된 값은 ANOVA를 이용하여 유의성을 판별하였다.
FT-IR 스펙트럼 조사 및 스펙트럼 데이터 다변량 통계분석
아프리칸 얌 62개의 구근 분말 20mg을 tube에 넣고 20% methanol 용액을 200μL씩 첨가하여 잘 섞어주었다. 각 tube를 50°C 수조에서 20분간 반응시킨 다음 13,000rpm에서 15분간 원심분리한 후 상징액을 새로운 tube에 옮겼다. 회수한 상징액은 원심분리과정을 반복하여 찌꺼기가 들어가지 않도록 조심스럽게 새로운 tube에 상징액을 옮겼다. 회수된 상징액은 -20°C에서 보관한 다음 FT-IR 스펙트럼 조사에 사용하였다.
FT-IR(Fourier transform infrared) 스펙트럼 조사는 Tensor 27(Bruker Optics GmbH, Ettlingen, Germany)를 사용하였고, DTGS(deuterated triglycine sulfate) 검출기로 분석하였다. 추출된 각각의 시료 5μL를 384-well ZnSe plate에 분주하여, 37°C hot plate에서 약 20분간 건조하였다. 건조된 ZnSe plate는 Tensor 27에 장착된 HTS-XT(Bruker Optics GmbH) 고효율 자동화 장치를 이용하여 스펙트럼을 조사하였다. 각 시료의 스펙트럼은 총 4,000-400cm-1 범위에서 그리고 4cm-1 간격으로 총 128회 반복 측정된 평균 스펙트럼을 분석에 사용되었다. 각 시료의 FT-IR 스펙트럼은 통계적 분석을 위해 각각 3반복 측정하였다. FT-IR 스펙트럼 조사 및 데이터 변환에 사용된 프로그램은 Bruker에서 제공하는 OPUS Lab(ver. 6.5, Bruker Optics Inc.)를 사용하였다. FT-IR 스펙트럼 데이터의 다변량 통계분석을 위해 먼저 FT-IR 스펙트럼 데이터의 baseline 교정, normalization 및 mean centering 등 스펙트럼의 전처리 과정을 R 프로그램(version 2.15.0, Auckland, New Zealand)을 이용하여 수행하였다. Baseline 교정을 위해 FT-IR 스펙트럼 분석 영역의 양 끝점(1,800-800cm-1)의 흡광도를 0으로 조정하였으며 실험상의 오차를 최소화하기 위하여 각 스펙트럼을 동일 면적으로 normalization 하였다. 이후 데이터의 mean centering 과정을 거쳐 2차 미분을 수행한 다음 전처리가 완료된 스펙트럼 데이터를 다변량 통계분석 분석을 위한 표준화된 데이터로 사용하였다. 가공된 FT-IR 스펙트럼 데이터는 NIPALS 알고리즘(Wold, 1966)을 이용하여 R 프로그램(version 2.15.0)에서 PCA(Principal component analysis)와 PLS-DA(Partial least square discriminant analysis) 분석(Fiehn et al., 2000; Trygg et al., 2007)을 수행하였다.
아프리칸 얌 구근으로부터 Total Carotenoids, Flavonoids 및 Phenolics 함량 예측 PLS 모델링
아프리칸 얌 구근의 FT-IR 스펙트럼 데이터로부터 total carotenoids, flavonoids, phenolics 함량 예측 모델을 개발하였다. 총 62개 아프리칸 얌 시료의 FT-IR 스펙트럼 데이터와 동일 시료로부터 얻어진 total carotenoids, flavonoids, phenolics 함량 실측 정량 데이터를 이용하여 X 변수에는 FT-IR 스펙트럼 데이터를 사용하였고, 3개의 Y 변수에는 UV-VIS spectro-photo-meter를 통해 얻어진 total carotenoids, flavonoids, phenolics 함량 정량 데이터를 각각 사용하였다. PLSR(partial least square regression) 분석은 R 프로그램(version 2.15.0)을 이용하였다. 예측 모델링의 정확도를 향상시키기 위하여 1개의 X 변수에 대해 3개의 Y 변수를 각각 교차검정을 실시하였다. 확립된 예측 모델링을 이용하여 각각의 아프리칸 얌 시료의 total carotenoids, flavonoids 및 phenolics 함량 예측을 수해하였다. 함량 예측 모델링의 정확도를 조사하기 위하여 아프리칸 얌 시료로부터 total carotenoids, flavonoids 및 phenolics 함량 실측치와 예측치에 대한 선형회귀분석을 수행하여 상관계수를 조사하였다.
결과 및 고찰
아프리칸 얌 구근으로부터 Total Carotenoids, Flavonoids 및 Phenolics 함량 조사
UV-VIS spectrophotometer를 이용하여 아프리칸 얌 구근에 존재하는 total carotenoids, flavonoids 및 phenolics 함량을 조사하였다(Table 1). 여러 아프리칸 얌 종들에 대한 각각의 성분에 대한 유의한 차이를 보이는지를 ANOVA 프로그램을 통해 평가한 결과 유의성(P < 0.05)이 있는 차이를 보였다. Total carotenoids 함량은 D. bulbifera가 0.61μg・g-1 dry weight(wt)로 아프리칸 얌 종 가운데서 가장 높았으며 다음으로 D. prahensilis 및 D. dumetorum이 각각 0.59 및 0.53μg・g-1 dry wt로 나타나 total carotenoids 함량이 높은 종임을 알 수 있었다. 반면에 D. alata와 D. cayensis는 다른 아프리칸 얌 종들에 비해 total carotenoids 함량이 낮은 종임을 알 수 있었다(Table 1). Total flavonoids 함량의 경우, D. dumetorum이 171μg・g-1 dry wt으로 가장 함량이 높은 종으로 나타났으며, D. bulbifera 가 다음으로 total flavonoids 함량이 높은 종임을 알 수 있었다. 아직까지 정확한 종의 동정이 이루어지지 않은 시료인 Dioscorea spp의 경우 비교적 total flavonoids 함량이 높은 종임을 알 수 있었다(Table 1). D. alata와 D. cayensis는 carotenoids의 함량분석 결과와 마찬가지로 total flavonoids 함량이 가장 낮은 종으로 나타났다. Total phenolic 함량의 경우 D. dumetorum이 3.56mg・g-1 dry wt로 가장 높은 종이며, carotenoids와 flavonoids 함량이 낮았던 D. alata가 다른 아프리칸 얌 종들에 비해 함량이 높음을 알 수 있었다(Table 1). 아프리칸 얌 시료의 기능성 성분 정량분석 결과를 보면, total flavonoids와 phenolics 함량에 비해 total carotenoids 함량이 낮게 나타났으며, total flavonoids와 phenolics 함량은 각각의 아프리칸 얌 종들 사이에 함량 차이가 매우 크게 나타남을 알 수 있었다(Table 1). 이 결과는 Yang et al.(2009)이 얌에 존재하는 total carotenoids, flavonoids, phenolics 함량 등 기능성 성분들의 경우 종에 따라서 질적 차이는 물론 양적 차이가 매우 크다는 보고와 일치한다.
아프리칸 얌 시료의 FT-IR 스펙트럼 비교분석
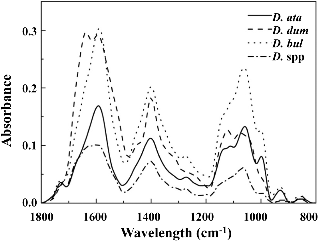
아프리칸 얌 시료로부터 전세포 추출물의 FT-IR 스펙트럼 데이터 다변량통계분석을 통해 아프리칸 얌의 대사체 수준에서 종간 유연관계 구명 및 식별체계를 확립하였다. 각 아프리칸 얌 시료의 FT-IR 스펙트럼을 비교한 결과 아프리칸 얌 시료들은 FT-IR 스펙트럼상의 1,700-1,500, 1,500-1,300, 1,100-950cm-1 부위에서 대사체의 양적, 질적 패턴 변화가 크게 이루어짐을 알 수 있었다(Fig. 1). FT-IR 스펙트럼의 1,700-1,500, 1,500-1,300 그리고 1,100-950cm-1 부위는 각각 아미노산 및 단백질의 amide bond I과 II, 핵산 및 인지질로부터 phosphodiester bond 및 인을 포함하는 유기산, 그리고 단당류나 복합 다당류를 포함하는 carbohydrates 계열의 화합물들의 질적, 양적 정보를 반영한다(D’Souza et al., 2008; Dumas and Miller, 2003; Lopez-Sanchez et al., 2010; Parker, 1983; Wolkers et al., 2004; Yee et al., 2004). 즉 FT-IR 스펙트럼 상의 질적, 양적 차이는 아프리칸 얌에 함유되어 있는 아미노산이나 단백질, 지방산, 그리고 탄수화물계통의 화합물들의 질적, 양적 차이가 현저하게 나타남을 의미한다. 따라서 FT-IR 스펙트럼 분석은 아프리칸 얌 시료들 사이에서 주요 대사체의 질적, 양적 변화를 조사하고 이들 화합물의 함량이 높은 계통이나 라인의 신속한 선발 수단으로 활용이 가능할 것으로 기대된다.
아프리칸 얌 시료의 FT-IR 스펙트럼 데이터 다변량통계분석
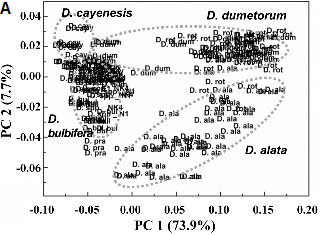
FT-IR 스펙트럼 데이터의 PCA 분석 결과 PC 1과 2 score는 전체 변이량의 각각 75.8%, 7.3%의 설명력을 갖고 있으며 이는 전체 변이량의 약 83.1%를 반영하고 있음을 알 수 있었다(Fig. 2A). 이처럼 설명력이 높은 PC1과 PC2를 기준으로 아프리칸 얌 시료들의 PCA score plot을 관찰한 결과, 아프리칸 얌 시료들은 PC 1을 기준으로 크게 좌우로 구분이 이루어지는 것을 관찰할 수 있었다. PCA score plot 상의 좌측에는 D. cayenesis, D. bulbifera, D. mangenotiana, D. prahensilis와 Dioscorea spp. Kenyan 종들이 주로 위치하였으며, 우측에는 D. alata, D. dumetorum과 D. rotundata 종들이 위치하였다. 이들 아프리칸 얌 시료들을 PC 2를 기준으로 보면 상하로 집단의 분포가 이루어짐을 알 수 있었다. 위쪽에는 D. dumetorum, D. rotundata에 속하는 시료들이 주로 분포하였으며, 반대로 아래쪽에는 주로 D. alata 시료들이 분포함을 알 수 있었다(Fig. 2A).
아프리칸 얌 시료의 PCA score plot상에서 공간적인 분포위치가 주는 생물학적인 정보를 파악하기 위하여 먼저 아프리칸 얌 시료들의 기능성 성분들 함량 차이 결과(Table 1)와 PCA score plot상의 이들 시료들의 위치와 상관관계를 조사하였다. Total carotenoids, flavonoids이 비교적 낮았던 시료인 D. alata의 경우 재미있게도 PCA score plot상에서 우측 하단에 별도의 그룹을 형성하였으며, 반대로 total carotenoids, flavonoids 및 phenolic 함량이 가장 높았던 시료인 D. dumetorum의 경우 PCA score plot상에서 우측 상단에 별도의 그룹을 형성하며 분포하는 것을 관찰할 수 있었다. 이상의 결과를 미루어볼 때 PCA score plot상에서 공간적인 분포위치와 이들 시료의 기능성 성분들 total carotenoids, flavonoids 및 phenolic의 함량과 밀접한 상관관계가 있음을 알 수 있었다.
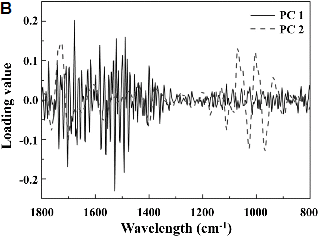
PCA score plot 상에서 기능성 성분들의 함량에 따른 아프리칸 얌 시료들의 집단 구분 및 클러스터링에 중요한 역할을 하는 FT-IR 스페트럼 부위를 조사하기 위하여 PC 1과 2를 결정하는데 중요한 FT-IR 스펙트럼 부위를 조사하였다(Fig. 2B). Loading value 분석 결과 아프리칸 얌 시료의 좌우 구분에 중요한 PC 1을 결정하는 중요한 FT-IR 스펙트럼 부위는 주로 1,700-1,500과 1,500-1,300cm-1 region임을 알 수 있었고, 얌 시료의 상하 구분에 중요한 PC 2의 경우 주로 1,100-950cm-1 region임을 알 수 있었다(Fig. 2B). 이들 FT-IR 스펙트럼 부위는 아프리칸 얌 시료의 FT-IR 스펙트럼 비교에서 보였던 차이가 큰 부위(Fig. 1)와 일치하는 것으로 amide I, II, 지방산과 carbohydrates 계열의 화합물들의 질적, 양적 차이가 아프리칸 얌의 대사체 수준 식별에 중요한 역할을 하고 있음을 의미하는 결과라 사료된다(Fig. 2B). 특히 기능성 성분들의 함량 차이에 따른 아프리칸 얌 시료의 구분에 있어서 중요한 역할을 하는 PC 2의 경우 carbohydrates 계열의 화합물들의 질적, 양적 차이가 크게 영향을 줌을 알 수 있었다. 이 결과로 미루어 볼 때 이들 당 계열의 일차대사산물들의 양적 변화가 이차대사산물의 질적, 양적 변화와 양의 상관관계에 놓여 있음을 의미하는 결과라 사료된다.
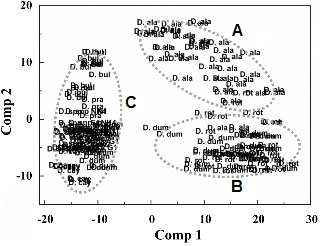
PLS-DA 분석의 경우 PCA 분석보다 더욱 확실하게 아프리칸 얌 시료들의 그룹 식별이 가능하였다(Fig. 3). 각각의 아프리칸 얌 시료들의 그룹 경계는 PCA에 비해 더욱 작아졌으며 동일 종에 속하는 각 시료들의 반복구들도 각 그룹내에 위치하여 PCA보다 아프리칸 얌의 식별능력이 향상되었음을 알 수 있었다. Total carotenoids, flavonoids 함량이 비교적 낮았던 시료인 D. alata의 경우 PCA score plot상에서 우측 상단에 별도의 그룹을 형성하였으며, 반대로 total carotenoids, flavonoids 및 phenolic 함량이 가장 높았던 시료인 D. dumetorum의 경우 PLS-DA score plot상에서 D. rotundata와 함께 우측 하단에 별도의 그룹을 형성하며 분포하는 것을 관찰할 수 있었다. 기능성 성분들의 함량이 중간인 그룹은 주로 좌측에 분포하였다(Fig. 3). 이상의 결과를 미루어볼 때 PCA와 마찬가지로 PLS-DA 역시 각 아프리칸 얌 시료들의 sccore plot상에서 공간적인 분포위치와 이들 시료의 기능성 성분들 total carotenoids, flavonoids 및 phenolic의 함량과 밀접한 상관관계가 있음을 알 수 있었다.
아프리칸 얌의 FT-IR 스펙트럼으로부터 Total Carotenoids, Flavonoids 및 Phenolic 함량 예측 PLS Regression 모델링
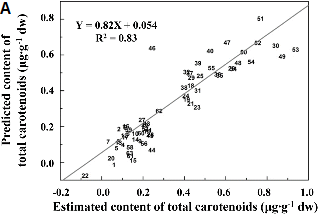
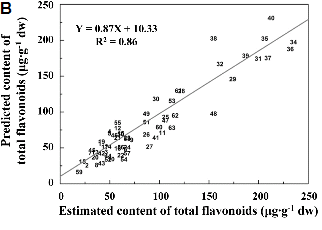
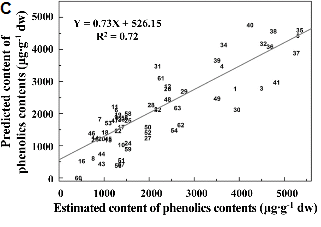
FT-IR 스펙트럼 데이터와 UV-VIS spectrophotometer를 이용하여 측정된 total carotenoids, flavonoids 그리고 phenolic 함량 데이터를 이용하여 각 성분별 함량 예측 PLS 모델링을 개발하였다(Fig. 4). Total carotenoids의 경우, PLS 모델링을 통해 FT-IR 스펙트럼 데이터로부터 예측된 함량 값과 동일 시료의 실측 함량 값을 이용하여 회귀분석을 수행한 결과 상관계수가 R2 = 0.83로 높게 나타났다(Fig. 4A). Total flavonoids와 total phenolic의 함량 예측 모델링을 통한 선형회귀분석 상관계수는 각각 R2 = 0.86(Fig. 4B) 및 0.72(Fig. 4C)로 나타났다. 이들 결과는 얌 시료의 FT-IR 스펙트럼 데이터 만으로도 이들 시료 내에 존재하는 total carotenoids, flavonoids 및 phenolic의 함량을 80-90% 정도 정확성으로 함량을 예측할 수 있는 결과라 사료된다. 아직 아프리칸 얌 시료에서 carotenoid 함량 예측 모델링 연구가 보고된 바 없어 정확한 비교는 어렵지만 carotenoid 함량이 높은 당근의 경우 FT-IR 스펙트럼과 total carotenoids 함량의 상관관계 분석을 통해 상관계수(R2)가 0.9정도임이 보고된 바 있다(Zude et al., 2008). Total flavonoids와 total phenolics의 함량 예측의 경우 커피(Páscoa et al., 2013)에서 보고된 바 있으며 이 경우 함량 예측 모델링의 상관계수는 각각 R2 = 0.94, R2 = 0.94로 본 연구에서 보여준 아프리칸 얌의 경우보다 상관계수가 높게 나타났다. 향후 PLS 모델링의 정확도 향상을 위한 시료의 분석조건 표준화, 모델링에 사용되는 분석시료의 개체 수 증대, 기능성 성분의 양적 변화가 큰 시료가 모델링에 활용되는 등의 보완이 이루어진다면 보다 정확한 성분 예측 모델링으로 활용이 가능할 것으로 기대된다. 아울러 얌의 경우 종간에 기능성 성분들의 양적, 질적 차이가 크게 이루어짐이 보고(Yang et al., 2009)된 바 있다. 또한 얌이 함유하고 있는 기능성 성분들에 대한 약리적 효과가 연구되고 있으며(Song et al., 2010; Yoon et al., 1989), 최근에는 기능성 성분들에 대한 연구가 매우 활발히 진행되고 있다(Kim et al., 2009; Kum et al., 2006; Kwon et al., 2010). 그러나, 기능성 성분을 정량 분석하기 위해서는 많은 시간이 필요하고, 대량의 시료를 분석하는데 어려움이 있다. 따라서 본 연구 결과를 토대로 기능성 성분 예측 모델링을 구축하고, 활용한다면 보다 쉽고, 빠르고 그리고 비교적 정확하게 기능성 성분을 예측할 수 있기 때문에 시간적, 비용적인 측면에서 보다 손쉽게 활용이 가능할 것으로 사료된다.
따라서 본 연구에서 확립된 대사체 수준에서 아프리칸 얌의 유용 기능성 성분 함량 예측 모델링은 아직 동정 및 표준화가 이루어지지 않은 다수의 아프리칸 얌 시료로부터 품질특성 평가 수단으로 활용이 가능하여 우수한 얌 품종이나 계통의 신속한 선발 수단으로서 활용이 가능할 것이다. 또한, 선발된 라인은 육종의 직접적인 소재로 활용이 가능하여 아프리칸 얌의 기능성 품종개발 가속화에 기여할 수 있을 것으로 예상된다.