서 언
배(Pyrus spp.)는 사과, 복숭아, 딸기 등과 함께 장미과에 속하는 온대 과수 작물의 하나이며, 유럽, 미국, 아프리카에서 재배 되는 서양배(P. communis L.)와 동양배로 크게 대별할 수 있다. 동양배는 우리나라, 중국 남부, 일본 등지에 재배되는 남방형 배(P. pyrifolia)와 중국과 일본의 북부지역 및 러시아 극동지역에서 재배되는 북방형 배(P. ussuriensis, P. bretschneideri)로 나누어 지며 P. communis와 P. pyrifolia가 가장 많이 재배되고 있다(Bell, 1990). 우리나라의 배 재배면적은 2014년 현재 13,127 ha로 매 년 감소 추세에 있으나 신품종 개발과 재배법 개선을 통해 생산량은 302,731톤으로 증가 추세에 있다(www.mafra.go.kr). 2016 년 7월 현재 품종생산 수입판매 신고된 548건과 품종보호 출원 및 등록된 48품종이 유통되고 있다(www.seed.go.kr).
배와 같은 목본류 작물의 신품종 심사는 나무와 가지, 잎, 꽃, 과실 등에서 발현되는 59개 형질을 조사하고 기존 품종과 상 호 비교하여 구별성을 판단하고 있다. 그러나 목본류의 경우 품종 특성 조사에 소요되는 기간이 장기간 소요되기 때문에 대 부분 육종가가 육성한 포장에서 직접 조사하는 현지심사 방식을 채택하고 있다. 따라서 형태적 특성조사에 의한 품종보호 출 원품종, 대조 및 표준 품종에 대한 정확한 평가가 어렵다. 이러한 문제점을 보완할 수 있는 방법이 분자표지 인자를 활용하여 품종별 데이터 베이스를 구축하고 기 알려진 품종에 대한 유전적 유연관계를 설정하는 것이다. 국제 식물 신품종 보호 동맹 (UPOV: International Union for the Protection of New Varieties of Plants)에서도 분자표지에 의한 품종별 데이터베이스 구축에 대한 가이드라인을 제시하고 있으며, 반복 재현성 및 품종별 다형성 정도가 높은 microsatellite나 single nucleotide polymorphism(SNP) 마커의 활용을 권장하고 있다(UPOV, 2010). 그러나 SNP 마커를 배의 품종별 데이터베이스 구축에 활용한 경우는 품종 식별 에 적합한 SNP 정보가 부족하기 때문에 국내외 연구자에 의해 거의 보고되지 않고 있다. 그러나 microsatellite 마커의 경우 배 품종 식별 및 유전자원의 다양성 평가의 경우 일본에서 Kimura et al.(2002)이 보고한 이래, 배의 과일 통조림, 주스, 건조된 과 일과 같은 품종보호품종의 가공품의 분석에까지 연구 범위를 확대하고 있다(Yamamoto et al., 2006). 이러한 분석에 주로 활용 된 마커는 2000년대 초반에 개발된 microsatellite 마커를 활용하였다는 점이며 몇몇 마커의 경우 대립유전자의 밴드 양상이 복 잡하고 다형성 정도가 낮아 유전적 거리가 좁은 최근 품종의 식별이 어렵다는 문제점이 제기되었다. 그러나 UPOV에서 제안 한 유전자 분석 지침서에서는 품종별 DNA 데이터베이스를 작성하기 위해서는 염기서열 정보가 논문 등을 통해 알려져 있고 여러 가지 분석기기, 실험실 및 실험자에 따라 동일한 결과를 나타내는 마커의 활용을 제안하고 있다(UPOV, 2010). 따라서 기 존에 개발되었던 배 품종 식별용 마커보다 다형성 정도가 높으면서 대립유전자의 패턴이 우수하고 반복 재현성이 높은 마커 의 개발이 필요한 것으로 판단되었다. 이들 마커를 대상으로 우리나라에서 육성된 배 품종보호출원 및 등록품종과 일본 등 해 외에서 육성된 품종 및 유전자원을 대상으로 정밀도 높은 데이터베이스 구축을 통한 유전적 거리의 추정은 향후 배 신품종 개발의 기초 자료로 활용될 수 있을 뿐만 아니라 품종보호권 강화 등에 크게 기여할 수 있으리라 판단된다.
따라서 본 연구에서는 국내외에서 재배되고 있는 배 품종 및 유전자원에 유전적 근연도를 조사하기 위하여, 380개 이상의 microsatellite 마커를 활용하여 대립유전자의 다형성 및 마커 별로 증폭되는 대립유전자의 패턴 등이 우수한 마커를 선정하고, 이를 국내외에서 재배되고 있는 배의 품종 및 유전자원에 대한 DNA 프로파일데이터 베이스 구축에 대한 일련의 연구를 수 행하여 얻어진 결과를 보고하는 바이다.
재료 및 방법
Microsatellite 분석
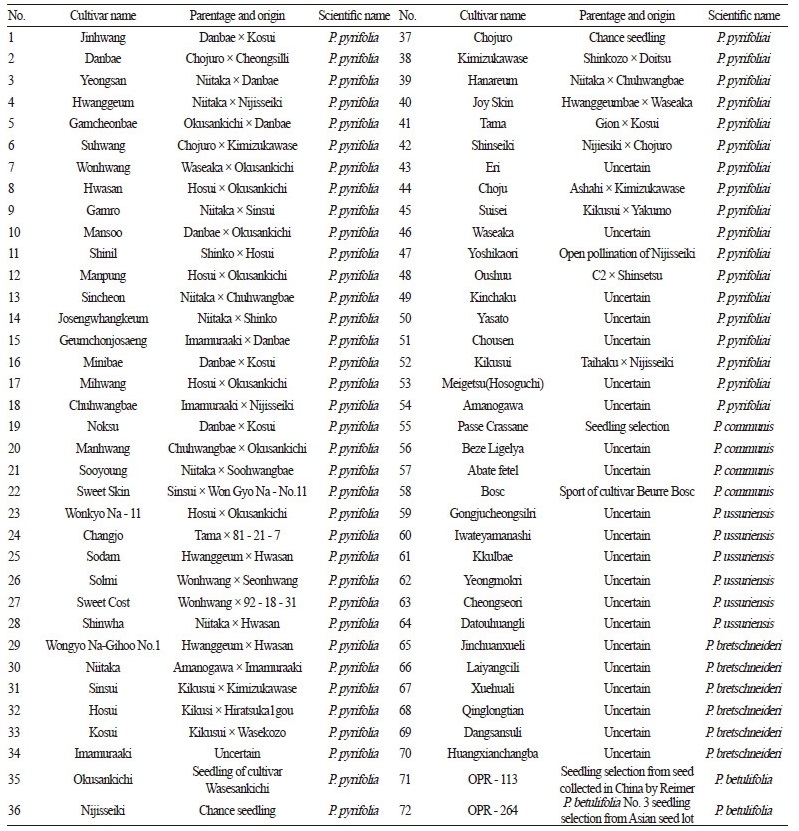
본 연구에서는 농촌진흥청 국립원예특작과학원에서 수집 보존하고 있는 배 유전자원 및 품종 72개(P. pyrifolia 54 개, P.communis 4개, P. ussuriensis 6개, P. bretschneideri 6개, P. betulifolia 2개)를 공시하여 microsatellite 마커의 분석 재료로 활 용하였다(Table 1). 공시 종의 어린 잎을 액체질소를 이용하여 마쇄한 다음 NucleoSpin®PlantⅡ(Cat. 740 770.250, Macherey- Nagel GmbH & Co., KG, Deutsch) 키트를 이용하여 genomic DNA를 분리 하였다. 추출된 DNA는 1.5% 아가로스젤에서 전기 영동하여 DNA 농도를 확인한 후 μL당 20ng의 농도로 희석하여 PCR 분석에 이용하였다.
Table 1. List of pear cultivars and germplasm samples genetically characterized using microsatellite markers.
 |
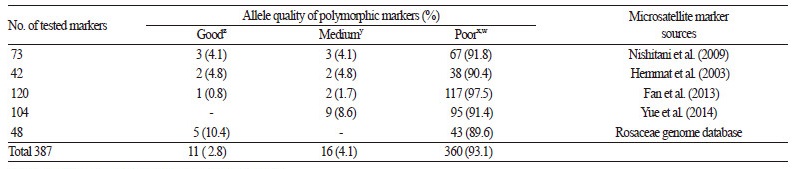
배 품종식별에 적합한 microsatellite 마커를 선발하기 위하여, 동양배로 분류되는 ‘Kinchaku’, ‘Gongjucheongsilri’, ‘Yasato’, 서양배인 ‘Passa Crassane’, ‘Beze Ligelya’, ‘Bosc’, ‘Abate fetel’, 미국 도입종인 ‘OPR - 264’와 387개의 microsatellite 프라이머를 이용하여 PCR하고 DNA증폭 산물을 QIAxcel Advanced System(Cat. 9001941, QIAGEN, Deutsch) 을 이용하여 전기 영 동한 다음 컴퓨터 프로그램(QIAxcel ScreenGel)에 의해 프라이머별 다형성 정도 및 대립유전자의 질적 특성을 Table 2의 조 사 기준에 의하여 분류하였다. Microsatellite의 대립유전자 특성이 단일밴드이거나 강한 주 밴드를 나타내는 분자표지를 선정 하여 프라이머의 정방향에 FAM, VIC, NED, PET의 화학 물질 중 한가지로 형광표지 하였다. 배 72품종 및 유전자원에 대한 DNA 프로파일 데이터베이스를 구축하기 위한 PCR 조성액은 게놈 DNA 20ng, 0.1μM의 형광 표지된 microsatellite primer, 2.0μL dNTP mixture(2.5mM), Taq polymerase 1.0U, 2.5μL의 10 × PCR buffer(50mM KCl, 20mM Tris - HCl, pH 8.0, 2.0mM MgCl2)에 초순수를 첨가하여 전체 부피를 30μL로 조절하였다. PCR(C1000, BioRad, USA) 조건은 94°C에서 30초간 denature 한 후, 55°C에서 30초간 annealing, 72°C에서 45초간 extension을 40cycle 수행하였다. Microsatellite 마커에 따른 배 품종별 대립 유전자의 크기를 추정하기 위하여, PCR 증폭산물1.0μL와 탈이온된 포름아마이드(deionized formamide) 10μL, size marker(LIZ500 size standard) 0.25μL를 혼합하고 94°C에서 2분간 변성시킨 후 자동염기서열분석기(Genetic Analyzer 3130XL, Applied Biosystems, Foster, USA)를 활용하여 전기 영동한 다음 GeneMapper(version 3.7) 프로그램(Applied Biosystems, Foster, USA)을 이용하여 각 마커 별로 대립유전자의 수와 대립유전자의 크기를 결정하였다 .
유전적 다양성 분석
Microsatellite 마커의 다양성을 조사하기 위하여 아래의 공식을 이용하여 Polymorphism information content(PIC) 값을 산 출하였다. 식에서 Pij는 마커 i의밴드들 중에서 j번째 공통 밴드 패턴의 빈도수이다(Anderson et al., 1993).
그리고 NTSYSpc(version 2.10b)(Rohlf 2000) 컴퓨터 프로그램을 이용하여 Jaccard 방법에 준하여 유전적 유사도 값을 계 산한 다음 unweighted pair-group method with arithmetical average(UPGMA)(Sneath and Sokal 1973) 방법으로 집괴 분석 하고 계통도를 작성한 다음 배 품종 및 수집종별 유전적 다양성 및 유연 관계를 비교 분석하였 다.
결과 및 고찰
Microsatellite 분석
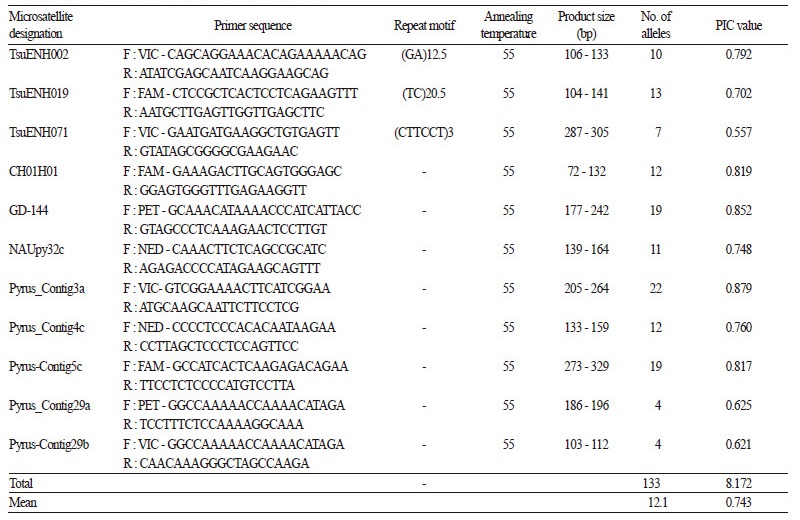
배 품종 식별 및 유전적 다양성 분석에 적합한 microsatellite 마커를 선정하기 위하여 일본(Nishitani et al., 2009), 중국(Fan et al., 2013; Yue et al., 2014), 미국(Hemmat et al., 2003), 및 국제 장미과 작물 게놈 데이터베이스(www.rosaceae.org)에서 보 고된 387개의 microsatellite 프라이머와 식물학적 특성이 다른 8개의 배 유전자원 및 품종(‘Kinchaku’, ‘Gongjucheongsilri’, ‘Yasato’, ‘Passa Crassane’, ‘Beze Ligelya’, ‘Bosc’, ‘Abate fetel’, ‘OPR - 264’)에 대한 프라이머별 다형성 정도 및 대립유전자의 질적 특성을 조사하였다(Fig. 1 and Table 2). 총 387개의 microsatellite 마커 중에서 360개는 증폭되는 대립유전자의 밴드 양 상이 복잡하거나 증폭반응이 미약하였고 일부 프라이머는 PCR 반응이 일어나지 않은 양상을 나타내었다. 그러나 나머지 27 개의 프라이머 중에서 11개는 품종 별로 하나의 명확한 주된 밴드를 나타내었고, 16개는 부가적인 밴드를 나타내면서 강한 주 된 피크를 보이는 것으로 나타났다. 따라서 11개의 프라이머를 대상으로 정방향의 5’ - 말단에 형광물질인 FAM, VIC, NED, PET를 각각 표지하여 배 72개의 품종 및 유전자원의 genomic DNA와 PCR하고 자동염기서열분석기를 이용하여 전기 영동 한 다음 다형성 정도를 조사한 바 (Table 3), microsatellite 프라이머에 따라 검출된 대립유전자의 수는 4 - 22개로 다양하게 나 타났으며 총 133개의 대립유전자가 검출되었고, 마커당 평균 대립유전자의 수는 12.1개로 분석되었다. 각 마커 별 공시 품종의 유전적 다형성 정도를 나타내는 PIC 값은 0.557 - 0.879까지 다양한 범위에서 분포하였으며, 평균값도 0.743으로 아주 높은 경향을 나타내었다. 특히, 10개 이상의 대립유전자를 가지면서 PIC 값이 0.70 이상인 TsuENH002, TsuENH019, CH01H01, GD - 144, NAUpy32c, Pyrus_Contig3a, Pyrus_Contig4c, Pyrus_Contig5c 마커는 배 유전자원 특성 평가 및 배 가공품의 품종 진위성 확인 및 농산물의 도난 사건 등에 효과적으로 활용될 수 있을 것으로 나타났다 .
Fig. 1.
Polymorphism of six microsatellite markers, CH01H01 (A), Pyrus - Contig3a (B), Pyrus - Contig4c (C), NAUpy32C (D), Pyrus - Contig5c (E), and Pyrus - Contig29a (F). PCR products were analyzed using a QIAxcel Advanced System (QIAGEN, Deutsch). M; QX DNA size marker (50 – 800bp); Lane 1, ‘Kinchaku’; 2, ‘Passa Crassene’; 3, ‘Beze Ligelya’; 4, ‘Gongjucheongsilri’; 5, ‘Yasato’; 6, ‘Abate fetal’; 7, ‘Bosc’; 8, ‘OPR-264’.
Table 3. Repeat motif, number of alleles, and polymorphism information content (PIC) of microsatellite markers selected for genetic
characterization of pear cultivars and germplasm samples.
 |
Microsatellite 마커를 이용한 유전적 다양성 분석에 대한 연구는, 일본의 Kimura et al.(2002)이 서양배와 동양배 등 여러 가 지 유형의 품종을 대상으로 9개의 microsatellite 마커(KA16, KU10, BGA35, BGT23b, NH004a, NH011b, NH013a, NH014a, NH015a)로 분석하였을 때 평균 대립유전자의 수는 14.8개임을 보고한 이래, 중국의 Bao et al.(2007)은 6개의 SSR 마커 (BGA35, KU10, BGT23b, NH004a, NH011b, NH015a)로 중국, 일본, 한국 등에서 수집한 98개의 배 유전자원 및 품종을 검 정한 결과 평균 28개의 대립 유전자가 검출됨을 제시하였다. 이들 연구자의 공통점은 분석에 활용된 유전자원의 종류만 다르지 9개의 마커 중 6개가 일치한다는 점이다. 그러나 최근에 여러 연구자에 의해 배와 사과 등에서 유래된 다수의 microsatellite 마커가 개발되면서 이들을 대상으로 다형성 정도가 높고 대립유전자의 패턴이 우수하면서 반복 재현성이 높은 마커의 선정은 배 품종의 동일성 여부 및 유전자원 특성 평가에 안정적으로 활용될 수 있다는 장점이 있다. 따라서 본 연구에서는 이러한 기준 에 적합한 11개의 마커를 선정할 수 있었다. 이 마커들은 일본에서 Nishitani et al.(2009)이 개발한 3개, Hemat et al.(2003)이 개 발한 2개, Fan et al.(2013)이 개발한 1개, 장미과 작물 게놈데이터베이스에서 선발한 5개로 구성되어 있다. Nishitani et al.(2009) 은 TsuENH002, 019, 071 마커를 동양배 11품종과 서양배 11품종에 대하여 분석하였을 때 대립유전자의 수는 1-4개의 범위 에 분포함을 보고하였고, Fan et al.(2013)은 배 whole genomic sequence를 통해 개발한 마커 NAUpy32c를 서양배 1품종과 일본 및 중국에서 유래된 동양배 2품종 및 Pyrus 속 유전자원 4점에 대하여 분석하였을 때 4개의 대립유전자가 나타남을 보고 한 바 있다. 그러나 본 연구에서 이 마커를 대상으로 배 품종 및 유전자원 72개에 대하여 분석하였을 때 대립유전자의 수가 4-13 개가 분포하는 양상을 나타내어 이들 연구자보다 대립유전자의 수가 많이 검출되었는데 이는 분석에 활용된 배 품종 및 유전 자원의 유전적 조성과 대립유전자의 검출에 활용된 분석기기가 다른 데서 비롯된 결과라고 추정된다. 한편, Hemmat et al. (2003)이 사과의 유전자 지도 작성에 활용했던 사과 유래의 microsatellite 마커인 CH01H01과 GD-144 및 장미과 식물 게놈 데이터베이스에서 선발한 Pyrus_contig3a, Pyrus_contig4c, Pyrus_contig5c, Pyrus_contig29a, Pyruscontig29b의 경우 지금까 지 유전자원의 특성 평가나 품종식별에 활용되지 않았던 새로운 마커로서 이를 본 연구에 공시된 재료에 대해 분석하였을 때 대립유전자의 수가 4-22개로 많고, PIC 값도 0.621-0.878까지 높게 나타났다. 따라서 본 연구에서 최종 선정된 배 품종식별용11개의 microsatellite 마커는 배 뿐만 아니라 다양한 장미과 작물의 유전적 유연관계 설정 및 품종별 데이터베이스 작성에 효 과적으로 사용될 수 있을 것으로 추정된다 .
품종식별력 검정 및 유전적 유사도 분석
배 및 사과에서 유래된 microsatellite 마커 중에서 다형성 정도가 높으면서 대립유전자의 밴드 패턴이 우수한 11개를 이용하 여 배 72품종 및 유전자원에 대한 유전적 유사도 정도를 분석한 바(Fig. 2), 공시품종 및 유전자원에 대한 전체 유사도 지수는 0.07-1.00으로 나타났다. 유전적 유사도 지수 0.21에서 4개의 대그룹으로 분류할 수 있었다.
Fig. 2.
Dendrogram depicting the classifications of 72 pear cultivars and germplasm samples constructed using the unweighted pair-group method with arithmetical average (UPGMA) and based on microsatellite markers. Numbers (1 – 72) on the right - hand side refer to the list of cultivars in Table 1. Scale at the bottom is Jaccard’s coefficient of similarity. Roman numerals indicate 4 major geographic groups in 72 pear cultivars and germplasm samples, and large ‘1’ and ‘2’ on the left represent two subgroups in 55 Asian pears cultivars
Ⅰ그룹에는 ‘Jinhwang’ 등 55품종이 포함되었으며, 유사도 지수 0.32에서 2개의 소그룹으로 구분할 수 있었다. Ⅰ- 1 그룹은 우리나라에서 육성되어 품종보호 등록된 21품종(‘Jinhwang’, ‘Manpung’, ‘Noksu’, ‘Sodam’, ‘Hwasan’, ‘Sweet Skin’, ‘Gamro’,‘Minibae’, ‘Wongyo Na-Gihoo No.1’, ‘Shinwha’, ‘Hwanggeum’, ‘Josaenghwanggeum’, Sooyoung’, ‘Joy Skin’, ‘Changjo’, ‘Hanareum’, ‘Sinil’, ‘Solmi’, ‘Suhwang’, Sincheon’, ‘Geumchonjosaeng’)과 중간모본인 ‘Wongyo Na - 11’과 일본품종인 ‘Niitaka’ 등 20품종이 포함되었다. 품종 육성 계보를 볼 때 일본에서 육성된 ‘Kosui’, ‘Hosui’, ‘Okusankichi’, ‘Sinsui’, ‘Niitaka’, ‘Nijisseiki’와 우리나라에서 육성된 ‘Hwasan’과 ‘Danbae’ 품종이 교배모본으로 활용된 품종이 속하였다. Ⅰ- 2 그룹은 우리나 라에서 육성되어 품종보호 등록된 ‘Yeongsan’, ‘Wonhwang’, ‘Mihwang’, ‘Mansoo’, ‘Manhwang’, ‘Sweet Cost’, ‘Gamcheon’ 등 7품종과 일본에서 육성된 ‘Okusankichi’ 등 5품종이 속하였으며, 특이하게 동양계 배중에서 P. bretschneideri에 속하는 ‘Laiyangcili’가 포함되었다. Ⅰ- 2 그룹에 속하는 품종들의 육성 계보를 볼 때 ‘Danbae’와 ‘Okusankichi’가 주로 교배모본으로 활용된 품종이 분포되었다. 특히, ‘Gamcheon’과 ‘Mihwang’의 경우 본 연구에서 선발된 분자표지에 의해서 구분이 되지 않았 는데, 두 품종의 육성 계보를 볼 때 양친 중에 ‘Okusankichi’가 부본 또는 모본으로 활용되었기 때문에 나타난 결과라고 추정되 며, 향후 두 품종의 형태적 특성이나 분자 마커의 수를 확대 분석하여 품종의 동일성 여부를 판단해야 될 것으로료 사된다.
Ⅱ 그룹은 우리나라, 중국, 일본에서 수집한 P. ussuriensis 6점과 중국에서 수집한 배 유전자원 P. bretschneideri 5점이 동일 한 그룹에 분포하였다. 분자 마커를 활용하여 배 유전자원을 대상으로 군집분석 하였을 때 종에 따라 뚜렷하게 구분되지 않다 는 것이 여러 연구자에 의해 지적되고 있다. Kimura et al.(2002)은 종이 다른 동양배와 서양배 60품종을 9개의 microsatellite 마커로 분석하였을 때 종에 따라 명확히 그룹화 되지 않는다고 하였다. Cho et et al.(2009)도 amplified fragment length polymorphism(AFLP) 마커를 활용한 배 유전자원의 유연관계 분석에서도 이와 유사한 연구결과를 발표한 바 있는데, 본 연구 에서도 Ⅰ그룹의 P. pyrifoliai내에 P. bretschneideri에 속하는 ‘Laiyangcili’ 분포하거나, Ⅱ 그룹내에 P. ussuriensis 6점과 P. bretschneideri 5점이 혼재하여 그룹화되는 양상을 나타내어 이들 연구자의 연구결과를 확인할 수 있었다 .
Ⅲ 그룹은 P. betulaefolia에 속하는 ‘OPR - 113’과 ‘OPR - 165’가 포함되었으며, Ⅳ 그룹은 P. communis에 속하는 ‘Passe Crassane’, ‘Beze Ligelya’, ‘Bosc’, ‘Abate fetel’ 등 4품종이 분포하였다. Ⅲ 그룹의 P. betulaefolia는 P. bretschneideri의 기원인 것으로 Challice and Westwood(1973)에 알려져 있으나, 본 연구에서 활용된 microsatellite 마커에 의해 독립적인 하나의 군으 로 그룹화되는 것으로 보아 이 두 종간에는 유전적으로 거리가 먼 것으로 확인하였는데, Bao et al.(2007)도 중국배 유전자원을 microsatellite 마커 6개로 분석하였을 때 P. betulaefolia와 P. bretschneideri는 종간에 유전적으로 거리가 먼 독립적인 군으로 분포함을 보고한 바 있다. 본 연구에서도 이들 연구자와 전혀 다른 microsatellite 마커로 분석하였을 때 P. betulaefolia에 속하 는 2개의 유전자원 ‘OPR - 113’과 ‘OPR265’는 P. bretschneideri에 속하는 ‘Laiyangcili’, ‘Dansansuli’, ‘Xuehuali’, ‘Huangxianchangba’, ‘Qinglongtian’은 서로 다른 독립적인 그룹에 분포하여 Bao et al.(2007)의 연구결과를 확인할 수 있었다. Ⅳ 그룹에 속하는 P. communis의 경우 microsatellite 마커에 의해 동양배와 서양배를 대상으로 유전적 다양성 분석시 종에 따라 뚜렷하게 구분되 지 않음을 보고하였으나(Kimura et al. 2002), Basil and Postman(2010)은 expressed sequence tags(EST)에서 유래된 13개의 microosatellite 마커를 활용하여 81개의 P. communis, 13개 P. pyrifolia와 20개의 P. ussuriensis 또는 P. bretschneideri 에 대 한 유전적 근연 관계를 분석하였을 때 P. communis는 하나의 독립적인 품종군으로 그룹화되나 P. pyrifolia, P. ussuriensis, P. bretschneideri 동일 그룹내에서 혼재함을 보고하였다. 본 연구에서도 Basil and Postman(2010)이 활용한 마커와 다른 11개의 microsatellite 마커를 72품종 및 유전자원 분석에 활용하였을 때 P. communis에 속하는 ‘Bosc’ 외 3품종이 P. pyrifolia, P. ussuriensis, P. bretschneideri, P. betulifolia 속하는 품종과 뚜렷이 구분되어 Basil and Postman(2010)의 연구결과와 유사한 경향을 나타내었다.
본 연구에서는 최근에 보고된 배 및 사과에서 유래된 387개의 microsatellite 마커 중에서 다형성이 양호할 뿐만 아니라 반복 재현성이 우수하면서 대립유전자의 패턴이 단순한 11개를 새롭게 선발하였다. 이들 마커를 활용하여 72개 배 품종 및 유전자 원에 대하여 분석한 결과 배의 식물 분류학적 특성 및 품종 육성 계보에 따라 뚜렷하게 그룹화되는 경향을 보였다. 따라서 이 마 커를 통해 구축된 DNA 프로파일 데이터베이스는 품종간 유연관계 설정을 통한 배 유전자원 특성 평가뿐만 아니라 품종보호 품종의 대조품종 선정 등에 매우 유용하게 이용될 수 있을 것으로 판단된다. 실제로 국립종자원에서는 무(Bae et al., 2015), 호박(Sim et al., 2015) 등의 작물에서 microsatellite마커를 이용하여 작성된 품종별 데이터베이스를 활용하여 신품종 보호 제도 에 적극 활용하고 있다. 한편, 본 연구에서 새롭게 선정된 microsatellite 마커에 의해 ‘Gamcheon’과 ‘Mihwang’은 식별이 되지 않았는데, 최근 배의 경우도 SNP 마커에 대한 정보가 다수 보고되고 있는 바(Montanari et al., 2013), 이를 활용하여 정밀 분석 이 이루어져야 될 뿐만 아니라 형태적 특성을 비교 분석하여 품종 특이적인 새로운 마커 개발이 필요할 것으로 사료된다.