서 언
감귤은 전세계적으로 재배되고 있는 중요한 과일 중 하나에 속하며, 종자에서 출발하여 꽃 피고 열매 맺기 까지 약 5-10년이 소요되는 긴 유년성(long juvenility)과 수정 후 하나의 종자에 여러 개의 배를 갖는 다배성(polyembryony)의 특성을 갖고 있다(Gmiter et al., 2012). 이러한 특성은 대부분의 감귤에서 흔히 나타나는데 난세포의 수정에 의한 것이 아니라 배낭 주변의 체세포 조직에서 유래한 주심배를 형성(nucellular embryony)하는 특성들을 갖고 있다(Esen and Soost, 1977). 이러한 특성들은 교배육종을 통한 감귤 품종육성에 장해가 된다.
감귤 품종육성 방법으로 교배육종 방법이 주요 수단으로 활용되고 있는데, 교배 종자에서 획득한 주심배와 유성배의 실생묘는 초기 유묘(seedling) 단계에서 형태적으로 구별하기가 쉽지 않다. 또한 감귤은 긴 유년성을 갖고 있기 때문에 열매를 맺기 까지 오랜 기간 동안 유묘를 유지 보존해야 한다. 따라서, 유묘 단계에서 교배 양친이 수정된 실생묘를 조기에 동정할 수 있다면 시간 및 관리 비용을 절감하고 시험포장을 효율적으로 이용할 수 있다. 주심배 실생과 유성배 실생묘를 조기 동정하는 방법으로 대사물질의 변화를 이용한 비색 분석법(Furr and Reece, 1946), 적외선 분광법(Pieringer and Edwards, 1967), 박층크로마토그래피(Tatum et al., 1978), 크로마토그래피(Weinbaum et al., 1982), 그리고 동질효소 패턴분석법(Ashari et al., 1988; Moore and Castle, 1988; Moon et al., 1991; Tusa et al., 2002) 등이 사용되었으나 이들 방법은 식물체 상태, 환경적 조건에 따라서 영향을 받기 때문에 실험자에 따라 동일한 결과를 얻지 못하는 문제점이 있다. 따라서, 이 방법들은 감귤 교배육종에서 교잡종 실생묘를 선발하기 위한 일반적인 방법으로는 효과적이지 못하다(Ruiz et al., 2000; Tusa et al., 2002).
최근 품종간의 유연관계 및 교잡종 실생묘의 동정방법으로 PCR 방법을 이용한 random amplified polymorphic DNA(RAPD)(Mondal and Saha, 2014; Maria Andrade et al., 2004; Lima et al., 2000; Yoo et al., 2009; AL-Anbari et al., 2014), simple sequence repeat(SSR)(Ahmad et al., 2012; Oliveira et al., 2002), inter-simple sequence repeat(ISSR) (Golein et al. 2011) 그리고 sequence-related amplified poly-morphism(SRAP)(Yun et al., 2011) 등과 같은 분자생물학적 방법들이 품종간의 유연관계 및 교잡종 실생묘의 동정에 사용되고 있다. 그러나 현재까지 감귤에서 분자생물학적 마커를 통한 교잡종 실생묘의 선발방법은 단일품종의 화분친을 이용한 교배조합에서만 이용되었다(Yun et al., 2011). 따라서, 선발된 화분친 특이적 마커들은 교잡종 실생묘 선발에 이용할 때 그 화분친이 쓰여진 교배조합에 한정되는 한계가 있었고, 다른 감귤 품종과의 교배조합에서는 공통적으로 활용 되지 못하는 문제점이 있다. 또한, 온주밀감은 국내에서 경제적으로 재배되고 있는 품종 중 노지에서 재배할 수 있는 거의 유일한 품종이지만, 상대적 낮은 당도, 향기 등의 문제점을 가진다. 이를 개선하기 위해 유전적으로 가깝고 조기 성숙형이며 껍질 벗김, 당도, 향기가 좋은 만다린 품종과의 교배육종을 실시하고 있다. 그러나, 온주밀감은 대표적 다배성 품종이고 웅성 및 자성 불임이 강해 교배육종시 교잡종 실생묘 획득이 매우 어렵고, 상대적으로 주심배실생은 세력이 강해 획득된 전체 실생에서 주심배실생이 차지하는 비율이 80% 정도에 이르는 문제점이 있다(Yun et al., 2011).
따라서 본 연구에서는 종자친으로 사용된 온주밀감 품종에 비특이적이면서 화분친으로 사용된 7종의 만다린 감귤품종에 공통적으로 활용 가능한 분자마커를 선발하여 온주밀감과 만다린 교배조합으로부터 효율적인 교잡종 실생묘를 선발하기 위해 수행되었다.
재료 및 방법
식물재료 및 Genomic DNA 분리
화분특이적 마커 선발을 위해 국립원예특작과학원 감귤시험장 포장에서 종자친 3종의 온주밀감(‘성전온주’, ‘남감20호’ 그리고 ‘궁천조생’)과 화분친 7종의 만다린 감귤(‘병감’, ‘Lee’, ‘Sunburst’, ‘기주밀감’, ‘부지화’[Citrus reticulata cv. Shiranuhi(“Kiyomi × Ponkan”)], ‘탐나는봉’ [Shiranuhi Nucellar seedling], ‘신예감’ [“Kiyomi × (Citrus reticulata)”] 품종에서 감귤 잎 시료를 채취하여 사용하였다. 채취한 시료는 -80°C 초저온 냉동고에 사용할 때까지 보관하였다. 전체 genomic DNA는 자동 핵산 추출 장치(Promega, Madison, WI)를 이용하여 분리하였고 사용할 때까지 -20°C에 보관하였다.
RAPD 분석
감귤 화분특이적 RAPD 분석에 적합한 프라이머를 선발하기 위하여 10개의 염기로 구성된 700종의 University of British Columbia(UBC, BC, Canada)프라이머는 바이오니아사(Bioneer, Corp., Daejeon, Korea)에서 구입하여 이용하였다. 교배조합에서 획득한 실생묘로부터 교잡종을 선발하기 위하여 프라이머 700개 중 1차 검정에서 37개의 프라이머를 선발 한 후 화분친을 공통적으로 선발할 수 있는 2개의 프라이머 중 UBC 27 프라이머만을 사용하였다(Table 1). PCR 반응액은 AccuPower PCR Premix(Bioneer, Corp., Daejeon, Korea) [250μM dNTP, 1.5 mM MgCl2, 1.0 unit TaqDNA polymerase, 10mM Tris-HCl(pH 9.0), 40mM KCl]에 genomic DNA 25ng 그리고 5 pmol의 프라이머를 첨가하여 20uL로 조정하였다. PCR 반응은 Takara PCR Thermal cycle(Takara, Japan)에서 45 cycle을 실시하였으며, denaturation은 94°C에서 1분, annealing은 38°C에서 1분, 그리고 extension을 72°C에서 2분간 수행하였다. 화분특이적 프라이머 선발에는 화분친과 종자친과의 밴드 양상만을 확인하기 위하여 증폭된 PCR 생성물은 1.2% agarose gel에서 100V로 25분 동안 전기영동하여 나타나는 밴드로 확인하였다. 또한, 교잡종 실생묘의 동정에는 교잡종 실생묘와 주심배의 밴드 양상을 정확하게 판독하기 위하여 증폭된 PCR 산물은 1.2% agarose gel에서 80V로 4시간 동안 전기영동 한 후 확인하였다.
Table 1. Pollen-specific RAPD primers. |
Primer | Sequence (5’- 3’) | Primer | Sequence (5’- 3’) |
UBC9 | CCTGCGCTTA | UBC539 | CTTACGTCAC |
UBC27 | TTTGGGGGGA | UBC550 | GTCGCCTGAG |
UBC37 | CGGGGGTTTT | UBC564 | CGGCGTTACG |
UBC41 | TTAACCGGGG | UBC568 | ACCTGTTCTC |
UBC236 | ATCGTACGTG | UBC576 | CACCTAATGG |
UBC254 | CGCCCCCATT | UBC596 | CCCCTCGAAT |
UBC262 | CGCCCCCAGT | UBC605 | CCGATCATTC |
UBC386 | TGTAAGCTCG | UBC617 | CGGACTATGT |
UBC405 | CTCTCGTGCG | UBC621 | GTCTGCGCTA |
UBC425 | CGTCGGGCCT | UBC625 | CCGCTGGAGC |
UBC451 | CTAATCTCGC | UBC645 | TACAGCGTTG |
UBC473 | ATCCCCAAGA | UBC659 | CGGTTTCGTA |
UBC478 | CGAGCTGGTC | UBC661 | CCTGCTTACG |
UBC485 | AGAATAGGGC | UBC676 | GCTAACGTCC |
UBC511 | GAATGGTGAG | UBC677 | TCTCAGGACA |
UBC513 | TATAVGACCC | UBC684 | CCACACGTAG |
UBC523 | ACAGGCAGAC | UBC688 | GCAGGAGCGT |
UBC528 | GGATCTATGC | UBC695 | GCTAATCAGC |
UBC530 | AATAACCGCC | | |
결과 및 고찰
RAPD를 이용한 화분특이적 마커 선발
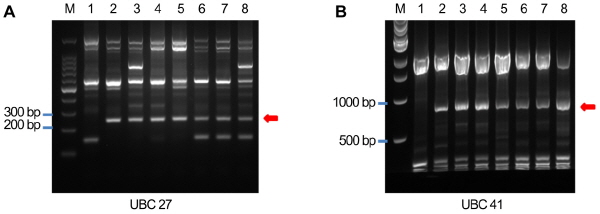
본 연구는 서로 다른 감귤 품종 간의 교배에서 교잡종 실생묘만을 조기에 동정할 수 있는 분자마커를 선발하기 위하여, UBC 프라이머 700개를 RAPD 방법을 사용하여 종자친인 온주밀감에는 없으면서 화분친으로 사용된 7종의 만다린 감귤에서 전체 혹은 일부 품종에만 공통적으로 PCR 증폭산물이 나타나는 UBC 프라이머 37개를 선발하였다(Table 1). 선발된 37종의 프라이머를 7개의 교배조합에 적용하였을 때 화분친의 특이적인 증폭산물이 관찰되는 프라이머를 최고 27종, 최저 13종을 선발하였다(Table 2). 즉, 종자친인 온주밀감에 화분친의 병감을 교배 하였을때 병감의 특정부위에만 공통적으로 증폭산물이 관찰되는 프라이머는 27개, ‘Lee’ 품종인 경우는 26개, ‘Sunburst’인 경우는 27개, ‘기주밀감’인 경우는 13, ‘부지화’는 20, ‘탐나는봉’은 21, 그리고 ‘신예감’은 18개에 이른다. 또한 선발된 37종의 UBC 프라이머들 중 일부는 화분친으로 사용된 감귤 품종들에 공통적으로 증폭산물이 관찰되는 것을 볼 수 있었다(Table 2, Fig. 1). 전체 7종의 만다린 감귤 품종의 화분친에 공통적으로 사용할 수 없지만 일부 한 품종을 제외한 나머지 6품종에 대하여 공통적으로 활용할 수 있는 UBC 528, 568, 677, 695 프라이머 4개를 선발하였다(Table 2). 이 중 UBC 568 프라이머는 화분친으로 사용한 7종의 만다린 감귤품종 중 ‘Lee’를 제외한 나머지 6종의 품종들의 동일한 위치에 증폭된 DNA 밴드 결과를 얻었다. 또한, UBC 528, UBC 677 그리고 UBC 695는 ‘기주밀감’ 품종에서 증폭 산물을 관찰할 수 없었다. 한편 UBC 27과 41 프라이머는 종자친에는 증폭산물이 없으면서 화분친으로 사용된 7종의 감귤 품종 모두에 동일한 크기의 DNA 밴드를 보였다(Fig. 1). 즉 UBC 27 프라이머를 이용하였을 때 종자친으로 사용된 온주밀감 품종은 200-300bp 사이에 PCR 증폭산물이 보이지 않으나 화분친으로 사용된 7종의 만다린 감귤 품종들은 전부 같은 위치에서 증폭산물을 확인할 수 있었다(Fig. 1A). 또한 UBC 41 프라이머는 500-1000bp 사이 같은 위치의 PCR 증폭산물을 확인 할 수 있었다(Fig. 1B). 이 결과는 종자친으로 3종의 온주밀감[(‘Morita unshiu’(‘성전온주’), ‘Nangan 20’(‘남감 20호’), ‘Miyagawawase’ (‘궁천조생’)과 화분친으로 7종의 만다린 감귤(‘Ponkan’(‘병감’), ‘Lee’, ‘Sunburst’, ‘Kinokuni’(‘기주밀감’), ‘Shinyegam’ (‘신예감’), ‘Tamnaneunbong’(‘탐나는봉’), ‘Shiranuhi’(‘부지화’)]을 이용한 교배조합으로부터의 교잡종 실생묘 선발에 있어 화분특이적 마커로 공통적으로 활용할 수 있을 것으로 생각된다. Yun et al.(2011)도 역시 RAPD와 SRAP 방법을 이용하여 ‘성전온주’와 ‘병감’의 교배조합에서 화분에 특이적으로 증폭되는 DNA산물을 마커로 활용하여 교잡종 실생묘를 판별하였다. 이러한 결과는 교배품종에 따라 종자친에서는 DNA 증폭 산물을 만들지 않고 화분친에만 특이적으로 DNA 증폭 산물을 만드는 프라이머를 사용함으로써 교잡종 실생묘들을 높은 확률로 선발 할 수 있을 것으로 생각된다.
|
Fig. 1. Pollen-specific amplification obtained from UBC primers. (A) UBC-27 primer, M : molecular weight markers (100 bp DNA Ladder); lane 1: mother plant (‘Miyagawa wase’); lane 2-8: pollen parents ‘Ponkan’, ‘Lee’, ‘Sunburst’, ‘Kinokuni’, ‘Shiranuhi’, ‘Tamnaneunbong’, and ‘Shinyegam’ mandarin. (B) UBC-41 primer, M : molecular weight markers (1.0 kb DNA Ladder); lane 1: mother plant (‘Miyagawa wase’); lane 2-8: pollen parents ‘Ponkan’, ‘Lee’, ‘Sunburst’, ‘Kinokuni’, ‘Shiranuhi’, ‘Tamnaneunbong’, and ‘Shinyegam’ mandarin. Arrows: pollen specific amplification. |
Table 2. Pollen-specific UBC primers used for selecting Citrus hybrids. |
Cultivars used as pollen parent | UBC primers able to distinguish maternal parent | No. of markers to select zygotic seedlings |
‘Ponkan’ | UBC27, UBC9, UBC37, UBC41, UBC254, UBC262, UBC386, UBC405, UBC425, UBC451, UBC473, UBC485, UBC511, UBC523, UBC528, UBC530, UBC568, UBC576, UBC596, UBC605, UBC617, UBC625, UBC676, UBC677, UBC684, UBC688, UBC695 | 27 |
‘Lee’ | UBC27, UBC9, UBC41, UBC254, UBC262, UBC386, UBC405, UBC425, UBC451, UBC473, UBC458, UBC511, UBC523, UBC528, UBC539, UBC550, UBC564, UBC596, UBC605, UBC617, UBC625, UBC659, UBC676, UBC677, UBC688, UBC695 | 26 |
‘Sunburst’ | UBC27, UBC9, UBC37, UBC41, UBC262, UBC386, UBC405, UBC451, UBC485, UBC511, UBC513, UBC523, UBC528, UBC530, UBC564, UBC568, UBC596, UBC605, UBC617, UBC621, UBC625, UBC645, UBC659, UBC676, UBC677, UBC684, UBC695 | 27 |
‘Kinokuni’ | UBC27, UBC41, UBC262, UBC386, UBC485, UBC530, UBC550, UBC568, UBC576, UBC605, UBC645, UBC659, UBC688 | 13 |
‘Shiranuhi’ | UBC27, UBC37, UBC41, UBC254, UBC262, UBC425, UBC473, UBC478, UBC523, UBC528, UBC530, UBC539, UBC568, UBC576, UBC596, UBC645, UBC676, UBC677, UBC688, UBC695 | 20 |
‘Tamnaneunbong’ | UBC27, UBC37, UBC41, UBC254, UBC262, UBC425, UBC473, UBC478, UBC523, UBC528, UBC530, UBC539, UBC568, UBC576, UBC596, UBC621, UBC645, UBC676, UBC677, UBC688, UBC695 | 21 |
‘Shinyegam’ | UBC27, UBC9, UBC37, UBC41, UBC236, UBC405, UBC425, UBC511, UBC528, UBC539, UBC568, UBC576, UBC596, UBC605, UBC625, UBC661, UBC677, UBC695 | 18 |
*Matenal parent is Citrus unshiu mandarin. Primers amplifying successfully in all 7 pollen parents are underlined and those in 6 pollen parents in bold. |
화분친 특이적인 마커를 이용한 교잡종 실생묘 선발
최근 주심배와 유성배 유래 실생묘의 동정에 있어 RAPD, SSR, SRAP등의 분자생물학적 동정 방법이 이용되고 있다(Ruiz et al., 2000; Oliveira et al., 2002, 2003; Scarano et al., 2003; Rao et al., 2008). Oliveira et al.(2003)은 “Cravo × Pêra”로부터 실생묘 선발에 있어 RAPD를 이용하였고 Oliveria et al.(2002)은 “Murcott × Pêra” 사이의 교배조합으로부터 실생묘 선발에 있어서 SSR 마커를 사용하였다. 또한 이전 연구에서와 같이 “성전온주 × 병감”인 경우는 RAPD 나 SRAP의 교차적인 방법을 사용하여 교잡종 실생묘를 효율적으로 선발 할 수 있었다(Yun et al., 2011). 그러나 이 모든 선행 연구는 교배조합을 통하여 얻어진 실생묘로부터 교잡종 실생묘 선발에 화분 특이적인 증폭산물을 가지고 선발하였으나 이는 하나의 교배조합에 따른 선발 마커로써 여러 교배조합에서 공통적으로 사용될 수 있는 마커는 아니다.
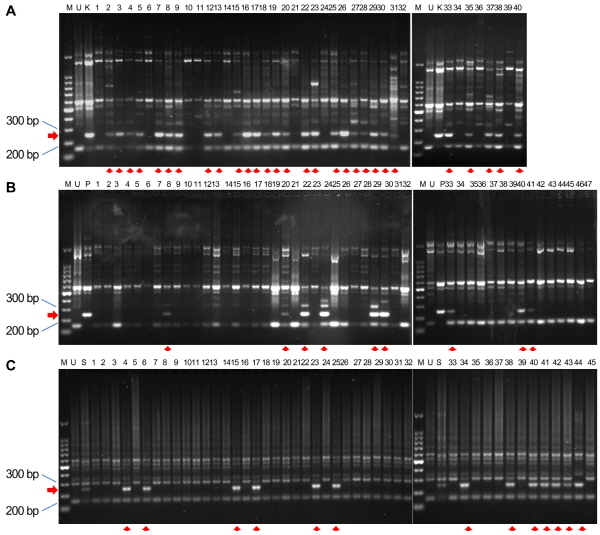
본 연구에서는 종자친인 3종의 온주밀감(‘성전온주’, ‘남감20호’, ‘궁천조생’)에는 증폭되지 않으면서 화분친인 7종의 만다린 감귤(‘병감’, ‘Lee’, ‘Sunburst’, ‘기주밀감’, ‘부지화’, ‘탐나는봉’, ‘신예감’)에만 공통적으로 증폭되어 나타나는 UBC 27과 UBC 41 프라이머를 선발 하였다. 교잡종 실생묘 선발에 이 두 프라이머를 교차적으로 사용한 결과 UBC 27 프라이머는 종자친으로 2종의 온주밀감(‘남감20호’, ‘궁천조생’)을 사용하고 화분친으로 3종의 만다린 감귤(‘기주밀감’, ‘병감’, ‘Sunburst’)을 사용하여 교배한 실생묘로부터 화분친에 공통적으로 증폭되는 밴드가 확인되어 교잡종 실생묘 선발에 사용이 가능하였다(Fig. 2). 반면, UBC 41은 종자친과 화분친 선발에는 공통적으로 구별되는 밴드가 증폭되어 나타나지만 교배한 실생묘로부터는 화분친에 공통적으로 증폭되어 나타나는 밴드가 확인되지 않아 본 연구의 교배조합에서 교잡종 실생묘 선발에는 적합하지 않다고 생각되었다(데이터 미제시). 따라서 종자친인 온주밀감에는 증폭되지 않으면서 화분친인 7종의 만다린 감귤에만 공통적으로 증폭되어 나타나는 프라이머 2개 중 UBC 27 프라이머만을 사용하여 “남감20호 × 기주밀감”, “남감20호 × 병감” 그리고 “궁천조생 × Sunburst”에 대한 교잡종 실생묘 여부를 조사하였다. “남감20호 × 기주밀감”인 경우는 실생묘 40개체 중 29개체(Fig. 2A), “남감20호 × 병감”인 경우는 47개체 중 9개체(Fig. 2B) 그리고 “궁천 × Sunburst”인 경우는 45개체 중 13개체(Fig. 2C)의 교잡 실생묘를 확인하였다. Fig. 2에서 보는 것처럼 교잡이 안된 실생묘들은 모두 종자친과 유전적으로 동일한 주심배이다. 그러나 “남감20호 × 기주밀감” 교배조합에서 1, 6, 10, 36 그리고 39 실생묘는 주심배이면서 종자친에 없는 밴드가 증폭된 점으로 보아 유전적으로 변이가 발생한 주심배실생 변이주라 여겨진다(Fig. 2A). 일반적으로 주심배는 종자친과 유전적적으로 동일하다(Kepiro and Roose, 2007). 그러나 감귤은 종종 주심배 실생변이가 발생하는데 예로 금전조생에 탱자화분을 교배하여 얻어진 금전조생의 주심배 실생묘인 히로시마 7호 등이 있다. Khan과 Roose(1988)는 감귤나무 한 그루의 위치에 따라서도 배의 유형과 수가 달리 생산되는데, 이는 최소 유전자들과, 화분종류 그리고 환경적 조건에 따라서 조절될 수 있다고 하였으나, 현재까지 주심배 실생변이가 발생하는 정확한 정보는 밝혀져 있지 않다. 따라서 위 주심배실생 변이주로 추정되는 개체들은 추후 열매가 결실된 후 과실 특이성 등 을 검증할 필요가 있다고 생각된다. 또한, UBC 27 프라이머를 사용하여 “남감20호 × 기주밀감”, “남감20호 × 병감” 그리고 “궁천조생 × Sunburst” 교잡종 실생묘들의 실생율은 각각 73, 19 그리고 29%로 “남감20호 × 기주밀감”의 교배조합에서 높은 확률의 교잡종 실생묘를 얻을 수 있었다(Table 3). 따라서 온주밀감의 품질을 개량하기 위하여 온주밀감과 같이 조숙성 이면서 상대적으로 높은 당도와 껍질을 벗기기 쉬운 특성을 가진 ‘기주밀감’을 화분친으로 사용하였을 때 이 프라이머를 사용하면 높은 확률의 교잡종 실생묘를 조기에 판단할 수 있어 향후 온주밀감 교배 육종에 활용할 수 있을 것으로 기대된다. 또한 본 연구에서처럼 여러 감귤 품종들의 화분친을 사용하여 공통적으로 선발할 수 있는 마커는 현재까지 감귤에서 알려진 보고가 없었으며 본 연구에서 선발한 이 프라이머의 증폭된 DNA 단편을 SCAR 마커로 개발 후 사용한다면, 온주밀감의 교잡종 실생묘 선발에 효율적으로 사용할 수 있을 것으로 기대된다.
|
Fig. 2. Identification of zygotic seedlings from citrus cultivars using the UBC-27 primer. (A) Hybrid populations of ‘Nangan 20’ unshiu mandarin and ‘Kinokuni’ mandarin screened for early identification of zygotic seedlings. M: molecular weight markers (100 bp DNA Ladder); U: ‘Nangan 20’ unshiu mandarin; K: ‘Kinokuni’ mandarin. Lanes 1-40: hybrid population from a cross of ‘Nangan 20’ unshiu mandarin and ‘Kinokuni’ mandarin. (B) Hybrid populations of ‘Nangan 20’ unshiu mandarin and ‘Ponkan’ mandarin screened for early identification of zygotic seedlings. M: molecular weight markers (100 bp DNA Ladder); U: ‘Nangan 20’ unshiu mandarin; P: ‘Ponkan’ mandarin. Lanes 1- 47 hybrid population from cross of ‘Nangan 20’ unshiu mandarin and ‘Ponkan’ mandarin. (C) Hybrid population of ‘Miyagawa wase’ unshiu mandarin and ‘Sunburst’ mandarin screened for early identification of zygotic seedlings. M: molecular weight markers (100 bp DNA Ladder); U: ‘Miyagawa wase’ unshiu mandarin; S: ‘Sunburst’ mandarin. Llanes 1-45 hybrid population from a cross of ‘Miyagawa wase’ unshiu mandarin and ‘Sunburst’ mandarin. Horizontal arrows indicate the pollen specific amplification. Vertical arrows indicate zygotic amplification. |
Table 3. Effectiveness of UBC-27 primer in selecting zygotic seedlings from Citrus hybrid cultivars. |
Primer name | Size of PCR fragment | Hybrid Cross | Total seedlings | No. of zygotic seedlings | Rate of zygotic seedlings (%) |
| | “Nangan 20 × Kinokuni” | 40 | 29 | 73 |
UBC27 | 200-300 | “Nangan 20 × Ponkan” | 47 | 9 | 19 |
| | “Miyagawa wase × Sunburst” | 45 | 13 | 29 |
Acknowledgements
본 연구는 농림축산식품부 Golden Seed 프로젝트 ‘조숙생력형 품종 개발’ 프로젝트의 세부프로젝트’연내 수확용 부피경감 온주밀감 품종 개발’ 과제와 농촌진흥청 ‘감귤 육성품종 보급확대 및 육성소재 자원화 기술 개발’ 주관과제의 세부과제 ‘무핵 만다린 육성 자원화 기반 기술 개발(PJ01027303)’과제의 지원에 이루어짐.
References
Ahmad, M., A. Javaid, H. ur-Rahman, S.I. Hussain, A. Ramzan, and A. Ghafoor. 2012. Identification of mandarin X orange hybrids using simple-sequence repeat markers. J. Agric. Res. 50:225-232.
AL-Anbari, A.K., N. Kanawapee, T.A. AL-Kazragi, A. Al-Mashhadani, S. Barusrux, P. Pornpongrungrueng, and P. Theerakulpisut. 2014. Genetic diversity of citrus (Rutaceae) in Iraq based on random amplified polymorphic DNA (RAPD) markers. Afr. J. Agric. Res. 9:1012-1019.
Andrade-Rodríguez, M., A. Villegas-Monter, G. Carrillo-Castañeda, and A. García-Velázquez. 2004. Polyembryony and identification of Volkamerian lemon zygotic and nucellar seedlings using RAPD. Pesq. Agropec. Bras. 39:551-559.
Ashari, S., D. Aspinall, and M. Sedgley. 1988. Discrimination of zygotic and nucellar seedlings of five polyembryonic citrus rootstocks by isozyme analysis and seedling morphology. J. Hortic. Sci. Biotechnol. 63:695-704.
Esen, A. and R.K. Soost. 1977. Adventive embryogenesis in citrus and its relation to pollination and fertilization. Am. J. Bot. 64:607-614.
Furr, J.R, P.C. Reece, and G. Hranciar. 1946. Identification of hybrid and nucellar citrus seedlings by a modification of the rootstock color test. Proc. Fla. State Hortic. Soc. 59:38-42.
Gmitter, F.G. Jr, C. Chen, M.A. Machado, A.A. Souza, P. Ollitrault, Y. Froethlicher, and T. Shimizu. 2012. Citrus genomics. Tree Genet. Genomes 8:611-626.
Golein, B., R. Fifaei, and M. Ghasemi. 2011. Identification of zygotic and nucellar seedlings in citrus interspecific crosses by inter simple sequence repeats (ISSR) markers. Afr. J. Biotechnol. 10:18965-18970.
Kepiro J.L. and M, L. Roose. 2007. Nuceller Embryony, p. 141-149. In: I.A. Khan (ed). Citrus Genetics Breeding and Biotechnology. CAB international, UK.
Khan I.A. and M, L. Roose. 1988. Frequency and characteristics of nucellar and zygotic seedlings in three cultivars of trifoliate orange. J. Am. Soc. Hortic. Sci. 113:105-110.
Lima, D.R., A.D. Vilarionnos, W. dos. Soares Filho, and C. de J. Barbosa. 2000. Identification of citrus zygotic seedlings by use of RAPD markers. Revista Brasileira de Fruiticultura 22:181-185.
Mondal, B. and R. Saha. 2014. Identification if zygotic and nucellar seedlings of Citrus reticulate and Citrus aurantifolia using RAPD. Int. J. Adv. Biotechnol. Res. 5:25-30.
Moon, D.K. and K.C. Ko. 1991. Isozymes as genetic markers in Citrus growing in Cheju and their use for identification of nucellar and zygotic seedlings. J. Kor. Soc. Hort. Sci. 32:59-65.
Moore, G.A. and W.S. Castle. 1988. Morphological and isozymic analysis of open-pollinated Citrus rootstock populations. J. Hered. 79:59-63.
Oliveira, A.C., A.N. Garcia, M. Cristofani, and M.A. Machado. 2002. Identification of citrus hybrids through the combination of leaf ape× morphology and SSR markers. Euphytica 128: 397-403.
Oliveira, R.P., C.I. Aguilar-Vildoso, and M.A. Machado. 2003. Selection processes in a citrus hybrid populationusing RAPD markers. Pesq. agropec. bras. Brasília. 38:1297-1302.
Pieringer, A.P. and G.J. Edwards. 1967. Identification of nucellar and zygotic citrus seedlings by infrared spectroscopy. J. Am. Soc. Hortic. Sci. 86:226-234.
Rao, M.N., J.R. Soneji, C. Chen, S. Huang, F.G. Gmitter. 2008. Characterization of zygotic and nucell-ar seedlings from sour orange-like citrus rootstock candidates using RAPD and EST-SSR markers. Tree Genet. Genomes 4:113-124.
Ruiz, C., M.P. Breto, and M.J. Asins. 2000. A quick methodology to identify sexual seedlings in citrus breeding programs using SSR markers. Euphytica 112:89-94.
Scarano, M.T., N. Tusa, L. Abbate, S. Lucretti, L. Nardi, and S. Ferrante. 2003. Flow cytometry, SSR and modified AFLP markers for the identification of zygotic plantlets in backcrosses between ‘Femminello’ lemon cybrids (2n and 4n) and a diploid clone of ‘Femminello’ lemon (Citrus limon L. Burm. F.) tolerant to malsecco disease. Plant Sci. 164:1009-1017.
Tatum, J., C.J. Hearn, and R.E. Berry. 1978. Characterization of citrus cultivars by chemical differentiation. J. Am. Soc. Hortic. Sci. 103:492-496.
Tusa, N., L. Abbate, S. Ferrante, S. Lucretti, and M.T. Scarano. 2002. Identification of zygotic and nucellar seedlings in citrus interploid crosses by means of isozymes, flow cytometry and ISSR-PCR. Cell Mol. Biol. Lett. 7:703-708.
Yoo, K.Y., K.H. Cho, I.S. Shin, J.H. Kim, S. Heo, J.H. Non, H.R. Kim. 2009. Analysis of Genetic Relationships of Grapevine Cultivars (Vitisssp.) in Korea Using RAPD Markers. Kor. J. Breed. Sci. 41:437-443.
Yun, S.H., Y.S. Moon, S.B. Jin, I.K. Kang, and D.H. Lee. 2011. Early Identification of Putative Zygo-tic Seedlings in Citrus Crosses between ‘Morita unshiu’(Citrus. unshiu Marc.) and ‘Ponkan’(C. reticulata Blanco) Using RAPD and SRAP. J. Life Sci. 21:502-508.
Weinaaum, S.A., E. Cohen, and P. Spiegel-Roy. 1982. Rapid screening of satsuma mandarin progeny to distinguish nucellar and zygotic seedlings. HortScience. 17:239-240.




