서 언
재료 및 방법
부유 과실로부터 분석용 과피시료의 채취
페놀화합물의 분석
Polyphenol Oxidase(PPO)와 Peroxidase(POD) 활성의 분석
지방산의 분석
결과 및 고찰
‘부유’ 단감 과피의 성분분포
불균등 성분분포의 원인
일광과 과피흑변 발생의 관계
서 언
과피흑변은 ‘부유’ 과실의 저장 중에 흔히 발생하는 생리적 장해의 하나이다. 저장 개시 후 2-3개월 무렵에 발생하기 시작하는 이 증상은 과실의 외관을 손상하여 상품 가치를 크게 떨어뜨리는데, 특히 근래에 들어 우리나라 단감의 해외 수출이 확대되고 있는 상황에서 수출 단감에서 발생하는 과피흑변은 주요한 수출 장애요인이 되기도 한다. 과피흑변은 과육에는 영향을 미침이 없이 과피 조직에 국한하여 흑색의 반점이 형성되는 현상인데, Park(1999)과 Choi(2013)의 해부학적 관찰에 의하면 반점의 흑색 색소는 0.5mm 이내 두께의 과피조직에 분포하는 석세포 주위에 침적된다. 일반적으로 식물 조직의 흑변 또는 갈변을 일으키는 물질은 melanin 색소인 것으로 알려져 있다(Günter and Whitaker, 1984; Macheix et al., 1990). Choi(2013)는 ‘부유’ 과실의 흑변 과피에 침적하는 흑색 색소를 alkali fusion의 방법으로 분해하여 분석한 결과 이 색소가 catechin에서 유래하는 allomelanin이라고 보고한 바 있다. 한편 Park(1999)은 흑변 과실에서 흑반의 형태는 크게 흑점상, 파선형, 운형상 등의 형태로 나타나며 반점의 외형적 형태에 따라 흑변 조직의 해부학적 구조에 차이가 있다고 하였는데, 이는 반점의 형태에 따라 흑변의 발생 원인이 다를 수 있음을 암시한다. 저자의 관찰에 의하면, 이 중 점형 또는 선형 반점의 과피흑변은 조직의 균열, 상처 또는 병의 감염 등으로 과피가 물리적으로 손상된 부위에서 종종 관찰되는 반면에, 구름 형태의 커다란 흑색 반점을 형성하는 운형 과피흑변은 대개 과피 조직의 상처나 병의 감염 등과는 무관하게 발생한다. 또한 선형 또는 점형의 흑반은 과실 전면에 흩어져서 발생하고 크기가 점점 커지지는 않는 반면 운형 흑반은 표면의 특정 부위(대개 적도면에서 꽃받침 사이)에서 수 cm2의 크기로 발생한 후 발생 초기에는 색이 짙지 않으나 저장 기간의 경과와 더불어 흑색이 짙어지면서 흑반의 크기가 점차 확대되는 경향을 보인다.
일반적으로 과피흑변은 과실을 MA 포장 없이 과습 상태에서 저장하면 심하게 발생하고 적절하게 MA 포장하여 저장하면 발생이 크게 감소하지만 MA 저장 후 포장을 해체하여 저장 또는 유통할 때 발생이 증가하는 것으로 알려져 있다. 그러나 과피흑변의 발생 원인은 아직 확실하게 밝혀져 있지 않다. 단지, 수확 후 예건 기간 없이 곧바로 저온 저장고에 입고하거나 과습 조건에서 저장할 때 또는 산소 투과율이 높은 필름으로 포장하여 MA 저장할 경우 과피흑변의 발생이 증가하는 점에 비추어 볼 때, 과실의 수분 함량이나 MA 포장 내 산소 농도가 과피흑변의 발생과 상관이 있을 것으로 추정하고 있다. 특히 산소 농도와 관련하여, Lee et al.(2000)은 부유 과실의 MA 저장에서 과실의 중량 대비 포장 필름의 면적이 넓을수록 포장 내 산소 농도가 높고 이러한 조건에서 과피흑변의 발생이 증가한다고 보고하였다. 그러나 비단 수확 후의 조건뿐만 아니라 병해충, 영양, 온도, 수분, 광 등과 같은 수확 전의 생육환경 요인이 과실의 저장 중에 발생하는 다양한 생리적 장해의 원인으로 작용할 수 있는데(Ferguson et al., 1999), 과피흑변과 관련하여 수확 전 요인에 대한 연구는 충분히 이루어져 있지 않은 것으로 보인다.
저자는 ‘부유’ 과실의 과피에 함유되어 있는 몇 가지 성분을 분석하던 중에 과실의 부위마다 성분 함량이 크게 다를 뿐만 아니라 이러한 성분 함량의 차이가 수확 전 일조와 관련이 있으며 일광이 저장 중 운형 흑반의 형성에 영향을 미침을 발견하였다. 따라서 본 논문에서는 ‘부유’ 과실의 저장 중에 발생하는 과피흑변의 여러 유형 중에서 특히 운형 흑색 반점의 발생이 생육 중 과실의 일광 노출과 관련이 있다는 사실을 처음으로 보고하면서 일광이 과피흑변을 유발하는 기구에 대해 논하고자 한다.
재료 및 방법
부유 과실로부터 분석용 과피시료의 채취
경남 진영의 과원에서 2012년 11월 중순에 수확하여 관행적인 방법으로 MA 저장 중인 ‘부유’ 과실 중에서 이듬해 2월 초에 과피에 운형의 흑반이 발생한 과실과 발생하지 않은 정상과실을 각각 수집하여 1차 실험에 이용하였다. 먼저, 수집한 흑변 과실에 대해, 과실 표면을 네 부위로 구분한 후 1부터 4까지의 시료번호를 부여하여 과피시료를 채취하였는데, 1번은 흑반 부위의 과피이고 4번은 흑반 반대편의 정상과피이며 2번과 3번은 각각 1번과 4번에 인접한 정상과피이다. 다음으로, 수집한 정상과실에 대해서는, 과실의 표면을 여덟 부위로 구분하여 과피시료를 채취하였는데, 각 부위에 대한 과피시료의 번호는 성분 분석을 완료한 후에 성분 함량이 가장 높은 부위를 1번으로 하여 인접한 부위에 대해 시계 방향으로 순차적으로 8번까지 부여하였다. 저장 과실을 이용한 1차 분석을 종료한 후, 2차 실험을 위한 부유 과실은 2013년 11월 중순에 경남 창원의 과원에서 수확하였다. 이 때에는 수확 작업시에 과실의 수관 내 위치와 방위를 표시한 테이프 조각을 과실에 부착해 두었다가 실험실에 운송한 직후 표시에 따라 동서남북 네 방향의 과실 표면에서 각각 과피시료를 채취하였다. 모든 과피시료는 약 2mm 두께로 채취하였으며 채취 직후 액체질소에 동결하여 분쇄한 후 분석에 이용할 때까지 -70°C에 보관하였다. 모든 분석에는 8반복의 시료를 이용하였다. 한편, 수확 시 방위를 표시해 둔 70개의 과실을 20kg들이 플라스틱 상자에 담아 대형 비닐로 느슨하게 포장한 후 -1.5°C에서 저온 저장하였고 저장 3개월 후 과피흑변 발생 여부를 관찰하고 사진 촬영하는데 이용하였다.
페놀화합물의 분석
과피시료 100mg에 1mL의 methanol을 가하고 시료분쇄기(BioMasher, Nippi, Japan)를 이용하여 마쇄한 후 20,000×g로 원심분리하여 얻은 methanol 추출액을 페놀화합물의 분석에 이용하였다. 그러나 quercetin과 kaempferol 화합물의 분석 시에는 methanol 추출액(50μL)에 1M HCl-methanol (150μL)을 가하고 60°C에서 20분간 가열하여 모든 형태의 quercetin과 kaempferol 배당체를 가수분해하여 aglycon으로 전환한 후 분석하였다. 페놀화합물은 HPLC-MS를 이용하여 분석하였으며 분석 조건은 Choi(2013)와 같았다.
Polyphenol Oxidase(PPO)와 Peroxidase(POD) 활성의 분석
1g의 과피시료에 5mL의 추출용매(0.1M sodium phosphate buffer, pH 7.0, 10mM ascorbic acid, 0.2% Triton X-100)를 가하고 Ultra-Turrax(IKA T-25, Germany)를 이용하여 마쇄한 후 20,000×g로 원심분리하여 단백질을 추출하였다. 추출한 단백질 시료는 Sephadex G50 cartridge(HiTrap Desalting 5mL, GE Healthcare, USA)를 통과시켜 정제한 후 PPO와 POD의 활성 분석에 이용하였다. 10μL(POD 측정 시) 또는 30μL(PPO 측정 시)의 단백질 추출액을 400μL의 assay 용액과 혼합한 후 실온(25°C)에서 30초 동안의 흡광도(400nm) 증가를 1초 간격으로 측정하였다. PPO와 POD의 활성은 시간-흡광도 그래프에서 직선 구간의 직선의 기울기 값으로부터 구하였다. PPO와 POD assay 용액은 각각 2mM 4-tert- butylcatechol(40mM sodum phosphate buffer, pH 4.0)와 16mM guaiacol + 2mM H2O2 + 0.2mM tropolon(40mM sodum phosphate buffer, pH 5.0)이었으며, 흡광도의 측정은 분광광도계(UV-1700, Shimadzu, Japan)을 이용하였다. 단백질 추출액의 단백질 함량은 protein-dye binding 방법으로 측정하였다(Bradford, 1976).
지방산의 분석
동결건조한 50mg의 과피시료에 1.5mL의 4% H2SO4-methanol과 산화방지제로서 10μL의 50mg・mL-1 buthylated hydroxytoluene/ methanol과 내부표준물질로서 10μL의 50mg・mL-1 heptadecanoic acid/hexane을 가하고 밀폐한 후 100°C에서 1.5시간 가열하여 지방산을 methyl 유도체화하였다. 메틸화된 지방산은 1.5mL의 hexane으로 용매 추출한 후 GC(GC-2010, Shimadzu, Japan)를 이용하여 분석하였으며, 총 지방산에 대한 포화 지방산의 비율로 지질포화도를 산출하였다. GC의 분석조건은 다음과 같았다; column = SP2330(30m × 0.32mm ID, 0.25um FT, Supelco, USA), 운반기체 = N2(2mL・min-1), 시료주입; 시료주입량 = 1μL, 주입기 온도 = 220°C, split ratio = 10, column 온도 프로그램; 170°C 2분 → 4°C/min으로 200°C까지 승온 → 15°C/min으로 250°C까지 승온, detector = FID (280°C).
결과 및 고찰
‘부유’ 단감 과피의 성분분포
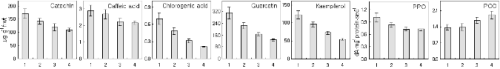
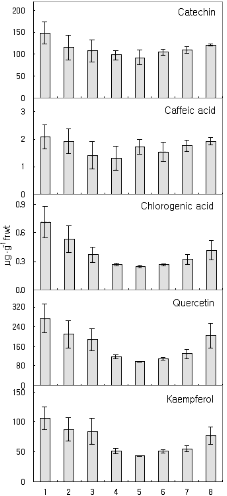
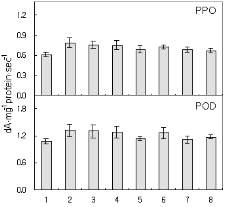
과피흑변이 발생한 과실에서 흑반 과피와 정상 부위의 과피 간에는 흑변의 유발과 관련된 특정 성분의 함량이나 효소의 활성에 차이가 있을 것으로 기대할 수 있다. 따라서 본 연구에서는 과피흑변의 발생 원인을 추적하는 방편으로, 우선, 운형 과피흑변이 발생한 과실을 대상으로 흑반 부위와 정상 부위 간에 페놀화합물 함량과 PPO 및 POD 활성의 차이가 있는지 분석하였다. 분석 결과, 흑반 부위의 과피는 정상 부위에 비해 catechin을 비롯한 모든 종류의 페놀화합물의 함량이 높았으며 흑반 부위에서 멀어질수록 함량이 점차 감소하여 흑반 반대편 부위의 정상 과피는 가장 낮은 페놀화합물 함량을 보였다. 한편 PPO는 페놀화합물의 분포와 동일한 양상으로 흑반 과피에서 높고 정상 과피에서 낮은 활성을 보였으나 POD의 활성은 이와 정반대의 분포를 보였다(Fig. 1). 이러한 성분 함량 또는 효소 활성의 차이가 과연 과피흑변 발생과 관련이 있는지 판단하기 위하여 이번에는 과피흑변이 발생하지 않은 정상 과실을 대상으로 부위별로 과피 시료를 채취하여 분석을 수행하였다. 모두 여덟 개의 정상과실을 대상으로 분석한 결과, 모든 과실에서 일관되게 페놀화합물 함량은 특정 부위(1번 부위)의 과피에서 가장 높고 그 반대편 부위(5번 부위)의 과피에서는 항상 가장 낮은 것으로 나타났다. 그러나 이와는 달리 PPO와 POD 활성은 과피 전체에 걸쳐 두드러진 부위별 차이를 보이지 않았다(Fig. 2). 따라서 이러한 분석 결과를 종합해 볼 때, 페놀화합물 함량의 부위별 분포의 차이는 정상과실과 흑변과실 모두에서 동일하게 관찰되는 현상으로서 과피흑변 발생의 직접적 원인은 아닌 것으로 보이지만 페놀화합물의 함량 증가가 흑변 발생에 유리한 조건을 제공할 수는 있을 것이다. 반면에, PPO와 POD 활성 분포의 차이는 과피흑변 과실에서만 관찰되었으며, PPO 활성의 증가와 POD 활성의 감소는 과피흑변의 유발과 모종의 관련이 있어 보인다.
불균등 성분분포의 원인
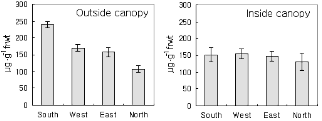
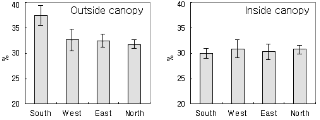
저장 과실을 대상으로 한 1차 실험에서, 비록 페놀화합물 함량이 높은 부위가 항상 흑변되는 것은 아니지만 흑변 부위의 페놀화합물 함량은 정상 부위에 비해 항상 높은 것으로 조사되었다. 이러한 사실은 페놀화합물의 불균등 분포를 야기한 어떤 요인이 과피흑변의 유발에도 관련되어 있음을 암시한다. 페놀화합물의 불균등 분포는 정상 과실에서도 보편적으로 관찰되는 현상이었으므로 이를 야기한 요인은 수확 전 요인일 가능성이 높다. 일반적으로 일광은 과실의 생육 기간 중 대사산물의 합성과 축적에 큰 영향을 미치는데, 일조의 차이를 유발하는 수관 내 과실의 위치나 과실의 부위에 따라 1차 또는 2차 대사산물의 함량에 차이가 나타날 수 있다(Feng et al., 2013; Magwaza et al., 2013; Yuri et al., 2010). 따라서 2차 실험에서는 페놀화합물의 불균등 분포를 유발하는 요인으로 일광을 가정하고 이를 확인하기 위한 분석을 수행하였다. 수관 외부에 위치한 남향 가지에서 수확한 과실로부터 동서남북의 네 방위로 구분해서 과피시료를 채취하여 quercetin을 분석한 결과, 그 함량은 직사 일광에 노출된 남향 과피에서 가장 높고 북향의 과피에서 가장 낮았다. 그러나 수관 내부에 위치하여 일광에 직접 노출되지 않았던 과실에서는 함량의 방위별 불균등 분포가 관찰되지 않았다(Fig. 3). 따라서 1차 실험에서 관찰된 페놀화합물의 과실 부위별 불균등 분포는 수확 전의 일광에 의해 야기된 것임을 확인할 수 있었다.
|
Fig. 3. Quercetin content on skin tissue of ‘Fuyu’ fruits harvested from outside and inside canopy (n = 8). Fruit surface was divided to 4 regions according to the direction from sun. |
일광과 과피흑변 발생의 관계
다음 단계로, 일광이 과피흑변을 유발하는 직접적인 원인이 될 수 있음을 확인하는 최선의 방법은 수확 작업시 과실의 방위를 표시해 두었다가 과피흑변 발생시에 표시해 둔 방위와 흑반의 위치를 비교하여 조사하는 방법일 것이다. Fig. 4는 이러한 조사 결과를 보이는데, 수확 시 일광에 노출되었던 남향 부위와 저장 중 흑반이 형성된 부위는 정확히 일치하였으며, 이로써 일광이 운형 흑반 형성의 일차적 원인이었음을 확인할 수 있었다. 한편, 일광에 지속적으로 노출되는 과실의 남향면은 북향면에 비해 온도가 상승하며 그 편차는 심하면 수십°C에 이를 수도 있다(Ferguson et al., 1998; Woolf et al., 1999). 따라서 과실의 생육 기간 중 남향면의 과피에서는 고온 스트레스에 순화하는 현상이 일어날 것으로 예상되는데, 이를 확인하기 위하여 과피의 지방산 포화도를 조사한 결과, 실제로 수관 외부의 남향 가지에서 수확한 과실의 남향면에서만 유독 포화지방산 비율이 높게 나타난 반면에, 직사일광에 노출되지 않은 수관 내부에서 수확한 과실에서는 지질포화도의 방위별 차이가 없었다(Fig. 5). 지질포화도의 이러한 차이는 일광의 여러 가지 효과가 고온에 대한 과실의 적응 현상과 관련이 있음을 강하게 암시한다(Antunes and Sfakiotakis, 2008; Shulte et al., 2013; Pearcy, 1978). 따라서 이러한 결과를 종합하면 일광이 부유 과실에서 과피흑변을 유발하는 기구에 대해 다음과 같은 시나리오를 추론해 볼 수 있다. (1) 생육 기간 중 직사일광에 노출되는 남향면의 과피 조직은 고온으로 인해 전반적으로 대사 속도가 증가하여 페놀화합물을 비롯한 대사산물의 고도 집적이 일어나는 한편 고온 순화 현상으로 인해 세포막의 지질포화도는 증가한다. (2) 이러한 과실을 수확하여 저장할 경우, 지질포화도가 높은 세포막은 저온에서 쉽게 경화되어 투과성이 증대되며(Antunes and Sfakiotakis, 2008; Pearcy, 1978) 이로 인해 평소 액포에 갇혀 있던 페놀화합물(Yamaki, 1984)이 액포 밖으로 유출됨에 따라 PPO에 의해 산화되어 melanin 색소가 생성된다. 이 시나리오가 옳다면 운형의 과피흑변 증상은 생육기간 중 고온에 적응한 과피 조직에서 일어나는 저온장해 증상(Antunes and Sfakiotakis, 2008)의 하나로 간주할 수 있을 것이다. 한편 이러한 시나리오 이외에, 일광에 노출된 과피는 일소 현상으로 인해 물리적 손상이 발생할 수 있으며 이로 인해 산소 투과성이 증가하여 과피흑변이 발생했을 가능성 또한 배제할 수 없으며 이에 대해서는 추가적인 확인이 필요해 보인다.