서 언
고온 스트레스 하에서 유기되는 산화 스트레스는 체내에 과다하게 생성된 활성 산소종에 의한 것으로 과산화수소(H2O2), 환원 산소종 및 hydroxyl radical(OH・) 등이 주를 이룬다(Fridovich, 1991). 이러한 활성 산소종은 세포막 구성성분인 불포화 지방산의 과산화 작용, 각종 효소의 불활성화 등과 같이 생리적으로 매우 중요한 세포질의 구성 요소에 피해를 입혀 장해를 유발한다(Monk et al., 1989). 하지만 식물은 superoxide dismutase(SOD), peroxidase(POX), catalase (CAT) 및 glutathione reductase(GR) 등과 같은 항산화 효소의 활성을 유도하여 활성 산소종으로부터 자신을 방어하고 있다(Bowler et al., 1992).
규소는 단위면적당 생산되는 식물의 건물중을 증가시키고 식물의 세포내, 세포벽, 세포 간극 및 외층에 축적되어(Marschner et al., 1990) 생물적 및 비생물적 스트레스에 대한 저항성을 향상시키는 역할을 한다고 알려져 있다(Epstein, 1999). 규소는 염 스트레스에 따른 엽록체의 손상과 그 대사작용의 장해를 완화시키는데 중요한 역할을 한다(Muneer et al., 2014). 또한 벼 재배시 규소를 배양액에 첨가하면 염류장해에 대한 식물체의 저항성이 향상되어 내건성이 증진된다(Matoh et al., 1986). 섬개야광나무의 미세번식시 규소를 배지에 첨가하여 배양하면 유리화 현상이 감소하고(Sivanesan et al., 2011), 분국화에 엽면처리하면 흰가루병에 대한 저항성을 향상시킨다(Park et al., 2013). 또한 규소는 고온 스트레스에 대한 벼(Agarie et al., 1998)와 국화(Song, 2012)의 저항성을 향상시켰다.
크리스마스 장식용 분화로 인기 있는 포인세티아는 12월에 출하하기 위해 고온기인 7-8월에 주로 번식하는데, 번식시설의 환경을 제대로 관리하지 못할 경우 고온 스트레스에 의해 모주의 삽수 생산량과 품질 뿐만 아니라 번식묘의 생장과 품질도 저하되는 경우가 많다. 따라서 본 연구에서는 고온기에 포인세티아의 모주와 번식묘의 생산시 발생하는 고온 스트레스와 관련된 문제점의 해결방안으로서 규소의 시비효과를 알아보고자 규소원(K2SiO3, Na2SiO3, CaSiO3)과 규소처리방법(저면관수, 엽면살포)을 달리하여 재배한 포인세티아의 생육과 스트레스 저항성을 조사하였다.
재료 및 방법
식물 재료와 규소 처리
분화용 포인세티아(Euphorbia pulcherrima Willd.) ‘Ichiban’의 삽수를 채취하여 평균온도 25 ± 2°C와 상대습도 80 ± 10%인 번식상에서 발근시킨 후 상토(Tosilee Medium, Shinan Grow Co., Jinju, Korea)가 담긴 10cm 화분에 정식하였다. 균일한 식물체를 선발하여 완전임의배치 하고, 순환식 저면관수시스템을 이용하여 양액을 공급하며 재배하였다. 규산염은 예비실험에서 가장 효과적이었던 50mg・L-1 Si 농도로 CaSiO3, Na2SiO3, 또는 K2SiO3를 용액으로 만들어 엽면살포하거나 또는 양액에 첨가하여 저면관수로 공급하였다. 양액에 첨가한 처리는 온실다용도액비[Ca(NO3)2・4H2O 708.0mg・L-1, MgSO4・7H2O 246.0mg・L-1, KNO3 505.0mg・L-1, NH4H2PO4 230.0mg・L-1, H3BO3 1.24mg・L-1, CuSO4・5H2O 0.124mg・L-1, Fe-EDTA 4.0mg・L-1, MnSO4・4H2O 2.2mg・L-1, H2MoO4 0.08 mg・L-1, ZnSO4・7H2O 1.15mg・L-1]에 혼합하여 매일 1회씩 저면관수로 공급하였고, 엽면살포 처리는 각 규산염을 증류수에 용해시켜 분무기로 잎이 충분히 젖도록 매주 1회씩 공급하였다. 저면관수 처리는 첨가된 규소에 의해 증가된 양액내 이온(Ca2+, Na+ 또는 K+)의 양을 조절하여 총 이온의 농도를 온실다용도액비와 동일하게 조정하였다. 저면관수에 의해 공급한 양액의 EC는 1.4-1.6mS・cm-1, 그리고 pH는 6.0으로 조절하였다. 식물을 재배하는 동안 온실의 평균기온은 23.0 ± 4°C이고 평균 상대습도는 70-80%이었다. 규소 처리에 의한 식물의 생육차이를 정확히 판단하기 위하여 생장억제제는 사용하지 않았다.
수확 후 고온처리
고온 스트레스에 대한 포인세티아의 저항성을 알아보기 위하여 규소를 처리하며 재배한 8주째에 식물생장상(KGC- 175VH, Koencon Co., Hanam, Korea)에 처리당 3반복씩 반복당 3개체를 완전임의배치하여 18일간 더 재배하였다. 식물생장상의 환경으로 광도는 410 ± 30μmol・m-2・s-1 PPFD, 온도는 35 ± 1°C, 그리고 습도는 70 ± 10%로 유지하였다. 고압나트륨(SON-T Pro 400W, Philips, USA)을 사용하여 1일 9시간의 명기와 15시간의 암기로 광주기를 조절하였다. 생장상으로 식물을 옮긴 직후 배지가 충분히 포화되게 양액을 관주하였고, 그 이후에는 매 2일마다 1회씩 300mL의 양액을 관주하였다.
생장측정
고온에서 재배한 18일째에 식물을 채취하여 초장, 경경, 근장, 뿌리의 생체중과 건물중을 조사하고 잎 조직내 Si, P, K, Ca 등 주요 원소의 함량을 측정하였다. 또한 고온 스트레스에 의한 식물체의 손상과 스트레스 내성 정도를 알아보기 위하여 electrolyte leakage percent(ELP), Fv/Fm(maximum quantum yield of photosystem II), 광합성율을 조사하고 scanning electron microscopy(SEM)로 기공을 관찰하고 wavelength dispersive X-ray(WDX)로 규소의 분포도를 조사하였다.
ELP는 Lutts et al.(1995)의 방법으로 측정하였으며, 성엽을 2차 증류수에 3회 세척하여 물기를 제거한 후 1cm2 크기로 잘라 25mL의 멸균수가 담긴 유리관에 넣었다. 유리관을 회전 진탕기에 고정시켜 120rpm에서 24시간 동안 용해하여 EC 측정기(Model C531, Consort MA, Turnhout, Belgium)로 측정한 값을 EC1로 나타냈다. EC1 측정 후 고압멸균기로 121°C에서 15분 동안 고압 멸균시켜 상온에서 식힌 후 다시 측정한 전기전도도 값을 EC2라고 하였다. 그리고 EC1과 EC2를 아래의 공식에 대입하여 ELP를 계산하였다(Lutts et al., 1995).
ELP = EC1/EC2 × 100(%)
휴대용 광합성 측정기(Li-6400, LI-COR, Inc., Lincoln, NE, USA)를 이용하여 오전 9시부터 오후 1시 사이에 신초 기부로부터 4-5번째의 잎의 광합성속도를 측정하였다. 고온 환경하에서 최적 환경으로의 변화 후 포인세티아의 광합성능력을 조사하기 위해 광합성율을 최적 환경(CO2 농도 600μmol・mol-1, 광도 1,000μmol・m-2・s-1 PPFD, 엽면적 6cm2, 온도 25°C)에서 측정하였다. 처리당 3개체씩 10초 간격으로 6회씩 측정하여 최고값과 최저값을 제외한 값의 평균값을 측정값으로 하였다.
엽록소형광측정기(PAM 2100, Walz, Effeltrich, Germany)를 이용하여 Fv/Fm을 Kooten and Snel(1990)의 방법으로 측정하였다. 광합성을 측정하였던 동일한 잎을 암 적응 클립으로 30분간 적응시킨 후 Fv/Fm값을 측정하였다.
포인세티아 잎 조직의 기공과 규소 분포도를 알아보기 위하여 WDS(JXA-8100, Jeol, Tokyo, Japan)가 장착된 SEM (LEO-435VP, Zesis, Jena, Germany)으로 관찰하였다. 최근에 전개한 가장 큰 잎을 종단면으로 절단하여 e-tube에 넣고, 0.1M phosphate buffer로 희석한 2.5% glutaraldehyde 고정액 1mL를 첨가하여 4°C에서 24시간 동안 처리하였다. 시료에 묻은 glutaraldehyde 고정액을 제거하기 위하여 0.1M phosphate buffer(137mM NaCl + 2.7mM KCl + 43mM NaHPO4 + 1.4mM KH2PO4)로 10분씩 3회 세척하였다. 세척 후 시료를 30, 50, 70, 90 및 100%(v/v) EtOH 용액으로 저농도부터 고농도 순서로 20분씩 탈수하였다. 탈수시킨 시료를 80% 아세톤에 30분간 건조 후 250-450Å의 금 입자로 2분간 도금하여 가속전압 20KV의 SEM으로 관찰하였다.
항산화 효소의 활성 분석
SOD(superoxidase dismutase), APX(ascorbate peroxidase activity), CAT(catalase), POD(peroxidases)의 활성과 총 단백질 함량을 측정하기 위해 0.5g의 잎 조직을 채취하여 1mM EDTA, 0.05% Triton X-100, 1mM polyvinylpyrrolidone, 그리고 1mM ascorbate가 첨가된 50mM phosphate(pH 7.0)에 균질화시켰다. 균질화된 샘플을 4°C에서 20분 동안 13,000 rpm으로 원심 분리하여 측정하였다.
SOD 활성은 NBT 환원법을 사용하여 측정하였다(Beauchamp and Fridovich, 1971). 50mM phosphate buffer(pH 7.8), 2mM riboflavin, 13mM methionine, 75μM NBT, 0.1mM EDTA 및 효소 추출액을 사용하였다. 반응 화합물을 첨가한 샘플을 25°C의 광 상태에서 30분간 반응시킨 후 흡광도를 560nm에서 측정하였다. 대조구는 광을 조사하지 않은 반응물을 사용하였다. Extinction coefficient는 100mM-1・cm-1을 사용하였다.
APX의 활성은 Chen and Asada(1989)의 방법에 준하여 pH 7.0에서 측정하였다. 반응 화합물은 50mM phosphate buffer(pH 7.0), 0.5mM ascorbate 및 효소 추출액을 사용하였고 과산화수소를 20mM 첨가하여 290nm에서 3분간 반응시켰다. Extinction coefficient는 290nm에서 2.8mM-1cm-1을 사용하였다.
CAT의 활성은 Aebi(1984) 방법에 따라 50mM phosphate buffer(pH 7.0)에 20mM H2O2와 추출액을 첨가한 후 흡광도 변화를 3분간 240nm에서 관찰하였다. H2O2의 molar extinction coefficient는 240nm에서 0.04μmol-1・cm-1을 사용하였다.
POD의 활성은 0.1M phosphate buffer(pH 7.0), 0.05mL guaiacol solution, 0.1mL 효소추출액, 그리고 0.03mL hydrogen peroxide를 혼합하여 흡광도를 436nm에서 측정하였다(Sadasivam and Manickam, 1996).
통계분석
통계분석은 SAS 프로그램(v. 9.1, Cary, NC, USA)을 사용하여 Duncan의 다중검정(DMRT)으로 5% 수준에서 유의성을 검정하였다.
결과 및 고찰
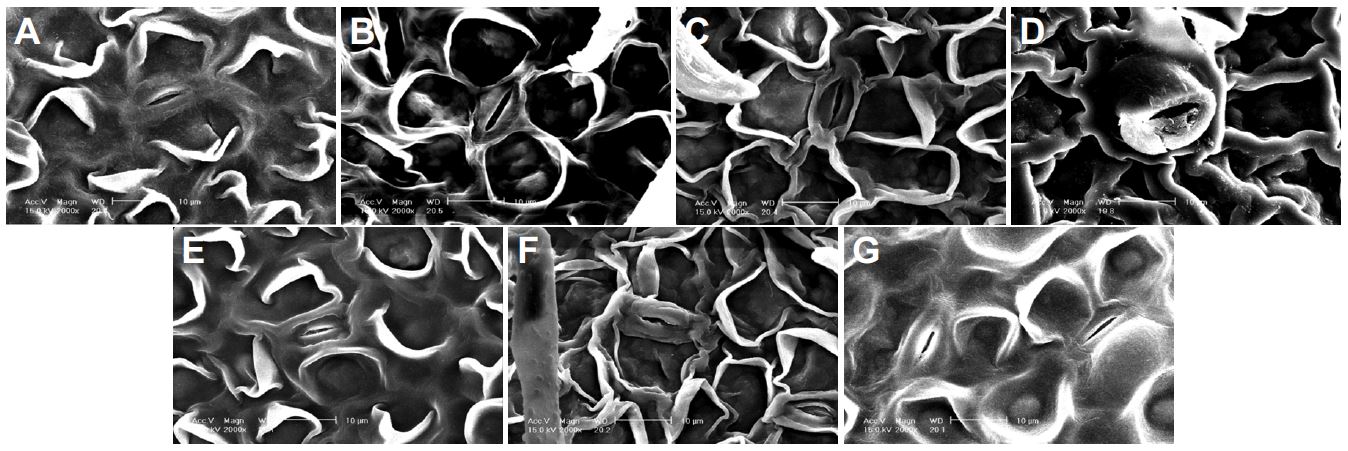
고온 스트레스 하에서 세 가지의 규산염이 포인세티아의 생장에 미치는 영향을 비교한 결과 대조구와 규소 처리구간에 차이가 없었다(자료 미제시). 하지만 포인세티아를 육안으로 관찰하였을 때 저면관수 K2SiO3처리와 Na2SiO3처리에서 대조구에 비해 잎이 시들고 잎 끝이 말리는 현상이 적었다(Fig. 1). 이것은 저면관수 K2SiO3처리와 Na2SiO3처리에서 대조구에 비해 기공이 명확하게 관찰(Fig. 2A-C)되었으므로 증산작용이 정상적으로 일어났기 때문에 나타난 결과라고 생각된다. 하지만 저면관수 Na2SiO3처리에서는 다른 규소원과 다르게 기공의 형태가 정상적이지 않았다(Fig. 2D). 규산염을 엽면살포한 모든 처리에서는 대조구와 저면관수 규산염처리에 비해 잎이 시드는 현상이 더 많이 발생하였다(Fig. 1). 엽면살포 규산염처리에서는기공이 찌그러지거나 정상적인 형태를 보이지 않아(Fig. 2E-G) 기공의 개폐 능력이 저하(Chung et al., 2007)되었을 것으로 생각된다.육안으로 관찰되었던 지상부 잎의 생장은 처리에 따라 차이를 보였으나 대부분이 고사하여 초장, 경경, 뿌리의 생장만 측정할 수 있었기 때문에 처리에 따라 생장(자료 미제시)이 차이가 없었던 것으로 판단된다.
규소함량은 저면관수 규산염 처리가 엽면살포 규산염 처리보다 많았다(Table 1). 이러한 결과는 밀(Guevel et al., 2007), 벼(Ma et al., 2006), 칼랑코에(Son et al., 2012)에서 유사하게 나타나, 규소는 뿌리를 통해 공급하는 것이 효과적일 것이라 생각된다. 규소는 저면관수 Na2SiO3에서 1.03µg・mg-1dw로 가장 많았고, 다음은 K2SiO3와 CaSiO3의 순이었다. 저면관수 K2SiO3처리에서는 K 함량이 54.5µg・mg-1dw, 그리고 Na2SiO3처리에서는 Na 함량이 9.8µg・mg-1dw로 다른 규산염 처리에 비해 증가하였다. 저면관수 K2SiO3처리에서 Mg의 함량이 낮아진 것을 볼 수 있었는데, 이것은 K+와 Mg2+사이에서의 길항작용으로 K+의 흡수가 증가되면서 Mg2+의 흡수를 방해(Marschner, 2003)한 것으로 판단된다. 저면관수 Na2SiO3처리에서 P과 Mg의 농도가 가장 높았는데, 이것은 칼랑코에에 Na2SiO3를 저면관수하였을 때 나타난 결과(Son et al., 2012)와 유사했다. Na2SiO3 처리에서 K의 함량이 낮아진 것은 Na+와 K+사이에서의 길항작용으로 인해 Na+의 증가가 K+의 흡수를 방해한 것이라고 판단된다. 엽면살포는 저면관수와 다르게 각 원소들 사이에 일정한 상관관계가 나타나지 않았다.
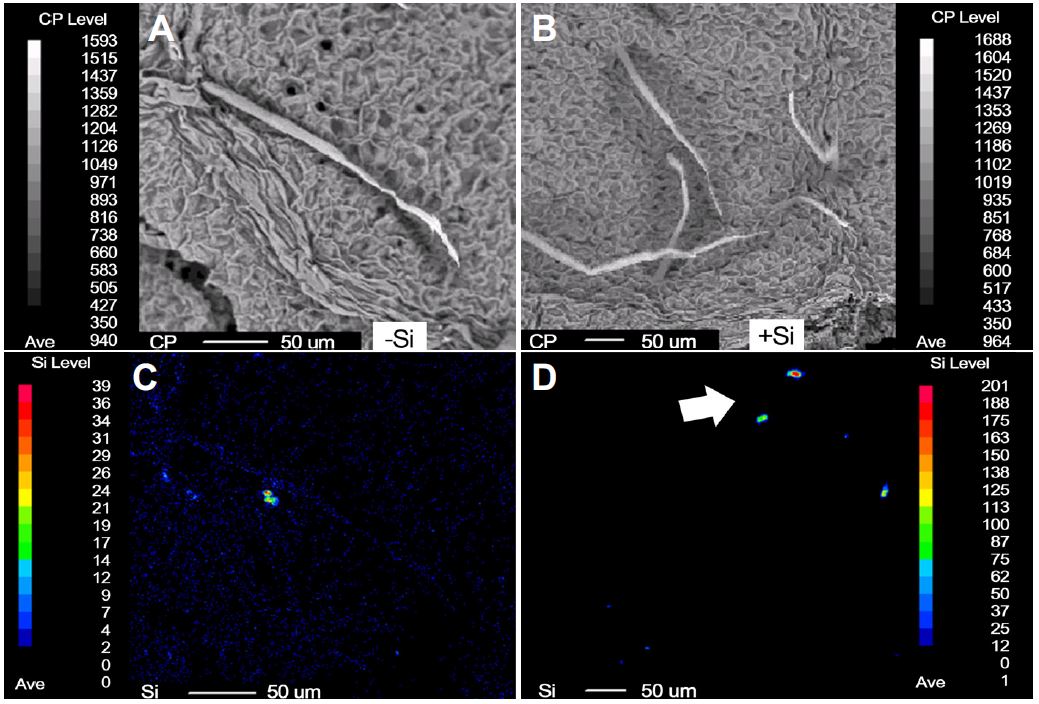
포인세티아의 잎 조직과 잎 조직 내 규소 분포도를 WDS로 관찰한 결과 대조구에서는 세포가 정상적인 형태를 보이지 않으면서(Fig. 3A) 규소가 매우 적게 분포하였으며(Fig. 3C), 규산염처리에서는 세포가 조밀하면서(Fig. 3B) 작은 규소 입자가 많이 분포되었다(Fig. 3D). 벼의 잎 표면에서는 규소가 모용(trichome), 후막세포, 그리고 아포플라스트에 분포되는 것으로 보고되었다(Sangster et al., 2001). Samuels et al.(1991)은 규소가 부족한 식물에게 규소가 첨가된 양액을 공급하였더니 모용 기부에 중합체 형태로 빠르게 축적되는 것을 발견하였다. 이와 같이 잎에서의 규소 분포는 수용성 규소염[Si(OH)4]이 일련의 증산작용으로 물관부를 통하여 배양액으로부터 식물체 내로 흡수된 것으로 판단되는데 흡수된 규소는 무정형의 silica gel (SiO2・nH2O)의 중합체 형태로 나타난 것으로 보고되었다(Jones and Handreck, 1967).
고온 스트레스 처리를 개시하면서 생장 챔버로 옮기지 않고 온실에서 계속 재배한 식물(Fig. 4A)에서는 화아가 형성되었으나 고온에서 규산염을 처리하지 않고 재배한 식물(Fig. 4B)에서는 화아가 형성되지 않았다. 이것은 고온 하에서 포인세티아의 화아의 형성이 지연되어 포엽의 착색과 개화가 지연되었음을 의미한다. 고온처리 후 줄기 기부에서의 신초는 대조구에서는 말려 있었으나(Fig. 5A) 저면관수 K2SiO3처리에서는 활짝 펼쳐져(Fig. 5B) 있었다. 이것은 규소가 식물체를 강건하게 하여 지제부의 신초를 생장하게 할 수 있었던 것으로 판단된다.
세포막의 손상으로 나타나는 ELP는 환경스트레스의 지표(Cordi et al., 1997)로 사용되고 있다. ELP는 처리에 따라 통계적인 유의성은 없었지만 저면관수 K2SiO3에서는 대조구에 비해 6% 감소하였다(Table 2). 규소를 처리하면 식물의 세포벽이 두꺼워지면서(Kim et al., 2002), 세포벽의 기계적 성질이 향상되어 전해질 유출이 감소(Agarie et al., 1998)한다. 하지만 본 연구결과에서는 반복간의 ELP 차이가 크고 개체수의 부족으로 신뢰성이 있는 결과를 얻지 못한 것으로 판단된다.
Fv/Fm은 엽록체의 틸라코이드막에서 방출되는 반응을 수치화한 값으로 식물의 광 이용 효율과 직접적으로 관여되는 대사 능력 정도를 간접적으로 보여 주는 수치이다(Lavorel and Etienne, 1977). 대부분의 식물에서 건강한 잎의 경우 Fv/Fm값이 보통 0.83 정도이며(Choi et al., 2004), 이 값보다 낮을 경우 식물이 스트레스에 노출되었거나 노화가 진전되었다고 할 수 있다. 포인세티아의 Fv/Fm값은 전체적으로 약 0.3-0.6의 수치를 나타냈으며, 저면관수 K2SiO3와 Na2SiO3처리가 엽면살포 K2SiO3와 CaSiO3처리보다 높았다(Table 2). 특히 Fv/Fm값은 저면관수로 규산염을 공급시 K2SiO3와 Na2SiO3처리는 각 0.669와 0.592로 CaSiO3의 0.357에 비해 높았다. 이와 같이 저면관수 Na2SiO3처리와 K2SiO3처리에서 대조구에 비해 ELP값은 낮고 Fv/Fm값과 광합성율이 높은 것으로 보아 고온에서 스트레스를 덜 받은 것으로 판단된다(Fig. 1 and Table 2).
포인세티아를 고온 스트레스 하에서 최적 환경에 노출시켰을 때의 광합성율을 조사하였다(Table 2). 광합성율은 저면관수 K2SiO3처리에서 3.15μmolCO2・m-2・s-1로 가장 높았다. 이것은 다른 처리구에 비하여 고온 스트레스의 영향이 적어 뿌리로부터 수분흡수가 정상적으로 이루어졌기 때문에 상대적으로 더 왕성한 증산작용을 한 것으로 생각된다. 이에 따라 포인세티아의 잎 표면의 온도가 낮아져(Song, 2012) 다른 처리구에 비해 광합성율이 높게 나타난 것으로 판단된다. 저면관수 CaSiO3처리에서는 광합성 속도가 0.69 μmolCO2・m-2・s-1로 가장 낮았다. 그 주된 원인은 저면관수 CaSiO3처리에서 뿌리의 생체중(자료 미제시)이 가장 적었기 때문인 것으로 생각된다.
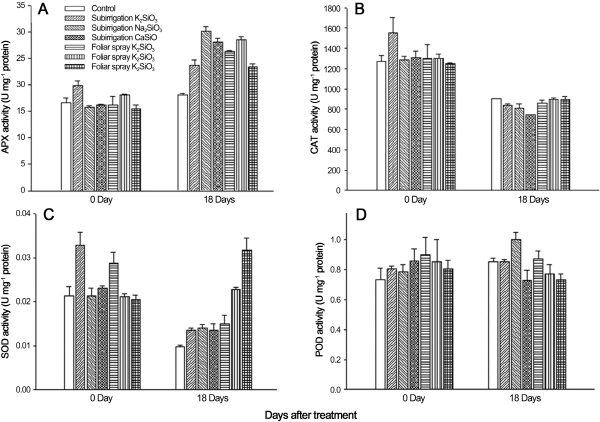
SOD는 산소분자로부터 한 개의 전자가 환원되어 생성되는 superoxide anion radical(O2-)을 제거시키는 작용(2O2 + 2H+ → H2O2 + O2)을 하는 효소로서 활성산소종에 대한 방어작용을 하는 대표적인 활성산소 저해제이다(Bannister et al., 1987). CAT, APX, POD는 환경 스트레스하에서 활성이 증가된 SOD에 의해서 생성되는 과산화수소를 물분자와 산소분자로(2H2O2 → O2 + 2H2O) 분해함으로써 과다한 활성산소종에 의한 피해를 감소시키는 것으로 알려져 있다(Kang et al., 1998). APX 활성이 규산염 처리에서 대조구에 비해 증가한 것은 고온 스트레스에 대한 방어기능이 향상된 것으로 판단된다(Fig. 6). 하지만 CAT, SOD 및 POD의 활성은 차이가 없거나 감소하였다(Fig. 6). CAT, SOD, 그리고 POD의 활성이 대조구에 비해 큰 차이가 나타나지 않은 것은 알 수 없지만, 각 항산화 효소의 작용은 식물, 처리온도, 기간에 따라 다르게 나타날 수 있음을 의미한다.
이러한 결과로 포인세티아는 저면관수를 통해 공급한 K2SiO3에서 규소가 가장 많이 흡수되었으며, 이러한 규소의 영향으로 고온 스트레스 하에서 식물의 Fv/Fm값과 광합성율이 증가하고 정상적으로 화아가 형성된 것으로 보아 식물의 저항성이 향상된 것으로 판단된다. 또한 규소의 사용으로 하절기 고온시에 모주를 관리하는데 나타나는 삽수의 생산량과 품질의 저하와 같은 문제점을 최소화할 수 있을 것이라 생각된다.