서 언
재료 및 방법
포장 조성과 복숭아 묘 재식
수체 전정 및 착과 조절
시험 처리 전후 토양 분석 및 처리 수체 선발
시비 관리 설정과 용성 인비 처리
신초 생장과 엽내 무기물 함량 분석
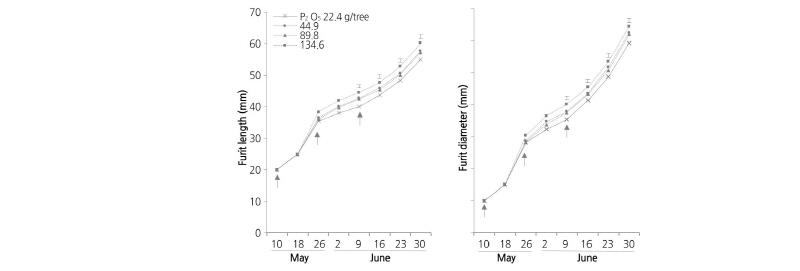
과실 생장과 특성 조사
통계 분석
결과 및 고찰
용성인비 덧거름 시비량에 따른 신초 생장과 엽내 무기물 함량
용성인비 덧거름 시비량에 따른 신초엽의 SPAD 값 변화
용성인비 덧거름 시비량에 따른 과실 비대 및 품질 특성
서 언
복숭아는 다른 과수에 비해 소비자 선호도와 소비량이 당도에 의해 크게 좌우된다. 하지만 대부분 노지에서 재배되고 있는 복숭아는 당도 저하의 주요인인 자연 강우를 회피하기 어렵다. 장마가 시작되는 7월 상순에 수확되는 조생종 복숭아 ‘유미’ 품종도 당도가 낮아(KSVC, 2009) 당도 증진을 위한 적합한 시비
관리 기술을 체계화하고 개발할 필요가 있다.
과수 재배에 있어 시비는 생육, 과실 품질 및 생산성을 좌우하는 요인으로 농촌진흥청에서는 질소, 인산 및 칼륨 3성분에 대한 표준 시비량을 제시하고 있다(NAAS, 2010). 인(phosphorus)은 핵산 및 ATP 구성 요소로서 에너지 전달, 세포 간 탄수화물 전류, 그리고 이에 따른 다양한 생화학적 대사에 영향을 준다(Hawkesford et al., 2012; Lambers and Poorter, 1992). 토양에 시비된 인산질 비료는 H2PO4-나 HPO42- 형태로 식물에 흡수되며 어린 조직에서 다량 발견된다(Lee et al., 2011; Shen et al., 2011).
과수류에서 인산질 비료 공급은 잎 및 과실 내 인 함량을 증가시켜 착화 및 수확량을 증가시키고(Neilsen and Hogue, 1990; Neilsen et al., 1999), 과실 내 당 함량의 증가와 신맛의 감소를 가져온다(Kim et al., 1999; Raese, 1987). 그리고 인산질 비료는 뿌리나 토양 미생물에서 분비되는 유기산에 의해 가용화되어 흡수된다(Sagoe et al., 1998). 그러나 수용성 인산질 비료의 토양 시비 시 토양의 물리․ 화학적 특성 변화와 다른 성분과의 길항 관계에 의해 인산의 불용화 및 흡수율 저하 등이 나타난다(Georage et al., 2005; Jakobsen, 2008; Yeo et al. 2016).
국내에서 인산질 비료에 대한 연구는 수경재배 시스템이 발달한 채소류에서 생육 단계 및 환경 변화에 따른 시비 체계가 심도 있게 연구되고 있으나(Choi, 2003; Choi and Park, 2007; Choi et al., 2009), 과수류에서는 사과나 배나무에서 질소질 비료(Choi et al., 2013; Ro et al., 2015)의 토양관주 시스템 연구 외에는 시비 관리 체계화를 위한 연구가 부족한 실정이다. 특히, 토양재배에서 구용성 용성인비를 전량 기비로 사용하도록 제시하고 있으나(NAAS, 2010), 다양한 환경에서 그 효과가 불규칙적으로 나타나고 있다. 특히, 인산질 비료가 토양 입자에 흡착되면 염류집적 요인으로 작용할 수 있는(Chung et al., 2008) 반면, 가용화된 상태에서 흡수되기 쉬우므로 뿌리 발생과 지상부 생장 시기에 부합한 인산 시용법에 대한 연구가 필요하다.
따라서 본 연구는 인산질 비료 분시 효과를 구명하기 위하여 복숭아 ‘유미’의 신초 생장 및 과실 품질에 미치는 용성인비의 덧거름 시용량의 영향을 분석하여 복숭아 품질 향상을 위한 인산 토양 시비방법의 기초 자료를 마련하고자 수행되었다.
재료 및 방법
포장 조성과 복숭아 묘 재식
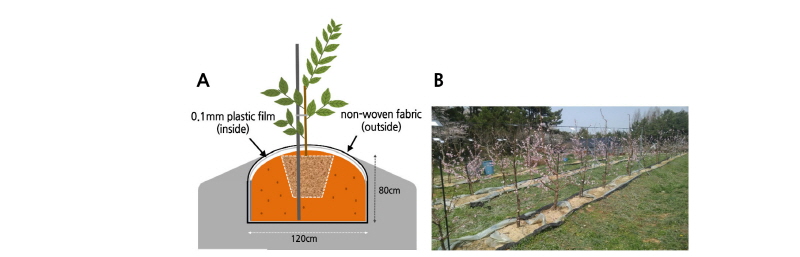
2.5m 간격의 재식 열을 만들기 위해 2015년 2월 원광대학교 과수실습포장을 너비 120cm, 깊이 50cm로 판 다음 중력에 의한 양분의 손실을 방지하기 위해서 검정 부직포와 0.1mm 두께의 플라스틱 필름을 이용하여 2중으로 재식 열의 바닥 및 측면 전체를 피복한 후 재식 토양 높이가 80cm가 되도록 마사토로 채웠다(Fig. 1A). 마사토의 성분 분석 결과 pH 5.72±0.10, EC 0.187±0.04dS·m-1였고, T-N과 P2O5는 각각 2.3± 0.24, 13.0± 0.41mg·kg-1였다. 치환성 양이온인 Ca, K, Mg, Na은 각각 4.54±0.32, 0.26±0.02, 2.26±0.36, 0.22±0.05cmolc·kg-1이었다.
당해 봄에 조성된 포장에 포트(직경 45cm, 높이 50cm)에서 자란 2년생 복숭아 ‘유미’의 묘를 2m 간격으로 재식하였다(Fig. 1B). 그리고 수체 간 토양 내 양․ 수분의 이동을 방지하기 위해서 묘목과 묘목 중간에 두께 0.1mm 두께의 플라스틱 필름으로 칸막이를 견고하게 설치하였다. 이후 2015년과 2016년도에는 농촌진흥청의 복숭아 수령별 표준시비량(NAAS, 2010)에 따라 요소, 용성인비, 염화칼륨으로 시비 관리를 하였다.
수체 전정 및 착과 조절
2017년 2월 상순에 재식 후 주간형으로 키운 복숭아 나무를 전정하였다. 전정 시 솎음전정을 통해 수체당 원가지 수를 조절한 후 원줄기 아래 부분에서 발생한 50cm 이상의 결과지를 50cm 길이로 동일하게 절단전정하였고, 결과지 수를 솎음전정으로 수체당 25개 정도로 조절하였다.
개화 시에 수체당 70% 정도를 적화하였고, 이후 수정 완료 후 2회에 걸쳐 30-50cm 정도의 장과지에는 2-3개, 20-30cm 정도의 중과지에는 1-2개, 20cm 이하의 단과지에는 1개 과실을 남기고 적과작업을 실시하였다. 봉지씌우기는 2차 적과작업과 함께 실시하였다. 병해충은 관행적 방제와 관찰에 의한 응급 방제를 실시하였다.
시험 처리 전후 토양 분석 및 처리 수체 선발
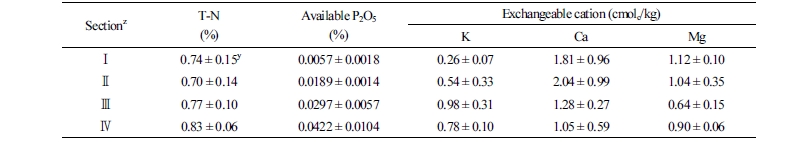
2017년 본 시험 수행 직전 농촌진흥청 종합검정실 분석 매뉴얼(RDA, 2013)에 따라 근권부 토양분석을 수행하였다(Table 1). 수체별 토양분석 결과에서 인산 함량에 따라 4구간으로 분류하였다. 전년도 예비시험에서 3년생 복숭아의 표준시비량(NAAS, 2010)을 기준으로 하여 0.5-1.5배 증시 처리에서 차이가 없었기 때문에 유효인산 함량이 가장 낮은 구를 표준 시비구로 처리하고 각각 2, 4, 6배 처리구를 배치하였다. 과실 수확 직후에 연구 수행 직전과 동일한 방법으로 각 처리구의 토양분석을 실시하였다.
시비 관리 설정과 용성 인비 처리
질소[요소, (NH2)2CO], 인산(용성인비, CaOBMgOP2O5NSO2-F, P2O5 17%), 칼륨(염화칼륨, KCl) 시비량은 농촌진흥청에서 제시한 4년생 복숭아 표준시비량(NAAS, 2010)을 기준으로 사용하였다. 본 시험 포장의 재식밀도(5m2/tree)는 농촌진흥청의 표준시비량의 기준의 1/3이었기 때문에 수체당 시비량을 요소 290g, 용성인비 330g, 염화칼륨 180g으로 설정하였다.
수체당 용성인비 330g의 60%는 밑거름으로 시비하였고, 40%인 132g를 덧거름으로 설정하였다. 용성인비 덧거름 시비량을 표준시비, 2배, 4배 및 6배로 하였는데 각각 인산(P2O5) 함량은 22.4g, 44.9g, 89.8g 및 134.6g이었다. 시비량을 처리별로 3등분하여 3회 분시하도록 설정한 후 가루로 분쇄하여 2% 구연산 용액에 완전히 녹이고 물을 혼합하여 20L/tree로 정량하였다. 분시 시기는 신초 생장 및 과실 비대기인 5월 10일, 5월 25일, 6월 9일이었다. 정량한 비료를 수체 원줄기를 중심으로 30cm 떨어진 근권부에 환상으로 15cm 깊이로 판 후 고르게 부어 주었다.
신초 생장과 엽내 무기물 함량 분석
2017년 5월 11일부터 10일 간격으로 결과지의 중간에서 자란 신초를 표시한 후 길이와 엽록소지수(SPAD)를 측정하였다. 신초 길이는 1m 자를 이용하여 cm 단위로 측정하였고, 잎의 엽록소지수는 신초의 중간 부위에 위치한 전엽이 끝난 건전한 잎을 대상으로 간이 엽록소측정기(SPAD-502, Minolta, Tokyo, Japan)를 이용하여 측정하였다.
엽내 무기물 함량은 수확 직후 신초의 중간 부위에 위치한 잎을 처리별로 채취하여 60°C의 건조기에서 3일간 건조시킨 후 분쇄하여 농촌진흥청 종합검정실 분석 매뉴얼(RDA, 2013)에 따라 총질소(T-N), P, K, Ca, Mg 함량을 분석하였다.
과실 생장과 특성 조사
과실 생장 변화를 보기 위해서 마지막 적과 후 처리별로 수체당 6개 과실을 표시한 후 1주일 간격으로 과실의 종경과 봉합선을 중심으로 최대 적도면 길이인 횡경을 측정하였다.
성숙과의 특성 조사는 7월 5일부터 2일 간격으로 3회 수확하여 과중, 가용성 고형물 함량, 과피 및 과육 경도, 과피색, 유리당 및 유기산 함량을 조사하였다. 경도는 종합 물성 측정기(Sun Rheo Meter, Compac-100, Sun Scientific Co., Ltd., Tokyo, Japan)를 이용하여 직경 3mm 어뎁터(No. 5) 진입도 방식으로 측정하였다. 전체 그래프 중 가장 높은 피크 값을 과피 경도, 이후 낮아진 피크 구간의 중간 값을 과육 경도로 간주하였다. 과피색은 chromameter(CR-200, Minolta Co., Ltd., Tokyo, Japan)를 L*, a*, b* 값 모드로 설정하여 과실의 적도면을 측정하였다. 유리당 함량은 과피를 제거한 과육 20g을 80% 에탄올 40mL에 넣어 마쇄한 후 3,000rpm으로 30분간 원심분리하여 얻은 상징액을 0.45µm membrane 필터로 여과시켜 HPLC(Ultimate 3000, Dionex Corp., Sunnyvale, CA, USA)로 분석하였다. 컬럼은 sugar-pak(300*6.5mm, Waters, Corp., Milford, MA, USA)이었고, 이동 속도는 0.5mL/min로 하였으며, 검출기는 굴절률검출기(Shodex RI-101, Showa Denko, Tokyo, Japan)를 이용하였다. 유리당은 자당, 과당, 포도당 및 솔비톨의 함량을 측정하였고, 그 외의 유리당은 당 조성에 극히 미량을 차지하여 그 함량을 무시하였다(Kim and Park, 2010). 경도와 유리당 함량을 분석하고 남은 과실을 거즈를 이용하여 착즙한 후 가용성 고형물 함량은 디지털 굴절당도계(PR-100, Atago Co., Ltd., Tokyo, Japan)로 측정하였고, 유기산 함량은 과즙 5mL을 0.1N NaOH로 적정하여 구연산 값으로 측정하였다.
통계 분석
통계 분석은 SPSS 프로그램(Version 19.0 SPSS Inc., Chicago, IL, USA)을 이용하여 95% 신뢰 수준(p ≤ 0.05)에서 최소 유의차 검정(LSD)을 실시하였다.
결과 및 고찰
용성인비 덧거름 시비량에 따른 신초 생장과 엽내 무기물 함량
용성인비의 덧거름 시비량에 따른 4년생 복숭아 ‘유미’의 신초 생장을 조사하였다(Fig. 2). 신초장은 5월 22일 조사할 때부터 표준시비보다 2-6배 처리구에서 감소하는 경향을 나타내었다. 특히, 6월 20일에서 7월 10일까지의 과실 성숙 단계에서는 그 차이가 더욱 컸다. 이 시기의 신초장은 표준시비구에서는 39.3-44.3cm인 반면 6배 처리구에서는 34.7-37.3cm로 12-16% 정도 억제되었다. 이러한 결과로 보아 기존 농촌진흥청 표준시비인 수체당 용성인비량 0.33kg보다 증시하면 신초 생장을 억제하는 효과가 있을 것으로 판단된다. 하지만 덧거름량을 2-6배 증시한 처리구 간에는 큰 차이가 보이지 않아 덧거름 증시에 따른 억제 정도를 예측하기는 어려웠다. 일반적으로 인산 시비량 증가에 따른 생육 저하 원인은 질소 흡수 저하(Hawkesford et al., 2012), 엽록소 성숙 및 광합성량 저하(Tagliavini et al., 1991), 철, 망간, 아연 등의 불용화에 따른 양분 불균형(Choi et al., 2009) 등인데, 본 결과는 토양에 시비된 질소의 흡수량 차이가 영향을 준 것으로 생각된다.
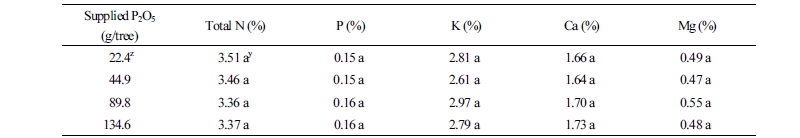
용성인비의 덧거름 시비량에 따른 수확 직후 엽내 무기물 함량을 분석한 결과(Table 2), 총 질소, 인, 칼륨, 칼슘, 마그네슘 등에서 처리 간 차이가 없었다. 식물체 내 N:P 비율은 식물의 양분이용효율에 영향을 주며(Close and Beadle, 2004), N보다는 P가 영향을 더 크게 영향을 미치기 때문에(Sadras, 2005), 질소와 인산 간 길항적 관계는 엽내 무기물 함량보다 신초 생장(Fig. 2)의 결과로 나타난 것으로 판단된다.
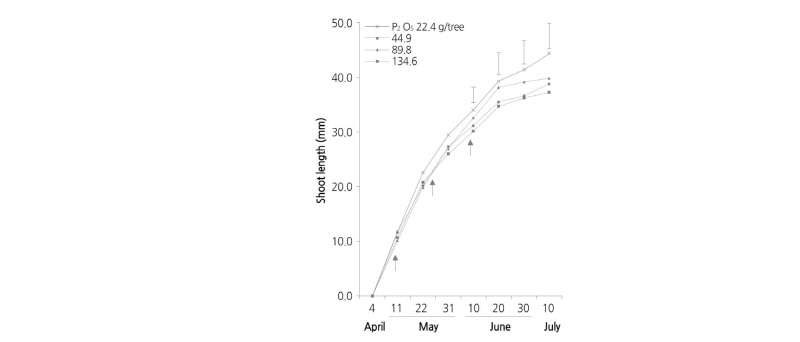
Fig. 2. Effects of the amount of P2O5 supplied via side dressing of fused phosphate fertilizer (FPF) on shoot growth in ‘Yumi’ peach. The arrows indicate the dates of side dressing application: May 10, May 25, and June 9. Vertical bars represent Fisher’s least significant difference (LSD) value (n=4).
과실 수확 직후 토양 내 무기물 함량을 조사하였다(Table 3). 총 질소, 칼륨, 칼슘 함량은 처리구 간 차이를 나타내지 않았지만, 유효 인산과 마그네슘 함량은 유의한 차이를 나타내었다. 용성인비 덧거름 6배 처리구에서는 표준시비구에서보다 3.0배의 유효인산 함량과 1.8배의 마그네슘 함량을 나타내었다. 용성인비에는 마그네슘이 14% 함유하고 있는데 처리구 간 마그네슘 함량 차이를 고려하면 인산이 마그네슘의 흡수를 다소 촉진시킨 것으로 생각된다. 토양분석의 결과에서 유효인산 함량과 투여된 처리별 함량을 고려하면 엽내 인산 함량 결과와 일치하지 않았다. 따라서 신초 생장(Fig. 2)을 엽내 함량 결과로 설명하기에는 부족하였다. Scowcroft and Silva(2005)도 목본성인 Acacia koa를 대상으로 3년간 인산 시비에 따른 생장 효과를 분석하였을 때 생장에 대한 인의 기여는 인정되나 이를 엽내 함량 분석으로는 설명되지 않는다고 하였다. 결국 토양 내 물리화학적 특성에 따른 흡수 차이(Georage et al., 2005; Jakobsen, 2008)를 고려하였을 때, 본 포장은 1:1형 광물인 마사토로 구성되었고 근권부가 밀폐 처리되어 토양 완충력이 낮은 상태로 기존 광물에 풍부한 변두리 전하(Fe-OH, Al-OH)에 의한 시비량에 따른 인산의 흡착(Kim, 2006) 정도가 불규칙하게 일어났을 가능성을 배제할 수 없었다.
용성인비 덧거름 시비량에 따른 신초엽의 SPAD 값 변화
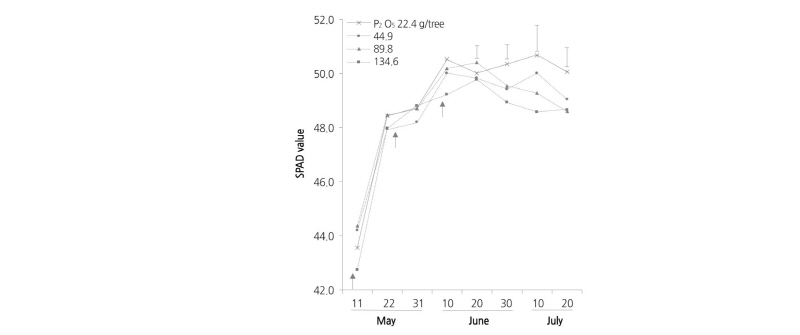
용성인비 덧거름 시비량에 따른 신초엽의 SPAD 값 변화를 조사하였다(Fig. 3). 신초엽의 SPAD 값은 5월 10일 조사까지 뚜렷한 차이를 나타내지 않았으나 이후 2-6배 처리구에서 유의하게 감소하였다. 이러한 결과는 용성인비 덧거름 시비량이 많을수록 흡수된 마그네슘 함량이 많았지만(Table 3), 질소의 흡수가 감소함(Table 2)에 따라 엽록소 생성이 저하된 것으로 생각된다. 질소 흡수량과 엽록소 함량 간에는 정의 상관성을 갖고 있어(Prsa et al., 2007) 고온 시 고농도의 인산 시비는 질소 흡수 저해를 가져와 엽록소의 성숙을 저하시켜 SPAD 값이 감소한 것으로 생각된다(Tagliavini et al., 1991).
Table 3. Fertilizer components in soil at the end of this study (in 2017) 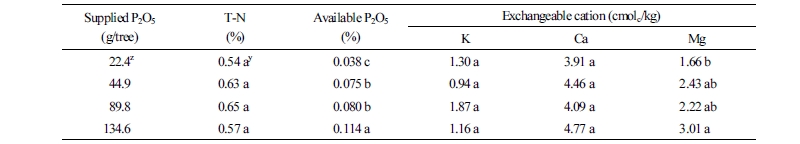 | |
zRefer to Table 2. yMean separation within columns by LSD test at p ≤ 0.05. | |
용성인비 덧거름 시비량에 따른 과실 비대 및 품질 특성
용성인비 덧거름 시비량에 따른 4년생 복숭아 ‘유미’의 과실 종경 및 횡경 변화를 조사하였다(Fig. 4). 조생종인 ‘유미’의 과실 종경과 횡경 비대는 경핵기가 짧아 이중 S자 생장 곡선을 보이지 않았다(Cho et al., 2000; Sandhu et al., 1983). 과실 종경과 횡경은 용성인비 시비량이 많은 처리구일수록 긴 경향이었다. 처리구 간 차이는 6월 2일 조사에서 뚜렷하게 나타낸 이후 그 차이는 증가하지 않아 인산 시비량이 많은 처리구에서 세포 분열은 더 잘 되었으나 이후 세포 비대에서는 크게 영향을 미치지 않은 것으로 생각된다. 첫 번째 용성인비 시비에 의해 ATP 생성량 및 세포 분열 차이를 발생시켰고, 2회 및 3회에는 시비량 누적에 따라 고농도 처리에서 세포 비대를 저하시키는 요인으로 작용한 것으로 판단되었다(Estime et al., 2003). 결국 최종 과실 크기 차이는 5월 26일 또는 6월 2일 전의 시비량 차이에서 유발된 것으로 판단되었다. 또한 2-3차 시비 시기는 2017년 고온 현상이 많았던 시기였는데(자료 미제시), 고농도 인산 시비에 따른 질소 흡수 저하(Table 2) 및 엽록소 성숙 저하(Tagliavini et al., 1991; Fig. 3)로 인한 동화산물 생성량 및 과실로의 전류량 저하가 세포 비대 저하의 원인으로 판단된다.
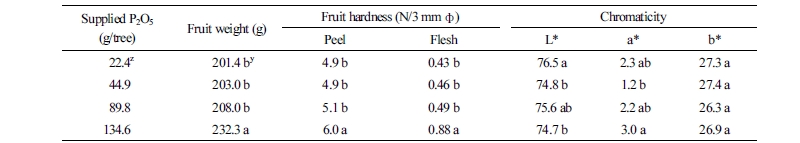
복숭아 ‘유미’ 성숙과의 과중, 과피 및 과육 경도는 시비량이 많은 처리구일수록 높은 경향을 나타내었다(Table 4). 특히, 6배 처리구에서는 표준시비구에서보다 과중이 15% 증가하였다. 과육 경도는 6배 처리구에서 2배 이상 증가하였다. 과피색은 뚜렷한 경향을 볼 수 없었다.
성숙과의 유리당, 가용성 고형물 함량 및 적정 산도를 비교하였다(Table 5). 복숭아 ‘유미’는 총 유리당 중 자당 비율이 81-82%였고, 포도당, 과당, 솔비톨 순이었다. 총 유리당에서 표준 시비구의 솔비톨 함량이 2.4%였지만 2-6배 처리구에서 1.6%로 낮았다. 가용성 고형물 함량은 처리 간 차이가 없었지만 적정 산도는 표준 시비구에 비해 2-6배 처리구에서 높은 경향이었다. 일반적으로 질소 시비는 과색, 과육 경도 및 가용성 고형물 함량과 부의 상관성이 있고(Nava et al., 2008), 과실의 성숙 단계에서는 당도가 증가하고 신맛 및 경도가 감소하며(Kim et al., 1999; Raese, 1987), 수확 시기에 따른 품종 간 생장단계에 따른 당 조성 비율이 다소 차이를 나타내기도 한다(Sandhu et al., 1983). 본 연구에서는 엽내 질소 함량(Table 2)과 성숙과 특성(Tables 4 and 5) 간에 다소 상이한 결과를 나타내었다. 특히, 유리당 함량이 증가하는 경향임에도 유기산 함량은 증가하여 당산비가 감소하는 경향을 나타내었는데, 이는 광합성 능력과 관계된 잎의 SPAD값과 엽내 질소 함량 및 기온이 높았던 시험 기간 등을 고려할 때, 용성인비 덧거름 시비량이 많은 처리구에서 광합성량에 비해 호흡에 인한 당 분해 및 유기산 합성량이 많았기 때문으로 판단된다.
용성인비 덧거름 6배 처리구에서 엽내 낮은 질소 함량(Table 2), 신초 생장 억제(Fig. 2), 중․후반부 엽록소 함량 저하(Fig. 3), 그리고 과실 특성(Fig. 4, Tables 4 and 5) 등을 전반적으로 고려할 때 용성인비 덧거름 시비량의 증가는 과실 숙기를 촉진시킨 것으로 생각된다. 숙기 촉진을 일으킨 주요 요인으로는 인산의 충분한 공급으로 생식 기관의 완성 시기, 그리고 과실의 세포분열 시기 및 정도가 촉진됨으로써 이후 과실로의 동화산물 전류 및 축적 시기도 빨라졌기 때문으로 판단된다. 하지만 본 연구 결과에서 인산 시비량에 따라 잎과 토양 내 인산 함량이나 다른 무기성분 함량에서 뚜렷한 차이가 나타나지 않아 향후 복합적 요인을 고려한 심도 있는 연구가 추가적으로 필요할 것으로 생각된다.