서 언
재료 및 방법
과실재료 및 수확 전 처리
CO2 처리 및 저장
품질 분석
알코올불용성 고형물 제조 및 펙틴 분석
Calcium 분석
통계 분석
결과 및 고찰
서 언
우리나라에서 재배되는 주 품종인 ‘설향’ 딸기(Fragaria × ananassa Duch.)는 풍산성이고 내병성이 강하지만 과실의 경도가 낮아 완숙한 다음에 수확하면 과실에 상처가 쉽게 발생하여 저장성이 떨어진다. 과피의 물리적 손상은 과실 표피를 빠르게 변색시켜 외관 품질을 떨어뜨리므로 이를 방지하기 위한 재배적 조치가 강구되고 있다. 수확 전 칼슘 살포는 경도를 높여 과실 저장성을 높여주는 긍정적인 효과가 있다(Chung et al., 1993; Smith and Gupton, 1993). 그러나 살포한 칼슘은 세포 내 이동이 쉽지 않아 수차례의 살포에도 조직의 칼슘 농도에는 차이가 없으며 고농도로 살포할 경우 피해가 발생하기도 하여 칼슘 처리의 효과가 균일하지 못하다(Crisosto et al., 2000; Manganaris et al., 2005).
키토산은 키틴의 탈아세틸화 반응으로 얻어지는 고분자화합물로 식품첨가제, 식용필름제조, 식이섬유 생산 등 다양한 용도로 활용되고 있다(Shahidi et al., 1999). 재배작물에 대한 키토산 살포는 딸기(Bhaskara-Reddy et al., 2000), 자두(Ruoyi et al., 2004), 그리고 사과와 오렌지(EI-Ghaouth et al., 2000; Galed et al., 2004)에서 부패와 갈변을 억제하고 안토시아닌 감소를 억제시켜 외관 품질을 증진시키는 효과가 있다. 키토산은 처리농도가 높을수록 또는 반복적으로 처리할 때, 부패 억제에 효과적이고 과실의 경도를 증진시키지만 성숙을 다소 지연시킨다고 보고되었다(Bhaskara-Reddy et al., 2000). 키토산 살포에서 기능성 물질을 첨가하여 식품기능성을 향상시킬 수 있는 가능성(Han et al., 2004)과 대체농약으로서의 가능성도 기대할 수 있지만(Tripathi and Dubey, 2004) 식물 표면에 쉽게 부착되지 않는 문제점이 있어 키토산 처리 효과가 균일하지 않다.
수확 후 고농도 CO2 처리는 딸기 과실의 부패, 호흡 그리고 에틸렌 생성을 억제시키고(Ke et al., 1991) 경도를 높이거나 경도 저하를 완화시킨다(Smith and Skog, 1992; Watkins et al., 1999). CO2 처리는 100%의 높은 농도로 단시간 처리할 때에도 유사한 효과를 보이는데(Goto et al., 1996; Ueda and Bai, 1993) 처리 효과는 품종(Matsumoto et al., 2010; Smith and Skog, 1992; Watkins et al., 1999), CO2 농도(Goto et al., 1995; Harker et al., 2000), 과실의 성숙상태(Goto et al., 1995), 그리고 처리 온도와 시간(Zhang and Watkins, 2005)에 따라 차이가 있다. CO2 처리에 의한 딸기의 경도 증가는 펙틴의 질적 변화와 관련이 있어 수용성 펙틴이 감소한다(Goto et al., 1996; Matsumoto et al., 2010). 또한 과실 경도는 조직의 칼슘 절대량보다 세포벽과 결합할 수 있는 칼슘 함량이 중요할 것으로 예상되어 세포벽으로 칼슘의 이행을 촉진할 수 있는 방안을 마련할 필요가 있다.
본 연구에서는 우리나라에서 가장 많이 재배되지만 육질이 약한 ‘설향’ 딸기에 대하여 수확 전후 칼슘-키토산 및 고농도 CO2 단기처리를 통하여 모의유통 중 저장력을 증진시킬 수 있는 방안을 모색하고자 하였다.
재료 및 방법
과실재료 및 수확 전 처리
충남 논산시 상월면 소재의 하우스 재배 딸기 농가를 선택하여 실험을 실시하였다. 수확 전 처리로 칼슘-키토산을 살포하였는데 키토산은 0.5% 초산에 용해시킨 1% 키토산(Kumhochem, Korea)과 탈이온수에 용해시킨 2% 염화칼슘액을 각각 동량으로 고르게 혼합한 다음 이를 250배액으로 희석하여 살포하였다. 준비된 칼슘-키토산액은 전착제를 혼용하여 수관전체에 살포하였는데 1주간격으로 3회 엽면 살포한 후, 2013년 3월 12일에 1차로 과실을 수확하였고, 그 후에는 4월 17일(4회 살포) 그리고 5월 2일(5회 살포)에 각각 수확하였다. 대조구는 무처리 하우스 1동을 선택하여 비교하였다. 약 80% 착색된 상태의 과실을 수확하여 실험실로 즉시 수송한 다음 외형을 살펴 크기가 균일하고 상처가 없는 과실을 선별하여 실험에 이용하였다.
CO2 처리 및 저장
가스처리는 저온챔버(60 × 64 × 121cm)를 이용하여 챔버 내부의 공기가 모두 치환될 수 있도록 처음 20분간은 25L・min-1의 유량으로 가스(공기 혹은 CO2)를 공급하였고 그 다음에는 5L・min-1의 유속으로 12시간 동안 처리하였다. 가스는 bubbler를 통과시키므로 챔버 내부 습도를 95% 이상으로 유지하였다. 가스 처리를 마친 과실은 PVC 상자(500g 용기)에 담아 랩핑하고 4°C에서 4일간 저장하였다. 저장을 마친 과실은 다시 2일간 상온에 노출시켜 모의 유통과정을 경과시켰다.
품질 분석
과피색은 Chroma meter(CR-400, Minolta, Japan)를 이용하여 적도면에서 측정하여 L*, a*, b*를 구하고 hue 값을 계산하였다. 경도는 texture analyzer(TMS-Pro, FMC, USA)를 이용하여 조사하였는데 측정 조건으로는 ∅3mm flat probe를 장착하고 이동속도 50mm・min-1와 침투 깊이 5mm로 설정하여 얻어진 최대하중을 Newton으로 표시하였다. 경도는 처리당 20과를 무작위로 선별하여 측정하였다.
네 겹의 거즈를 이용하여 착즙한 과즙으로 가용성고형물과 산 함량을 조사하였는데 가용성고형물 함량은 굴절당도계(ATAGO, Japan)를 이용하였고 산 함량은 과즙 5mL에 탈이온수 35mL를 가한 후 0.1N NaOH로 적정하고 구연산으로 환산하였으며 처리당 3반복(10과/반복)으로 조사하였다.
무름 장해는 모든 과실을 건전과는 0, 과육 면적의 25% 미만의 장해는 1, 50% 미만은 2, 50% 이상은 3로 구분하여 장해 지수를 구한 다음 합산하고, 총 조사대상 과실수로 나누어 지표로 산출하였다. 부패율은 처리당 부패가 발생한 과실의 수를 백분율로 나타내었다. 본 실험은 반복없이 처리당 3 상자(500g/상자)의 과실을 전수 조사하였다.
알코올불용성 고형물 제조 및 펙틴 분석
과육 25g에 95% EtOH을 최종 농도가 80%가 되도록 가하고 유화기(Ultra-Turrax T25, IKA-Labortechnik, Staufen, Germany)를 이용하여 1분 동안 최대 속도로 마쇄하였다. 마쇄물은 끓는 수조 상에서 20분 동안 refluxing하고 상온으로 식혀주었으며 miracloth(CalbioChem, Lajolla, CA, USA)를 이용하여 200mL 80% ethanol, 50mL 100% ethanol 그리고 50mL 100% acetone을 순차적으로 가하여 용해성분을 제거하고 잔사는 모아 상온에서 휘발성 성분이 제거된 다음 60°C에서 건조시켜 알코올불용성물질(ethanol insoluble solids, EIS)로 삼았다.
펙틴 추출은 Cheng and Huber(1996)의 방법을 약간 수정하여 실시하였다. 즉, EIS 20mg에 25mL의 탈이온수를 가하여 12시간 동안 상온에서 shaker를 이용하여 추출하고 원심분리(15,000rpm, 10분)한 다음 상징액을 모아 수용성펙틴(water soluble pectin, WSP)으로 삼았다. 순차적으로 잔사에 50mM Na-acetate buffer(pH 6.5)에 용해시킨 50mM ethylene-diaminetetraacetic acid 25mL를 가하여 전술한 방법으로 추출하여 chelator 용해성 펙틴(chelator soluble pectin, CSP)으로 간주하였고 계속하여 50mM Na2CO3(20mM NaBH4 함유) 25mL으로 추출하여 sodium carbonate 용해성 펙틴(sodium carbonate soluble pectin, SSP)으로 간주하였다. 펙틴 분석은 Blumenkrantz and Asboe-Hansen(1973)의 방법을 이용하였고 표준 당으로 무수 galacturonic acid(Sigma, USA)를 이용하였다.
Calcium 분석
세포벽 결합형 칼슘은 EIS에 잔류하는 칼슘을 분석하여 결합형 칼슘으로 간주하였다. 즉, EIS 10mg을 회화로(Dongyang Science CO., Korea)를 이용하여 600°C에서 6시간 동안 회화시킨 다음 잔사에 0.1N HCl 10mL를 가하여 용해시킨 후 원자흡광분석계(AA-7000, Shimadzu, Japan)를 이용하여 칼슘을 측정하였다.
통계 분석
모든 실험은 특정하지 않는 한 3반복으로 수행하였으며 통계 분석은 SPSS Software package(version 20.0) 프로그램을 이용하여 Tukey’s Multiple range test를 수행하였다.
결과 및 고찰
Table 1. Effect of pre- and post-harvest treatments of Ca-chitosan and/or 100% CO2 on the firmness of ‘Seolhyang’ strawberry fruit during storage and after exposure to ambient temperature. |
Storage (days) | Treatmentz | | Firmness (N) |
Preharvest | Postharvest | April 17 | May 2 |
0 | Untreated | - | | 0.36 | 0.32 |
Ca-chitosan | - | | 0.39 | 0.33 |
1 | Untreated | Air | | 0.40 by | 0.35 b |
Ca-chitosan | Air | | 0.42 b | 0.41 b |
Untreated | CO2 | | 0.66 a | 0.68 a |
Ca-chitosan | CO2 | | 0.76 a | 0.73 a |
4 | Untreated | Air | | 0.40 b | 0.43 c |
Ca-chitosan | Air | | 0.45 b | 0.43 c |
Untreated | CO2 | | 0.80 a | 0.65 b |
Ca-chitosan | CO2 | | 0.83 a | 0.83 a |
4 + 2x | Untreated | Air | | 0.42 c | 0.38 b |
Ca-chitosan | Air | | 0.42 c | 0.39 b |
Untreated | CO2 | | 0.62 b | 0.63 a |
Ca-chitosan | CO2 | | 0.76 a | 0.63 a |
Significant | | |
Storage (A) | ** | *** |
Treatment (B) | *** | *** |
A × B | * | * |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. yDifferent letters within same storage date indicate the significant difference at p < 0.05 by Tukey’s multiple range test. xFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. *,**,***Significant at p < 0.05 or 0.01, 0.001, respectively. |
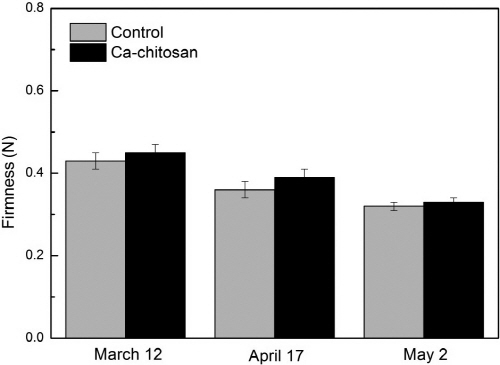
수확 전 칼슘-키토산 용액의 누적 살포에 따른 가시적 장해는 모식물체나 과실에서 전혀 관찰되지 않아 수확 전 키토산 살포는 안전하였다. 과실 경도는 수확시기가 늦을수록 수확 전 처리에 관계없이 감소하여 대조구의 딸기는 5월 수확한 과실의 경도가 3월 수확한 과실 경도의 74% 수준이었고 칼슘-키토산 처리구의 딸기도 73% 수준이었다. 3월과 4월에 수확한 과실에서는 비록 통계적 유의차는 없으나 수확 전 칼슘-키토산을 처리한 과실의 경도가 다소 높았다(Table 1 and Fig. 1). 생육후기인 5월은 기온이 높아 과실 생장 속도가 빨라 개화 후 성숙까지 소요되는 기간이 크게 단축되므로 조직이 단단하게 자라지 못하여 경도가 낮아진 것으로 생각된다. 고온기에 수확한 과실에서는 수확 전 칼슘-키토산 살포의 효과도 뚜렷하지 않았는데 처리한 칼슘과 키토산 모두 40mg・L-1로 농도가 낮았기 때문으로 추정된다.
과실의 연화가 빠르게 진행되는 4월 이후의 과실에 대한 수확 전후 처리효과를 검토하기 위하여 칼슘-키토산 4회 살포한 4월 17일 그리고 5회 살포한 5월 2일 각각 수확한 과실을 대상으로 고농도 CO2 단기처리에 따른 경도 변화를 조사하였다(Table 1). CO2 처리는 수확 전 처리에 관계없이 경도를 유의하게 증가시켰다. 4월 수확한 과실의 수확 당일 대조구와 Ca-chitosan 처리구의 경도는 각각 0.36N과 0.39N이었는데 수확 1일 후 대기 처리구의 과실 경도는 수확 전 처리에 관계없이 0.4-0.42N으로 다소 증가하는데 그쳤다. 반면에 CO2 처리구 과실의 경도는 0.66-0.76N으로 수확 전 처리를 실시하지 않은 과실의 경도 증가율은 83.3%, 그리고 수확 전 처리를 병행한 경우 102.6%으로 차이를 보여주었다. 4일간의 저온저장 중 과실 경도는 수확 전 처리에 관계없이 CO2 처리에서 통계적으로 유의하게 높은 수준으로 유지되었고 상온 노출 2일 후에는 수확 전후 처리를 병행한 과실의 경도가 가장 높았고 다음이 CO2 처리만 실시한 과실이었으며 CO2 처리를 실시하지 않은 경우에는 경도 변화가 없었다. 상온노출 후 대조구 과실의 경도도 크게 감소하지 않았는데 본 연구에서 모든 과실을 랩핑하였으므로 포장 내부에 축적된 CO2의 영향이 있었을 것으로 추정된다(Vicente et al., 2003). 5월에 수확한 과실도 유사하였으나 CO2 처리만 실시한 과실의 경도가 병행 처리한 과실보다 경도의 감소가 빠르게 진행되었으나 상온노출 2일 후에는 처리간 차이가 없었다. CO2 처리 과실의 경도가 4일 저온저장과 2일간 상온 노출 후에도 수확 당일보다 높아 ‘설향’ 품종에서 CO2 처리의 잔류 효과는 최소 6일 이상 지속되는 것으로 판단된다. 따라서 수확 전 칼슘-키토산 처리가 경도에 미치는 영향은 제한적이었지만 CO2 처리와 병행할 때 상승적인 효과가 관찰되었다.
|
Fig. 1. Effect of preharvest Ca-chitosan spray on ‘Seolhyang’ strawberry fruit firmness between harvest seasons. Strawberries were grown in the plastic houses. Ca-chitosan was sprayed 3 to 5 times among harvest dates. Data were the average of 20 fruit ± SD. |
Table 2. Effect of pre- and post-harvest treatments of Ca-chitosan and/or 100 kPa CO2 on pectin composition of ‘Seolhyang’ strawberry fruit during storage and after exposure to ambient temperature. |
Storage (days) | Treatmentz | | Acid Sugar (μg GA・20 mg-1 EIS) |
Preharvest | Postharvest | WSP | CSP | SSP |
0 | Untreated | - | | 110.68 | 55.14 | 100.00 |
| Ca-chitosan | - | | 136.29 | 61.90 | 102.49 |
1 | Untreated | Air | | 124.64 ay | 55.28 b | 97.25 a |
| Ca-chitosan | Air | | 131.73 a | 54.96 b | 86.84 a |
| Untreated | CO2 | | 78.66 b | 94.78 a | 91.12 a |
| Ca-chitosan | CO2 | | 76.14 b | 113.72 a | 102.79 a |
4 | Untreated | Air | | 127.51 a | 64.98 c | 94.19 a |
| Ca-chitosan | Air | | 116.46 b | 56.28 c | 108.98 a |
| Untreated | CO2 | | 100.89 b | 93.61 b | 92.90 a |
| Ca-chitosan | CO2 | | 45.45 c | 116.12 a | 99.97 a |
4 + 2x | Untreated | Air | | 91.08 ab | 54.42 b | 86.91 a |
| Ca-chitosan | Air | | 114.48 a | 57.51 b | 93.06 a |
| Untreated | CO2 | | 55.45 b | 109.59 a | 98.51 a |
| Ca-chitosan | CO2 | | 57.15 b | 110.48 a | 98.31 a |
Significant | | | | |
Storage (A) | | *** | NS | NS |
Treatment (B) | | *** | *** | * |
A × B | | *** | NS | * |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. yDifferent letters within same storage date indicate the significant difference at p < 0.05 by Tukey’s multiple range test. xFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. ns,*,***Nonsignificant or significant at p < 0.05, 0.001. |
Table 3. Effect of pre- and post-harvest treatments of Ca-chitosan and/or 100% CO2 on bound calcium of ‘Seolhyang’ strawberry fruit during storage and after exposure to ambient temperature. |
Storage (days) | Treatmentz | Bound Calcium (μg・mg-1 EIS) |
Preharvest | Postharvest |
0 | Untreated | - | 8.37 |
Ca-chitosan | - | 6.95 |
1 | Untreated | Air | 12.91 by |
Ca-chitosan | Air | 13.44 b |
Untreated | CO2 | 12.79 b |
Ca-chitosan | CO2 | 16.29 a |
4 | Untreated | Air | 11.83 b |
Ca-chitosan | Air | 14.07 b |
Untreated | CO2 | 12.87 b |
Ca-chitosan | CO2 | 17.44 a |
4 + 2x | Untreated | Air | 11.47 b |
Ca-chitosan | Air | 12.79 ab |
Untreated | CO2 | 17.72 a |
Ca-chitosan | CO2 | 15.47 ab |
Significant | |
Storage (A) | NS |
Treatment (B) | *** |
A × B | ** |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. yDifferent letters within same storage date indicate the significant difference at p < 0.05 by Tukey’s multiple range test. xFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. ns,**,***Nonsignificant or significant at p < 0.01, 0.001, respectively. |
수확 전후 처리가 과육의 펙틴 변화에 미치는 영향을 조사한 결과(Table 2), WSP의 변화가 현저하였는데 수확 전 칼슘-키토산 처리는 펙틴 변화에 뚜렷한 영향을 주지 않았지만 수확 후 CO2 처리는 수확 전 처리에 관계없이 WSP를 현저히 감소시켰고 수확 전후 병행처리에서 그 차이가 더욱 뚜렷하였다. 또한 CSP은 WSP와 달리 CO2 처리에 의하여 증가하였는데 병행처리에 의한 상승 효과는 뚜렷하지 않았다. SSP는 처리 간 차이가 확인되지 않아 기존의 연구(Hwang et al., 2012)와 마찬가지로 CO2 처리는 WSP를 CSP로 전환시켜 calcium pectate를 촉진하여 경도를 높이는 것으로 확인되었다. EIS 결합형 칼슘 함량은 조사 시기와 처리에 따라 경향이 일정하지 않았지만 수확 전 칼슘-키토산 처리만으로는 EIS 결합형 칼슘 농도를 증가시키지 못하였으나 CO2와 병행 처리하였을 때에는 결합형 칼슘 함량을 현저히 높여주었다(Table 3). 본 연구에서 처리한 칼슘-키토산 용액의 염화칼슘 및 키토산 농도는 각각 40mg・L-1에 불과하여 칼슘-키토산 처리로 과실로 이행한 칼슘의 양은 적었을지라도 CO2 처리는 결합형 칼슘 농도를 증가시키는 것으로 판단된다. 수용성 펙틴과 경도 변화를 함께 고려할 때, 수확 전 칼슘-키토산 처리가 과실의 칼슘 함량을 크게 높이지는 못했을지라도 수확 후 CO2 처리가 칼슘의 펙틴과의 결합을 촉진시켜주어 펙틴의 질적 변화를 초래한 것으로 생각된다. 따라서 수확 전 칼슘-키토산 처리와 수확 후 CO2 병행처리는 펙틴 변화를 통하여 과실 경도를 증진시켜 주는 것으로 이해되었다.
모의 유통 과정에서의 처리 간 과실의 색을 비교하였을 때 4월 17일 수확한 과실의 경우 L* 값은 CO2 처리보다 수확 전 칼슘-키토산 처리의 영향을 더욱 받는 것으로 보이는데 수확 후 처리에 관계없이 칼슘-키토산 살포처리에서 높은 경향이었다(Table 4). 또한 hue 값은 칼슘-키토산 처리구에서 높아 과피색의 변화가 지연된 것으로 판단되었다. 이러한 결과는 키토산이 과실 표면을 코팅하여 저장기간 동안 과피 색의 변화를 감소시킨 것으로 판단된다. 그러나 상온 노출 2일 후에는 처리 간 차이가 관찰되지 않았고 5월 2일 고온기에 수확한 과실에서는 더욱 차이가 명확하지 않았다.
4월 17일 수확한 대조구 과실의 가용성고형물 함량은 9.88°Brix이었으며 칼슘-키토산 처리구는 9.15°Brix로 칼슘-키토산 처리구의 딸기가 무처구의 딸기에 비하여 다소 낮았다(Table 5). 저장 후에도 칼슘-키토산 처리에서 다소 낮은 경향이었다. 반면에 5월 2일 수확 과실의 수확 당일의 가용성고형물 함량은 칼슘-키토산 처리구에서 8.65°Brix이었고 대조구 과실은 8.47°Brix로 처리구 과실의 가용성고형물 함량이 다소 높았으나 저장 기간에는 칼슘-키토산 처리구에서 전반적으로 낮았다. 따라서 CO2 처리는 가용성고형물 수준에 영향을 미치지 않은 것으로 평가되지만 칼슘-키토산 처리는 낮추는 결과였다.
Table 4. Effect of pre- and post-harvest treatments of Ca-chitosan and/or 100% CO2 on skin color of ‘Seolhyang’ strawberry fruit during storage and after exposure to ambient temperature. |
Storage (days) | Treatmentz | | April 17 | | May 2 |
Preharvest | Postharvest | L* | hue | L* | hue |
0 | Untreated | - | | 39.91 | 34.97 | | 43.22 | 35.78 |
Ca-chitosan | - | | 40.02 | 36.99 | | 38.79 | 32.30 |
1 | Untreated | Air | | 37.96 bcy | 32.76 b | | 43.38 ab | 37.85 ab |
Ca-chitosan | Air | | 40.55 b | 35.78 ab | | 40.07 c | 35.78 b |
Untreated | CO2 | | 37.33 bc | 32.63 b | | 44.00 a | 39.17 a |
Ca-chitosan | CO2 | | 42.90 a | 37.38 a | | 41.22 bc | 37.62 ab |
4 | Untreated | Air | | 37.24 c | 31.09 b | | 44.23 a | 39.59 a |
Ca-chitosan | Air | | 40.44 ab | 36.23 a | | 40.87 b | 36.52 b |
Untreated | CO2 | | 37.76 bc | 32.30 b | | 44.51 a | 37.90 ab |
Ca-chitosan | CO2 | | 41.00 a | 36.08 a | | 40.94 b | 35.95 b |
4 + 2x | Untreated | Air | | 38.64 a | 33.03 a | | 41.86 a | 37.63 a |
Ca-chitosan | Air | | 39.24 a | 34.35 a | | 37.56 b | 32.24 c |
Untreated | CO2 | | 39.35 a | 33.06 a | | 42.06 a | 37.07 bc |
Ca-chitosan | CO2 | | 39.49 a | 34.26 a | | 39.18 b | 34.94 b |
Significant | | | | | |
Storage (A) | NS | NS | | *** | *** |
Treatment (B) | *** | *** | | *** | *** |
A × B | ** | NS | | NS | NS |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. yDifferent letters within same storage date indicate the significant difference at p < 0.05 by Tukey’s multiple range test. xFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. ns,**,***Nonsignificant or significant at p < 0.01, 0.001, respectively. |
가용성고형물과 달리 산 함량은 수확시기 및 처리 간 차이가 뚜렷하지 않았고 특히 저장 후 상온에 노출시킨 다음에는 수확 전후 처리 간 차이가 없었다(Table 5).
과피 장해는 전반적으로 CO2 처리보다 칼슘-키토산 살포의 영향을 더욱 크게 받는 것으로 나타났지만 수확 시기가 늦을수록 수확 전 처리의 효과는 감소하였지만 상온노출 후에는 수확 전 칼슘-키토산 처리 과실의 장해발생 정도가 적었으며 수확시기에 따른 경향도 유사하였다(Table 6).
저온저장 중에는 두 수확일자 모두에서 부패한 과실이 관찰되지 않았지만(Table 6) 상온 노출 후에는 4월 17일 수확한 과실의 공기 처리와 CO2 처리에서 각각 13.3%와 6.7%로 칼슘-키토산을 살포하지 않는 경우에만 부패가 관찰되었다. 키토산은 천연 항균 물질로서 과실 표면에 보호막을 형성하여 부패균의 감염과 생장을 억제시키고 증산을 억제하며(El-Ghaouth et al., 1992; Hirano and Nagao, 1989) 숙주식물의 항균력을 높이므로(Molloy et al., 2004; Sathiyabama and Balasubramanian, 1998) 수확 전 처리한 칼슘-키토산이 수확 후 발생하는 과피 장해와 부패를 낮춘 것으로 판단된다.
이상의 결과를 살펴볼 때 수확 전 칼슘-키토산 처리는 딸기 과실의 품질과 저장성 향상에 긍정적이었으며 수확 후 CO2 처리를 병행하였을 때 과실 경도가 증가시키므로 상가적 효과를 얻을 수 있었다. 이러한 처리의 효과는 수확 시기가 늦어질수록 감소하였는데 고온기에는 과실의 생장 속도가 빠르기 때문에 칼슘-키토산 살포 주기가 길 경우 과실 표면이 충분히 코팅되지 않는 것이 처리 효과를 감소시키는 원인일 가능성이 있다. 전반적으로 ‘설향’과 같이 저장성이 낮은 딸기에서 수확 전 칼슘-키토산 처리는 과피 장해 및 부패 억제를 통한 품질 향상의 대안이 될 수 있으며 수확 후 고농도 CO2 단기 처리와 병행할 경우 상승적인 효과를 얻을 수 있을 것으로 기대된다.
Table 5. Effect of pre- and post-harvest treatments of Ca-chitosan and/or 100% CO2 on soluble solids and acidity of ‘Seolhyang’ strawberry fruit during storage and after exposure to ambient temperature. |
Storage (days) | Treatmentz | | Harvest Date |
April 17 | | May 2 |
Preharvest | Postharvest | Solids (°Brix) | Acidity (%) | Solids (°Brix) | Acidity (%) |
0 | Untreated | - | | 9.88 | 0.68 | | 8.47 | 0.51 |
Ca-chitosan | - | | 9.15 | 0.69 | | 8.65 | 0.70 |
1 | Untreated | Air | | 9.10 a | 0.65 ay | | 9.13 a | 0.53 c |
Ca-chitosan | Air | | 9.03 a | 0.69 a | | 8.47 b | 0.62 b |
Untreated | CO2 | | 9.67 a | 0.64 a | | 9.08 a | 0.52 c |
Ca-chitosan | CO2 | | 9.00 a | 0.67 a | | 8.20 b | 0.70 a |
4 | Untreated | Air | | 9.58 a | 0.65 ab | | 9.08 a | 0.54 a |
Ca-chitosan | Air | | 9.13 a | 0.72 a | | 8.03 b | 0.65 a |
Untreated | CO2 | | 9.44 a | 0.57 b | | 8.90 a | 0.58 a |
Ca-chitosan | CO2 | | 8.40 b | 0.58 b | | 7.57 b | 0.53 a |
4+2x | Untreated | Air | | 9.85 a | 0.78 a | | 9.85 a | 0.78 a |
Ca-chitosan | Air | | 8.88 bc | 0.76 a | | 8.88 bc | 0.76 a |
Untreated | CO2 | | 9.53 ab | 0.78 a | | 9.53 ab | 0.78 a |
Ca-chitosan | CO2 | | 8.48 c | 0.77 a | | 8.48 c | 0.77 a |
Significant | | | | | | |
Storage (A) | | NS | *** | | *** | *** |
Treatment (B) | | *** | ** | | *** | *** |
A × B | | * | ** | | * | *** |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. yDifferent letters within same storage date indicate the significant difference at p < 0.05 by Tukey’s multiple range test. xFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. ns,*,**,***Nonsignificant or significant at p < 0.05, 0.01, 0.001, respectively. |
|
Table 6. Effect of pre- and post-harvest treatments of chitosan and/or 100% CO2 on the quality of ‘Seolhyang’ strawberry fruit during after exposure to ambient temperature. |
Storage (days) | Treatmentz | | Harvest Date |
April 17 | | May 2 |
Preharvest | Postharvest | Skin injuryy | Decay (%) | Skin injury | Decay (%) |
4 | Untreated | Air | | 0.65x | - | | 0.70 | - |
Ca-chitosan | Air | | 0.30 | - | | 0.45 | - |
Untreated | CO2 | | 0.50 | - | | 0.45 | - |
Ca-chitosan | CO2 | | 0.30 | - | | 0.40 | - |
4 + 2w | Untreated | Air | | 1.17 | 13.3 | | 1.77 | 30.8 |
Ca-chitosan | Air | | 0.37 | - | | 0.87 | 14.8 |
Untreated | CO2 | | 1.00 | 6.7 | | 1.46 | 11.1 |
Ca-chitosan | CO2 | | 0.53 | - | | 0.73 | 3.7 |
zFruit were sprayed with calcium-chitosan 4 to 6 times prior to harvest as preharvest treatment and exposed to 100% CO2 or air for 12 h as postharvest treatment. ySkin injury was determined in the range 0 (sound) to 3 (severe). xData were collected from pooled sample of 3 styrofoam trays without replication. wFruit were exposed to ambient temperature for 2 days after 4 day storage at 4°C. |
Acknowledgements
본 연구는 농촌진흥청 농업현장실용화기술개발사업 지원(PJ0101382014)에 의해 수행되었음.
References
Bhaskara Reddy, M.V., K. Belkacemi, R. Corcuff, F. Castaigne, and J. Arul. 2000. Effect of pre-harvest chitosan sprays in post-harvest infection by Botrytis cinerea and quality of strawberry fruit. Postharvest Biol. Technol. 20:39-51.
Blumenkrantz, N. and G. Asboe-Hansen,. 1973. New method for quantitative determination of uronic acids. Anal. Biochem. 54:484-489.
Cheng, G.W. and D.J. Huber. 1996. Alterations in structural polysaccharides during liquefaction of tomato locule tissue. Plant Physiol. 111:447-457.
Chung, H.D., K.Y. Kang, S.J. Yun, and B.Y. Kim. 1993. Effect of foliar application of calcium chloride on shelf-life and quality of strawberry fruits. J. Kor. Soc. Hort. Sci. 34:7-15.
Crisosto, C.H., K.R. Day, R.S. Jonson, and D. Garner. 2000. Influence of in-season foliar calcium sprays on fruit quality and surface discoloration incidence of peaches and nectarines. J. Amer. Pomol. Soc. 54:118-122.
El-Ghaouth, A., J. Arul, A. Asselin, N. Benhamou. 1992. Antifugal activity of chitosan on post-harvest pathogens: Induction of morphological and cytological alterations in Rhizopus stolonifer. Mycol. Res. 96.9:769-779.
El-Ghaouth, A., J.L. Smilanick, and C.L. Wilson. 2000. Enhancement of the performance of Candida saitoana by the addition of glycolchitosan for the control of postharvest decay of apple and citrus fruit. Postharvest Biol. Technol. 19:103-110.
Galed, G., M.E. Fernández-Valle, A. Martínez, and A. Heras. 2004. Application of MRI to monitor the process of ripening and decay in citrus treated with chitosan solutions. Magnetic Resonance Imaging 22:127-137.
Goto, T., M. Goto, K. Chachin, and T. Iwata. 1995. Effect of high carbon dioxide with short-term treatment on quality of strawberry fruits. J. Japan. Soc. Food Sci. Technol. 42:176-182. (In Japanese with English summary)
Goto, T., M. Goto, K. Chachin, and T. Iwata. 1996. The mechanism of the increase of firmness in strawberry fruit treated with 100% CO2. J. Japan. Soc. Food Sci. Technol. 43:1158-1162.
Han, C., Y. Zhao, S.W. Leonard, and M.G. Traber. 2004. Edible coatings to improve storability and enhance nutritional value of fresh and frozen strawberries (Fragaria × ananassa) and raspberries (Rubus ideaus). Postharvest Biol. Technol. 33:67-78.
Harker, F.R., H.J. Elgar, C.B. Watkins, P.J. Jackson, and I.C. Hallett. 2000. Physical and mechanical changes in strawberry fruit after high carbon dioxide treatments. Postharvest Biol. Technol. 19:139-146.
Hirano, S. and N. Nagao. 1989. Effects of chitosan, pectic acid, lysozyme, and chitinase on the growth of several phytopathogens. Agr. Biol. Chem. 53:3065-3066.
Hwang, Y.S., J.H. Min, D.Y. Kim, J.G. Kim, and D.J. Huber. 2012. Potential mechanisms associated with strawberry fruit firmness increases mediated by elevated pCO2. Hort. Environ. Biotechnol. 53:52-59.
Ke, D., L. Goldstein, M. Omahony, and A.A. Kader. 1991. Effect of short-term exposure to low O2 and high CO2 atmosphere on quality attributes of strawberries. J. Food Sci. 56:50-54.
Manganaris, G.A., M. Vasilakakis, I. Mignani, G. Diamantidis, and K. Tzavella-Klornari. 2005. The effect of preharvest calcium sprays on quality attributes, physicochemical aspects of cell wall components and susceptibility to brown rot of peach fruits (Prunus persica L. cv. Andross). Sci. Hortic. 107:43-50.
Matsumoto, K., Y.S. Hwang, C.H. Lee, and D.J. Huber. 2010. Changes of firmness and pectic polysaccharide solubility in three cultivars of strawberry fruit following short-term exposure to high pCO2. J. Food Quality. 33:312-328.
Molloy, C., L.H. Cheah, and J.P. Koolaard. 2004. Induced resistance against Sclerotinia slerotiorum in carrots treats with enzymatically hydrolyzed chitosan. Postharvest Biol. Technol. 33:61-65.
Ruoyi, K., Y. Zhifang, and L. Zhaoxin. 2004. Effect of coating and intermittent warming on enzymes, soluble pectin substances and ascorbic acid of Prunus persica (Cv. Zhonghuashoutao) during refrigerated storage. Food Res. Intl. 38:331-336.
Sathiyabama, M. and R. Balasubramanian. 1998. Chitosan induces resistance components in Arachis hypogaea against leaf rust caused by Puccinia arachidis Speg. Crop Protection. 17:307-313.
Shahidi, F., J.K. Kamil Arachchi, and Y. Jeon. 1999. Food applications of chitin and chitosan (Review). Trends Food Sci. Technol. 10:37-51.
Smith, B.J. and C.L. Gupton. 1993. Calcium applications before harvest affect the severity of anthracnose fruit rot of greenhouse- grown strawberries. Acta Hort. 348:477-482.
Smith, R.B. and L.J. Skog. 1992. Postharvest carbon dioxide treatment enhances firmness of several cultivars of strawberry. HortScience 27:420-421.
Tripathi, P. and N.K. Dubey. 2004. Exploitation of natural products as an alternative strategy to control postharvest fungal rotting of fruit and vegetables (Review). Postharvest Biol. Technol. 32:235-245.
Ueda, Y. and J.H. Bai. 1993. Effect of short term exposure of elevated CO2 on flesh firmness and ester production of strawberry. J. Japan. Soc. Hort. Sci. 62:457-464.
Vincente, A.R., G.A. Martinez, A.R. Chaves, and P.M. Civello. 2003. Influence of self-produced CO2 on postharvest life of heat-treated strawberries. Postharvest Biol. Technol. 27:265-275.
Watkins, C.B., J.E. Manzano-Mendez, J.F. Nock, J. Zhang, and K.E. Maloney. 1999. Cultivar variation in response of strawberry fruit to high carbon dioxide treatments. J. Sci. Food Agric. 79:886-890.
Zhang, J.J. and C.B. Watkins. 2005. Fruit quality, fermentation products, and activities of associated enzymes during elevated CO2 treatment of strawberry fruit at high and low temperatures. J. Amer. Soc. Hortic. Sci. 130:124-130.



