서 언
재료 및 방법
식물 재료 및 온도 처리
광 흡수스펙트럼, 총 안토시아닌 함량 분석
화색 측정
High performance liquid chromatography
Real-Time PCR
통계처리
결과 및 고찰
장미 화색소 구성과 화아 발달 단계별 착색특성
고온처리에 따른 화색 발현과 안토시아닌 축적 특성
안토시아닌 생합성 관련 유전자 발현 양상
서 언
안토시아닌은 수분 매개체를 유인하거나 자외선과 같은 환경 스트레스에 대한 보호, 섭식 저해 등 다양한 기능을 가지고 있으며, 화색을 조절하는 안토시아닌의 생합성 활성은 환경적 신호와 발달에 관여하는 신호 사이의 상호작용이 요구된다(Stommel et al., 2009). 페튜니아(Petunia hybrida)에서는 지베렐린, 광, 그리고 당 신호가 화관에서 안토시아닌 합성을 유도하는 전사조절자(master transcription regulators)를 조절하기 위해서 상호작용한다(Weiss, 2000). 또한, 안토시아닌의 생합성은 액포 pH, 보색소, 금속이온, 당치환과 같은 내적 요인과 온도, 광도, 광질 등 환경적 요인에 의하여 조절된다(Kim, 1999). 특히 온도는 안토시아닌 축적에 직접적인 영향을 주는 대표적인 환경적 요인으로, 일반적으로 저온은 phenylalanine ammonia-lyase(PAL), chalcone synthase (CHS)과 같은 안토시아닌 생합성 관련 유전자들의 전사 수준을 높임으로써 안토시아닌 함량을 증가시킨다(Christie et al., 1994; Leyva et al., 1995). 안토시아닌 함량을 증가시키는 저온의 범위는 식물에 따라 다양하다. 옥수수(Zea mays L.)에서는 15°C의 저온이 가장 효과적이었고, 지속적인 저온보다 단기간의 저온처리 이후 높은 온도로 전환해주는 것이 더 효과적이었다(Christie et al., 1994). 적정 저온(17/12°C)과 고온(32/27°C)에서 재배된 페튜니아의 CHS 발현량은 화관(corolla)의 발달 초기에는 저온에 의해 증가하였지만, 이후에는 차이를 보이지 않았다(Shvarts et al., 1997). 또한, CHS 발현에 관한 온도의 효과가 안토시아닌 축적과 항상 일치하지는 않았기 때문에 번역 이후의 효과(post-translational effect)가 있을 수 있다고 제안하였다(Shvarts et al., 1997). 애기장대(Arabidopsis thaliana)에서는 광 유도유전자인 PAL과 CHS에 의해 저온이 항상 효과적이지는 않았다(Leyva et al., 1995).
고온에 관한 많은 연구는 지속적인 고온에 초점을 맞추었는데, 포도(Vitis vinifera L. × Vitis labrusca L.)에서 야간의 지속적인 고온은 UDP-glucose flavonoid-3-O-glucosyltransferase (UFGT)의 활성 감소를 통하여 안토시아닌 축적을 억제했다(Mori et al., 2005). 반면 일시적인 고온에 관한 연구는 한정적으로 수행되었다. 72시간 고온처리를 받은 절화용 장미 ‘Jaguar’에서는 안토시아닌 함량이 감소하고, 처리 시기에 따라 cyanin과 pelargonin의 비율이 변화하였다(Dela et al., 2003). 7일간 고온처리를 받은 적색 국화에서는 안토시아닌 함량이 감소하고, flavanone 3-hydroxylase(F3H), dihydroflavonol 4-reductase(DFR), anthocyanidin synthase(ANS)의 발현량이 감소하였다. 하지만 flavonoid 3’-hydroxylase(F3’H)의 발현량은 품종에 따라 차이를 보였다(Huh et al., 2008).
다양한 화색에 대한 요구를 충족시킬 수 있는 복색화(bi- color flowers)는 두 가지 이상의 다른 색채를 가지는 꽃을 의미한다. 반점무늬(Iida et al., 2004), 꽃잎의 앞뒤 색이 다른 것(Quintana et al., 2007), 개화 당시의 색과 후기의 색이 다른 것(Vaknin et al., 2005)과 특정 부위의 문양(Saito et al., 2006) 모두 복색화라고 할 수 있다(Kim, 1999). 복색화는 반점 무늬와 부채꼴 무늬를 가지는 카네이션(Dianthus caryophyllus)(Itoh et al., 2002), 부위별 색이 다른 Ipomoea속 식물들(Iida et al., 2004)과 페튜니아(Saito et al., 2006)에서 주로 연구되었다. 기부와 말단의 축을 따라 착색된 패턴은 세포분화 과정에서 색소 생합성을 조절하는 유전자로 transposons이 삽입되거나 제거되어 형성된다(Inagaki et al., 1994). 반면 축과 수직으로 착색된 패턴은 유전자 발현의 공간적, 일시적인 조절을 위한 새로운 메커니즘의 가능성을 제시하였고, 페튜니아 ‘Baccara Rose Picotee’에서 chalcone의 합성은 특정 공간적(site-specifically)으로 조절된다는 것이 보고되었다(Saito et al., 2006).
복색 장미 ‘Pinky Girl’은 하나의 색을 가지는 단색 장미와는 다르게 백색인 기부와 분홍색인 가장자리로 구별이 가능한 장미이다. 최근 소비자의 다양한 화색의 요구가 높아지면서 복색 장미의 판매량이 증가하였다(Byun et al., 2005). 또한 저온 조건인 겨울철에는 복색 발현이 우수하므로 매우 높은 가격으로 거래되고 있다. 하지만 상습적으로 고온 스트레스에 노출되는 여름철에는 복색의 발현이 저하되어 상품성이 떨어지고 거래 가격이 낮아지는 등 농가에 직접적인 피해를 주고 있다(Kim and Lieth, 2012; Korea Agro-Fisheries & Food Trade Corporation, 2014). 따라서 본 연구는 복색 장미 ‘Pinky Girl’을 대상으로 꽃잎의 주요 색소와 착색 특성, 그리고 화아 발달 중 일시적인 고온 스트레스에 따른 화색 관련 유전자들의 발현 양상을 분석하여 고온기 복색 장미의 불량한 착색 기작을 이해함으로써 여름철 장미 절화 생산관리에 활용하고자 실시하였다.
재료 및 방법
식물 재료 및 온도 처리
식물 재료는 2010년 농촌진흥청에서 육성한 복색 장미 품종 ‘Pinky Girl’(Rosa hybrida L.)을 주・야간 온도 25/18°C, 습도 50 ± 10%, 광도 700 ± 100µmol・m-2・s-1으로 조절되는 생육상 환경에서 재배하였다. 화아의 발달 단계를 직경에 따라 6단계(S1: 4.5-7.5mm, S2: 7.5-10.5mm, S3: 10.5-13.5mm, S4: 13.5-16.5mm; S5: 16.5-19.5mm, S6: 19.5mm <)로 구분하였고, 온도처리는 꽃봉오리에서 꽃잎이 출현하기 직전 단계(S4)에서 3일간 엽소 현상이 발생하지 않는 최고 온도 조건인 39°C(고온처리구)와 25°C(대조구)로 처리하였다. 이때 야간온도는 고온처리구와 대조구 모두 18°C로 같게 유지하였다. 고온처리 후에는 다시 정상적인 온도인 25/18°C로 관리하여 개화를 유도하였고, 개화 시기인 S6에 도달한 꽃잎을 백색인 기부(basal part)와 분홍색인 가장자리(marginal part)를 구분하고 양측 단면부터 각각 10mm까지 부위를 채취하여 분석에 사용하였다.
광 흡수스펙트럼, 총 안토시아닌 함량 분석
채취한 꽃잎의 기부와 가장자리 부위 각 1g씩 세절하여 0.1% HCl methanol로 4°C 암소에서 24시간 추출한 후 UV-VIS spectrophotometer(UV-2450, Shimadzu, Japan)을 이용하여 400nm-700nm의 파장 범위에서 최대 흡수 파장과 흡광도를 측정하였다. 총 안토시아닌 함량은 530nm와 653nm에서 흡광도를 측정한 후 Total Anthocyanin = A530-0.24 × A653 식을 이용하여 구하였다(Murray and Hackett, 1991). 표준시약은 cyanidin-3,5-di-O-glucoside(cyanin), pelargonidin-3,5-di- O-glucoside(pelargonin)(Sigma, USA)를 사용하였다(Ogata et al., 2005).
화색 측정
화색은 색차 색도계(CR-10, MINOLTA, Japan)를 이용하여 L*(darkness-brightness), a*(green-red), b*(blue-yellow)를 측정한 후, McGuire(1992)의 수식을 이용하여 C*와 h*값을 구하였다.
High performance liquid chromatography
전처리는 Longo and Vasapollo(2005)를 참고하여 액체질소로 동결시킨 꽃잎의 기부와 가장자리 각각 3g을 마쇄한 후 0.1% HCl methanol 20mL로 4°C 암소에서 22시간 3회 반복 추출하였다. 추출한 시료는 5,000rpm, 4°C에서 15분간 원심분리하고 30mL의 상등액은 CCA-111(EYELA, Japan)을 사용하여 25°C에서 감압 농축시켰다. 색소 농축액은 2mL의 0.01% HCl methanol로 녹인 후, 활성화되어 있는 C18 Sep-Pak cartridge(Waters, Milford, USA)에 로딩시켰다. 4mL의 0.01% aqueous HCl로 세척하고, 4mL의 0.01% HCl methanol로 색소를 추출하였다. 색소 추출액은 감압 농축시킨 후 1.5mL의 0.01% HCl methanol로 녹이고 0.2µL syringe filter(Macherey- nagel, Duren, Germany)를 이용하여 여과한 후 Table 1의 조건으로 분석하였다. 표준시약은 cyanin과 pelargonin(Sigma, USA)을 사용하였다(Ogata et al., 2005).
Real-Time PCR
장미 안토시아닌 생합성 과정에서 확인된 9가지의 유전자 CHS, chalcone isomerase(CHI), F3H, F3’H, DFR, ANS, flavonol synthase(FLS), flavonoid 3-glucosyltransferase(3GT), flavonoid 5-glucosyltransferase(5GT)의 발현양상을 분석하기 위해 액체질소로 동결시킨 꽃잎 기부와 가장자리를 분쇄한 다음 Plant RNA mini Kit(PhileKorea Technology, Korea)를 이용하여 total RNA를 분리하였다. Total RNA 1µg, random primer, 10mM dNTP를 혼합하고, 최종부피가 10µL가 되도록 DEPC 처리된 dH2O를 넣고 잘 섞은 후 합성 반응액을 65°C에서 5분, 얼음에서 2분간 반응시켰다. 합성 반응액에 5xRT Buffer와 RNase inhibitor 10 unit과 역전사 중합효소 200 unit을 첨가하고 최종 부피가 10µL가 되도록 DEPC 처리된 dH2O를 넣고 잘 섞은 후 37-45°C에서 30-60분, 70°C에서 15분간 반응시켜 cDNA를 합성하였다. PCR은 1/10 희석한 cDNA 3µL에 QuantiSpeed SYBR Master Mix 10µL, forward primer 1µL, reverse primer 1µL, RNase-free water 5µL를 혼합한 후 Eco Real-Time PCR(Illumina, USA)을 사용하여 수행하였다. 실험에 사용된 primer는 Table 2와 같고, 각 실험의 결과는 Eco software v4.0.7(Illumina, USA)을 이용하여 분석하였다.
통계처리
통계분석용 프로그램인 SAS package(Statistical analysis system, version 9.2, SAS Institute Inc., USA)를 이용하여 ANOVA(Analysis of variance) 분석을 실시하였으며 각 처리간의 유의성은 DMRT(Duncan’s new multiple range test) 5% 수준으로 하였다.
결과 및 고찰
장미 화색소 구성과 화아 발달 단계별 착색특성
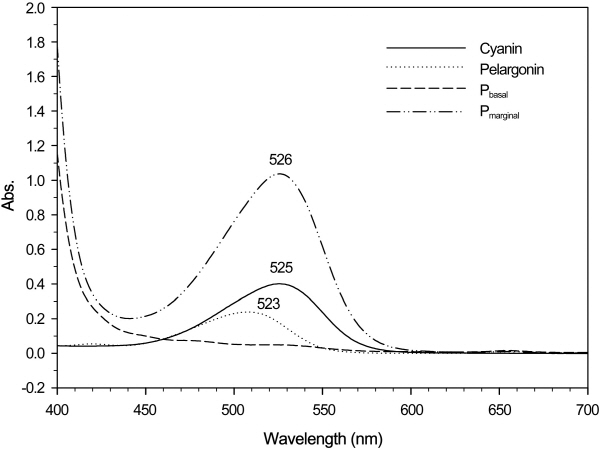
복색 장미 ‘Pinky Girl’의 꽃잎 부위에 따라 함유하고 있는 주된 색소를 알아보기 위하여 400-700nm의 파장 범위에서 흡광도를 측정하였다. Cyanin 표준시약은 525nm, pelargonin 표준시약은 523nm에서 최대 흡광도를 나타냈으며, 꽃잎 가장자리 부위 역시 526nm에서 최대 흡광도를 나타냈다(Fig. 1). 이와 같이 표준시약과 꽃잎 가장자리 부위의 흡광 경향이 유사하므로 ‘Pinky Girl’의 화색소는 cyanin과 pelargonin으로 구성되어 있고, Ogata et al.(2005)이 장미에서 첫 번째로 안정적인 화색소를 cyanin이라고 보고한 점을 고려할 때 cyanin이 ‘Pinky Girl’의 화색을 결정하는데 주요한 역할을 한다고 판단된다(Kim, 1999). 한편 가시적인 착색을 확인할 수 없었던 꽃잎 기부에서는 가장자리와는 달리 cyanin과 pelargonin의 최대 흡광도를 보이지 않았다(Fig. 1).
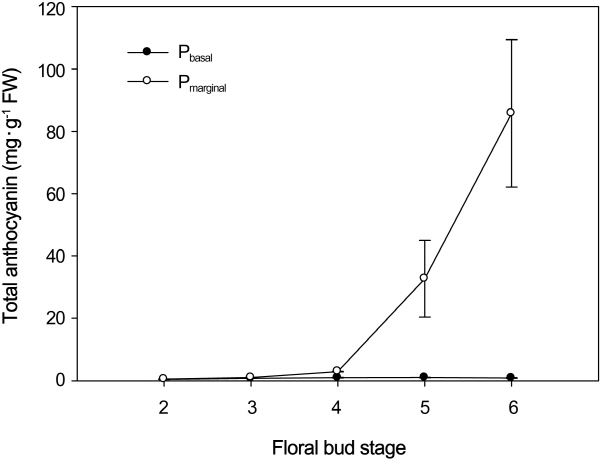
화아 발달 단계 중 꽃잎의 기부와 가장자리를 구분할 수 있는 S2부터 부위별 총 안토시아닌 함량을 측정한 결과, 기부에서는 발달 단계에 따라 가시적으로 색 변화를 관찰할 수 없었던 것과 마찬가지로 총 안토시아닌 함량이 유의적으로 증가하지 않았다. 반면에 가장자리에서는 S2부터 옅은 분홍색을 보이고 점차 진한 분홍색으로 착색되는 것을 관찰 할 수 있었고, 총 안토시아닌 함량 역시 유의적으로 증가하였다. 특히 꽃봉오리가 열리기 직전 단계인 S4부터는 함량이 급격하게 증가하기 시작하여 복색 발현이 뚜렷하게 나타났고, S6에서는 기부의 100배 이상인 85.731µg・g-1FW의 함량이 측정되었다(Fig. 2). 이러한 가장자리에서의 착색은 적색 장미 ‘Jaguar’에서 꽃봉오리가 터지기 직전인 S3와 S4에서 안토시아닌 축적이 가장 빠르게 진행된 결과와 일치하였다(Dela et al., 2003).
고온처리에 따른 화색 발현과 안토시아닌 축적 특성
고온이 화색 발현에 미치는 영향을 알아보기 위하여 꽃봉오리가 터지기 직전인 S4에서 3일 간 고온 처리(39/18°C) 후 S6에서 화색을 관찰한 결과, 가장자리의 색이 옅어졌고 전반적으로 꽃잎의 화색 발현이 현저히 저하되었다(Fig. 3). 고온처리로 꽃잎 가장자리의 L*값은 61.3으로 증가하여 밝아졌고, a*값은 41.8로 감소하여 적색 발현이 현저하게 저하되었음이 확인되었다. 채도를 나타내는 C*값 또한 41.8로 감소하여 고온처리로 화색이 품종 고유색에서 상대적으로 멀어졌음을 알 수 있었다(Table 3). 분홍색의 아시아틱 나리(Lilium × elegans Thumb.) ‘Brindisi’ 역시 여름철에 재배했을 때 겨울철과 비교하면 꽃잎의 L*값이 증가하고 a*값과 b*값이 감소하는 등 색상 발현이 저하되었다(Burchi et al., 2010). 따라서 화아 발달 과정 중 고온 노출은 이후 꽃잎의 착색에 부정적인 영향을 주는 것을 확인할 수 있었다.
|
Fig. 3. Effect of high temperature treatment on the petal color of bicolored rose ‘Pinky Girl’. A and C: Control (25/18°C); B and D: High temperature treatment (39/18°C). |
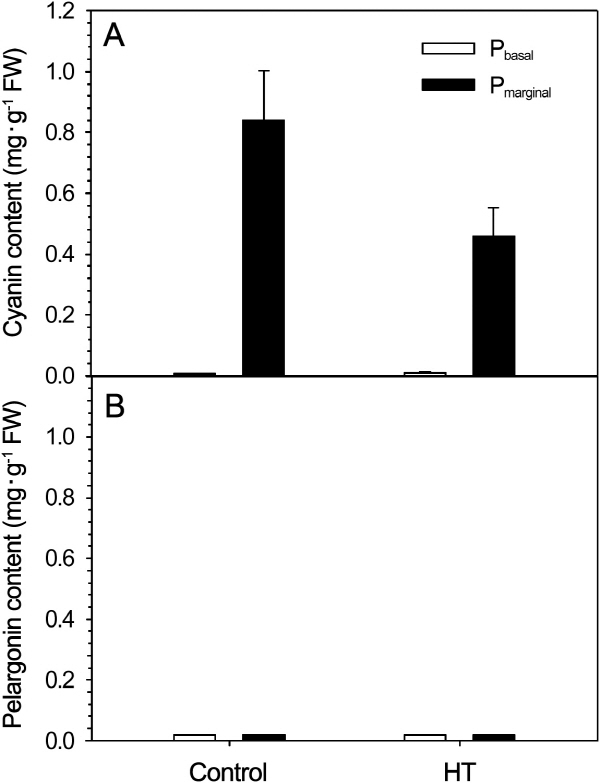
한편 색차계 수준의 화색변화가 실제 화색소의 축적과 관련이 있는지를 확인하고자, 꽃잎의 기부와 가장자리를 나누어 앞서 확인된 주색소 cyanin과 pelargonin의 함량을 HPLC로 측정하였다(Kim, 1999). Cyanin과 pelargonin의 피크는 각각 12분, 19분대에서 검출되었다. Cyanin의 함량은 꽃잎 기부에서는 유의적 차이를 보이지 않았지만 가장자리에서는 고온처리구가 대조구보다 45.5% 감소하였다(Fig. 4A). 한편 Pelargonin의 함량은 cyanin에 비해 현저히 낮았으며 기부와 가장자리 모두 유의적 차이를 보이지 않았다(Fig. 4B). 한편 cyanin과 pelargonin 색소를 모두 가진 적색 장미 ‘Jaguar’에서 꽃잎이 출현하기 직전 단계에서 고온 스트레스를 받았을 때 pelargonin과 비교해 cyanin이 상대비율이 낮아지며 적색 발현이 저하되었다(Dela et al., 2003). 한편 분홍색이며 기부가 백색인 복색 ‘Pinky Girl’은 ‘Jaquar’에 비해 cyanin이 상대적으로 적고 pelargonin은 거의 검출되지 않아 두 화색소간 상대 비율의 변화보다는 cyanin의 감소가 착색불량의 직접적인 원인으로 판단된다.
안토시아닌 생합성 관련 유전자 발현 양상
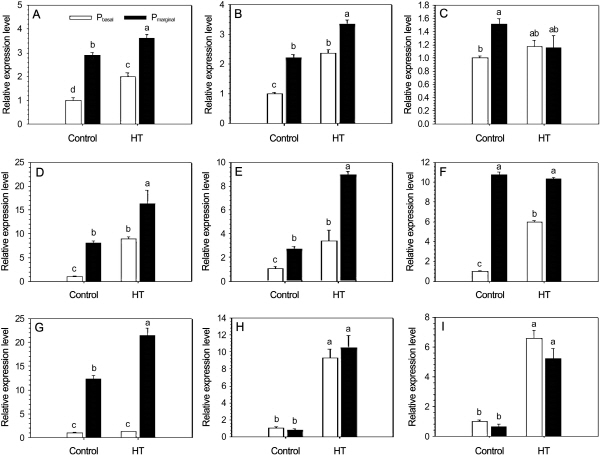
고온에 의한 화색소 축적 감소와 안토시아닌 생합성 관련 유전자들의 발현과의 관계를 살펴보았다. 먼저 대조구에서는 3GT와 5GT를 제외한 나머지 안토시아닌 생합성 유전자들은 꽃잎 기부보다 가장자리에서 더 많이 발현되었다(Fig. 5). 이러한 결과는 꽃봉오리 발달 초기에 발현하는 EBGs(early biosynthetic genes)인 CHS, CHI, F3H, F3’H의 발현이 상대적으로 기부에서 낮았기 때문에 당이 결합하지 않은 anthocyanidins의 함량이 기부에서 적었을 것이라고 예상할 수 있다. 한편 glucose와의 결합을 통해 안토시아닌을 생성 및 안정화하는 3GT와 5GT의 발현 정도가 비슷함에도 불구하고 꽃잎 기부에 안토시아닌이 매우 적기 때문에(Fig. 2) 거의 검출되지 않은 결과로도 해석할 수 있다(Jeon, 2001).
DFR의 기질인 dihydrokaempferol을 flavonol의 한 종류인 kaempferol로 전환시켜 anthocyanidins 생성을 저하하는 FLS 발현은 예상과는 다르게 기부보다 가장자리에서 현저하게 높았다. 이러한 결과는 분석 시점이 꽃봉오리 발달 초기가 아닌 후기이기 때문일 가능성이 있으며, 복색 장미 ‘Pinky Girl’의 총 안토시아닌 축적은 FLS보다는 앞에서 언급한 EBGs인 CHS, CHI, F3H, F3’H에 의한 영향이 더 크기 때문으로도 생각된다.
꽃잎 기부와 가장자리 부분을 나누어 비교해 보면, 기부에서는 F3H와 ANS를 제외한 CHS, CHI, F3’H, DFR, FLS, 3GT, 5GT 모두 고온 처리구에서 높게 발현되었다. 가장자리에서는 F3H와 FLS를 제외한 모든 유전자가 역시 고온 처리구에서 높았다(Fig. 5). 이러한 발현 패턴은 Fig. 4에서 보면 cyanin과 pelargonin의 함량 패턴과는 일치하지 않았는데 그 원인으로 다음 몇 가지 가능성을 제시할 수 있다.
첫 번째로 안토시아닌 관련 유전자들의 번역 이후의 다른 메커니즘 관여이다. 열대 과수 리치(Litchi chinensis Sonn.) ‘Sanyuehong’과 ‘Guinuo’ 두 품종 사이에 안토시아닌 축적과 생합성 관련 유전자 발현 양상이 상호 반대의 경향을 보였다. 안토시아닌 함량은 ‘Guinuo’에서 약 4배 정도 높았지만, LcCHS, LcCHI, LcF3H, LcANS의 발현은 ‘Sanyuehong’에서 더 높았다(Wei et al., 2011). 옅은 분홍색인 국화 ‘Argus’는 보라색인 ‘ARTI-purple’보다 안토시아닌 함량은 현저하게 낮았지만, 생합성 관련 유전자 발현은 더 높게 나타났다(Sung et al., 2013). 이러한 결과들은 안토시아닌 축적이 생합성 관련 유전자들과는 별개로 번역 이후의 다양한 메커니즘에 의해서 조절될 수 있다는 것을 보여준다.
두 번째는 MYB와 같은 조절유전자의 관여이다. 안토시아닌 생합성은 flavonoid pathway에서 구조유전자들을 활성화하는 MYB, basic helix-loop-helix(bHLH) 그리고 WD40 repeat protein으로 구성된 전사복합체에 의해 조절된다(Koes et al., 2005). Yamagishi(2011)는 오리엔탈 나리에서 흰색 품종 ‘Siberia’와 ‘Rialto’에서 MYB12의 발현은 차이를 보였지만 CHS는 차이를 보이지 않았다고 하였는데, 이러한 결과는 MYB가 종과 품종에 따라 다른 유전자들의 전사를 조절한다는 것을 의미한다. 이럴 경우 복색 장미 ‘Pinky Girl’에서도 고온 스트레스를 받은 시점에서의 조절유전자 발현 분석이 필요할 수 있다.
안토시아닌 생합성에 중요한 역할을 하는 생합성 관련 유전자는 종, 품종에 따라 매우 다양하다. 배 ‘Yunhongli No.1’에서는 PpCHS, PpANS, PpUFGT가 안토시아닌 생합성에 중요한 유전자로 알려졌다(Zhang et al., 2012). 노란색 꽃잎에 보라색 반점이 있는 팬지에서는 안토시아닌 함량이 급격하게 증가할 때 보라색 반점 부위에서 각각 73배, 62배나 발현되는 VwDFR, VwANS이 중요하다(Li et al., 2014). 복색 장미 ‘Pinky Girl’의 경우 9개의 유전자 중에서 F3H의 꽃잎 기부에 대한 가장자리 발현은 대조구에서 1.514배였던 반면 고온처리구에서는 0.985배로 낮아졌으며, 특히 가장자리의 발현은 다른 8개의 유전자에서는 증가했던 것과 달리 26.7% 감소하였다. 이처럼 F3H 발현 양상이 고온 처리구에서 뚜렷하게 구별되므로 ‘Pinky Girl’의 복색을 나타내는데 의미 있는 유전자로 판단된다.
이상에서 복색 장미 ‘Pinky Girl’의 착색 시점은 꽃봉오리가 터지기 직전으로 이 시기 고온 스트레스에 노출될 경우 cyanin의 축적이 현저하게 저하되어 복색 발현이 불량하게 된다. 이러한 착색반응은 안토시아닌 생합성 관련 유전자들의 발현과 연관성이 있는 것으로 확인되었으나, ‘Pinky Girl’에서는 앞에서 언급한 리치((Wei et al., 2011)에서와 같이 예외적으로 일치하지 않았다. 화색소 축적과정은 여러 단계에서 다양한 유전자들이 관여하고 있기 때문에 개별 유전자의 발현 유무와 화색소 축적간의 직접적인 연관성에 관한 추가적인 연구가 필요할 것으로 판단된다.