서 언
재료 및 방법
시험 지역
수박 재배
생육 조사 및 분석
결 과
수박 생육 및 수량
토양 화학성 변화
고 찰
토양의 염류농도에 대한 DTPA의 영향
수박 생육에 대한 DTPA의 영향
토양의 염류농도에 대한 DTPA의 영향
서 언
시설재배지는 토양에 염류가 집적되기 쉬워 지속적인 작물 생산을 위해 토양 관리가 필요하다. 외부와 차단된 비가림막으로 시설재배지에서 용탈되는 물과 염류의 양은 적은 데다가, 농가에서는 이런 상황을 고려하지 않고 토양 개량 목적으로 과잉시비하고 있는 실정이다. 2016년에 조사된 전라북도 시설재배지 토양의 평균 염류농도는 3.0dS·m-1였고, 작물생산을 위한 적정 농도범위(2dS·m-1 이하)를 초과하는 시설재배지는 57.7%로 나타났다(NIAS, 2017).
토양에서 염류 집적은 작물 생산성을 떨어뜨리는 요인 중에 하나이다. 먼저 염류 지역의 토양수는 삼투포텐셜이 낮아 작물이 이용하기 어렵고, 그 결과 작물 생육도 불량하게 된다(Bernstein, 1975). 또한 나트륨성 토양과 같이 다량 존재하는 특정 염 성분은 경우에 따라 토양의 통기성 및 투수성을 불량하게 하거나 작물에 독성을 일으키기도 하고 작물의 양분 흡수 불균형을 일으킬 수도 있다(Lee and Yun, 2014; Lee et al., 2016). 식물체 내 미량원소 중 붕소(B) 농도가 높을 경우 작물 생육이 저해되기도 한다(Choi and Kang, 2005). 시설재배지의 경우 과량 시비에 의해 여러 영양 염류들이 집적되는 경향을 보이고, 작물은 이런 염류에 의한 수분 스트레스를 받기 쉬우며, 또한 특정 양분의 축적에 의한 생육 저해 현상이 발생할 수 있다.
시설재배지의 염류집적 문제를 해결하기 위해 토양 담수, 관개방법 개선, 개량제 처리 등 다양한 방법이 개발되어 적용되고 있다(Kim et al., 2010; Wee et al., 2010; Park et al., 2012). 염류 토양을 담수시키거나 벼 재배지로 활용할 경우 토양 내 염을 용탈시킬 수 있으나(Kim et al., 2010), 작물생산을 일시적으로 중단하거나 다른 작물을 재배해야 한다는 부담이 있고 염류 용탈로 지하수 또는 하천이 오염될 수 있다는 우려도 있다. 점적관수와 같은 방법은 관개의 용이성, 물 절약, 근권 내 염 제어 등의 긍정적 효과가 있고 많은 농가에서 활용되고 있다(Park et al., 2012). 또한 토양 개량제로 유기물질은 토양의 영양염류의 부동화 및 용이한 용탈을 위해 이용되기도 한다(Wee et al., 2010). 이와 같이 시설재배지에서 작물의 염류피해를 줄이기 위한 여러 방법들이 적용되고 있지만, 여전히 추가적인 개선이 요구되고 있는 실정이다.
토양 중 금속 이온의 활성을 조절할 수 있는 물질로 킬레이트제가 활용되기도 한다. 킬레이트제는 금속 양이온과 안정한 형태의 착물을 형성할 수 있고 그 결과 금속 양이온의 활성을 낮출 수 있다(Rengel, 1999). 대표적인 킬레이트제로 DTPA (diethylenetriamine pentaacetic acid), EDTA(ethylenediamine tetraacetic acid), APCAs(aminopolycarboxylic acids), EDDS(ethylenediamine-N,N’-disuccinate), NTA(nitrilo triacetic acid)가 있고(Evangelou et al., 2007), 이들은 토양에서 중금속을 제거하거나 수경재배에서 미량원소의 유효도를 높이기 위해 이용되고 있다. 킬레이트제는 중금속으로 오염된 토양에서 중금속의 추출을 증가시킬 수 있고 식물에 의한 중금속 흡수도 증가시킬 수 있다(Blaylock et al., 1997; Lee et al., 2004; Tandy et al., 2004). 또한 킬레이트제는 수경재배에서 작물의 철 흡수를 도와 작물 생육을 증가시킬 수 있다 (Weinstein et al., 1954; Noh et al., 2017).
기존 연구의 대부분은 킬레이트제가 불용성화합물 형태로 존재하는 금속의 이용성을 증가시킬 수 있다는 점에 중점을 두고 진행되었다. 그러나 킬레이트제는 수용성 형태의 금속과 착물을 형성함으로써 이온의 농도와 식물에 대한 이용성을 낮출 수 있고 식물의 스트레스도 줄일 수 있지만, 이에 대한 연구는 많지 않다. 염류집적 시설재배지에 킬레이트제를 활용하는 일부 연구가 보고되었다. Kim et al.(2012)은 염류농도가 24.5-28.5dS·m-1로 매우 높은 토양에 EDTA, DTPA를 300mM 농도로 처리할 경우 토양에 따라 다른 경향을 보였는데, EDTA 처리는 일부 토양의 염류 농도를 유의적으로 20% 증가시켰고 DTPA 처리는 일부 토양의 염류 농도를 유의적으로 10% 감소시켰다고 보고하였다. Kim et al.(2013)의 연구에 의하면 염류농도가 8.6dS·m-1로 집적된 시설재배지에서 비료 3요소(N-P-K)에 DTPA를 추가 처리하였을 때 오이의 건중량은 변화가 없었고, 토양 화학성에서도 유의적인 변화가 없었다. 또한 Kim et al.(2015)의 연구는 염류농도가 2.2dS·m-1로 비교적 낮은 시설재배지에 비료를 시비하지 않고 DTPA만 처리하였을 때 고추 수확량의 유의적인 증가는 없었고, 관주한 용액의 DTPA 농도를 0.19mM로 증가시킬 경우 고추가 고사하였다고 보고하였다. 이들 연구는 영양염류가 집적된 토양에서 비료 시비없이 DTPA를 이용하여 양분 유효도를 증가시킴으로써 작물을 재배하는 데에 초점이 맞추어져 있고, 염류 농도를 낮추거나 양분 불균형을 해소하기 위한 연구는 없는 상황이다.
본 연구에서는 킬레이트제가 토양에 다량으로 존재하는 금속 양이온 중 Ca2+, Mg2+ 등의 2가 양이온과 착물을 형성하고 이들 양이온의 유효도를 낮춤으로써 염류가 집적된 시설재배지에서 식물의 염류피해를 줄일 수 있다고 가정하였다. 또한 킬레이트제 처리에 따른 2가 양이온의 유효도 감소로 K+, Na+와 같은 다른 1가 양이온의 식물 이용성이 증가할 수 있다고 가정하였다. 따라서 본 연구에서는 이 가설을 검토하고자 염류가 집적된 시설재배지 농가에 비료의 표준시비와 함께 킬레이트제로 DTPA를 농도별로 처리하여 수박을 재배하였고, 수박 생육과 토양 화학성의 변화에 대해 조사하였다. 킬레이트제로 DTPA는 EDTA에 비해 염류직접 토양에서 더 효율적으로 작용한다고 판단하여 선정하였다(Kim et al., 2012).
재료 및 방법
시험 지역
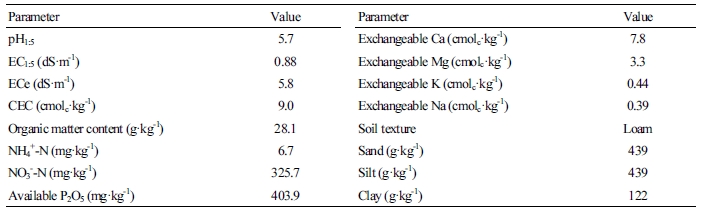
시험은 전라북도 고창군 성내면 동산리(N 35°32'29.09", E 126°44'19.65")에 위치한 시설하우스에서 2017년 2월부터 6월까지 수행하였다. 시험포장의 토양은 석천통이고 토성은 양토였다. 이곳은 시설하우스를 설치한 후 약 20년간 수박을 재배한 농가 포장으로, 작물 재배를 위해 복합비료, 유박비료, 볏짚을 주로 시비하였고, 비료는 표준시비량의 1.5–2배를 매년 시비하였다. 시험 전 토양의 경우 1:5비율의 물로 침출한 용액의 전기전도도(EC1:5)는 0.88dS·m-1이었고 포화침출액의 전기전도도(ECe)는 5.8dS·m-1이었으며, ECe/EC1:5 비율은 6.6이었다(Table 1). 시험 전 토양의 ECe/EC1:5 비율은 작물재배 후 토양의 포화침출액 전기전도도를 구하는 데에 이용하였다. 토양의 양이온교환용량(CEC)는 9.0cmolc·kg-1이었고, 토양의 교환성 양이온 중 Ca2+는 7.8cmolc·kg-1, Mg2+는 3.3cmolc·kg-1, K+는 0.44cmolc·kg-1, Na+는 0.39cmolc·kg-1으로 Ca2+의 농도가 높고 K+는 상대적으로 낮았다.
수박 재배
작물재배를 위해 질소, 인산, 칼륨 비료는 표준시비량에 따라 요소, 용성인비, 염화칼리를 이용하여 각각 13.8kg N/10a, 4.9kg P2O5/10a, 8.7kg K2O/10a의 양으로 시비하였다. 토양 산도 개량을 위한 석회물질로 소석회[Ca(OH)2]를 200kg/10a, 유기질 비료로 가축분퇴비를 330kg/10a 처리하였다. 사용한 가축분퇴비의 조성으로 건물중 유기물은 83.1%, 질소는 2.3%, 인산은 2.7%, 칼륨은 2.0%, 석회는 8.5%, 고토는 1.39%였다. 퇴비, 인산 비료는 정식 3주 전에 모두 기비로 시비하였고, 질소와 칼륨은 정식 전후에 각각 3회, 2회로 나누어서 시비하였다. 기비 시비 후 약 20cm 깊이로 경운을 하여 시설하우스 내부의 토양이 전체적으로 균일하게 분포하도록 하였다.
수박(Citrullus lanatus)은 대과종인 ‘조생삼복’을 2017년 3월 6일에 재식거리 270×40cm로 정식하였다. 킬레이트제로 DTPA(diethylene triamine pentaacetic acid)를 사용하였고, 수박을 정식한 후 30일째 부터 7일 간격으로 8회 관주하였다. 1회 DTPA 처리량을 0, 0.18, 0.3, 0.6, 1.8kg/10a로 달리하여 처리구를 두었고, 수박 생육기 동안의 총 처리량은 0, 1.44, 2.4, 4.8, 14.4kg/10a이었다. 시설하우스(600m2)의 양쪽 부분을 제외하고 가운데 부분에 대해 5곳으로 나누어 무작위로 처리구를 두었고, 한 처리구당 면적은 72m2로 하였다. 처리구 5곳은 염류농도가 서로 비슷하였다. 각 처리구별로 1회 관주량은 6,000L/10a이었고, 관주액의 DTPA 농도는 0%(0mM), 0.003%(0.08mM), 0.005%(0.13mM), 0.01%(0.25mM), 0.03% (0.76mM)이었다.
생육 조사 및 분석
각 처리구별로 3 등분하여 반복구를 두어 생육 조사와 식물체 및 토양 분석을 하였다. 각 반복구에서 무작위로 3지점을 선택하여 식물체 생육 조사 후 평균하였고, 각 지점의 토양을 혼성 채취하여 분석하였다. 생육 조사와 분석은 각 항목에 대해서 동일한 사람이 수행하였다. 엽장(leaf length), 엽폭(leaf width), 엽병장(petiole length), 경경(stem diameter), SPAD 값에 대해서는 정식 후 45일에 현장 조사하였다. 각 반복구에서 무작위로 세 지점을 선택하여 식물체 생육 조사 후 평균을 냈다. 정식 후 100일에 지상부 식물체와 토양을 채취하여 분석에 이용하였다. 이때에도 각 반복구에서 무작위로 세 지점을 선택하여 지상부 식물체를 채취하여 분석 후 평균하였고, 토양의 경우 혼성 채취하여 분석하였다. 수박 과실의 경우 과장(fruit length), 과폭(fruit width), 과피 두께(fruit rind thickness), 과중(fruit fresh weight), 수확량(total yield), 당도(sugar content)를 분석하였다. 당도는 과즙을 취하여 굴절식 당도계(Master-M, Atago, Japen)로 측정하였다. 과실을 제외한 지상부 식물체는 물로 세척한 다음 65°C에서 건조하여 분쇄한 후 N, P, Ca, Mg, K 함량 분석에 이용하였다. 식물체 N는 원소분석기(Vario MAX CN, Elementar, Germany)로 분석하였고, 식물체 P, Ca, Mg, K는 시료를 HNO3와 H2O2로 분해한 후 유도결합플라즈마 분광광도계(ICP-OES, Integra Dual, GBC, Australia)로 측정하였다. 채취한 토양 시료는 풍건 후 2mm 체로 걸러 분석에 이용하였다. 토양 pH와 EC는 토양 10g에 증류수 50mL를 가하여 1:5 비율로 추출하여 pH-EC 측정기(HI5522, Hanna, USA)로 측정하였고, 유효인산은 Lancaster 법으로 침출하여 비색정량(UV-2600, Shimadzu, Japan)하였다(NIAST, 2000). 교환성 양이온(K+, Ca2+, Mg2+, Na+)은 pH 7의 1M NH4OAc로 추출한 후 유도결합플라즈마 분광광도계(ICP-OES, Integra Dual, GBC, Australia)로 측정하였다. 토양의 암모니아태 질소는 2M KCl로 침출하여 MgO를 혼합하여 증류하면서 분리된 암모니아를 2%붕산용액에 포집한 후 0.01N 황산용액으로 적정하였으며, 질산태 질소는 0.025 M Al2(SO4)3로 추출하여 이온선택성 전극(pH-250L, Isteck, Korea)으로 측정하였다.
토양 및 식물체 데이터에 대한 통계 분석은 R 프로그램(R i368 3.4.1)을 활용하였고 패키지는 Agricolae로 유의수준 5%로 던컨다중검정(Duncan's multiple range test)을 실시하였다.
결 과
수박 생육 및 수량
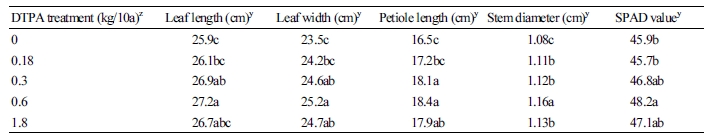
수박 줄기와 잎의 외형적인 생육은 대조구와 비교하여 DTPA 처리에 의해 증가하였다(Table 2). DTPA 처리량이 0.6kg/10a까지 단계적으로 증가함에 따라 엽장(leaf length), 엽폭(leaf width), 엽병장(petiole length), 경경(stem diameter), SPAD 값이 증가하였다. 그리고 대조구와 비교하여 0.6kg/10a의 DTPA 처리구에서 엽장은 5.0%, 엽폭은 7.2%, 엽병장은 11.5%, 경경은 7.4%, SPAD값은 5.0%의 유의적인(p < 0.05) 증가가 있었고, 0.6kg/10a에서 1.8kg/10a으로 처리량을 3배 증가시켰을 경우 전체적으로 낮아지는 경향을 보였다.
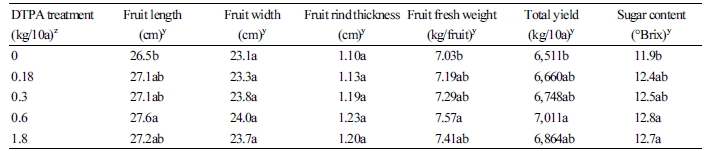
수박 과실의 수확량은 대조구와 비교하여 DTPA처리에 의해 증가하였다(Table 3). DTPA 처리량이 0.6kg/10a으로 점차 증가함에 따라 과장(fruit length), 과폭(fruit width), 과피 두께(fruit rind thickness), 과중(fruit fresh weight), 수확량(total yield), 당도(sugar content)는 증가하였다. 특히 0.6kg/10a의 DTPA 처리구에서 수확량이 가장 많았고, 대조구와 비교하여 증가한 비율은 과장이 4.2%, 과폭이 3.9%, 과피 두께가 11.8%, 과중 및 수확량이 7.7%, 당도가 7.6%였으며, 이 중에서 과장, 과중, 수확량, 당도에서 차이가 유의적이었다(p < 0.05).
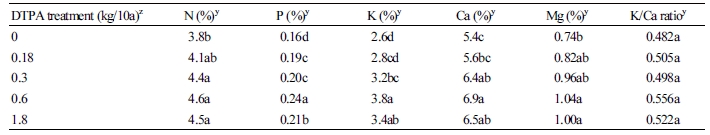
지상부 식물체의 양분 함량은 대조구와 비교하여 DTPA 처리에 의해 증가하는 경향을 보였고, DTPA 처리량이 0.6kg/10a으로 단계적으로 증가함에 따라 양분 함량도 증가하였다(Table 4). 0.6kg/10a 처리구 식물의 양분 함량은 무처리구와 비교하여 모두 유의적으로 증가하였고, 이 중에서 인산(P)가 가장 크게 증가하였으며(54.0%), 그 뒤를 이어 K가 45.9%, Mg가 40.9%, Ca이 27.6%, N가 22.0% 증가하였다. DTPA 처리량을 0.6kg/10a에서 1.8kg/10a로 3배 증가시켰을 경우 전체적으로 다시 낮아지는 경향을 보였다. 식물체의 양분 중에서 K와 Ca의 비율(K/Ca)은 처리구 사이에 유의적인 차이가 없었고 (p > 0.05), 단지 0.6kg/10a의 DTPA 처리구에서 가장 높은 경향을 보였다.
토양 화학성 변화
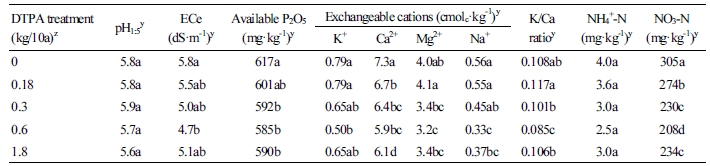
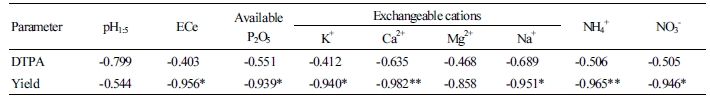
수박 재배 후 대조구 토양의 pH는 재배 전 토양와 비슷하였고, DTPA 처리농도별 유의적인 pH 차이는 없었다(Table 5). 대조구 토양의 염류농도(ECe)는 재배 전 토양과 같았고, DTPA 처리구에서는 재배 전 토양과 비슷하거나 낮아졌다. DTPA 처리량이 0.6kg/10a으로 단계적으로 증가함에 따라 ECe는 5.8에서 4.7dS·m-1으로 직선적으로 감소하였고(r = -0.981, p < 0.05, n = 4), 그 후 DTPA 처리량을 1.8kg/10a로 3배 증가시켰을 때 ECe는 5.1dS·m-1로 다시 증가하였다. 처리구별 교환성양이온(K+, Ca2+, Mg2+, Na+), 유효인산, 무기태질소(NH4+, NO3-)의 농도 변화도 염류농도의 변화 양상과 비슷하였다. 이중에서 K+(r = -0.956, p < 0.05), Ca2+(r = -0.986, p < 0.05), Na+(r = -0.957, p < 0.05), 유효인산(r = -0.941, p = 0.059), NH4+(r = -0.972, p < 0.05), NO3-(r = -0.954, p < 0.05)은 모두 DTPA 처리량이 0.6kg/10a로 점차 증가함에 따라(n = 4) 직선적으로 감소하였고, 그 후 1.8kg/10a 처리에서 다시 증가하였다. 교환성 양이온 중 K와 Ca 비율(K/Ca)은 대조구와 비교하여 0.6kg/10a의 DTPA 처리구에서 유의적으로(p < 0.05) 가장 낮았다. 토양 중 교환성 Mg2+ 이온은 DTPA 처리량과 낮은 상관성을 보였다(r = -0.861, p > 0.05, n = 4). 전체 처리구(n = 5)에 대해 비교하였을 경우, DTPA 처리량과 토양의 각 화학성 인자들 사이의 상관성은 낮았다(Table 6). 그러나 염류농도는 K+(r = 0.952, p < 0.05), Ca2+(r = 0.956, p < 0.05), 유효인산(r = 0.960, p < 0.05), NH4+(r = 0.990, p < 0.05), NO3-(r = 0.986, p < 0.05)의 각 인자들과 높은 상관성을 보였다. 반면에 수박 수확량과 비교하였을 경우 pH는 낮은 상관성을 보였고(p = 0.34), ECe, 유효인산, 교환성 양이온(K+, Ca2+, Na+), NH4+, NO3-는 유의적인 상관성을 보였으며(p < 0.05), 교환성 Mg2+도 높은 상관성을 보였다(p = 0.063).
고 찰
토양의 염류농도에 대한 DTPA의 영향
DTPA는 pKa가 1.8인 약산성임에도 불구하고(Moeller and Thompson, 1962), 토양의 pH는 거의 변화가 없었다. DTPA 최대 처리량인 14.4kg/10a을 토양 무게 기준으로 환산할 경우, 토양 밀도 1.1Mg·m-3와 깊이 15cm 기준에서 0.02cmolc·kg-1이다. 이 양은 토양의 양이온교환용량(9.0cmolc·kg-1)의 0.2%로 토양의 완충용량에 비해 적어 토양 pH를 거의 변화시키지 않았다.
수박 재배 후 토양 염류농도는 무처리구보다 DTPA 처리구에서 낮았다. DTPA 처리에 의한 토양 염류농도의 변화는 2가지 요인으로 생각해 볼 수 있다. 먼저 킬레이트제는 금속 양이온과 착물을 형성하여 토양 내 이온들의 조성을 변화시킬 수 있다. Kim et al.(2012)는 킬레이트제를 처리할 경우 토양에서 침출된 양이온의 농도가 증가하였고 침출된 양이온의 농도는 이온의 종류에 따라 크게 달라진다고 보고하였다. 토양에서 금속 양이온은 자유이온 형태, 토양 콜로이드에 흡착된 교환성 형태, 음이온과 결합된 불용성 형태, 유기물 및 무기광물의 구성 형태로 존재한다. 이중 불용성 형태는 DTPA와 결합할 경우 이온화되므로 토양 내 이온 농도는 증가할 수 있다. 다른 한편으로 금속 양이온 중 자유이온 및 교환성 형태가 DTPA와 결합할 경우 양이온의 자유이온 형태는 감소하지만 결합물이 수용성 형태로 존재한다는 점과 약산인 DTPA의 해리에 의해 이온이 생성된다는 점을 고려할 때, 토양 침출용액의 염류농도는 적게 변화될 것이다. Kim et al.(2012)의 연구에서 토양을 고농도(300mM)의 DTPA 또는 EDTA 용액으로 침출할 경우 증류수로 침출했을 때와 비교하여 침출액의 염류농도는 –10%에서 +20%의 변화를 보였다. 본 연구에서 관주액의 최대 처리 농도는 0.76mM으로 기존 연구에 비해 매우 낮아 DTPA 처리에 의한 토양 염류농도의 변화는 미세할 것으로 예상되나, 이와는 다르게 염류농도가 최대 20% 변화되었다. 두 번째 요인으로 식물 생육 증가 및 흡수에 의한 토양 영양염류 농도의 감소이다. 본 연구에서 식물체의 영양염류 함량은 분석하였지만 식물체 전체 건물중을 측정하지 않아 영양염류 흡수량을 구할 수 없어 토양 염류농도 변화와 양적 비교는 할 수 없었다. 그러나 DTPA 처리량과 토양 EC 사이의 상관성은 낮았으나(r = -0.403), DTPA 처리에 따른 수박 생육의 변화가 토양 EC의 변화와 상관성이 높았다(r = -0.956, p < 0.05)는 것이 식물 생육 증가로 토양의 염류농도가 낮아졌다는 것을 뒷받침해준다.
수박 재배 후 토양에 대한 DTPA의 영향은 염류별 농도에서 더욱 뚜렷하게 나타났다. Ca2+, Mg2+처럼 다원자가 양이온은 DTPA와 안정한 착물을 형성할 수 있고(Abdulla and Smith, 1963; Lindsay, 1979; Kim et al., 2015), 그 결과 이들 이온들의 식물 이용성과 토양 잔류량에 영향을 줄 수 있다. 그러나 토양 내 교환성 Ca2+, Mg2+ 이온의 농도 변화는 DTPA 처리량과 상관성이 낮았고, 식물 생육량과 높은 상관성을 보였다(Table 6). 그 외에 DTPA와 비교적 덜 안정한 착물을 형성하는 양이온(K+, Na+, NH4+)뿐만 아니라 음이온(유효인산, NO3-)도 식물 생육과 높은 상관성을 보였다. 이와 같은 결과는 DTPA를 적정 수준으로 처리할 경우 식물 생육의 증가와 함께 영양염류의 흡수 증가로 토양 염류농도가 낮아질 수 있음을 보여준다. 그러나 DTPA를 적정 수준 이상으로 증가시킬 경우 오히려 식물에 독성이 나타날 수 있고(Wallace et al., 1974; Rengel, 1999), 이 경우 토양 염류농도를 낮추는 효과도 더 이상 기대할 수 없음을 보여준다.
수박 생육에 대한 DTPA의 영향
염류토양에서 DTPA 처리로 수박 생육은 증가했다. DTPA를 0.6kg/10a로 처리하였을 경우 무처리구와 비교하여 잎과 줄기의 생육은 5.0-11.5% 증가했고, 과실은 4.2-11.8% 증가했다. 식물의 양분이용 및 생육에 대한 킬레이트의 영향은 기존 연구자들 사이에서 상반된 결과를 보여주고 있다. 철 유효도가 낮은 배양액에서 킬레이트는 해바라기의 외형적인 생육을 증가시켰다(Weinstein et al., 1954). 그러나 다른 연구에서는 킬레이트 화합물을 처리할 경우 Fe의 이용성은 증가하지만, Mn, Cu 등 다른 미량원소의 이용성과 밀 생육은 오히려 낮아졌다(Rengel, 1999). 또한 염류 영향을 받는 시설재배지를 대상으로 토양에 DTPA를 처리할 경우 작물 생육량은 통계적으로 유의적인 변화가 없었다(Kim et al., 2013, 2015). 이와 같이 기존연구는 양분의 유효도가 낮은 상황을 제외하고 킬레이트 화합물이 작물의 생육에 긍정적인 영향을 주지 않았지만, 본 연구는 이들 기존 연구와 대조적인 결과를 보여주고 있다.
본 연구지역 토양은 염류농도 5.8dS·m-1이고, 교환성 양이온 중 Ca2+(7.8cmolc·kg-1)와 Mg2+(3.3cmolc·kg-1)가 토양 양이온교환용량(9.0cmolc·kg-1)를 초과하여 존재하는 염류토양이다. 그리고 교환성 Ca2+와 Mg2+ 농도는 수박에 적합한 농도(Ca2+: 5.0-6.0cmolc·kg-1, Mg2+: 1.5-2.0cmolc·kg-1)에 비해 높았다(NIAST, 2010). 반면에 교환성 K+(0.44cmolc·kg-1)는 다른 양이온과 비교하여 낮은 농도로 존재하였고, 수박 재배에 적합한 K+ 농도(0.7-0.8cmolc·kg-1)와 비교해도 낮았다(NIAST, 2010). 이와 같은 상황에서 이온 사이의 경쟁에서 밀려 K+의 식물 이용성은 더욱 낮아질 수 있고, 식물의 양분 불균형으로 생육이 불량해 질 수 있다.
염류농도가 높은 상황에서 DTPA는 작물의 생육을 증진시키는 작용을 할 수 있다. DTPA는 금속 양이온과 착물을 형성함으로써 이들 양이온의 활성을 낮출 수 있고(Rengel, 1999), 그 결과 토양 염류농도를 개선시킬 수 있다. Kim et al.(2012)에서 300mM DTPA 용액으로 토양을 포화 침출할 경우 전기전도도가 28.5dS·m-1에서 25.9dS·m-1로 낮아졌다. 본 연구에서 0.6kg/10a의 DTPA 처리를 토양 포화침출액으로 환산(토양 깊이 15cm 적용)할 경우 0.08mM에 해당한다. 이 양은 기존 처리농도(300mM)의 0.027%로 매우 적은 양이기 때문에, 작물 생육 증가의 원인으로 DTPA 처리에 의한 염류농도 개선 효과만으로 설명하기에 충분하지 않다.
킬레이트제의 다른 효과는 토양 이온 활성의 불균형을 개선함으로써 작물 생육을 증가시키는 것이다. EDTA, DTPA 등의 킬레이트 화합물은 교환성 양이온 중 Ca2+에 대한 안정화 상수가 가장 높고 그 다음으로 Mg2+이며 K+는 매우 낮다(Lindsay, 1979). 따라서 DTPA를 처리할 경우 과량으로 존재하는 Ca2+의 활성은 낮아지고 적은 양으로 존재하는 K+의 활성은 상대적으로 높아질 것으로 기대되며, 이는 수박의 양이온 흡수와 수박 재배 후 토양에 잔류한 양이온의 변화에서 잘 나타나고 있다. 수박의 Ca 함량은 0.6kg/10a의 DTPA 처리구에서 무처리구에 비해 27.6% 증가하였지만 K의 함량은 45.9%로 더욱 크게 증가하였다. 그리고 토양 내 함량도 Ca2+는 19.6% 감소하였지만 K+는 37.2%로 더욱 크게 감소하였다. 이와 같은 결과를 반영하여 0.6kg/10a의 DTPA 처리구에서 토양 내 K/Ca의 비율이 유의적으로 가장 크게 감소하였고, 수박의 양분 함량에서도 통계적인 유의성은 없었으나 같은 경향을 보였다. 이는 DTPA 처리에 의해 상대적으로 K+의 활성이 증가하여 식물체가 부족한 K를 더 잘 흡수하였음을 보여준다. 토양 이온 및 식물 양분의 불균형 해소는 염류뿐만 아니라 수분 스트레스에 대한 식물 저항성의 증가에 기여할 수 있다(Dehkordi, 2017).
DTPA 처리에 의한 식물의 양분흡수 불균형 해소는 마그네슘(Mg)과 인(P)에서도 나타났다. DTPA 처리로 수박의 Mg, P 함량은 증가하였고, 0.6kg/10a의 처리구에서 무처리구에 비해 각각 40.9%, 54.0% 증가하여 Ca의 증가량(27.6%)보다 컸다. DTPA는 Ca2+과 더 안정한 착물을 형성하기 때문에(Lindsay, 1979), Mg2+의 흡수량이 상대적으로 더 증가할 수 있었다. 또한 토양에서 인산은 Ca, Mg, Fe 등의 양이온과 결합하여 안정화되지만, 이들 양이온들이 킬레이트제에 의해 착물을 형성하거나 식물에 의해 흡수제거되면서 인산의 유효도가 증가하였을 것이다(Kim et al., 2012). 이와 같이 DTPA 처리에 의한 식물의 양분 불균형 해소로 광합성을 포함한 생리활성이 증가하여 수박의 당도 및 식물의 생육이 증가할 수 있었다.
양분 분균형 해소에 대한 DTPA 작용에도 불구하고 DTPA 처리량을 증가시킴에 따라 수박의 생육이 지속적으로 증가하진 않았다. 0.6kg/10a에서 1.8kg/10a로 DTPA 처리량을 증가시킬 경우 식물의 생육과 양분 함량이 감소하였다. 기존 연구에서 고농도의 킬레이트 화합물은 식물의 미량원소 흡수를 저해하여 독성 징후를 일으킬 수 있다고 보고하였다(Wallace et al., 1974). 킬레이트 화합물 처리로 양이온 형태 미량원소의 자유이온 활성이 낮아질 수 있고(Rengel, 1999), 그 결과 이들 미량원소의 식물 흡수가 저해될 수 있다(Parker and Pedler, 1997). 킬레이트 화합물은 식물체에 흡수될 수 있고(Weinstein et al., 1954), 그 결과 킬레이트 자체 또는 대사물질 또는 킬레이트 착물에 의해 독성이 나타날 수 있다고 추측되기도 한다(Rengel, 1999). 킬레이트 화합물이 식물체 내에서 금속 양이온과 착물을 형성할 경우 금속 이온의 활성이 저하되고 효소활성을 포함한 생리적 기능이 저하될 수 있다는 것이 독성의 예가 될 수 있다. 아직 이에 대해 밝혀진 것은 없고, 작물 재배에 킬레이트 화합물의 작용 기능을 높이기 위해서는 킬레이트 화합물의 독성 작용에 대해 더 연구되어야 할 것이다.
결론적으로 시설재배지 염류 토양에 킬레이트 화합물로 DTPA를 처리할 경우 수박의 양분 흡수 및 생육이 증가하였다. 특히 영양염류 중 Ca2+의 비율이 높은 염류 토양에서 DTPA는 Ca2+에 비해 양과 유효도가 낮은 양분들의 식물 이용성을 증가시킴으로써 양분 흡수 불균형을 해소하였고 수박의 생육 및 당도를 증가시켰다. 그러나 DTPA 최적 처리량(0.6 kg/10a)에 비해 3배 증가(1.8 kg/10a)시켰을 경우 DTPA의 긍정적 효과는 줄어들었다. 따라서 본 연구는 염류농도가 높은 시설재배지에서 DTPA는 식물의 염류 피해 및 양분흡수 불균형을 해결하기 위해 사용될 수 있음을 제시해 준다.