서 언
재료 및 방법
실험재료
수체살포용 1-MCP(S1-MCP, HarvistaTM) 처리 및 저장조건
과실 특성
내생 에틸렌 발생량
세포벽물질(Alcohol insoluble substance, AIS) 추출
Uronic acids 및 total sugar 함량
세포벽 분해효소 추출
세포벽 분해효소 활성
결과 및 고찰
수확 시 과실 특성
저장기간별 과실 특성
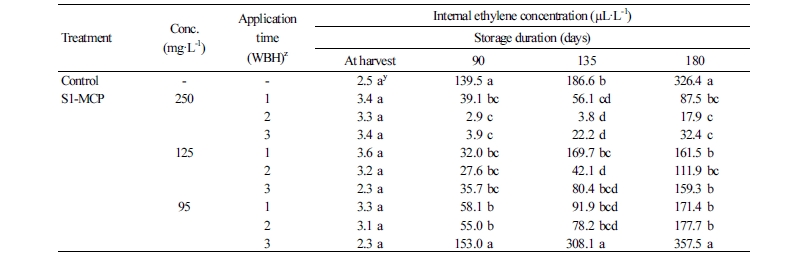
내생 에틸렌 발생량
Uronic acid(UA)와 total sugar(TS)의 함량
세포벽 분해효소 활성
서 언
‘후지’ 과실의 특성은 당도 14-15°Brix, 산도 0.3-0.4%로 식미가 우수하며, 저온저장 시 5-6개월간 품질이 유지되어 다른 품종에 비해 저장성이 강한 것이 특징이다. 이런 장점은 소비자 수요 증가 및 수출 활성화에 중요한 요인이 되고 있다. 사과의 품질을 유지하기 위해 일반적으로 실시해 온 저온저장은 과실의 저장성을 유지하는 데 한계가 있고, 공기조성을 조절하는 controlled atmosphere(CA) 저장이 과실의 저장 중 품질을 유지하는 데 탁월한 효과를 보여왔다(Park and Yoon, 2005, 2006). 그러나 국내에서 생산되는 ‘후지’ 사과는 밀발생이 심하여 CA저장 시 저산소(1-3%)와 고 이산화탄소 조건(1-3%)에 노출되면 내부 갈변이 다발생하여(Kweon et al., 1998; Park et al., 2012) 실용화되지 못하고 있다.
최근에는 사과를 수확한 후 에틸렌작용억제제인 1-methylcyclopropene(1-MCP)를 훈증처리하여 과실의 저장성을 유지시키고 있다(Kim et al., 2018; Park et al., 2011). 사과 과실에서 1-MCP 처리는 호흡량 및 에틸렌 발생량을 저하시켜 경도 및 산 함량 등을 유지하면서 과실 품질을 유지하는 데 우수한 효과를 보이고 있다(Lim et al., 2007; Moran and McManus, 2005; Toivonen and Lu, 2005). 그러나 훈증처리용 1-MCP는 과실을 일괄 수확한 후에 처리를 해야 하는 단점이 있어 최근에 미국 AgroFresh사에서 수확전 수체살포용 1-MCP(HarvistaTM)가 개발되어 ‘McIntosh’, ‘Empire’, ‘Delicious’ 사과에 320, 250, 160, 125mg·L-1의 농도로 처리하였을 때 저장동안 과실품질을 유지하는 데 효과적이라는 연구가 진행되어 왔다(DeEll and Behrouz, 2010; Watkins et al., 2010, Yuan and Li, 2008). 반면, 국내에서는 ‘감홍’ 사과에서만 수체살포용 1-MCP에 대한 연구(Yoo et al., 2013)가 수행되었다.
따라서 본 연구는 수확전 수체살포용 1-MCP 처리가 ‘후지’ 사과의 저온저장 중 과실 품질, 세포벽 구성성분 및 세포벽 분해효소들의 활성에 미치는 영향을 구명하고자 실시되었다.
재료 및 방법
실험재료
경북 상주시 낙동면 소재의 농가에 재식되어 있는 8년생 ‘후지’(/M.9) 품종을 대상으로 수세가 안정되고 균일한 나무를 선정하여 실험재료로 사용하였다.
수체살포용 1-MCP(S1-MCP, HarvistaTM) 처리 및 저장조건
S1-MCP는 미국 AgroFresh사로부터 제공받아 시험을 수행하였다. S1-MCP처리는 250, 125, 95mg·L-1의 농도로 각각 수확 3주전(10월 12일), 2주전(10월 19일) 및 1주전(10월 26일)에 수체살포하였으며, 과실 수확은 11월 2일에 실시하였다.
과실의 저장조건은 온도 0 ± 1°C, 상대습도 85-90%로 설정하였고, 저장기간은 180일간이었으며 저장 90일후부터 45일 간격으로 90일(1월 31일), 135일(3월 17일), 180일(5월 1일)에 과실 특성을 조사하였다.
과실 특성
과실 경도는 직경 11mm plunger를 장착한 과실 경도계(Fruit Tester, FT327, Italy)를 사용하여 과실 적도면의 과피를 제거한 후 과실 당 3회 측정한 값을 평균하여 Newton(N) 값으로 나타내었다. 산 함량은 과즙 5mL를 0.1N NaOH로 적정한 후 사과산으로 환산하였고, 가용성 고형물 함량은 디지털당도계(PR-201α, ATAGO, Japan)를 이용하였으며, 과피의 색도는 색차계(CR-10, Konica Minolta, Osaka, Japan)를 이용하여 측정하였다.
내생 에틸렌 발생량
내생 에틸렌 발생량은 조사 1일전에 과실을 저장고에서 꺼내어 실온(25°C)에서 품온을 평형시킨 후 측정하였다. 1개의 과실을 1반복으로 하여 5개의 과실을 대상으로 1mL 주사기를 꽃받침 부위에 삽입하여 과심 내 gas 1mL를 채취한 뒤 FID(flame ionization detector)를 장착한 gas chromatography(GC2010, Shimadzu, Kyoto, Japan)를 이용하여 측정하였다. Gas chroma-tography의 분석 조건은 Porapak Q(80/100 2m, Youngin Frontier, Korea) column을 이용하였으며, injector temperature 100°C, oven temperature 90°C, detector temperature 200°C로 설정하였고, carrier gas는 He, flow rate는 분당 20mL로 하였다.
세포벽물질(Alcohol insoluble substance, AIS) 추출
세포벽물질의 추출은 Rose et al. (1998)이 행한 방법으로 수행하였다. ‘후지’ 과실의 과피를 제거한 과육 50g에 95% ethanol 250mL를 가한 뒤 항온수조(SH-SAKWB, Samheung21, Korea)에서 40분간 끓인 후 과육을 마쇄하여 여과하였다. 여과 후 남은 잔사는 끓인 ethanol 500mL, chloroform:methanol(1:1, v/v) 500mL, acetone 500mL를 사용하여 차례로 세척하였다. 세척이 끝난 잔사는 30°C의 oven에서 건조시킨 후 이를 세포벽물질(AIS)로 하였다.
Uronic acids 및 total sugar 함량
Uronic acid 함량은 carbazole 비색법(Bitter and Muir, 1962)으로 실시하였다. 함량은 표준물질인 galacturonic acid를 사용하여 검량선에 의해 산출하였다. Total sugar 함량은 phenol-sulfuric acid 방법(Dubois et al., 1956)으로 정량하였다. 함량은 표준물질인 glucose를 사용하여 검량선에 의해 산출하였다.
세포벽 분해효소 추출
효소의 추출은 Pressey(1983)의 방법으로 행하였다. 과피를 제거한 과육 50g에 10mM sodium phosphate buffer(pH 7.0) 100mL를 가하고, 시료 1g당 0.5mg의 polyvinylpolypyrrolidone를 넣어 10분간 균질화한 다음 1M이 되게 NaCl을 가하여 4시간동안 교반한 후 12,000×g에서 60분간 원심분리하여 상징액을 얻었다. 이 상징액을 (NH4)2SO4로 85% 포화·염석하고, 12,000×g에서 60분간 원심분리하여 얻은 침전물을 10mM sodium phosphate buffer(pH 7.0)에 현탁시킨 뒤, 10mM sodium phosphate buffer(pH 7.0) 용액에서 48시간 투석한 다음 12,000×g에서 60분간 원심분리한 상징액을 조효소액으로 하였다. 모든 효소의 추출은 4°C에서 행하였다.
세포벽 분해효소 활성
α-Galactosidase, β-galactosidase, β-glucosidase, α-arabinosidase, α-mannosidase 및 β-xylosidase의 활성들은 각각의 p-nitrophenyl-glycoside를 기질로 하였을 때 생성되는 p-nitrophenol의 양을 측정하여 가수분해하는 정도를 UV-VIS spectrophotometer(UV-1800, Shimadzu, Kyoto, Japan)를 이용해 효소 활성도로 측정하였다. 즉, 각각의 기질들을 10mM sodium acetate buffer(pH 4.0)에 0.2% 되게 녹인 용액 125µL에 10mM sodium acetate buffer(pH 4.0) 250µL를 vortex로 잘 혼합한 후, 효소액 250µL를 가하여 30°C에서 60분간 반응시킨 다음 1M Na2CO3 1mL를 가하여 반응을 정지시키고, 410nm에서 흡광도를 측정하였다. 각각의 효소 활성도는 30°C에서 1시간 동안 1mmole의 p-nitrophenol이 효소작용에 의해 생성되는 것을 1unit로 하였다.
결과 및 고찰
수확 시 과실 특성
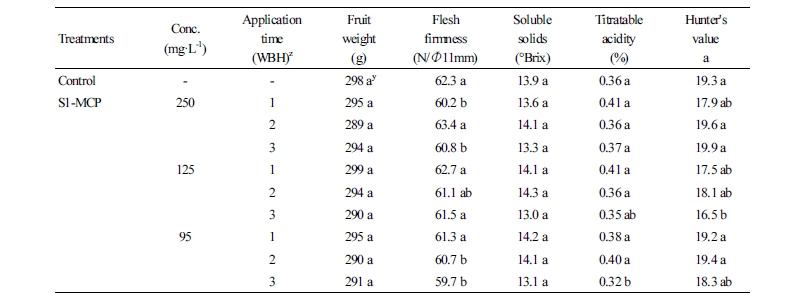
수확 전 수체살포용 1-MCP(S1-MCP)처리에 따른 수확 시 과실 품질 특성을 보면(Table 1), 과중, 경도, 가용성 고형물 및 산 함량은 S1-MCP 처리와 무처리 과실들 간에 차이를 거의 보이지 않았다. 그리고 과실의 착색 정도는 처리들에 따른 차이는 보이지 않았으나, S1-MCP 125mg·L-1 수확 3주전 처리구는 16.5로 무처리 과실에 비하여 착색이 지연되는 결과를 보여 일관성이 없었다. 따라서 이러한 결과는 S1-MCP 처리가 ‘후지’ 과실의 착색에 미치는 영향은 크게 없는 것으로 판단하였다. ‘Delicious’ 사과에 S1-MCP를 처리한 후 수확 시의 착색, 가용성 고형물 함량은 차이가 없었지만 과실의 경도는 1회 살포 시는 차이가 없었고 2회 살포 시에는 증가한다고 하였다(Yuan and Li, 2008). 본 연구결과에서도 1회 살포 시로 동일한 결과를 보였다. 따라서 ‘후지’ 사과의 수확 전 S1-MCP 처리는 수확 시 과실의 품질에 미치는 영향은 없는 것으로 판단되었다.
저장기간별 과실 특성
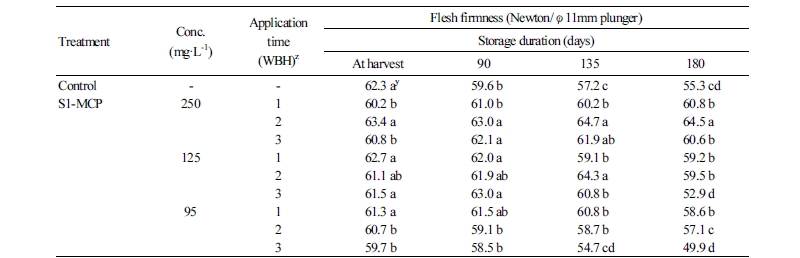
저장기간동안 ‘후지’ 과실의 경도 변화를 보면(Table 2), 무처리 과실은 수확 시 62.3N이었으나, 저장 180일 후에는 55.3N으로 급격히 감소하였고, S1-MCP 처리 과실들은 저장기간이 길어지면서 무처리 과실에 비하여 높은 경도를 유지하였다. 특히, S1-MCP 250mg·L-1 농도에서는 수확 1, 2, 3주전 처리 과실 모두에서 저장 180일 후에도 수확 시와 차이를 보이지 않았다. 하지만 125와 95mg·L-1 농도에서는 처리농도가 낮거나 살포시기가 빠를수록 저장기간 동안 과실의 경도가 감소하는 결과를 보였다. 그러나 Yuan and Li(2008)는 S1-MCP 처리가 과실의 연화를 지연시켰고, 살포농도, 시기 및 횟수는 영향을 미치지 않는다고 하였다. 이는 본 결과와 비교해 보면 S1-MCP가 과실의 경도를 유지시키는 효과는 동일하였지만 살포농도, 시기 및 횟수와는 다른 결과를 보인 것은 품종의 차이에서 나타난 결과라고 판단되었다.
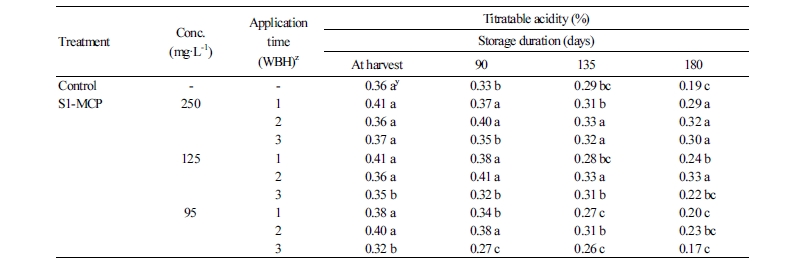
저장기간별 산 함량의 변화를 보면(Table 3), 무처리 과실은 수확 시 0.36%였고, 저장 180일 후에는 0.19%로 급격히 감소하였다. 그러나 S1-MCP 250 및 125mg·L-1 농도에서는 저장 180일 후에도 0.22-0.33%로 무처리 과실에 비하여 높은 산 함량을 보여 경도의 변화와 동일한 결과를 보였다. 이는 과실의 연화가 진행되면서 유기산이 일부 호흡기질로 이용되면서 산 함량이 감소하는데 1-MCP 처리가 호흡을 억제하여 산 함량의 감소를 억제하는 결과(Rupasinghe et al., 2000; Toivonen and Lu, 2005)로 S1-MCP 처리가 과실의 경도와 산 함량을 유지하여 과실 품질 유지에 우수한 효과를 보이는 것으로 판단되었다.
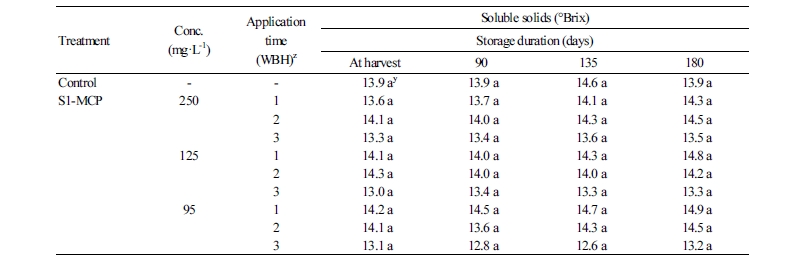
가용성 고형물 함량 변화를 보면(Table 4), 저장기간 동안에 무처리와 S1-MCP 처리 과실과의 차이는 보이지 않아 훈증용 1-MCP 처리 시 경도와 산 함량은 높게 유지시키지만 가용성 고형물 함량의 변화는 없었다(Lim et al., 2007)는 결과와 동일하였다.
내생 에틸렌 발생량
내생 에틸렌 발생량(Table 5)은 무처리 과실은 수확 시 2.5µL·L-1에서 저장 180일 후에는 급격히 증가하여 326.4 5µL·L-1였다. 반면, S1-MCP 95mg·L-1 수확 3주전 처리 과실을 제외한 나머지 처리구에서는 저장 180일 후에 17.9-177.7mg·L-1로 낮은 내생 에틸렌 발생량을 보였다. 특히, S1-MCP 250µL·L-1 농도의 수확 2, 3주전 처리 과실들은 각각 17.9와 32.4µL·L-1로 다른 처리구에 비하여 내생 에틸렌 발생량이 현저히 낮았다. 이는 과실을 수확하기 전에 S1-MCP 처리가 낮은 농도에서는 저장기간이 길어지면서 에틸렌 발생량이 증가하고, 살포농도가 높아질수록 에틸렌 발생량이 감소됨을 확인할 수 있었다. ‘Delicious’ 사과에서도 S1-MCP 처리 시 에틸렌 발생량이 현저히 감소되었는데(Yuan and Li, 2008), 이는 1-MCP가 에틸렌 수용체에 결합되므로써 에틸렌의 작용을 저해하였고(Blankenship and Dole, 2003), 또한 에틸렌의 생합성과 관련된 ACS(ACC synthase)와 ACO(ACC oxidase)를 coding하는 유전자인 CM-ACS1과 CM-ACO1의 발현량이 1-MCP 처리 시 현저히 낮았고, 특히 CM-ACS1은 저장기간동안 발현량에 거의 변화가 없었으며 CM-ACO1의 발현량은 그 증가시점이 1-MCP에 의해 현저히 지연된 결과로 해석된다(Cha et al., 2006).
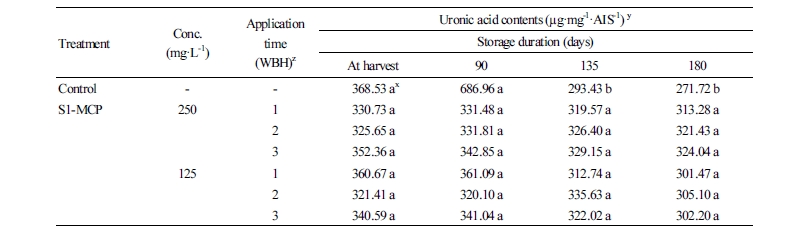
Uronic acid(UA)와 total sugar(TS)의 함량
S1-MCP 처리 후 과실의 저장기간동안 세포벽 중층의 주요 구성물질인 UA 함량 변화를 보면(Table 6), 무처리 과실의 경우 수확 시에는 368.53µg·mg-1·AIS-1였고, 저장 180일 후에는 271.72µg·mg-1·AIS-1로 그 함량이 26% 정도 감소하였다. 그러나 S1-MCP 처리 과실들은 수확 시와 비교하여 저장 180일 후에도 그 함량이 미미하게 감소하는 경향을 보였다. 과실의 연화는 세포벽 구성성분과 구조변화에 따라 일어나며, 그 가운데 펙틴질의 가용화 및 분해와 밀접한 관련이 있는 것으로 알려져 있다(Huber, 1983). S1-MCP 처리 과실들이 저장기간이 증가하여도 UA의 함량 변화가 거의 일어나지 않은 것은 세포벽 중층의 붕괴가 발생하지 않았음을 간접적으로 보여주고 있다. 사과(Chun et al., 1999)와 감(Kang et al., 1998) 과실에서 에틸렌 처리 후 저장기간이 길어지면 세포벽 구성성분인 펙틴함량이 감소하게 되는데, 이는 과실의 연화가 진행되면 세포벽 중층의 구성성분인 펙틴질은 분해가 일어나고 이때 난용성 펙틴은 감소하고, 가용성 펙틴은 증가하게 된다(Knee and Bartley, 1980). 따라서 본 결과에서도 무처리 과실들은 저장기간이 증가할수록 에틸렌발생이 증가하면서(Table 5) 세포벽 중층의 펙틴을 분해한 결과로 UA의 함량이 감소하였고, 반면 S1-MCP처리 과실들은 에틸렌 발생량이 낮은 수준으로 유지되면서 세포벽 중층을 구성하는 펙틴층의 분해가 지연되면서 펙틴층의 주성분인 UA함량이 감소되는 것을 억제한 것으로 판단되었다.
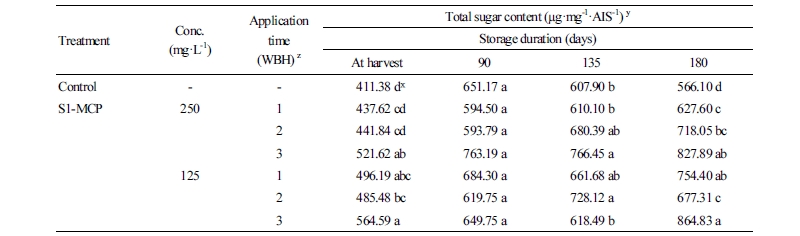
과실 세포벽의 TS함량 변화를 보면(Table 7), 수확 시 무처리 과실은 411.38µg·mg-1·AIS-1이었고, 저장 180일 후에는 566.10µg·mg-1·AIS-1이었다. 그러나 S1-MCP처리 과실들의 TS 함량은 저장 180일 후에 627.60-864.83µg·mg-1·AIS-1으로 무처리 과실에서 보다 높은 함량을 보였다. 펙틴질은 세포벽 중층을 구성하는 주성분으로 인접한 세포의 일차세포벽 사이에 존재하면서 세포 간의 결합을 견고하게 하며(Huber, 1983), 세포벽 중층은 galacturonic acid, rhamnose, arabinose, galactose와 같은 sugar group으로 이루어져 있으며, 이들 당들은 과실의 연화가 진행되면 세포벽 중층으로부터 분해되면서 유리되어 그 함량이 감소하게 된다(Gross, 1983). 따라서 본 결과에서도 무처리 과실들은 저장기간이 길어지면서 과실의 연화가 진행되어 TS함량이 감소하였고, S1-MCP처리 과실들은 이들 TS들이 세포벽 중층으로부터 분해가 지연되면서 저장 180일 후에도 높은 TS 함량을 보였다.
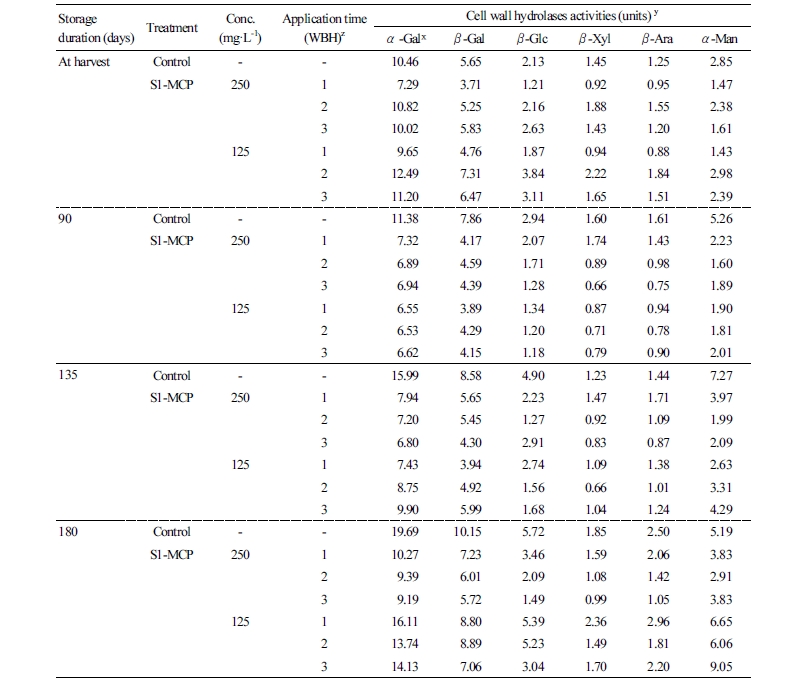
세포벽 분해효소 활성
저장기간 동안 ‘후지’ 과실의 세포벽 분해효소들의 활성 변화를 보면(Table 8), 수확 시에 무처리 과실에서는 α- galactosidase >β-galactosidase >β-glucosidase >α-mannosidase >β-arabinosidase >β-xylosidase 순으로 활성이 높았다. 특히, 과실의 연화가 진행되면서 α-galactosidase와 β-galactosidase의 활성이 증가하였고, β-glucosidase, α-mannosidase, β-arabinosidase, β-xylosidase들은 다소 활성이 증가하는 경향을 보였지만 그 정도는 미미하였다. 그리고 S1-MCP 처리 과실들은 저장기간이 길어지면서 전체적으로 세포벽 분해효소들의 활성은 수확 시에 비하여 증가하였지만 무처리 과실과 비교해서는 현저히 낮은 활성을 보였다. 특히, S1-MCP 250mg·L-¹ 처리에서 β-galactosidase의 활성이 무처리에 비하여 가장 낮은 비율로 감소하였다. 과실의 연화는 경도 감소를 수반하고, 이와 함께 세포벽 구성성분의 구조적 붕괴가 진행된다(Redgwell and Fry, 1993). 이러한 세포벽의 구조적 붕괴는 펙틴을 분해하는 세포벽 분해효소들이 관여하고 있다(Kang et al., 1999). 그리고 β-galactosidase의 역할은 세포벽 중층으로부터 galactose를 유리시킴으로써 과실 연화에 직접적인 역할을 하여(Gross, 1983; Kang et al., 1997, 1998, 1999) 과실의 성숙과 연화가 진행됨에 따라 그 활성이 높아지는 것으로 알려져 있다(Bartley and Knee, 1982). 또한 과실에서 세포벽 분해효소들의 활성은 에틸렌 생성이 개시되면서 증가하게 되어(Bartley, 1977) 과실의 연화가 진행된다고 하였다. 본 연구에서도 S1-MCP 처리 과실들에서 높은 경도(Table 2)와 산 함량(Table 3)이 유지되었고, 또한 에틸렌 발생량이 감소한 것(Table 5)이 세포벽 분해효소들의 활성을 감소시켰음을 확인할 수 있었다.
이상의 결과를 종합해 보면, ‘후지’ 과실에 S1-MCP 250mg·L-¹ 농도로 수확 2, 3주전 처리했을 때 저장기간이 길어지면서 과실 경도와 산 함량이 높게 유지되었고, 내생 에틸렌 발생량이 현저히 감소하면서 UA와 TS의 함량을 높게 유지시켰다. 또한 세포벽 분해효소들의 활성을 낮추어 과실의 저장력 향상에 따른 상품성을 유지하는 효과를 보였다. 따라서 S1-MCP를 수확 전 과실에 살포하여 저장하였을 때 과실의 저장성을 향상시키는 결과를 보여 현장에서의 적용가능성을 보여 주었다.